ISO表格-设计(工艺)文件更改记录
ISO9001表格大全
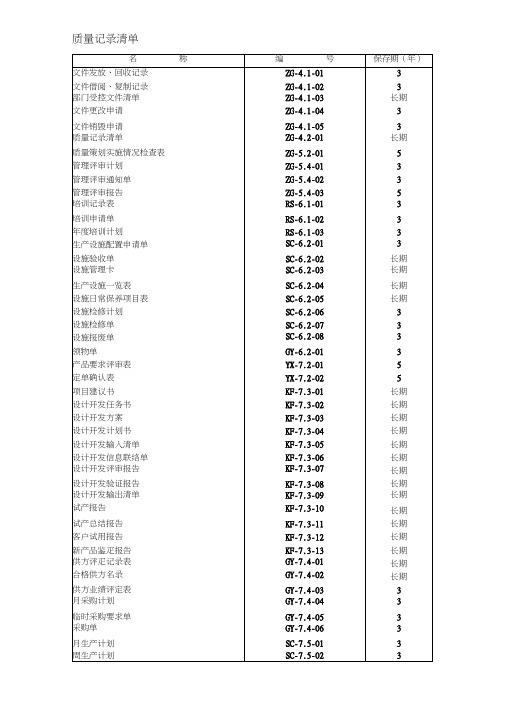
质量记录清单文件发放、回收记录编号:ZG-4.1-02部门受控文件清单部门:编号:ZG-4.1-03文件更改申请更改后内容:受此影响引起的其它更改文件名称:文件销毁申请所在部门意见:--------------------------------------------- 签名:日期:文件保管部门意见:签名:日期:管理者代表意见:签名:日期:质量记录清单编号:ZG-4.2-01质量策划实施情况检查表编号:ZG-5.2-01 序号: 质量策划项目名称: 执行部门:管理评审计划编号:ZG-5.4-01 评审目的:评审参加部门、人员:管理评审通知单编号:ZG-5.4-02 序号: 评审会议时间: 评审会议地点:参加人员:评审内容要点:培训记录表编号:RS-6.1-01 序号:考核方式及成绩:考核合格率:备注:培训申请单培训内容:年度培训计划设施验收单生产设施一览表编号:SC-6.2-04设施安装调试情况:设施验收结论:参加验收人员:备注:使用部门签名: 日期:生产部签名: 日期:编制:日期:设施日常保养项目表编号:SC-6.2-05设施名称:设施编号:使用部门:保养人:备注注:保养后,用“ V”表示日保,“ ”为周保、“ ”为月保,“ X”表示有异常情况,应在“异常情况记录”栏予以记录。
编制: 日期: 批准: 日期:设施检修单编号:SC-6.2-07设施使用部门:序号:备注:设施报废单编号:SC-6.2-08备注:领物单领物单编号:GY-6.2-01 序号:随机附件及资料:领用部门:使用人:批准:经手:日期:生产要求评审表编号:YX-7.2-01定单确认表编号:YX-7.2-02 序号:顾客名称|定货日期交付日期顾客对产品型号规格、技术要求、质量要求、数量及其他要求:评审结论(对局面评审的产品要求,应注明评审表编号:):承办人签名:日期:顾客确认:联系人:地址:电话:传真:由E编:日期: 备注:0.本表仅用于对口头定单的记录、确认,对常规产品的老客户可视同执行;1.对于有特殊产品要求的顾客,必须对产品要求进行评审、填写“产品要求评审表”,并正式签定合同;2.顾客确认可采取多种方式,如对方加盖公章的回函、传真,或对有多年业务往来的老客户记录其定货人姓名等方式。
ISO15189质量管理表格记录大全

ISO15189质量管理体系记录表格大全
保密执行情况检查记录表
注:每季度末由综合组负责人对各部门检查一次。
公正性执行情况检查记录表
质量监督记录表(1)
质量监督记录表(3)
注:质量监督员随时(至少1次/月)选择重点、难点、疑点及易出错环节进行监督并记录。
内部文件一览表
第页
文件发放与回收记录
第页
文件补发申请表
文件修订/作废申请表□修订□作废□新增
修订页
技术规范和标准目录
第页
编制:确认:
ISO15189程序文件目录
文件和记录调阅记录表
合同评审表
合同修改单
新增检验项目申请表
新检验项目评审表
新增检验项目临床应用反馈意见表
各位主任及医师:您好!
为了使检验科的工作持续改进,使检验项目设置更好的适应临床诊疗和病人的需要,请您对新项目的应用提出宝贵意见和建议。
我们对您的理解和支持表示感谢!
委托实验申请单
标本签收单
委托实验项目一览表
合格委托实验方登记表
委托实验方能力调查表
供应商评价表
供应商一览表
采购申请表
仪器设备验收报告
采购供应部物资申请审批表
注:1.此表仅用于医院物资管理系统的已登记的耗材申购,产品信息须与系统信息一致。
2.新增耗材按审批结果采购。
检验试剂标准物质耗材验收单
试剂入出库登记表
注:认真如实填写。
保存备查!
化学危险品管理记录表
注:认真如实填写。
保存备查!
专业人员讨论记录表部门:。
ISO9000记录表单汇编

记录表格格式受控状态:分发号:目录1.质量治理体系文件更改单(表CX4231) (5)2.治理评审报告(表CX5611-1) (6)3.评审组成员签字表(表5611-2) (7)4.设备购置申请单(表CX6311-1) (8)5.设备维修、三保验收单(表CX6311-2) (9)6.工艺装备设计申请单表(CX6312-1) (10)7.(工艺装备加工申请单表CX6312-2) (11)3 / 1498. 工艺装备验收单(表CX6312-3) (12)9.工艺装备周期检验单(表CX6312-4) (13)10.工艺装备返修单(表CX6312-5) (14)11.工艺装备报废单(表CX6312-6) (15)12.吊具周期检验单(表CX6312-7) (16)13.过程(4M1E)监督检查记录(表CX6411-1) (17)14.质量信息传递表(表CX6511-1) (18)15.车间月质量考核报表(表CX6511-2) (19)16.合同评审报告(表CX7211-1) (20)17.合同更改记录(表CX7211-2) (21)18.合同评审会签单(表CX7211-3) (22)19.合同评审组成员签字表(表CX7211-4) (23)20.首件鉴定目录表(表CX7382-1) (24)21.首件生产总结(表CX7382-2) (25)22.首件检验总结(表CX7382-3) (27)23.首件鉴定证书(表CX7382-4) (29)24.鉴定组成员签字表(表CX7382-5) (30)25.采购产品检验请托单(表CX7411-1) (31)26.紧急放行单(表5 / 149CX7411-2) (32)27.代料单(表CX7411-3) (33)28.供方产品质量保证能力评价记录(表CX7411-4) (34)29.合格供方名录(表CX7411-5) (35)30.产品交接清单(表CX7511-1) (36)31.技术通知单(表CX7511-2) (38)32.试件交接清单(表CX7511-3) (39)33.技术问题处理单(表CX7511-4) (40)34.工艺问题处理单(表CX7511-5) (41)35.专门过程确认表(表CX7511-6) (42)36.试制和生产预备状态检查报告(表CX7512-1) (43)37.工艺审查意见表(表CX7513-1) (48)38.固体推进剂性能预示评审报告(表CX7514-1) (49)39.转批单(表CX7531-1) (51)40.质量复查报告单(表CX7571-1) (52)41.产品质量复查报告(表CX7571-2) (53)42.型号产品质量复查问题统计表(表CX7571-3) (57)43.产品质量评审证书(表CX7572-1) (58)44.评审组成员签字表(表CX7572-2) (59)7 / 14945.产品总装测试通知单(表CX7572-3) (60)46.工艺评审打算表(表CX7381-1) (61)47.国营红峡化工厂信息顾客反馈表(表CX7573-1) (62)48.产品售后服务报告单(表CX7573-2) (63)49.顾客反馈信息处理单(表CX7573-3) (64)50.购置测量设备申请表(表CX7611-1) (65)51.测量设备送检通知单(表CX7611-2) (66)52.测量设备处置单(表CX7611-3) (67)53.测量设备报废通知单(表CX7611-4) (68)54.测量设备封存申请单(表CX7611-5) (69)55.测量设备启封申请单(表CX7611-6) (70)56.测量设备报废申请单(表CX7611-7) (71)57.内部质量审核不合格项报告(表CX8221-1) (72)58.质量治理体系内部审核报告(表CX8221-2) (73)59.例外放行单(表CX8241-1) (74)60.检验结果通知单(表CX8241-2) (75)61.不格品审理单(表CX8311-1) (76)62.质量成本统计表(表CX8412-1) (77)63.质量本分析表(表CX8412-2) (78)9 / 14964.技术归零报告(表CX8521-1) (79)65.治理归零报告(表CX8521-2) (83)表CX4231质量治理体系文件更改单编号:11 / 149表CX5611-1管理评审报告表CX5611-2评审组成员签字表编号:GS年月日表CX6311-1设备购置申请单申请单位:年月日15 / 149一式四份:1、机动处;2、供销处;3、财务处;4、打算生产处表CX6311-2设备维修、三保验收单使用单位:年月日17 / 149表CX6312-1工艺装备设计申请单编号:表CX6312-2工艺装备加工申请单编号:19 / 149表CX6312-3工艺装备验收单编号:21 / 149表CX6312-4工艺装备周期检验单编号:表CX6312-523 / 149工艺装备返修单编号:表CX6312-6工艺装备报废单编号:25 / 149表CX6312-7吊具周期检验单编号:表CX6411-1过程(4M1E)监督检查记录编号:27 / 149表CX6511-1质量信息传递表编号:29 / 149表CX6511-2车间月质量考核报表填报单位:填报时刻:年月日31 / 149车间质量助理:车间主任:车间检验:表CX7211-1合同评审报告编号:33 / 149表CX7211-2合同更改记录编号:35 / 149表CX7211-3合同评审会签单编号:37 / 149表CX7211-4合同评审组成员签字表编号:39 / 149表CX7382-1首件鉴定目录表编号:制表:批准:41 / 149表CX7382-2(2-1)首件生产总结编号:43 / 149表CX7382-2(2-2)填写:批准:45 / 149表CX7382-3(2-1)首件检验总结编号:47 / 149表CX7382-3(2-2)填写:批准:49 / 149表CX7382-4首件鉴定证书编号:。
ISO13485记录表格 汇总

地址
邮政编码
产品/类别
电话/传真
联系人
质量得分(占60%):(合格批次/到货总批次)×60
质量评分:
交货期(占20%)(按期到货的批次/到货总批次)×20
质量评分:
其他(占20%)(包括价格、包装、售后服务等)
质量评分:
总评分及处理建议:
生产供应部负责人: 日期:
主管领导意见:
签名: 日期:
性能指标
随机附件
和文件
维修记录
备注
设备封存(启用)申请表
序号:编号:GNKJ/QR-6.3-09
设施名称
设备编号
型号/规格
申请日期
使用部门
封存/启用
主要技术性能:
封存/启用说明:
备注:
生产供应部意见:
经理:
质量管理部意见:
经理:
技术部意见:
经理:
主管领导批准:申请人:
低值易耗品报废单
序号:编号:GNKJ/QR-6.3-10
供方现场评定记录
序号:编号:GNKJ/QR-7.4-06
供方名称
供品名称
电话/传真
联系人
地址
邮政编码
设备能力:
评定结论:
评定人员:职务:
日期:
人员能力:
检测能力:
体系能力:
记录:审核;批准:
物资采购合同评审表
序号:表格编号:GNKJ/QR-7.4-07
合同类别
采购合同编号
供方名称
供方营业执照号
采购物资
序号
文件名称
编号
版本/状态
复印份数
复印人
领导审批
复印时间
备注
ISO内审员记录表格表格格式(20210109222649)

10
在体系的贯彻、实施及 改进过程中,如何发挥 领导作用?(询问)
编号:
受审核部门:
审核日期:
序 号
审核内容及方法
现场审核记录
标准条款 号
判定
1
在质量手册中,是否规 定了质量方针和质量 目标?以及与此有关 的管理、执行、验证人 员的职责、权限和相互 关系?(询问、查证)
4.1
2
组织体系及过程测量 和监控点是否确定并 有效?对测量和监控 结果是否有分析、改进 活动?(询问、查证)
8.5
查表
内部质量审核检
编号:XWQR07-22
受审核部门:生产物资副总
审核员:
审核日期:序号:
序 号
审核内容及方法
现场审核记录
标准条
款号
判定
1
如何提咼部门内员工 的质量意识?并将质
4.1
量方针的要求转化为 每个员工的责任、追求 和行为?(询问)
2
生产一块涉及到大量 的质量记录,怎么确保 这些数据真实有效? 否对数据进行了整 理分析,并为改进和管 理提供信息?(询问、 查证)
内部质量审核检
查表
受审核部门:
核日期:
序 号
审核内容及方法
现场审核记录
标准条款 号
判定
1
组织是否按照规定要 求建立、实施、保持和 改进质量管理体系? 怎么体现PDCA的原 则?(询问)
4.1
2
组织质量管理体系中 的过程、以及过程间的 关系是否被确定和管 理?(询问、查证)
4.1
3
如何让全体员工了解 质量方针和质量目标, 并将质量方针的要求 转化为每个员工的责 任、追求和行为?(询 问)
ISO13485更改控制表格汇编(中英文)
ISO9001/ISO13485/医疗器械生产质量管理规范文件范例文件制修订记录ISO9001/ISO13485/医疗器械生产质量管理规范文件范例目录1、更改申请单Change Order Request2、更改紧急执行记录单Record for Emergent Change ImplementationISO9001/ISO13485/医疗器械生产质量管理规范文件范例更改申请单CO No.B.更改来源/类别/原因/Justification for New Change/ Source of Change/ Category of Proposed Change 更改来源(Source of Change):[ ]CNR [ ]ANR [ ]投诉Complaints [ ]CAPA [ ] 其他(Other单号Reference No:更改类别(Category of Proposed Change):[ ]标签&包装类(Labeling & Packaging)[ ]生产/工艺类(Production/ Process)[ ]物料类(Material )[ ]技术/性能类(Technology or Performance Change)[ ]其他(Other):更改原因([ ]产品改进[ ]供应商原因[ ]其他(Other)_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________C. 库存处理Inventory Disposition:物料现有库存Current Material Inventory [ ] N/A; [ ] Accept; [ ] Re-Work; [ ] Destroy; [ ] Phase-Out 供方/在途库存Supplier or Transportation Inventory [ ] N/A; [ ] Accept; [ ] Re-Work; [ ] Destroy; [ ] Phase-Out 半成品/成品库存Semi-finished/Finished product Inventory [ ] N/A; [ ] Accept; [ ] Re-Work; [ ] Destroy; [ ] Phase-Out在线/周转库库存In process/In transfer warehouse Inventory [ ] N/A; [ ] Accept; [ ] Re-Work; [ ] Destroy; [ ] Phase-Out备注Remark_____________________________________________________D. 风险分析If Risk Analysis neededISO9001/ISO13485/医疗器械生产质量管理规范文件范例[ ] No, 理由Reason: ____ __________] Yes, 风险分析报告请见附件Risk Management Report as attachment.是否需验证/确认If Verification/Validation needed[ ] No, 理由Reason: ____ __________ ______] Yes, 验证方案请见附件Protocol attached.更改后有效性评估Assessment of the Change Effectiveness[ ] No, 理由Reason: ____ __________] Yes, 评估方案请见Section N. Evaluation Protocol.是否需临床是否需法规申报H.涉及更改的文件编号及版本号Doc No./Version____________________________________________________________ _______________ _ Pre-review and Pre-ApprovalK. 验证/确认记录/报告Verification/ Validation Record/ ReportISO9001/ISO13485/医疗器械生产质量管理规范文件范例M. 更改执行Implementation涉及文件更改否( ) No Document Changes Required是( ) 文件更改单编号DCR Reference:涉及库存处理否( ) No Inventory Disposal Required是( ) 处理结果Result of Disposal:Relevant CAPA 否( ) No CAPA Required是( ) CAPA编号CAPA number:其他处理Other:N. 更改有效性评估Assessment of the Change Effectiveness评估方案Evaluation Protocol:签名Signature 日期Date主管Supervisor 日期Date质量部QA 日期Date 结论Conclusion:ISO9001/ISO13485/医疗器械生产质量管理规范文件范例签名Signature 日期Date主管Supervisor 日期Date质量部QA 日期DateISO9001/ISO13485/医疗器械生产质量管理规范文件范例更改紧急执行记录单Record for Emergent Change ImplementationNo.。
ISO9001质量管理体系表格大全 41个

2020最新ISO9001质量管理体系表格
有效文件清单
文件发放范围审批表
收/发文记录
文件更改记录
作废文件登记表
文件销毁记录
记录清单
编号:序号:
管理评审计划
管理评审记录
管理评审报告
年度员工培训计划表
编制部门负责人: (盖章) 编制人: (盖章)
编制日期:年月日
培训人员名册
培训教育计划表
培训教育申请表编号:
特种工序人员培训记录表
设备管理卡
设备日常保养记录
编号:
设施名称:设施编号:使用部门:保养人:月:
常情况记录”栏予以记录。
设备检修计划编号:
执行部门:
公司设备一览表
2020最新
2020最新
合同台帐
编号:
合同负责人:制表人:
2020最新
合同评审记录表
供方评价表
合格供方名册
原材料计划表
采购验收单
监视和测量校准计划
回访登记表
顾客满意度调查表编号:
年度内部审核计划表编号:
第次内部审核计划编号:
会议签到表编号:
会议记录编号:
检查表编号:
不合格报告编号:
不合格品控制、处置记录
纠正措施记录表
预防措施记录表
第次内部审核报告编号:
年度员工教育培训计划表编号:
培训教育申请表编号:
内审日程安排编号:。
ISO9001设计和开发控制程序(含表格)

设计和开发控制程序※※※※※※※※※此文件未经批准﹐不准复印※※※※※※※※※※1 目的对设计和(或)开发的全过程进行控制,确保产品能满足顾客的需求和期望及有关法律、法规要求。
2 范围适用于本公司新产品的设计、开发全过程,包括引进产品的转化、定型产品及生产过程的技术改进等。
3 职责3.1 研发部负责设计、开发全过程的组织、协调、实施工作,进行设计和(或)开发的策划、确定设计、开发的组织和技术的接口、输入、输出、验证、评审,设计和(或)开发的更改和确认等。
3.2 总工程师负责审核项目建议书、下达设计和(或)开发任务书,负责批准设计开发方案、设计开发计划书、设计开发评审、设计开发验证报告,负责审核试产报告。
3.3 总经理负责批准项目建议书、试产报告。
3.4 物控部负责所需物资的采购。
3.5 业务部负责根据市场调研或分析,提供市场信息及新产品动向,负责提交顾客使用新产品后的《客户试用报告》。
3.6 品质部负责新产品的检验和试验。
3.7 生产中心负责新产品的加工试制和生产。
4 程序4.1 设计和(或)开发的策划4.1.1 设计和(或)开发项目的来源a)业务部与顾客签定的新产品合同或技术协议。
根据总经理批准的相应的《产品要求评审表》,总工下达《设计开发任务书》,并将与新产品有关的技术资料转交研发部;b)业务部根据市场调研或分析提出《项目建议书》,报总工审核、总经理批准后,总工下达《设计开发任务书》,并将相关背景资料转交研发部;c)研发部综合各方面信息,提交《项目建议书》,报总工审核、总经理批准后,总工下达《设计开发任务书》,交研发部实施;d)生产中心根据技术革新需要,提交《项目建议书》,报总工审核、总经理批准后,总工下达《设计开发任务书》,交研发部组织实施。
4.1.2 研发部经理根据上述项目来源,确定项目负责人,将设计开发策划的输出转化为《设计开发方案》、《设计开发计划书》。
计划书内容包括:a)设计开发的输入、输出、评审、验证、确认等各阶段的划分和主要工作内容;b)各阶段人员职责和权限、进度要求和配合单位;c)资源配置需求,如人员、信息、设备、资金保证等及其他相关内容。
ISO9001-2015全套记录表格

质量记录清单
文件发放、回收记录
文件借阅、复制记录
部门受控文件清单
文件更改申请
文件销毁申请
质量记录清单
质量策划实施情况检查表
管理评审计划
管理评审通知单
管理评审报告
培训记录表
培训申请单
年度培训计划
生产设施配置申请单
设施验收单
生产设施一览表
编制:日期:
设施日常保养项目表
编号:SC-6.2-05
注:保养后,用“V”表示日保,“ ”为周保、“ ”为月保,“X”表示有异常情况,应在“异常情况记录”栏予以记录。
设施检修计划
编号:SC-6.2-06
编制:日期:批准:日期:
编号:SC-6.2-07
编号:SC-6.2-08
领物单
领物单
生产要求评审表
编号:YX-7.2-01
订单确认表
项目建议书
设计开发任务书
总工程师签名:年月日
设计开发方案
设计开发信息联络单
试产报告
新产品鉴定报告
供方业绩评定表
月采购计划
临时采购要求单
采购单
月生产计划
物料标识卡
物资收发卡
领料单
随工单
生产日报表
顾客财产问题反馈表。
新版质量管理体系审核检查表

√ √
√
5.5.1
职权和权限
受审部门的职责是什么?
√
√
5.5.1
职权和权限
最高管理者的职责、权限
1、最高管理者是否明确其各项职责?
2、最高管理者是否指定了管理者代表、是否恰当地明确了管理者代表的职责和权限?
√
√ √
管理者的作用
1、管理者是否为实施、控制和改进质量管理体系提供必要的资源,包括人力资源、专项技能、技术和财务资源?提供资源的途径是否明确?
3、电子形式文件的使用是否有效?如何控制?(查文件控制程序)
4、组织的质量管理体系是否: 1)、识别和确认了质量管理体系所需的过程?组织中的应用?(查阅组织机构图、产品工艺流程图、产品技术标准) 2)、确定这些过程的顺序和相互作用?(查阅职能分配表和质量手册中关于质量职能的描述) 3)、确定可以用于保持这些过程的运作与控制的有效性的准则和方法。(查产品标准,抽查关键过程、特殊过程监测方法的相关规定)
制定的文件控制程序是否符合要求?
1、文件控制程序内容是否完整,是否有可操作性?
2、程序是否对文件的编制、批准、发布、存档、查找、修订、评审做出了规定?
3、程序文件是否有效版本?
4、外来文件(如标准)是否包括在控制范围之内?
5、是否规定了文件夹的保管办法?
6、是否规定了适时和定期评审文件的有效性?
7、对体系的运行起关键作用的岗位是否得到现行有效文件?
5、质量手册和程序是否相互协调,是否有可操作性?
√ √ √ √ √
质量手册的控制情况
手册的发放、更改是否符合文件控制要求?(查文件发放记录、文件更改记录以及文件换版后的控制情况)
工艺文件编写规范

4.1.4作业指导书编写格式:
4.1.4.1表头为公司标志(Times New Roman五号黑体上英文下中文,中间横线为红色,英文字母i字点为红色);接下主题(作业流程图)为小初号加粗字体。
4.1.4.2第2行为小三号黑体,内容为作业指导书英文名全称。
文件名称:
工艺文件编写规范
生效日期:
1.0目的:以标准统一格式来规范文件编写,确保文件编写规范,体现工艺文件格式化与实用性。
2.0适用范围:适用于工艺文件的编写与编写格式。
3.0职责:
3.1工程部:负责工艺文件的编写、整理、修改、备份存档。
3.2ISO办:负责工艺文件的分发、回收、改版、保存、销毁。
4.1.4.3.4表内右边表框为绘编作业过程示意图,示意图的对应作业点要做对应文字标注。
4.1.4.3.5表内右下边第1栏为(作业类别),写有项目:焊锡(S)、装配(A)、品质检查(Q)、包装(P)、修理(RP)、加工(R)、插件(B)、点焊(SW)或对应岗位的作业类别标称并在项目前加选项框(□),并打上“√”。
4.6文件更改/分发、保存流程:按《文件控制程序》4.2、4.3相关项执行。
文件名称:
工艺文件编写规范
生效日期:
5.0附件:
文件编号编写规范:
TW--MI--X X—X X X X X X
产品型号
产品类别代号
产品类型代号
部门代号
文件代号
公司代号
说明:A、“部门代号”为编写文件的部门代号。例如:工程部代号------PE。
4.1.5SMT作业指导书编写格式:
4.1.5.1表内左边第1行为(贴片位置使用元件说明),第3行第1列为(序号),是编写位置元件序号;第2列为(元件型号/规格),是编写作业位置的元件型号/规格;第3列为(用量),是编写元件用量;第4列为(位置),是编写元件的贴装位置;第5列为(备注),用于相对应栏注解。
ISO质量体系管理表格--质量记录清单(精)

质量记录清单质量记录清单质量记录清单质量记录清单质量记录清单不符合项报告编号:序号:注:本表一式一份,由审核组织给责任部门。
内部质量管理体系审核报告(可另附纸叙述)编号:序号:顾客财产问题通知单编号:序号:产品质量信息反馈单编号:序号:注:本表一式四联内部质量损失统计台帐收文处理情况登记表检验原始记录口头订单登记台帐设施(工、模、卡具)管理台帐质量信息反馈统计台帐原材料、外协外购件入库验收统计台帐产品质量统计台帐单位:(精)产品售后服务登记表(精)文件回收情况登记表(精)计量周期校准计划(精)计量器具报废申请单编号:零(台)件质量抽查记录十堰有限公司车间:零件名称;零件号:经济合同签订履行台帐、统计、分析一览表单位:年月日十堰市有限公司设备日常点检卡机床编号:型号:年月操作者:机电技术文件发放登记表编号:年月生产物资计划单年月日编号:审批:审核:编制:年月日注:本表随生产计划同时下发,份数同生产计划.采购计划单位: 年月日编号:主管:计划员:外协、外购件检验通知单墙报单位:编号: 年月日注:本表一式两份,供销科及技术质检科各一份.生产计划年月编号:审批: 编制:日期:年月份销售产值、销售产品产量指标计划表编制单位:主管领导:审核:制表人:年月日十堰市有限公司产品质量征求意见书注:本表一式一份,收回后由保存年月份原材料购销存月报表墙报人:墙报日期:年月日文件发放登记表编号:注:本表只限发放文件使用.产品报价单发表日期:编号:申报单位(公章):审核:制表:报送日期:年月日注:本单一式两份。
设备检修计划执行部门:编号: 序号:编制:日期:批准:日期:设施报废单使用部门: 编号:序号:。
ISO9001质量管理体系表格大全 41个

ISO9001质量管理体系表格有效文件清单编号:序号文件名称文件编号序号文件名称文件编号文件发放范围审批表编号:文件名称文件编号申请单位数量申请发放范围:负责人:年月日审批意见:审批人:年月日收/发文记录编号:序号:序号文件名称文件编号发放序号发文单位数量收文人签字日期备注文件更改记录编号:序号:文件名称文件编号申请部门文件颁发号申请更改原因及更改内容:更改前页码更改后页码编制人:审核:批准:年月日作废文件登记表编号:序号:序号文件名称编号数量作废文件部门备注文件销毁记录编号:序号:文件名称文件编号申请部门数量申请销毁原因:申请人:年月日审核部门意见:负责人:年月日审批:批准:记录清单编号:序号:序号质量记录名称记录编号使用部门保存期填表人:编号:评审日期评审时间地点管理评审内容:评审准备要求:参加评审人员:编制:审核:批准:日期:编号:S评审日期主管部门参评人员记录及纪要起草人会议日期纪要(可附加页)管理评审报告编号:管理评审报告评审时间主持人地点参加评审人员:评审目的:评审内容:评审情况综述:评审结论:措施要求:年度员工培训计划表编号:序号培训项目培训内容培训方式培训人数培训时间教育经费投入12345678910保障措施公司领导审批意见:签字:年月日编制部门负责人:(盖章)编制人:(盖章)编制日期:年月日培训人员名册编号:序号:序号姓名性别年龄文化程度工作部门岗位级别培训时间证书编号备注培训教育计划表编号:序号:时间地点主讲人培训对象人数内容培训部门审核培训教育申请表编号:培训班名称申请时间主讲人办学地点主办单位申请人特种工序人员培训记录表编号:序号:序号特殊工种姓名性别年龄证件号年审日期身份证号填表人:审核人:设备管理卡编号:设施名称本厂编号型号(规格)验收日期生产厂家使用部门主要技术参数:随机附件及资料:检修历史记录:备注:填写人:日期:设备日常保养记录编号:设施名称:设施编号:使用部门:保养人:月:保养项目123456789101112131415161718192212223242526272829331异常情况记录备注注:保养后,用“V”表示日保,“△”为周保,“○”为月保,“X”有异常情况,应用在“异常情况记录”栏予以记录。
ISO9001-2015产品图纸技术文件更改管理规范

产品图纸、技术文件更改管理规范(ISO9001:2015)1.目的与适用范围:1.1.为了加强本公司产品图纸及技术文件的更改管理,特制订本制度。
1.2.本制度适用于本公司所有产品图纸、技术文件的管理。
2.管理职责:2.1.本公司自行设计和仿制设计产品的图样及技术文件更改,由技术部负责管理。
2.2.由用户提供的图样及按用户提供的样品、技术文件设计的产品更改,按合同协议办理。
2.3.产品配套电气图样的更改有工程部负责管理。
3.制度内容:3.1、产品图样的修改只能由产品设计人员或产品技术管理人员进行,其他人员无权修改。
3.2、产品图样及技术文件需要更改时,必须由产品设计人员或产品技术管理人员按填写更改通知单,并按技术责任制的规定履行签字手续,经过审批后方可实施。
(更改通知单见附件1.2)3.3、凡属纠正错误、校正重量、填写补充数据、补充遗漏尺寸、增加技术要求等引起的更改由产品设计人员或产品技术管理人员提出,经技术负责人审核后实施。
3.4、凡属产品主要零部件结构,材质、外观等引起的更改,由工艺人员、各车间管理人员、客户、协作单位、书面提出;经产品设计人员分析可行后,产品设计人员提出修改方案,经技术部负责人审核后,再实施修改。
重大修改须经主管技术总经理批准后实施.3.5、试制产品、一次性生产的产品,其图样或技术文件有明显错误,影响正常生产时,允许先改生产复印图,事后补办更改通知书。
3.6、图样的更改当破坏了互换性时,应在图样后加注尾号或另外绘制新图,并应相应地更改与其有关的所有图样或文件。
3.7、图纸技术文件更改时,与其相关连的设计文件应同时发出更改通知单进行相应的更改。
3.8、通(借)用件的图样更改,不得破坏通(借)用性质,否则应绘制新图,另编图号;原通(借)用件的图样仍然保留。
图号改变时,所有相关的图样或文件作相应修改。
3.9:更改方法:3.9.1:CAD文件的更改方法3.9.1.1. 带更改标记的更改方法a.在CAD文件上删去被更改的部分,输人新内容,靠近更改部位画圆、圆内填写相应的更改标记,自该圆用细实线引至更改部位。
ISO9001-2015技术文件编号规范

技术文件编号规范(ISO9001:2015)1.目的规范和统一设计文件的编号,使设计文件便于生产组织及存档管理。
2.范围适用于公司内所有技术图纸及技术文件。
3.职责3.1 设计人员对各类图纸、表格、设计变更单,技术核定单要统一分类,随时记录,避免编号重复。
3.2 各设计小组主任负责各单项工程的编号登记工作。
4.程序4.1 工程设计文件中只有设计图纸、图表及材料表进行统一编号,设计说明、图纸目录、工程项目表、计算书不编制图号、分别编写页次、总页次。
4.2 工程设计图纸和图表必须标明工程名称,项目名称、图号或编号等。
4.3 工程设计图纸、图号编制方法。
4.3.1 结构图纸、图号编制。
分格图(或立面图)图号 A 例顺序号A01立剖图 B B05平剖图 C C04节点图 D D12德信诚培训网立框图 A —K A05—K01分格编号图 A —BH A06—BH03预埋件位置及剖面图MJ MJ03测量放线图CL CL04施工放线图SG SG05角片安装图 A —A08—J134.3.2设计变更的编号例:合同号——G 201507-G024.3.3 技术核定单编号例:合同号——J 201505-J064.3.4 构件组装图图号合同号——例:财务合同主管顺序号98012-PZ04统一编制型材组框XZ构件类别铝板组装PZ钢件组装GZ玻璃组装BZ玻璃合片BH4.3.5 单件加工图号合同号——例:顺序号98012-JG30型材LJG类别代号钢材及附件JG玻璃BJG铝板PJG石材SJG4.3.6 设计图表类编号合同号——例顺序号98012-T04 ISO9001-2015内审员升级培训(100元) ISO9001-2015内审员培训(200元) :。
文件更改申请单(ISO9001四级文件表格)

批准意见:同意发布
批准人(总经理):
批准人(总经理):
文件发放/更改申请单
文件名称:
GB/T19001-2016/ISO9001:2015《质量管理体系要求》
申请人(行政负责人):
文件发布日期:2020年1月10日
理由:
GB/T19001-2016/ISO9001:2015《质量管理体系 要求》
申请人(行政负责人):
批准意见:同意发布
文件发放/更改申请单
文件名称:组织环境与相关方要求管理程序,风险和机遇应对管理程序
申请人(行政负责人):
文件发布日期:2020年1月10日
理由:
按照国家新标准GB/T19001-2016/ISO9001:2015《质量管理体系 要求》,增加新程序文件《组织环境与相关方要求管理程序》《风险和机遇应对管理程序》,全体员工进行学习.
文件发放/更改申请单
文件名称:质量手册
申请人(行政负责人):
文件发布日期:2020年1月10日
理由:
按照国家最新标准《ISO9001:2015质量管理体系要求》,结合本公司实际情况进行编制,确定了本公司的质量管理体系,阐明了质量方针和质量目标,是本公司法规性文件
申请人(行政负责人):
批准意见:同意发布
批准人总经理):
文件发放/更改申请单
文件名称:GB/T19000-2016/ISO9000:2015术语
申请人(行政负责人):
文件发布日期:2020年1月10日
理由:
国家新标准GB/T19000-2016/ISO9000:2015术语,全体员工进行学习
申请人(行政负责人):
批准意见:同意发布
批准人(总经理):
ISO9001体系记录表格格式模板(全)

38.固体推进剂性能预示评审报告(表CX7514-1)……………………………49
39.转批单(表CX7531-1)………………………………………………………51
40.质量复查报告单(表CX7571-1)……………………………………………52
29.合格供方名录(表CX7411-5)………………………………………………35
30.产品交接清单(表CX7511-1)………………………………………………36
31.技术通知单(表CX7511-2)…………………………………………………38
32.试件交接清单(表CX7511-3)………………………………………………39
使用单位:年月日
设备编号
设备名称
型号
维修类型
维修原因
维修内容和部位
机械
电器
润滑
更换零件名称和部位
存在技术问题记录
验收结论
是否要鉴定
维修单位
维修检验
使用单位
机动处
表CX6312-1
工艺装备设计申请单编号:
使用单位
设计单位
型号
工艺装备名称
类别
申请时间
完成时间
技术要求:
工艺师(员)
校对
审核
复审意见
批准
备注
申请单位:年月日
申
请
设
备
概
况
设备
名称
型号
规格
数量
单价(估)
总价
国别厂家
主机
辅机
使用工房
总功率
用水、电及其它能源情况
外形尺寸
申
