免除知情同意签字申请表
知情同意豁免申请

知情同意豁免申请
XXXXXX医院伦理委员会:
我公司拟在贵院开展XXXX产品的临床验证试验。
该产品属于体外诊断试剂,本次临床验证的方式为对比试验,采用体外测试,所使用的样本为医院门诊和体检测定后的剩余样本,不与患者直接接触,不涉及患者个人隐私,不向病人提供检测报告。
实验结果仅用于对比研究,不作为辅助诊断依据。
根据国家食品药品监督管理总局发布的《体外诊断试剂临床试验技术指导原则》(2014年第16号通告附件)中“临床试验必须符合赫尔辛基宣言的伦理学准则,必须获得临床试验机构伦理委员会的同意。
研究者应考虑临床试验用样本,如血液、羊水、胸水、腹水、组织液、胸积液、组织切片、尿液、骨髓等的获得或试验结果对受试者的风险性,应提交伦理委员会的审查意见及受试者的知情同意书。
对于例外情况,如客观上不可能获得受试者的知情同意或该临床试验对受试者几乎没有风险,可经伦理委员会审查和批准后免于受试者的知情同意。
”本次临床验证试验属于例外情况,对受试者几乎没有风险。
基于以上情况,特此申请豁免受试者的知情同意,因本次试验而造成的任何后果由我公司承担。
请伦理委员会审查、批准!
申办方:
年月日。
严重或意外的不良事件报告评估表

免除知情同意申请表项目名称申请专业主要研究者申办单位组长单位注: 对于以下两种情况之一,伦理委员会可以批准免除知情同意。
但是,请注意:免除知情同意,伦理委员会也可以要求研究者向受试者提供研究告知信息。
1.利用以往临床诊疗中获得的病历/生物标本的研究,申请免除知情同意✉本研究使用的病历或生物标本是以往临床诊疗中获取的。
请说明:本项研究所使用的肿瘤标本、血液标本及脑脊液标本均为患者标本的二次利用。
分别取自于:送检常规病理检查后剩余的肿瘤组织;送检常规血液检查后剩余的血液;患者因自身病情需要,送检脑脊液检查后剩余的脑脊液。
✉本研究对受试者的风险不大于最小风险1。
请说明:本研究使用的标本均为正常诊疗过程中剩余的组织标本,对患者无附加风险。
✉免除知情同意不会对受试者的权利和健康产生不利的影响。
请说明:患者只需接受疾病的正常诊疗过程,任何医疗待遇与权益不会受到影响✉受试者的隐私和个人身份信息得到保护。
请说明:患者在试验中的个人资料均属保密,组织标本将以编号数字而非姓名加以标示。
可以识别患者身份的信息不会透露给研究小组以外的成员。
所有研究成员和研究申办方都被要求对患者身份保密。
患者档案将仅供研究人员查阅。
为确保研究按照规定进行,必要时,政府管理部门或伦理审查委员会成员按规定可以在研究单位审查患者资料。
这项研究成果发表时,将不会披露患者个人的任何资料✉若规定需获取知情同意,研究将无法进行(病人有权知道其病历/标本可能用于研究,其拒绝或不同意参加研究,不是研究无法实施、免除知情同意的证据)。
请说明:患者有权知道其组织标本可能用于研究,有权拒绝参加研究。
1最小风险(Minimal Risk):指试验中预期风险的可能性和程度不大于日常生活、或进行常规体格检查或心理测试的风险。
本研究不利用病人/受试者以前已明确地拒绝利用的医疗记录和标本。
2. 研究病历/生物标本的二次利用,申请免除知情同意以往研究已获得受试者的书面同意,允许其他的研究项目使用其病历或标本。
3.免除知情同意书审查工作表资料文档

编号:SHSY-IEC-BG/04.03/04.0
免除知情同意书审查工作表
一、利用以往临床诊疗中获得的病历/生物标本的研究,申请免除知情同意
适用性判断
➢本项研究为:利用以往临床诊疗中获得的病历/生物标本的观察性研究:口是,口否
审查要素
1.研究目的是重要的:口是,口否
2.研究对受试者的风险不大于最小风险:口是,口否
3.免除知情同意不会对受试者的权利和健康产生不利的影响:口是,口否
4.受试者的隐私和个人身份信息得到保护:口是,口否
5.若规定需获取知情同意,研究将无法进行(病人有权知道其病历/标本可能用于研究,其拒绝或不同意
参加研究,不是研究无法实施、免除知情同意的证据):口是,口否
6.本研究不利用病人/受试者以前已明确地拒绝利用的医疗记录和标本:口是,口否
二、研究病历/生物标本的二次利用,申请免除知情同意
适用性判断
➢本项研究为:研究病历与生物标本的二次利用,即利用以往研究项目、经知情同意收集的病历或标本进行研究,申请免除知情同意:口是,口否
审查要素
1.以往研究已获得受试者的书面同意,允许其它的研究项目使用其病历或标本:口是,口否
2.本次研究符合原知情同意的许可条件:口是,口否
3.受试者的隐私和身份信息的保密得到保证:口是,口否。
免除知情同意申请书

免除知情同意申请书一、什么是免除知情同意。
在一些特殊情况下呀,我们可能会涉及到免除知情同意这个事儿呢。
比如说,当研究对参与者的风险极低,几乎可以忽略不计的时候,就有可能考虑免除知情同意。
就像我们在校园里做一个小小的调查,只是问问大家每天大概喝多少水,这种简单的调查对大家没什么危害,要是一个个去获取知情同意,就会变得特别繁琐。
又或者是在紧急情况下,根本来不及获取知情同意了。
想象一下,在医院里突然来了很多因为突发事件受伤的患者,医生要马上进行一些常规的检测或者紧急处理来挽救生命,这个时候要是还纠结于知情同意,可能就会耽误救治的黄金时间。
所以在这些特殊的、有正当理由的情况下,就可能会出现免除知情同意的情况。
这申请书可重要啦。
一方面呢,这是对规则和伦理的一种尊重。
虽然我们想要免除知情同意,但也得经过正规的程序,让相关的部门或者人员知道我们这么做是有合理原因的。
不能随随便便就觉得不需要别人同意就去做一些涉及到他人的事儿。
另一方面呢,这也是为了保护自己哦。
比如说做研究的人员,如果不写这个申请书,万一后面出了点什么小状况,别人可能就会说你怎么能不经过同意就做呢?有了这个申请书,就相当于有了一个保障,证明自己是按照规定的流程在考虑这件事情的。
1. 项目的基本介绍。
这个项目是做什么的呀?得讲清楚。
如果是研究项目,就要说研究的目的是什么。
就像是我们要研究校园里的小动物分布情况,那这个目的就得写明白,让看申请书的人一下子就知道这个事儿是怎么回事。
然后还有项目的实施方式,是通过观察呢,还是要做一些小小的标记之类的。
就像观察小动物可能就是在校园的某些角落设置观察点,这个也要详细地说出来。
2. 为什么要免除知情同意。
这个部分可关键了。
得把免除的理由说得明明白白的。
是因为前面说的风险低呢,还是紧急情况。
如果是风险低,那就要具体解释怎么个低法。
比如说只是统计校园里树木的种类,不会对任何人或者环境造成危害。
要是紧急情况,就得把紧急的状况描述清楚,像刚刚说的医院里突然来了很多患者那种紧急性,要让看申请书的人能够感同身受,觉得确实有免除的必要。
免除知情同意书申请
哈尔滨医科大学附属第一医院伦理委员会
The Ethics Committee of Frist Affiliated Hospital of Harbin Medical Universit y
第 1 页 共 1 页 编号:
IRB-AF/SQ-10/01.0
免除知情同意书申请
研究信息
1、在正常的教育、培训环境下开展的研究,如:
① 对常规和特殊教学方法的研究:□是,□否,□不适用
② 关于教学方法、课程或课堂管理的效果研究,或对不同的教学方法、课程或课堂管理进行对比研究:□是,□否,□不适用
2、涉及教育、培训测试(认知、判断、态度、成效)、访谈调查、或公共行为观察的研究: □是,□否,□不适用
3、对于既往存档的数据、文件、记录、病理标本或诊断标本的收集或研究,并且这些资源是公共资源,或者是以研究者无法联系受试者的方式(直接联系或通过标识符)记录信息的:□是,□否,□不适用
4、食品口味和质量评价以及消费者接受性研究:
① 研究用健康食品不含添加剂:□是,□否,□不适用
② 研究用食品所含食品添加剂在安全范围,且不超过国家有关部门标准,或化学农药或环境污染物含量不超出国家有关部门的安全范围:□是,□否,□不适用。
拒绝心理咨询知情同意书

拒绝心理咨询知情同意书
本文档旨在确认对心理咨询的拒绝,并明确知情同意的意愿。
请仔细阅读以下内容,如果您同意,请在底部签字确认。
甲方:
姓名: [填写姓名]
身份证号: [填写身份证号]
乙方:
心理咨询师姓名: [填写咨询师姓名]
机构名称: [填写机构名称]
声明:
我,甲方,在此确认我不打算接受乙方提供的心理咨询服务。
我已经理解并知晓心理咨询的作用和可能效益,但我对此并无兴趣。
我明白,心理咨询可以帮助人们处理情绪障碍、减轻心理痛苦
以及提供相关的支持和指导。
然而,我对乙方提供的心理咨询服务
不感兴趣,无论是因为个人原因还是其他因素。
我明白,乙方是经过专业培训和资质认证的心理咨询师,能够
提供专业的帮助和支持。
我对乙方的职业背景和经验表示尊重,并
希望他/她能够为其他需要帮助的人提供有效的心理咨询服务。
我确认,我对拒绝心理咨询不负有后悔或追索的义务。
我了解,如果我在将来有需要,我可以重新考虑并主动寻求心理咨询服务。
本文档一经签署后,将对甲方和乙方具有约束力,并被视为双
方真实的意愿。
签字确认:
甲方签字:____________________
日期:____________________
乙方签字:____________________ 日期:____________________。
豁免知情同意申请【模板】

豁免知情同意申请
项目名称:__________________
项目负责人:_________________
申请类别:(请勾选)
□申请免除知情同意•利用以往临床诊疗中获得的病历/生物标本的研究
□申请免除知情同意•研究病历/生物标本的二次利用
□申请免除知情同意签字•签了字的知情同意书会对受试者的隐私构成不正当的威胁,联系受试者真实身份和研究的唯一记录是知情同意文件,并且主要风险就来自于受试者身份或个人隐私的泄露
□申请免除知情同意签字•研究对受试者的风险不大于最小风险,并且如果脱离“研究”背景,相同情况下的行为或程序不要求签署书面知情同意。
如访谈研究,邮件/电话调查。
致**大学附属第一医院临床科研和实验动物伦理委员会:
本次研究样本为……,……(需说明时间段、疾病类型、病例/标本的样本数等)因此本次研究对受试者几乎没有风险性,可不提交及受试者的知情同意书。
故申请豁免签署受试者知情同意书。
临床主要研究者:
年月日。
医院科研项目申报伦理审查豁免知情同意申请表
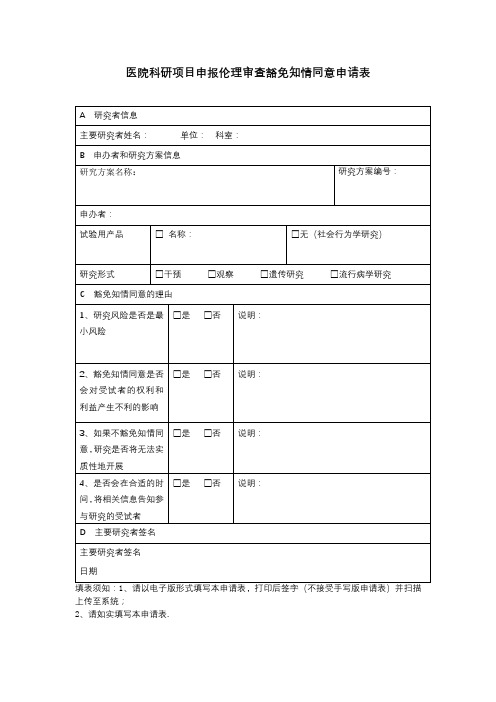
医院科研项目申报伦理审查豁免知情同意申请表
A 信息
研究方案名称:
研究方案编号:
申办者:
试验用产品
□ 名称:
□无(社会行为学研究)
研究形式
□干预 □观察 □遗传研究 □流行病学研究
C 豁免知情同意的理由
1、研究风险是否是最小风险
□是 □否
说明:
2、豁免知情同意是否会对受试者的权利和利益产生不利的影响
□是 □否
说明:
3、如果不豁免知情同意,研究是否将无法实质性地开展
□是 □否
说明:
4、是否会在合适的时间,将相关信息告知参与研究的受试者
□是 □否
说明:
D 主要研究者签名
主要研究者签名
日期
填表须知:1、请以电子版形式填写本申请表,打印后签字(不接受手写版申请表)并扫描上传至系统;
免除免签知情同意书申请表

所使用的数据或标本为以往临床诊疗、疾病监测或临床研究中获得的,请
说明
2
是否使用研究参与者明确拒绝利用的数据或标本,请说明
3
若规定需获取知情同意,研究将无法进行(研究参与者有权知道其数据或标本可能用于研究,其拒绝或不同意参加研究,不是研究无法实施、免除知情同意的证据)
4
研究参与者隐私和个人身份信息是否得到保护,请说明
免除/免签知情同意书申请表
项目名称
ቤተ መጻሕፍቲ ባይዱ申办方
研究者
承担科室
一、免除知情同意(不适用请跳过)
(一)利用以往临床诊疗、疾病监测或临床研究中获得的数据或标本进行的研究,且潜在研
究参与者已签署知情同意书允许该数据或标本用于其它临床研究的(不适用请跳过)
1
请提供原知情同意书所对应的伦理审查意见号或己签署的知情同意书
5
后续是否需要随访或再次向研究参与者获取信息,请说明
二、申请免除知情同意书签字(不适用请跳过)
(一)签了字的知情同意书会对研究参与者的隐私构成不正当的威胁,联系研究参与者真实身份和研究的唯一记录是知情同意文件,主要风险就来自于研究参与者身份或个人隐私的泄
(二)其它情况,比如通过邮件、微信、钉钉或电话等方式进行问卷调研,已向研究参与者或监护人提供书面知情同意书或获得受试者或监护人的口头知情同意,请说明
2
本研究是否超出原知情同意书许可的范围,请说明
3
研究参与者隐私和个人身份信息是否得到保护,请说明
4
后续是否需要随访或再次向研究参与者获取信息,请说明
(二)利用以往临床诊疗、疾病监测或临床研究中获得的数据或标本进行的研究,且潜在研究参与者未签署知情同意书允许该数据或标本用于其它临床研究(不适用请跳过)
科研项目免知情同意书伦理审查申请表【模板】

C参与研究者(所有参研人员)信息
(见附件一)
D签名
主要研究者声明
我保证以上信息真实准确,并负责该项目全过程中的质量保证,承诺该项目数据真实可靠,操作规范,符合国家相关法律法规的要求。本人承诺本研究团队人员与该项目无利益冲突。如有失实,愿意承担相关责任。
主要研究者签名: 日期:
研究类型
□利用以往临床诊疗中获得的医疗记录和生物标本的研究
研究目的:
研究对受试者的风险:
请具体说明免除知情同意对受试者的权利和健康是否产生不利的影响:
保护受试者的隐私和个人身份信息得到保护:
□是 □否(若选“是”,请具体说明)
若规定需获取知情同意,研究将无法进行
□是 □否(若选“是”,请具体说明)
受试者先前已明确拒绝在将来的研究中使用其医疗记录和标本
***研项目免知情同意书伦理审查申请表
研究方案名称/版本号:
申请日期:
伦理委员会受理编号:
申请状态: □初始审查 □复审
A 主要研究者信息
主要研究者姓名/职称:
主要研究者联系电话:邮箱:
主要研究者指定联系人姓名: 手机:
主要研究者目前在研临床研究项目数量:
B研究方案信息
本中心完成例数:预期试验起止时间:
□是 □否
□利用以往研究中获得的医疗记录和生物标本的研究(研究病历/生物标本的二次利用)
以往研究已获得受试者的书面同意,允许其他的研究项目使用其病历或标本
□是 □否(若选“是”,请具体说明)
本次研究符合原知情同意的许可条件
□是 □否(若选“是”,请具体说明)
受试者的隐私和身份信息得到保密
□是 □否(若选“是”,请具体说明)
E秘书组建议审查方式
免知情同意申请书

免知情同意申请书尊敬的伦理委员会/相关管理部门:申请人姓名:____________________申请人身份:____________________联系方式:____________________申请日期:____________________一、申请事项本人/我们(以下统称“申请人”)在此申请免除在以下研究项目中的知情同意程序:研究项目名称:____________________研究项目编号:____________________研究项目负责人:____________________研究开始日期:____________________研究结束日期:____________________二、申请理由1. 研究性质:本研究的性质为____________________(描述研究类型,如观察性研究、回顾性研究等),不涉及任何干预措施,对研究对象不会产生直接的生理或心理影响。
2. 风险评估:经过充分的风险评估,本研究对研究对象可能产生的风险极低,且不会对研究对象的生活质量造成影响。
3. 信息获取:本研究所需的数据和信息将通过____________________(描述数据获取方式,如公共数据库、匿名化病历资料等)获得,无需直接与研究对象接触。
4. 隐私保护:本研究将严格遵守相关隐私保护法规,确保研究过程中不会泄露任何可能识别研究对象身份的信息。
5. 法律法规:根据____________________(引用相关法律法规或政策文件)的规定,本研究符合免除知情同意的条件。
三、承诺与保证1. 申请人承诺,本研究将严格遵守国家有关法律法规、伦理准则和科研诚信原则。
2. 申请人保证,研究过程中将采取一切必要措施保护研究对象的隐私和权益。
3. 申请人同意,如有必要,伦理委员会/相关管理部门可以要求提供额外的信息和文件,以支持本申请。
4. 申请人承诺,在研究过程中如遇到任何可能影响研究对象权益的情况,将立即向伦理委员会/相关管理部门报告,并采取相应措施。
免除知情同意签字申请表

项目名称
申请专业
主要研究者
申办单位
组长单位
注:对于批准的免除知究告知信息并获得口头知情同意。
1.研究属于以下类别之一:
签署的知情同意书会对受试者的隐私构成不正当的威胁;联系受试者真实身份和研究的唯一记录是知情同意文件,并且主要风险就来自于受试者身份或个人隐私的泄露。
请说明:
本研究对受试者造成的风险不大于最小风险,如果脱离“研究”背景,相同情况下的行为或程序不要求签署书面知情同意(如访谈研究,邮件/电话调查)。
请说明:
2.如果免除知情同意签字,本研究会做到:
向受试者或其法定代理人提供书面告知信息。
获得受试者或其法定代理人的口头知情同意。
口头知情同意记录在案。
申请人签名日期
免除知情同意申报资料

免除知情同意申请表
Application form for exemption of informed consent
项目名称:
一、免除知情同意的情形
□利用以往临床诊断中获得的病例/生物标本的研究,申请免除知情同意
□研究病例/生物标本的二次利用,申请免除知情同意
□体外诊断试剂临床研究,申请免除知情同意
二、是否涉及其他伦理委员会
□否□是,请说明:
三、研究摘要,并请说明符合免除审查的理由
建议从以下几个方面来说明:
1.研究目的和研究摘要;
2. 研究对受试者的风险是否小于最小风险;
3. 免除知情同意是否对受试者的权利和健康产生不利的影响;
4. 本研究不利用病人/受试者以前已明确地拒绝利用的医疗记录和标本;
5.若涉及研究病例/生物标本的二次利用,需同时符合以下2个条件:以往研究已获得受试者的书面同意,允许其它的研究项目使用其病例或标本;本次研究符合原知情同意的许可条件;
6.明确规定研究过程中不收集受试者的隐私和个人身份信息,并且有严格的措施保障受试者的隐私和个人身份信息不被泄露,具体措施请说明:
7.诊断试剂临床试验涉及的标本是在用于医疗诊断和治疗后的剩余标本或标本库标本;标本已隐去了受试者个人信息及可识别身份信息,仅用代码标识的标本
四、是否涉及既存数据或样本的研究
□否
□是,请简要说明当时招募受试者的方法及获取知情同意的方法:
五、其他问题(如申办者研究期限、研究者参加研究的任务已经完成等)
□无
□有,请说明:
报告人:报告日期:。
医院临床研究豁免知情同意伦理审查申请表
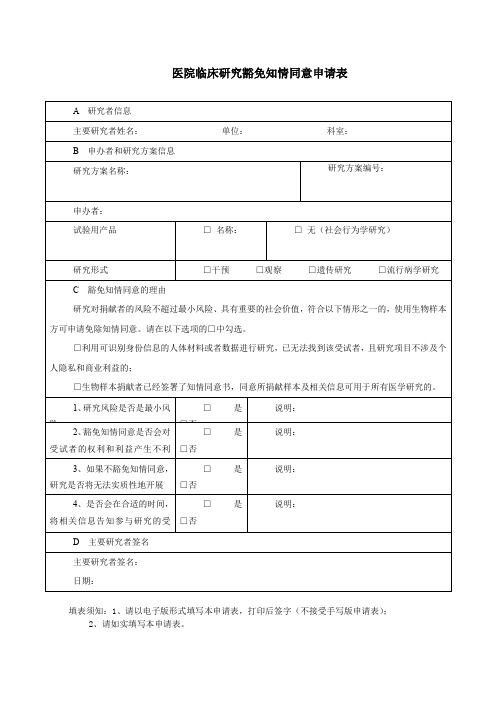
□生物样本捐献者已经签署了知情同意书,同意所捐献样本及相关信息可用于所有医学研究的。
1、研究风险是否是最小风险
□是□否Biblioteka 说明:2、豁免知情同意是否会对受试者的权利和利益产生不利的影响
□是□否
说明:
3、如果不豁免知情同意,研究是否将无法实质性地开展
□是□否
说明:
4、是否会在合适的时间,将相关信息告知参与研究的受试者
□是□否
说明:
D主要研究者签名
主要研究者签名:
日期:
填表须知:1、请以电子版形式填写本申请表,打印后签字(不接受手写版申请表);
2、请如实填写本申请表。
医院临床研究豁免知情同意申请表
A研究者信息
主要研究者姓名:单位:科室:
B申办者和研究方案信息
研究方案名称:
研究方案编号:
申办者:
试验用产品
□名称:
□无(社会行为学研究)
研究形式
□干预□观察□遗传研究□流行病学研究
C豁免知情同意的理由
研究对捐献者的风险不超过最小风险、具有重要的社会价值,符合以下情形之一的,使用生物样本方可申请免除知情同意。请在以下选项的□中勾选。
豁免知情同意申请表【模板】

申办单位
组长单位
注:对于以下两种情况之一,伦理委员会可以批准豁免知情同意。但是,请注意:豁免知情同意,伦理委员会也可以要求研究者向受试者提供研究告知信息。
1.利用以往临床诊疗中获得的病历/生物标本的研究,申请豁免知情同意
□
本研究使用的病历或生物标本是以往临床诊疗中获取的。
请说明:
2.研究病历/生物标本的二次利用,申请豁免知情同意
□
以往研究已获得受试者的书面同意,允许其他的研究项目使用其病历或标本。
请说明:
□
本次研究符合原知情同意的许可条件。
请说明:
□
受试者的隐私和身份信息的保密得到保证。
请说明:
主要研究者签名:日期:
请说明:
□
受试者可能遭受的风险不超过最小风险。
请说明:
□
豁免知情同意不会对受试者的安全和权益产生负面影响。
请说明:
□
利用可识别身份信息的人体材料或者数据进行研究,已无法找到受试者,且研究项目不涉及个人隐私和商业利益。
请说明:
□
生物样本捐献者已经签署了知情同意书,同意所捐献样本及相关信息可用于所有医学研究。
免除知情同意申请书

免除知情同意申请书尊敬的[受理部门/相关负责人]:我是[申请人姓名]。
今天写这个申请书呢,心里是五味杂陈,但又充满了希望,希望您能耐心听我讲讲我的情况。
我知道知情同意是一件非常重要的事情,一般情况下那是必须得有的程序。
可是,我现在面临的状况真的有些特殊,就像走在一条弯弯绕绕的小路上,找不到别的出口,只能向您申请免除知情同意啦。
一、我的特殊情况。
我所在的[具体情况背景,例如项目、事件等],情况真的很紧急。
就好比着火了,大家都在忙着救火,根本没有时间去走那一套完整的知情同意流程。
每一分每一秒都特别宝贵,如果还按照常规流程来,可能会导致[描述可能产生的严重后果,例如失去最佳的治疗时机、错过重要的机会等]。
这可不仅仅是我一个人的事情,还牵扯到很多和我一样的小伙伴呢。
而且啊,这个事情的性质决定了即使没有知情同意,也不会对任何人造成实质性的伤害。
我们就像一群在暴风雨中想要找个地方躲雨的小蚂蚁,只是想尽快找到一个解决办法,让大家都能好过一点。
二、关于信息保护的保证。
我明白大家可能会担心信息泄露之类的问题。
您放心,我和我的小伙伴们都是特别守规矩的人。
我们会像守护宝藏一样守护所有相关的信息。
如果能够免除知情同意,我们也绝对不会把这些信息透露给任何不相关的人。
就像小松鼠守护自己的松果一样,紧紧地看住,不会让它有任何闪失。
我们会建立自己的一套信息管理办法,保证所有的信息都是安全的、保密的。
要是有谁敢违反这个规定,那我们就像对待破坏蜂巢的坏蛋一样,绝不轻饶。
三、对可能影响的理解。
我也清楚免除知情同意可能会带来一些影响。
但是在这个特殊的时候,我觉得我们可以把这些影响降到最低。
我们会尽我们所能去弥补可能因为缺少这个流程而产生的小漏洞。
就像缝衣服一样,虽然可能少了一颗纽扣,但我们会用其他的方式把这个小缺口补上,让整件事情看起来还是那么完整、那么和谐。
我真的是特别诚恳地向您提出这个申请。
我知道这可能有点不符合常规,但是就像在生活中有时候我们也得打破一些小规矩才能解决大问题一样。
免除知情同意申请报告

免除知情同意申请报告
伦理委员会:
项目名称:
一、免除审查的具体内容
□免除知情同意的审查□免除知情同意书签字的审查□免除部分或全部受试者签署书面知情同意的可能情况的审查
二、是否涉及其他伦理委员会
□否□是,请说明:
三、研究摘要,并请说明符合免除审查的理由
四、是否涉及既存数据或样本的研究
□否
□是,请简要说明当时招募受试者的方法及获取知情同意的方法:
五、其他问题(如申办者研究期限、研究者参加研究的任务已经完成等)
□无
□有,请说明:
报告人:报告日期:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
本研究对受试者造成的风险不大于最小风险,如果脱离“研究”背景,相同情况下的行为或程序不要求签署书面知情同意(如访谈研究,邮件/电话调查)。
请说明:
2.如果免除知情同意签字,本研究会做到:
向受试者或其法定代理人提供书面告知信息。
获得受试者或其法定代理人除知情同意签字申请表
项目名称
申请专业
主要研究者
申办单位
组长单位
注:对于批准的免除知情同意书面签字,伦理委员会一般要求研究者向受试者提供书面的研究告知信息并获得口头知情同意。
1.研究属于以下类别之一:
签署的知情同意书会对受试者的隐私构成不正当的威胁;联系受试者真实身份和研究的唯一记录是知情同意文件,并且主要风险就来自于受试者身份或个人隐私的泄露。
