硫酸锌溶液的电解
锌电积一种“烧板”的原因分析及处理

锌电积一种“烧板”的原因分析及处理文章阐述一种锌电积“烧板”的特征,并详细分析“烧板”产生的原因,结合生产实际提出处理措施。
标签:锌电积;有机物;烧板前言锌电解沉积是湿法炼锌系统的末端,是将净化后的硫酸锌溶液(新液)送入电解槽内通以直流电在阴极上析出金属锌(阴极锌),通过下面反应式进行反应:ZnSO4+H2O=Zn↓+H2SO4+1/2O2↑当电解溶液内存在杂质时析出的阴极锌会在杂质作用下重新溶解到液体内,并放出氢气,我们称之为阴极锌的返溶,俗称“烧板”。
[1]电积过程大面积”烧板”使得阴极锌产量下降,直流电单耗升高,大量电能损失,资源浪费,也使生产成本增加。
因此,需要严加控制“烧板”发生。
1 “烧板”发生及其特征2014年下半年净化工序更改除钴工艺,由原来的锌粉两段高温锑盐除钴更改为β-萘酚除钴工艺。
除钴工艺的优化大幅降低了锌粉和蒸汽消耗,按年产10万吨锌计算,年生产成本节约近1000万。
但新工艺运行以来,电解工序先后出现4次阴极锌大面积“烧板”事故,“烧板”时间一般持续3-5天,最长可达半月之久。
这几次发生的“烧板”事故与过去都不同。
表现为阴极锌大面积针眼,背面发黑,透酸严重,电解槽内出现大量白色泡沫且厂房内酸雾很浓。
阴极锌的边缘和中间出现局部返溶。
在阴极锌板面的中间出现3-5厘米不等的窟窿,板面出现反复析锌,表面形成年轮状。
在未返溶部分,致密度非常好,板面光亮,熔铸直产率也比较高。
2 原因分析(1)由于烧板的初期存在针眼和透酸,因此,曾怀疑常规元素超标导致,于是对新液和废液内的常规元素进行分析。
从表1可以看出常规元素除氯根外都在合格范围内,特别是对电解影响比较大的砷、锑、锗等含量都比较低,氯根基本不会对阴极锌板面产生影响,因此,可以排出常规元素影响。
(2)排除常规元素后,我们将关注的重点落在系统内添加的有机物上。
且这几次的“烧板”与资料内介绍的有机物烧板特征相似,如阴极锌下部和边缘有返溶现象,现场酸雾突起,槽内沸腾泛白等[2]。
电解硫酸锌方程式

电解硫酸锌方程式
电解硫酸锌方程式是指将硫酸锌溶液通过电解分解反应转化为锌金属和氧气的化学反应。
该反应可以用如下方程式表示:
ZnSO4 -> Zn + O2
在该方程式中,ZnSO4代表硫酸锌,Zn代表锌金属,O2代表氧气。
电解是一种通过外加电流使溶液中的化学物质发生氧化还原反应的方法。
在电解过程中,正极(阳极)会发生氧化反应,负极(阴极)会发生还原反应。
在电解硫酸锌中,硫酸锌溶液被电解时,硫酸锌分解成锌金属和氧气。
具体来说,硫酸锌是一种离子化合物,它在溶液中会完全离解成锌离子(Zn2+)和硫酸根离子(SO42-)。
在电解过程中,阳极上的氧化反应将发生,硫酸根离子(SO42-)会被氧化为氧气(O2),同时释放出电子。
而在阴极上的还原反应将发生,锌离子(Zn2+)会被还原为锌金属,并吸收电子。
总体来说,电解硫酸锌的反应方程式描述了硫酸锌溶液中的离子被电解分解为锌金属和氧气的过程。
通过电解,硫酸锌被分解成了其组成离子,并在阳极和阴极上发生了相应的氧化和还原反应。
这样的电解反应在实际应用中有一定的重要性。
例如,在电镀工业中,电解硫酸锌可以被用来镀锌。
在这个过程中,锌金属可以被沉
积在其他材料表面上,起到保护和防腐的作用。
此外,电解硫酸锌还可以用于制备其他锌化合物,如硫酸锌的盐类。
总结起来,电解硫酸锌方程式描述了硫酸锌溶液在电解过程中分解为锌金属和氧气的反应。
这个反应在电镀和制备锌化合物等领域有一定的应用价值。
锌冶金学硫酸锌溶液电解沉积.pptx

(2)小部分氧与阳极表面作用,参与形成过氧化铅(PbO2)阳极膜,形 成阳极钝化而起不溶性阳极的作用,并保护阳极不受腐蚀。
(3)一部分氧与溶液中二价锰作用形成高锰酸和二氧化锰,其反应为:
2MnSO4 + 3H2O + 5O2 = 2HMnO4 + 2H2SO4 该反应生成的MnO4-使无色硫酸锌溶液变成紫红色。 高锰酸继续与硫酸锰作用:
✓铜形成圆形透孔,周边不规则; ✓镍呈葫芦瓢形孔洞; ✓钴呈独立小圆孔,甚至烧穿成洞; ✓锗形成黑色圆环,严重时形成大面积针状小孔; ✓锑使阴极表面呈条沟状; ✓砷使阴极表面起皱纹,失去光泽,或呈苞芽状。
第30页/共101页
➢5.3.1.2 杂质在电解时的行为
第31页/共101页
➢5.3.1.2 杂质在电解时的行为
MnO2在阳极过多地析出,会增加浸出工序的负担,也会引起电积液中Mn2+ 的贫化而直接影响析出锌质量。
第24页/共101页
✓5.2.2 阳极反应
当溶液中含有氯离子时,在阳极氧化析出氯气, 污染车间空气,并腐蚀阳极:
2C1-2e = C12↑
E0=1.36V
C1- + 4H2O - 8e = C1O4- + 8H+ E0=1.39V
对于不同的阴极金属,常数b接近于0.12; 常数a值则介于0.1~ 1.5V之间,且受温度的影响大。
第12页/共101页
✓5.2.1 阴极反应
第13页/共101页
✓5.2.1 阴极反应
第14页/共101页
✓5.2.2 阳极反应
采用含银0.5~1%的铅银合金板作不溶阳极, 阳极上发生的主要反应是氧的析出:
硫酸锌水溶液的电积过程

硫酸锌水溶液的电积过程一、实验目的通过锌电积的实验过程,了解电积有关的仪器设备及操作,掌握槽电压、电流密度、电流效率以及电能消耗的测试与计算方法。
二、基本原理锌电积一般采用Pb-Ag( 1%)合金作阳极,纯铝板作阴极,以酸性硫酸锌溶液作电解液。
当通以直流电时,阴、阳极发生以下电化学反应:阴极 Zn 2++2e=Zn E o =-0.763V阳极 H 2O-2e=1/2O 2+2H + E o =-1.229V总反应 2221Zn H O Zn 2H O 2+++=++直流电三、实验方法、试剂和仪器设备实验方法如图示:试剂:硫酸锌,硫酸,铝板,铅板,抽水泵仪器设备:直流稳压稳流电源,万用电表,电解槽四、实验操作步骤1、先将铝阴极置于天平称重并记下重量,然后将铝阴极放入电解槽内,取出测量其浸入溶液的实际尺寸并计算面积,再根据已确定的铝阴极电流密度计算出所需电流强度。
2、接线:将直流稳压稳流电源、电解槽、阴阳极等仪器联结好,即可通电,并记下通电起始时间、电流强度及槽电压。
3、通电开始实验正常进行,可按规定项目进行记录。
4、电解进行30~45分钟实验结束,关闭所有电源。
同时取出铝阴极置于沸水中置2分钟,以除去硫酸盐结晶,然后放入烘箱烘干再取出称重,记下电解后阴极的重量。
五、安全措施及应注意的事项1、线路联结必须严格按操作步骤进行,经检查后方可通电,否则易损坏仪器设备并造成实验中断。
2、实验过程中,不得任意摆弄仪器开关、旋钮以及各接触点,以免因接触不良断电影响实验。
3、如遇仪器设备发生故障或因接触不良而引起断电,应立即报告认真检查原因及时处理。
六、数据的整理与分析1、记录内容:实验日期、题目名称A 、技术条件:a 、温度:室温b 、阴极面积: m 2c 、阴极电流密度:D K = 350~500A/m 2d 、电流强度: Ae 、同名极距:4~6cmf 、电解液成分(g/L):硫酸锌 0.75~0.8mol/L ,硫酸 1.0mol/LB 、电解前后铝阴极重量的变化。
一水硫酸锌的介绍、使用方法以及作用

一水硫酸锌的介绍、使用方法以及作用一水硫酸锌介绍一水硫酸锌,化学式为ZnSO4·H2O,是一种白色晶体粉末,是锌离子和硫酸根离子的化合物。
它是一种重要的工业原料,广泛用于电镀、印染、农业等领域。
一水硫酸锌的制备方法1.直接从硫酸和锌中生成:将锌精矿和浓硫酸混合,加热至50℃以上,反应生成二水合硫酸锌,然后加入适量蒸馏水,控制pH值为2~3,反应产生一水合硫酸锌,离心、干燥即可得到一水合硫酸锌。
2.从锌氢氧化物和硫酸中生成:将锌氢氧化物和浓硫酸混合,加热至85℃以上,反应生成一水合硫酸锌,离心、干燥即可得到一水合硫酸锌。
一水硫酸锌的使用方法1. 电镀一水硫酸锌在电镀行业中是一种广泛应用的电解液。
通过将一水硫酸锌溶液作为电解液,通过阳极和阴极的反应,形成锌层,从而实现对不同材料的电镀。
2. 印染一水硫酸锌被广泛用于印染工业中,主要用于棉、麻、丝等天然纤维和人造纤维的硫染色。
它可以与邻菲罗啉、氨和尘蚀剂等配合使用,以加速染料的着色反应。
3. 养殖业一水硫酸锌作为一种矿物营养素,可以用于养殖业中,以满足动物的生长发育和饲料增效的需要。
常用剂量是每吨饲料添加0.1%-0.2%的一水硫酸锌。
4. 其他工业领域一水硫酸锌在其他工业领域中也有广泛应用。
例如,它可以用作造纸工业的防腐剂,作为化学反应的催化剂,以及在橡胶、油漆和染料制造等方面发挥作用。
一水硫酸锌的作用1.电镀:一水硫酸锌作为电解液被广泛应用于金属电镀领域。
通过它可以制备出具有均匀光泽的金属制品,同时提高金属材料的防腐性能,延长使用寿命。
2.印染:一水硫酸锌可以加速染料的着色反应,提高染色效率。
此外,它还可以增加染料对纤维的亲和力,从而使染色更加牢固,不易褪色。
3.养殖业:锌是人体和动物所需的重要微量元素之一,在动物体内参与各种代谢过程。
一水硫酸锌作为一种矿物营养素,能够增强动物的免疫力和抗病能力,促进生长发育,提高繁殖能力。
4.其他工业领域:一水硫酸锌还可以用作催化剂,促进各种化学反应。
锌电解槽计算
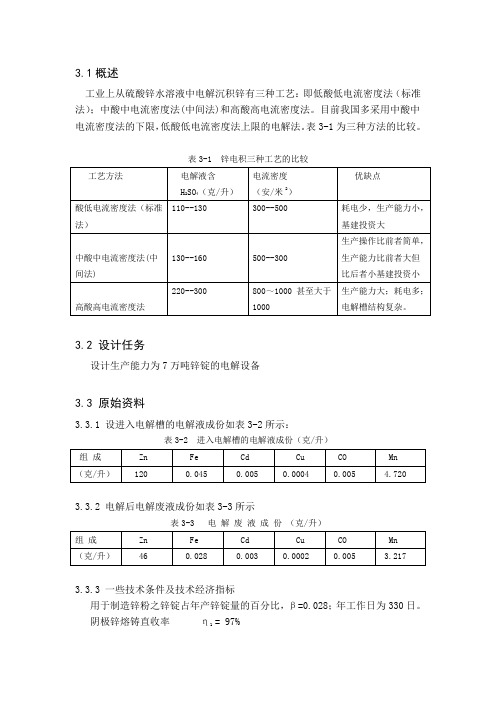
3.1概述工业上从硫酸锌水溶液中电解沉积锌有三种工艺:即低酸低电流密度法(标准法);中酸中电流密度法(中间法)和高酸高电流密度法。
目前我国多采用中酸中电流密度法的下限,低酸低电流密度法上限的电解法。
表3-1为三种方法的比较。
表3-1 锌电积三种工艺的比较3.2 设计任务设计生产能力为7万吨锌锭的电解设备3.3 原始资料3.3.1 设进入电解槽的电解液成份如表3-2所示:表3-2 进入电解槽的电解液成份(克/升)3.3.2 电解后电解废液成份如表3-3所示表3-3 电 解 废 液 成 份 (克/升)3.3.3 一些技术条件及技术经济指标用于制造锌粉之锌锭占年产锌锭量的百分比,β=0.028;年工作日为330日。
阴极锌熔铸直收率 η1 = 97%阴极电流密度 D 阴 = 520安培 槽电压 V 槽 = 3.20伏 电流效率 ηi = 98%阴极规格 长×宽×厚= 1000×666×4(毫米)3.4 工艺过程及设备计算3.4.1物料平衡及电解槽计算 阴极锌成份的计算在电积过程中,一部分铜、铁、镉与锌一齐在阴极上沉积,一升电解液得到的阴极锌含金属量如表3-4所示。
表3-4 一升电解液沉积的金属量(克)铅-银阳极在电解过程中被腐蚀,使一部分铅进入到阴极锌中。
设阴极锌含铅0.006%则进入到阴极锌中铅的量为:0038.0100006.00072.64=⨯克那么阴极锌的成份如表3-5所示。
表3-5 阴 极 锌 成 份3.4.2 所需电解槽数量的计算 (1)每日应产出的阴极锌量的计算。
Q 1=ηβm Q )1(+吨 式中: Q 1----每日应产出阴极锌的数量,吨; Q ----设计生产能力,吨锌锭/年;β----用于制造锌粉之锌锭占年产锌锭量的百分比,%; m ----年工作日,日;η----阴极锌熔铸直收率,%。
Q 1=22597.0330)028.01(70000=⨯+吨/日(2)阴极有效总面积及片数的计算 阴极有效总面积的计算。
硫酸锌做电解液对称电池的循环寿命

《硫酸锌做电解液对称电池的循环寿命》1. 硫酸锌电解液的基本原理硫酸锌在电化学中被广泛应用,尤其是作为电解液对称电池的重要组成部分。
作为一种含有锌离子和硫酸根离子的溶液,硫酸锌电解液具有很高的导电性和化学稳定性,这使得它成为制造对称电池的理想候选方案。
在对称电池中,硫酸锌电解液能够实现高效的电池循环,从而提高电池的循环寿命。
2. 硫酸锌电解液对电池循环寿命的影响硫酸锌电解液对电池循环寿命的影响是一个复杂的问题,需要考虑很多因素。
硫酸锌电解液的浓度和纯度对电池的循环寿命有重要影响。
一般来说,较高浓度和较高纯度的硫酸锌电解液能够更好地维持电池性能,并延长其循环寿命。
电解液的循环稳定性也是决定电池循环寿命的重要因素。
如果硫酸锌电解液在循环中发生分解或者污染,都会降低电池的循环寿命。
选用高质量的硫酸锌电解液并严格控制循环条件,是保证电池循环寿命的关键。
3. 提高硫酸锌电解液对称电池循环寿命的途径为了提高硫酸锌电解液对称电池的循环寿命,需要从多个方面进行改进。
应该加强对硫酸锌电解液质量的管控,确保其浓度和纯度符合要求。
应该优化电池的设计结构和工艺,以最大限度地减少硫酸锌电解液的分解和污染。
对硫酸锌电解液的循环条件和参数进行优化,也可以有效地延长电池的循环寿命。
4. 个人观点和理解作为一种重要的电化学材料,硫酸锌电解液对对称电池的循环寿命具有重要影响。
在实际应用中,我们应该重视对硫酸锌电解液质量的管控,并通过技术手段不断寻求提高其循环稳定性的方法。
只有这样,才能实现对称电池的高性能和长循环寿命。
5. 总结硫酸锌电解液对电池循环寿命的影响是一个复杂而重要的问题,需要综合考虑多个因素。
通过优化硫酸锌电解液的质量和循环条件,以及不断提高对称电池的设计和制造工艺,才能实现高性能和长循环寿命的电池。
在这篇文章中,我们深入探讨了硫酸锌电解液对对称电池循环寿命的影响,以及提高循环寿命的方法。
希望对您有所帮助。
硫酸锌作为一种重要的电解液,在对称电池中发挥着关键的作用。
锌电解工艺操作规程

南丹县南方有色冶炼有限责任公司NDNF/JS—SC06~2010锌电解工艺操作规程发放编号:控制状态:编制:梁世心审核:刘旭升曹晓星批准:2010年7月20日发布2010年8月1日实施南丹县南方有色冶炼有限责任公司发布1 范围本规程包括锌电解的工艺流程、大体原理、原材料及其要求、工艺操作条件、职位操作法、产出物料及其质量要求、主要技术经济指标和主要设备。
2 工艺流程锌电解工艺流程见图13 大体原理电解锌沉积大体原理经净化除去各类有害杂质的硫酸锌水溶液,以Pb~Ag为主要成份的多元合金板作阳极,纯铝压延板作阴极,在外电势直流电作用下,溶液中带正电荷的锌离子在阴极按(1)式放电沉积Zn2++SO42-+2e→Zn↓+ SO42-(1)而溶液中带负电荷的OH离子在阳极上按(2)式放电析出。
2H++2OH-2e→2H++H2O+1/2O2↑(2)硫酸锌水溶液电解沉积进程总反映按(3)式进行。
ZnSO4+H2O=Zn↓+H2SO4+1/2O2↑(3)空气冷却塔冷却原理从塔上部喷洒下来的热电解废液与从塔下鼓入的空气逆流运动,由于对流、热传导,电解废液中水分的蒸发带走汽化潜热,使电解废液冷却。
4 原材料及其质量要求电解新液化学成份(mg/L)Zn 120~180g/L Mn ~15g/L Cu≤Cd≤Co≤Ni≤As≤Sb≤Ge≤Fe≤20比重:~。
物理规格:清亮、无色、透明、无悬浮物。
碳酸锶应符合GB/T10660的规定具体要求:白色、无臭、无味、粉末状、不溶于水、比重,含SrCO3≥95%,无严重结块及其它杂物。
骨胶、茶褐色、半透明固体,片状或W形颗粒状,无异物。
酒石酸锑钾(俗称吐酒石):工业纯锌电解沉积5.1.1 电解新液成份()。
5.1.2 电解废液成份:Zn 40~65g/L H2SO4 130~220g/L。
5.1.3 混合比15~20:15.1.4 槽温32~45℃5.1.5 流量150~200m3/h·列5.1.6 日平均电流密度400~550A/m2,短时最高电流密度≯650A/m2。
锌电解操作工艺

锌电解操作工艺(2010-12-27 19:20:34)转载标签:杂谈一范围本标准规定了电解工艺的基本原理,。
工艺操作条件,岗位操作法, 原材料质量要求,产出物料质量要求,主要技术经济指标和主要设备.二工艺目的及原理1.工艺目的使溶液中的锌通过电积提锌得到锌片,再熔铸成成品锌。
1.原理锌电积一般釆用Pb-Ag(1%Ag)合金板为阳极,纯铝板为阴极,以酸性硫酸锌水溶液作为电解液,当通以直流电时,在阴极上发生锌的析出,在阳极上放出氧气。
阴极上 Zn2++2e=Zn阳极上 H2O-2e=1/2O2 +2H+总反应式为 ZnSO4+H2O=Zn+H2SO4+1/2O2因此,随着电解过程的进行,电解液中的含锌量不断减少,硫酸含量不断增加,为了保持电积条件的稳定,必须不断抽取一部分电解作为废液返回浸出,同时,相应地加入净化了的中性硫酸锌溶解,以补充所消耗的锌量,维持电解液中一定的H+,Zn2+含量,并稳定电解系统中的体积。
三硫酸锌溶液电解锌的生产工艺流程四原辅材料质量要求。
1. 新液成份(g/l)符合企业标准的规定Zn120-150 Cu≤0.002 Cd≤0.003 Fe≤0.015 Co≤0.0015 Ni≤0.0015 As≤0.003 Sb≤0.0005 Ge≤0.00005Mn2.5-52. 废液成份(g/l)Zn35-60 H+140-200五工艺操作条件1. 槽温 37 -42℃2. 电流密度 500-550A/m23. 槽电压3.2-3.3V4. 析出周期 24h5. 同极中心距 62mm6 . 添加剂(1) 吐酒石:出槽前3min-5 min加入电解槽内,一般加入量为0..05-0.1g/槽(2) 骨胶:装槽前1h-3h后加入电解槽内,加入量一般为0.25kg/t锌析出-0.5 kg/t析出锌(3) 碳酸锶视锌析出含铅情况,每班在电解槽内加8次,每次加10-20 kg7. 周期管理掏槽周期 30-40d平刷阳极周期 4-5d平整阴极周期30-40d8. 空气冷却塔主要技术条件进液温度 37-42℃出液温度 30-37℃喷洒压力 0.05MPa清理周期 1-2个月六岗位操作法1. 按槽上把<四关>、槽下<七不准>操作法进行操作(1)槽上把<四关>(a) 导电关:导电头擦亮打紧,两极对正,极距均匀,消灭短、断路板;(b) 极板关:接触准确,及时平整阴阳极板,不合格阴极铝板不装槽;(c) 检查关:精心检查,调整,保证导电良好, 槽上整齐清洁,杂物不得入内;(d) 添加剂关:适时、适量添加添加剂(吐酒石、骨胶、碳酸锶)。
硫酸锌溶液的电积过程
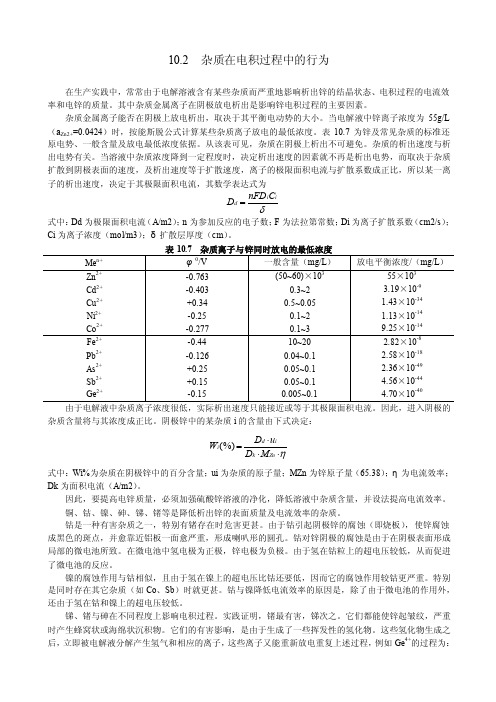
10.2 杂质在电积过程中的行为在生产实践中,常常由于电解溶液含有某些杂质而严重地影响析出锌的结晶状态、电积过程的电流效率和电锌的质量。
其中杂质金属离子在阴极放电析出是影响锌电积过程的主要因素。
杂质金属离子能否在阴极上放电析出,取决于其平衡电动势的大小。
当电解液中锌离子浓度为55g/L (a Zn2+=0.0424)时,按能斯脱公式计算某些杂质离子放电的最低浓度。
表10.7为锌及常见杂质的标准还原电势、一般含量及放电最低浓度依据。
从该表可见,杂质在阴极上析出不可避免。
杂质的析出速度与析出电势有关。
当溶液中杂质浓度降到一定程度时,决定析出速度的因素就不再是析出电势,而取决于杂质扩散到阴极表面的速度,及析出速度等于扩散速度,离子的极限面积电流与扩散系数成正比,所以某一离子的析出速度,决定于其极限面积电流,其数学表达式为δii d C nFD D =式中:Dd 为极限面积电流(A/m2);n 为参加反应的电子数;F 为法拉第常数;Di 为离子扩散系数(cm2/s );Ci 为离子浓度(mol/m3);δ扩散层厚度(cm )。
杂质含量将与其浓度成正比。
阴极锌中的某杂质i 的含量由下式决定:η⋅⋅⋅=Zn k id i M D u D W (%)式中:Wi%为杂质在阴极锌中的百分含量;ui 为杂质的原子量;MZn 为锌原子量(65.38);η为电流效率;Dk 为面积电流(A/m2)。
因此,要提高电锌质量,必须加强硫酸锌溶液的净化,降低溶液中杂质含量,并设法提高电流效率。
铜、钴、镍、砷、锑、锗等是降低析出锌的表面质量及电流效率的杂质。
钴是一种有害杂质之一,特别有锗存在时危害更甚。
由于钴引起阴极锌的腐蚀(即烧板),使锌腐蚀成黑色的斑点,并愈靠近铝板一面愈严重,形成喇叭形的圆孔。
钴对锌阴极的腐蚀是由于在阴极表面形成局部的微电池所致。
在微电池中氢电极为正极,锌电极为负极。
由于氢在钴粒上的超电压较低,从而促进了微电池的反应。
锌电解的目的与原理

锌电解的目的与原理锌电解是一种常见的电化学反应,其目的是通过电解过程将锌金属转化为溶解态的锌离子。
锌电解的原理基于电解质溶液中的离子迁移和电子转移。
锌电解的目的之一是用于锌的提取和精炼。
锌是一种重要的金属,广泛应用于电池、合金、镀层等领域。
通过锌电解,可以将锌金属从矿石或废旧物品中提取出来,并得到高纯度的锌。
锌电解的原理涉及到电解质溶液中的离子迁移和电子转移。
在锌电解中,通常使用含有锌离子的电解质溶液,如硫酸锌溶液。
锌离子在溶液中以Zn2+的形式存在。
在锌电解过程中,需要一个电解槽,其中包含两个电极:阳极和阴极。
阳极通常由铅制成,阴极则是锌金属板。
阳极和阴极之间通过电解质溶液连接。
当外部电源连接到电解槽时,电流开始流动。
在电解质溶液中,锌离子会向阴极迁移,同时电子从阴极流向阳极。
在阴极上,锌离子接受电子并还原为锌金属。
这个过程称为还原反应。
还原反应的化学方程式为:Zn2+ + 2e- →Zn在阳极上,电子流向阳极,发生氧化反应。
在锌电解中,通常发生水的氧化反应,生成氧气和氢离子。
氧化反应的化学方程式为:2H2O →O2 + 4H+ + 4e-整个锌电解过程可以总结为:锌离子在电解质溶液中向阴极迁移,接受电子并还原为锌金属,同时水在阳极发生氧化反应,生成氧气和氢离子。
锌电解的原理还涉及到电解质溶液中的离子迁移。
在电解质溶液中,离子迁移是由于电场力的作用。
当外部电源连接到电解槽时,电源产生的电场会引起溶液中的离子迁移。
正离子(如锌离子)会向阴极迁移,负离子则会向阳极迁移。
锌电解的效果受到多种因素的影响,包括电流密度、电解质浓度、温度等。
较高的电流密度和较低的电解质浓度可以提高锌电解的效率。
此外,温度的升高也有助于提高锌电解的效果。
总之,锌电解是一种通过电解质溶液中的离子迁移和电子转移将锌金属转化为溶解态的锌离子的过程。
锌电解的目的是用于锌的提取和精炼,其原理涉及到锌离子的还原和水的氧化反应,以及电解质溶液中的离子迁移。
硫酸锌溶液的电解

精选课件
与铜电解精炼 的异同之处?
3
5.1 锌电解液成分及锌电积生产过程
▪ 5.1.1 锌电解液
主要成分:
硫酸锌:Zn2+(40~60g/L)
硫 酸:H2SO4(110~140g/L) 水
杂质成分:
少量金属的硫酸盐、部分阴离子(Cl-、F- )。
精选课件
11
5.2.1 阴极反应
在锌电积时移向阴极的正离子主要有Zn2+、H+。因此, 在阴极上可能进行如下两个主要反应:
Zn2+ + 2e = Zn E θ Zn2+/Zn = -0.763 V 2H+ + 2e = H2 E θ H+/H2 =0.0 V
电化学理论:较板阴极,并联交错悬挂于槽内,
通以直流电,在阴极析出金属锌,在 阳极放出氧气。
随着电积的不断进行电解液含锌
量逐渐减少,而硫酸含量则逐渐增加, 为保证电积条件的稳定,必须不断地 补充新液。
电积一定时间后,提出阴极板,
剥下压延铝板上的析出锌片送往熔铸 工序。
精选课件
5
❖5.5 锌电解车间的主要设备
在实际的电积锌过程中,必须考虑由极化现象而产生电极
反应的超电压()对实际析出电位的影响。
(1) Zn2+ → Zn的极化作用很小,故析出锌的超电位可以忽略不计; (2) 氢在锌阴极上析出的超电位很大(约1.1V)。
E Zn = -0.763 -Zn = -0.763 V
E H2 =0 -H =-1.1精V选课件
杂质含量(mg/L)要求:
Cd<0.3、Co<0.3、Sb<0.03、Ge<0.03 、
5硫酸锌溶液的电解沉积原理(2)

5硫酸锌溶液的电解沉积原理(2)5.2.2阴极过程5.2.2.1在工业生产条件下,锌电积液中含有Zn2+50~60g/L和H2SO4120-180g/L。
如果不考虑电积液中的杂质,则通电时,在阴极上仅可能发生两个过程。
(1)锌离子放电,在阴极上析出金属锌:Zn2++2e=Zn φ?(18)=―0.763V (18)(2)氢离子放电,在阴极上放出氢气:2H++2e=H2 φ?(19)=0.000V (19)在这两个放电反应中,究竟哪一种离子优先放电,对于湿法炼锌而言是至至关重要的。
从各种金属的电位序(见表4―4)来看,氢具有比锌更大的正电性,氢将从溶液中优先析出,而不析出金属锌。
但在工业生产中能从强酸性硫酸锌溶液中电积锌,这是因为实际电积过程中,存在由于极化所产生的超电压。
金属的超电压一般较小,约为0.03伏,而氢离子的超电压则随电积条件的不同而变。
塔费尔通过实验和推导总结出了超电压与电流密度的关系式,即著名的塔费尔公式:ηH=a+blgD K式中ηH——氢的超电压,a——常数,即电极上通过单位电流密度时的超电压值,随阴极材料、表面状态、溶液组成和温度而变;b——;只随电解液温度而变。
D k——阴极电流密度。
因此,电积时可创造一定条件,由于极化作用氢离子的放电电位会大大地改变,使得氢离子在阴极上的析出电位值比锌更负而不是更正,因而使锌离子在阴极上优先放电析出。
这就是锌电积技术赖以成功的理论依据。
5.2.2从以上分析可见,氢的超电压在锌电积实际生产中具有重要意义。
根据塔费尔公式,影响氢在阴极析出的超电压的主要因素有:由塔费尔公式可见,a值改变,氢的超电压就改变,即氢的超电压随阴极材料而定。
表5—1列出了在不同金属阴极上析出氢的超电压值。
从表中可以看出,在不同金属的阴极上氢析出超电压值相差较大。
大体上可分为三类:高超电压金属:Pb、Cd、Hg、T1、Zn、Sn;中超电压金属:Fe、Co、Ni、Cu、Au。
硫酸锌水溶液的电积过程

1 2
三、实验原理
硫酸锌溶液电积过程采用Pb-Ag(1%)合金作 阳极,纯铝板作阴极,以酸性硫酸锌溶液作电解 液。当通以直流电时,阴、阳极发生以下电化学 反应:
阴极 Zn2++2e
阳极 O2--2e
Zn
O2
总反应 Zn2++O2-+电
(一)简述实验的基本原理与实验方法; (二)数锯记录与计算
1. 技术条件
a、温度 ℃; b、阴极面积 m2;c、阴极电流密度 A/m2;d、极距 e、电解液成分(mol/L):硫酸锌 Mol/L,硫酸 Mol/L。 cm;
2. 电解前后铝阴重量的变化
电解前重(克) 铝阴极 电解后重(克) 增重(克)
电能消耗 平均槽电压 锌电化当量 1000 电流效率 100 %( kwh / t . zn )
五、学生实验报告要求
(三)思考题 1. 在湿法冶金中,电积与电解精炼在概念上有何 不同,如何区别,指出它们之间的不同处? 2. 在锌电积过程中溶液的主成分会发生什么变化 ,这些变化对电积会产生什么影响,如何克服?
硫酸锌水溶液的电积过程
材料学院(材料加工实验中心):姚怀
Henan University of Science & Technology
一、实验目的 通过硫酸锌溶液电积实验过程, 了解与电积过程有关的仪器设备 及操作。 掌握稳压稳流电源的应用以及电 流效率、电能消耗的测试与计算。
二、实验设备及药品
四、实验内容
4、待电解液加热到35-40℃时,通电,迅速调解 电流,使其与计算的电流相接近,并记下通电起 始时间、电流强度及槽电压; 5、电解进行30-45分钟实验结束,关闭所有电源 ,同时取出铝阴极置于蒸馏水中2分钟,以除去硫 酸盐结晶,然后放入烘箱烘干再取出称重,记下 电解后阴极的重量。
硫酸锌溶液的电解

contents
目录
• 电解原理及基本概念 • 实验装置与操作方法 • 阳极反应及产物鉴定 • 阴极反应及产物鉴定 • 电解过程中能量转化与效率评估 • 硫酸锌溶液电解应用前景展望
01 电解原理及基本概念
电解定义与过程描述
电解定义
电解是指在电场作用下,电解质 溶液或熔融电解质中阴阳离子发 生定向迁移,并在电极上发生氧 化还原反应的过程。
用率。
在环保领域应用前景探讨
废水处理
硫酸锌溶液电解过程中产生的氢氧根离子可以与废水中的 重金属离子发生沉淀反应,从而去除废水中的污染物。
大气污染治理
利用硫酸锌溶液电解产生的臭氧等强氧化剂,可以氧化分 解大气中的有害气体,达到治理大气污染的目的。
土壤修复
通过向污染土壤中添加硫酸锌溶液并进行电解,可以使土 壤中的重金属离子发生迁移和转化,降低土壤毒性。
在硫酸锌溶液中,存在锌离子 (Zn^2+)和硫酸根离子(SO4^2)。
02 实验装置与操作方法
实验器材准备及搭建过程
01
02
03
电源
提供稳定的直流电源,通 常使用电池或电源供应器。
电解槽
用于容纳硫酸锌溶液的容 器,通常由玻璃或塑料制 成。
电极
用于连接电源和电解槽的 导体,常用的电极材料包 括铜、锌等。
提高电解过程的效率。
06 硫酸锌溶液电解应用前景 展望
在冶金领域应用潜力挖掘
提取金属锌
01
通过电解硫酸锌溶液,可以高效地提取金属锌,为冶金工业提
供重要的原料。
制备锌合金
02
电解得到的金属锌可以与其他金属元素合成锌合金,扩展其在
冶金领域的应用范围。
锌电积车间工艺.2021最全优质PPT

2OH-_2e H2O+½O2↑(阳极反应) 硫酸锌溶液电解沉积总反应式为:
直流电
ZnSO4+H2O+e
Zn+H2SO4+½ O2↑
2
1.2 工艺流程
药剂制备槽
新液 新液贮槽
药剂中转槽
风冷塔集液池 缓冲喂液槽
去浸出
废液贮槽
电 解槽 溶液冷却循环池
风冷塔
3
二 锌电积厂房基本条件
2.1 基本参数:
产能
在最佳性能,所有管道和风冷塔分布系统都是干净的才能 实现。总的来说,废液循环泵是关键,废液循环泵每分钟 必须产大约3800L溶液到主喂液管。这时是在运行中的列 和槽中均匀的分布。每个槽每分钟大约接收60L溶液。流 过电解槽的溶液又返回到废液循环槽。废液循环泵必须将 足够的溶液泵到风冷塔,以确保废液循环泵不受限制。
槽内阴阳极板接触使电能消耗在短路发热上,而不是用于锌的沉 积。锌的枝状结晶和阳极板上的二氧化锰层太多,会增加接触的几率 。避免或限制这种现象的发生,阳极板必须保证有效的拍平周期。
10
四 电解液的循环
4.1电解液的循环
• 流过电解槽的精确的电解液流量是很重要的。工艺操作 人员的职责是让流量最大化流入电解车间。这只有在泵处
长,—电流效率会降低,锌片含铅也会升高。 —杂质含量和有机物的添加
7
3.2 杂质对电解的影响 杂质的类型 杂质对电解的影响很大,具体可分成以下几类:
※氟 使析出锌难剥,氟能溶解阴极铝表面的氧化层,使在电积时锌和铝
相互渗透,紧紧地吸附在一起,即析出锌难以剥离。 ※氯
氯的一个很重要的反应是在阳极释放氯气。氯气释放在空气中是很 有危害的,同样氯还溶解阳极。它对阳极板来说是危害很大的杂质。 锰离子含量可以抑制氯的危害.
硫酸锌溶液的电解沉积讲义

硫酸锌溶液的电解沉积-原理(1)5.1概述硫酸锌溶液的电解沉积是湿法炼锌流程中四个重要工序中的最后一个。
其目的主要是从硫酸锌溶液中提取纯度高的金属锌。
电积的技术经济指标不仅反映出整个炼锌工艺的好坏,而且因直接消耗大量电能,在很大程度上影响着电锌厂的生产成本。
硫酸锌溶液的电解沉积是湿法炼钟的最后一个生产工序。
其目的主要是从硫酸锌溶液中提取纯度高的金属锌。
硫酸锌溶液电解沉积就是:以净化的硫酸锌溶液作电解液,以铅银合金板(含银1%)做阳极,压延铝板做阴极,在直流电的作用下,阴极上析出金属锌(称阴极锌),在阳极上放出氧气。
随着过程的不断进行,电解液中的含锌量不断减少,硫酸含量不断增加,至一定程度后就不能再供正常电积之用。
这时的电解液叫做废电解液(电积废液)。
废电解液连续不断地从电解槽的出液端溢出,一部分与新液混合供电解液循环用,一部分送往浸出车间供浸出用。
每隔一定时问取出阴极将析出锌剥下进去熔化铸锭,成为锌成品。
阴极铝板经过清刷处理以后,再装入电解槽中,继续进行电解沉积。
电解沉积锌的过程一般可以分为三种方法:标准法、中酸中电流密度法、和高酸高电流密度法。
标准法采用300~400A/m2的电流密度,电解液含酸100~130g/L,中酸中电流密度法采用400~600A/m2的电流密度,电解液含酸130~160g/L;高酸高电流密度法采用600~1000A/m2的电流密度,电解液含酸220~300g/L。
三种方法原理是一样的,只不过是所用的电流密度和电积液酸度有较大差别而已。
增加电流密度,可提高电积槽的锌产量,但电积液必须除去更多的热量,纯度要求也更严格。
过去采用低酸低电流密度法的电锌厂较普遍,但它限制了生产过程的强化。
因此,现在的电锌厂多使用中酸中电流密度法,在操作良好的条件下,可以获得高于90%的电流效率。
采用高酸高电流密度法的电锌厂(如美国克洛格电锌厂,采用960A/m2,H2SO4260g/L的作业条件)必须在高锌含量下作业,以保证溶液中的锌酸比高于足以避免析出锌反溶的程度,返回的废液由于含酸高,更容易溶解焙砂中的铁酸锌。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电化学理论:较正电位的离子优先在阴极上放电析出
在实际的电积锌过程中,必须考虑由极化现象而产生电极 反应的超电压()对实际析出电位的影响。
(1) Zn2+ → Zn的极化作用很小,故析出锌的超电位可以忽略不计; (2) 氢在锌阴极上析出的超电位很大(约1.1V)。
E Zn = -0.763 -Zn = -0.763 V E H2 =0 -H =-1.1 V
MnSO4+HMnO4+2H2O = 5MnO2↓+3H2SO4
生成的MnO2 ,一部分沉于槽底形成阳极泥,一部分 附于阳极表面形成比较致密的MnO2薄膜,保护阳极不受 腐蚀。(Mn<1.8g/L) 在 正 常 条 件 下 , 氧 的 析 出 约 占 阳 极 总 电 流 的 98%, Mn2+氧化生成MnO2约占1%。
电解槽内发生的总反应为: Zn2+ + H2O = Zn + 1/2O2 + 2H+
5.2.1 阴极反应
在锌电积时移向阴极的正离子主要有Zn2+ 、H+ 。因此, 在阴极上可能进行如下两个主要反应: Zn2+ + 2e = Zn 2H+ + 2e = H2 E θ Zn2+/Zn = -0.763 V E θ H+/H2 =0.0 V
同氢在阴极析出一样,氧在阳极析出也有超电位存在;不 同的时,生产中力求降低氧的超电位已提高电能效率。
阳极上放出的氧,消耗于三个方面:
(1)大部分氧在阳极表面形成气泡,并吸附少量的酸和水 逸出电解槽形成酸雾,使设备腐蚀,劳动条件恶化; (2)小部分氧与阳极表面作用,参与形成过氧化铅 (PbO2)阳极膜,形成阳极钝化而起不溶性阳极的作用,并 保护阳极不受腐蚀。(阳极镀膜) (3)一部分氧与溶液中二价锰作用形成高锰酸和二氧化锰, 其反应为: 2MnSO4 + 3H2O + 5O2 = 2HMnO4 + 2H2SO4 该反应生成的MnO4-使无色硫酸锌溶液变成紫红色。 高锰酸继续与硫酸锰作用:
在锌电积过程中,氢气析出不可避免。为了提高锌的电 流效率,必须设法提高氢析出超电压。 氢析出超电压与阴极材料、阴极表面状态、电流密度、 电解液温度、添加剂及溶液成份等因素有关。氢的超电压随
电流密度的增大、电解液温度的下降以及添加胶等而增大,
随着电解液酸度的提高和中性盐浓度的增加而降低,当溶液 中加有铜、锑、铁、钴等大大降低超电压。
5.5 锌电解车间的主要设备
5.5.5 剥锌机
5.2 锌电积过程的理论基础
锌电积的电解液的主要成份为ZnSO4、H2SO4和H2O, 并含有微量杂质金属铜、镉、钴等的硫酸盐。对于纯硫酸 锌溶液,通以直流电时,发生的电极反应为:
阴极 Zn2+ + 2e = Zn
阳极
H2O - 2e = 1/2O2 + 2H+
Hale Waihona Puke ZnSO4 H2O Zn H2SO4 1 O2 2
与铜电解精炼 的异同之处?
5.1 锌电解液成分及锌电积生产过程
5.1.1 锌电解液 主要成分: 硫酸锌:Zn2+(40~60g/L) 硫 酸:H2SO4(110~140g/L) 水 杂质成分: 少量金属的硫酸盐、部分阴离子(Cl-、F- )。 杂质含量(mg/L)要求: Cd<0.3、Co<0.3、Sb<0.03、Ge<0.03 、 Fe<10 、Cl<50~100 、F<10 、Mn<1.8g/L
5.2.2 阳极反应
阳极上主要有两类反应:一是铅阳极少量氧化溶解;二是 析出氧气。 析出氧的反应:
2OH- - 2e = H2O + 1/2O2 SO4 2- - 2e = SO3 + 1/2O2 Eθ=0.401V Eθ= 2.42 V
电化学理论:在阳极上较负电位的离子优先放电
因此,在阳极发生的主要是0H-的放电析出氧气的反应,随着反应的 进行溶液中H+不断增加,从而与硫酸根离子结合形成硫酸,这是锌焙砂浸 出过程中所需要的,保证了整个锌冶金过程的酸平衡。
3、负离子的影响
氯离子会腐蚀阳极,使阴极锌的含铅量增加而降低电锌 质量,同时缩短阳极寿命。 Pb + 6H+ + ClO3- = Pb2+ + Cl- + 3H2O 当有MnO2存在时,可抑制氯离子的危害。 MnO2 + 4H+ + 2Cl- = Mn2+ + C12 + 2H2O 氟离子会破坏阴极铝板表面的氧化膜,使锌与铝板发生 粘结,使锌片难于剥离。加入酒石酸锑钾可改善剥离情况。
综上所述,为了生产高纯度的锌,提高电效、降低电耗, 对净化液中及精矿中的杂质含量严格要求在限度以下 。
《锌冶金》
硫酸锌溶液的电解沉积
5 硫酸锌溶液的电解沉积
5.1 锌电解液成分及锌电积生产过程 5.2 锌电积过程的理论基础 5.3 锌电解车间的主要生产设备及布置 5.4 锌电解的正常操作 5.5 锌电解生产的主要技术条件与指标分 析 5.6 阴极锌熔铸
锌的电解沉积是湿法炼锌的最后一个工序,是用电解的 方法从硫酸锌水溶液中提取纯金属锌的过程。
铅阳极溶解反应:
阳极可能发生的反应有以下四个:
(1)Pb + SO42- - 2e = PbSO4 Eθ =-0.356V Eθ =1.685V
(2)PbSO4 + 2H2O - 2e = PbO2 + 4H+ + SO42(3)Pb + 2H2O - 4e = PbO2 (4)2OH- - 2e = H2O + 1/2O2 Eθ =0.655V Eθ=0.401V
5.1.2 锌电积生产过程
硫酸锌溶液的电积过程是将已经 净化好的硫酸锌溶液以一定比例同废 电解液混合后连续不断地从电解槽的 进液端送入电解槽内。 铅银合金板(含银1%)阳极和压 延铝板阴极,并联交错悬挂于槽内, 通以直流电,在阴极析出金属锌,在 阳极放出氧气。 随着电积的不断进行电解液含锌 量逐渐减少,而硫酸含量则逐渐增加, 为保证电积条件的稳定,必须不断地 补充新液。 电积一定时间后,提出阴极板, 剥下压延铝板上的析出锌片送往熔铸 工序。
2、比锌负电性杂质的影响
钾、钠、铝、镁、钙等杂质比锌更负电性,在电积时不 在阴极析出,因此对锌化学成分影响不大。但这类杂质 在富集后会使电解液的粘度和电阻增大而增加电能消耗, 特别是镁。当钙含量过高时,易形成硫酸钙与硫酸锌的 共结晶,造成冷却器和管道的结垢现象,阻塞管道,影 响操作。 锰离子除上述不良影响外,Mn7+离子会使砷、锑危害更 严重。但锰还有有益的作用,如生成MnO2对铅阳极有一 定的保护作用,同时可以吸附砷、锑、钴,减少他们的 危害。
(超电位较高)
首先发生反应(1),铅溶解并生成硫酸铅,由于硫酸铅的溶解度很小, 便开始在阳极表面结晶析出,直到整个硫酸铅膜覆盖整个阳极表面时为止, 然后开始发生反应(4),但因氧的析出超电位较高,所以实际先发生反应 (3)和(2),即铅直接氧化或二价铅离子的再氧化成四价状态,生成二 氧化铅。二氧化铅逐步将硫酸铅膜所替代,此过程为阳极镀膜。 二氧化铅成为进行正常阳极反应,即氧析出过程的工作表面。
1、比锌正电性杂质的影响
铅、镉、锡、铋较锌优先放电并在阴极上沉积析出,降 低电锌质量。 铁、铜、钴、镍在阴极上较锌优先析出,降低电锌质量, 在阴极上造成各种“烧板”现象,显著降低电解锌生产的电流 效率从而使产品的电耗增大。 锗、砷、锑严重地降低电流效率和增加电能消耗。锗与锑 共存时危害加剧,锗、锑还会加剧其它杂质的危害。锗、砷、 锑都会使阴极锌起皱,严重时产生蜂窝状或海绵状沉积物,严 重降低电锌质量。向电解液中加入胶质,可不同程度地消除锗 与锑的危害。
5.2.3 电解液中的杂质在电积过程中的行为
电解液中微量杂质的存在,能改变电极和溶液界面的结 构,直接影响到析出锌的结晶状态,降低电流电效率及电锌 质量。 电解液中的杂质可分为三类:
1、比锌正电性的杂质:Fe、Co、Ni、Cu、Pb、Cd、As、Sb
2、比锌负电性的杂质:K、Na、Ca、Mg、Al、Mn 3、阴离子:F-、Cl-
