第五章分子发光分析法
分子发光分析法

3.检测器 3.检测器
荧光计采用光电管作检测器 荧光分光光度计采用光电倍增管作检测器 电感耦合器件(charge couple device, CCD)
四、荧光分析方法与应用
1. 特点: 特点: (1)灵敏度高 比紫外-可见分光光度法高2~4个数量级
?
光度法 A = lg I0/I = KC 荧光法 I= KC
(c) 刚性平面结构:可减少分子振动,减少与溶剂的相互作用 刚性平面结构:
(d) 取代基效应 取代基效应:给电子取代基使荧光增强;吸电子取代基使荧光减弱 如苯胺和苯酚荧光较强,而硝基苯为非荧光物质 (e)重原子效应 )重原子效应:卤素取代基随原子序数的增加,荧光减弱,而磷光增强
(3)荧光螯合物 荧光螯合物
I p = 2 . 3ϕ p I o c
式中:Ip 为磷光效率,Io 为激发光的强度人为磷光物质的摩尔吸收系数,b为 试样池的光程。在一定的条件下,ϕ 、I p、 、b均为常数,因此上式可写成: κ
I p = Kc
根据上式可以用磷光强度对磷光物质浓度制作定量分析的标准曲线
2. 温度对磷光强度的影响:随着温度的降低,磷光逐渐增强 温度对磷光强度的影响: 3.重原子效应: 3.重原子效应:重原子的高核电荷使磷光分子的电子能级交错,容易引 重原子效应 起或增强磷光分子的自旋轨道偶合作用,从而使S 起或增强磷光分子的自旋轨道偶合作用,从而使S1→ T1的体系间窜跃 概率增大,有利于增大磷光效率。 4.室温磷光 4.室温磷光 (1)固体基质:在室温下以固体基质吸附磷光体,增加分子刚性、减少三重 态猝灭等非辐射跃迁,从而提高磷光量子效率。 (2)胶束增稳:利用表面活性剂在临界浓度形成具多相性的胶束,改变磷光 体的微环境、增加定向约束力,从而减小内转换和碰撞等去活化的几率,提 高三重态的稳定性。 (3)敏化磷光: 激发三重态将能量转移于另一易发磷光的受体,让其法磷光
分子发光—荧光、磷光和化学发光法

第5章分子发光—荧光、磷光和化学发光法(Molecular Emisssion and Luminescence)(3学时)教学目的和要求:1.学会分子发光——荧光、磷光和化学发光原理。
2.了解分子发光——荧光、磷光和化学发光法的特点和应用。
教学要点和所涵盖的知识点:荧光、磷光和化学发光原理、仪器、分析方法及应用重点和难点:荧光的原理、仪器、分析方法及应用。
分子发光:处于基态的分子吸收能量(电、热、化学和光能等)被激发至激发态,然后从不稳定的激发态返回至基态并发射出光子,此种现象称为发光。
发光分析包括荧光、磷光、化学发光、生物发光等。
物质吸收光能后所产生的光辐射称之为荧光和磷光。
第一节荧光分析法一、概述分子荧光分析法是根据物质的分子荧光光谱进行定性,以荧光强度进行定量的一种分析方法。
荧光分析的特点:灵敏度高:视不同物质,检测下限在0.1~0.001μg/mL之间。
可见比UV-Vis 的灵敏度高得多。
选择性好:可同时用激发光谱和荧光发射光谱定性。
结构信息量多:包括物质激发光谱、发射光谱、光强、荧光量子效率、荧光寿命等。
应用不广泛:主要是因为能发荧光的物质不具普遍性、增强荧光的方法有限、外界环境对荧光量子效率影响大、干扰测量的因素较多。
二、基本原理1、分子荧光的产生处于分子基态单重态中的电子对,其自旋方向相反,当其中一个电子被激发时,通常跃迁至第一激发态单重态轨道上,也可能跃迁至能级更高的单重态上。
这种跃迁是符合光谱选律的,如果跃迁至第一激发三重态轨道上,则属于禁阻跃迁。
单重态与三重态的区别在于电子自旋方向不同,激发三重态具有较低能级。
在单重激发态中,两个电子平行自旋,单重态分子具有抗磁性,其激发态的平均寿命大约为10-8s;而三重态分子具有顺磁性,其激发态的平均寿命为10-4~1s以上(通常用S和T分别表示单重态和三重态)。
处于激发态的电子,通常以辐射跃迁方式或无辐射跃迁方式再回到基态。
辐射跃迁主要涉及到荧光、延迟荧光或磷光的发射;无辐射跃迁则是指以热的形式辐射其多余的能量,包括振动弛豫( VR)、内部转移(IR)、系间窜跃(IX)及外部转移(EC)等,各种跃迁方式发生的可能性及程度,与荧光物质本身的结构及激发时的物理和化学环境等因素有关。
分子荧光分析法

能发射荧光物质条件: ①物质分子在紫外-可见光区有较强吸收的特定结构。 ②分子必须有较高的荧光效率。 ③Фf=发射荧光的量子数/吸收激发光的量子数
第五章 分子荧光分析法
2.分子结构与荧光的关系 (1)共轭双键结构:芳环杂环化合物,含共轭双键
脂肪烃π-π激 (2)分子的刚性平面:效应增加,可使荧光效率增
标作图E荧-λ激 (2)荧光光谱:固定入激以λ荧为横坐标,E荧纵坐
标作图E荧-λ荧
第五章 分子荧光分析法
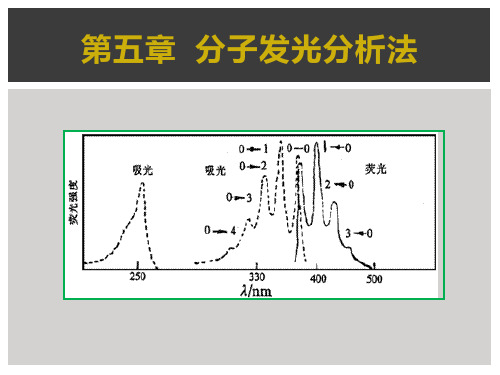
4.激发光谱和荧光光谱的关系: (1)荧光发射光谱不随激发波长而改变。只强度改
变。因此荧光光谱只有一个谱带。 (2)激发光谱和荧光光谱呈现镜像对称关系。
第五章 分子荧光分析法
二、分子结构与荧光关系
第五章 分子荧光分析法
2.荧光的产生:分子跃迁到较高能级后,以无辐射 跃迁的形式下降到第一电子激发态的最低振动 能级,以光的形式放出所吸收的能量,由第一 电子激发态的最低振动能级回到基态各振动能 级,这种光称为荧光。
3.激发光谱和荧光光谱:是定性和定量分析的基础 (1)激发光谱:固定入荧以λ激为横坐标,E荧纵坐
第五章 分子荧光分析法
第一节 基本原理
一、分子荧光的发生过程
1ቤተ መጻሕፍቲ ባይዱ分子的激发态 (1)去活化过程:当分子吸收一定能量后,处于激
发态的分子不稳定,其电子以辐射跃迁或无辐射 跃迁释放出多余的能量回到基态,这个过程为分 子去活化过程。 (2)单线态:分子受辐射激发时,电子从最高占有 轨道跃迁到较高空轨道,受激电子自旋仍保持方 向相反,称激发单线态。 (3)三线态:受激电子自旋方向反转,电子自旋为 平行时是激发三线态。
构造:激发光源——单色器——样品池——单色 器——检测器等四部分
分子发光光谱法

振动驰豫
S2
S1 系
间
内转换
跨 跃
T1
外转换
S0 λ1 吸光
λ2 λ3 吸光 荧光
S0 λ4 磷光
荧光发射:当分子处在单重态的最低振动能层时, 去激发过程是以10-7~10-9s左右的时间内发射一个 光子回到基态。
磷光发射:激发态分子经过系间跨跃到激发三重态 后,并经过迅速的振动驰豫到达第一激发三重态 (T1)的最低振动能级上,从T1态分子经发射光子 返回基态。 磷光的寿命比荧光的要长得多
• 从图中看出 • 磷> 荧> 激 * 易产生荧光 n * 易产生磷光
二、激发光谱和发射光谱
固定荧光的最大发射波长,然后改变激发光的波 长,根据所测得的荧光强度与激发光波长的关系作图, 得到激发光谱曲线。
选择最大激发波长作为激发光波长,然后测定不 同发射波长时所发射的荧光或磷光强度,得到荧光或 磷光光谱曲线。
碰撞熄灭将随温度的升高而增加;将随溶液黏度的减小而增大。
(ⅱ)能量转移 它是指处于激发单重态的荧光分子M*与熄灭 剂相互作用后,发生能量转移,使熄灭剂得到激发,其反应如下
(ⅲ) 组成化合物的熄灭 它是指熄灭剂和荧光分子在基态时发生 配合反应,生成不发荧光的配合物。
(ⅳ) 自熄灭和自吸收 当荧光物质浓度较大时,常会发生自 熄灭现象,这可能由于激发态分子之间的碰撞引起能量损 失。假如荧光物质的吸收光谱和发射光谱有较大的重叠, 由荧光物质发射的荧光,有一部分可能会被它自身的基态 分子所吸收,这种现象称为自吸收。随荧光物质浓度的增 加,自吸收现象将会加剧。
荧光—荧光分析法
光致发光:以光源来激发而发光 磷光—磷光分析法
化学发光:以化学反应能激发而发光—化学发光分析
法
仪器分析作业03参考答案(第三、五章紫外可见分光光度法+分子发光分析法)华南理工大学仪器分析

01. 溶液有颜色是因为它吸收了可见光中特定波长范围的光。
若某溶液呈蓝色,它吸收的是什么颜色的光?若溶液无色透明,是否表示它不吸收光?答:溶液呈蓝色,表明其吸收了蓝光的互补光,即黄光(若答是吸收了黄光外的所有可见光,不能说错,但是这样的情况过于巧合,少见!)。
若溶液无色透明,仅能说明其不吸收可见波段的光。
2. 分别在己烷和水中测定某化合物UV-Vis 光谱,发现该化合物的某个吸收峰由285 nm (己烷)蓝移至275 nm (水),(1)判断产生该吸收峰的跃迁类型;(2)试估算该化合物与水生成氢键的强度。
答:(1)溶剂极性增大,λmax 蓝移,表明该吸收峰是由n →π*跃迁产生的。
(2)()()⎪⎪⎭⎫⎝⎛λ-λ⋅⋅=己烷氢键max O H max A 11hc N E 2 ⎪⎭⎫ ⎝⎛⨯⨯⨯⨯⨯⨯⨯⨯=--99834-23102851-102751100.31063.61002.61mol J 28.15-⋅=3. 按从小到大顺序对下列化合物的λmax 排序,并简单说明理由(不要想得太复杂)A. NO 2B. NO 2t-C 4H 9t-C 4H 9 C.NO 2CH 3 D. NO 2C 2H 5答:B<D<C<A (空间位阻依次减小,共轭程度依次增加,λmax 红移)4. 某化合物分子式为C 10H 16,用其他仪器方法已经证明有双键和异丙基存在,其紫外光谱λmax =230 nm (ε=9000),1mol 该化合物只能吸收2 mol H 2,加氢后得到1-甲基-4异丙基环己烷,试确定该化合物的可能结构。
答: 1mol 该化合物只能吸收2 mol H 2,且其紫外光谱λmax =230 nm (ε=9000)可知该化合物含两个共轭但非同环双键(同环共轭双键基值为253 nm );该化合物含异丙基(双键不会出现在异丙基上),根据加氢后产物结构可推出该化合物可能结构如下:根据Woodward 规则可计算出该化合物的λmax =214+5(环外双键)+5⨯2(烷基取代)=229 nm ,与所测值相符。
分子发光分析法与分子吸收分光光度

分子发光分析法与分子吸收分光光度
分子发光分析法和分子吸收分光光度法(MMS)是物理化学中测定物质含量和生物物质含
量的两种常用方法。
它们之间有共同点和不同之处,本文主要就这二者的原理和方法进行
介绍。
分子发光分析法(MALS)是用物质中的激发态分子把紫外线能量转换为可见光,用以表征
物质的测定方法。
该方法工作原理为紫外线照射激发态分子,激发态分子把紫外线能量转
变为可见光,然后通过光电器件检测发出的可见光,最终得出物质的测定结果。
MALS技术的优点在于检测结果准确,具有快速性,还可以检测生物样本中物质含量。
而分子吸收分光光度(MMS)是通过测量物质吸收入射光的程度,来表征物质的检测方法。
这种技术工作原理是将光源照射在样本上,样本中的物质会吸收一部分入射的紫外线,而
剩下的光经过反射和透射而到达检测器,最终通过计算获得物质的测定数值。
比较MMS和MALS,MMS技术具有更高的灵敏度,可以进行更细小物质的检测,而且不受多种物质的干扰,也可以检测生物样本中的物质含量。
总之,MALS和MMS都是通过激发态分子转换紫外线能量为可见光,然后通过光电器件检测可见光,来判断物质的含量的两种常用技术,它们的优点和特点主要是MALS检测结果准确,具有快速性,而MMS则具有更高的灵敏度,可以进行更细小物质的检测,也可以检测
生物样本中的物质含量。
分子发光分析法

第五章 分子发光分析法: 基态分子吸收了一定能量后,跃迁至激发态,当激发态分子以辐射跃迁形式将其能量释放返回基态时,便产生分子发光。
第一节 荧光分析法一、概 述 :分子荧光分析法是根据物质的分子荧光光谱进行定性,以荧光强度进行定量的一种分析方法。
与分光光度法相比,荧光分析法的最大优点是灵敏度高和选择性高。
二、荧光产生的基本原理(一)分子荧光的产生(二)荧光效率及其影响因素1.荧光效率2.荧光与分子结构的关系(1)产生荧光的条件①必须含有共轭双键这样的强吸收基团,并且体系越大, 电子的离域性越强,越容易被激发产生荧光;大部分荧光物质都含有一个以上的芳香环,且随共轭芳环的增大,荧光效率越高,荧光波长越长。
②分子的刚性平面结构有利于荧光的产生③.取代基对荧光物质的荧光特征和强度的影响 给电子基团:-OH 、-NH2、-NR2和-OR 等可使共轭体系增大,导致荧光增强。
吸电子基团:-COOH 、-NO 和-NO2等使荧光减弱。
随着卤素取代基中卤原子序数的增加,使系间窜跃加强,物质的荧光减弱,而磷光增强。
3.环境因素对荧光强度的影响(1)溶剂极性对荧光强度的影响: 一般来说,电子激发态比基态具有更大的极性。
溶剂的极性增强,对激发态会产生更大的稳定作用,结果使物质的荧光波长红移,荧光强度增大. 奎宁在苯、乙醇和水中荧光效率的相对大小为1、30和1000。
(2)温度荧光强度的影响: 一般情况下,辐射跃迁的速率基本不随温度而改变,而非辐射跃迁的速率随温度升高而显著增大。
对大多数的荧光物质而言,升高温度会使非辐射跃迁概率增大,荧光效率降低。
由于三重态的寿命比单重激发态寿命更长,温度对于磷光的影响比荧光更大。
(3)pH 对荧光强度的影响:共轭酸碱两种体型具有不同的电子氛围,往往表现为具有不同荧光性质的两种体型,各具有自己特殊的荧光效率和荧光波长。
另外,溶液中表面活性剂的存在,可以使荧光物质处于更有序的胶束微环境中,对处于激发单重态的荧光物质分子起保护作用,减小非辐射跃迁的概率,提高荧光效率。
第五章分子发光—荧光、磷光和化学发光法

2.化学发光效率
发射光子的分子数 cl ce em 参加反应的分子数
激发态分子数 化学效率: ce 参加反应分子数
发光效率:
em
产生光子数 激发态分子数
时刻t 的化学发光强度(单位时间发射的光量子数):
dc I cl t cl dt
dc/dt 分析物参加反应的速率;
目 录
5-1 荧光和磷光光谱法
5-1-1 5-1-2 5-1-3 5-1-4 基本原理 荧光分析仪器 荧光分析方法的特点与应用 磷光分析法
5-2 化学发光与生物发光分析法
5-1-1 基本原理
5-1-1-1 5-1-1-2 5-1-1-3 5-1-1-4 荧光和磷光的产生 光谱曲线 荧光的影响因素 荧光强度的定量关系
5-1-1-4 荧光强度的定量关系
根据Parker方程,荧光强度F与荧光物质的浓度c 之间的关系是:
F 2.3kI 0 Fcl[1 (2.3cl) / 2! (2.3cl) 2 / 3! ]
k 与仪器有关的常数
I0 激发光的强度 F 荧光量子产率 荧光物质在激发波长处的摩尔吸光系数 l 光程长度。
当cl项很小时,括号内第二项及以后的高次项均 可忽略不计,Parker方程可简化为: F 2.3kI 0 Fcl F = Kc
5-1-2 荧光分析仪器
5-1-2-1 荧光分析仪器框图
光源
消除溶液中可能共存的其它 光线的干扰,以获得所需要 的荧光.
显示
激发光单色器
信号处理
I0
样品池 F 发射光单色器 (荧光单色器) 检测器
4.化学发光反应的类型
(1)气相化学发光反应 a. 一氧化氮与O3的发光反应(可测定空气中NO2的含量) NO + O3 → NO2* NO2* → NO2 + h
分析化学-分子发光分析法
3. 流式细胞术(FCM) 对悬液中的单细胞或其他生物粒子,通过检测
标记的荧光信号,实现高速、逐一的细胞定量 分析和分选的技术。
§4 化学发光分析法
Chemiluminescence Analysis
基本原理 化学发光反应类型 化学发光测量仪器 化学发光分析法的应用
一、基本原理
化学发光是由于化学反应而导致的光发射。 发生于生命体系的化学发光称为生物发光。 生物发光均有酶(荧光素酶)参加。
最大化学发光强度与发光物质浓度成正 比: Icl max = Kc
化学发光的积分值与发光物质浓度成正 比: Icl = Kc
二、化学发光反应的类型
直接化学发光
A 十 B C* , C* C 十 hν
间接(敏化)化学发光 A 十 B C* + D , C*+ F C 十 F*
F* F 十 hν
三、New technique of fluorescence analysis
1. 激光荧光分析 F 与 I0 成正比,激光的强度大,可提高
荧光法的灵敏度。
2.时间分辨荧光分析
由于不同分子的荧光寿命不同,在激发 和检测之间延缓一段时间,使不同荧光寿命 的物质达到分别检测的目的。
时间分辨荧光免疫法 将稀土元素的螯合物标记抗体,与体液中 的抗原结合。当加入一种增效剂时,稀土 元素被释放出来,形成新的螯合物,能产生 长寿命的 荧光(10 ~1000 μs)。待样品中 蛋白质等物质所发荧光完全衰减后进行测定, 可有效消除背景干扰。 已用于测定甲胎蛋白、促性腺绒毛激素、 皮质醇等体内微量物质的测定。
2.化学发光免疫分析仪
化学发光免疫分析是将化学发光分析和 免疫分析相结合而建立的一种超微量分析 技术。兼具发光分析的高灵敏性和抗原抗 体反应的高特异性的特点。
分子发光分析法

分子发光分析法基态分子吸收了一定能量后,跃迁至激发态,当激发态分子以辐射跃迁形式将其能量释放返回基态时,便产生分子发光(Molecular Luminescence)。
依据激发的模式不同,分子发光分为光致发光、热致发光、场致发光和化学发光等。
光致发光按激发态的类型又可分为荧光和磷光两种。
本章讨论分子荧光(Molecular Fluorescence)、分子磷光(Molecular Phosphorescence)和化学发光(Chemiluminescence)分析法。
第一节荧光分析法一、概述分子荧光分析法是根据物质的分子荧光光谱进行定性,以荧光强度进行定量的一种分析方法。
早在16世纪,人们观察到当紫外和可见光照射到某些物质时。
这些物质就会发出各种颜色和不同强度的光,而当照射停止时,物质的发光也随之很快消失。
到1852年才由斯托克斯(Stokes)给予了解释,即它是物质在吸收了光能后发射出的分子荧光。
斯托克斯在对荧光强度与浓度之间的关系进行研究的基础上,于1864年提出可将荧光作为一种分析手段。
1867年Goppelsroder应用铝—桑色素络合物的荧光对铝进行了测定。
进入20世纪,随着荧光分析仪器的问世,荧光分析的方法和技术得到了极大发展,如今已成为一种重要且有效的光谱分析手段。
荧光分析法的最大优点是灵敏度高,它的检出限通常比分光光度法低2~4个数量级,选择性也较分光光度法好。
虽然能产生强荧光的化合物相对较少,荧光分析法的应用不如分光光度法广泛,但由于它的高灵敏度以及许多重要的生物物质都具有荧光性质。
使得该方法在药物、临床、环境、食品的微量、痕量分析以及生命科学研究各个领域具有重要意义。
二、基本原理(一)分子荧光的产生大多数分子含有偶数电子。
根据保里不相容原理,基态分子的每一个轨道中两个电子的自旋方向总是相反的,因而大多数基态分子处于单重态(2S+1=1),基态单重态以S0表示。
当物质受光照射时,基态分子吸收光能就会产生电子能级跃迁而处于第一、第二电子激发单重态,以S1、S2表示。
第五章 分子发光分析法

s
体系间窜跃( 不同多重态, 体系间窜跃( isc ):不同多重态,有重叠的转动能级间的非辐 射跃迁( S1→T1跃迁 跃迁) 磷光发射:电子由第一激发三重态 射跃迁( S1→T1跃迁) 。磷光发射:电子由第一激发三重态 的最低振动能级( =0)跃迁至基态各振动能级 跃迁至基态各振动能级( T1→S0跃迁 跃迁)。 的最低振动能级(v=0)跃迁至基态各振动能级( T1→S0跃迁)。 S2 Intersystem Crossing 系间窜跃 S1 磷光发射 Phosphorescence T1
第五章 分子发光分析法
基态分子吸收一定能量后,跃迁至激发态, 基态分子吸收一定能量后,跃迁至激发态,当激 发态分子以辐射跃迁形式将其能量释放返回基态时 分子以辐射跃迁形式将其能量释放返回基态 发态分子以辐射跃迁形式将其能量释放返回基态时, 便产生分子发光 分子发光( 便产生分子发光(Molecular Luminescence)。 )。 依据激发的模式不同,分子发光分为光致发光 依据激发的模式不同,分子发光分为光致发光 按激发的类型又可分为荧光和磷光两种)、 荧光和磷光两种)、热致发 (按激发的类型又可分为荧光和磷光两种)、热致发 场致发光和化学发光等 光、场致发光和化学发光等。 本 分子荧光(Molecular Fluorescence)、 分子荧光( )、 章 分子磷光( 分子磷光(Molecular Phosphorescence) ) 化学发光( 化学发光(Chemiluminescence) )
S0 λ2 λ1
内转移( ) 相同多重态的两个电子能级之间 之间( 内转移(ic) :相同多重态的两个电子能级之间(如S2 S1,S1 S0)的非辐射跃迁 。 )
S2 T1 S1
S0 λ2 λ1
5 荧光分析

3. 刚性平面结构
荧光物质的刚性和平面 性增加,有利于荧光发射。
芴 联苯
F=1
F=0.2
-O
O C
O
N N
荧光黄 不产生荧光
产生荧光
偶氮苯
COO-
F=0.92
-O C COOO
N N
偶氮菲
酚酞 产生荧光 不产生荧光
H3C CH3
萘 VA
CH2OH
F(萘)= 5F(VA)
4. 取代基效应
一、分子荧光与磷光的产生
luminescence process of molecular fluorescence phosphorescence
1.单重态与三重态
电子激发态的多重度:M=2S+1 S为电子自旋量子数的代数 和(0或1); 单重态:全部轨道里的电子都是自旋配对的,S=0,M=1; 三重态:分子具有自旋不配对的电子,S=1,M=3. 平行自旋比成对自旋稳定(洪特规则),三重态能级比相应单重 态能级低; 大多数有机分子的基态处于单重态;
1
K1 [M*]
M* Q k 2 M Q ΔH K2 [M*] [Q]
共振能量转移:
D* D hv , A hv A*
分子内能量转移:
N
D* ( S1 ) A( S 0 ) D( S 0 ) A* ( S1 ) D* (T1 ) A( S 0 ) D( S 0 ) A* ( S1 )
CH3 CH3
hv
+
_
N
CH3
CH3
(3) 氧的熄灭作用 氧分子是荧光、磷光的熄灭剂,
1
3
M O 2 3 M* 3 O 2
分析化学(仪器分析)第五章 分子发光分析法

“重原子效应”--- 随着卤素取代基原子序数的增 加,物质的荧光减弱,磷光增强的现象。 分子中由于重原子的存在导致容易发生系间 窜跃的效应,产生的原因是原子序数高的重原子 的电子自旋和轨道间的相互作用变大,容易发生 自旋偶合作用,使S1-T1的体系间窜跃显著增加 所致。
23
② 静态猝灭(组成化合物的猝灭) 由于部分荧光物质分子与猝灭剂分子生成非荧光 的配合物而产生的。此过程往往还会引起溶液吸收 光谱的改变。 ③ 转入三重态的猝灭(S1—T1–– S0) 分子由于系间的跨越跃迁,由单重态跃迁到三重 态。转入三重态的分子在常温下不发光,它们在与 其它分子的碰撞中消耗能量而使荧光猝灭。 溶液中的溶解氧对有机化合物的荧光产生猝灭效 应是由于三重态基态的氧分子和单重激发态的荧光 物质分子碰撞,形成了单重激发态的氧分子和三重 态的荧光物质分子,使荧光猝灭。
18
(3)环境因素对荧光的影响
a. 溶剂的影响 电子激发态比基态具有更大的极性, 溶剂的极性增强,对激发态会产生更大的 稳定作用,使荧光波长红移,强度增大。 b. 温度的影响 辐射跃迁的速率不随温度而变,而非 辐射跃迁的速率随温度升高而显著增大。 温度升高,使得非辐射跃迁概率增大。 T增大, φf减小
26
如果 固定激发光波长为其 最大激发波长,然后测定 不同的波长时所发射的荧 光或磷光强度,即可得到 荧光或磷光发射光谱曲线。 荧光强度最大时的波长即 为发射波长λem 激发光谱和荧光光谱是荧 光测定时选择激发波长和 荧光测量波长的依据,也 可以用于鉴别荧光物质
27
激发光谱与发射光谱的关系
分子发光分析法概况课件

分子发光分析法的优缺点
优点
高灵敏度
分子发光分析法通常具 有很高的灵敏度,能够 检测出低浓度的目标物
。
选择性
某些发光分子可以与目 标物发生特异性反应, 从而提高分析的选择性
。
操作简便
分子发光分析法通常操 作简单,所需仪器设备 相对简单,便于现场快
速检测。
缺点
背景干扰
发光分析法容易受到环 境背景光的影响,如日 光、荧光等,导致检测
01
02
研发能够延长发光分子寿命 的技术,以减少检测过程中
的误差和不确定性。
03
04
克服背景干扰
研究和发展能够有效排除背 景光干扰的技术和方法,以 提高检测的稳定性和准确性
。
拓展应用领域
进一步探索发光分析法在环 境监测、生物医药、食品安 全等领域的应用,以满足更
广泛的需求。
06 结论
总结分子发光分析法的概况与重要性
结果不稳定。
发光衰减
某些发光分子的发光强 度会随时间衰减,影响 检测的准确性和稳定性
。
成本较高
某些高灵敏度的发光分 子和仪器设备成本较高 ,限制了其在某些领域
的应用。
未来发展方向与挑战
提高灵敏度和选择性
延长发光寿命
进一步研发具有更高灵敏度 和选择性的发光分子,以满 足更低检测限和更高准确性
的需求。
新型的分子发光分析方法和技术不断 涌现,如荧光免疫分析、荧光偏振免 疫分析、时间分辨荧光免疫分析等。
02
分子发光分析法的基本原理
分子发光的过程与机制
01
分子发光是指分子吸收能量后,由基态跃迁至激发态,再由激 发态回到基态时释放光子的过程。
02
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2021/2/7
5. 化学与生物发光分析的应用
(1) 该发光反应速度慢,某些金属离子可催化反应;利用 这一现象可间接测定这些金属离子。可测痕量的Cu2+ 、Mn2+ 、Co2+、V4+、Fe2+、 Fe3+、 Ni2+、Ag+、Au3+、Hg2+等
2. 仪器设备简单
不需要光源、单色器和背景校正;
3. 发射光强度测量无干扰
无背景光、散射光等干扰;
4. 线性范围宽 5. 分析速度快
缺点:可供发光用的试剂少;发光反应效率低(大大低于生 物体中的发光);机理研究少。
2021/2三、装置与技术
instrument and technology
装置流程:
发光反应室
光检测器
信号放大器
显示与记录
发光反应可采用静态或流动注射的方式进行: 静态方式:用注射器分别将试剂加入到反应器中混合, 测最大光强度或总发光量;试样量小,重复性差; 流动注射方式:用蠕动泵分别将试剂连续送入混合器, 定时通过测量室,连续发光,测定光强度;试样量大;
2021/2/7
SO2 + 2H2 → S + 2H2O S + S → 2S2 * S2 * → S2 + h 发射光谱范围:350~460nm; 最大发射波长:394nm; 灵敏度: 0.2 ng/cm-3; 发射光强度与硫化物浓度的平方成正比。
2021/2/7
(3)液相中的化学发光反应
Cu、机M理n研、究Co较、多V、,F在e、分C析r、中C应e用、最Hg多、;Th可等测。痕量的H2O2 、 应用最多的发光试剂:鲁米诺(3-氨基苯二甲酰肼); 化学发光反应效率:0.15~0. 05; 鲁米诺在碱性溶液中与双氧水的反应过程:
NADH + FMA + H+ NAD+ + FMNH2
黄素酶
FMNH2 + RCHO + O2 FMN + RCOOH + H2O + h 最大发射波长495 nm;
2021/2/7
二、特点 characteristics
1. 灵敏度极高
例:荧光素酶和磷酸三腺甙(ATP)的化学发光分析,可测 定210-17。Mol/L的ATP,即可检测出一个细菌中的ATP含量
(2) 可检测低至 10-9 mol/L 的H2O2; (3) 间接测定某些生物试样
氨基酸 +
氨基酸氧化酶
O2
酮酸 +NH3 + H2O2
葡萄糖氧化酶
葡萄糖 + O2 + H2O 葡萄糖酸 + H2O2
通过测定生成的H2O2 ,确定氨基酸、葡萄糖含量。
2021/2/7
草酸二酯(能量提供体)+高浓度双氧水+稠环芳烃(能量接 受体)+金属离子+溶剂组成的反应体系,可发出很强的可见光 ,发光效率高,使用不同的稠环芳烃,发射出不同颜色的光( 冷光源)。
2021/2/7
生物发光分析应用 1
在pH 7~8;荧光素酶(E)和Mg2+的存在下,荧光素
(LH2)与磷酸三腺甙(ATP)的反应,生成磷酸腺甙(AMP)荧光 素和荧光素酸的复合物和镁的焦磷酸盐(ppi):
ATP
+
LH2
+
E
+
Mg2+
pH7 - 8
AMP·LH2
·E
+Mg
ppi
+
2H+
复合物与氧反应,产生化学发光:
AMP·LH2 ·E + O2 [氧化荧光素]* + AMP+CO2 + H2O [氧化荧光素]* 氧化荧光素 + h
最大发射波长562nm;
2021/2/7
生物发光分析应用 2
烟酰胺腺嘌呤二核苷酸(NADH)在细菌中的黄素酶作用 下,在氧化型黄素单核苷酸(FMA)存在下,发生发光反应 :
NADH脱氢酶
c. 乙烯与O3的发光反应
乙烯与O3反应,生成激发态乙醛:
CH2O* → CH2O + h 最大发射波长:435nm;对O3的特效反应;线性响应 范围1 ng/cm-3 ~1g/cm-3;
2021/2/7
(2)火焰中的化学发光反应
在富氢火焰中,也存在着很强的化学发光反应; a. 一氧化氮
谢谢
NO + H → HNO* HNO * → HNO + h 发射光谱范围:660~770nm; 最大发射波长:690nm; 在富氢火焰中: NO2 + 2H → NO + H2O 该反应十分迅速;
2021/2/7
b.硫化物
挥发性硫化物SO2 、H2S 、CH3SH、 CH3SCH3等在富 氢火焰中燃烧,产生很强的化学发光(蓝色):
