高中化学一萃取颜色汇总
最新高二化学颜色知识点归纳

最新高二化学颜色知识点归纳正文第一篇:最新高二化学颜色知识点归纳最新高二化学颜色知识点归纳高中频道为各位学生同学整理了高二化学颜色知识点归纳,供大家参考学习。
请关注高中频道。
铁:铁粉是黑色的;一整块的固体铁是银白色的。
Fe2+浅绿色Fe3O4黑色晶体Fe(OH)2白色沉淀Fe3+黄色Fe(OH)3红褐色沉淀Fe(SCN)3血红色溶液FeO黑色的粉末Fe(NH4)2(SO4)2淡蓝绿色Fe2O3红棕色粉末FeS黑色固体铜:单质是紫红色Cu2+蓝色CuO黑色Cu2O红色CuSO4(无水)-白色CuSO4 5H2O蓝色Cu2(OH)2CO3-绿色Cu(OH)2蓝色[Cu(NH3)4]SO4深蓝色溶液BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl、Mg(OH)2、三溴苯酚均是白色沉淀Al(OH)3白色絮状沉淀H4SiO4(原硅酸)白色胶状沉淀Cl 2、氯水黄绿色F2淡黄绿色气体Br2深红棕色液体I2紫黑色固体HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾CCl4无色的液体,密度大于水,与水不互溶KMnO4--紫色MnO4-紫色Na2O2-淡黄色固体Ag3PO4-黄色沉淀S-黄色固体AgBr-浅黄色沉淀AgI-黄色沉淀O3-淡蓝色气体SO2-无色,有剌激性气味、有毒的气体SO3-无色固体(沸点44.80C)品红溶液红色氢氟酸:HF腐蚀玻璃N2O4、NO无色气体NO2红棕色气体NH3无色、有剌激性气味气体第二篇:高二化学颜色知识点归纳高二化学颜色知识点归纳查字典化学网为各位学生同学整理了高二化学颜色知识点归纳,供大家参考学习。
更多内容请关注查字典化学网。
铁:铁粉是黑色的;一整块的固体铁是银白色的。
Fe2+浅绿色Fe3O4黑色晶体Fe(OH)2白色沉淀Fe3+黄色Fe(OH)3红褐色沉淀Fe(SCN)3血红色溶液FeO黑色的粉末Fe(NH4)2(SO4)2淡蓝绿色Fe2O3红棕色粉末FeS黑色固体铜:单质是紫红色Cu2+蓝色CuO黑色Cu2O红色CuSO4(无水)白色CuSO45H2O蓝色Cu2(OH)2CO3绿色Cu(OH)2蓝色[Cu(NH3)4]SO4深蓝色溶液BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl、Mg(OH)2、三溴苯酚均是白色沉淀Al(OH)3白色絮状沉淀H4SiO4(原硅酸)白色胶状沉淀Cl2、氯水黄绿色F2淡黄绿色气体Br2深红棕色液体I2紫黑色固体HF、HCl、HBr、HI均为无色气体,在空气中均形成白雾CCl4无色的液体,密度大于水,与水不互溶KMnO4--紫色MnO4-紫色Na2O2淡黄色固体Ag3PO4黄色沉淀S黄色固体AgBr浅黄色沉淀AgI黄色沉淀O3淡蓝色气体SO2无色,有剌激性气味、有毒的气体SO3无色固体(沸点44.80C)品红溶液红色氢氟酸:HF腐蚀玻璃N2O4、NO无色气体NO2红棕色气体NH3无色、有剌激性气味气体以上就是小编为大家整理的高二化学颜色知识点归纳。
高中化学沉淀颜色

高中常见沉淀的颜色黄色:AgI 、溴水(黄 --橙、 FeS 2、某些蛋白质加硝酸。
淡黄色:S 、 Na 2O 2、 TNT(三硝基甲苯、 AgBr棕黄色:FeCl 3溶液、碘水(深黄 --褐黑色:CuS 、 Ag 2S 、 Cu 2S 、 FeS 、 FeO 、 Fe 3O 4、 MnO 2、 CuO 、 Ag 2O 、 I 2(紫黑、 Si (灰黑、 C 、 Ag 、 KMnO 4(紫黑绿色:CuCl 2溶液、 Cu 2(OH 2CO3、FeSO 4• 7H 2O (浅绿、 F 2(浅黄绿、 Cl 2(黄绿、氯水(浅黄绿红色:CuO 、Cu 、Fe (SCN 2+、甲基橙在酸性环境中、紫色石蕊试液在酸性环境中、酚酞在碱性环境中、品红试液、红磷(暗红、 Br2(深红棕、 Br2在 CCl4溶液中(紫红、苯酚被空气氧化(粉红棕色:固体 FeCl 3、固体 CuCl 2 NO2(红棕、 Fe 2O 3(红棕紫色:KMnO 4溶液、 I 2在 CCl 4溶液中褐色:Fe (OH 3(红褐蓝色:CuSO 4/5H2O 、 Cu (OH 2、淀粉遇碘、紫色石蕊试液在碱性环境中, Cu 2+的稀溶液有色反应产生的沉淀有颜色红褐色絮状沉淀:Fe(OH3浅绿色沉淀:Fe(OH2蓝色絮状沉淀:Cu(OH2白色沉淀:CaCO 3, BaCO 3, AgCl, BaSO4,(其中 BaSO 4、 AgCl 是不溶于 HNO 3的白色沉淀 ,CaCO 3 BaCO 3是溶于 HNO 3的白色沉淀 ,Mg(OH2.淡黄色沉淀 (水溶液中 ----S微溶于水 ------------Ca(OH2,CaSO 4,生成的溶液或气体有颜色1、水溶液中含有 Fe 3+的为黄色 . 如 :Fe2(SO43、 FeCl 3、 Fe(NO3 3溶液2、水溶液中含有Cu 2+为蓝色, 如:CuCl2、Cu(NO3 2、CuSO 4溶液;但是, CuSO 4•5H2O 是蓝色 , 无水 CuSO 4是白色3、红棕色液体 :Br24、红棕色的气体:NO 2; SO 2, 无色有刺激性的气体; H 2S, 有臭鸡蛋气味的气体铁:铁粉是黑色的;一整块的固体铁是银白色的。
高中化学颜色大全

高中化学颜色大全1、黑色固体:石墨、炭粉、铁粉、FeS、CuS、CuO、MnO2、Fe3O42、红色固体:Cu、Cu2O、Fe2O3 、HgO、红磷3、淡黄色固体:S、Na2O2、AgBr4、紫黑色固体:KMnO4、5、黄色固体:AgI 、Ag3PO46、绿色固体: Cu2(OH)2CO37、蓝色晶体:CuSO4•5H2O8、蓝色沉淀Cu(OH)29、红褐色沉淀:Fe(OH)310、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)11、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,MnO4-溶液为紫红色,其余溶液一般无色。
12、不溶于酸的白色沉淀:BaSO4 、AgCl13、不溶于水的白色沉淀CaCO3 (溶于酸)、BaCO3(溶于酸)、Al(OH)3、Mg(OH)2 等14、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)(3)红棕色气体:Br2(气体)NO2(4)黄绿色气体:Cl2(5)臭鸡蛋气味气体:H2S15、具有刺激性气味的液体:盐酸、硝酸、醋酸、酒精16、有毒的: 气体:CO SO2 H2S 液体:CH3OH 固体:NaNO2 CuSO4(可作杀菌剂,与熟石灰混合配成天蓝色的粘稠状物质——波尔多液)化学式颜色化学式颜色化学式颜色Cu 紫红Au 黄S 黄B 黄或黑F2 淡黄绿C(石墨) 黑Cl2 黄Br2 红棕C(金刚石) 无Si 灰黑I2 紫黑P 白、黄、红棕化学式颜色化学式颜色化学式颜色NO2 棕红ClO2 黄Na2O2 浅黄K2O 黄Pb3O4 红MnO 绿化学式颜色化学式颜色化学式颜色CuO 黑MnO2 黑Ag2O 棕黑FeO 黑ZnO 白Fe3O4 黑Hg2O 黑Fe2O3 红棕HgO 红或黄Cu2O 红化学式颜色化学式颜色化学式颜色Fe(OH)3 红褐HNO2 亮蓝Cu(OH)2 蓝化学式颜色化学式颜色化学式颜色CuFeS2 黄ZnS 白Ag2S 黑FeS 黑棕FeS2 黄Sb2S3 黑或橙红HgS 红PbS 黑CuS 黑Cu2S 黑FeCl3•6H2O 棕黄FeSO4 9H20 蓝绿Fe2(SO4)3.9H2O 棕黄Fe3C 灰FeCO3 灰Ag2CO3 黄Ag3PO4 黄CuCl2 棕黄AgF 黄CuCl2 7H2O 蓝绿AgCl 白CuSO4 白AgBr 浅黄CuSO4 5H2O 蓝AgI 黄Cu2(OH2)CO3 暗绿六、盐溶液中离子特色:化学式颜色化学式颜色化学式颜色Cu2+ 蓝MnO4- 紫红[CuCl4]2- 黄Cr2O72- 橙红Fe2+ 浅绿Fe3+ 棕黄物质颜色物质颜色物质颜色氯水黄绿溴水黄-橙碘水黄褐溴的有机溶液橙红-红棕I2的有机溶液紫红其它:蛋白质遇浓变黄、遇淀粉变蓝、TNT 淡黄、遇酚酞溶液变紫黄色:AgI、Ag3PO4、P4(黄磷)、溴水(黄--橙)、FeS2、Al2S3、甲基橙在弱酸性、中性或碱性环境中、某些蛋白质加硝酸。
高中化学质除杂加物质颜色表格总结
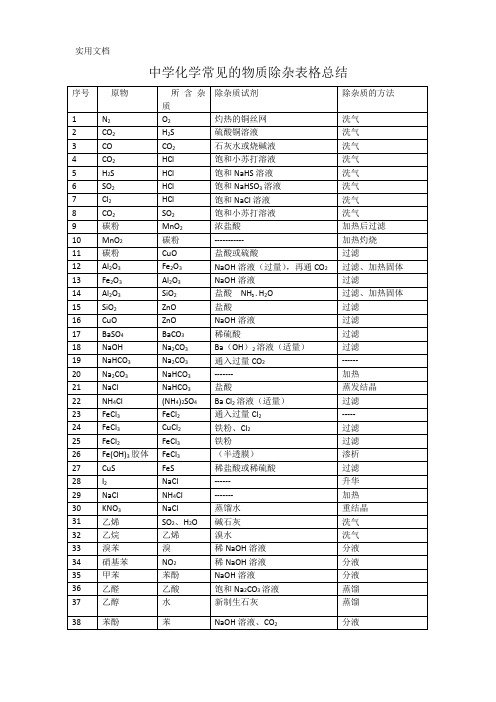
中学化学常见的物质除杂表格总结净化气体的量注意的问题:(1)需净化的气体中含有多种杂质时,除杂顺序:一般先除去酸性气体,如:氯化氢气体,CO2、SO2等,水蒸气要在最后除去。
(2)除杂选用方法时要保证杂质完全除掉,如:除CO2最好用NaOH不用Ca(OH)2溶液,因为Ca(OH)2是微溶物,石灰水中Ca(OH)2浓度小,吸收CO2不易完全。
方法:1杂质转化法:欲除去苯中的苯酚,可加入氢氧化钠,使苯酚转化为苯酚钠,利用苯酚钠易溶于水,使之与苯分开2吸收洗涤法;欲除去二氧化碳中混有的少量氯化氢和水,可使混合气体先通过饱和碳酸氢钠溶液,再通过浓硫酸即可除去3沉淀过滤法;欲除去硫酸亚铁溶液中混有的少量硫酸铜,加入少量铁粉,待充分反应后,过滤除去不溶物即可4加热升华法;欲除去碘中的沙子,即可用此法5溶液萃取法;欲除去水中含有的少量溴,可采用此法6结晶和重结晶;欲除去硝酸钠溶液中少量的氯化钠,可利用二者的溶解度不同,降低溶液温度,使硝酸钠结晶析出,可得到纯硝酸钠晶体7分馏蒸馏法;欲除去乙醚中少量的酒精,可采用多次蒸馏的方法8分液法;欲将密度不同且又互不相溶的液体混合物分离,可采用此法,如将苯和水分离9渗析法;欲除去胶体中的离子,可采用此法。
如除去氢氧化钠胶体中的氯离子高中化学常见有色物质归类1、黑色固体:石墨、炭粉、铁粉、FeS、CuS、CuO、MnO2、Fe3O42、红色固体:Cu、Cu2O、Fe2O3 、HgO、红磷3、淡黄色固体:S、 Na2O2、 AgBr4.紫黑色固体:KMnO4、I2 5、黄色固体: AgI 、Ag3PO4 6、绿色固体: Cu2(OH)2CO3 7、蓝色晶体:CuSO4·5H2O8 、蓝色沉淀 Cu(OH)2 9、红褐色沉淀: Fe(OH)310、白色固体:MgO、P2O5、CaO、 NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)11、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,MnO4-溶液为紫红色,其余溶液一般无色。
高中化学常用物质溶解性表及沉淀颜色

.高中化学常用物质溶解性表及积淀颜色Fe2O3+3H2SO4= Fe2(SO4)3+3H2O铁锈溶解溶液呈黄色铁器除锈Al2O3+3H2SO4= Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4=CuSO4+H2O黑色固体溶解溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O白色固体溶解MgO+H2SO4=MgSO4+H2O白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O红褐色积淀溶解溶液呈黄色Ba(OH)2+ H2SO4=BaSO4+2H2O生成白色积淀不溶解于稀硝酸查验SO42 的原理BaCl2+ H2SO4=BaSO4+2HCl 生成白色积淀不溶解于稀硝酸查验 SO42 的原理Ba(NO3)2+H2SO4=BaSO4+2HNO3 生成白色积淀不溶解于稀硝酸查验 SO42 的原理Na2O+2HNO3=2NaNO3+H2O白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O黑色固体溶解溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+ H2O白色固体溶解MgO+2HNO3=Mg(NO3)2+ H2O白色固体溶解CaO+2HNO3=Ca(NO3)2+ H2O白色固体溶解NaOH+HNO3=NaNO3+ H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O红褐色积淀溶解溶液呈黄色3NaOH + H3PO4=3H2O + Na3PO4.3NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+ H2O汲取COO2H2中的CO22NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 办理硫酸工厂的尾气( SO2 )FeCl3+3NaOH=Fe(OH)3+3NaCl溶液黄色褪去有红褐色积淀生成。
高中化学萃取颜色问题教案

高中化学萃取颜色问题教案
主题:化学实验——萃取颜色问题
时间:1课时
教学目标:
1.了解溶剂的选择对于颜色萃取的影响。
2.掌握颜色萃取实验的操作方法。
3.能够分析实验数据,得出结论。
教学重点和难点:
1.理解颜色溶液的萃取原理。
2.掌握实验操作中的注意事项。
教学准备:
1.化学实验室
2.甲苯、酒精等溶剂
3.色谱仪
4.色素溶液
教学步骤:
1.导入:通过一个生活中的例子引入颜色萃取的概念,激发学生的兴趣。
2.实验操作:
a.将两种颜色相间的溶液滴在白纸上,观察混合颜色。
b.将该混合溶液分别加入甲苯和酒精中,摇匀后观察颜色变化。
c.使用色谱仪分析两种溶液中的各种色素成分。
3.实验分析:
a.通过实验数据和观察结果,引导学生讨论不同溶剂对于颜色萃取的影响。
b.帮助学生总结颜色萃取的原理,并得出结论。
4.实验总结:让学生回答一些问题,总结颜色萃取实验的重要性和应用。
5.课堂讨论:鼓励学生分享对于颜色萃取实验的思考和体会。
6.作业布置:要求学生结合实验结果,撰写一份实验报告。
教学延伸:
1.让学生自行设计颜色萃取实验,尝试使用其他不同的溶剂。
2.组织学生参与化学实验设计比赛,以颜色萃取为主题。
教学评价:
通过学生实际操作和讨论,考察学生对于颜色萃取实验的理解和实验操作能力。
并通过学生的实验报告评价他们的实验总结和分析能力。
高中化学常见物质颜色总结精编版

高中化学常见物质颜色总结精编版高中化学常见物质颜色总结精编版MQS system office room 【MQS16H-TTMS2A-MQSS8Q8-MQSH16898】高中化学常见物质颜色总结红色:Fe2O3红棕色;Fe(OH)3红褐色;[Fe(SCN)]2+红色(或血红色);Cu2O红色(或砖红色);被氧化的苯酚(即苯醌)粉红色;石蕊在pH<5的溶液中呈红色;酚酞在pH8~10的溶液中呈浅红色;NO2红棕色;红磷暗红色;Br2深棕红色;品红溶液红色;Bi微红色;充氦气、氖气的灯管红色;CoCl2·6H2O红色;Cu紫红色;*甲基橙在pH<的溶液中显红色。
紫色:MnO4—紫红色;I2紫黑色;I2蒸汽紫色;I2的CCl4溶液紫红色;碘溶于苯或汽油呈紫色或紫红色;石蕊在pH5~8的溶液中呈紫色。
灰色:硒;Fe(OH)2变成Fe(OH)3的中间产物灰绿色。
棕色:CuCl2晶体棕黄色;FeCl3晶体棕红色黄色:S、AgI、Ag3PO4、Fe3+、不纯硝基苯黄色;Na2O2、三硝基甲苯、AgBr、F2、硝化甘油、NaNO2黄色;尿素白色或淡黄色;*甲基橙在pH>的溶液中呈黄色。
蓝色:Cu2+、Cu(OH)2、CuSO4·5H2O、Co2O3蓝色;石蕊在pH>8的溶液中呈蓝色;I2遇淀粉变蓝色;液态、固态的氧气淡蓝色;CoCl2天蓝色。
黑色:木炭、焦炭、黑色火药、MnO2、CuO、CuS、Cu2S、PbS、Ag2S、FeS、Fe3O4黑色;Si灰黑色;石油黑色或深棕色;煤焦油黑褐色。
绿色:Fe2+浅绿色;Cl2淡黄绿色;CuCl2浓溶液绿色(很浓黄绿色、稀则蓝色);碱式碳酸铜绿色。
褐色:Ag2O褐色;溶解了溴的溴苯褐色;碘酒褐色。
黄色:氯气,过氧化钠,单质硫蓝色:铜离子,淀粉遇碘黑色:四氧化三铁(磁性),氧化铜,碳血红色:硫氰化铁紫色:苯酚遇三氯化铁紫黑色:碘白色:硫酸钡,氯化银铁:铁粉是黑色的;一整块的固体铁是银白色的。
高二化学知识点之化学颜色

高二化学知识点之化学颜色蓝色:新制Cu(OH)2固体、胆矾、硝酸铜、溶液中淀粉与碘变蓝、石蕊试液碱变蓝、pH试纸与弱碱变蓝等。
浅蓝色:臭氧、液氧等蓝色火焰:硫、硫化氢、一氧化碳的火焰。
甲烷、氢气火焰(蓝色易受干扰)。
⑤ 以绿色为色的物质浅绿色:Cu2(OH)2CO3,FeCl2,FeSO47H2O。
绿色:浓CuCl2溶液、pH试纸在约pH=8时的颜色。
深黑绿色:K2MnO4。
黄绿色:Cl2及其CCl4的萃取液。
⑥ 以紫色为基色的物质KMnO4为深紫色、其溶液为红紫色、碘在CCl4萃取液、碘蒸气、中性pH试纸的颜色、K+离子的焰色等。
⑦ 以黑色为基色的物质黑色:碳粉、活性碳、木碳、烟耽氧化铜、四氧化三铁、硫化亚铜(Cu2S)、硫化铅、硫化汞、硫化银、硫化亚铁、氧化银(Ag2O)。
浅黑色:铁粉。
棕黑色:二氧化锰。
⑧ 白色物质无色晶体的粉末或烟尘;与水强烈反应的P2O5;难溶于水和稀酸的:AgCl,BaSO3,PbSO4;难溶于水的但易溶于稀酸:BaSO3,Ba3(PO4)2,BaCO3,CaCO3,Ca3(PO4)2,CaHPO4,Al(OH)3,Al2O3,ZnO,Zn(OH)2,ZnS,Fe(OH)2,Ag2SO3,CaSO3等;微溶于水的:CaSO4,Ca(OH)2,PbCl2,MgCO3,Ag2SO4;与水反应的氧化物:完全反应的:BaO,CaO,Na2O;不完全反应的:MgO。
⑨ 灰色物质石墨灰色鳞片状、砷、硒(有时灰红色)、锗等。
(2)离子在水溶液或水合晶体的颜色① 水合离子带色的:Fe2+:浅绿色;Cu2+:蓝色;Fe3+:浅紫色呈黄色因有[FeCl4(H2O)2] 2-;MnO4-:紫色:血红色;:苯酚与FeCl3的反应开成的紫色。
②主族元素在水溶液中的离子(包括含氧酸根)无色。
运用上述规律便于记忆溶液或结晶水合物的颜色。
(3)主族金属单质颜色的特殊性ⅠA,ⅡA,ⅣA,ⅤA的金属大多数是银白色。
高一化学物质的颜色总结

高一化学物质的颜色总结高一化学物质的颜色总结常见的有色离子有: 有色离子的颜色 2+2+Cu铜离子-----------蓝色 Fe 亚铁离子-----------浅绿 3+2+Fe铁离子 -----------棕黄Mn 锰离子-----------浅粉 2+2+Co钴离子-----------粉色 Ni镍离子---------绿色 2+3+Cr亚铬离子 -----------蓝绿 Cr铬离子 -----------绿色 2+3+Cd镉离子 -----------蓝绿 Au金离子--------金黄 -2-MnO4高锰酸根离子---紫红色MnO4锰酸根离子 ---------墨绿 2-2-CrO4铬酸根离子----黄色 Cr2O7 重铬酸根离子 -------橙 2+2-Fe(SCN)硫氰合铁络离子---血红 CuCl4四氯合铜络离子--------黄色黑色:氧化铜,氧化亚铁,四氧化三铁红色:铜(有时候说是其他色)红棕色:氧化铁血红色:硫氰化铁紫色固体:高锰酸钾白色沉淀:碳酸钡,碳酸钙,氯化银,氢氧化铝,硫酸钡,硫酸钙黄色沉淀:碘化银淡黄色沉淀:溴化银红褐色沉淀:氢氧化铁氯气:黄绿色红棕色气体:二氧化氮(一)、固体的颜色2、绿色固体:碱式碳酸铜1、红色固体:铜,氧化铁3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属 8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁(二)、液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液 13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液 14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液 15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)、气体的颜色17、红棕色气体:二氧化氮 18、黄绿色气体:氯气 19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢气体等大多数气体。
【高中化学】高考化学考点梳理 颜色

【高中化学】高考化学考点梳理颜色
【高中化学】高考化学考点梳理颜色
收集和分类
高考
化学复习知识点和考点。
我希望大多数考生能够理清知识点,记住考点,为考试做好充分准备。
>>>
高中三年级
化学知识点汇总<<<
二、颜色
铁:铁粉是黑色的;一整块的固体铁是银白色的。
fe2+――浅绿色fe3o4――黑色晶体fe(oh)2――白色沉淀fe3+――黄色fe(oh)3――红褐色沉淀fe(scn)3――血红色溶液
FeO——黑色粉末Fe(NH4)2(SO4)2——浅蓝绿色Fe2O3——红棕色粉末FES——黑色固体
铜:单质是紫红色cu2+――蓝色cuo――黑色cu2o――红色cuso4(无水)―白色cuso45h2o――蓝色cu2(oh)2co3―绿色cu(oh)2――蓝色[cu(nh3)4]so4――深蓝色溶液
BaSO 4、BaCO 3、Ag 2CO 3、CaCO 3、AgCl、Mg(OH)2和三溴苯酚为白色沉淀物,Al(OH)3为白色絮状沉淀物,h4sio 4(原硅酸)为白色胶体沉淀物
cl2、氯水――黄绿色f2――淡黄绿色气体br2――深红棕色液体
高中英语
i2――紫黑色固体hf、hcl、hbr、hi均为无色气体,在空气中均形成白雾
CCl4-无色液体,密度大于水,与水不混溶KMnO4-紫色MnO4-紫色Na2O2-浅黄色固体Ag3PO4-黄色沉淀s-黄色固体AgBr-浅黄色沉淀AgI-黄色沉淀O3-浅蓝色气体SO2-无色,刺激性气味有毒气体SO3无色固体(沸点44.80c)品红溶液红色氢氟酸:HF腐蚀性玻璃N2O4,无无色气体NO2红棕色气体NH3无色气体有刺激性气味。
高二化学知识点汇总:颜色系统总结

ห้องสมุดไป่ตู้
精心整理 色 MnO4-——紫色
Na2O2—淡黄色固体 Ag3PO4—黄色沉淀 S—黄色固体 AgBr—浅黄 色沉淀
AgI—黄色沉淀 O3—淡蓝色气体 SO2—无色,有剌激性气味、有 毒的气体
SO3—无色固体(沸点 44.80C)品红溶液——红色氢氟酸:HF—— 腐蚀玻璃
N2O4、NO——无色气体 NO2——红棕色气体 NH3——无色、有剌 激性气味气体
精心整理
高二化学知识点汇总:颜色系统总结
高二化学知识点总结:颜色 铁:铁粉是黑色的;一整块的固体铁是银白色的。Fe2+——浅绿 色 Fe3O4——黑色晶体 Fe(OH)2——白色沉淀 Fe3+——黄色 Fe(OH)3——红褐色沉 淀 Fe(SCN)3——血红色溶液 FeO——黑色的粉末 Fe(NH4)2(SO4)2——淡蓝绿色 Fe2O3—— 红棕色粉末 FeS——黑色固体 铜:单质是紫红色 Cu2+——蓝色 CuO——黑色 Cu2O——红色 CuSO4(无水)—白色 CuSO4·5H2O——蓝色 Cu2(OH)2CO3—绿色 Cu (OH)2——蓝色[Cu(NH3)4]SO4——深蓝色溶液 BaSO4、BaCO3、Ag2CO3、CaCO3、AgCl、Mg(OH)2、三溴苯酚均 是白色沉淀 Al(OH)3 白色絮状沉淀 H4SiO4(原硅酸)白色胶状沉淀 Cl2、氯水——黄绿色 F2——淡黄绿色气体 Br2——深红棕色液 体 I2——紫黑色固体 HF、HCl、HBr、HI 均为无色气体,在空气中均形成白雾 CCl4——无色的液体,密度大于水,与水不互溶 KMnO4--——紫
最新高中化学必修一笔记(整理精华版)..

第1节认识化学科学一、化学的含义和特征1、化学的含义:在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的自然科学。
2、特征:认识分子和制造分子。
3、物质的变化分为两种:物理变化和化学变化。
二、化学的形成和发展1661年,英国,波义耳提出化学元素的概念,标志着近代化学诞生。
1771年,法国,拉瓦锡建立燃烧现象的氧化学说。
1803年,英国,道尔顿提出了原子学说。
1869年,俄国,门捷列夫发现元素周期表。
三、元素与物质的关系1、元素的存在状态:物质都是有元素组成的,元素在物质中以游离态和化合态两种形式存在,在这两种状态下,分别形成单质和化合物。
2、研究物质的顺序:金属非金属→氢化物↓↓金属氧化物非金属氧化物↓↓碱含氧酸↓↓盐盐3、氧化物的酸碱性:第2节 研究物质性质的方法和程序一、研究物质的基本方法:观察、实验、分类、比较等方法。
(一)Na 的性质1、物理性质:钠是一种银白色金属,熔点为97.8℃,沸点为882.9℃,密度为0.97g/cm 3。
2、化学性质:容易失去一个电子,形成Na +(稳定结构),还原性极强。
(1)与非金属反应:①4Na+O 2====2Na 2O ②2Na+O 2====Na 2O 2 ③2Na+Cl 2====2NaCl④2Na+S==== Na 2S(2)与水反应:2Na+2H 2O====2NaOH+H 2↑现象:浮:Na 浮在水面上;熔:融化成一个小球;游:四处游动;响:发出咝咝响声;红:试液变红。
(3)与酸反应:2Na+2HCl====2NaCl+H 2↑(4)与盐反应:①2Na+2H 2O+CuSO 4====Cu(OH)2↓+Na 2SO 4+H 2↑ ②6Na+6H 2O+2FeCl 3====2Fe(OH)3↓+6NaCl+3H 2↑ ③4Na+TiCl 4(熔融状)高温Ti+4NaCl(5)Na 在空气中的一系列变化:Na −→−2O Na 2O −−→−O H 2NaOH −−−→−O H CO 22,Na 2CO 3·10H 2O −−→−风化Na 2CO 34Na+O 2====2Na 2O → Na 2O+H 2O====2NaOH →2NaOH+9H 2O+CO 2====Na 2CO 3·10H 2O → Na 2CO 3·10H 2O 风化Na 2CO 3+10H 2O ↑3、Na 的保存:钠通常保存在煤油或石蜡油中。
中学化学物质颜色及颜色反应总结

中学化学常见物质颜色一、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3、HgO、红磷▲硫:淡黄色▲Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色(如:CuSO4溶液、CuCl2溶液、Cu(NO3)2溶液);凡含Fe2+的溶液呈浅绿色(如:FeSO4溶液、FeCl2溶液、Fe (NO3)2溶液);凡含Fe3+的溶液呈棕黄色(如:Fe2(SO4)3溶液、FeCl3溶液、Fe (NO3)3溶液),其余溶液一般为无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2,红褐色↓:Fe(OH)3 ,白色↓:其余不溶性碱为白色。
6.颜色反应(燃烧)CO、H2S、H2、CH4、S、乙醇在空气中燃烧火焰的颜色均为淡蓝色。
(硫在氧气中燃烧呈蓝紫色火焰)。
二.褐色物质1.碘酒、溴苯中溶有溴均呈褐色或浅褐色。
2.煤焦油呈黑褐色。
3.Fe(OH)3胶体、Fe(OH)3沉淀呈红褐色。
三.火焰颜色1.铜,铁在氯气中燃烧产生棕色烟。
2.氢气在氯气中燃烧呈苍白色火焰。
四.灰色物质1.As、Sn、Fe3C为灰色。
2.Fe、Cr、Mn等的单质粉末状态一般为灰黑。
五.紫色物质和紫色反应(一)物质1.pH在5--8时石蕊试液、KMnO4溶液、I2的汽油或CCl4 溶液、苯酚与FeCl3溶液反应的产物呈紫色2.钾的焰色反应呈浅紫色3.氩气的灯光呈紫蓝色4、碘蒸气呈紫色(二)反应1、苯酚与FeCl3溶液反应的产物呈紫色。
2、I-与强氧化剂反应生成紫黑色的碘2I- +2e-==I2六.黄色物质和黄色反应(一)物质1.钠的焰色反应、AgI,Ag3PO4,蛋白质与浓硝酸反应的产物、pH>4.4时的甲基橙溶液、pH 在5-6时的pH试纸呈黄色。
高中化学一萃取颜色汇总
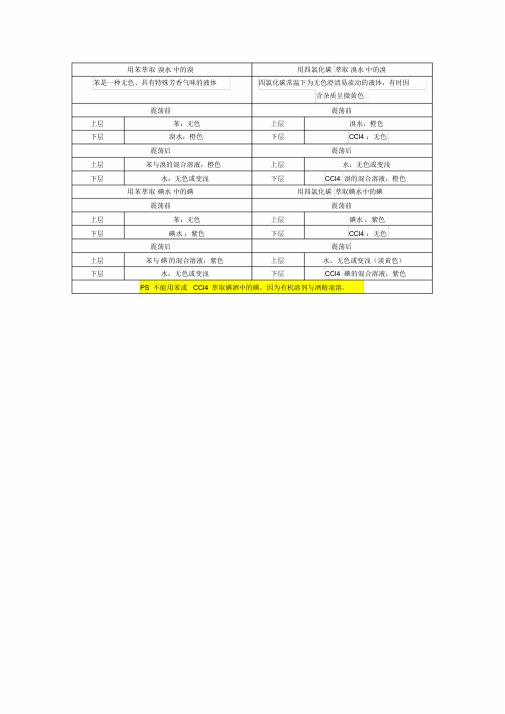
用苯萃取溴水中的溴用四氯化碳萃取溴水中的溴
苯是一种无色、具有特殊芳香气味的液体四氯化碳常温下为无色澄清易流动的液体,有时因
含杂质呈微黄色
震荡前震荡前
上层苯:无色上层溴水:橙色
下层溴水:橙色下层CCl4 :无色
震荡后震荡后
上层苯与溴的混合溶液:橙色上层水:无色或变浅
下层水:无色或变浅下层CCl4 溴的混合溶液:橙色用苯萃取碘水中的碘用四氯化碳萃取碘水中的碘
震荡前震荡前
上层苯:无色上层碘水:紫色
下层碘水:紫色下层CCl4 :无色
震荡后震荡后
上层苯与碘的混合溶液:紫色上层水:无色或变浅(淡黄色)下层水:无色或变浅下层CCl4 碘的混合溶液:紫色PS 不能用苯或CCl4 萃取碘酒中的碘,因为有机溶剂与酒精混溶。
高中化学萃取颜色变化及溶液颜色特征

溶液的颜色都是因为里面有特殊有色离子的存在导致的
二价铜离子蓝色或者四蓝绿色
一价铜砖红色
二价铁(亚铁)淡绿色
三价铁黄色
高锰酸根离子紫红色
锰酸根离子绿色
二价锰离子淡粉色
四价锰(二氧化锰)黑色
重铬酸根离子橙色
铬酸根离子黄色
氯化铜浓溶液,硝酸铜浓溶液绿色
特殊的是石蕊酚酞遇酸碱变色就不说了
但是有一个特殊的是三价铁离子遇SCN-变为血红色(重点)
如果遇到什么溶液即可根据对应的有色离子判断颜色.
高考常见的是碘水和溴水的萃取分液
碘水本身是棕黄色,加入密度小于水的萃取剂,例如苯,则上层有机层为紫红色,下层水层为无色;若加入密度大于水的萃取剂,例如CCl4,则上层水层为无色,下层有机层为紫红色.
溴水本身是橙黄色,加入密度小于水的萃取剂,例如苯,则上层有机层为橙红色,浓度更大的话会呈现红棕色,下层水层为无色;若加入密度大于水的萃取剂,例如CCl4,则上层水层为无色,下层有机层为橙红色,浓度大也会呈现红棕色.。
(完整版)高中化学一萃取颜色汇总
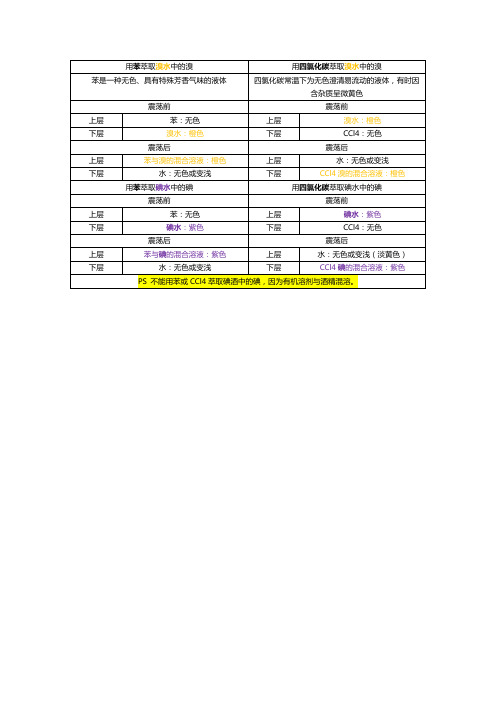
用四氯化碳萃取溴水中的溴
苯是一种无色、具有特殊芳香气味的液体
四氯化碳常温下为无色澄清易流动的液体,有时因含杂质呈微黄色
震荡前
震荡前
上层
苯:无色
上层
溴水:橙色
下层
溴水:橙色
下层
CCl4:无色
震荡后
震荡后
上层
苯与溴的混合溶液:橙色
上层
水:无色或变浅
下层
水:无色或变浅
下层
CCl4溴的混合溶液:橙色
用苯萃取碘水中的碘
用四氯化碳萃取碘水中的碘
震荡前
震荡前
上层ห้องสมุดไป่ตู้
苯:无色
上层
碘水:紫色
下层
碘水:紫色
下层
CCl4:无色
震荡后
震荡后
上层
苯与碘的混合溶液:紫色
上层
水:无色或变浅(淡黄色)
下层
水:无色或变浅
下层
CCl4碘的混合溶液:紫色
PS不能用苯或CCl4萃取碘酒中的碘,因为有机溶剂与酒精混溶。
高中化学一萃取颜色汇总之欧阳道创编
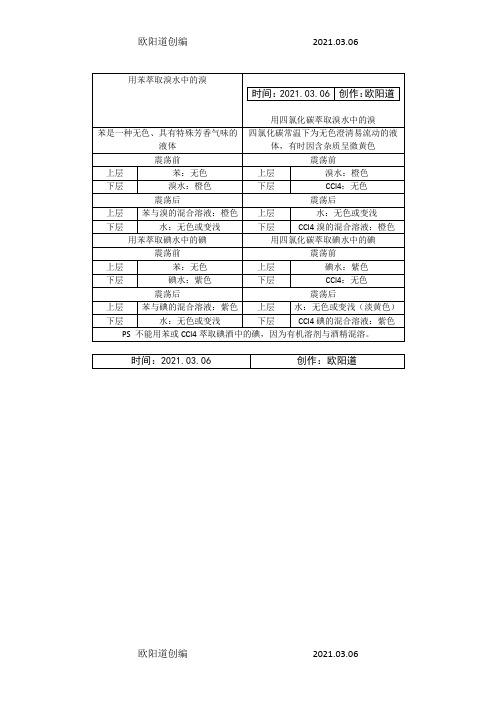
水:无色或变浅
下层
CCl4溴的混合溶液:橙色
用苯萃取碘水中的碘
用四氯化碳萃取碘水中的碘
震荡前
震荡前
上层
苯:无色
上层
碘水:紫色
下层
碘水:紫色
下层
CCl4:无色
震荡后
震荡后
上
下层
水:无色或变浅
下层
CCl4碘的混合溶液:紫色
PS不能用苯或CCl4萃取碘酒中的碘,因为有机溶剂与酒精混溶。
用苯萃取溴水中的溴
时间:2021.03.06
创作:欧阳道
用四氯化碳萃取溴水中的溴
苯是一种无色、具有特殊芳香气味的液体
四氯化碳常温下为无色澄清易流动的液体,有时因含杂质呈微黄色
震荡前
震荡前
上层
苯:无色
上层
溴水:橙色
下层
溴水:橙色
下层
CCl4:无色
震荡后
震荡后
上层
苯与溴的混合溶液:橙色
上层
水:无色或变浅
时间:2021.03.06
创作:欧阳道
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用四氯化碳萃取溴水中的溴
苯是一种无色、具有特殊芳香气味的液体
四氯化碳常温下为无色澄清易流动的液体,有时因含杂质呈微黄色
震荡前
震荡前
上层
苯:无色
上层
溴水:橙色
下层
溴水:橙色
下层
CCl4:无色
震荡后
震荡后
上层
苯与溴的混合溶液:橙色
上层
水:无色或变浅
下层
水:无色或变浅
下层
CCl4溴的混合溶液:橙色
用苯萃取碘水中的碘
用四氯化碳萃取碘水中的碘
震荡前
震荡前
上层
苯:无色
上层
碘水:紫色
下层
碘水:紫色
下层
CCl4:无色震荡后 Nhomakorabea震荡后上层
苯与碘的混合溶液:紫色
上层
水:无色或变浅(淡黄色)
下层
水:无色或变浅
下层
CCl4碘的混合溶液:紫色
PS不能用苯或CCl4萃取碘酒中的碘,因为有机溶剂与酒精混溶。
