氨合成铁系催化剂
氨合成塔催化剂升温还原方案

氨合成塔催化剂升温还原方案氨合成铁触媒通常均以氧化态形式存在(FeO、Fe2O3),而其只有在α-Fe状态下才具有活性,起到催化作用,因此在利用前必需将氧化铁还原成α-Fe,且还原质量的好坏将直接阻碍其利用寿命及企业的经济效益,必需严格依照还原方案进行操作,确保催化剂还原质量。
一、还原方程式及理论出水量一、方程式:FeO+H2=Fe+H2O+QFe2O3+H2=2Fe+3H2O-Q二、理论出水量:3、气体流程循环机出口的气体经油分分离油水后,分成三股:第一股10%的环隙气从下部沿内外筒环隙进入塔上部,从塔顶引出,与热交的热气体汇合后约30-35%再进入冷管制。
第二股5%左右零米冷激气从上部进入合成塔上部,用来调剂合成塔上部温度。
第三股,被塔外热互换器加热到170-200℃、约65-70%的主线气体进入合成塔下部的换热器管内,气体加热到360-410℃,经中心管进入触媒层表面。
通过第一绝热层反映后,气体温度达到460-470℃,与段间冷却器出来的气体在混合散布器内混合,温度降到400-430℃,进入径向框与内筒的环隙向下,从圆周方向径向流向径向筐Ⅰ中部的换热器。
气体通过换热器外壳进入管间,气体从换热器管间上部折流向下,温度降至310-340℃出塔。
出塔气经废热回收器进热互换器管内(下进上出)温度90℃,进入水冷却器,水冷出来的气体降温到40℃,进入冷凝蒸发分离器(1)气体进冷凝器管内,再进氨蒸发器管内,进分离器,分离氨后的气体经导气管从分离器底部引来,再进冷凝蒸发分离器(2),气体进冷凝器关键,再进氨蒸发器管内,出氨蒸发器的气体,与补气油分来的新鲜气汇合,经分离器分离氨后,通过氨蒸发器的中心管进入上部冷凝器的管内,从冷凝蒸发器(2)的冷凝器管内出来的气体在进入冷凝蒸发分离器(1)的冷凝器的管间,冷却进入管内的水冷后的热气体,本身温度提高到25℃以上进入循环机,开始新的一轮循环。
二、还原前的预备工作一、各分析仪器齐全,水汽浓度取样管,出水掏出点接管畅通。
氨合成催化剂简介

氨合成催化剂简介史** 309010**** 化工090*合成氨工业的巨大成功不仅解决了人类因人口增长所需要的粮食,而且带动了一系列基础理论的发展。
合成氨工业创立的本身就包含着伟大的创造性和光辉的科学思想。
Haber和Bosch提出的化学平衡与质量作用定律的应用、高压反应技术、封闭流程操作、动态反应速率概念,Mittasch提出的混合催化剂的概念以及化学家、工程师、物理学家、材料学家与各种工匠群体合作的成功先例等,推动了整个化学工业和材料工业的发展。
合成氨催化剂是多相催化领域中许多基础研究的起点。
许多多相催化科学的基本理论和概念都来自于或首先试用于催化合成氨。
合成氨工业及其催化过程的巨大成功奠定了多相催化科学的基础。
氨合成熔铁催化剂是世界上研究得最成功、最透彻的催化剂之一。
本报告主要介绍传统Fe3O4基熔铁催化剂。
氨合成催化剂的新进展也将予以简介。
熔铁催化剂的组成及特性熔铁催化剂的主要成分为Fe3O4,其含量为90%左右,助催化剂主要是Al2O3、K2O、CaO、MgO等金属氧化物以及SiO2非金属氧化物,通常用磁铁矿为原料,由熔融法制备。
在催化剂装填至反应器后,由铁氧化物还原得到的α-Fe是氨合成反应的主催化剂,但由纯铁氧化物还原得到的催化剂在合成氨过程中很快会失活。
作为助催化剂的Al2O3、K2O、CaO、MgO、SiO2等氧化物不被还原,虽然对氨合成不具有催化作用,但它们改善了α-Fe的催化活性,增强了耐热和抗毒能力,延长了使用寿命。
其中,Al2O3、Cr2O3、MgO、V2O5、ZrO2、TiO2、SiO2等高温难熔氧化物属于结构性助催化剂,它们能增加催化剂在还原和操作时的抗热能力和抗毒能力,起着增大表面积、稳定结构的作用,但却降低了每单位总表面积的比活性和还原速度。
K2O、CaO等碱金属、碱土金属和稀土金属氧化物作为电子性助催化剂,同结构性助催化剂的作用相反,它们能增加单位表面积的比活性,但却削弱了抗热和抗氧毒物的能力。
多种合成氨催化剂比较分析论文
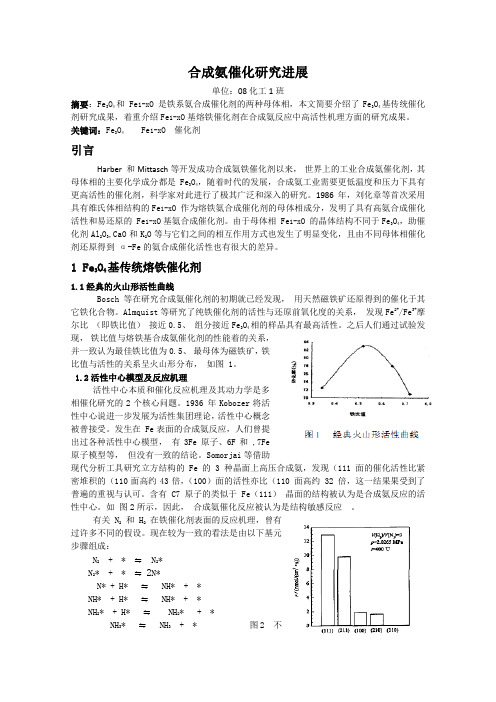
合成氨催化研究进展单位:08化工1班摘要:Fe3O4和Fe1-x O 是铁系氨合成催化剂的两种母体相,本文简要介绍了Fe3O4基传统催化剂研究成果,着重介绍Fe1-x O基熔铁催化剂在合成氨反应中高活性机理方面的研究成果。
关键词:Fe3O4Fe1-x O 催化剂引言Harber 和Mittasch等开发成功合成氨铁催化剂以来,世界上的工业合成氨催化剂,其母体相的主要化学成分都是Fe3O4,随着时代的发展,合成氨工业需要更低温度和压力下具有更高活性的催化剂,科学家对此进行了极其广泛和深入的研究。
1986年,刘化章等首次采用具有维氏体相结构的Fe1-x O作为熔铁氨合成催化剂的母体相成分,发明了具有高氨合成催化活性和易还原的Fe1-x O基氨合成催化剂。
由于母体相 Fe1-x O 的晶体结构不同于Fe3O4,助催化剂Al2O3,CaO和K2O等与它们之间的相互作用方式也发生了明显变化,且由不同母体相催化剂还原得到α-Fe的氨合成催化活性也有很大的差异。
1 Fe3O4基传统熔铁催化剂1.1经典的火山形活性曲线Bosch 等在研究合成氨催化剂的初期就已经发现,用天然磁铁矿还原得到的催化于其它铁化合物。
Almquist等研究了纯铁催化剂的活性与还原前氧化度的关系,发现Fe2+/Fe3+摩尔比(即铁比值)接近0.5、组分接近Fe3O4相的样品具有最高活性。
之后人们通过试验发现,铁比值与熔铁基合成氨催化剂的性能着的关系,并一致认为最佳铁比值为0.5、最母体为磁铁矿,铁比值与活性的关系呈火山形分布,如图 1。
1.2活性中心模型及反应机理活性中心本质和催化反应机理及其动力学是多相催化研究的2个核心问题。
1936 年Kobozer将活性中心说进一步发展为活性集团理论,活性中心概念被普接受。
发生在 Fe表面的合成氨反应,人们曾提出过各种活性中心模型,有3Fe原子、6F和 ,7Fe原子模型等,但没有一致的结论。
Somorjai等借助现代分析工具研究立方结构的Fe的 3 种晶面上高压合成氨,发现(111 面的催化活性比紧密堆积的(110面高约43倍,(100)面的活性亦比(110 面高约 32 倍,这一结果果受到了普遍的重视与认可。
氨合成的催化剂

氨合成的催化剂一、引言氨合成是一种重要的工业化学反应,广泛应用于制造化肥等领域。
在氨合成反应中,催化剂起着至关重要的作用。
本文将详细介绍氨合成反应中常用的催化剂。
二、铁系催化剂铁系催化剂是氨合成反应最早采用的催化剂之一。
这种催化剂主要由铁、钴、锆等金属组成,其特点是具有较高的活性和选择性。
此外,铁系催化剂还具有良好的耐久性和稳定性,在工业生产中得到了广泛的应用。
三、钌系催化剂钌系催化剂是近年来被广泛研究和应用的一种新型催化剂。
这种催化剂主要由钌、锰等金属组成,其特点是具有较高的活性和选择性,并且在高温下仍能保持稳定性。
此外,钌系催化剂还具有良好的抗毒性,在氨合成反应过程中能够有效地抵御碳氢物质等有害物质对其产生的影响。
四、钼系催化剂钼系催化剂是一种常用的氨合成催化剂,主要由钼、铝等金属组成。
这种催化剂具有较高的活性和选择性,并且在高温下仍能保持稳定性。
此外,钼系催化剂还具有良好的抗毒性和耐腐蚀性,在氨合成反应中表现出色。
五、其他催化剂除了以上几种催化剂外,还有许多其他类型的氨合成催化剂。
例如,铑系催化剂、镍系催化剂、银基催化剂等都具有一定的应用前景。
这些新型催化剂在提高反应效率、降低生产成本等方面都具有重要作用。
六、结论综上所述,氨合成反应中的催化剂种类繁多,每种催化剂都具有其独特的优点和缺点。
在实际生产中,应根据不同情况选择最适合自己需求的催化剂,以达到最佳效果。
同时,未来还需要进一步研究和开发新型高效稳定的氨合成催化剂,以满足不断增长的市场需求。
氨合成的催化剂

氨合成的催化剂引言氨是一种重要的化工原料,广泛应用于农业、化肥制造、化工合成等领域。
而氨合成过程中最关键的环节就是催化剂的选取。
本文将会全面介绍氨合成催化剂的种类、工作原理、制备方法以及相关的工业应用,以加深我们对氨合成催化剂的了解。
催化剂种类在氨合成过程中,常用的催化剂主要包括铁系催化剂、钌系催化剂和铑系催化剂。
这些催化剂具有高效能、稳定性好的特点,被广泛应用于工业生产中。
铁系催化剂铁系催化剂是氨合成过程中最常见的催化剂之一。
传统的铁系催化剂主要是以铁为主要成分,常配以适量的铝、钾等元素。
这类催化剂具有成本低、晶体结构稳定等优点,然而其催化活性相对较低,需要高温和高压下进行反应。
近年来,随着纳米技术的发展,铁基纳米催化剂成为了新的研究热点,其催化活性和选择性得到了极大的提高。
钌系催化剂钌系催化剂是氨合成中的另一类重要催化剂。
钌具有较高的催化活性和选择性,常作为铁系催化剂的替代品使用。
研究表明,钌催化剂在较低温下即可实现氨合成反应,大大降低了能耗。
此外,钌系催化剂对反应物质的吸附性能和解离能力较强,可以促进氨合成反应的进行。
铑系催化剂铑系催化剂在氨合成领域中也有着广泛的应用。
铑是一种包括铑金属和铑氧化物等在内的化合物,具有较高的催化活性和稳定性。
铑催化剂不仅可用于氨合成反应的催化剂,还可以在其他化学反应中发挥重要作用。
然而,铑系催化剂的价格较高,限制了其在工业生产中的应用。
催化剂在氨合成反应中起到了至关重要的作用。
一方面,催化剂可以提供活性位点,吸附反应物质并降低其解离能力,从而促进反应的进行。
另一方面,催化剂还可以降低反应的活化能,提高反应的速率。
具体而言,催化剂与反应物之间会发生物理吸附和化学吸附的过程。
在物理吸附中,反应物只是通过分子间的范德瓦尔斯力与催化剂表面相互作用。
而在化学吸附中,反应物会与催化剂发生化学反应,生成中间体。
通过物理吸附和化学吸附的交替作用,反应物逐步转化为产物。
催化剂的选择需要考虑多个因素,如催化活性、化学稳定性、抗中毒性等。
合成氨催化剂的生产和技术

合成氨催化剂的生产和技术发布时间:2023-01-04T05:52:04.717Z 来源:《中国科技信息》2023年17期作者:张鹏[导读] 合成氨广泛用于工业硝酸、盐铵和化肥的生产过程,间接促进了国民经济的发展。
与此同时,有关工业对氨的需求以吨计有所增加,这是工业建设和化学发展的基本原料之一。
张鹏陕西黄陵煤化工有限责任公司陕西延安 727307摘要:合成氨广泛用于工业硝酸、盐铵和化肥的生产过程,间接促进了国民经济的发展。
与此同时,有关工业对氨的需求以吨计有所增加,这是工业建设和化学发展的基本原料之一。
但是,作为工业发展和国民经济的重要参与者,传统的合成氨往往消耗更多的能源,产生较少的效益。
因此,对合成氨催化剂的研究开发不断进行推导。
本文介绍了合成氨催化剂的研究开发,讨论了最新的合成氨研发趋势,供参考。
关键词:合成氨;催化剂;新技术;研究进展前言作为合成氨化工的重要原料,在中国工业建设和经济生产中发挥着十分重要的作用,合成氨相关催化剂的开发也是化工发展的重要组成部分。
但是,我们还必须认识到,合成氨工业在实际生产中也消耗大量能源在全球气候日益受到灾害威胁的时候,化学研究人员必须加倍努力,改进现有的催化剂,以提高合成氨工业的总体效率。
1 铁基催化剂的研究1.1铁系氨合成催化剂A-110-1催化剂是一种以铁-氨为基础的合成催化剂,主要由磁铁矿的传统熔炼形成。
为了提高催化剂活性和稳定性,结构催化剂如Al2O3、K2O、CaO、BaO等。
已添加到准备中。
其作用是利用这些高熔点折射氧化物作为活性物质的α-Fe晶体的绝缘材料,防止容易发生摩擦的微晶接触,从而提高催化剂体的热稳定性。
SiO2 _ 2通常是从磁铁矿原料引入的,其适当存在类似于Al2O3,它可以稳定铁颗粒,提高催化剂的热阻和水的毒性。
催化剂的组成和含量在熔化状态下相互作用,影响催化剂的活性和热稳定性。
尤其是还原催化剂表面化学成分对催化剂的活性和稳定性起着重要作用。
合成氨工艺催化剂

合成氨工艺催化剂引言合成氨是一种重要的化工原料,广泛应用于农业肥料、塑料、石油化工等领域。
在合成氨的生产过程中,催化剂起着关键作用。
本文将详细介绍合成氨工艺催化剂的种类、性能以及制备方法。
催化剂种类合成氨工艺催化剂主要分为三类,分别为铁基催化剂、铁铅共催化剂和铜铁催化剂。
铁基催化剂铁基催化剂是合成氨工艺中最常用的催化剂之一。
它使用铁作为主要活性组分,通常与铝、钛、硅等辅助载体配合使用。
铁基催化剂具有良好的催化性能和稳定性,能够在相对较低的温度下即可实现合成氨的转化。
铁铅共催化剂铁铅共催化剂是在铁基催化剂的基础上进行改进的一种催化剂。
它通过铅的引入,可以进一步提高催化剂的催化活性和选择性。
铁铅共催化剂在工业生产中有广泛应用,并取得了良好的效果。
铜铁催化剂铜铁催化剂是近年来发展起来的一类新型催化剂。
相比于传统的铁基催化剂,铜铁催化剂具有更高的催化活性和选择性。
这得益于铜与铁之间的协同作用,能够加速反应速率并改善催化剂的稳定性。
催化剂性能合成氨工艺催化剂的性能主要包括催化活性、选择性和稳定性。
催化活性催化活性是指催化剂对于反应底物的转化能力。
合成氨的生产过程是一个高温高压的反应过程,因此催化剂需要具备较高的催化活性,才能保证反应的效果和产量。
选择性选择性是指催化剂在反应过程中对不同反应产物的选择性。
对于合成氨工艺而言,目标产物是氨气,因此催化剂需要具备高的选择性,以避免产生过多的副产物。
稳定性稳定性是催化剂的另一个重要性能指标。
由于合成氨反应条件的严苛性,在长时间的反应过程中,催化剂会受到高温高压等因素的影响,容易发生失活。
因此,稳定性是评价催化剂性能的关键指标之一。
催化剂制备方法合成氨工艺催化剂的制备方法多种多样,常见的方法包括物理混合法、浸渍法和共沉淀法。
物理混合法物理混合法是最简单的制备方法之一,它将催化活性组分与载体物理混合,通过高温煅烧使其形成均匀分散的催化剂颗粒。
物理混合法制备的催化剂成本较低,但催化活性和稳定性相对较差。
2023年合成氨工艺参考题库含答案6

2023年合成氨工艺参考题库含答案(图片大小可自由调整)第1卷一.全能考点(共50题)1.【单选题】施工升降机司机()酒后作业。
工作时间内司机不应与其他人员闲谈,不应有妨碍施工升降机运行的行为。
A、宜B、不宜C、严禁D、可以2.【判断题】变换催化剂置换降温合格后将系统保持常压即可。
3.【单选题】根据《中华人民共和国消防法》规定,建设单位在验收后应当报住房和城乡建设主管部门备案,住房和城乡建设主管部门应当进行()。
A、抽查B、复查C、验收D、确认4.【单选题】下面关于真空度表述正确的是()。
A、真空度等于大气压减去绝压B、真空度是负值C、真空度等于绝压减去大气压5.【单选题】其他单位和个人通过研究提出的地震预测意见,应当向所在地或者所预测地的()书面报告,或者直接向国务院地震工作主管部门书面报告。
收到书面报告的部门或者机构应当进行登记并出具接收凭证。
A、国家负责管理地震工作的部门或者机构B、省级以上地方人民政府负责管理地震工作的部门或者机构C、县级以上地方人民政府负责管理地震工作的部门或者机构6.【单选题】用人单位已经不存在或者无法确认劳动关系的职业病病人,申请医疗救助和生活等方面的救助可以向地方人民政府()部门。
A、所在地卫生行政B、民政C、劳动保障行政7.【判断题】降低温度、提高压力有利于氨的冷凝分离。
8.【判断题】短时间进入毒物区,无需佩戴防护用品,憋口气就行。
9.【判断题】土方开挖前需有技术负责人进行安全技术交底,作业人员必须清楚开挖面下的电缆、管线等情况,办理作业票后方可施工。
10.【判断题】建筑工程施工现场的消防安全由施工单位负责。
实行施工总承包的,由总承包单位负责’最新解析’。
11.【单选题】以下论述错误的是()、(D)A、液压系统的设计不合理,会导致液压油温升高B、液压系统的压力损耗过大,会导致液压油温升高C、液压系统的容积损耗过大,会引起液压油发热D、液压油中混有空气,会引起液压油发热12.【多选题】请指出图中作业存在的安全隐患()。
2023年合成氨工艺考试历年真题荟萃4卷合1(附带答案)卷1

2023年合成氨工艺考试历年真题荟萃4卷合1(附带答案)(图片大小可自由调整)全文为Word可编辑,若为PDF皆为盗版,请谨慎购买!第一卷一.全能考点(共50题)1.【判断题】灭火的基本方法包括窒息法、隔离法、冷却法和抑制法。
参考答案:√2.【判断题】发生硫化氢泄漏起火,在没有切断气源的情况下,不能熄灭正在燃烧的气体。
参考答案:√3.【单选题】液氨泵启动前冷却排气的目的是()。
A、加速启动进度B、防止泵体产生温差应力和启动后产生气蚀现象C、进行充分的置换参考答案:B4.【单选题】《建筑法》规定的责令停业整顿、降低资质等级和吊销资质证书的行政处罚,由()决定。
A、建设行政主管部门B、颁发资质证书的机关C、中国建筑业协会D、国务院参考答案:B5.【单选题】高温变换反应是()。
A、吸热反应B、放热反应C、自热反应参考答案:B6.【判断题】如不能完全消除和预防坠落危害,应评估工作场所和作业过程的坠落危害,选择安装使用脚手架、操作平台等。
参考答案:×7.【判断题】用万能工具显微镜的影象法测量螺纹牙型半角,是将中央目镜视场内米字线的十字中心虚线螺纹牙型影象的边缘调整参考答案:√8.【单选题】《安全生产法》规定,从业人员发现直接危及人身安全的紧急情况时,()。
生产经营单位不得因此而降低其工资、福利等待遇或者解除与其订立的劳动合同。
A、有权停止作业或者在采取可能的应急措施后撤离作业场所B、经请示分管安全的领导,可以停止作业、撤离作业场所C、经过安全技术人员检测,可以停止作业、撤离作业场所参考答案:A9.【单选题】发生生产安全事故后,施工单位应当首先采取可靠措施()。
需要移动现场物品时,应当做出标记和书面记录,妥善保管有关证物。
A、立即上报事故情况B、抢救伤亡人员,防止事故扩大C、降低经济损失D、保护事故现场,妥善保护证物参考答案:B10.【判断题】爆破施工中必须执行“一炮三检”制度,即装药前检查、装药后检查及爆破前检查。
2023年合成氨工艺备考押题二卷合一带答案35

2023年合成氨工艺备考押题二卷合一带答案(图片大小可自由调整)全文为Word可编辑,若为PDF皆为盗版,请谨慎购买!第1卷一.全能考点(共100题)1.【单选题】透平高速暖机时间比低速暖机时间()。
A、短B、长C、一样参考答案:A2.【判断题】充装高低压液化气体奥氏体不锈钢罐式集装箱,运行期间无异常情况的,首次全面检验及年度检验时可免除罐体的内部检验项目。
参考答案:×3.【判断题】盾构机内部产生高温或低温的零部件及可出人的区域范围应有警示标识,表面应保持整洁,严禁堆放杂物及易燃物品,接触表面应采取防护措施。
参考答案:√4.【单选题】去除助燃物的灭火方法是()。
A、隔离法B、窒息法C、冷却法参考答案:B5.【单选题】发现煤气中毒人员,采取以下行动中,()急救方法是正确的。
A、在现场马上给伤员做人工呼吸B、迅速打开门窗通风,并将病人送到新鲜空气环境C、关好门窗,防止煤气外泄参考答案:B6.【单选题】合成系统氮气增加会使系统压差()。
A、升高B、无影响C、降低参考答案:A7.【单选题】我国工业企业噪声卫生标准采用()。
A、声压级B、声级C、D、声级参考答案:B8.【单选题】发生生产安全事故后,施工单位应当首先采取可靠措施()。
需要移动现场物品时,应当做出标记和书面记录,妥善保管有关证物。
A、立即上报事故情况B、抢救伤亡人员,防止事故扩大C、降低经济损失D、保护事故现场,妥善保护证物参考答案:B9.【单选题】场车紧急制动时,司机可将制动踏板迅速踩到底,必要时腾出右手____。
A、转动转向盘B、拉驻车制动装置C、按喇叭参考答案:B10.【单选题】易燃液体充装时应控制流速,其流速不得超过3m/s,其原因是()。
A、防溢出B、防静电C、防温度升高参考答案:B11.【单选题】环保监测中的COD表示()。
A、化学耗氧量B、生化需氧量C、空气净化度参考答案:A12.【单选题】氨合成塔内催化剂采用分段换热的目的是使反应更接近()。
合成氨工艺知识100题及答案

17、【单选题】化工污染物都是在生产过程中产生的,其主要来源()。
A、化学反应副产品,化学反应不完全B、燃烧废气,产品和中间产品C、化学反应不完全的副产品,燃烧废气,产品和中间产品18、【单选题】变换系统化催化剂床层经常超温会造成其活性()。
(B)A、不变B、下降C、上升19、【单选题】合成催化剂一氧化碳中毒后,合成系统内甲烷含量会()。
(A)A、上升B、不变C、下降20、【单选题】合成催化剂装于()。
(C)A、外简中B、换热器C、触媒筐21、【单选题】同一抢救者轮番进行口对口人工呼吸和胸外按压术比列为:胸部按压数/人工呼吸数=()。
(B)A、5/1B、15/2C、18/122、【单选题】向大气排放有害物质的工业企业应设在当地()最小频率风向被保护对象的上风侧。
(C)A、春季B、全年C、夏季23、【单选题】在中暑的几种类型中,最为凶险的是()。
(B)A、热痉挛热射病C、热衰竭24、【单选题】在冬季,水环式真空泵停运后要对泵体进行哪种操作()。
(C)A、保温B、充液C、排液25、【单选题】在易燃易爆场所穿()最危险。
(B)A、布鞋B、带铁钉鞋C、胶鞋26、【单选题】在有害环境性质未知、是否缺氧未知及缺氧环境下,选择的辅助逃生型呼吸防护用品应为()。
(A)A、携气式B、过滤式C、全面罩27、【单选题】安全验收评价报告是安全验收评价工作形成的主要成果之一,它的作用一是帮助企业查隐患、落实整改措施;二是()。
(B)A、提出施工过程中的安全对策措施B、为政府安全生产监督管理提供建设项目安全验收的依据C、指导事故分析与重大事故模拟28、【单选题】建设项目职业病危害预评价和职业病危害控制效果评价, 应当由依法取得相应资质的()承担。
(A)A、职业卫生技术服务机构B、评价机构C、职业卫生检测机构29、【单选题】当生产经营单位的生产工艺和技术发生变化时,应急预案()。
(B)A、应当废弃不用B、应当及时修订C、可以免于重新备案30、【单选题】急性中毒现场抢救的第一步是()。
氨合成铁系催化剂

氨合成熔铁催化剂氨合成熔铁催化剂,目前合成氨工业中普遍使用的主要是以铁为主体的多成分催化剂,又称铁触媒。
1、组成1.1组成主要成分是Fe3O4,含量在90%左右。
助催化剂为K2O、Al2O3、CaO、MgO等,含量小于催化剂总质量的9%,低压催化剂还增加了CoO(A201等)。
其按作用不同分为两类,一类是结构型助剂,如Al2O3、Cr2O3、ZrO2、TiO2、MgO、CaO、SiO2等难熔氧化物。
另一类是电子型助剂,如K20。
每种类型助剂都有各自的最佳添加量,一般均在0.6%〜1.0%范围。
1.2物理结构氧化态催化剂主体是磁铁矿,其化学计量式是FeO.Fe2O3或Fe3O4。
晶体结构类似于尖晶石(MgAl2O4)的结构(90%以上是具有反尖晶石结构、不均匀复杂体系的磁铁矿)。
是四面体和八面体结构的堆积结果。
其中形成两种间隙:四面体间隙和八面体间隙。
三价的金属离子占据四面体间隙的一半和八面体间隙的一半,二价的铁离子占据八面体间隙(Fe3+(Fe2+,Fe3+))。
磁铁矿的一个单胞(晶体的最小结构单元)由32个氧离子和24个铁离子所组成,即8(Fe3O4)。
按结晶学原理,32个氧原子按照面心立方堆积的每一单胞,有64个四面体间隙和32个八面体间隙。
如上所述,除了24个被铁离子占据以外,其余大部分是空的,因此可加入助催化剂占据这些空隙形成间隙固溶体。
而且化学式相近的物质,结构类型相同且质点(离子、原子或分子)半径近于相等的物质,可以发生同晶取代,生成置换固溶体,例如三价铝即可置换部分三价铁,形成置换固溶体。
(含量小于4%时主要生成置换固溶体。
若三氧化二铝全部取代氧化铁则生成FeOAl2O3)1.3化学特点铁触媒在500 °C左右时的活性最大,这也是合成氨反应一般选择在500 °C左右进行的重要原因之一。
但是,即使是在500 C和30 MPa时,合成氨平衡混合物中NH3的体积分数也只为26.4%,即转化率仍不够大。
工业合成氨催化剂合成氨的反应机理和动力学方程的探讨

工业合成氨催化剂合成氨的反应机理和动力
学方程的探讨
合成氨(NH3)催化剂是指催化合成氨的物质,在工业中常用的
催化剂是铁系和钼系催化剂。
合成氨的反应机理分为三个步骤,其中
分别是氮气和氢气的吸附,化学反应以及氨的脱附。
氮气和氢气在催
化剂表面吸附,然后它们形成吸附层,接下来发生了原子的化学反应,最后生成氨并脱附。
以铁系催化剂为例,反应的主要步骤可以简化为:
1. 氮气和氢气的吸附
N2 + 3H2 -> 2NH3 (催化剂表面)
2. 氮氢反应
N2 + 3H2 -> 2NH3。
这个反应是可逆的,在反应的过程中有两个主要变量:反应温度
和反应压力。
反应温度越高,反应速率也就越快。
但是,高温下NH3
的生成速率成本太高,所以压力常常被用来增加反应速率。
催化反应通过催化剂表面的反应中心来催化反应,反应后的产物
从表面脱附。
反应速率可以用反应的速率方程来描述,其中反应速率
的大小与反应中物质的浓度有关。
可以用以下的马斯京根方程来描述
反应速率:
ra = kPn[N2]1/2[H2]3/2
其中ra是反应速率,k是反应速率常数,P是合成气压力,n是
反应速率方程的反应级数,[N2]和[H2]分别是氮气和氢气的浓度。
因
为反应中氮气和氢气的浓度非常低,所以反应级数和浓度之间的关系
被推测为1/2和3/2。
总之,合成氨的反应机理和动力学方程是工业上制造氨气的关键。
通过研究这些方程,我们可以更好地理解如何优化反应条件,以获得
更高的产量和更高的效率。
合成氨工艺考试题库含答案

合成氨工艺考试题库含答案1、【单选题】()建立健全应急物资储备保障制度,完善重要应急物资的监管、生产、储备、调拨和紧急配送体系。
( C )A、企业B、社会C、国家2、【单选题】一旦发现有人晕倒在有限或密闭容器内,下面最适合的急救方法是()。
( A )A、佩戴防毒面具或空气呼吸器,在有人监护的情况下施救。
B、腰间系上绳子,第一时间跳下去,把中毒者拉上来。
C、第一时间跳下去,把中毒者背上来。
3、【单选题】一般情况下,安全帽能抗()kg铁锤自1m高度落下的冲击。
( A )A、3B、2C、44、【单选题】下面关于真空度表述正确的是()。
( A )A、真空度等于大气压减去绝压B、真空度是负值C、真空度等于绝压减去大气压5、【单选题】不允许含氧化合物进入合成系统,主要原因是()。
( B )A、防止与氢发生爆炸B、防止与催化剂中的铁反应生成四氧化三铁C、防止与催化剂中氧化亚铁反应生成四氧化三铁6、【单选题】个体防护用品只能作为一种辅助性措施,不能被视为控制危害的()手段。
( A )A、主要B、可靠C、有效7、【单选题】事故应急救援的总目标是通过有效的应急救援行动,尽可能的减少人员伤亡和财产损失。
事故应急救援具有不确定性、()、复杂性、后果影响易猝变等特点。
( B )A、长期性B、突发性C、必然性8、【单选题】从业人员为防御物理、化学、生物等外界因素伤害所穿戴、配备和使用的各种护品的总称称为()。
( B )A、个体防护用品B、个体防护装备C、空气呼吸器9、【单选题】从事酸碱作业时,作业人员需佩戴()。
( B )A、布手套B、耐酸碱手套C、皮手套10、【单选题】从气化带入甲醇洗的机械杂质主要是()。
( C )A、金属杂质B、各类结晶C、炭黑11、【单选题】以下()出血最具危险性,如不及时处理将造成生命危险。
( C )A、静脉出血B、毛细血管出血C、动脉出血12、【单选题】以下关于接触毒物工人作业规定说法不正确的是()。
氨合成工艺流程中

氨合成工艺流程中氨是一种重要的化学品,在工业生产中有广泛的应用。
氨的合成工艺流程主要包括催化剂选择、催化剂制备、反应器设计、原料选择、工艺参数控制等几个步骤。
以下是氨合成工艺流程的详细介绍。
一、催化剂选择与制备氨的合成通常采用铁催化剂或钴催化剂。
铁催化剂适用于低温低压条件下的氨合成,而钴催化剂适用于高温高压条件下的氨合成。
铁催化剂的制备通常是将铁矿石经过高温还原生成的金属铁与氧气反应生成Wüstite。
然后将Wüstite与氨气或氮气进行还原,得到铁催化剂。
钴催化剂的制备通常是将硫酸钴溶液与氨气或氮气反应,生成无水氯化钴。
然后将无水氯化钴与氢气在高温下进行还原,得到钴催化剂。
二、反应器设计氨的合成通常采用固定床反应器。
反应器的设计考虑到催化剂的运动和热力学特性,以实现高效的氨合成。
反应器的结构一般分为上部进料区、中部反应区和下部产物区。
进料区通常设有预加热装置,将气体的温度升高到反应温度。
反应区通常由几个催化剂填料层组成。
填料层可以增加反应的接触面积,提高反应效率。
产物区通常设有冷却装置,将反应产生的热量带走,保持反应的温度。
三、原料选择氨的合成的原料通常包括氢气和氮气。
氢气一般来自于天然气或石油制气的副产物。
氮气一般来自于空分设备。
四、工艺参数控制氨的合成的工艺参数主要包括温度、压力和气体比例等。
温度影响氨的生成速度和催化剂的寿命,通常保持在200-500°C之间。
压力影响氨的产率和催化剂的活性,通常保持在100-300atm之间。
氢气和氮气的比例影响氨的选择性和氨的产率,通常保持在1:3-3:1之间。
五、氨的分离与精制氨合成反应产生的气体混合物中含有大量的惰性气体和杂质。
因此需要对气体进行分离和精制。
通常采用液气分离和吸附分离的方法。
液气分离通常采用吸附剂或凝析剂将气体中的氨吸附或凝形成液体,然后通过蒸馏或吸附解吸将氨分离出来。
吸附分离通常采用活性碳吸附剂,通过气体分子的表面吸附来分离氨。
2023年合成氨工艺参考题库附答案

2023年合成氨工艺参考题库含答案(图片大小可自由调整)第1卷一.全能考点(共50题)1.【判断题】承包人必须有一套健全的项目财务管理制度,按规定的权限和程序对项目资金的使用和费用的结算支付进行审核、审批,使其成为施工成本控制的一个重要手段。
2.【单选题】综合应急预案应当包括本单位的应急组织机构及其职责、预案体系及响应程序、()、应急培训及预案演练等主要内容。
A、应急预案管理B、编制依据和目的C、事故预防及应急保障3.【单选题】关于个人防护的要求,不适宜的是()。
A、接触有毒粉尘时,作业人员应穿防尘工作服,戴机械过滤式防毒口罩B、接触强酸、强碱时,作业人员应穿耐酸、耐碱工作服C、接触有毒烟雾时,作业人员应佩戴化学过滤式防毒口罩或面罩4.【单选题】易燃液体充装时应控制流速,其流速不得超过3m/s,其原因是()。
A、防溢出B、防静电C、防温度升高5.【判断题】限制火灾爆炸事故蔓延的措施是分区隔离、配置消防器材和设置安全阻火装置。
6.【单选题】海因里希事故因果连锁理论认为,中断事故连锁的进程,就可避免事故的发生。
根据这一原理,企业安全生产工作应以()为中心。
A、形成注重安全的良好环境B、使用无缺点的人C、防止人的不安全行为、消除物的不安全状态7.【单选题】在药壶爆破时,爆破飞石对人的最小安全距离时()m。
A、200B、300C、4008.【判断题】从事化工作业人员必须佩带防护镜或防护面罩。
A、温度变化B、地基不均匀沉降C、地震D、荷载过大10.【单选题】防治噪声污染的最根本的措施是()。
A、采用吸声器B、从声源上降低噪声C、减振降噪11.【单选题】施工升降机严禁()用行程限位开关作为停止运行的控制开关。
A、严禁B、可以C、不能D、不可12.【单选题】生产性粉尘对人体有多方面的不良影响,能引起严重的职业病--矽肺的粉尘是含有()。
A、有毒物质B、游离二氧化硅C、放射性物质13.【单选题】比水轻的非水溶性可燃、易燃液体火灾,原则上不能用()扑救。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氨合成熔铁催化剂
氨合成熔铁催化剂,目前合成氨工业中普遍使用的主要是以铁为主体的多成分催化剂,又称铁触媒。
1、组成
1.1组成
主要成分是Fe3O4,含量在90%左右。
助催化剂为K2O、Al2O3、CaO、MgO等,含量小于催化剂总质量的9%,低压催化剂还增加了CoO(A201等)。
其按作用不同分为两类,一类是结构型助剂,如Al2O3、Cr2O3、ZrO2、TiO2、MgO、CaO、SiO2等难熔氧化物。
另一类是电子型助剂,如K20。
每种类型助剂都有各自的最佳添加量,一般均在0.6%~1.0%范围。
1.2 物理结构
氧化态催化剂主体是磁铁矿,其化学计量式是FeO.Fe2O3或Fe3O4。
晶体结构类似于尖晶石(MgAl2O4)的结构(90%以上是具有反尖晶石结构、不均匀复杂体系的磁铁矿)。
是四面体和八面体结构的堆积结果。
其中形成两种间隙:四面体间隙和八面体间隙。
三价的金属离子占据四面体间隙的一半和八面体间隙的一半,二价的铁离子占据八面体间隙(Fe3+(Fe2+,Fe3+))。
磁铁矿的一个单胞(晶体的最小结构单元)由32个氧离子和24个铁离子所组成,即8(Fe3O4)。
按结晶学原理,32个氧原子按照面心立方堆积的每一单胞,有64个四面体间隙和32个八面体间隙。
如上所述,除了24个被铁离子占据以外,其余大部分是空的,因此可加入助催化剂占据这些空隙形成间隙固溶体。
而且化学式相近的物质,结构类型相同且质点(离子、原子或分子)半径近于相等的物质,可以发生同晶取代,生成置换固溶体,例如三价铝即可置换部分三价铁,形成置换固溶体。
(含量小于4%时主要生成置换固溶体。
若三氧化二铝全部取代氧化铁则生成FeOAl2O3)
1.3 化学特点
铁触媒在500 ℃左右时的活性最大,这也是合成氨反应一般选择在500 ℃左右进行的重要原因之一。
但是,即使是在500 ℃和30 MPa时,合成氨平衡混合物中NH3的体积分数也只为26.4%,即转化率仍不够大。
在实际生产中,还需要考虑浓度对化学平衡的影响等,例如,采取迅速冷却的方法,使气态氨变成液氨后及时从平衡混合气体中分离出去,以促使化学平衡向生成NH3的方向移动。
2、应用及用途
2.1 催化类型
熔铁催化剂一般用于氧化还原反应。
2.2 应用
主要用于合成氨厂的氨合成过程,催化的反应为
N2+3H2→2NH3
目前国内大型合成氨厂主要使用A103、A110系列和ICI47-1型号,而其他型号主要用于中、小型合成氨厂。
此类催化剂也可用于冶金工业、电子工业中催化氨分解制纯氢和纯氮气体。
A106主要用于冶金工业、电子工业使氨分解为纯净的H2和N2。
NH4分解温度650℃,常压下空速1000~2000 h-1。
A110-4在低温下有较高活性,是一种理想的合成氨催化剂,用于冶金、电子工业中是氨分解为纯净的H2和N2,亦可用于H2,N2混合气中脱除CO,CO2。
另外此催化剂暴露在空气中会迅速燃烧失去活性。
3、制备方法
制法基本为熔融法。
将磁铁矿(Fe3O4)砂精选,然后与氧化铝、石灰石、硝酸钾一起混合,若有其他助剂也同时混入。
混合均匀后置于电炉中,再加一定量金属铁,通电使这些物料熔融。
待完全熔化后,倾出至铁盘中,待冷却后破碎、磨角、过筛分级,即得无规则形状的氧化态成品。
若制备预还原型产品,则将氧化态成品置于还原炉中,用含氢气体在一定温度下进行还原,然后降温钝化,制得预还原型催化剂。
球形催化剂是将熔融物料引入特殊的成球设备,使其在冷却过程中形成球状。
4、使用方法
还原活化将Fe3O4用合成气或H2还原为金属Fe,还原时维持温度<500℃。
5、失活
5.1 衰老
催化剂在长期高温下使用,其中的微晶逐渐长大,减少了内表面积,微晶长大的速度与温度有关,长期处在高温下使用还可能破а-Fe微晶结构,使其变为另一种晶形而失活。
衰老与催化剂的热稳定性有关,热稳定性是指催化剂高温下抗重结晶的能力,超过某一温度重结晶的现象十分显著。
这个温度叫耐热温度。
5.2 中毒
原料气中某些组份与催化剂发生作用,使其组成、结构发生变化,降低甚至使催化剂失去活性。
中毒分为两类,一类叫暂时性中毒,另一类叫永久性中毒。
由氧及含氧化合物引起的中毒,可以通过重新还原使催化剂恢复活性,这叫暂时性中毒。
由As,P,S,Cl化合物、润滑油等物质引起的中毒,使催化剂原有的性质,结构彻底发生变化,不能再还原恢复活性,这叫永久性中毒。
铁催化剂在合成塔内长期使用后,活性逐渐下降。
那么把催化剂具有足够活性的使用期限,称为催化剂的寿命。
催化剂的寿命一方面取决于其组成喝制备方法及工艺条件;另一方面取决于原料气的净化程度及操作质量。
后者会引起活性下降,活性下降的原因主要可分为两类:即催化剂的衰老和中毒。
铁催化剂的抗毒性能很差,所以要求合成气中含硫量小于0.1ppm。
5.3 原理
(1)O2、H2O:它们的存在会氧化催化剂活性表面,在氢气气氛中,被氧化部分又被还原,如此循环往复,引起催化剂铁微晶的长大或晶型转变,导致催化剂活性下降。
轻度的氧化,如及时处理,可使催化剂恢复或部分恢复活性。
而一旦氧化过于严重,催化剂的活性将永久性地丧失。
(2)S、P、As、Cl以及它们的化合物:这类物质会在催化剂的活性中心形成稳定的表面化合物,钝化催化剂的活性中心,一般说来,这种毒害作用是不可逆的。
(3)CO+CO2:合成气中的CO将与氢作用而向甲烷转化,一方面消耗了原料氢,生成了另一种毒物水并增加了惰气浓度,另一方面放出了大量的热( -206.2kJ/mo1)引起催化剂的烧结。
CO2的毒害作用是与催化剂中助剂K2O发生化学反应,使得催化剂的结构发生变化,引起催化剂性能的降低。
(4)油:油的来源一般是高压机和合成系统的循环机。
当油进入催化剂床层后,如薄膜覆盖在催化剂的表面,阻碍合成气向催化剂表面的扩散。
在高温下,油还会发生裂解碳化,堵塞催化剂的机械孔道。
另一方面,油的成份中常含有有机硫,而硫又是一种更为厉害的毒物。
6、再生。
