人教版高中化学选修5 第四章第二节 糖类--葡萄糖果糖麦芽糖蔗糖的结构和转化
人教化学选修5第四章第二节 糖类(共24张PPT)

➢葡萄糖的用途(性质决定用途)
作为营养物质、制药、制镜、制糖果
果糖分子不像葡萄糖分子那样含有醛基, 果糖是一种多羟基酮,结构简式为:
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH 果糖是否也像葡萄糖一样具有还原性,能发 生银镜反应呢?
★催化氧化成醛 因为乙醇中含有—OH官能团
葡萄糖结构简式为:
CH2 CH CH CH CH CHO OH OH OH OH OH
或 属CH于2多OH羟(基CH醛OH)4CHO
探究二:葡萄糖的化学性质 (由结构猜想)
➢葡萄糖的化学性质
与新制银氨溶液反应 ①醛基的性质: 与新制Cu(OH)2反应
与H2加成 酯化 ② 羟基的性质: 与钠反应 消去反应 ③ 人体内氧化反应-人体能量主要来源:
CH 2OH
CH 2OH
在酸性条件下,果糖不能转变为葡萄糖,所以
不能被溴水氧化。所以,可用溴水区别葡萄糖和果糖
探究四:结合果糖的结构简式预测它的 化学性质
小结:
结构简式 ①羟基的性质
葡萄糖
②醛基的性质
化学性质
③人体内氧化反应
④发酵生成酒精 结构简式
果糖
①羟基的性质
化学性质
②羰基的性质 ③碱性条件下,能被银氨溶液
到淡蓝
色Cu(OH)
沉淀
2
生成
。
在新制Cu(OH)2悬浊液试管里,立即加
入10%葡萄糖溶液2mL,振荡后观察现
象; 然后再加热观察现象。
探究一:根据下列信息推出葡萄糖的分子结构 1、 P80实验4—1 ,认真观察现象,由实验现象
分析葡萄糖具有什么官能团? 说明葡萄糖分子中含有—CHO。 2、在一定条件下,1mol葡萄糖与1molH2反应, 还原成正己六醇。
【人教版化学】选修五第四章第二节糖类课件

多元醇的性质
D.葡萄糖是单糖
3.葡萄糖是单糖的原因是 B A.在糖类中含碳原子数最少 B.不能水解成为更简单的糖 C.结构最简单 D.分子中只有一个醛基
4.下列有机物既能在常温下溶于水,又能产
生银镜反应的是
C
A.甲醇
B. 甲酸乙酯
C.葡萄糖
D.苯酚
5.关于葡萄糖的叙述错误的是
A.是白色晶体,能溶于水
氧化
G COOH
CH2Br CH2Br
CH2OH
CHO
COOH
CH2OH
CHO
O
H :结构为 CH2 CH2
CO CO
O
练:某有机物A,完全燃烧生成22gCO2和9gH2O, (1)求A的C、H原子个数比是 1:2
(2)若燃烧所用A的质量为15g,其实验式为 CH2O
① 若A的蒸气密度是同温同压下氢气密度的 30 倍,则A的分子式为 C2H4O2
4、葡萄糖的用途
葡萄糖
生活中——糖果 工业上——制镜 医药上——迅速补充营养
(二) 果糖
分子式: C6H12O6
结构简式:
CH2—CH—CH—CH—C—CH2OH OH OH OH OH O
多羟基酮
葡萄糖
果糖
分子式 结构特点
C6H12O6(同分异构体)
多羟基醛
多羟基酮
存
在 自然界散布最广,葡萄及甜味水果中
第二 节
糖类
概念:从结构上看,它一般是多羟基醛或多羟 基酮,和它们的脱水缩合物。 来源——绿色植物光合反应的产物 组成——由C、H、O元素组成 糖类习惯称碳水化合物,通式:Cn(H2O)m
1.有甜味的不一定是糖。 判断: 2.没有甜味的也可能是糖。
高中化学人教版选修五4.2糖类

AC
B、二者含有C、H、O三种元素的质量分数相同,且互为
同分异构体
C、它们均属于糖类,且都是高分子化合物
D、都可用(C6H10O5)n表示,但淀粉能发生银镜反应,而 纤维素不能
蔗糖 麦芽糖
C12H22O11 (二糖)
淀粉
(C6H10O5)n (多糖)
合缩 水
纤维素
水解 缩合
C6H12O解6(单糖)发酵 C2H5OH+CO2
1.下列关于糖的说法正确的是(BD) A.糖类中除含有C、H、O三种元素外,还 可能含有其他元素 B.葡萄糖是多羟基醛 C.能发生银镜反应的物质一定属于醛类 D.糖类可划分为单糖、低聚糖、多糖三类
2.下列有机物既能在常温下溶于水,又能 发生银镜反应的是(C)
A.甲醇
B. 甲酸乙酯
C.葡萄糖
D.苯酚
2、纤维素
(1)存在:植物茎、叶和果皮 如棉花、亚麻、木材、稻草、麦秸等
(2)物理性质 白色、无味,不溶于水和有机溶剂
(3)化学性质
①水解反应
(C6H10O5)n+nH2O 浓H2SO4 nC6H12O6
纤维素
葡萄糖
②酯化反应: 硝酸纤维、醋酸纤维
人体中没有水解纤维素的酶,纤维素在 人体中主要是加强胃肠的蠕动,有通便 功能
5.关于淀粉和纤维素的叙述中,正确的是( D ) A.分子式相同,互为同分异构体 B.都是多糖,化学性质完全相同 C.分子式不同,所含的碳、氢、氧元素的质量比不相同 D.都能水解,且水解最终产物相同
6.能把乙醇、乙酸、甲酸、葡萄糖溶液用一种试剂区 别开,这种试剂是( C ) A.溴水 B.银氨溶液 C.新制的氢氧化铜悬浊液 D.酸性高锰酸钾溶液
如大米、小麦、土豆等 (2)物质性质:
人教版高中化学选修五课件4-2糖类

(C6 H10O5 ) n nH 2O 催化剂 nC6 H12O6
(纤维素)
(葡萄糖)
OH
浓硫酸
ONO2
C6H7O2–OH+3nHO-NO2—+3nHC2O6H7O2–ONO2
OH n
ONO2 n
纤维素三硝酸酯(硝酸纤维)
OH
(C6H7O2)
OH OH
n
+ 3nHOOCCH3
浓硫酸 (C6H7O2)
O
─C─H O
─C─ O
─C─OH O
─C─O─
如何设计实验验证?
可能存在的常见官能团的验证
(1)可能存在—OH ①发生酯化反应;②与Na反应放出氢气,与 NaOH、Na2CO3不反应。
(2)可能含—CHO ①与银氨溶液水浴加热发生银镜反应. ②与新制Cu(OH)2加热生成砖红色沉淀;
(3)可能存在—COOH ①与指示剂作用;②与NaHCO3反应放出CO2
请根据以上实验数据推断该有机物分子(C6H12O6)的 结构简式。
多糖:由很多单糖分子按照一定的方式,通过分子间脱水结合 而成的糖类。
多糖一般不溶于水,无甜味,无还原性,是高分子化合物。 高分子化合物:式量从几万到几十万的化合物。
三、淀粉纤维素
注意:淀粉与纤维素虽均用(C6H10O5)n表示其分子组成,但由于 聚合度不同故两者不是同分异二节糖类
自学提炼 糖类的组成和分类
(一)组成 糖类是由C、H、O三种元素组成。
大多数糖可用分子通式Cn(H2O)m表示,故糖类物质又称 碳水化合物。 注意:(1)糖分子中H、O原子并不以H2O分子的形式存在; (2)少数糖不符合此通式,如:鼠李糖C6H12O5; 符合此通式的并不都属糖,如:CH3COOH、HCHO。 (二)分类与相互转化关系
人教版高中化学选修五第四章第二节糖类教学课件 (共16张PPT)

A、主要来源是光合作用 B、人体所需的营养素之一 C、生物体维持生命活动所需
能量的唯一来源 D、糖类与生物体的结构有关
巩固练习
2、葡萄糖不能发生下列反应中的( D )
A、酯化反应 B、加成反应 C、氧化反应 D、水解反应
巩固练习
3、下列关于糖类的叙述正确的是( C )
2、果糖:
分子式:C6H12O6 结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH 多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的 影响有很强的还原性,所以果糖能被银氨溶液 和新制氢氧化铜氧化。
在酸性条件下,果糖不被溴水氧化,可用溴水 区分葡萄糖和果糖。
巩固练习
说明葡萄糖分子中含有一个醛基
(2)葡萄糖的分子组成和结构 分子式: C6H12O6
结构简式:
CH2 CH CH CH CH CHO OH OH OH OH OH
或CH2OH(CHOH)4CHO
结构特点:含官能团醛基和羟基 预测:葡萄糖的化学性质
(3)化学性质(具有醇与醛的共同性质)
【演示实验4-1】 实验1、银镜反应
二、葡萄糖与:
白色晶体,有甜味,易溶于水, 稍溶于乙醇,不溶于乙醚。
(2)葡萄糖的分子组成和结构 科学推理:
根据下列信息推出葡萄糖的分子组成 葡萄糖的相对分子质量为180,其中含碳40%, 氢6.7%,其余是氧。求分子式。
葡萄糖分子式:C6H12O6
科学推理:
现象: 试管内壁形成光亮的银镜
反应方程式: CH2OH(CHOH)4CHO + 2Ag(NH3)2OH →△ 2Ag↓+
CH2OH(CHOH)4COONH4 + 3NH3 + H2O
高二化学选修5课件4-2-1葡萄糖蔗糖.ppt

形成银镜。
人
教
反 应 的 化 学 方 程 式 : CH2OH(CHOH)4CHO +
版 化 学
2Ag(NH3)2OH ―△―→ CH2OH(CHOH)4COONH4 + 2Ag↓ +
3NH3+H2O。
第四章 生命中的基础有机化学物质
(3)葡萄糖与新制氢氧化铜反应。
在加热的条件下,葡萄糖与新制氢氧化铜反应生成氧化
版 化
学
许多糖还是重要的工业原料。
第四章 生命中的基础有机化学物质
人 教 版 化 学
第四章 生命中的基础有机化学物质
【例1】 下列对糖类的叙述正确的是( )
A.含有C、H、O三种元素的有机物叫糖类
B.糖类物质均能与银氨溶液在加热时发生反应生成银 人 教
镜
版 化
学
C.糖类物质都有甜味
D.糖是多羟基醛,多羟基酮和它们的脱水缩合的产物
有甜味的不一定就是糖(如糖精),故C选项不正确。A、B、
C都不正确。则D必正确。
【答案】 D
第四章 生命中的基础有机化学物质
有关糖类物质的叙述中正确的是( )
A.糖类物质一定有甜味,有甜味的物质一定是糖
人
教
B.单糖一定不能发生水解反应
版 化
学
C.糖类物质又叫碳水化合物,其分子式都可用
Cn(H2O)m表示,不符合此通式的不属于糖类
________溶于乙醇,甜味仅次于________。
第四章 生命中的基础有机化学物质
7 . 在 ________ 条 件 下 , 蔗 糖 可 水 解 成 ________ 和 ________,水解反应的化学方程式为:________________。
8.麦芽糖的分子式为________,与蔗糖互为________,人
人教版高二化学选修五 第四章 第二节 糖类 (共32张PPT)

3.葡萄糖和果糖
1.葡萄糖
蔗糖
白糖、红糖、冰糖有什么区别?
红糖、白糖、冰糖都来自于甘蔗。先做出红糖, 经提炼后做成白糖,白糖脱水结晶成为冰糖。 红糖是热性的,红糖生姜汤可以去寒,治感冒。 红糖还有补血作用,产后吃红糖、鸡蛋。 白糖是清凉的,夏天西红柿拌白糖,可以去暑。 如果被开水烫着了,可以抹白糖水。 冰糖润肺生津,梨加冰糖可以治疗咳嗽,润肺化 痰。老人口干,可含一块冰糖。
(2)组成和结构
蔗糖由1分子葡萄糖和1分子果糖,脱去1分子水 形成,分子式为C12H22O11,分子中无醛基
(3)物理性质
白色晶体,有甜味,易溶于水、较难溶于乙醇
(4)化学性质(水解)
稀硫酸
C12H22O11+H2O 蔗糖
C6H12O6+C6H12O6 葡萄糖 果糖
(5)用途
甜味剂
蔗糖水解产物的检验
甜味剂
小结
一、糖的定义 二、糖的分类
葡萄糖 单糖 果糖 蔗糖 糖 低聚糖 麦芽糖 淀粉 多糖 纤维素
当堂检测
1.下列关于糖类的说法正确的是( C ) A.糖类物质的组成都符合Cm(H2O)n B.葡萄糖比果糖要甜 C.含有醛基的糖就是还原性糖 D.糖类是具有甜味的物质
∆
葡萄糖中含有-CHO,为还原糖
用途
工业制镜 糖果制造业
医 药 工 业
葡萄糖可直接被人体 吸收。因此,体弱和 血糖过低的患者可利 用静脉注射葡萄糖溶 液的方式来迅速补充 营养。
高二化学人教版选修五课件第四章第二节糖类(43张)

②还原性:麦芽糖分子中含醛基,能发生银镜反应,是一种 还原 型
二糖。
四、淀粉与纤维素 1.淀粉和纤维素都是由多个 葡萄糖 分子脱水而形成的, 其分子式为 (C6H10O5)n ,淀粉、纤维素的每个葡萄糖单元仍 有 三个 羟基,所以其分子式也可写成[C6H7O2(OH)3]n 。由于 二者 n 不同,所以不是同分异构体。 2.淀粉和纤维素都属于天然 高分子化合物 ,相对分子质 量较大。
2.蔗糖溶液、麦芽糖溶液和蔗糖水解产物的还原性实验
实验步骤 实验现象
结论解释
注意事项
加入蔗糖的试管 无明显现象,加入 麦芽糖的试管产
生红色沉淀
蔗糖分子内 无醛基;麦芽 糖分子内有 醛基,是还原
性糖
①蔗糖水解实验 需要用水浴加热; ②检验水解产物 葡萄糖时,一定要 先加 NaOH 溶液
加入银氨溶液的
答案: C
3.下列说法中正确的是( ) A.碘化钾溶液能使淀粉显蓝色 B.纤维素的水解难于淀粉的水解 C.用淀粉制乙醇仅发生了水解反应 D.多糖一般没有还原性,但有甜味
解析:单质碘才能使淀粉显蓝色,A 项错误;淀粉在稀 酸或酶的作用下就能水解,纤维素在稀酸或浓酸并加压下才 能水解,可见纤维素比淀粉更难水解,B 项正确;用淀粉制 乙醇的过程:淀粉催—化①—→剂葡萄糖酒—化②—→酶乙醇,其中反应①是 水解反应,反应②不是水解反应,C 项错误;多糖一般无还 原性,也没有甜味,D 项错误。
糖没有还原性,不能发生银镜反应;麦芽糖属于二糖,能
发生银镜反应。
答案: D
1.淀粉
[新知探究]
人教版高二化学选修5第4章第2节-糖类-ppt课件(共50张PPT)

人教版高二化学选修5第4章第2节-糖 类-ppt 课件(共 50张PPT)
3.淀粉的物理性质 ①淀粉是_白__色、_无___味的_粉__末__状物质; ②__不__溶于冷水; ③在热水中产生__糊_化___作用(即食物由生 变熟的过程)
思考: 如何设计实验证明淀粉的水解已经开始?
如何证明淀粉的水解已经完全?
如何证明水解没有发生?
淀粉液
硫酸 加热
水解液
碘水 现象A
NaOH
溶液
中和液
银氨溶液 水浴加热
现象B
现象
结论
现象A 溶液变蓝
现象B 无银镜生成
淀粉没有水解
溶液变蓝 有银镜生成 溶液无现象 有银镜生成
淀粉部分水解 淀粉完全水解
人教版高二化学选修5第4章第2节-糖 类-ppt 课件(共 50张PPT)
C6H12O6
葡萄糖
果
糖 互为同分异构体
麦芽糖
C12H22O11
含醛基
C12H22O11+H2O
麦芽糖
催化剂 2C6H12O6
葡萄糖
三、淀粉、纤维素(多糖)
(C6H10O5)n
淀粉、纤维素的结构比较:
都是由多个葡萄糖脱水形成的。
(1).淀粉、纤维素的分子式为:
(C6H10O5)n
(2).但是葡萄糖分子间的结合方式不同,
分子中含有约_几__千___个单糖单元; 相对分子质量为几十万至百万 ; (2)属于_天__然__高__分___子_化合物; (_3有_)__纤差维异素。结构与淀粉_不__同,所以性质
人教版高二化学选修5第4章第2节-糖 类-ppt 课件(共 50张PPT)
人教版高中化学选修5 第四章第二节 糖类--葡萄糖果糖麦芽糖蔗糖的结构和转化
才可以参加还原反应(例如,银镜反应)。
但具体是为什么,现在具体谈一谈。
我们知道糖是多羟基醛(果糖是酮),之所以糖能发生还原反应是因为其含有醛基的结构。
那么,比较蔗糖和麦芽糖时就从它们有无醛基开始。
我们知道蔗糖与麦芽糖是二糖,是由两个单糖组成的(蔗糖是由一分子葡萄糖和一分子果糖组成;麦芽糖由两分子葡萄糖组成)。
之所以蔗糖不能参加还原反应而麦芽糖却可以肯定是蔗糖不含有醛基,而麦芽糖含有。
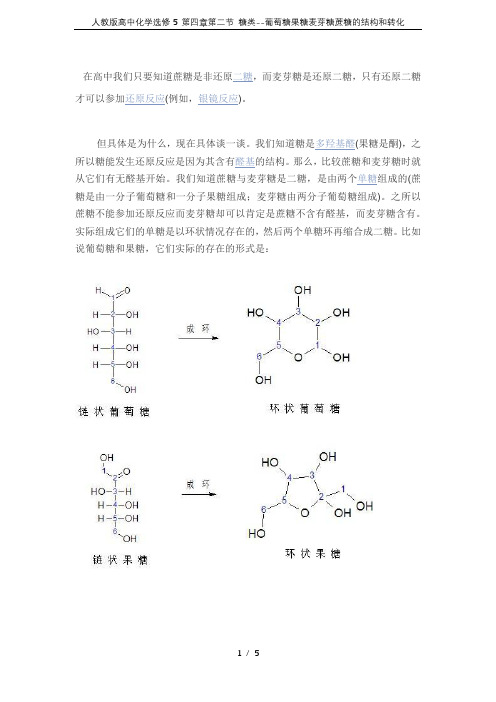
实际组成它们的单糖是以环状情况存在的,然后两个单糖环再缩合成二糖。
比如说葡萄糖和果糖,它们实际的存在的形式是:在环状的单糖的结构中,只要和环上的氧原子相邻最近碳上连有羟基,那么该糖就含有还原性,就像所举的例子中环状葡萄糖1号碳上有羟基,果糖2号碳上有羟基,所以它们都是还原糖,都可以发生还原反应。
现在,开始解释蔗糖和麦芽糖的还原性问题。
实际蔗糖和麦芽糖的结构如下:我们发现,麦芽糖的两个含氧环中有一个环的离环上氧最近的碳(即1号碳)上有羟基,所以它有还原性可以参加还原反应;而蔗糖的两个环中找不到这样的羟基,所以它没有还原性,不能参加还原反应。
补充:环状的糖中如果有上述像麦芽糖中1号碳这样的羟基,或者葡萄糖1号碳和果糖2号碳上的羟基的话,就会解离出醛基,那么就会有还原性了。
如果你是高中生,那么能理解到这里就可以了。
下面我解释的是高中以外的内容,可以试着理解一下。
链状的糖是怎么形成环状的?其实是它反生了半缩醛(酮)反应,反应式如下:上述反应中,如果R1和R2中至少有一个为H时,产物就为半缩醛,如果都为烃基那么就称为半缩酮~其实链状单糖就是反生了这个反应才成环的。
比如说链状葡萄糖中(如上述图),1号的醛基碳就与5号碳的羟基缩合成了半缩醛而成环的。
通过观察半缩醛(酮)反应,发现该反应是可逆反应,也就是说在反应过程中环状的糖是可以再变回链状的糖,从而会产生游离的醛基(或酮基)产生还原性从而可以参加还原反应。
观察半缩醛或半缩酮发现,它们的结构特点是两个氧原子夹着一个碳原子(两个氧原子必须直接连在所夹的碳原子上),其中一个氧原子必须得连着H原子,另一个必须连着非H原子(一般为烃基)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
才可以参加还原反应(例如,银镜反应)。
但具体是为什么,现在具体谈一谈。
我们知道糖是多羟基醛(果糖是酮),之所以糖能发生还原反应是因为其含有醛基的结构。
那么,比较蔗糖和麦芽糖时就从它们有无醛基开始。
我们知道蔗糖与麦芽糖是二糖,是由两个单糖组成的(蔗糖是由一分子葡萄糖和一分子果糖组成;麦芽糖由两分子葡萄糖组成)。
之所以蔗糖不能参加还原反应而麦芽糖却可以肯定是蔗糖不含有醛基,而麦芽糖含有。
实际组成它们的单糖是以环状情况存在的,然后两个单糖环再缩合成二糖。
比如说葡萄糖和果糖,它们实际的存在的形式是:
在环状的单糖的结构中,只要和环上的氧原子相邻最近碳上连有羟基,那么该糖就含有还原性,就像所举的例子中环状葡萄糖1号碳上有羟基,果糖2号碳上有羟基,所以它们都是还原糖,都可以发生还原反应。
现在,开始解释蔗糖和麦芽糖的还原性问题。
实际蔗糖和麦芽糖的结构如下:
我们发现,麦芽糖的两个含氧环中有一个环的离环上氧最近的碳(即1号碳)上有羟基,所以它有还原性可以参加还原反应;而蔗糖的两个环中找不到这样的羟基,所以它没有还原性,不能参加还原反应。
补充:
环状的糖中如果有上述像麦芽糖中1号碳这样的羟基,或者葡萄糖1号碳和果糖2号碳上的羟基的话,就会解离出醛基,那么就会有还原性了。
如果你是高中生,那么能理解到这里就可以了。
下面我解释的是高中以外的内容,可以试着理解一下。
链状的糖是怎么形成环状的?其实是它反生了半缩醛(酮)反应,反应式如下:
上述反应中,如果R1和R2中至少有一个为H时,产物就为半缩醛,如果都为烃基那么就称为半缩酮~其实链状单糖就是反生了这个反应才成环的。
比如说链状葡萄糖中(如上述图),1号的醛基碳就与5号碳的羟基缩合成了半缩醛而成环的。
通过观察半缩醛(酮)反应,发现该反应是可逆反应,也就是说在反应过程中环状的糖是可以再变回链状的糖,从而会产生游离的醛基(或酮基)产生还原性从而可以参加还原反应。
观察半缩醛或半缩酮发现,它们的结构特点是两个氧原子夹着一个碳原子(两个氧原子必须直接连在所夹的碳原子上),其中一个氧原子必须得连着H原子,另一个必须连着非H原子(一般为烃基)。
这样,麦芽糖中(如上述图)的1号碳被两个氧原子所夹,而其中的一个氧原子连着一个H原子,刚好是半缩醛,所以可以产生游离的醛基。
而蔗糖没有半缩醛结构,所以不能产生游离的醛基(或酮基)。
补充:
蔗糖是由单糖通过下述反应形成的:
反应式首先是可逆的,就是说蔗糖可以通过加入一分子的水(即糖的水解反应),而变回一分子的葡萄糖和一分子的果糖,从而又具有还原性。
这也与"蔗糖不能发生银镜反应,而水解后可以反生银镜反应"的事实相符。
蔗糖之所以不具还原性就是因为两分子的单糖是通过它们还原性的半缩醛(酮)的羟基脱水缩合而成的,从而不再具有半缩醛结构,也就不会产生游离的醛基而具有还原性了。
补充:
在实验中发现,葡萄糖和果糖都可以反生银镜反应,但是高中所学的可以发生银镜反应的物质是醛类。
葡萄糖是醛,可以反生银镜反应这个好理解,可果糖没有醛基只有酮基,酮基是不发生银镜反应的,为什么会与实验结果不相符?原来,葡萄糖在碱性的条件下可以转化成果糖,同样果糖又可以转化成葡萄糖(这个反应称为单糖的差相异构化),这个过程在碱性的条件下是可逆的过程。
反应式如下:
银铵溶液是碱性的,恰好可以发生这样的反应。
虽然果糖不含醛基,但是可以在银铵溶液中转化成葡萄糖而含有醛基,从而发生银镜反应。
