常见血液系统肿瘤免疫表型
WHO软组织肿瘤免疫表型大全
2013版WHO软组织肿瘤免疫表型大全2014-11-06艾迪康病理诊断主要根据2013年“WHO肿瘤分类——软组织和骨肿瘤”翻译而来第1章脂肪细胞肿瘤(adipocytictumours)良性1、脂肪瘤(lipoma)免疫表型:成熟脂肪细胞表达S-100、leptin和HMGA2阳性。
2、脂肪瘤病(lipomatosis)免疫表型:和正常脂肪相似。
3、神经脂肪瘤病(lipomatosisof nerve)免疫表型:因为病变的所有成分均存在于正常神经内,故免疫组化对诊断没有帮助。
4、脂肪母细胞瘤(lipoblastoma)/脂肪母细胞瘤病(lipoblastomatosis)免疫表型:脂肪细胞表达S-100和CD34,原始间叶细胞常表达desmin。
5、血管脂肪瘤(angiolipoma)免疫表型:血管内皮成分CD31等内皮标记阳性,细胞性血管脂肪瘤增生的梭形细胞CD31阳性,证明为血管内皮。
6、软组织平滑肌脂肪瘤(myolipomaof soft tissue)免疫表型:梭形细胞SMA和desmin染色弥漫强阳性,证明为平滑肌分化;ER 和PR阳性也有报道;HMB-45阴性。
7、软骨样脂肪瘤(chondroidlipoma)免疫表型:成熟脂肪细胞S-100强阳性,脂肪母细胞S-100弱阳性,随脂肪细胞逐渐成熟S-100染色逐渐增强。
无脂肪母细胞分化特征的细胞S-100阴性。
少数病例角蛋白阳性,但EMA一致阴性。
8、梭形细胞脂肪瘤/多形性脂肪瘤(spindlecell lipoma/pleomorphic lipoma)免疫表型:梭形细胞脂肪瘤和多形性脂肪瘤中的梭形细胞均为CD34强阳性,S-100罕见阳性,偶见desmin阳性。
9、冬眠瘤(hibernoma)免疫表型:冬眠瘤细胞通常表达S-100阳性。
除梭形细胞亚型中梭形细胞成分CD34阳性外,其他冬眠瘤亚型CD34均阴性。
新的冬眠瘤标记物还包括UCP1。
血液病免疫分型

血液病免疫分型血液病的免疫分型主要根据免疫表型和免疫遗传学特征进行分类。
以下是一些常见的血液病免疫分型:1. 急性淋巴细胞性白血病(Acute Lymphoblastic Leukemia,ALL)的免疫分型:- B-ALL:由B淋巴细胞系发展而来。
- T-ALL:由T淋巴细胞系发展而来。
2. 慢性淋巴细胞性白血病/小淋巴细胞淋巴瘤(Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma,CLL/SLL)的免疫分型:- CD5+/CD23+/CD20+:典型的B淋巴细胞来源。
- CD5-/CD23+/CD20+:非典型的B淋巴细胞来源。
- CD5+/CD23-/CD20+:突变的B淋巴细胞来源。
3. 急性髓系白血病(Acute Myeloid Leukemia,AML)的免疫分型:- 标准化治疗亚组(NCCN标准化治疗亚组):包括核准的AML-M0至AML-M7亚型。
- 非标准化治疗亚组:包括AML-M0、AML-M6和AML-M7亚型以外的亚型。
4. 慢性髓性白血病(Chronic Myeloid Leukemia,CML)的免疫分型:- Ph染色体阳性(Ph+):含有Ph染色体(Philadelphia染色体)。
5. 骨髓增殖性肿瘤(Myeloproliferative Neoplasm,MPN)的免疫分型:- 慢性骨髓性白血病(Chronic Myeloid Leukemia,CML):Ph染色体阳性。
- 原发性骨髓纤维化(Primary Myelofibrosis,PMF):包括JAK2V617F突变和CALR基因突变。
- 骨髓增殖性肿瘤不分类型(Myeloproliferative Neoplasm,NOS):不符合上述分类的其他骨髓增殖性肿瘤。
这些免疫分型对于血液病的诊断、预后评估和治疗选择具有重要意义。
注意,具体的免疫分型细节可能因研究、疾病进展和新兴的治疗手段而不断改变。
白血病免疫表型 方法学比对

白血病免疫表型方法学比对白血病是一种由于骨髓中恶性克隆细胞的快速增殖导致的血液恶性肿瘤。
免疫表型是指通过检测细胞表面的分子标记来确定细胞类型和状态的方法。
在白血病的免疫表型研究中,常用的方法包括流式细胞术和免疫组化染色。
流式细胞术是一种通过检测细胞表面的抗原分布来确定细胞类型和状态的方法。
在白血病的免疫表型研究中,流式细胞术常用于分析白血病细胞表面的免疫分子标记,例如CD标记。
CD标记是一种用于区分不同细胞类型和状态的标记物。
通过流式细胞术可以确定白血病细胞的表面CD标记的表达情况,从而确定其免疫表型。
免疫组化染色是一种通过使用特异性抗体来检测细胞内或细胞表面蛋白的方法。
在白血病的免疫表型研究中,免疫组化染色常用于检测白血病细胞中特定蛋白的表达情况。
通过免疫组化染色可以确定白血病细胞中特定蛋白的表达水平,进而确定其免疫表型。
除了流式细胞术和免疫组化染色,还有其他一些方法可以用于白血病的免疫表型研究。
例如,多色流式细胞术可以同时检测多个免疫分子标记,提高免疫表型的准确性和效率。
此外,还可以利用质谱分析等技术来确定白血病细胞中特定蛋白的表达水平。
研究白血病的免疫表型可以帮助医生确定疾病的类型和进展情况,指导治疗方案的选择。
例如,通过分析白血病细胞中CD标记的表达情况,可以确定其所属的亚型,从而指导相应的治疗。
此外,免疫表型研究还可以用于监测治疗的效果,评估疾病的预后。
然而,白血病的免疫表型研究也存在一些挑战和限制。
首先,由于白血病细胞的异质性,不同患者之间、甚至同一患者的不同时间点之间可能存在免疫表型的变化。
因此,需要对不同样本进行多次检测,以确定免疫表型的稳定性和一致性。
其次,由于免疫表型的分析涉及到复杂的仪器设备和专业知识,需要有经验丰富的技术人员进行操作和解读结果。
此外,还需要建立可靠的标准和参考范围,以便对免疫表型结果进行解释和比对。
白血病的免疫表型研究是一项重要的临床技术,可以用于确定疾病类型和进展情况,指导治疗方案的选择。
免疫微环境 表型

免疫微环境表型
免疫微环境是肿瘤免疫治疗中一个重要的概念,它指的是肿瘤组织内部免疫细胞和分子所构成的微小环境。
根据对免疫检查点抑制剂应答效率的不同,基于T细胞的浸润情况,可以将肿瘤免疫微环境分为三种不同的表型,分别是免疫沙漠(immune-desert)型、免疫排斥(immune-excluded)型和免疫炎症(immune-inflamed)型。
1. 免疫沙漠型:这种表型的肿瘤缺乏T细胞的浸润,通常对免疫检查点抑制剂治疗不敏感。
2. 免疫排斥型:这种表型的肿瘤虽然有T细胞的浸润,但由于肿瘤细胞产生的某些分子或细胞因子,这些T细胞被排斥在肿瘤细胞之外,同样也对免疫检查点抑制剂治疗不敏感。
3. 免疫炎症型:这种表型肿瘤被T细胞深度浸润,并且显著响应免疫检查点抑制剂的治疗。
以上内容仅供参考,建议查阅关于“免疫微环境表型”的资料、文献,或者咨询生物学家,以获取更全面和准确的信息。
临床血液体液学检验题库(3)

临床血液体液学检验题库(3)一、单选题1、下列为TTP的实验室检查特点为,除外(C)。
A、血小板数减少B、血管内溶血的指标阳性C、血管性血友病因子减少或缺乏D、血管性血友病因子裂解酶异常2、关于原发性血小板增多症实验室特点不符合的是(C)。
A、外周血白细胞常增加,偶有中性幼稚粒细胞B、骨髓增生活跃或明显活跃,可见大量血小板成片分布C、骨髓中粒系、红系常有形态改变D、ADP、肾上腺素诱导的血小板聚集反应常减低或消失3、白细胞中,细胞核染色质呈疏松网状的是(D)。
A、中性粒分叶粒细胞B、嗜酸性粒细胞C、嗜碱性粒细胞D、单核细胞4、杜勒小体的描述,正确的是(C)。
A、脂肪变性B、胞核残留物C、胞质局部不成熟D、巨大深染的嗜天青颗粒5、肾病综合征患者尿液最常见的改变是(D)。
A、乳糜尿、上皮管型B、脓尿、白细胞管型C、血尿、血红蛋白管型D、蛋白尿、复粒细胞、脂肪管型6、关于淀粉样小体,错误的是(D)。
A、多呈圆形或卵圆形B、中央含碳酸钙沉淀物C、有同心圆线纹的层状结构D、数量随年龄的增长而减少7、间日疟原虫患者血液检验,采血时间最好在(B)。
A、病人发热时B、发作后数小时到10余小时C、发冷时D、出汗时8、最可能检出溶组织内阿米巴滋养体的标本是(A)。
A、黏液脓血便B、成形粪便C、脓血痰液D、肝穿刺液9、以下为遗传性易栓症,除外(B)。
A、遗传性蛋白C缺陷症B、抗磷脂综合征C、活化蛋白C抵抗D、异常纤维蛋白原血症10、血清铁蛋白增加见于下列疾病,除外(A)。
A、慢性失血B、恶性肿瘤C、肝癌D、病毒性肝炎11、静脉穿刺时消毒皮肤面积应至少多大(C)。
A、3cm*3cmB、4cm*4cmC、5cm*5cmD、6cm*6cm12、血清铁有明显昼夜规律,波动范围达(C)。
A、5%~10%B、10%~20%C、20%~30%D、30%~40%13、下列疾病中D-D不升高的是(D)。
A、肺栓塞B、DICC、重症肝炎D、陈旧性血栓14、血液恶性肿瘤免疫表型分析最常用的数据采集和分析策略是哪种(B)。
白血病免疫分型讲课最终本

白血病免疫分型讲课最终本引言白血病是一种常见的血液系统恶性肿瘤,其发生与免疫系统的异常功能有着密切的联系。
免疫分型是指根据白血病细胞表面的免疫表型特征对其进行分类和鉴定的方法。
通过免疫分型,我们可以更好地理解白血病的发生机制,为个体化治疗提供参考依据。
本文将重点介绍白血病的免疫分型方法及其临床应用。
1. 白血病的免疫分型白血病的免疫分型是基于白血病细胞的免疫表型特征进行分类和鉴定的方法。
在临床上,常用的免疫分型方法主要包括免疫组织化学染色、流式细胞术和免疫基因重排检测等。
1.1 免疫组织化学染色免疫组织化学染色是一种通过对组织切片中的细胞进行特异性标记,以观察和分析细胞表面抗原表达情况的方法。
通过对白血病组织切片进行免疫组织化学染色,可以确定白血病细胞的免疫表型特征,从而进行免疫分型。
1.2 流式细胞术流式细胞术是一种通过流式细胞仪对细胞进行单个细胞的快速、准确地分析的方法。
通过标记白血病细胞表面的特定抗原,并利用流式细胞仪进行检测和分析,可以确定白血病细胞的免疫表型特征,进而进行免疫分型。
1.3 免疫基因重排检测免疫基因重排检测是一种通过检测白血病细胞中免疫相关基因的DNA或RNA重组情况,来确定白血病细胞的免疫表型特征的方法。
通过免疫基因重排检测,可以发现白血病细胞克隆性演变和克隆扩增的过程,为免疫分型提供重要依据。
2. 白血病免疫分型的临床应用白血病免疫分型在临床上有着重要的应用价值。
通过免疫分型,可以更准确地确定白血病的诊断和分型,为患者提供个体化的治疗方案。
此外,免疫分型还可以评估患者的预后风险和治疗反应,指导治疗方案的调整。
2.1 诊断和分型免疫分型可以通过确定白血病细胞的免疫表型特征,帮助医生更准确地进行白血病的诊断和分型。
不同类型的白血病具有不同的免疫表型特征,通过免疫分型可以将白血病分为急性淋巴细胞白血病(ALL)、急性非淋巴细胞白血病(AML)等不同亚型,进而为患者提供合理的治疗方案。
05血液系统疾病-05血液系统肿瘤(淋巴瘤)

• 临床表现-霍奇金淋巴瘤
• 青年多见
• 无痛性浅表淋巴结肿大,以颈部淋巴 结最多见;病变可从一个或一组淋巴 结开始, 也可开始即为多发。
临床表现-霍奇金淋巴瘤
• 深部淋巴结肿大伴压迫症状 纵隔;腹膜后;硬膜外 • 器官实质浸润:肝脾肿大、肺浸润、胸 膜浸润、胸腰椎破坏、脊髓和脑浸润 • 全身症状:发热、盗汗、疲乏、消瘦、 皮肤瘙痒
光镜下:
淋巴结正常结构部分或全部破坏,
由肿瘤取代。
瘤组织成分较单一,以一种细胞类
型为主(monoclonality)。
B-cell small lymphocytic
B cell
不同种类的淋巴瘤在临床表现和治 疗反应上有很大差异,因此,必须通 过各项检查识别出具有独特临床表现、 组织学改变、免疫表型(B细胞:CD19、 CD20;T细胞:CD45RO、CD2、 CD3)、 遗传学特征的淋巴瘤亚型,并进行分 类。
混合细胞型(mixed cellularity)HL 50岁,男性,单核,双核R-S细胞多
病理及分型
非霍奇金淋巴瘤
(non-Hodgkin’s lymphoma,NHL)
病理形态学特点及分类
• 肉眼观:
• 淋巴结不同程度肿大。早期活动不
粘连,晚期粘连融合成结节状。
• 切面灰白色、鱼肉状,质地较软
周围T细胞淋巴瘤
• • • • • • 一组异质性肿瘤(多型性、T免疫母细胞) 主要侵犯副皮质区,最后破坏整个淋巴结 由核有扭曲的多形性细胞构成 免疫表达CD2、CD3、CD5等T细胞标志 T细胞受体单克隆性重排 高度恶性,进展快
Lymphoblastic(T),convoluted
T cell
• 病因及发病机制
血液肿瘤细胞免疫表型检测在白血病诊断分型中的应用 陈毅晟

血液肿瘤细胞免疫表型检测在白血病诊断分型中的应用陈毅晟发表时间:2013-05-06T09:09:01.810Z 来源:《中外健康文摘》2013年第7期供稿作者:陈毅晟[导读] AML细胞免疫分型与 FAB分型的某些类型有一定相关性。
陈毅晟(云南省维西县疾病预防控制中心 6746000)【中图分类号】R733.7【文献标识码】A【文章编号】1672-5085(2013)07-0144-02【摘要】目的探讨血液肿瘤细胞免疫表型检测在白血病诊断及分型中的价值。
方法应用ABC-AP免疫组化二步法检测60例血液肿瘤白血病细胞14种抗原标记,结合临床、骨髓细胞形态学及细胞化学染色对血液肿瘤白血病进行诊断及分型。
结果58例初发血液肿瘤白血病患者中,急性髓细胞白血病(AML)27例(45.0%),急性B淋巴细胞白血病(B-ALL)18例(30.0%),急性T淋巴细胞白血病(T-ALL)5例(8.3%),慢性淋巴细胞白血病(CLL)6例(10.0%),慢性髓细胞白血病(CML)2例(3.3%),慢粒急淋变(CML-ALL变)2例(3.3%)。
结论血液肿瘤细胞免疫表型检测白血病细胞抗原,为白血病的诊断及分型提供了重要依据。
【关键词】白血病骨髓检查骨髓涂片免疫组织化学诊断血液细胞形态学检查是白血病诊断非常重要的手段,但有其局限性。
血液肿瘤白血病细胞免疫分型是利用单克隆抗体检测白血病细胞的细胞膜或细胞浆抗原,分析其细胞免疫表型,以了解被测白血病细胞所属细胞系列及其分化程度。
我们对60例住院及门诊白血病患者应用免疫组化二步法检测白血病细胞抗原,并对白血病再进一步进行诊断及免疫表型分析。
1.材料与方法1.1研究对象:选择住院及门诊白血病患者60例(初发患者58例)。
其中,男40例,女20例,年龄5-80岁,平均年龄43.3岁(14岁以下儿童4例)。
1.2试剂:白血病免疫分型检测试剂盒选自进口分装单克隆抗体。
T细胞系列:CD3、CD5、CD7;B细胞系列:CD10、CD19、CD20;髓细胞系列:CD13、CD14、CD33、CD68、MPO、CD41、非系列特异性:CD34、HLA-DR。
WHO软组织肿瘤免疫表型大全
2013版WHO软组织肿瘤免疫表型大全2014-11-06艾迪康病理诊断主要根据2013年“WHO肿瘤分类——软组织和骨肿瘤”翻译而来第1章脂肪细胞肿瘤(adipocytictumours)良性1、脂肪瘤(lipoma)免疫表型:成熟脂肪细胞表达S-100、leptin和HMGA2阳性。
2、脂肪瘤病(lipomatosis)免疫表型:和正常脂肪相似。
3、神经脂肪瘤病(lipomatosisof nerve)免疫表型:因为病变的所有成分均存在于正常神经内,故免疫组化对诊断没有帮助。
4、脂肪母细胞瘤(lipoblastoma)/脂肪母细胞瘤病(lipoblastomatosis)免疫表型:脂肪细胞表达S-100和CD34,原始间叶细胞常表达desmin。
5、血管脂肪瘤(angiolipoma)免疫表型:血管内皮成分CD31等内皮标记阳性,细胞性血管脂肪瘤增生的梭形细胞CD31阳性,证明为血管内皮。
6、软组织平滑肌脂肪瘤(myolipomaof soft tissue)免疫表型:梭形细胞SMA和desmin染色弥漫强阳性,证明为平滑肌分化;ER 和PR阳性也有报道;HMB-45阴性。
7、软骨样脂肪瘤(chondroidlipoma)免疫表型:成熟脂肪细胞S-100强阳性,脂肪母细胞S-100弱阳性,随脂肪细胞逐渐成熟S-100染色逐渐增强。
无脂肪母细胞分化特征的细胞S-100阴性。
少数病例角蛋白阳性,但EMA一致阴性。
8、梭形细胞脂肪瘤/多形性脂肪瘤(spindlecell lipoma/pleomorphic lipoma)免疫表型:梭形细胞脂肪瘤和多形性脂肪瘤中的梭形细胞均为CD34强阳性,S-100罕见阳性,偶见desmin阳性。
9、冬眠瘤(hibernoma)免疫表型:冬眠瘤细胞通常表达S-100阳性。
除梭形细胞亚型中梭形细胞成分CD34阳性外,其他冬眠瘤亚型CD34均阴性。
新的冬眠瘤标记物还包括UCP1。
临床血液学检验:11血液病MICM检验

形态M
病理及免疫组织化学的优缺点
• 标本直接固定,不容易损失信息,恶性细胞比例更客观,对一 些抽不出或少见细胞,仍可诊断。如伴骨髓纤维化、MM、淋巴瘤、 转移癌、组织细胞、巨噬细胞、树突细胞、何杰金细胞等 • 可以直接观察到组织结构,容易确定恶性细胞的组织部位 • 诊断慢、受诊断者个人经验及知识水平影响大 • 对一些组织结构无破坏、细胞形态改变不大的细胞,难以鉴定良 恶性及成熟度 • 有些恶性细胞在液体中,难以获取组织标本,难以判断组织结构
MICM分型原则中各检测技术简介
形态M 细胞形态及细胞化学分析的优缺点
优点:
直观:镜下直接观察细胞形态,对MDS的诊断、一 些少见的、大的恶性细胞的确定优于流式细胞分析恶 性细胞的比例更准确:
简单快速,有显微镜即可完成报告
缺点: 人为因素影响大 难以鉴别细胞的成熟阶段,B、T等系列的恶性细胞 细胞较成熟时,难以鉴别良恶性 不能提供太多的预后信息
伴再现性遗传学异常的AML
AML with t(8;21)(q22;q22) AML with inv(16)(p13.1q22) or t(16;16) APL with t(15;17)(q22;q12) AML with t(9;11)(p22;q23) AML with t(6;9)(p23;q34) AML with inv(3)(q21q26.2) or t(3;3) AML -M7 with t(1;22)(p13;q13) ? AML with mutated NPM1 ? AML with mutated CEBPA
ቤተ መጻሕፍቲ ባይዱ
MICM分 型
2016
FAB分型及WHO分类
1827年, 法国的Alfred Velpeau 描述第一例白血病 1847 年,Virchow首次提出了“白血病”这个名称 1976年,法、美、英3国7位血液学家以光镜下的形态为主,
急性髓系白血病112例流式细胞术检测免疫表型研究

急性髓系白血病112例流式细胞术检测免疫表型研究作者:董进梅张峰罗娇来源:《中外医疗》 2013年第13期董进梅张峰罗娇云南省普洱市人民医院血液科,云南普洱 665000[摘要] 目的探讨流式细胞术检测在急性髓系白血病诊断中的意义。
方法回顾分析在该院就诊初治的急性髓系白血病患者(AML)112例,采用流式细胞术CD/SSC双参数散点图设门的方法对患者骨髓细胞进行12种抗原监测,并结合FAB法则对其进行标准分类,并对不同亚型中抗原表达的差异性进行有效比较。
结果在112例初治的急性髓系白血病患者中,表达指数最高的是CD、CD、CD,分别为100%、94.5%、77.9%。
而在淋系抗原中,CD的表达指数最高为30.5%,其次为的CDl9、、26.9%、CD的16.7%。
而且有些免疫表型与FAB法则分类具有一定的相关性。
结论在急性髓系白血病诊断中运用流式细胞术检测有助于急性髓系白血病患者诊断和分型的准确性,对于急性髓系白血病患者选择治疗方案以及预后的判断具有重要意义。
[关键词] 急性髓系;白血病;流式细胞术;免疫表型[中图分类号] R733[文献标识码] A[文章编号] 1674-0742(2013)05(a)-0174-02急性髓系白血病包括所有非淋巴细胞来源的急性白血病,是一种具有高度异质性特性的疾病群,可由正常的髓系细胞分化发育过程中不同阶段的造血祖细胞恶性变转化而来[1]。
其发病原因及发病机制相对复杂,目前世界临床医学界普遍认为,大多白血病引发因素是由于环境因素与细胞遗传物质相互作用造成的。
由于AML患者本身白细胞质量差,自身抵抗力底下,患者被感染几率高,治疗困难且并发症多。
而且常伴有皮肤黏膜出血最常见为眼底、球结膜的出血现象。
流式细胞术(Flow Cytometry,FCM)是一种在功能水平上对液流中单列的细胞或者是其它微生物粒子快速逐一的进行筛选以及定量分析的检测手段[2],同传统的荧光镜检查相比,其具有高速、精准、多用途等优点,在基础研究和临床实践被广泛的运用,且在细胞生物学、血液学、免疫学、遗传学及临床检验等各领域各学科中也发挥着重要的作用。
血液系统肿瘤分类

血液系统肿瘤分类1. 引言血液系统肿瘤是指发生在血液系统中的恶性肿瘤,包括白血病、淋巴瘤和骨髓瘤等。
这些肿瘤的发生与血液系统中的细胞异常增殖和分化失控有关。
了解血液系统肿瘤的分类对于诊断、治疗和预后评估具有重要意义。
2. 白血病分类白血病是一种由白血病细胞在骨髓和外周血中异常增殖导致的恶性肿瘤。
根据病变细胞的类型和临床特征,白血病可分为急性白血病和慢性白血病两大类。
2.1 急性白血病急性白血病是一种由幼稚的、未成熟的白血病细胞异常增殖导致的恶性肿瘤。
根据细胞起源和临床特征,急性白血病可分为急性淋巴细胞性白血病(ALL)和急性髓系白血病(AML)两类。
2.1.1 急性淋巴细胞性白血病(ALL)急性淋巴细胞性白血病是一种由幼稚的淋巴细胞异常增殖导致的恶性肿瘤。
根据细胞表面标记物的表达和临床特征,ALL可进一步分为B细胞型和T细胞型。
•B细胞型ALL:约占所有ALL的80%,表现为骨髓和外周血中异常增殖的B 淋巴母细胞。
•T细胞型ALL:约占所有ALL的20%,表现为骨髓和外周血中异常增殖的T 淋巴母细胞。
2.1.2 急性髓系白血病(AML)急性髓系白血病是一种由幼稚的髓系细胞异常增殖导致的恶性肿瘤。
根据髓系细胞的分化程度和临床特征,AML可进一步分为多种亚型。
•M0型:未分化髓系细胞型。
•M1型:幼稚髓系细胞型。
•M2型:幼稚髓系细胞型,包括急性髓系白血病中最常见的亚型。
2.2 慢性白血病慢性白血病是一种由成熟的白血病细胞异常增殖导致的恶性肿瘤。
根据病变细胞的类型和临床特征,慢性白血病可分为慢性淋巴细胞性白血病(CLL)和慢性髓系白血病(CML)两类。
2.2.1 慢性淋巴细胞性白血病(CLL)慢性淋巴细胞性白血病是一种由成熟的B淋巴细胞异常增殖导致的恶性肿瘤。
根据淋巴细胞表面标记物的表达和临床特征,CLL可进一步分为多种亚型。
•CLL/SLL:小淋巴细胞型淋巴瘤/慢性淋巴细胞性白血病。
•B细胞前体淋巴细胞白血病:表达B细胞前体抗原的CLL亚型。
血液肿瘤的最新分类这些你一定要懂!【医学养生常识】

血液肿瘤的最新分类这些你一定要懂!
文章导读
WHO的血液系统肿瘤分类主要依据细胞系来源确定肿瘤类型,包括四种类型:髓系肿瘤、
淋巴系肿瘤、组织细胞肿瘤和肥大细胞肿瘤。
髓系肿瘤
在FAB分类中髓系肿瘤包括3类:急性髓系白血病(AMLS)、骨髓增生异常综合征(MDSs)
及骨髓增殖性疾病(MPDs)。
新的WHO分类建议将髓系肿瘤分为4类:骨髓增殖性疾病(MPDs)、骨髓增生异常综合征(MDSs)、骨髓增生异常/骨髓增殖性疾病(MD/MPDs)、急性
髓系白血病(AMLS)。
各类髓系肿瘤,根据细胞形态学、免疫表型、遗传学特点和l临床特
点,又进一步被分类。
淋巴系肿瘤
1994年修订的欧美淋巴瘤分类(REAL分类),是根据形态学、免疫表型、遗传特征及临床
特点对疾病进行分类。
WHO在此基础上结合几年来运用REAL分类的经验,略作修改,
制定了新的WHO淋巴系肿瘤的分类。
修订包括一些命名的改变,变异型、亚群的分类,
假定型的确定等。
分类主要将淋巴系肿瘤分为:T/NK细胞肿瘤、B细胞肿瘤及霍奇金病。
白血病免疫分型的基础

白血病免疫分型的基础白血病是一类以恶性克隆性造血干细胞增殖为特征的血液系统恶性肿瘤。
根据白血病患者免疫系统的表现和特征,可以将白血病分为多种免疫分型。
免疫分型对于指导白血病的治疗和预后评估具有重要意义。
白血病的免疫分型主要基于白血病细胞表面标志物的检测结果,通过免疫学方法对白血病细胞进行分类。
根据不同的免疫分型,可以更好地了解白血病的发展过程和预后情况,为临床治疗提供指导。
一、急性淋巴细胞白血病(ALL)的免疫分型急性淋巴细胞白血病是一种起源于淋巴细胞前体的恶性肿瘤。
根据ALL细胞表面的免疫表型,可以将ALL分为常见型、T-ALL、B-ALL 和非T非B淋巴细胞白血病。
1. 常见型ALL:常见型ALL细胞表面表达CD10、CD19、CD20等B 细胞标志物,具有较好的预后。
2. T-ALL:T-ALL细胞表面表达CD2、CD3、CD4、CD5等T细胞标志物,预后较差,易发生中枢神经系统浸润。
3. B-ALL:B-ALL细胞表面表达CD19、CD20等B细胞标志物,预后因不同的表型差异而有所不同。
4. 非T非B淋巴细胞白血病:非T非B淋巴细胞白血病细胞表面不表达典型的T细胞或B细胞标志物,预后较差。
二、慢性淋巴细胞白血病(CLL)的免疫分型慢性淋巴细胞白血病是一种起源于成熟淋巴细胞的恶性肿瘤。
根据CLL细胞表面的免疫表型,可以将CLL分为ZAP-70阳性型和ZAP-70阴性型。
1. ZAP-70阳性型:ZAP-70阳性型CLL预后较差,易发生淋巴结肿大和外周血细胞减少。
2. ZAP-70阴性型:ZAP-70阴性型CLL预后相对较好,疾病进展较慢。
三、急性髓系白血病(AML)的免疫分型急性髓系白血病是一种起源于骨髓干细胞的恶性肿瘤。
根据AML细胞表面的免疫表型,可以将AML分为M0-M7七个亚型。
1. M0亚型:M0亚型AML细胞表面不表达常见的髓系标志物,预后差。
2. M1亚型:M1亚型AML细胞表面表达CD13、CD33等髓系标志物,预后相对较好。
血液循环和CTC表型
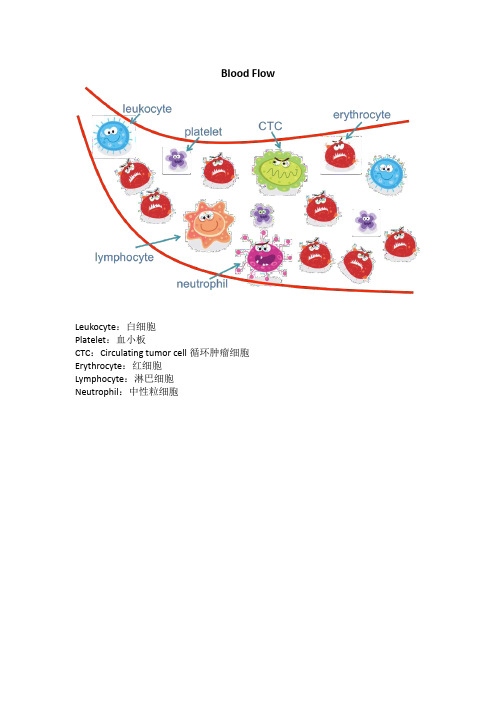
Blood Flow
Leukocyte:白细胞
Platelet:血小板
CTC:Circulating tumor cell循环肿瘤细胞Erythrocyte:红细胞
Lymphocyte:淋巴细胞
Neutrophil:中性粒细胞
CTC phenotype
Chemoresistance:化学抗性
Organ colonization:器官移植
Target organ:靶器官
Extravasation:外渗
Invasion:侵入
EMT:epithelial- mesenchymal transition上皮细胞-间充质转化
Migration:迁移
Intravasation:内渗
Apoptosis:细胞凋亡
Evasion:逃避(如果是指肿瘤细胞逃避免疫,我们一般译为:肿瘤的免疫逃逸)Evasion of apoptosis: 细胞凋亡的免疫逃逸(肿瘤细胞的特点)
Differentiated cancer cell:分化的癌细胞(如果是与分化不良的细胞对应,我们会译为分化的细胞,相对恶性程度会小一些)
EMT transitioned cell:上皮细胞-间充质转化细胞
CTC:Circulating tumor cell循环肿瘤细胞
Immune cells:免疫细胞
Red blood cell:红细胞。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CD20 dim
注意事项
B-PLL
HLA-DR CD19 CD20 CD5(-) CD22 CD23(-) CD10(-) clonal SIg 强阳性 CD20 bright
MCL(Mantle)
HLA-DR CD19 CD20 CD5 CD22 CD23(-) CD10(-)
SIg Bright,Cyclin D1过度表达
T-ALL
cCD3 CD5 CD7 CD1 CD2 dualCD4/CD8 CD10+/- CD34-/+
注意事项 一般不表达淋巴细胞标记 还表达CD15 CD19+ t(8;21)预后好
CD2(+) 考虑M4Eo 成熟的细胞表达glycophorin
注意事项
t(1;19) -CD34(-)预后差 L3 丢失T细胞抗原的情况比较常见
FCC(Follicular) HLA-DR CD19 CD20 CD5(-) CD22 CD23+/- CD10
CD(-)少于20%
HCL(Hairy)
HLA-DR CD19 CD20 CD5(-) CD22 CD23(-) CD10(-) CD11c CD25 CD103 sIgD common,CD22和CD11c表达非常强
淋巴造血系统肿瘤的免疫表型
急性髓细胞白血病
急性淋巴细胞白血病
分类 M0 M1 M2 M3 M4/M5 M6 M7
常见表型 HLA-DR CD13 CD33 CD34 CD7 cMPO 与M0相同 HLA-DR CD13 CD33 more CD15 less CD34 HLA-DR(-) CD13 CD15 CD33 CD34-/+ HLA-DR CD14 CD15 CD33 CD4weak HLA-DR CD13-/+ CD33+/- CD34 CD45 HLA-DR -/+ CD33+/- CD34 CD41 CD61
注意事项 CD4/CD8双阳性少见,但比B-PLL恶性程度高 有TCR基因的重排,如果同时表达CD3和CD56 恶性程度较高 临床常见血红蛋白减少,BPC下降和肝脾肿大
克隆性TCR基因重排
分类 CLL
常见表型 HLA-DR CD19 CD20 CD5 CD22(-) CD23 CD10(-) clonal SIgM
分类
常见表型
B precursor
HLA-DR CD19 CD20-/+ CD10+/- CD34 TdT SIg(-)
Pre-B
HLA-DR CD19 CD20+/- CD10 CD34(-) cIgM(+) TdT+/-
B-ALL
HLA-DR CD19 CD20 CD22 CD24 CD10+/- CD34(-) Sig
分类 T-PLL T-LGL NK-LGCD5 CD7 CD4 CD8(-) CD2 CD3 CD5(-) CD7(-) CD4 CD8dim CD16 CD57 CD56(-) CD2 CD16 CD 56 CD57(-) CD3(-) CD2 CD3 CD5 CD7(-) CD4 CD8(-) HLA-DR强阳性 CD25 CD2 CD3 CD5 CD7 CD4(-) CD8(-)
Plasma Cell Dyscrasias HLA-DR(-) CD19(-) CD20(-) CD22(-) CD38 CD45 clonal cIg
CD38强阳性,CD45dim
T淋巴细胞增殖性疾病 (T-LPD)
B淋巴细胞增殖性疾病 (B-LPD)
