第二章烷基化反应
烃基化反应和烷基化反应

烃基化反应和烷基化反应烃基化反应和烷基化反应是有机化学中常用的反应类型,它们分别指的是在分子中引入烃基或烷基基团的化学反应。
烃基化反应是指在有机分子中引入烃基(或烯烃基)的化学反应。
这种反应可以通过直接的取代反应或通过碳-碳键断裂和重组来实现。
常见的烃基化反应包括Wurtz反应和Corey-House反应等。
Wurtz反应是一种重要的烃基化反应,它是通过反应两个卤代烃与金属钠或金属钾来实现的。
在反应中,卤代烃首先与金属钠或金属钾发生失去卤根离子(X-)的反应,生成自由基的烷基钠或烯烃基钠。
然后,两个烷基钠或烯烃基钠通过反应生成一个新的碳-碳键,产生所需的烃基化产物。
Wurtz反应在合成有机化合物和精细化工中得到了广泛的应用。
Corey-House反应是另一种重要的烃基化反应。
该反应是通过卤代烷与Grignard试剂反应来引入烃基。
在反应中,卤代烷通过和Grignard试剂反应失去卤根离子,生成烷基或烯烃基中间体。
然后,这些中间体再和电子亲和性较强的电子受体反应,形成烃基化产物。
Corey-House反应常用于精细化工和药物合成领域。
烷基化反应是指在有机分子中引入烷基基团的化学反应。
这种反应通常通过取代反应或通过碳-碳键断裂和重组来实现。
常见的烷基化反应包括自由基取代反应和卤代烃与卡宾反应等。
自由基取代反应是一类常用的烷基化反应。
在这种反应中,通常是通过光解或热解能够产生自由基的化合物来引发反应。
在自由基取代反应中,自由基首先与烷基化底物中的氢原子发生反应,形成碳-碳键和碳-碳键。
这种反应常用于合成药物、染料等有机化合物。
卤代烃与卡宾反应也是一种重要的烷基化反应。
在这种反应中,卤代烃与卡宾中间体反应,生成烷基化产物。
卡宾中间体是一类高度反应性的中间体,它是由碳-氧键断裂或碳-卤键断裂形成的。
卡宾中间体在反应中通常通过与醛、酮等具有亲核性的化合物反应,形成烷基化产物。
卡宾反应在合成有机化合物中具有重要的应用和研究价值。
羰基化合物的α-烷基化和催化烷基化反应
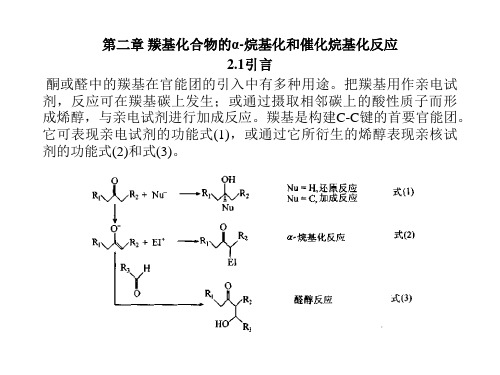
2.4 配位型的环内手性传递 配位型的手性烯醇体系,金属离子在固定原有的手性和烯醇部分之 间的立体化学关系至关重要。 2.4.1β-羟基酸 在烯醇化过程中这些底物可以形成E烯醇或者Z烯醇,对这两种烯醇 体系的任何一种而言,配位作用在确定烯醇对映面的选择中都可能 是决定性的。如图2.12所示,由于Re面进攻Z-或E-烯酵,结果都形 成了主要的组分。
从一些易得的环氧基硅烷基醚开始,合成α,α—二取代α—氨基酸衍 生物:
具有张力的氨基醇衍生的酮酯或酰胺与格氏试剂反应,制备对映体 纯叔-α -羟基酸 :
2.6 双内酰亚胺体系 甘氨酸和其它氨基酸经过二酮哌嗪,进行O—甲基化得到六元杂环产 物,水解以后以高对映体过量获得了α-甲基氨基酸。
2.7 用于羰基化合物的α-烷基化的手性辅剂一览表
三乙基铝化合物可从氢化铝和乙烯很经济地以工业规模制备,因此 这类化合物成功的烷基化反应肯定会开辟一个活跃的新研究领域。
一些新配体:
2.10 ZnR2对酮的催化不对称加成: 叔醇不对称中心的对映选择性形成 许多生物活性的天然产物含有季碳原子,通过碳亲核试剂对酮的加 成来不对称合成叔醇近来越来越受到关注(也参见2.5节)。 DAIB(142)催化二苯基锌对酮的对映选择性加成:
樟脑磺酰胺-钛醇盐衍生物催化二甲基锌和二乙基锌对潜手性酮的对 映选择性加成:
2.11 不对称氰醇化反应 光学活性的磺肟145和Ti(OPri)4生成手性钛试剂催化三甲基甲硅烷基 氰化物对醛的不对称加成。
假定的反应机理:
139(X=CN)催化三甲基甲硅烷基氰化物与醛的反应。手性的二氰 基络合物在原位生成,不对称氰硅烷化给出的e.e.值达到75%。
在同环桥键羟基氨基二茂铁(—)—130存在下,11种芳族和脂族醛与 Et2Zn进行烷基化反应。生成的醇具有67%一97%的e.e.值。这种 二茂铁催化剂成功地用于使芳族醛和直链或支链脂族醛的烷基化, 产生的仲醇e.e.值高达97%。即使用β—支链的脂族醛,得到的光 学产率也比用131所报道的要高。
烷基化反应的简介PPT课件

★ 2.烷基化试剂 ★ 3.催化剂
★ 4. 芳环上C-烷化反应特点 5.C-烷基化方法
第4页/共35页
★ 1.C-烷基化反应历程
催化剂路易大多是斯酸、质子酸或酸性氧化物,催化剂的作用是使烷
基化剂转变成活泼的亲电质点 —— 碳正离子。烷基正离子进攻芳环发生亲
电取代反应。
H3C CH2 Cl
非离子表面活性剂
CH2CH2CN N CH2CH2CN
第22页/共35页
★ 2.N-烷化反应类型
(3)缩合——还原型: 所用N-烷化剂为醛和酮类。
O
R C H + H NH2
OH - H-OH
R CH NH2
〔H〕
R CH NH
R CH2 NH2
O
R C R` + H NH2
烷基化反应是指向有机化合物分子中的碳、氮,氧等原子上引入烃基增 长碳链(包括烷基、烯基、炔基、芳基等)的反应,其中以引入烷基最为重 要。 3.可发生烷基化反应的有机物:芳烃、活泼亚甲基化合物、胺类等。 4.烷基化试剂种类:醇、烯烃、硫酸二甲酯、卤代烷、环氧化物、醛、酮等。
第1页/共35页
二、烷基化反应的类型
一、烷基化反应的简介
1.研究作用: 可以合成塑料、医药、溶剂、合成洗涤剂、药物、染料、香料、催化剂、
表面活性剂等功能性产品。如通过C—烷基化反应可制得阴离子表面活性剂; 通过O-烷基化可制得聚乙二醇型非离子表面活性剂;通过N-烷基化合成
的季铵盐是重要的阳离子表面活性剂、相转移催化剂、杀菌剂等。 2.定义:
是有大量铝盐废液生成,有时由于副反应而不适于活泼芳烃(如:酚、 胺类)的烷基化反应。 (2)质子酸
大学有机化学反应方程式总结胺的烷基化与亚胺化反应

大学有机化学反应方程式总结胺的烷基化与亚胺化反应胺(amine)是含有氮原子的有机化合物,可分为一级胺、二级胺、三级胺等不同类型。
在有机化学中,烷基化和亚胺化是两种常见的反应类型。
本文将对胺的烷基化和亚胺化反应进行总结。
一、烷基化反应烷基化是指将烷基基团引入到胺分子中,形成相应的烷基胺化合物。
1. 一级胺的烷基化反应一级胺(R-NH2)的烷基化反应一般使用烃基卤代烷(R’-X)作为烷化试剂,常见的反应类型有SN2和亲电取代两种。
(1)SN2机理在碱性条件下,亲电取代反应被基质上的氢氧根离子(OH-)或醇根离子(RO-)催化。
反应机理如下:R-NH2 + R’-X → R-NH-R’ + X-其中,R代表烃基,X代表卤素。
(2)亲电取代机理在酸性条件下,亲电取代反应被一个亲电试剂催化,如硫酸酯(RO-SO3H)或酰氯(RCOCl)等。
反应机理如下:R-NH2 + R’-X → R-NH-R’ + HX二级胺(R-NHR’)的烷基化反应与一级胺类似,也可以使用烃基卤代烷作为烷化试剂。
反应机理如下:R-NHR’ + R’’-X → R-NHRR’’ + X-其中,R、R’、R’’代表烃基,X代表卤素。
3. 三级胺的烷基化反应三级胺(R-NR’R’’)的烷基化反应一般使用烃基卤代烷作为烷化试剂,反应机理与一、二级胺相似。
二、亚胺化反应亚胺(imine)是胺与醛或酮反应生成的化合物。
通常亚胺化反应会生成亚胺和水。
1. 一级胺的亚胺化反应一级胺(R-NH2)的亚胺化反应一般与酮(R’’-C(=O)-R’’)或醛(R’’-C(=O)-H)反应,反应机理如下:R-NH2 + R’’-C(=O)-R’’ → R-N=C(R’’)-R’’ + H2O其中,R代表烃基,R’’代表有机基团。
2. 二级胺的亚胺化反应二级胺(R-NHR’)的亚胺化反应与一级胺类似,也可以与酮或醛反应生成亚胺和水。
三级胺(R-NR’R’’)的亚胺化反应一般与酮或醛反应生成亚胺和水。
烷基化反应

D、只有乙烯作烷基化剂时,生成乙苯,碳原子数3以上的烯 烃,生成支链芳烃(如异丙苯的制备)。
+CH3 CH CH2 AlCl3
CH3 CH 70% CH3
CH2CH2CH3 30 %
(2)质子酸:硫酸、氢氟酸和磷酸。
5位
CH3CHCH2CH2CHCHCH2CH2CH2CH2CH2CH3
6位 2位
利用丙烯烷基化-酸解技术生产2-萘酚和丙酮,此技术 比过去磺化、碱熔制2-萘酚更先进。
H2SO4 65 O C
SO3H 160OC
SO3H NaO H
O Na
AlCl3 80O C
CH(CH3)2 (1) oxidation
CH3 C CH3 CH3
(3)低温、低活性催化剂利于形成邻对位异构体;高活性催 化剂如三氯化铝、高温利于形成间位异构体;使用BF3、氯化 锌等更温和的催化剂,利于克服间位异构体的生成。
(4)碳烷基化反应可能发生重排。因此,用伯卤代烷、伯
醇、端烯作烷基化剂时,常发生重排,形成混合物。
+CH3 CH CH2 AlCl3
卤代烃的烷基化反应
(1)烷基相同时,不同的卤素形成的卤代烷烃的反应活性 顺序为RI >RBr>RCl 。
(2)卤代烷烃中卤素相同时,不同的烷基则反应活性顺序 为:
CH2X > R3CX > R2CHX > RCH2X> CH3X
(3)不能用卤代芳烃如氯苯、溴苯代替卤代烷进行烷基化 反应,因为连接在芳环上的卤素反应活性较低,不能进行 烷基化反应。
烷基化反应在精细有机合成中的应用
O
CNH2
烷基化反应

CH2
+ HCl
六、用醇对芳环的C-烷基化
• 醇类是反应能力较弱的烷基化剂,它 们只适用于活泼芳族化合物(例如苯胺、 苯酚和萘等)的C-烷基化。 • 常用的烷基化催化剂有路易斯酸和质子 酸等。 • 1.用醇对芳胺的C-烷基化
NH2
C4H9OH H2O ZnCl2催化 210℃, 0.8MPa
NHC4H9
CH3 C O + 2 OH CH3 CH3
H 催化 脱水缩合
HO
C CH3
OH + H2O
(双酚A)
8.3 N-烷基化
• 定义:氨、脂肪族或芳香族胺类氨基上的氢原 子被烷基取代,或者通过直接加成而在氮原子 上引入烷基的反应叫N-烷基化反应。 • 这是制取各种脂肪族和芳香族伯、仲、叔胺的 主要方法,其反应通式如下:
OH OH (CH3)2CHOH +
磷酸催化 二甲苯溶剂回流
OH OH + H2O C(CH3)3
七、用醛类对芳环的C-烷基化
• 1、醛对酚类的C-烷基化 • 甲醛与过量苯酚在无机酸催化作用下反应, 可制得4,4'-二羟基二苯甲烷(双酚F):
H C H O+ OH
H
H HO C H OH + H2O
4、用醛或酮的N-烷基化
• 氨或胺类化合物和许多醛或酮可发生还 原性烷基化,即伴随有还原反应的烷基 化反应,其化学反应通式如下:
H R C O H + NH3
H2O
R C NH
亚胺
还原剂
RCH2NH2
伯胺
R R
/
R C O + NH3
H2O
R
/
C
亚胺
(精品课件)烷基化反应

4 烷基化反应定义:一般而言,有机分子中的氢原子(包括某些官能团上的,如羟基和氨基等)被烷基取代,可称为烷基化反应。
意义:在药物分子中引入烷基可增加其脂溶性,或形成新的官能团赋予药物以特殊性能。
如丁卡因药效为普鲁卡因的10倍。
本章内容:醇、酚的氧烷化,胺的氮烷化,活泼亚甲基及芳烃的碳烷化等反应。
4.1 氧原子上的烷基化反应在氧原子上烷基化是获得醚,尤其是不对称醚的通用方法。
4.1.1 以卤代烃为烷基化试剂醇、酚的钠盐或醇、酚在碱(钠、氢氧化钠以及氢氧化钾等)的存在下与卤代烷生成醚的反应称为Williamson反应,是合成不对称醚的最常用方法。
(1) 反应机理Williamson反应是典型的SN2反应。
此外,醇、酚与卤代烷的反应也可按SN1机理进行。
(2) 影响因素底物的影响:①伯卤代烷一般为SN2机理;叔卤代烷一般为SN1机理;而仲卤代烷可SN1也可SN2。
②由于芳环的吸电子作用,使得酚的活性一般弱于醇。
③底物的空间位阻对反应速率影响较大。
溶剂的影响:极性溶剂可促进反应。
SN2反应一般在碱性条件下进行;而SN1反应一般在酸性或近中性(可为弱碱性)条件下进行。
(3) 反应示例①苯海拉明的合成反应机理:双分子亲核取代(SN2)。
②糖环6-伯羟基的保护在极性溶剂中,Ph3CCl可形成非常稳定的碳正离子Ph3C+,此步为控制步骤,该碳正离子形成后迅速与伯羟基结合,生成醚。
反应机理:碳正离子历程(SN1)。
③卤代烃为芳卤的情况:对硝基苯乙醚(非那西丁中间体)的合成反应机理:加成-消除机理。
反应活性:I<Br<Cl<F;芳环上一定要有吸电子基。
4.1.2 以芳磺酸酯为烷基化试剂氧原子的吸电子作用使得芳磺酸酯成为很好的离去基团,当与其相连的碳原子受到醇的进攻时,芳磺酸基很容易离去。
常见的芳磺酸酯包括苯磺酸酯、对甲苯磺酸酯、对硝基苯磺酸酯、对卤苯磺酸酯以及对三氟甲基苯磺酸酯等。
反应示例:鲨肝醇的合成(SN2反应)。
烷基化反应的简介

07
烷基化反应研究前沿与挑战
研究现状概述
烷基化反应类型
目前已知的烷基化反应主要包括 Friedel-Crafts 烷基化、烯烃的烷 基化、芳烃的烷基化等,每种类 型都有其特定的反应条件和机理 。
催化剂研究
催化剂在烷基化反应中起着至关 重要的作用,目前研究主要集中 在寻找高效、环保的催化剂,如 固体酸催化剂、离子液体催化剂 等。
02 03
烯烃烷基化反应数据处理
通过测定反应前后烯烃和卤代烃的含量变化来计算反应的 转化率和选择性;通过气相色谱等手段对产物进行分离和 定量分析。
羧酸烷基化反应数据处理
通过测定反应前后羧酸和卤代烃的含量变化来计算反应的 转化率和选择性;通过红外光谱、核磁共振等手段对产物 进行结构鉴定。同时,还可以通过对比实验数据,优化反 应条件,提高反应的效率和产物的纯度。
05
烷基化反应在有机合成中的应用
药物合成中的应用
1 2 3
合成药物活性成分
通过烷基化反应,可以合成具有特定药理活性的 药物分子,如抗癌药物、抗病毒药物等。
改善药物性质
烷基化反应可用于改善药物的溶解性、稳定性以 及生物利用度等性质,从而提高药物的疗效和安 全性。
药物代谢研究
烷基化反应在药物代谢研究中也有重要应用,可 以通过模拟体内代谢过程,研究药物在体内的转 化和代谢途径。
天然产物合成中的应用
合成复杂天然产物
通过烷基化反应,可以合成具有复杂结构的天然产物,如萜类、 生物碱等,这些天然产物往往具有重要的生物活性。
天然产物结构修饰
烷基化反应可用于对天然产物的结构进行修饰,从而改变其生物活 性和药理作用,为药物设计和开发提供新的思路。
合成天然产物类似物
烃化_精品文档

O +
CH2Br
DMF OCH2Ph
CF3CH2OH CH2Ph OH
2.1.3醇、酚羟基的保护
在有醇、酚羟基的化合物中,同时存在其他的官 能团,这些官能团发生转换、氧化或还原反应 时,为了不使羟基发生变化,可先将羟基与某些 试剂反应,生成稳定的衍生物,待其他的官能团 转化完成后,再脱除保护基,恢复羟基。
叔卤代烃在强碱中优先发生消除反应,而不 是O-烃化反应。
CH3
CH3O C CH3 的合成
CH3
(1)CH3ONa
+ Cl
CH3 C CH3 CH3
消除 -HCl
CH3
碱
(2)CH3Cl + HO C CH3
CH3
CH3 CH3 C CH2
稳定
CH3O
CH3 C CH3 CH3
在中性或弱碱性条件下,叔卤代烃也可以进 行单分子的亲核取代反应(SN1),也可得 到O-烃化产物。
ROH RCl / R2SO4
• 混合醚:
ROR
ROH + R'Cl
ROR'
• 醇进行O-烃化反应的烃化剂有:
卤代烃RX
硫酸酯(芳磺酸酯)R2SO4、R 环氧烷,如:环氧乙烷
SO3R'
其他的烃化剂
卤代烃RX为烃化剂:
醇在碱(钠、氢氧化钠、氢氧化钾)存在下与 卤代烃RX反应制备混醚,称为威廉森法 (Williamson)。
NO2 非那西丁的中间体
叔卤代烃在强碱中优先发生消除反应,而不是 O-烃化反应。
在中性或弱碱性条件下,叔卤代烃也可以进行 单分子的亲核取代反应(SN1),也可得到O-烃 化产物。
• (2) 醇的影响
chap2 中间体及重要的单元反应

(2)磺化试剂和主要磺化法 磺化方法: a.直接磺化:磺酸基取代碳原子上的氢(为主要的)。 b.间接磺化:磺酸基取代碳原子上的卤素和硝基。 常用的磺化试剂: 浓硫酸,发烟硫酸,三氧化硫和氯磺酸。
苯环的磺化:
CH3
H2SO4
CH3
SO3 H
CH3
+
SO3H
NO2
H 2SO4 SO3
.
NO 2
SO3H
O C [O] O C O
(2)有机分子失去部分氢的反应
O 2N CH3 [O] O 2N CH CH NO 2
SO 3H
SO 3H
SO 3H
Fe HC I
H2N
CH
CH
NH2
SO 3H
SO 3H D. S. D 酸
1.10 成环缩合反应
(1)生成新的碳环
O C O C O AlCl3 C O R O OH C R H2SO4 . SO3 C R O
a.氨基是供电子基,在染料分子的共轭系统中引入氨基,染 料颜色加深。 b.与纤维上的羟基、氨基、睛基等极性基团形成氢键,可提 高染料的亲和力(或称直接性)。
c.通过芳伯胺重氮化、偶合,可合成一系列偶氮染料。
d.通过氨基可以引入其它基团。 e.生成杂环化合物。
(2)引入氨基的反应:硝基还原、氨解反应
(1)烷基化和芳基化的目的:
a.在染料分子中引入烷基和芳基后,可改善染料的坚牢度和溶解性能。 b.在芳胺的氨基和酚羟基上引入烷基和芳基,可改变染料的颜色和色光。 c.可克服某些含氨基、酚羟基染料遇酸、碱变a.芳烃的烷基化——常用卤烷和烯烃; b.氨基的烷基化或芳基化——醇、酚、环氧乙烷、卤烷、硫酸酯和烯烃 衍生物。 c.酚类的烷氧基和芳氧基化——卤烷、醇和硫酸酯。
烷基化

R C N CH2R
亚胺
还原剂
(RCH2)2NH
仲胺
作业
• 1.何谓烷基化?芳环上的C-烷基化有什 么特点? • 2.试举例说明N-烷基化合成的精细化学 品。
NH3 + R Z RNH2
/ /
RNH2 + HZ RNHR + HZ RNR2
/ /
+ R Z
RNHR + R Z
+ HZ
式中R-Z代表烷基化剂,包括醇、卤烷、酯等化合物。
• 1、用醇类的N-烷基化
• 醇的烷基化活性较弱,所以反应需在较强烈的 条件下才能进行。(相当于亲电取代反应历程) • 但某些低级醇(甲醇、乙醇)价廉易得,所以 工业上仍常选作活泼胺类的烷基化剂。 如
CH3
④
芳环上取代基的影晌
• 芳环上的C-烷基化是亲电取代反应。 • 当芳环上有提供电子的烷基时,使反应容 易进行。 • 当芳环上含有吸电基时,它使芳环钝化。 • 如果在芳环上同时有致活和致钝的取代基 时,则付氏反应常常可以顺利完成。 • 硝基苯不能发生 C- 烷基化反应,但它可以 作C-烷基化的溶剂。
OH OH (CH3)2CHOH +
磷酸催化 二甲苯溶剂回流
OH OH + H2O C(CH3)3
七、用醛类对芳环的C-烷基化
• 1、醛对酚类的C-烷基化 • 甲醛与过量苯酚在无机酸催化作用下反应, 可制得4,4'-二羟基二苯甲烷(双酚F):
H C H O+ OH
H
H HO C H OH + H2O
2、卤烷烷基化 3、醇烷基化 4、醛和酮烷基化
• 机理:芳烃上的C-烷基化反应都属于亲 电取代反应。
烷基化反应ppt课件

2.1.3 用醇作烷化剂的C-烷化反应
反应历程
质 子 化 + +
R O H + H
R O H 2
解 离 +
R + H O 2
实例
(1)芳胺的C-烷化
N H 2
+ C H O H ,H O 4 9 2 Z n C l 2 2 1 0 C ,0 . 8 M P a
o
N H C H 4 9
异 构 化 Z n C l 2 o 2 4 0 C ,2 . 2 M P a
A r H 慢 离 子 对 烷 基 正 离 子
• 回顾
在Lewis酸催化作用下,芳烃及其衍生物与烯 烃、卤烷、酰卤、酸酐等活性组分反应形成新的 C-C键的反应,叫做傅氏反应。 引入烷基的反应叫做傅氏烷基化反应; 引入酰基的反应叫做傅氏酰基化反应。
反应的影响因素 (1)烷基化试剂的活性
1 R 1 R
O
O
(5)烯烃和炔烃:CH2=CH2, CH3CH=CH2, R-CH=CH2, CH2=CHCN, CH2=CHCOOCH3, CH≡CH; (6)羰基化合物:HCHO, CH3CHO, C3H7CHO, Ph-CHO, CH3COCH3, O
2.1 C-烃化
有机化合物分子中碳原子上的氢被烃 基所取代的反应叫做C-烃化反应。 F-C烷基化反应: R R 烃化剂:烯烃; 卤烷; H O H N 2 R 醇、醛、酮。 反应历程:酸催化的亲电取代反应。
A l C l 3
C C l
二 氯 二 苯 甲 烷
+ 2 H C l
2.1.2 H = C H + H 2
C H C H 2 3
烷基化反应

烷基化反应有机化合物分子中连在碳、氧和氮上的氢原子被烷基所取代的反应。
碳原子上的烷基化①羰基的a碳上氢的烷基化。
羰基的a碳上的氢呈弱酸性,羰基的a碳原子在强碱(如氨基钠、氢化钠)的作用下,能与卤代烷发生烷基化反应,生成a碳烷基化产物:酮和酯的直接烷基化会发生自身缩合;也会发生多烷基化反应。
要获得a-碳单烷基化产物,可用四氢吡咯、吗啉等仲胺制成烯胺,再与活泼的卤代烷(碘甲烷、卤代苄等)反应,生成取代的烯胺,经水解即得烷基化的羰基化合物:②活泼亚甲基的烷基化。
处于两个活性基团之间的亚甲基比较活泼,在醇钠作用下容易烷基化。
活性基团可以是硝基、羰基、酯基或氰基等。
例如取代的丙二酸酯合成法和乙酰乙酸酯合成法:H2C(COOC2H5)2+C2H5O-Na+CH(COOC2H5)2-Na++C2H5OHCH(COOC2H5)2-Na+RXRCH(COOC2H5)2+NaXCH3COCH2COOC2H5+C2H5O-Na+(CH3COCHCOOC2H5)-Na++C2H5OH式中R为烷基;X为卤素。
取代的丙二酸酯、乙酰乙酸酯水解后容易脱羧、分解成取代乙酸或酮,此反应广泛用于有机合成。
这些烷基化反应都是在无水条件下进行的。
③相转移催化的烷基化。
利用相转移催化剂使处于两个互不相溶的液相系统中的反应物进行反应。
无需在无水条件下操作,可以用浓氢氧化钠水溶液代替无水醇钠。
反应条件温和,操作简便。
常用的催化剂有四级铵盐(Q+X-),如(n-C4H9)4N+HSO4-、四级磷盐[(C2H5)3P+CH2C6H5]Cl-或冠醚等。
反应物于界面处与碱作用,生成负碳离子。
后者与四级铵盐正离子形成离子对,转移到有机相中,与卤代烷进行烷基化反应。
例如:氧原子上的烷基化醇钠与卤代烷反应生成醚,这是合成不对称醚的重要方法:RONa+R′XROR′+NaX酚的酸性较醇强,采用氢氧化钠可生成芳香氧负离子,然后进行烷基化。
例如:硫酸二酯类也是常用的烷基化试剂,其活性比卤代烷高,反应条件温和,一般只有一个烷基参加反应。
烷基化反应机理

(CH3)3 C CH2
CH3 C CH3
(CH3)3 CH
CH3 (CH3)3 C CH2 CH CH3
(CH3)3 C
烷基化反应机理
一、链引发 在异丁烷与烯烃的烷基化反应过程中,烯烃得到氢质子H+形成正碳离子为链的
引发过程,如下图中所生成的叔丁基正碳离子对烷基化反应起着至关重要的作用。
CH3
(1)
烷基化反应原理
2020年3月16日
CONTENTS
目 录
1 正碳离子的概念 2 正碳离子的化学行为 3 烷基化链式反应机理 4 烷基化反应的产物分布解释
正碳离子的概念
在各种有机化学反应中,中间产物大体可以分为3种类型:自由基、阳离子、阴离子。 烷基化反应属于其中的阳离子反应,即生成了正碳离子。随着人们对烷基化反应机理不 断探索与认识的日渐成熟,普遍接收的是正碳离子——链式反应机理。 正碳离子是一个带正电荷的碳原子,它只有6个外层电子,是缺电荷的,其通式可以写为:
C8H18+C4H10→ C5H12 + C7H16
烷基化反应产物分布
原料烯烃 烷烯比
产物组成,% 2,3-二甲基丁烷 2-甲基戊烷 3-甲基戊烷 C6合计 2,2,3-三甲基丁烷 2,3-二甲基戊烷 2,4-二甲基戊烷 2-甲基己烷 3-甲基己烷 C7合计 2,2,4-三甲基戊烷 2,2,3-三甲基戊烷 2,3,4-三甲基戊烷 2,3,3-三甲基戊烷 2,3-二甲基己烷 2,4-二甲基己烷 2,5-二甲基己烷 3,4-二甲基己烷 C8合计 C9+
C
围绕正碳离子的取代物可以是氢原子,也可以是甲基基团,其四种形式分别为:
H
H
H
CH3
HC H
第二章 烃化反应-3碳原子上的烃化反应

12
3. 应用特点
(1)烃基的异构化:制备稳定的烷基芳烃 氯代正丙烷在AlCl3存在下,生成丙基正离子,该正离 子可转变成更稳定的异丙基碳正离子,然后进攻苯环
Withdrawing Group) ,如- NO2 、- SO3H 、- CN 、 和与环直接相连的羰基 (包括醛、酮、羧酸和酯)的 芳环底物、使芳环活性降低, Friedel-Crafts 烷化反 应不易发生。
8
随堂练习题
相同条件下,下列化合物进行傅-克(Friedel-Crafts) 烷基化反应的活性顺序是( )。
得定位:烷基芳烃的位置选择性 一般符合定位规律,高温下易得不正常的间位产物
15
(3) 氯甲基化反应(Blanc反应)(掌握) 在无水ZnCl2存在下,芳烃与甲醛及氯化氢作用, 芳环上的氢原子被氯甲基 (-CH2Cl)取代,称氯甲基化 反应 (chloromethylation reaction) (Blanc反应)。
36
③ 应用实例4-维拉帕米中间体的合成
维拉帕米,抗心律失常药,为一种钙离
子内流的抑制剂,在心脏,钙离子内流 受抑制使窦房结和房室结的自律性降低。
37
自学内容
2. 醛、酮、羧酸衍生物的α位C-烃化(自学) 3. 烯胺的C-烃化(自学) 4. 相转移催化反应(自学)
38
小结
芳烃的Friedel-Crafts烷基化反应(重点)
炔烃的C-烃化反应 格氏试剂的C-烃化反应
烃基化反应和烷基化反应

烃基化反应和烷基化反应
烃基化反应和烷基化反应是有机化学中常见的反应类型,用于在有机化合物中引入烃基或烷基基团。
这些反应是通过将一个氢原子替换为烃基或烷基基团来实现的。
烃基化反应是通过引入烃基基团到有机分子中的反应。
其中一种常见的烃基化反应是亲核烃基化反应,它基于亲核取代反应的机理。
在亲核烃基化反应中,一个亲核试剂攻击有机分子上的一个碳原子,替代其上的氢原子,并形成新的C-C键。
这样,有机分子的化学性质和功能都可以发生变化。
另一种常见的烷基化反应是烷基化反应,其中一个非活泼的烷基试剂作为亲电试剂,引入一个烷基基团到有机分子中。
在烷基化反应中,这个亲电试剂会与有机分子中的亲电中心发生反应,比如与一个烯烃中的双键发生加成反应,或与一个芳环中的芳烃发生芳烃取代反应,从而引入一个烷基基团。
这些反应具有广泛的应用,可以用于合成各种化合物,如药物、合成材料、农药等。
它们在有机合成中起着重要的作用,能够构建复杂的有机分子骨架,并引入不同的化学功能团。
烃基化反应和烷基化反应的研究和发展是有机化学领域的重点之一,不断推动着有机化学的进步和应用的拓展。
第二章_烷基化反应

R2NH R3N
R2NH +
跟卤代烃的反应是主要方法之一, 缺点:易得到混合胺
1.伯氨的常用制备方法
(1):氨水和卤代烃的反应
O OH Br 70% NH2 NH3(70mol) O OH
用大大过量的氨水,抑制进一步反应, 该方法在工业中应用广泛
NO2 Cl O2N NH3/AcONH4 170 oC, 6h O2N NO2 NH2
CCl4/AlCl3 10-30 oC,3 h Cl Cl O H2O 80ຫໍສະໝຸດ O OH 95% CH2CH2CN
冠状动脉扩张药派克西林中间体
O OH C6H6/AlCl3 25 C, 4 h
o
冠状动脉扩张药普尼拉明中间体
MeO MeO CN AlCl3 MeO MeO
镇痛药延胡索乙素中间体
1.反应机理 :C+ 离子对芳环的亲电进攻
差向异构
OH CH3 cis CH3I/NaH/THF 50℃, 1 h OCH3 CH3 cis (100%)
OH CH3 trans
CH3I/NaH/THF 50℃, 1 h
OCH3 CH3 trans (100%)
多卤代物的醚化
CHCl3 + 3 CH3ONa CH(OCH3)3
CCl4
+
多卤代烃,甲醛,环氧乙烷
二.格氏试剂的C-烷基化 格氏试剂
OMe
Case:
NHBoc OH
PhCH2Br
NHBoc O
H N O O
二、酚的O-烷基化
1.卤代烃为烃化剂
CONH2 OH EtBr/NaOH 80~100℃, 19.6 x 10exp4 Pa CONH2 OEt
烷基化反应

F-C 烷基化反应
全名叫福瑞德―克拉夫反应、就是苯环上发生的酰基化或烷基(乙、丙稀等)化 反应 。
在苯环上引入酰基或 者烷基,常用路易士酸或质子酸催化,最长用的无水三氯化铝(A1C13)催化剂,是苯环衍生化的 重要 反应。
烷基化反应∶1、把烃基引入有机化合物分子中的C、N、O(氢、氮等)原子上的反应称为烷基化反应,也可简
称烷化。
2、利用加成或置换反应将烷基引入有机物分子中的反应过程。
烷基化反应作为一种重要的合成手
段广泛应用的于许多化学工生产过程。
3、烷基—即饱和烃基、是烷烃分子中失掉一个氢原子后剰余的烃基(如甲基、乙基等),烯烃是
最便宜和活泼的烷基化剂,常用的烯烃有乙烯、丙烯等。
重要。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C7H15-n Ph2CH2NHSO2CF3
NaH/DMF
PhCH=N C7H15-n
10%HCl/THF heat/3h
n-C7H15NH2 80%
2.仲氨,叔胺的常用制备方法 (1):直接卤代烃的反应
MeNH2/EtOH Br
110 oC, 18h
NHMe + 78%
N
Me trace
Cl
Cl
COOH
OMe OH
COOMe
4.缩合试剂(DCC,偶氮二羧酸酯)
PhOH + PhCH2OH H
NCN HOR
NHCONH
DCC 100℃
PhOCH2Ph
H H
NC N O R HOAr
+ ArOR
PPh3/EtOOCN=NCOOEt
OR
OH + ROH
EtOOCN=NCOOEt PPh3
ArOH +Ph3PN NCOOEt
OH Br
NaOH
CH(OCH3)3 C(OCH3)4
O
2.磺酸酯为烃化剂
CH2OH CHOH CH2OH
Me2CO/HCl
CH2OH
CH-O C(CH3)2
CH2-O
C18H37OTs/KOH/Tol >110℃, 3 h
CH2OC18H37
CH-O C(CH3)2
CH2-O
EtOH/HCl ,2h
40% aq MeNH2 Cl
NHMe
NO2
DMSO, 25-35 oC
N
O CH2C
NO2
C2H5OH,HCl 33~35 oC,1h
COCH2NH2.HCl
O2N
氯霉素中间体
反应条件温和,
思考:该中间体能否用Gabriel反应做?
(4):三氟甲磺酰胺法
(CF3SO2)2O + PhCH2NH2
Et3N/CH2Cl2 -78 oC
Ph2CH2NHSO2CF3
Ph2CH2NHSO2CF3 n-C7H15Br/NaOH
Ph-CH-CH-OMe + Ph-CH-CH-OH
(25%)
(75%)
酸碱下的不同位点,易聚合
4.烯烃为烃化剂
CH3ONa CN
H3CO
CN
H O
H OH +
H3PO4 H
BF3 -20oC-0oC O
HO
叔丁基醚制备
5.氟硼酸三烷基傟盐为烃化剂
O OH
NH2
L-valine
NaNO2/HBr H2O
2.硫酸二甲酯为烃化剂
CHO
OH OCH3
Me2SO4/NaOH
CHO
OCH3 OCH3
3.重氮甲烷为烃化剂
_ H2C N+ N
+ HOR
H3C N N OR
O R = Ar or R'-C-
- N2 CH3OR
OMe OMe Excessive CH2N2
OH OH 2 mol CH2N2
COOMe
CH2OC18H37 CHOH CH2OH
对甲苯磺酸酯,甲磺酸酯,三氟甲磺酸酯
3.环氧乙烷为烃化剂
Ph-CH-CH2 + MeOH O
H2SO4 ,5h
OMe
OH
Ph-CH-CH-OH + Ph-CH-CH-OMe
(90%)
(10%)
Ph-CH-CH2 + MeOH O
CH3ONa ,5h
OH
OMe
苯拉海明
NMe2
差向异构
OH
CH3 cis
CH3I/NaH/THF 50℃, 1 h
OCH3
CH3 cis (100%)
OH CH3I/NaH/THF
CH3 trans
50℃, 1 h
OCH3
CH3 trans (100%)
多卤代物的醚化
CHCl3 +
3 CH3ONa
CCl4
+
4 CH3ONa
分子内醚化,制备环氧
第二章
烷基化反应
(Alkylation Reaction)
➢ C-O键的形成
➢ C-N键的形成
➢ C-C键的形成
第一节 氧原子上的烷基化反应 (醇和酚的烷基化)
一、醇的O-烷基化
Cat. H2SO4
OH
O
heat
简单醚或对称醚的制备
混合醚常用制备方法 1.卤代烃为烃化剂
ROH + R' X
Base
COOEt
ROH
EtOOCNHNHCOOEt
+ Ph3P O R ArO-
ArOR + Ph3PO
第二节 氮原子上的烷基化反应
一.氨及脂肪胺的N-烷基化反应
(一)氨及胺和卤代烃的反应
RX + NH3
RNH3+X-
Base
RNH2
RNH3+X- + NH3
RNH2 + NH4+X-
RNH2 + RX
R2NH
R2NH + RX
R3N
跟卤代烃的反应是主要方法之一, 缺点:易得到混合胺
1.伯氨的常用制备方法
(1):氨水和卤代烃的反应
O
OH Br
NH3(70mol) 70%
O
OH NH2
用大大过量的氨水,抑制进一步反应, 该方法在工业中应用广泛
NO2 Cl
O2N
NH3/AcONH4 170 oC, 6h
NO2 NH2
O2N
制备芳香胺
(2):Gabriel 反应
O KOH/EtOH
NH
O RX/DMF
N-K+
O
O NR O
NH2NH2
HCl/H2O 180 oC
O
O
NH NH
+
RNH2
O
COOH COOH
+ RNH2
应用范围较广,除少数活性较差的 卤代芳烃之外,适于各种带伯卤代 烃的取代基
NH2 NH
ROR'
Williamsion Reaction
NaI,KI,促进反应加速
RI > RBr > RCI
非拉西丁中间体
EtOH/NaOH
O2N
Cl
heat
O2N
OEt
95%
Ph CH Br + Me2N
Ph
ONa
二甲苯 heat
Ph CH OH + HCl.Me2N
Ph
NaOH/二甲苯
CH O
Cl
heat
低沸点卤代烃
CONH2 OEt
OCH3
NaH
OH +
Br NaH/THF reflux
OH + ClCH2OCH3
NaH/THF r.t.
OBn OMOM
分子内氢键的影响
O HO OH
1eq CH3I/NaOH
O HO OCH3
HO
O
OO H
OMe
1eq CH3I/NaOH MeO
O
OO H
OMe
N
MeOபைடு நூலகம்
抗疟药伯胺喹Primaquine
NH2
N
+
MeO
O N NH NO MeO
O N Br O
O
Br
Br +
NH
O
(3):Délépine 反应(乌洛托品)
N RX
NN N
N
HCl/EtOH N N+ RX-
N
RNH2
N NN
N
+ O2N
COCH2Br C6H5Cl
33~38 oC,1h
N N N+
(CH3)3O+BF4r.t.
O OH
Br
OMe Br
OH Br
Case:
NHBoc OH
PhCH2Br
NHBoc O
H N
O O
二、酚的O-烷基化
1.卤代烃为烃化剂
CONH2
EtBr/NaOH
OH
80~100℃, 19.6 x 10exp4 Pa
OH
CH3I/K2CO3/acetone
heat
