中华人民共和国卫生部公告2010年第3号
Fl201011231425392572

(二)国家毒物学计划NTP (二)国家毒物学计划NTP
3、研究结果及研究项目Study Results & 研究结果及研究项目Study Project: 提供研究报告Study Report, Research Project: 提供研究报告Study Report, 研究数据搜索Study Searches,同行专家评审, 研究数据搜索Study Data Searches,同行专家评审, 病理学表格Pathology Review,研 病理学表格Pathology Table for Peer Review,研 究报告摘要与联想,最新研究领域。 究报告摘要与联想,最新研究领域。均能进行检索 及获取全文。 及获取全文。
CSTE中心是疾病控制方面的流行病学中心, CSTE中心是疾病控制方面的流行病学中心,含有大 中心是疾病控制方面的流行病学中心 量的流行病方面的会议信息, 流行病、传染病、 量的流行病方面的会议信息,如:流行病、传染病、 心血管疾病等等会议信息。 心血管疾病等等会议信息。大量的流行病学方面的 出版物信息:关于慢性流行病学、传染病, 出版物信息:关于慢性流行病学、传染病,如:肝 艾滋病等;职业、环境报告等等信息。 炎,艾滋病等;职业、环境报告等等信息。还能与 美国疾病控制中心等多个组织机构连接。 美国疾病控制中心等多个组织机构连接。
美国国立卫生研究院国家环境卫生科学 研究所( 研究所(National Institute of Sciences, Environmental health Sciences, NIEHS) NIEHS)/
(一)环境基因组计划Environmental Genome Project: 环境基因组计划Environmental (/envgenom/home.htm)
国家药品监督管理局关于终止保护有关中药保护品种的通告(第3号)

国家药品监督管理局关于终止保护有关中药保护品种的通告(第3号)文章属性•【制定机关】国家药品监督管理局•【公布日期】2001.08.24•【文号】国药监注[2001]390号•【施行日期】2001.08.24•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】药政管理正文国家药品监督管理局关于终止保护有关中药保护品种的通告(第3号)(国药监注[2001]390号)各省、自治区、直辖市药品监督管理局:根据《中药品种保护条例》及有关文件规定,国家中药品种保护审评委员会组织审评委员对第三批保护期届满的中药保护品种进行了全面审查,对不符合延长保护期要求的品种提出了终止保护的意见。
根据国家中药品种保护审评委员会的审查意见,经我局审核,同意对下列品种(附件1)终止保护,现通告如下:一、对终止保护的中药品种,其生产企业不得冠以“国家中药保护品种”的称谓进行宣传,其品种还可以继续生产、销售和使用。
二、对卫生部“关于发布中止有关中药同品种药品生产批准文号的通报(第3号)”(卫药发[1996]第19号)(附件2)中止药品批准文号效力的品种,自本通告发布之日起,对涉及终止保护的品种(附件1)解除其中止药品批准文号效力的约束力,有关企业可据此向当地省级药品监督管理部门申请恢复其批准文号效力。
三、各省(区、市)药品监督管理部门对上述有关企业提出恢复其批准文号效力的申请可以受理,并参照《仿制药品审批办法》的规定办理。
特此通告。
附件:1.终止保护的品种名单(第3批)2.卫药发[1996]第19号(只发有关单位)国家药品监督管理局二00一年八月二十四日附件1:终止保护的品种名单(第3批)─────────────────────────────────────────序号药品名称企业名称─────────────────────────────────────────1刺五加注射液黑龙江乌苏里江制药有限公司─────────────────────────────────────────2刺五加注射液黑龙江省完达山制药厂─────────────────────────────────────────3风湿圣药吉林省辉南天泰药业股份有限公司─────────────────────────────────────────4福寿胶囊厦门中药厂─────────────────────────────────────────5骨刺消痛涂膜剂北京同仁堂股份有限公司同仁堂药酒厂─────────────────────────────────────────6冠心安口服液哈药集团中药二厂─────────────────────────────────────────7冠心安口服液北京同仁堂科技发展股份有限公司制药厂─────────────────────────────────────────8康氏牛黄解毒丸北京同仁堂股份有限公司同仁堂制药厂─────────────────────────────────────────9烧伤净喷雾剂北京同仁堂科技发展股份有限公司制药厂─────────────────────────────────────────10小儿肺热咳喘冲剂四川光大制药有限公司─────────────────────────────────────────11腰腿痛丸山东省临沂银雀山制药厂─────────────────────────────────────────12腰腿痛丸大连海洋药业有限公司─────────────────────────────────────────13腰腿痛丸锦州同德中药药业有限责任公司─────────────────────────────────────────14腰腿痛丸本溪普济制药有限公司─────────────────────────────────────────15优福宁胶囊南京同仁堂药业有限责任公司─────────────────────────────────────────16枣仁安神液北京同仁堂股份有限公司同仁堂制药厂─────────────────────────────────────────17壮骨药酒北京同仁堂股份有限公司同仁堂药酒厂─────────────────────────────────────────附件二:卫生部文件卫药发[1996]第19号─────────────────────────────────────关于中止有关中药同品种药品生产批准文号的通报(第3号)各省、自治区、直辖市卫生厅(局)根据国务院《中药品种保护条例》和我部卫药发(1995)第23号文件的有关规定,现将“国家中药保护品种”第3号公告中涉及应中止药品生产批准文号的同品种(见附件)印发给你们,对涉及的有关品种,请你厅(局)及时中止有关企业的药品生产批准文号并监督其停止生产。
卫生部通告()3号

卫生部通告()3号篇一:卫生部涉及饮用水卫生安全产品检验规定卫生部涉及饮用水卫生安全产品检验规定(节选)(自_年_月1日起实施)1. 涉及饮用水卫生安全产品检验时限说明:1. 本表中所列时间为完成该类产品全部检验项目所需时间.2. 检验时限为自正式受理样品之日起至出具检验报告之日.3. 检验机构受理样品时应将出具报告时间及相关事宜通知送检单位.4. 特殊情况(例如检验时限内含长假)由检验机构与送检单位协商确定检验时限.如遇滤速甚慢的水质处理器(如陶瓷滤芯.滤膜阻塞),则检验时限应予延长.水样滤过时间(天)=额定总净水量/每日滤水量.5. 各类一般水质处理器.矿化水器.纯净水处理器(不含大型水质处理器),如卫生安全性与卫生功能性检验在同一检验机构检验,则全部检验时限可缩短为45天.6. 检验机构应将本表内容向送检单位公布.1. 涉及饮用水卫生安全产品检验所需样品数量及规格说明:1.管材检验为取6升浸泡液用作检验,则不同管内径(mm)所需管长度(m)如下:2.管件按内表面估计,5_cm2加入1升浸泡液浸泡.3.各种家用净水器.矿化水器需样8台,其中用于卫生安全性检验3台,卫生功能性检验5台.4.颗粒状材料以表观体积计算,加入50倍体积的浸泡液;膜组件和结构滤芯以外观面积计算,5_cm2加入1升浸泡液浸泡.浸泡液配制采用>附录A方法制备.浸泡时间24h ? 1h,浸泡温度25℃±5℃.5.上述样品所产生的水样不足检验所需时,由检验单位与送检单位协商确定样品数量.但检验机构应在受理样品之前告知送检单位. 6.检验机构应将本表内容向送检单位公布. 3.涉及饮用水卫生安全产品检验项目及要求3.1 与生活饮用水接触的输配水设备(管材.管件.蓄水容器.止水材料)检验项目篇二:卫生部涉及饮用水卫生安全产品检验规定卫生部涉及饮用水卫生安全产品检验规定1. 涉及饮用水卫生安全产品检验时限说明:1.本表中所列时间为完成该类产品全部检验项目所需时间. 2.检验时限为自正式受理样品之日起至出具检验报告之日.3.检验机构受理样品时应将出具报告时间及相关事宜通知送检单位.4.特殊情况(例如检验时限内含长假)由检验机构与送检单位协商确定检验时限.如遇滤速甚慢的水质处理器(如陶瓷滤芯.滤膜阻塞),则检验时限应予延长.水样滤过时间(天)=额定总净水量/每日滤水量.5.各类一般水质处理器.矿化水器.纯净水处理器(不含大型水质处理器),如卫生安全性与卫生功能性检验在同一检验机构检验,则全部检验时限可缩短为45天.6. 2. 涉及饮用水卫生安全产品检验所需样品数量及规格说明:2.管件按内表面估计,5_cm加入1升浸泡液浸泡.3.各种家用净水器.矿化水器需样8台,其中用于卫生安全性检验3台,卫生功能性检验5台.4.颗粒状材料以表观体积计算,加入50倍体积的浸泡液;膜组件和结构滤芯以外观面积计算,5_cm2加入1升浸泡液浸泡.浸泡液配制采用>附录A方法制备.浸泡时间24h ? 1h,浸泡温度25℃±5℃.5.上述样品所产生的水样不足检验所需时,由检验单位与送检单位协商确定样品数量.但检验机构应在受理样品之前告知送检单位.6.检验机构应将本表内容向送检单位公布.3.涉及饮用水卫生安全产品检验项目及要求3.1 与生活饮用水接触的输配水设备(管材.管件.蓄水容器.止水材料)检验项目说明:1.聚合物单体和添加剂如氯乙烯.苯乙烯.环氧氯丙烷.甲醛.丙烯腈.邻苯二甲酸二(2-乙基己基)酯可根据具体聚合物类别选项测定,也可以增加新项目. 2.有者为选测项目.3.√ 由省级卫生行政部门认定的检验机构检验. 4.○ 由卫生部认定的检验机构检验.5.国内外有标准,首次用于涉水产品,做毒理实验;国内外无标准,首次用于涉水产品,制定水中最高允许浓度.6.检验机构应将本表内容向送检单位公布.3.2 与生活饮用水接触的防护材料(涂料.内衬等)检验项目1.浸泡30天中,第一次(第一天)和最后一次(第三十天)全分析,中间四次测定感官指标.溶解性总固体.耗氧量和第一次全分析的超标项目. 2.有者为选测项目.3.√ 由省级卫生行政部门认定的检验机构检验. 4.○ 由卫生部认定的检验机构检验.5.检验机构应将本表内容向送检单位公布.3.3 与生活饮用水接触的水处理材料检验项目篇三:涉及饮用水卫生安全产品分类目录/retype/zoom/7933ee44bb68a98270fefa1b?pn=1__=0_y=66_raww=_1_rawh=27_o =png_6_0_0_0_0_0_0_892.979__62.879_type=pic_aimh=27_md5sum=633a4e_64_ cfdcc4_8d47d9f6958d_sign=e1d31b44de_zoom=_png=0-641_jpg=0-776”target=“_blank”>点此查看中央政府门户网站_年_月_日 _时_分来源:卫生部网站【推荐【字体:大中小】卫生部关于印发>的通知卫监督发〔_〕80号各省.自治区.直辖市卫生厅局,新疆生产建设兵团卫生局,中国疾病预防控制中心.卫生部卫生监督中心:为进一步加强涉及饮用水卫生安全产品监督管理,规范涉及饮用水卫生安全产品的分类和产品范围,我部组织对>进行了修订.现将修订后的>(以下简称>)印发给你们,请遵照执行.省级以上卫生行政部门要按照>和卫生部的有关规定,对列入>的产品进行卫生行政许可.对已受理,但未列入>产品的卫生行政许可申请,省级以上卫生行政部门不予发放卫生行政许可批件,并做好相关的解释工作.已获得卫生行政许可批件,但未列入>的产品可继续使用卫生行政许可批件,卫生行政许可批件到期后,原批准机关不再受理该产品的卫生行政许可延续申请,并注销卫生行政许可批件.附件:涉及饮用水卫生安全产品分类目录(_年版)二○一一年九月二十二日附件涉及饮用水卫生安全产品分类目录(_年版)一.输配水设备(一)管材.管件.(二)蓄水容器.(三)无负压供水设备.(四)饮水机.(五)密封.止水材料:密封胶条.密封圈.二.防护材料(一)环氧树脂涂料.(二)聚酯涂料(含醇酸树脂).(三)丙烯酸树脂涂料.(四)聚氨酯涂料.三.水处理材料活性炭.活性氧化铝.陶瓷.分子筛(沸石).锰沙.熔喷聚丙烯(聚丙烯棉).铜锌合金(KDF).微滤膜.超滤膜.纳滤膜.反渗透膜.离子交换树脂.碘树脂等及其组件.四.化学处理剂(一)絮凝剂.助凝剂.聚合氯化铝(碱式氯化铝.羟基氯化铝).硫酸铁.硫酸亚铁.氯化铁.氯化铝.硫酸铝(明矾).聚丙烯酰胺.硅酸钠(水玻璃)及其复配产品.(二)阻垢剂.磷酸盐类.硅酸盐类及其复配产品.(三)消毒剂.次氯酸钠.二氧化氯.高锰酸钾.过氧化氢.五.水质处理器(一)以市政自来水为原水的水质处理器.活性炭净水器.粗滤净水器.微滤净水器.超滤净水器.软化水器.离子交换装置.蒸馏水器.电渗析水质处理器.反渗透净水器.纳滤净水器等.(二)以地下水或地表水为水源的水质处理设备(每小时净水流量≤25m3/h).(三)饮用水消毒设备.二氧化氯发生器.臭氧发生器.次氯酸发生器.紫外线消毒器等.六.与饮用水接触的新材料和新化学物质使用新材料或新化学物质制造的与生活饮用水接触的输配水设备.防护材料.水处理材料和化学处理剂.。
中华人民共和国卫生部公告 2010年 第23号

中华人民共和国卫生部公告 2010年第23号
佚名
【期刊名称】《中华人民共和国国家卫生和计划生育委员会公报》
【年(卷),期】2011(0)1
【摘要】根据《中华人民共和国食品安全法》和《食品添加剂新品种管理办法》的规定,经审核,现批准溶菌酶等8种物质为食品添加剂,批准环己基氨基磺酸钠等22种食品添加剂和叶酸等3种营养强化剂扩大使用范围及用量.
【总页数】5页(P7-11)
【关键词】中华人民共和国;卫生部;食品添加剂;公告;食品安全法;营养强化剂;品种管理;氨基磺酸
【正文语种】中文
【中图分类】D922.16
【相关文献】
1.中华人民共和国卫生部、中华人民共和国工业和信息化部、中华人民共和国农业部、国家工商行政管理总局、国家质量监督检验检疫总局公告 [J], 无;;;;;
2.中华人民共和国卫生部、中华人民共和国工业和信息化部、中华人民共和国商务部、国家工商行政管理总局、国家质量监督检验检疫总局、国家粮食局、国家食品药品监督管理局公告 [J], ;
3.中华人民共和国卫生部公告2008年第6号卫生部公告22种食品添加剂扩大使用范围、使用量 [J],
4.国家体育总局,中华人民共和国商务部,中华人民共和国卫生部,中华人民共和国海关总署,国家食品药品监督管理局公告第9号2009年兴奋剂目录公告 [J], ;;;;;
5.中华人民共和国公安部、中华人民共和国商务部、中华人民共和国卫生部、中华人民共和国海关总署、国家安全生产监督管理总局、国家食品药品监督管理局发出关于将羟亚胺列入《易制毒化学品管理条例》的公告 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。
关于批准DHA藻油、棉籽低聚糖等7种物品为新资源食品及其他相关规定的公告(2010年 第3号)

关于批准DHA藻油、棉籽低聚糖等7种物品为新资源食品及其他相关规定的公告(2010年第3号)根据《中华人民共和国食品安全法》和《新资源食品管理办法》的规定,现批准DHA藻油、棉籽低聚糖、植物甾醇、植物甾醇酯、花生四烯酸油脂、白子菜、御米油等7种物品为新资源食品,允许玫瑰花(重瓣红玫瑰Rose rugosa cv. Plena)、凉粉草(仙草Mesona chinensis Benth.)作为普通食品生产经营,允许夏枯草(Prunella vulgaris L.)、布渣叶(破布叶Microcos paniculata L.)、鸡蛋花(Plumeria rubra L.cv.Acutifolia)作为凉茶饮料原料使用。
生产经营上述食品应当符合有关法律、法规、标准规定。
特此公告。
中华人民共和国卫生部二○一○年三月九日附件:DHA藻油棉子低聚糖中文名称棉子低聚糖英文名称Raffino-oligosaccharide主要成分棉子糖基本信息来源:棉花的种子(棉籽)棉子糖结构式:分子式:C18H32O16分子量:504生产工艺简述以棉籽为原料,经浸油、脱酚、提糖、脱色、快速降温、干燥粉碎等步骤获得棉子低聚糖。
食用量≤5克/天质量要求性状淡黄色或白色粉末总糖≥70.0%棉子糖≥45.0%水分≤5.0%灰分≤5.0%游离棉酚≤10mg/kg溶剂残留正己烷≤1mg/kg乙醇≤10 mg/kg其他需要说明的情况使用范围不包括婴幼儿食品植物甾醇酯中文名称 植物甾醇酯 英文名称 Plant sterol ester基本信息来源:大豆油、菜籽油、玉米油、葵花籽油、塔罗油 β-谷甾醇酯结构式: 菜油甾醇酯结构式:分子式:C 47O 2H 80 分子式:C 46O 2H 78 分子量:676 分子量:662豆甾醇酯结构式:分子式:C 47O 2H 78 分子量:674生产工艺简述利用大豆油等植物油馏分或塔罗油为原料,通过皂化、萃取、结晶等工艺得到植物甾醇,然后将植物甾醇和葵花籽油脂肪酸进行酯化生产得到植物甾醇酯。
2010_GMP完整版

药品生产质量管理规范(2010年修订)目录《药品生产质量管理规范(2010年修订)》发布 (1)关于发布《药品生产质量管理规范(2010年修订)》无菌药品等5个附录的公告 (3)关于实施《药品生产质量管理规范(2010年修订)》有关事宜的公告 (4)药品生产质量管理规范(2010年修订)(卫生部令第79号) (6)第一章总则 (6)第二章质量管理 (6)第一节原则 (6)第二节质量保证 (7)第三节质量控制 (8)第四节质量风险管理 (9)第三章机构与人员 (9)第一节原则 (9)第二节关键人员 (10)第三节培训 (13)第四节人员卫生 (13)第四章厂房与设施 (14)第一节原则 (14)第二节生产区 (15)第三节仓储区 (16)第五节辅助区 (17)第五章设备 (18)第一节原则 (18)第二节设计和安装 (18)第三节维护和维修 (18)第四节使用和清洁 (18)第五节校准 (19)第六节制药用水 (20)第六章物料与产品 (21)第一节原则 (21)第二节原辅料 (22)第三节中间产品和待包装产品 (23)第四节包装材料 (23)第五节成品 (24)第六节特殊管理的物料和产品 (24)第七节其他 (24)第七章确认与验证 (25)第八章文件管理 (27)第一节原则 (27)第二节质量标准 (28)第三节工艺规程 (29)第四节批生产记录 (31)第六节操作规程和记录 (33)第九章生产管理 (33)第一节原则 (33)第二节防止生产过程中的污染和交叉污染 (35)第三节生产操作 (35)第四节包装操作 (36)第十章质量控制与质量保证 (37)第一节质量控制实验室管理 (37)第二节物料和产品放行 (43)第三节持续稳定性考察 (44)第四节变更控制 (45)第五节偏差处理 (46)第六节纠正措施和预防措施 (47)第七节供应商的评估和批准 (47)第八节产品质量回顾分析 (49)第九节投诉与不良反应报告 (50)第十一章委托生产与委托检验 (51)第一节原则 (51)第二节委托方 (51)第三节受托方 (51)第四节合同 (52)第十二章产品发运与召回 (52)第二节发运 (53)第三节召回 (53)第十三章自检 (54)第一节原则 (54)第二节自检 (54)第十四章附则 (54)附录1:无菌药品 (60)第一章范围 (60)第二章原则 (60)第三章洁净度级别及监测 (60)第四章隔离操作技术 (64)第五章吹灌封技术 (64)第六章人员 (65)第七章厂房 (66)第八章设备 (67)第九章消毒 (67)第十章生产管理 (67)第十一章灭菌工艺 (69)第十二章灭菌方法 (70)第十三章无菌药品的最终处理 (72)第十四章质量控制 (72)第十五章术语 (73)附录2:原料药 (74)第一章范围 (74)第二章厂房与设施 (74)第三章设备 (74)第四章物料 (75)第五章验证 (75)第六章文件 (77)第七章生产管理 (77)第八章不合格中间产品或原料药的处理 (80)第九章质量管理 (81)第十章采用传统发酵工艺生产原料药的特殊要求 (81)第十一章术语 (82)附录3:生物制品 (84)第一章范围 (84)第二章原则 (84)第三章人员 (84)第四章厂房与设备 (85)第五章动物房及相关事项 (86)第六章生产管理 (87)第七章质量管理 (88)第八章术语 (89)附录4:血液制品 (90)第一章范围 (90)第二章原则 (90)第三章人员 (90)第四章厂房与设备 (91)第五章原料血浆 (91)第六章生产和质量控制 (92)第七章不合格原料血浆、中间产品、成品的处理 (93)附录5:中药制剂 (94)第一章范围 (94)第二章原则 (94)第三章机构与人员 (94)第四章厂房设施 (95)第五章物料 (95)第六章文件管理 (96)第七章生产管理 (97)第八章质量管理 (97)第九章委托生产 (98)第十章术语 (99)《药品生产质量管理规范(2010年修订)》发布2011年02月12日发布历经5年修订、两次公开征求意见的《药品生产质量管理规范(2010年修订)》(以下简称新版药品GMP)今天对外发布,将于2011年3月1日起施行。
卫生部公布的新资源食品名单及既是食品又是药品名单(截止到2010年3月15日)

既是食品又是药品的品种目录在药材中,卫生部曾分两次公布过既是食品又是药品的品种目录。
对普通商店、副食店及在农贸市场中经营这些品种的经营户,不需发《药品经营企业许可证》;但是,以药品经营的名义和形式从事上述品种经营的,必须依据《药品管理法》获得《药品经营企业许可证》,否则,按无证经营的有关规定处理。
卫生部曾公布的两批名单有69种:八角茴香、刀豆、姜(生姜、干姜)、枣(大枣、酸枣、黑枣)、山药、山楂、小茴香、木瓜、龙眼肉(桂圆)白扁豆、百合、花椒、芡实、赤小豆、佛手、青果、杏仁(甜、苦)、昆布、桃仁、莲子、桑椹、榧子、淡豆鼓、黑芝麻、蜂蜜莴苣、薏苡仁、枸杞子、乌梢蛇、蝮蛇、酸枣仁、牡蛎、栀子、甘草、代代花、罗汉果、肉桂、决明子、莱菔子、陈皮、砂仁、乌梅、肉豆蔻、白芷、菊花、藿香、沙棘、郁李仁、白果、薤白、薄荷、丁香、高良姜、香、火麻仁、桔红、茯苓、香薷、红花、紫苏、麦芽、黄芥子、鲜白茅根、荷叶、桑叶、鸡内金、马齿苋、鲜芦根。
卫生部新公布的既是食品又是药品的名单有8种:蒲公英、淡竹叶、胖大海、金银花、余甘子、葛根、鱼腥草。
作为普通食品管理的食品新资源名单:油菜花粉、玉米花粉、松花粉、向日葵花粉、紫云英花粉、荞麦花粉、芝麻花粉、高梁花粉、魔芋、钝顶螺旋藻、极大螺旋藻、刺梨、玫瑰茄、蚕蛹广东省报卫生部加药食品名单:淮山药、葛花、玉竹、艾叶、沙参、桑叶、黄精、白术、银花、梅花、狗脊、槐花、白芍、麦冬、芦荟、天冬、苍术、益智、胖大海、何首乌、枇杷叶、夏枯草、淡竹叶、蒲公英、巴戟、绞股蓝、灯心草、鸡血藤、茵陈蒿、竹壳茶、木棉花、鸡蛋花、藤茶、广东凉茶、广东凉粉、冬虫夏草、白花蛇舌草、白茅根、芦根。
卫生部公布的新资源食品名单卫生部批准作为食品新资源使用的物质,共分为九类:1、中草药和其他植物人参、党参、西洋参、黄芪、首乌、大黄、芦荟、枸杞子、巴戟天、荷叶、菊花、五味子、桑椹、薏苡仁、茯苓、广木香、银杏、白芷、百合、山苍籽油、山药、鱼腥草、绞股蓝、红景天、莼菜、松花粉、草珊瑚、山茱萸汁、甜味藤、芦根、生地、麦芽、麦胚、桦树汁、韭菜籽、黑豆、黑芝麻、白芍、竹笋、益智仁2、果品类大枣、山楂、猕猴桃、罗汉果、沙棘、火棘果、野苹果3、茶类金银花茶、草木咖啡、红豆茶、白马蓝茶、北芪茶、五味参茶、金花茶、胖大海、凉茶、罗汉果苦丁茶、南参茶、参杞茶、牛蒡健身茶4、菌藻类乳酸菌、脆弱拟杆菌(BF-839)、螺旋藻、酵母、冬虫夏草、紫红曲、灵芝、香菇5、畜禽类熊胆、乌骨鸡6、海产品类海参、牡蛎、海马、海窝7、昆虫爬虫类蚂蚁、蜂花粉、蜂花乳、地龙、蝎子、壁虎、蜻蜒、昆虫蛋白、蛇胆、蛇精8、矿物质与微量元素类珍珠、钟乳石、玛瑙、龙骨、龙齿、金箔、硒、碘、氟、倍半氧化羧乙基锗(Ge-132)、赖氨酸锗9、其它类牛磺酸、SOD、变性脂肪、磷酸果糖、左旋肉碱这些是药食两用的中药和微量元素及菌类等可用于食品的物质,卫生部并没有在同一个文件中全部罗列出来,而是每年都有变化。
中华人民共和国卫生部公告2010年第3号

2006-2008年深圳市水产品污染状况分析———王舟黄薇潘柳波等—167—表22006年深圳市贝类毒素检测结果样品名称生物法试剂盒麻痹性毒素(MU /g )腹泻性毒素(MU /g )麻痹性毒素(ng /g )腹泻性毒素(ng /g )鲍鱼<0.875--18.27海螺<0.875--28.27花蛤-- 3.8982.43扇贝--19.8557.14花甲<0.875--28.72象牙蚌<0.875--未检出鲍鱼仔--9.4872.87注:0.875MU /g 为该方法检出限;“-”为未检测。
表32007-2008年深圳市淡水水产品肝吸虫囊幼检测结果鱼种2007年2008年检测份数阳性份数阳性率(%)检测份数阳性份数阳性率(%)鲩鱼13430.771218.33鲫鱼12216.671317.69大头鱼14214.291218.33鲤鱼15213.331100福寿鱼2129.5214428.57生鱼130011218.18乌头鱼1200---桂花鱼12001000鲢鱼9005120.00鲮鱼---100鲈鱼---100鲶鱼---100塘虱鱼---100合计121129.92921010.87注:“-”为未检测。
3讨论从3年的监测数据来看,深圳市的水产品均存在不同程度的污染,主要污染项目为副溶血性弧菌、铅和亚硝酸盐。
副溶血性弧菌存在于水体,是水产品引起食物中毒的主要致病菌,在微生物引起的食物中毒中,副溶血性弧菌居各种病因之首[4]。
水产品中铅污染是由于铅在水体和沉积物中积聚所致。
深圳地区水网众多,人们素有吃鱼生的习惯,肝吸虫囊蚴存在于淡水鱼虾中,人群肝吸虫感染率与生食鱼生有直接关系[5],不洁鱼生也是引发食物中毒的诱因之一[6]。
为了遏制肝吸虫病的抬头趋势,提高广大市民的健康水平,应当从防治两方面着手。
首先是“防”,通过宣传,让广大市民了解肝吸虫病的流行病学知识,坚决不吃鱼生、未煮熟的淡水虾及鱼片粥等食物,防患于未然;其次是“治”,对于已发现肝吸虫抗体阳性的人群,建议积极做病原学检查,根据检查结果做相应的治疗,避免造成更大的伤害。
卫医政发〔2010〕99号卫生部关于印发二、三级综合医院药学部门基本标准(试行)的通知

卫医政发〔2010〕99号卫生部关于印发二、三级综合医院药学部门基本标准(试行)的通知卫生部关于印发二、三级综合医院药学部门基本标准(试行)的通知卫医政发〔2010〕99号各省、自治区、直辖市卫生厅局,新疆生产建设兵团卫生局:为加强医院药学部门管理,促进临床合理用药,保证用药安全,根据《中华人民共和国药品管理法》和《医疗机构管理条例》等法律、法规,我部组织制定了《二、三级综合医院药学部门基本标准(试行)》(以下简称《标准》)。
现印发给你们,请遵照执行。
药学部门符合《标准》要求的医院,要继续加强管理,不断提高医院药学服务水平。
尚不具备《标准》规定条件的医院,要加强对药学部门的建设,增加人员,配置设备,改善条件,健全制度,逐步建立标准化规范化的医院药学部门。
二○一○年十二月三日二、三级综合医院药学部门基本标准(试行)为加强综合医院药学部门的规范化管理,指导医院加强药学部门内涵建设,促进医院药学发展,提高药学服务质量和药物治疗水平,确保药品质量,保障医疗安全,根据《药品管理法》和《医疗机构管理条例》等法律、法规,制定本基本标准。
医院药学部门是医院专业技术科室,负责有关的药事管理和药学专业服务工作,并承担监督与推进相关药事法规落实的职责。
药事管理和药学专业服务工作主要包括本医院药品保障供应与管理;处方适宜性审核、药品调配以及安全用药指导;实施临床药师制,直接参与临床药物治疗;药学教育、与医院药学相关的药学研究等。
医院药学部门的设置:二级综合医院设置药剂科,三级综合医院设置药学部。
二级综合医院药剂科基本标准一、分区布局(一)药剂科的分区应当以病人为中心,坚持统一管理及整体性原则,确保其功能与任务的落实。
(二)药剂科的面积、布局和流程合理,应当能够保障其正常工作开展的需要;区域划分合理,工作区与非工作区应当分别设置。
(三)根据医院规模、任务与药剂科开展药学专业技术工作的实际需要,药剂科应当设置相应的工作室,如药品调剂室、药品库、临床药学室和质量监控室等。
即食谷物粉(食品安全企业标准)

食品安全国家标准 食品中蛋白质的测定
GB 5009.6
食品安全国家标准 食品中脂肪的测定
GB 5009.11
食品安全国家标准 食品中总砷及无机砷的测定
GB 5009.12 GB 5009.22 GB 5009.82 GB 5009.88 GB 5009.89 GB 5413.11 GB 5413.18 GB 5413.21 GB 5413.31 GB/T 6543 GB 7096 GB 7101 GB 7718 GB 7949 GB 8270 GB 8820 GB 9683 GB 11674 GB 14751 GB 14754 GB 14755 GB 14757 GB 14880 GB 14881 GB/T 16919 GB 19640 GB/T 20706 GB/T 20880 GB/T 20884 GB/T 20886 GB/T 22492 GB/T 22493 GB/T 23529 GB 25531 GB/T 26762 GB 28050 GB 29921 GB 30616 GH/T 1030 DBS 32/009 JJF 1070 NY/T 749 NY/T 777 NY/T 834
即食谷物粉
1 范围 本标准规定了即食谷物粉的要求、试验方法、检验规则、标志、包装、运输及贮存。 本标准适用于以膨化谷物粉(荞麦粉、薏苡仁粉、小米粉、糙米粉、燕麦粉、红豆粉、大豆粉、黑豆
粉、绿豆粉中的一种或数种)或酶解谷物粉(大米粉、燕麦粉、糙米粉)或谷物配方粉为主要原料,添加 或不添加水果粉(青木瓜粉、葡萄粉、椰子粉、甜橙粉)、水苏糖、红萝卜粉、白芷、核桃粉、黄瓜籽粉、 骨胶原蛋白肽、酶解鱼骨粉、莱菔子、陈皮、麦芽、南瓜籽粉、精肽粉、松花粉、食用酵母、麦芽糊精、 果糖、大豆肽粉、中链甘油三酯、葡萄糖、马齿苋、可可粉、冬瓜、植脂末、鸡内金、灰树花、清蛋白多 肽、银耳、黄花菜、花生、藕节、大枣、养心菜、海藻糖、大豆蛋白粉、人参(人工种植)、茯苓、山药、 莲子、白扁豆、猴头菇粉、耳叶牛皮消、a-乳白蛋白、乳清蛋白粉、亚麻籽油粉、紫苏子油粉、大麦苗粉 (麦绿素)、螺旋藻粉、蛋白核小球藻,添加或不添加新资源食品:圆苞车前子壳、小麦低聚肽、菊粉、 低聚木糖、玛咖、γ-氨基丁酸、乳矿物盐、β-羟基-β-甲基丁酸钙、辣木叶粉,添加或不添加营养强化 剂:维生素 B1、维生素 C、维生素 D、烟酸、葡萄糖酸锌、葡萄糖酸亚铁、焦磷酸铁,添加或不添加食品 添加剂:三氯蔗糖、异麦芽酮糖、甜菊糖苷、羧甲基纤维素钠、黄原胶和食品用香精,部分原料烘干、粉 碎,经过筛、配料、混合、制粒或不制粒、包装制成的即食谷物粉。
医疗卫生法律法规知识

• 由全国人民代表大会制定或修改的刑事、民事、国 家机构的和其他的基本法律。
如:《中华人民共和国宪法》、《中华人民共和国民法通 则》、《中华人民共和国刑法》等。
• 由全国人民代表大会常务委员会制定的其他法律;或者由 全国人民代表大会常务委员会进行补充、修改由全国人民 代表大会制定的法律。 如:《中华人民共和国婚姻法》、《中华人民共和国劳动 合同法》、《中华人民共和国执业医师法》、《中华人民 共和国食品卫生法》等。
• 部门规章:由国务院各部和其他具有行政管理职能 的机构,在本部门的权限范围内制定。并由部门首 长签署命令予以公布;
• 地方政府规章:由各省、自治区、直辖市(含较大 的市)的人民政府,根据法律、行政法规和地方性 法规制定,由省长或者自治区主席,或者市长签署 命令予以公布。
法律、法规、规章的法律效力?
(《中华人民共和国执业医师法》第三章第二十二条 )
医师在执业活动中应享受哪些权利?
(一)在注册的执业范围内,进行医学诊查、疾病调查、医学处置、出具相应 的医学证明文件,选择合理的医疗、预防、保健方案;
(二)按照国务院卫生行政部门规定的标准,获得与本人执业活动相当的医疗 设备基本条件;
• 《消毒管理办法》(2002年3月28日卫生部令第27号发布) • 《药品不良反应报告和监测管理办法》(2004年3月4日卫
生部、国家食品药品监督管理局发布,国家食品药品监督管 理局令第7号) • 《放射诊疗管理规定》(2006年1月24日卫生部令第46号发 布) • 《医院感染管理办法》(2006年7月6日卫生部令第48号发 布)
如:《重庆市医疗机构管理条例》、《重庆市中医 药条例》、《重庆市预防控制性病艾滋病条例》 等。
医疗机构临床基因扩增管理办法(卫生部2010年)

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载医疗机构临床基因扩增管理办法(卫生部2010年)地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容卫生部办公厅关于印发《医疗机构临床基因扩增管理办法》的通知中华人民共和国卫生部卫办医政发〔2010〕194号各省、自治区、直辖市卫生厅局,新疆生产建设兵团卫生局:为进一步规范临床基因扩增检验实验室管理,保证临床诊断科学、合理,保障患者合法权益,根据《医疗机构管理条例》、《医疗机构临床实验室管理办法》,我部对《临床基因扩增检验实验室管理暂行办法》(卫医发〔2002〕10号)进行了修订,制定了《医疗机构临床基因扩增检验实验室管理办法》。
现印发给你们,请遵照执行。
医疗机构临床基因扩增检验实验室管理办法第一章总则第一条为规范医疗机构临床基因扩增检验实验室管理,保障临床基因扩增检验质量和实验室生物安全,保证临床诊断和治疗科学性、合理性,根据《医疗机构管理条例》、《医疗机构临床实验室管理办法》和《医疗技术临床应用管理办法》,制定本办法。
第二条临床基因扩增检验实验室是指通过扩增检测特定的DNA或RNA,进行疾病诊断、治疗监测和预后判定等的实验室,医疗机构应当集中设置,统一管理。
第三条本办法适用于开展临床基因扩增检验技术的医疗机构。
第四条卫生部负责全国医疗机构临床基因扩增检验实验室的监督管理工作。
各省级卫生行政部门负责所辖行政区域内医疗机构临床基因扩增检验实验室的监督管理工作。
第五条以科研为目的的基因扩增检验项目不得向临床出具检验报告,不得向患者收取任何费用。
第二章实验室审核和设置第六条医疗机构向省级卫生行政部门提出临床基因扩增检验实验室设置申请,并提交以下材料:责验收行政部门执业许可证》(一)《医疗机构执业许可证》复印件;(二)医疗机构基本情况,拟设置的临床基因扩增检验实验室平面图以及拟开展的检验项目、实验设备、设施条件和有关技术人员资料;(三)对临床基因扩增检验的需求以及临床基因扩增检验实验室运行的预测分析。
卫生部公布的新资源食品目录(更新至2013年2月28日)

使用范围
食用量
发布日期
Dunaliella Salina (extract)
不包括婴幼儿食品
≤15毫克/天(以β-胡 萝卜素计)
发布来源
备注
产品的胡萝卜素含量2- 8%,其标签、说明书标注 为盐藻;产品的胡萝卜素含 量≥8%,其标签、说明书
标注为盐藻提取物。
Fish Oil (extract)
Diacylglycerol Oil
——
Sucrose Ployesters
Medium- and long-chain triacylglycerol oil
婴幼儿不宜食用 ——
—— ≤3克/天
—— ≤50克/天 ≤20克/天 ≤5克/天
—— ≤10.6 克/天
≤30克/天
2013/1/4
卫生安全指标应符合我国相
关于批准茶树花等7种新
Acai
——
Phylloporia ribis (Schumach:Fr.)Ryvarden
婴幼儿、儿童及食用真 菌过敏者不宜食用
Chlorella pyrenoidesa
不包括婴幼儿食品
Linderae aggregate leaf
婴幼儿、儿童、孕期及 哺乳期妇女不宜食用
Moringa oleifera leaf
——
Panax Ginseng C.A.Meyer
孕妇、哺乳期妇女及14 周岁以下儿童不宜食用
16
肠膜明串珠菌肠膜亚种
Leuconostoc.mesenteroides subsp.mesenteroides
——
17
蚌肉多糖
Hyriopsis cumingii polysacchride
食品安全制度法规体系变迁的核心

食品安全制度法规体系变迁的核心新中国成立以来,我国食品安全监管体制和机构经历了多次变迁,在法律法规、监管体制等方面也取得了重大成果。
2009 年《食品安全法》的正式实施,标志着我国食品监管理念从1995 年的保障“食品卫生”转变为保障“食品安全,保障公众身体健康和生命安全”。
2015 年新修订的《食品安全法》中首次出现保健食品、特殊医学用途配方食品、婴幼儿配方乳粉三大类食品为特殊食品的法律概念,具有划时代的里程碑意义。
特殊食品作为食品的重要组成部分,事关特定人群的身体健康和生命安全。
中国已经成为全球最大特殊食品消费市场,市场规模超过6000 亿元。
随着国民经济的发展和人民消费水平的不断提高,以营养保健为主的食品消费正逐步成为民众消费的主流,特殊食品市场需求在不断增长。
特殊食品正成为食品企业转型升级的新热点。
2019 年是新中国成立70 周年,亦是新《食品安全法》颁布施行第四年。
回首过去,我国的三类特殊食品监管工作爬坡过坎、滚石上山,经历了惨痛的教训,亦在发展中不断规范,在规范中谋求新的发展。
回顾和梳理新中国成立以来,我国三类特殊食品的监管法规体系演变历程,必将为推进新时期持续做好特殊食品安全性监管工作发挥积极的作用。
一新中国成立初期至2015年以前,中国三类特殊食品监管体系经历了混合过渡阶段,各自在阵痛中不断完成自我成长01 保健食品1 保健食品制度的确立(1)新中国成立初期国家经济委员会在协同劳动部对从事有毒有害、高温、井下作业工人的保健食品和矿山工人的粮食、营养补助食品的供应情况进行调查研究的基础上, 于1963年3 月向国务院总理写了《关于从事有毒有害、高温、井下作业工人的食品供应情况和意见的报告》, 国务院以国经周字216 号文件批转了这个报告 [2]。
根据此文件, 原劳动部、原卫生部等七部门于1963 年7 月19 日联合发布了《关于贯彻国务院批转国家经济委员会报告实行保健食品制度的联合通知》, 据此, 我国正式建立保健食品制度。
食品标签瑕疵不影响食品安全 且不会对消费者造成误导的不适用惩罚性赔偿

食品标签瑕疵不影响食品安全且不会对消费者造成误导的不适用惩罚性赔偿——淡小龙诉天虹商场股份有限公司等买卖合同纠纷案要点提示:消费者依据《中华人民共和国食品安全法》及相关司法解释的规定向食品经营者主张价款十倍的惩罚性赔偿,须以食品经营者存在销售明知是不符合食品安全标准的食品的违法行为为前提。
食品标签存在瑕疵,但不影响食品安全亦不会对消费者造成误导的,消费者据此主张价款十倍的惩罚性赔偿,不予支持。
案例索引:一审:深圳市龙岗区人民法院(2016)粤0307民初3224号。
二审:深圳市中级人民法院(2016)粤03民终9669号。
申诉:广东省高级人民法院(2016)粤民申5816号。
一、案情再审申请人(一审原告、二审上诉人):淡小龙。
被申请人(一审被告、二审被上诉人):天虹商场股份有限公司。
(以下简称“天虹公司”)被申请人(一审被告、二审被上诉人):天虹商场股份有限公司坂田天虹商场。
(以下简称“天虹坂田商场”)淡小龙诉称,2016年1月9日其在天虹坂田商场处购买到菇品世家虫草花70包,单价25.8元,共计价款1806元。
购买后查询相关文件(关于批准塔格糖等6种新食品原料的公告(2014年第10号)及(2009年第3号)发现蛹虫草是新资源食品,婴幼儿及儿童食用后对少年儿童可能导致早熟,因此儿童不宜服用。
该产品未按要求标示出不适宜人群及食用量,应为不安全食品,具有重大食品安全隐患。
上述产品违反《中华人民共和国产品质量法》第二十七条第一款第五项及《中华人民共和国食品安全法》第六十七条第九项规定,天虹坂田商场作为销售商在履行了《中华人民共和国产品质量法》第三十三条后应当知道所售商品是否符合国家标准。
天虹坂田商场的行为严重侵犯了包括原告在内的广大消费者的合法权益,给原告造成了严重的经济损失,淡小龙请求判令天虹公司、天虹坂田商场退还淡小龙购物款1806元、赔偿十倍货款18060元。
天虹公司、天虹坂田商场辩称,其销售的产品来源合法、质量合格且已尽到合理审查义务。
2010年卫生部关于【基础护理三个文件】

卫生部文件卫生部关于印发《住院患者基础护理服务项目(试行)》等三个文件的通知(卫医政发〔2010〕9号)各省、自治区、直辖市卫生厅局,新疆生产建设兵团卫生局:为进一步加强医院临床护理工作,规范护理行为,落实基础护理,改善护理服务,保证护理质量,我部组织制定了《住院患者基础护理服务项目(试行)》、《基础护理服务工作规范》和《常用临床护理技术服务规范》。
现印发给你们,请遵照执行。
附件:1.住院患者基础护理服务项目2.基础护理服务工作规范3.常用临床护理技术服务规范二0一0年一月二十二日住院患者基础护理服务项目(试行)一、特级护理二、一级护理三、二级护理四、三级护理基础护理服务工作规范一、整理床单位(一)工作目标。
保持床单位清洁,增进患者舒适。
(二)工作规范要点。
1.遵循标准预防、节力、安全的原则。
2.告知患者,做好准备。
根据患者的病情、年龄、体重、意识、活动和合作能力,有无引流管、伤口,有无大小便失禁等,采用与病情相符的整理床单位的方法。
3.按需要准备用物及环境,保护患者隐私。
4.护士协助活动不便的患者翻身或下床,采用湿扫法清洁并整理床单位。
5.操作过程中,注意避免引流管或导管牵拉,密切观察患者病情,发现异常及时处理。
与患者沟通,了解其感受及需求,保证患者安全。
6.操作后对躁动、易发生坠床的患者拉好床栏或者采取其他安全措施,帮助患者采取舒适体位。
7.按操作规程更换污染的床单位。
(三)结果标准。
1.患者/家属能够知晓护士告知的事项,对服务满意。
2.床单位整洁,患者卧位舒适、符合病情要求。
3.操作过程规范、准确,患者安全。
二、面部清洁和梳头(一)工作目标。
使患者面部清洁、头发整洁,感觉舒适。
(二)工作规范要点。
1.遵循节力、安全的原则。
2.告知患者,做好准备。
根据患者的病情、意识、生活自理能力及个人卫生习惯,选择实施面部清洁和梳头的时间。
3.按需要准备用物。
4.协助患者取舒适体位,嘱患者若有不适告知护士。
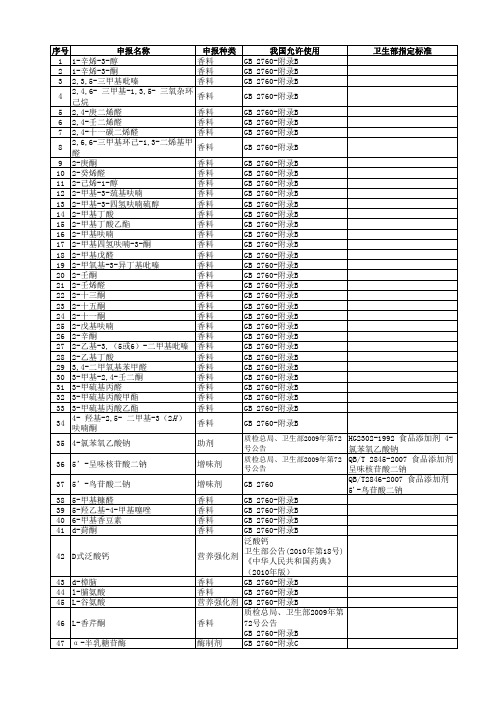
《食品安全法实施前已有进口记录但尚无食品安全国家标准的食品添加剂目录》
GB 2760-附录B
环糊精葡萄糖苷转移酶(生产用菌 137 株:地衣芽孢杆菌Bacillus licheniformis 138 黄葵籽油 139 茴香醇 140 活性炭 141 肌醇 142 己醛 143 己酸烯丙酯 144 己酸乙酯 145 甲基环戊烯醇酮 146 甲基纤维素 147 甲硫醇 148 间甲酚 149 姜黄 150 姜油(生姜油) 151 椒样薄荷油 152 菊花黄浸膏 153 聚苯乙烯 154 聚甘油聚亚油酸酯 155 聚氧乙烯木糖醇酐单硬脂酸酯 156 157 158 159 聚异丁烯 糠醇 糠基甲基硫醚 可可酊
卫生部指定标准
GB 2760-附录B
质检总局、卫生部2009年第72 号公告 质检总局、卫生部2009年第72 号公告
GB 2760
HG2302-1992 食品添加剂 4氯苯氧乙酸钠 QB/T 2845-2007 食品添加剂 呈味核苷酸二钠 QB/T2846-2007 食品添加剂 5'-鸟苷酸二钠
42 D式泛酸钙 43 d-樟脑 44 l-脯氨酸 45 L-谷氨酸 46 L-香芹酮 47 α -半乳糖苷酶
质检总局、卫生部2009年第72 QB2078-1995 食品添加剂 甘 号公告 草抗氧物 GB 2760
120 甘草酸一钾及三钾 121 甘牛至油 122 格蓬油 123 庚醛 124 瓜尔胶 125 广藿香油 126 硅胶 127 硅酸钙 128 果胶酶 129 过氧化氢酶 130 海藻提取物 131 核苷酸 132 黑豆红 133 黑胡椒油 134 红茶酊 135 红花黄 136 胡萝卜籽油
序号1申报名称申报种类香料香料香料我国允许使用卫生部指定标准1辛烯3醇1辛烯3酮235三甲基吡嗪246三甲基135三氧杂环己烷24庚二烯醛24壬二烯醛24十一碳二烯醛266三甲基环己13二烯基甲醛2庚酮2癸烯醛2己烯1醇2甲基3巯基呋喃2甲基3四氢呋喃硫醇2甲基丁酸2甲基丁酸乙酯2甲基呋喃2甲基四氢呋喃3酮2甲基戊醛2甲氧基3异丁基吡嗪2壬酮2壬烯醛2十三酮2十五酮2十一酮2戊基呋喃2辛酮2乙基35或6二甲基吡嗪2乙基丁酸34二甲氧基苯甲醛3甲基24壬二酮3甲硫基丙醛3甲硫基丙酸甲酯3甲硫基丙酸乙酯4羟基25二甲基32h呋喃酮gb2760附录bgb2760附录bgb2760附录b234香料gb2760附录b56香料香料香料gb2760附录bgb2760附录bgb2760附录b78香料gb2760附录b9香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料香料gb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录bgb2760附录b10111213141516171819202122232425262728293031323334香料gb2760附录b354氯苯氧乙酸钠助剂质检总局卫生部2009年第72号公告hg23021992食品添加剂4氯苯氧乙酸钠qbt28452007食品添加剂呈味核苷酸二钠qbt28462007食品添加剂5鸟苷酸二钠365呈味核苷酸二钠增味剂质检总局卫生部2009年第72号公告375鸟苷酸二钠增味剂gb27603839405甲基糠醛5羟乙基4甲基噻唑6甲基香豆素d葑酮香料香料香料香料gb2760附录bgb2760附录bgb2760附录bgb2760附录b泛酸钙卫生部公告2010年第18号中华人民共和国药典2010年版gb2760附录bgb2760附录b营养强化剂gb2760附录b质检总局卫生部2009年第72号公告gb2760附录b酶制剂gb2760附录c4142d式泛酸钙营养强
无菌医疗器械法律法规清单

2011.9.16 2011.12.1 2011.1.1 2011.1.1 2000.9.1 1989.4.1 2002.5.29 1999.10.1 2006.1.1 2003.6.17 2007.6.15
关于发布自测用血糖监测系统注册申报资料指导原则的通知 2010.10.18 关于医疗器械产品生产许可证管理工作中有关问题的通知 安全生产许可证条例 关于印发《境内第三类和进口医疗器械注册文件受理标准》 的通知 2002版《医疗器械分类目录》 《医疗器械注册产品标准编写规范》 关于医疗器械产品注册后说明书更改备案有关事项的公告 关于执行《医疗器械生产监督管理办法》有关问题的通知 《〈医疗器械生产企业许可证〉审批操作规范》 关于发布第一批禁止委托生产的医疗器械目录的通知 关于公布第一批不需申请《医疗器械经营企业许可证》的第 二类医疗器械产品名录的通知 关于部分医疗器械产品检测有关问题的公告 关于发布境内第三类和境外医疗器械注册审批操作规范的通 告 关于发布医疗器械注册证书补办程序等6个相关工作程序的 通告 关于发布申请注销医疗器械注册证书办理程序的通告 关于医疗器械注册证书变更申请有关事项的通知 关于对部分出口药品和医疗器械生产实施目录管理的通告 1999.12.30 2004.1.7 2002.1.12 2002.8.28 2002.11.7 2004.3.11 2004.10.13 2004.10.27 2005.4.22 2005.5.26 2006.4.30 2007.7.23 2007.8.21 2007.10.22 2007.12.25 2008.10.17 2009.5.20
2011.1.27 2012.2.29 2008.7.23 2007.10.17 2007.7.15 2006.5.29 1993.12.1 2010.4.29 2008.3.26
放射性职业病危害预评价报告

放射性职业病危害预评价报告[公众号:安全生产管理]声明1、XX检测技术服务有限公司遵守国家有关法律、法规,在项目评价过程坚持客观、真实、公正的原则,并对所出具的《建设项目放射性职业病危害评价报告表》承担法律责任。
2、本项目评价工作依据有关职业病防治的法律、法规、规章、标准、规范,及委托单位提供的相关文件进行。
3、委托单位提供的各类文件、证件、工作流程、设备基本情况、防护设施等资料是本次评价的重要依据,委托单位应对所提供资料原件及复印件的真实性负责,如因委托单位提供虚假资料导致评价结果出现偏差,本公司概不负责。
4、本次评价所涉及内容(建设项目地址、工作流程、设备基本情况、防护设施、布局、劳动定员、工作班制等)发生重大变更时,应重新进行评价。
5、本报告无编制人、审核人、签发人签名无效;涂改或未加盖本公司公章无效。
6、本报告各页均为报告不可分割的部分,使用者单独抽出某页而导致的误解或用于其他用途而造成的后果,本公司不承担相应的责任。
7、本公司不对本报告复印件负责。
8、如对评价报告有异议,请于收到本报告之日起十五日内向本公司提出书面意见,过期不再受理。
目录1 概述 (1)1.1 概况及任务来源 (1)1.2 评价目的 (1)1.3 评价范围 (1)1.4 评价内容 (2)1.5 主要评价依据 (2)2 项目概况 (3)3 辐射源项分析 (4)4 职业病危害因素分析 (4)4.1 工作场所平面布局 (4)4.2 危害因素分析 (6)4.3 建设项目分类 (6)5 拟采取的防护措施 (7)5.1 屏蔽 (7)5.2 通风 (8)5.3 警示标志 (8)5.4 个人防护用品 (8)5.5 防放射性污染、三废处理与其他 (9)6 放射防护管理 (9)6.1 防护管理制度 (9)6.2 防护管理人员 (10)6.3 放射工作人员配置 (10)6.4 个人剂量监测 (10)6.5 职业健康检查 (10)6.6 教育培训 (11)6.7 应急准备与响应 (11)6.8 档案管理 (12)7 结论与建议 (12)7.1 结论 (12)7.2 建议 (13)8 附件 (13)附件1:委托书 (14)附件2:医疗机构执业许可证 (14)附件3:放射诊疗许可证 (14)附件4:设备装置列表 (14)附件5:建设项目机房新造方案 (14)附件6:警示标志、通风等防护设施及措施设置方案 (14)附件7:建设项目防护用品配备方案 (14)附件8:人员配备计划 (15)附件9:工作场所分区 (16)附件10:放射防护管理组织 (16)附件11:放射事件应急处理预案 (16)附件12:制度汇编 (16)附件1:委托书附件2:医疗机构执业许可证附件3:放射诊疗许可证附件4:设备装置列表附件5:建设项目机房新造方案附件6:警示标志、通风等防护设施及措施设置方案附件7:建设项目防护用品配备方案附件8:人员配备计划XX市XX医院数字化医用X射线摄影系统建设项目人员配置方案1、为顺利开展医用影像诊断工作,依据相关要求,我院拟为CT建设项目配置如下工作人员:2、为了维护放射工作人员的合法权益和保持放射工作人员的身体健康,上述放射工作人员要在职业健康体检结果显示无职业禁忌症后,同时取得放射卫生法律和防护培训合格证,方可上岗。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2006-2008年深圳市水产品污染状况分析———王
舟黄薇潘柳波等—167—
表2
2006年深圳市贝类毒素检测结果
样品名称生物法
试剂盒
麻痹性毒素
(MU /g )腹泻性毒素(MU /g )
麻痹性毒素
(ng /g )
腹泻性毒素(ng /g )鲍鱼<0.875--18.27海螺<0.875--28.27花蛤-- 3.8982.43扇贝--19.8557.14花甲<0.875--28.72象牙蚌<0.875--未检出鲍鱼仔
-
-
9.48
72.87
注:0.875MU /g 为该方法检出限;“-”为未检测。
表32007-2008年深圳市淡水水产品肝吸虫囊幼检测结果
鱼种2007年
2008年
检测份数阳性份数阳性率
(%)检测份数阳性份数
阳性率(%)鲩鱼13430.771218.33鲫鱼12216.671317.69大头鱼14214.291218.33鲤鱼15213.331100福寿鱼2129.5214428.57生鱼130011218.18乌头鱼1200---
桂花鱼12001000鲢鱼9005120.00鲮鱼---100鲈鱼---100鲶鱼---100塘虱鱼---100合计
121
12
9.92
92
10
10.87注:“-”为未检测。
3讨论
从3年的监测数据来看,深圳市的水产品均存
在不同程度的污染,主要污染项目为副溶血性弧菌、铅和亚硝酸盐。
副溶血性弧菌存在于水体,是水产品引起食物中毒的主要致病菌,在微生物引起的食
物中毒中,副溶血性弧菌居各种病因之首[4]。
水产
品中铅污染是由于铅在水体和沉积物中积聚所致。
深圳地区水网众多,人们素有吃鱼生的习惯,肝吸虫囊蚴存在于淡水鱼虾中,人群肝吸虫感染率与生食鱼生有直接关系[5]
,不洁鱼生也是引发食物中
毒的诱因之一
[6]。
为了遏制肝吸虫病的抬头趋势,
提高广大市民的健康水平,应当从防治两方面着手。
首先是“防”,通过宣传,让广大市民了解肝吸虫病的流行病学知识,
坚决不吃鱼生、未煮熟的淡水虾及鱼片粥等食物,防患于未然;其次是“治”,对于已发现肝吸虫抗体阳性的人群,建议积极做病原学检查,根据检查结果做相应的治疗,避免造成更大的伤害。
综上所述,为防止食源性疾病的发生,水产品应煮熟煮透后方可进食。
加强卫生处理,对水产品清洗、盐渍、冷藏、运输应严格按卫生规定管理。
参考文献
[1]李泽瑶.水产品安全质量控制与检验检疫手册[M ].北京:企
业管理出版社,
2003.[2]OSHIMA Y.
Post-column derivatization HPLC
methods for
paralyticshellfish poisons [M ]//HALLEGRAEFF G M.Mannual on Harmful MarineMicroalgae.Paris :UNESO ’s Workshops ,
1995:81-94.
[3]郑云雁.食品中污染物的中国国家标准及国际法典标准对比
(一)化学污染物[J ].中国食品卫生杂志,2002,14(1):47-53.
[4]刘秀梅,陈艳,王晓英,等.1992-2001年食源性疾病暴发资
料分析-国家食源性疾病监测网[J ].卫生研究,2004,33(6):725-73.
[5]刘小宁,冯月菊,任文锋,等.华支睾吸虫病流行区流行病学研
究[J ]
.热带医学杂志,2003,3(4):404-406.[6]陈炳卿,刘志诚,王茂起.现代食品卫生学[M ]
.北京:人民卫生出版社,2001:檪檪檪檪檪檪檪檪檪檪檪檪殏
殏
殏
殏
777-
779.公告栏
中华人民共和国卫生部公告
2010年
第3号
根据《中华人民共和国食品安全法》和《新资源食品管理办法》的规定,现批准DHA 藻油、棉籽低聚糖、
植物甾醇、植物甾醇酯、花生四烯酸油脂、白子菜、御米油等7种物品为新资源食品,允许玫瑰花(重瓣红玫瑰Rose rugosa cv.Plena )、
凉粉草(仙草Mesona chinensis Benth.)作为普通食品生产经营,允许夏枯草(Prunella vulgaris L.)、布渣叶(破布叶Microcos paniculata L.)、鸡蛋花(Plumeria rubra L.cv.Acutifolia )作为凉茶饮料原料使用。
生产经营上述食品应当符合有关法律、
法规、标准规定。
特此公告。
附件:7种新资源食品目录(略)
二○一○年三月九日。
