大学化学课件-国外原版教材-5
College Chemistry Chapter 04

Lead box Gold foil
Tro's "Introductory Chemistry", Chapter 4
Fluorescent screen
15
Rutherford’s Results
• Over 98% of the a particles went straight through. • About 2% of the a particles went through, but were deflected by large angles. • About 0.01% of the a particles bounced off the gold foil.
―...As if you fired a 15‖-canon shell at a piece of tissue paper and it came back and hit you.‖
Tro's "Introductory Chemistry", Chapter 4 16
Rutherford’s Conclusions
Tro's "Introductory Chemistry", Chapter 4 9
The Atom Is Divisible
• Work done by J. J. Thomson and others proved that the atom had pieces called electrons. • Thomson found that electrons are much smaller than atoms and carry a negative charge.
1. Each Element is composed of tiny, indestructible particles called atoms.
2019精品美国著名大学课件化学

University of Cambridge
The University of Cambridge, one of the world's top ten universities, was set up in 1209. It is located in the scenic town of Cambridge. It has been called "the city, the university". Although it was imbued with a strong academic atmosphere here, it's still a fastpaced and modern city with the bustling commercial life, and without losing the typical rural scenery of England.
The Famous University in UK
Contents
University of Oxford University of Cambridge University of Birmingham Durham University
Name: University of Oxford Motto: Dominus illuminatio mea President:Andrew Hamilton Area:Oxford in England
University of Cambridge
University of Cambridge
The Cambridge University is a public research University .It is the second-oldest University in both England and the English-speaking world, and the seventh-oldest globally. The university’s name comes from the Latinized from of Cambridge.
化学选修5第一章全课件-PPT

环状化合物
(含有碳原子组成的环状结构)
芳香化合物
OH (含苯环)
树状分类法!
4
练习:按碳的骨架分类:
1、正丁烷
2、正丁醇
OH
3、环戊烷
4、 环己醇
链状化合物___1_、___2____。 环状化合物_3_、___4__, 它们为环状化合物中的_脂___环___化合物。
5
OH
5、环戊烷 6、环辛炔 7、环己醇
(E) C-C ∣
C
(B)
∣
C-C -C
பைடு நூலகம்
CC (D) ∣ ∣
C- C
(F) C - C- C ∣
C
C
C-C
(G)
∣
C- C
(H)
C- C ∣∣
CC
49
下列命名中正确的是( C ) A、3-甲基丁烷 B、3-异丙基己烷 C、2,2,4,4-四甲基辛烷 D、1,1,3-三甲基戊烷。
50
练习2:写出下列烯烃或炔烃同分异构体并命名
其中_____无_____为环状化合物中的脂环化合物, 其中__1_0_-_-_1_2___为环状化合物中的芳香化合物。
7
大家应该也有点累了,稍作休息
大家有疑问的,可以询问和交流
8
下列三种物质有何区别与联系? A芳香化合物: 含有苯环的化合物
B芳香烃: 含有苯环的烃。
C苯的同系物:有一个苯环,环上侧链全为烷烃基 的芳香烃。
—OH —COOH
⑧
⑨
—OH
⑩
—CH3 —CH3
CH3 —C—CH3
CH3
10
2、按官能团进行分类。
烃的衍生物: P4 烃分子里的氢原子可以被其他原子
有机化学英文课件chapter6-78页PPT资料

Electrophilic Additions
• hydrohalogenation using HCl, HBr, HI • hydration using H2O in the presence of H2SO4 • halogenation using Cl2, Br2 • halohydrination using HOCl, HOBr • oxymercuration using Hg(OAc)2, H2O followed by
M acintosh PICT im age form at is not supported
6-2
Characteristic Reactions
M acin to sh P IC T im ag e fo rm at
is n o t su p p o rted
6-3
Characteristic Reactions
u Heat of reaction, DH0: the difference in enthalpy between reactants and products
• exothermic reaction: a reaction in which the enthalpy of the products is lower than that of the reactants; a reaction in which heat is released
u Addition is regioselective
• regioselective reaction: an addition or substitution reaction in which one of two or more possible products is formed in preference to all others that might be formed
大学化学课件-国外原版教材-3

Metathesis Reactions
Metathesis reactions involve swapping ions in solution: AX + BY AY + BX. Metathesis reactions will lead to a change in solution if one of three things occurs:
Copyright 1999, PRENTICE HALL
Chapter 4
4
Properties of Solutes in Aqueous Solution
Strong and Weak Electrolytes
Strong electrolytes: completely dissociate in solution. For example:
Copyright 1999, PRENTICE HALL Chapter 4 10
Acids, Bases, and Salts
Strong and Weak Acids and Bases
Strong acids and bases are strong electrolytes.
They are completely ionized in solution.
Copyright 1999, PRENTICE HALL
Chapter 4
12
Acids, Bases, and Salts
Strong and Weak Acids and Bases
Copyright 1999, PRENTICE HALL
国外大学部分现用教材及教学参考书
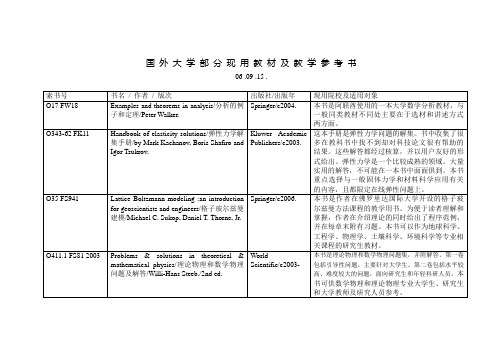
Introductory quantum optics/量子光学介绍/Christopher Gerry, Peter Knight.
CambridgeUniversityPress/c2005.
本书是一本高水平的量子光学的基础著作。主要介绍了光的量子力学本质和光与物质的相互作用,以及量子化的电磁场。
World Scientific/c1999
本书为新加坡世界科技出版公司出版的理论和实验物理学院的讲义:粒子物理学和场理论的第一卷。这套丛书是为高年级大学生和研究生写的,内容既全面又丰富,是这方面的一种重要著作。
O413 FP87
Scattering and structures :essentials and analogies in quantum physics/散射和结构:量子物理学中的要点和相似性/Bogdan Povh, Mitja Rosina ; translated by Martin Lavelle.
TN911.2 FS17
Coding for data and computer communications/用于数据与计算机通信的编码/David Salomon.
Springer/c2005.
本书特点为:1.对编码领域提供了全面的报道,特别强调了数字编码的实用性;2.提供了大量的实例和附有答案的练习来帮助读者容易地掌握本书的内容;3.包括有关数据隐藏的一个扩大的章节;4.包括支持本书的具有补充材料的网站;5.详尽的参考文献、有用的术语汇编、索引及附录。
O343-62 FK11
Handbook of elasticity solutions/弹性力学解集手册/by Mark Kachanov, Boris Shafiro and Igor Tsukrov.
适用于大学双语有机教学的原版教材——Organic Chemistry-Structure and Function

宋怡
双语 教材开发和建设 的滞后 已经成为制 约我 国高校双语教学发展 的客观瓶颈之一. 当前 的主要对策是选择 原版英 文教 材 ,O r g a n i c c h e m i s t r y — s t mc t u r e a n d F u n c t i o n 是一本优 秀的原 版大学 有机化学教材. 1 内容简介 表 1 章节 内容及 t ・ 化学热点”部分 内 容 一览表 《 有机化学—— 结构与功能 》 是 一本适 节 内容 化 学热点 有机分子的结构和其中的化学键 l 一 1 糖 :最古老的人工合成有机化合 用 于化学及 生 物医学 等专 业 的基 础 有机 化 l 学教材.该教材对有机化学基础 知识 进行 了 2 烷烃 :不 舍官 能 团的有 机 分子 较为全面的整合 , 以官 能团为 主线贯 穿体 系 4 脂环 烃 结构 , 突出强调 了构效关 系和有 机合 成的重 5 立体 化学
需要什么信息 ;P : ( p r o c e e d ) 如 何有逻辑地解题.( 3 ) 制作化学 反应路径 图 , 提供 了各 官能 团相关化学反应 ,以及 官能团 之 间相互转化 的途径 , 促进学生形成合成方 法的概念 图. ( 4 ) 色彩运用 目的性强 , 帮助学生进行 概念 辨析 .主官能团和其他 基团间 ,光谱特征 和具体 官能团结 构间 ,反应机理 中亲核基 团、亲 电基 团、 自由基 和离去基 团等都有明显的颜色区别 .( 5 ) 配套学习软件功能强 大 , 包括学习指南 、 网络试题库 、 探究实验 、 有机分子 的三维动画 , 光谱软件和多媒体课件等学习模块. 2 . 3 面向真 实世界 第 6版更 注重将 化学概 念应用 于真实情境 , 在 每章 的导言中提出了一些与学生 日 常生活经验相联系的 问题.强调有机 化学在生 物医学和工业 的应 用.如第五章手 性药物及 自然界的手性 ; 第 九章 聚乙烯及其医疗用途等.融入了 有机化学在生命科学 、 工业生 产 、 绿色化学和环境检测与治理方面的新应用.如介绍 了有机化学在生命科学 、工业生产 、 环 境监控和治理方面的新应用 ,将概念学习和科学 实践 相联 系 ,有利 于激发学生的兴趣 和成 功愿望. 综 上所述 , 选 用教材 时 , 建议 以国 内优秀教材为主线 , 同时融入原版教材 的内容与特点 , 中英 文教材 并用 , 在提 高学生 专业英语水 平的同时 ,能有效避 免学科 损伤 的出现.
化学原理Chemistry英文课件thermochemistry

C (s, graphite) + O2 (g) = CO2 (g) DHrxn0 = - 393.5 kJ Then, DHf0(CO2, g) = - 393.5 kJ/mol
i.e. DHfo = 0 for any element in its most stable form.
DH0f (O2, g) = 0
The standard enthalpy of reaction carried out at 1 atm.
System is the specific part of the universe that is of interest in the study.
Open system closed system Isolated system
mass & energy exchanged
only energy exchanged
How much heat is evolved when 266 g of white phosphorus (P4) burn in air?
P4 (s) + 5O2 (g)
P4O10 (s) DH = -3013 kJ
266 g P4
x
1 mol P4 123.9 g P4
x
3013 kJ 1 mol P4
w = -14 L•atm x
101.3 J 1L•atm
=
-1400
J
DE = q + w
(1)At constant volume
DV = 0, w =0
DE = qv
At constant volume, the heat adsorbed or released to its surrounding is totally used to increase or decrease the system internal energy.
《OrganicChemistry—StructureandFunction》——

《Organic Chemistry—Structure and Function》——一本适用于大学双语有机教学的原版教材宋怡(南京市北圩路41号 210017 南京晓庄学院化学系)摘要:教材问题已经成为制约我国双语教学发展的客观瓶颈之一。
本文介绍了一本适用于大学双语有机教学的优秀原版教材,希望能够为解决双语有机配套教材匮乏的问题提供一些有用的信息。
双语教学实践正在我国如火如荼的开展,而配套教材匮乏已经成为制约双语教学健康发展的客观瓶颈之一。
当前的主要对策是引进外国原版教材。
我们向大家推荐其中一本优秀的原版大学有机化学教材。
1 内容简介《有机化学——结构与功能》(Organic Chemistry—Structure and Function ,K.Peter C.V ollhardt, Neil E. Schore编,第三版,New Y ork W.H.Freeman and Company 2000年出版)是一本适用于化学及生物医学等专业的基础有机化学教材。
该教材对有机化学基础知识进行了较为全面的整合,以官能团为主线贯穿体系结构,突出强调了构效关系和有机合成的重要地位。
全书篇幅较长,共分26章。
每一章除主要内容外还包括以下几个单元:Chemical Highlight:与本章节内容相关的扩展资料Chapter Integration Problem:本章综合例题及解答New Reaction:本章新涉及的化学反应Reaction Summary Road Map:化学反应总结而成的路径图Important Concepts:重要概念总结Problem:本章习题章节内容及Chemical Highlight部分内容一览表2 特点分析2.1整体突出构效关系许多学生把有机看作是大量的令人望而生畏的知识点,要消除这种误解,帮助学生学习和理解有机化学,最佳途径是给学生提供一个知识的框架,学生能够围绕该框架组织自己的知识点。
化学人教选修5新导学课件第一章认识有机化合物第4节第2课时(49张)

2.核磁共振氢谱 根据核磁共振氢谱可以确定有机物分子中含
有的氢原子的乙数醇 目及类型。 甲醚 例如:乙醇和甲醚的核磁共振氢谱比较
核磁共
振氢谱
结论
氢原子类型=吸收峰数目=3 不同氢原子的个数之比=不同吸 收峰的面积之比=2﹕1﹕3
氢原子类型=吸收峰数目=1 只有一种类型的氢原子
(2典01例62·济南高二检测)化合物A的相对分子 质量为136,分子式为C8H8O2。A分子中只 含一个苯环且苯环上只有一个取代基,其
终是有机元素分析仪器的领导者和前驱者, 那么现代化的元素分析仪有什么作用呢?
课前新知预习
一、元素分析与相对分子质量的测定
1.元素分析: (1)定性分析:确定有机物的元素组成。CO2 用化H2学O 方法鉴定N2 有机物的元SO2素组成。如燃烧
后,一般碳生成_________、氢生成 _________、氮生成_________、最简硫整数生比成 实_验_式_______、Cl生成HCl。 (2)定量分析:确定有机物的实验式。
规律方法指导:(1)有机物完全燃烧后产物只 有CO2和H2O,不能错误判断有机物只含碳、 氢两种元素,还可能含氧元素。
(2)大多数有机物的实验式和分子式是不同的, 但个别有机物的实验式和分子式相同,如 乙醇(C2H6O),甲烷(CH4)等。
〔变式训练1〕(2017·重庆一中期末)某烃分 子的不饱和度为C5,分子内的碳原子数为8。 该烃的分子式为( )
(4)A 为 乙 醇 可 以 发 生 分 子 内 脱 水 生 成 乙 烯 气 体 , 故 方 程 式 为 : CH3CH2OH―浓17―硫0℃酸→CH2CH2↑+H2O
(5)乙醇与 SOCl2 加热下反应,同时生成二氧化硫和氯化氢两种气体,则该 反应的化学方程式为:
美国化学会综合项目普通化学教材Chemistry

美国化学会项目-普通化学教材Chemistry一,章本教材,分11个主题章。
Chapter 1. Water:A Natural Wonder水:自然奇迹Chapter 2. Aqueous Solutions and Solubility水溶液与溶解性Chapter 3. Origin of Atoms 原子来源Chapter 4. Structure of Atoms原子构造Chapter 5. Structure of molecules分子子构造Chapter 6. Chemical Reactions化学反映Chapter 7. Chemical Energetics:Enthalpy 化学能:焓Chapter 8. Entropy and Molecular Organization 熵与分子构成Chapter 9. Chemical Equilibrium化学平衡Chapter 10:Reduction and Oxidation:Electrochemistry 氧化与还原:电化学Chapter 11. Reaction Pathways 反映途径二,各章内容Chapter 1. Water:A Natural WonderSection 1.1. Phases of Matter物质相Section 1.2. Atomic Models 原子模型Section 1.3. Molecular Models分子模型Section 1.4. Valence Electrons in Molecular Models:Lewis Structures 分子模型中价电子:路易斯构造Reflection and projection 反思与延伸Section 1.5. Arranging Electron Pairs in Three Dimensions 三维排列电子对Section 1.6. Polarity of the Water Molecule水分子极性Reflection and projection 反思与延伸Section 1.7. Why Is Water Liquid at Room Temperature? 室温下水为什么是液体Section 1.8. Further Structural Effects of Hydrogen Bonding in Water水中氢键构造效果Section 1.9. Hydrogen Bonds in Biomolecules生物分子氢键Reflection and projection 反思与延伸Section 1.10. Phase Changes:Liquid to Gas 相变:液体到气体Section 1.11. Counting Molecules:The Mole 数分子:摩尔Reflection and projection 反思与延伸Section 1.12. Specific Heat of Water:Keeping the Earth's Temperature Stable 水热:保持大气温度稳定Section 1.13. Outcomes Review复习Section 1.14. EXTENSION -- Liquid Viscosity扩展-液体粘度Chapter 2. Aqueous Solutions and SolubilitySection 2.1. Substances in Solution溶液中物质Section 2.2. Solutions of Polar Molecules in Water极性分子在水中溶液Reflection and projection 反思与延伸Section 2.3. Characteristics of Solutions of Ionic Compounds in Water离子化合物在水中溶液特点Section 2.4. Formation of Ionic Compounds离子化合物生成Section 2.5. Aqueous Solutions of Ionic Compounds离子化合物水溶液Reflection and projection 反思与延伸Section 2.6. Precipitation Reactions of Ions in Solution溶液中离子沉淀反映Section 2.7. Solubility Rules for Ionic Compounds离子化合物溶度积规则Reflection and projection 反思与延伸Section 2.8. Concentrations and Moles浓度和摩尔Section 2.9. Mass-Mole-Volume Calculations质量-摩尔-体积计算Reflection and projection 反思与延伸Section 2.10. Reaction Stoichiometry in Solutions溶液反映定量关系Reflection and projection 反思与延伸Section 2.11. Solutions of Gases in Water气体溶于水溶液Section 2.12. The Acid-Base Reaction of Water with ItselfSection 2.13. Acids and Bases in Aqueous Solutions酸碱在水溶液中Section 2.14. Stoichiometry of Acid-Base Reactions酸碱反映定量关系Section 2.15. Chemical Reactions of Dissolved Carbon Dioxide溶解二氧化碳化学反映Section 2.16. Outcomes Review复习Section 2.17. EXTENSION -- La Chatelier's PrincipleChapter 3. Origin of AtomsSection 3.1. The Nuclear Atom原子核Section 3.2. Spectroscopy and Stellar Composition光谱和恒星成分Section 3.3. Evolution of the Universe:Stars宇宙进化:恒星Reflection and projection 反思与延伸Section 3.4. Nuclear Reactions核反映Section 3.5. Nuclear Reaction Energies核反映能Reflection and projection 反思与延伸Section 3.6. Cosmic Elemental Abundance and Nuclear Stability宇宙中元素分布量与核稳定性Section 3.7. Formation of Planets:The Earth行星形成:地球Reflection and projection 反思与延伸Section 3.8. Outcomes Review复习Section 3.9. EXTENSION:Isotopes:Age of the Universe and a Taste of Honey扩展-宇宙年龄与蜂蜜味道Chapter 4. Structure of AtomsSection 4.1. Periodicity and the Periodic Table周期性与周期表Section 4.2. Light as a Wave光被看作波Reflection and projection 反思与延伸Section 4.3. Photoelectric Effect:Light as a Particle光电效应:光被看作粒子Reflection and projection 反思与延伸Section 4.4. Why Atomic Spectra Look the Way They Do:Quantum Model of Atoms原子量子模型Section 4.5. If a Wave Can Be a Particle,Can a Particle Be a Wave?如果波能是粒子,粒子可以是波吗?Reflection and projection 反思与延伸Section 4.6. The Wave Model of Electrons in Atoms原子中电子波模型Section 4.7. Energies of Electrons in Atoms:Why Atoms Don't Collapse原子中电子能量:为什么原子不坍陷Reflection and projection 反思与延伸Section 4.8. Multi-electron Atoms:Electron Spin多电子原子:电子自旋Section 4.9. Electron Shells and Periodicity电子壳层和周期性Reflection and projection 反思与延伸Section 4.10. Wave Equations and Atomic Orbitals波方程与原子轨道Section 4.11. Outcomes Review复习Section 4.12. EXTENSION -- Energies of a Spherical Electron Wave扩展-球面电子波能量Chapter 5. Structure of moleculesSection 5.1. Isomers同分异构体Section 5.2. Lewis Structures and Molecular Models of Isomers路易斯构造与同分异构体分子模型Reflection and projection 反思与延伸Section 5.3. Sigma molecular orbitals西格马分子轨道Section 5.4. Sigma Molecular Orbitals and Molecular Geometry西格马分子轨道和分子几何形状Reflection and projection 反思与延伸Section 5.5. Multiple Bonds多重键Section 5.6. Pi Molecular Orbitals派分子轨道Reflection and projection 反思与延伸Section 5.7. Delocalized pi orbitals离域派分子轨道Section 5.8. Representations of Molecular Geometry描绘分子几何形状Reflection and projection 反思与延伸Section 5.9. Stereoisomerism立体异构现象Reflection and projection 反思与延伸Section 5.10. Functional Groups -- Making Life Interesting功能团—使生命有趣Reflection and projection 反思与延伸Section 5.11. Molecular Recognition分子辨认Section 5.12. Outcomes Review复习Section 5.13. EXTENSION -- Antibonding Orbitals:The Oxygen Story扩展-反键轨道:氧故事Chapter 6. Chemical ReactionsSection 6.1. Classifying Chemical Reactions化学反映分类Section 6.2. Ionic Precipitation Reactions离子沉淀反映Reflection and projection 反思与延伸Section 6.3. Lewis Acids and Bases:Definition路易斯酸碱:定义Section 6.4. Lewis Acids and Bases:Bronsted-Lowry Acid-Base Reactions路易斯酸碱:Bronsted-Lowry酸碱反映Reflection and projection 反思与延伸Section 6.5. Predicting Strengths of Lewis/Bronsted-Lowry Bases and Acids测Lewis/Bronsted-Lowry酸碱强度Reflection and projection 反思与延伸Section 6.6. Lewis Acids and Bases:Metal Ion Complexes路易斯酸碱:金属离子络合物Reflection and projection 反思与延伸Section 6.7. Lewis Acids and Bases:Electrophiles and Nucleophiles路易斯酸碱:亲电与亲核Section 6.8. Formal Charge形式电荷Reflection and projection 反思与延伸Section 6.9. Oxidation-Reduction Reactions:Electron Transfer氧化还原反映:电子转移Reflection and projection 反思与延伸Section 6.10. Balancing Oxidation-Reduction Reaction Equations氧化还原反映方程式配平Section 6.11. Oxidation-Reduction Reactions of Carbon-containing Molecules含碳分子氧化还原反映Section 6.12. Outcomes Review复习Section 6.13. EXTENSION -- Titration扩展-滴定Chapter 7. Chemical Energetics:EnthalpySection 7.1. Energy and Change能量和变化Section 7.2. Thermal Energy (Heat) and Mechanical Energy (Work)热能(热)和机械能(功)Section 7.3. Thermal Energy (Heat) Transfer热能(热)传递Reflection and projection 反思与延伸Section 7.4. State Functions and Path Functions状态函数和途径(过程)函数Section 7.5. System and Surroundings体系与环境Reflection and projection 反思与延伸Section 7.6. Calorimetry and Introduction to Enthalpy热量测定和焓简介Reflection and projection 反思与延伸Section 7.7. Bond Enthalpies键焓Reflection and projection 反思与延伸Section 7.8. Standard Enthalpies of Formation原则生成焓Section 7.9. Harnessing Energy in Living Systems生命体系能量运用Reflection and projection 反思与延伸Section 7.10. Enthalpy Revisited再访焓Reflection and projection 反思与延伸Section 7.11. What Enthalpy Doesn't Tell Us焓没告诉咱们Section 7.12. Outcomes Review复习Section 7.13 EXTENSION -- Gases:Pressure-Volume Work扩展-气体:压力体积功Chapter 8. Entropy and Molecular OrganizationSection 8.1. Mixing and Osmosis混合与渗入Section 8.2. Probability and Change也许性与变化Section 8.3. Counting Molecular Arrangements in Mixtures计算混合物分子排列Section 8.4. Implications for Mixing and Osmosis in Macroscopic Systems宏观世界里混合与渗入本质Reflection and projection 反思与延伸Section 8.5. Energy Arrangements Among Molecules分子中能量排布Section 8.6. Entropy熵Reflection and projection 反思与延伸Section 8.7. Phase Changes and Net Entropy相变与净熵Section 8.8. Gibbs Free Energy吉布斯自由能Reflection and projection 反思与延伸Section 8.9. Thermodynamics of Rubber橡胶热力学Section 8.10. Colligative Properties of Solutions溶液依数性Section 8.11. Osmotic Pressure Calculations渗入压计算Reflection and projection 反思与延伸Section 8.12. Thermodynamic Calculations for Chemical Reactions化学反映热力学计算Reflection and projection 反思与延伸Section 8.13. Why Oil and Water Don't Mix为什么油水不混合?Section 8.14. Ambiphilic Molecules:Micelles and Bilayer Membranes两亲分子:胶束和双分子膜Section 8.15. The Cost of Molecular Organization分子堆积代价Section 8.16. Outcomes Review复习Section 8.17. Osmosis and Cell Membranes渗入压与细胞膜Chapter 9. Chemical EquilibriumSection 9.1. The Nature of Equilibrium平衡本质Reflection and projection 反思与延伸Section 9.2. Mathematical Expression for the Equilibrium Condition平衡条件数学表达Section 9.3. Acid-Base Reactions and Equilibria酸碱反映和平衡Reflection and projection 反思与延伸ReSection 9.4. Solutions of Conjugate Acid-Base Pairs:Buffer Solutions共轭酸碱对溶液:缓冲溶液Section 9.5. Acid-Base Properties of Proteins蛋白质酸碱性质Reflection and projection 反思与延伸Section 9.6. Solubility Equilibria for Ionic Salts离子盐溶解平衡Reflection and projection 反思与延伸Section 9.7. Thermodynamics and the Equilibrium Constant热力学与平衡常数Section 9.8. Temperature Dependence of the Equilibrium Constant平衡常数与温度关系Reflection and projection 反思与延伸Section 9.9. Thermodynamics in Living Systems生命体系热力学Section 9.10. Outcomes Review复习Section 9.11. EXTENSION -- Competing Equilibria扩展-平衡竞争Chapter 10:Reduction and Oxidation:ElectrochemistrySection 10.1. Electrolysis 电解Reflection and projection 反思与延伸Section 10.2. Electric Current from Chemical Reactions化学反映电流Section 10.3. Work From Electrochemical Cells电池做功Reflection and projection 反思与延伸Section 10.4. Concentration Dependence of Cell Potentials浓度对电池电势影响Section 10.5. Free Energy and Electrochemical Cells:The Nernst Equation自由能和电化学电池:能斯特方程式Section 10.6. Combining Cell Potentials for ReactionsReflection and projection 反思与延伸Section 10.7. Half-Cell Potentials:Reduction Potentials半电池电势:还原电势Section 10.8. Reduction Potentials and the Nernst Equation还原电势和能斯特方程式Reflection and projection 反思与延伸Section 10.9. Carbon-Containing Reducing Agents:Glucose含碳还原剂:葡萄糖Section 10.10. Coupled Redox Reactions偶联还原反映Reflection and projection 反思与延伸Section 10.11. Outcomes Review复习Section 10.12. EXTENSION -- Cell Potentials and Non-Redox Equilibria扩展-电池电势与非还原平衡Chapter 11. Reaction PathwaysSection 11.1. Pathways of Change途径变化Section 11.2. Measuring and Expressing Rates of Chemical Change测量和表达化学变化速率Reflection and projection 反思与延伸Section 11.3. Reaction Rate Laws反映速率定律Section 11.4. Reaction Pathways or Mechanisms反映途径与机理Reflection and projection 反思与延伸Section 11.5. More Ways to Analyze Rate Data分析速率数据更多方式Reflection and projection 反思与延伸Section 11.6. Temperature and Reaction Rates温度与反映速率Section 11.7. Light:Another Way to Activate a Reaction光:另一种方式活化反映Reflection and projection 反思与延伸Section 11.8 Outcomes Review复习Section 11.9. EXTENSION -- Enzymatic Catalysis扩展-酶催化美国化学会项目-普通化学教材简介周伟红(吉林大学化学学院,长春 130022,)摘要:W.H.Freeman and Company 出版Chemistry,是美国化学会一种项目。
《有机化学》第五版ppt文档全文免费预览

过程。
05
有机化合物的结构与性质
有机化合物的结构表示方法
构造式
用元素符号和短线表示化合物分子中原子的排列和结合方式的式 子。包括分子式、结构式和结构简式。
空间构型
用模型或图形表示有机分子中原子或原子团的相对空间位置。包 括球棍模型、比例模型和空间填充模型。
有机化学与医药科学
01
02
药物合成
有机化学是药物合成的基 础,通过有机合成可以制 备出具有特定药理活性的 药物分子。
药物分析
有机化学方法可用于药物 的质量控制和分析,确保 药物的纯度和有效性。
药物设计与优化
基于有机化学原理,可以 设计和优化药物分子的结 构,提高药物的疗效和降 低副作用。
有机化学与材料科学
反应等。
醇、酚、醚
醇
醇是脂肪烃基与羟基直接相连的有机化合物。根据羟基所连碳原子的类型不同,醇可分为伯 醇、仲醇和叔醇。醇具有亲水性,能与水形成氢键,因此易溶于水。此外,醇还能发生氧化、 酯化、脱水等反应。
酚
酚是芳香烃环上的氢原子被羟基取代的有机化合物。酚具有特殊的芳香气味,微溶于水,易 溶于有机溶剂。酚具有弱酸性,能与碱反应生成盐和水。此外,酚还能发生氧化、取代等反 应。
《有机化学》第五版ppt文档全文 免费预览
• 绪论 • 烃类化合物 • 烃的衍生物 • 有机合成与反应机理 • 有机化合物的结构与性质 • 有机化学在日常生活中的应用
01
绪论
有机化学的研究对象
碳氢化合物
有机功能材料
研究碳氢化合物及其衍生物的结构、 性质、合成和反应机理。
研究具有光、电、磁等特殊功能的有 机材料的设计、合成与应用。
国外化学课件

A hot air balloon rises because
molecules become lighter when heated.
are equal in density to 1981 pennies.
cannot be compared to 1981 pennies
All of the substances on the periodic table are classified as elements because they
the average speed of movement of the individual molecules.
The molecules in a test tube filled with cold water move more slowly than the molecules in a large tank of warm water. What is responsible for this difference in molecule speed?
Cations
H+ Hydrogen Na+ Sodium Mg+2 Magnesium Ca+2 Calcium Ag+1 Silver
mo’ Cations
Fe+2 Iron (II) Ferrous Fe+3 Iron (III) Ferric Cu+1 Copper (I) Cuprous Cu+2 Copper (II) Cupric NH4+ Ammonium
国外大学部分现用教材及教学参考书-清华大学图书馆
06 .12.29.
索书号
书名/作者/版次
出版社/出版年
现用院校及适用对象
C8 FU93m2005
Mind on statistics/统计思想/Jessica M. Utts, Robert F. Heckard./2nd ed./时代教育.国外高校优秀教材精选
机械工业出版社/2005.
本书是经典生物学教材,历经时间考验,已经出版至第十版。本书结构严谨、基础知识丰富、系统性强;篇幅适中、语言生动,尤其适合中国人阅读英文。书中附有全书彩图光盘,方便师生使用。本书在线资源库更加丰富多彩,适合作为高等院校低年级普通生物学双语教材。
Q3 FG325 2003
Genetics :from genes to genomes/遗传学:从基因到基因组/Leland Hartwell ... [et al.]/科学版研究生教学丛书
G206 FL77 2003
Theories of human communication/人类传播学理论/Stephen W. Littlejohn./7th ed./新闻与传播系列教材.英文原版系
TsinghuaUniversityPress/c2003.
美国学者斯蒂芬·小约翰(Stephen W.Littlejohn)的《传播理论》堪称传播学中的一部上乘之作。本书自1978年第一版问世,迄今为止已经出到第七版。本书内容包罗广泛,涉猎渊深。不仅包括对传播研究的基本探讨,而且涉及大量与传播研究有关的思想、理论或学科,比如哲学、语言学、符号学、社会学、心理学、人类学等内容。它帮助学生理解对人类传播进行研究和探讨的多种途径,提供了一种多理论、多学科综合的观点,是新闻与传播学的经典教材。
化学鲁科版选修5 第1章第1节 认识有机化学 课件(67张)

当用系统命名法给烷烃命名时,在“汉字”与“阿拉伯 数 字 ” 而 多 个 位 置 数 字 间 用 “,”分隔。如:2,3,3-三甲基-4-乙基辛烷。
【解析】 ①中最长碳链为 7 个碳原子,应从右端起点 编号,②中最长碳链为 8 个碳原子,应从左端起点编号,③ 中最长碳链为 8 个碳原子,应从右端起点编号,④中最长碳 链为 7 个碳原子,应从左端起点编号。
③写名称:将 取代基 的名称写在烷烃名称的前面,在 取代基前面用阿拉伯数字注明它在烷烃主链上所处的位置, 并用短线“-”将数字与取代基名称隔开。若主链上有 相同 的取代基,可以将取代基合并,用汉字数字表示取代基的个 数,用“,”将表示取代基位置的阿拉伯数字隔开;主链上 有不同的取代基,要把 简单 的写在前面、 复杂 的写在后 面。
有机化学的发展
1.有机化学 (1)定义:以 有机化合物 为研究对象的学科。 (2)研究范围:包括有机化合物的来源、结构、 性质 、 合成、应用,以及有关理论和方法学等。
2.有机化学的发展历程
发展阶段 时代
主要成就和标志
17世纪 生活应用:使用酒、醋、染色植物和草药 物质提取:瑞典化学家 舍勒 提取了酒石酸、柠檬
【答案】 A
烷烃系统命名的步骤和原则
【问题导思】 ①烷烃系统命名的基本步骤有哪些? 【提示】 烷烃系统命名的基本步骤有:①选主链② 定编号③写名称。 ②烷烃命名的基本原则是什么? 【提示】 烷烃命名遵循的五原则是指:①最长②最 近③最多④最小⑤最简。
1.命名步骤
2.烷烃命名的五原则 (1)最长原则:应选最长的碳链作主链; (2)最近原则:应从离支链最近一端对主链碳原子编号; (3)最多原则:若存在多条等长碳链时,应选择含支链较 多的碳链作主链; (4)最小原则:若相同的支链距主链两端等长时,应以支 链位号之和为最小的原则对主链碳原子编号; (5)最简原则:若不同的支链距主链两端等长时,应从靠 近简单支链的一端对主链碳原子编号。
有机化学英文课件chapter5

3. Name substituents 4. Number the carbon, locate and name substituents,
locate the double bond, and name the main chain
M a c in to s h P IC T im a g e fo r m a t
is n o t s u p p o r te d
5-11
Common Names
Despite the precision and universal acceptance of IUPAC nomenclature, some alkenes, particularly low-molecular-weight ones, are known almost exclusively by their common names
5-6
Cis,Trans Isomerism in Alkenes
Cis,trans isomers: isomers that have the same connectivity but a different arrangement of their atoms in space due to the presence of either a ring or a carbon-carbon double bond
• the two carbon atoms of a double bond and the four atoms bonded to them lie in a plane, with bond angles of approximately 120°
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Copyright 1999, PRENTICE HALL
Chapter 5
20
Hess’s Law
In the above enthalpy diagram note that DH1 = DH2 + DH3
Copyright 1999, PRENTICE HALL Chapter 5 21
Enthalpies of Formation
Relating DE to Heat and Work
Copyright 1999, PRENTICE HALL
Chapter 5
9
First Law of Thermodynamics
Endothermic and Exothermic Processes
Endothermic: absorbs heat from the surroundings. Exothermic: transfers heat to the surroundings. An endothermic reaction feels cold. An exothermic reaction feels hot.
Copyright 1999, PRENTICE HALL
Chapter 5
10
First Law of Thermodynamics
State Functions
State function: depends only on the initial and final states of system, not on how the internal energy is used.
Copyright 1999, PRENTICE HALL Chapter 5 6
First Law of Thermodynamics
Relating DE to Heat and Work
Energy cannot be created or destroyed. Energy of (system + surroundings) is constant. Any energy transferred from a system must be transferred to the surroundings (and vice versa). From the first law of thermodynamics:
Copyright 1999, PRENTICE HALL Chapter 5 15
Calorimetry
Heat Capacity and Specific Heat
Copyright 1999, PRENTICE HALL
Chapter 5
16
Calorimetry
Constant-Pressure Calorimetry
From Physics: • Force is a push or pull on an object. • Work is the product of force applied to an object over a distance: w=Fd • Energy is the work done to move an object against a force. • Kinetic energy is the energy of motion:
1J
We sometimes use the calorie instead of the joule: 1 cal = 4.184 J (exactly) A nutritional Calorie: 1 Cal = 1000 cal = 1 kcal
Copyright 1999, PRENTICE HALL Chapter 5 4
when a system undergoes a physical or chemical change, the change in internal energy is given by the heat added to or absorbed by the system plus the work done on or by the system: DE = q + w
• If 1 mol of compound is formed from its constituent elements, then the enthalpy change for the reaction is called the enthalpy of formation, DHof . • Standard conditions (standard state): 1 atm and 25 oC (298 K). • Standard enthalpy, DHo, is the enthalpy measured when everything is in its standard state. • Standard enthalpy of formation: 1 mol of compound is formed from substances in their standard states. • If there is more than one state for a substance under standard conditions, the more stable one is used.
Copyright 1999, PRENTICE HALL
Chapter 5
3
The Nature of Energy
Energy Units
SI Unit for energy is the joule, J: E k 1 mv 2 1 2 kg 1 m/s 2 2 2 2 2 1 kg m / s
Copyright 1999, PRENTICE HALL
Chapter 5
7
First Law of Thermodynamics
Relating DE to Heat and Work
Copyright 1999, PRENTICE HALL
Chapter 5
8
First Law of Thermodynamics
Atmospheric pressure is constant! D H = qP qrxn = -qsoln = -(specific heat of solution) (grams of solution) DT.
Copyright 1999, PRENTICE HALL
Chapter 5
Copyright 1999, PRENTICE HALL
Chapter 5
18
Calorimetry
Bomb Calorimetry (Constant-Volume Calorimetry)
qrxn = -CcalorimeterT.
Copyright 1999, PRENTICE HALL
Chapter 5
Chapter 5
5
First Law of Thermodynamics
Internal Energy
• Internal Energy: total energy of a system. • Cannot measure absolute internal energy. • Change in internal energy, DE = Efinal Einitial
Thermochemistry
David P. White University of North Carolina, Wilmington
Chapter 5
Copyright 1999, PRENTICE HALL Chapter 5 1
The Nature of Energy
Kinetic and Potential Energy
Copyright 1999, PRENTICE HALL
Chapter 5
11
First Law of Thermodynamics
State Functions
Copyright 1999, PRENTICE HALL
Chapter 5
12
Enthalpy
Enthalpy, H: Heat transferred between the system and surroundings carried out under constant pressure. Can only measure the change in enthalpy: DH = Hfinal - Hinitial = qP
Copyright 1999, PRENTICE HALL Chapter 5 14
Calorimetry
Heat Capacity and Specific Heat
Calorimetry = measurement of heat flow. Calorimeter = apparatus that measures heat flow. Heat capacity = the amount of energy required to raise the temperature of an object (by one degree). Molar heat capacity = heat capacity of 1 molific heat capacity = heat capacity of 1 g of a substance. q = (specific heat) (grams of substance) T. Be careful of the sign of q.
2 1 Ek mv 2
Copyright 1999, PRENTICE HALL Chapter 5 2
