盐类水解的应用1
盐类水解的应用及原理

盐类水解的应用及原理1. 应用•盐类水解在食品加工中的应用–调味剂:盐类水解可以增加食品的鲜味,提升口感。
–食品防腐:盐类水解可以抑制食品中细菌的繁殖,延长食品的保质期。
•盐类水解在化妆品中的应用–护肤品:盐类水解可以改善皮肤质地,增加皮肤的保湿性。
–洗发水:盐类水解可以去除头皮屑,并增强发质。
•盐类水解在农业中的应用–作物生长促进:盐类水解可以为作物提供氮、磷、钾等营养元素,促进作物的生长。
–土壤改良:盐类水解可以调节土壤的酸碱度和结构,改良土壤的肥力。
2. 原理盐类水解是指盐类在水中离子化的过程,其中溶解的盐分解成阳离子和阴离子。
盐类在水中水解的原理主要包括以下几个方面:•水的极性:水是一种极性分子,具有正负两极,使得离子能够在水中溶解而发生水解。
•离子间作用力:水中的离子与其他离子或极性分子发生静电作用,增加了离子在水中溶解的可能性。
•晶格能:溶解盐时需要克服盐晶格的结合力,这需要提供一定的能量,使得水解过程变得不可逆。
•水解反应:盐的水解反应使得盐解离成其阳离子和阴离子。
水解反应的速率与盐的溶解度、水的温度和压力等因素有关。
3. 盐类水解的应用案例3.1 食品加工中的应用案例•味精的制备:味精是一种常用的调味品,制备味精需要通过盐类水解,使得谷氨酸钠被水解并形成味精。
•肉类加工中的腌制:盐类水解在肉类加工中的腌制过程中起到调味和防腐的作用,增加肉质的鲜嫩。
•熟食加工中的使用:盐类水解可以加速熟食中的食材的水解和溶解,提高熟食的风味和质量。
3.2 化妆品中的应用案例•护肤品中的使用:盐类水解通过提供皮肤所需的营养物质,有助于保护皮肤和改善皮肤质地。
•洗发水的配方:盐类水解可以通过调节头皮的酸碱度,清洁头皮并去除头皮屑,改善发质。
3.3 农业中的应用案例•土壤改良:通过添加盐类水解制剂到土壤中,可以改善土壤的结构和肥力,促进作物的生长。
•肥料制备:盐类水解可以将肥料中的营养元素分解为可供作物吸收的形式,提高肥料的效率。
盐类水解的应用

对于硝酸铜来说,其水解产物是氢氧化铜,而氢氧化铜是弱碱。因此,蒸干后得到的是氢氧化铜,灼烧后得到氧化铜。
当盐的水解生成强碱时,通常蒸干溶液时可以得到原物质。例如,碳酸钠的水解产物是氢氧化钠,而氢氧化钠是强碱。因此,蒸干后得到的是碳酸钠。
8、判断溶液酸碱性越弱越水解
Kb 次氯酸铵溶液显碱性
化肥的施用
09
PART
铵态氮肥与草木灰不能混用
铵态氮肥不能与草木灰(K2CO3)混用,因为草木灰中的碳酸根离子与铵根离子双水解反应,生成氨气把氮元素跑掉,从而降低肥效。
9、化肥的施用
THANKS
感谢观看
保存FeSO4溶液:保存FeSO4溶液时,需加H2SO4抑制Fe2+水解,并加Fe防止Fe2+被氧化。
保存Na2CO3溶液:保存Na2CO3溶液时,不用磨口玻璃塞,因为Na2CO3溶液水解显碱性,会与SiO2反应生成黏合剂Na2SiO3。
保存NaF溶液:保存NaF溶液时,不能用玻璃瓶,因为NaF会水解生成HF,HF会与玻璃中的SiO2反应,从而腐蚀玻璃。
钛白粉(TiO2)的制备
制备原理:TiCI4 + (x+2)H2O = TiO2.XH2O + 4HCI
4、无机化合物的制备
盐溶液蒸干所得产物的判断
05
PART
当盐的水解生成难挥发性的强酸时,通常蒸干溶液可以得到原物质。例如硫酸铜溶液的水解产物是氢氧化铜和硫酸,而硫酸是难挥发性酸,因此蒸干后得到的是硫酸铜。
CIO¯水解
6、特殊情况
灭火器原理
06
PART
6、灭火器原理
第三课时 盐类水解的应用(30张)

(3)在空气中操作,空气中有强氧化性物质氧气, 如有还原性,会被氧化
如:Na2SO3等盐在加热蒸干过程中要发生 氧化还原反应,最后得到的固体为Na2SO4。
总结:将溶液经蒸干灼烧,最终所得物质填入下表
AlCl3 FeCl3 CuCl2 MgCl2 Al2(SO4)3 FeCl2 Na2SO3 NaHCO3
1、用纯碱去油污,加热去油污效果好,请用平衡原理 加以解释
纯碱为Na2 CO3 ,水解的离子方程式为:
CO32— + H2O
HCO3— + OH— ,水
解是吸热的,温度高,溶液碱性强,去油
污效果好。
2、用明矾和铁盐可以净化水的原因分析
Al 3+ + 3H2O
Al(OH)3 (胶体) + 3H +
Fe 3+ + 3H2O
原因:NH4Cl+H2O NH3 ·H2O+HCl
Mg+2HCl = MgCl2 + H2↑
HCl消耗,平衡正移, NH3 ·H2O浓度 增大,分解产生NH3
7、判断加热蒸干并灼烧某些盐溶液得到固体产物
(1)将氯化铁溶液蒸干并灼烧得到红综色固体 Fe2O3,结合化学用语和适当的文字加以解释。
原因: FeCl3+ 3H2O
HCl
8、MgCl2稀溶液得到无水MgCl2固体(分两步) 第一步:加热、浓缩、冷却、结晶、过滤
得到: MgCl2 ·6H2O
第二步:MgCl2 ·6H2O在干燥的HCl的气流中加热
MgCl2 + 2H2O
Mg(OH)2 + 2HCl
HCl
HCl的作用:将生成水带走,
生活中盐类水解的应用

【应用二】泡沫灭火剂
塑料筒里面放入的是什 么药品?
外筒放入的是什么药品?
【应用二】泡沫灭火剂
药品:塑料内筒放Al2(SO4)3溶液、 铁质外筒放NaHCO3溶液
Al3++3H2O
Al(OH)3+3H+,
HCO3-+H2O
H2CO3 +OH-,
H++ OH-
H2O
总式:Al3++3HCO3- = Al(OH)3↓+3CO2↑
1. 若要配制 FeCl2溶液需要加入(
)D
A、加少量稀盐酸 B、加少量氢氧化钠
C、加少量铁粉 Al3++3H2O
Al(OH)3+3H+,
吸附能力强,可以吸附水里悬浮的杂质,并形成沉淀,
D、加少量稀盐酸 和铁粉
科学使用化肥,是农作物高产的有利保证,为了同时对农作物施用分别含N、P、K三种元素的化肥,对于给定的化肥:
HCO3- +OH- (主要),
哪些呈碱性( 哪些呈碱性(
)
硬脂酸(C17H35COOH)是一种一元弱酸
FeCl3溶液Fe3+能发生水解
②)⑤
① FeCl3 ② NaClO ③ (NH4)2SO4
④ AgNO3 ⑤ Na2S ⑥ K2SO4
3.科学使用化肥,是农作物高产的有利保证,为了同时对农作物施用
【应用四】纯碱去污
Na2CO3 俗名:纯碱、苏打
CO32-水解
CO32-+H2O HCO3-+H2O
HCO3- + OH- 正反应吸热 H2CO3 + OH- 正反应吸热
纯碱的去污能力也是由于CO32-水解显弱碱性
盐类水解的应用

盐类水解可以调节食品的酸碱度,如 柠檬酸钠、醋酸钠等,用于改善食品 口感和延长保存时间。
防腐剂
某些盐类可以水解产生酸性或碱性物 质,用于食品保存,如碳酸钠、碳酸 氢钠等。
洗涤剂与清洁剂
01
02
03
肥皂
油脂与氢氧化钠反应生成 肥皂,再通过盐类水解产 生氢氧化钾,使肥皂更加 细腻、易于溶解。
洗衣粉
洗衣粉中的成分如碳酸钠 、硅酸钠等可以水解产生 碱性物质,有助于去除衣 物上的污渍。
石油加工
在石油加工过程中,盐类水解反应可以用于生产各种石油化工产品,如用氢氧化 钠脱硫、用硫酸处理油渣等。
04
盐类水解在环境保护领域的应 用
水处理与废水处理
硬水软化
通过盐类水解反应,可以将硬水中的 钙、镁等离子转化为沉淀物,从而降 低水的硬度,使其更适合生活和工业 应用。
废水处理
盐类水解可以应用于废水处理中,通 过调节废水pH值,促进某些有毒物质 的沉淀和去除,提高废水处理效率。
冶金工业
提取金属
通过盐类水解反应,可以将矿石 中的金属元素提取出来,如用硫 酸铜溶液浸出铜矿中的铜。
金属表面处理
盐类水解反应可以用于金属表面 处理,如镀锌、镀铬等,提高金 属的耐腐蚀性和耐磨性。
石油化工
石油开采
在石油开采过程中,盐类水解反应可以用于提高石油采收率,如使用表面活性剂 降低油水界面张力。
盐类水解的原理
盐类水解的原理是中和反应的逆反应,即盐中的酸根离子或碱离子与水电离出 的氢离子或氢氧根离子结合,形成弱酸或弱碱,改变了溶液的酸碱性。
盐类水解的重要性
盐类水解在化学工业中的应用
盐类水解在化学工业中有着广泛的应用,如通过控制溶液的 酸碱性来制备和分离物质,以及在电镀、制药、纺织等行业 中应用。
盐类水解应用的例子

盐类水解应用的例子
盐类水解应用的例子
1. 食用食品:食用盐水解可以提取水溶性营养成分,如维生素、蛋白质、淀粉等,从而制作出更美味的食品。
2. 工业化学:盐类水解可把植物油或动物油中的脂肪和油脂分解成小分子的物质,从而制作润滑剂、漆、清洁剂等产品。
3. 生物工程:盐类水解可分解细胞壁和蛋白质,获取植物细胞和蛋白质的隐藏组分,从而制造植物细胞培养基、基因技术产物等生物制品。
4. 生物酶:盐类水解可分解生物体内的蛋白质,提取活性酶,并掩盖酶的活力,从而制备各种酶制剂、细胞分析剂、实验试剂等产品。
5. 农业:盐类水解可分解植物细胞壁,从而得到植物细胞壁的组分,如有机酸、碳水化物等,从而研制出植物生长调节剂和农药。
- 1 -。
盐类的水解应用

盐类的水解应用1. 哎呀,今天咱们来聊聊盐类水解这个有趣的话题!化学老师总说:"盐类水解就像是化学界的变色龙,能让溶液显现不同的酸碱性,在生活中可有大用处啦!"2. 小明家种花时,妈妈总爱用硫酸铝调节土壤。
老师解释说:"这就是盐类水解的应用啊,硫酸铝遇水后,就像个魔法师,能让土壤变酸,某些花儿就特别喜欢这种环境。
"3. 做豆腐时放的石膏,也是利用盐类水解原理。
张奶奶笑着说:"以前不懂为啥石膏能让豆浆变成豆腐,原来是水解在起作用,就像变魔术一样!"4. 李叔叔家的鱼塘用生石灰调节水质。
"这也是盐类水解的妙用,"化学老师说,"生石灰遇水后就像个清道夫,能调节水质酸碱度,让鱼儿住得舒服。
"5. 化肥里的磷酸铵施到地里,也会发生水解。
农业专家王大叔说:"这就像给庄稼准备了一桌营养大餐,水解后的物质正好被庄稼吸收。
"6. 小红家用明矾洗菜,老师说:"明矾遇水后的水解反应,就像个小警察,能抓住蔬菜里的脏东西。
"7. 制药厂利用碳酸钠水解制取某些药物。
厂里的张工程师说:"这个过程就像是化学界的厨师,把复杂的原料'烹饪'成药物。
"8. 纺织厂用醋酸铝处理布料。
"这是利用醋酸铝水解产生的胶体,"老师解释说,"就像给布料穿上了一件防水衣。
"9. 造纸厂用明矾做纸张增白剂。
小华参观造纸厂时问:"为啥要用明矾啊?"工人师傅说:"明矾水解后就像个画家,能让纸张变得又白又亮。
"10. 食品工业中,碳酸氢钠的水解让面团发松。
面包师傅说:"这就像给面团装了个小气球,让面包松松软软的。
"11. 化妆品中也有盐类水解的应用。
化妆品研发师说:"某些金属盐的水解产物就像天然的护肤品,能调节皮肤的酸碱度。
盐类水解的应用归纳与分析

盐类水解的应用归纳与分析要点一、盐类水解的应用1.某些物质水溶液的配制配制能水解的强酸弱碱盐,通常先将盐溶于相对应的酸中,然后加水稀释至刻度,得到要配制的浓度。
如配制FeCl3溶液:先将FeCl3溶于稀盐酸,再加水冲稀至所需浓度。
配制强碱弱酸盐的水溶液,应加入少量相对应的强碱,抑制弱酸酸根的水解。
如配制硫化钠的水溶液时,应先滴入几滴氢氧化钠,再加水冲稀至所需浓度。
2.某些活泼金属与强酸弱碱盐反应Mg放入NH4Cl、CuCl2、FeCl3溶液中产生氢气。
如:Mg+2NH4+=Mg2++2NH3↑+H2↑3.明矾、三氯化铁等净水Al3++3H 2O Al(OH)3(胶体)+3H+Fe3++3H 2O Fe(OH)3(胶体)+3H+原因:胶体吸附性强,可起净水作用。
4.苏打洗涤去油污CO 32―+H2O HCO3―+OH―,加热,去油污能力增强。
原因:加热,促进CO32―的水解,碱性增强,去油污能力增强。
5.泡沫灭火器原理成分:NaHCO3、Al2(SO4)3NaHCO 3水解:HCO3―+H2O H2CO3+OH―碱性Al 2(SO4)3水解:Al3++3H2O Al(OH)3+3H+酸性原理:当两盐混合时,氢离子与氢氧根离子结合生成水,双方相互促进水解:Al3++3HCO3―=Al(OH)3↓+3CO2↑6.施用化肥普钙[Ca(H2PO4)2]、铵态氮肥不能与草木灰(K2CO3)混用原因:K 2CO3水解显碱性:CO32―+H2O HCO3―+OH―3Ca(H2PO4)2+12OH―=Ca3(PO4)2↓+12H2O+4PO43―NH4++OH-=NH3↑+H2O 降低肥效7.判断物质水溶液的酸碱性的大小。
(1)相同物质的量浓度的物质的溶液pH由大到小的判断:相同阳离子时,阴离子对应的酸的酸性越弱,盐越易水解,pH越大;相同阴离子时,阳离子对应的碱的碱性越弱,盐越易水解,pH越小。
如Na2SiO3、Na2CO3、NaHCO3、NaCl、NH4Cl,pH越来越小。
高中化学 盐类水解的应用

2.在化学实验中的应用 (2)某些物质水溶液的配制 ②配制强碱弱酸盐溶液时,需在水中加入少量相应的强碱溶液,可抑制弱酸根离子的水解。 如何配制Na2CO3、K2S溶液呢? (3)试剂的贮存 例:Na2CO3、Na2SiO3、NaF等强碱弱酸盐能否贮存于玻塞试剂瓶中?为什么? (4)判断溶液中离子能否大量共存 发生双水解而不能大量共存的离子有:
盐类水解反应的应用
一.盐类水解的综合利用 2.在化学实验中的应用 (1)判断盐溶液的pH大小: ③同类型的盐比较:
对于强酸弱碱盐,其对应弱碱碱性越弱,盐溶液pH越小;
对于强碱弱酸盐,其对应弱酸酸性越弱,盐溶液pH越大; 例题:等浓度的下列溶液pH由大到小的顺序是相同浓度的下 列盐溶液的pH由大到小的顺序为 ②>③>④>① ?
条 1、盐中必须有弱酸根离子或弱碱阳离子
件 2、盐必须溶于水
盐
类
1、弱的程度越大,水解能力越强
的 水
规 2、盐的浓度越小,水解程度越大 律
解
3、温度越高,水解程度越大
特 1、为酸碱中和的逆反应 征 2、水解程度一般微弱
(3)<(1) <(2) <(5) <(4) <(6)
5、混合溶液中各离子浓度大小比较:根据电离程度、水解程度的相对大小分析 (1)分子的电离大于相应离子的水解:①NH4Cl~NH3•H2O、②CH3COOH~CH3COONa 例题:列出在0.1mol/L的NH4Cl和0.1mol/L的NH3•H2O混合溶液中,各离子浓度大小顺序
例析盐类水解的十大应用

例析盐类水解的十大应用
盐类水解是一种重要的化学反应,它可以将盐类分解成其他化合物,并产生一些有用的物质。
盐类水解的十大应用如下:
1、制造食品添加剂:盐类水解可以用来制造食品添加剂,如酸味剂、香料、色素等,以改善食品的口感和外观。
2、制造医药:盐类水解可以用来制造一些药物,如抗生素、抗病毒药物、抗炎药物等,以治疗疾病。
3、制造清洁剂:盐类水解可以用来制造清洁剂,如洗衣粉、洗洁精等,以清洁衣物和家具。
4、制造润滑剂:盐类水解可以用来制造润滑剂,如机油、润滑油等,以润滑机械设备。
5、制造燃料:盐类水解可以用来制造燃料,如汽油、柴油等,以满足人们的能源需求。
6、制造化妆品:盐类水解可以用来制造化妆品,如护肤霜、粉底液等,以改善人们的外观。
7、制造染料:盐类水解可以用来制造染料,如染料、染料等,以染色纺织品。
8、制造纸张:盐类水解可以用来制造纸张,如纸张、纸板等,以满足人们的文具需求。
9、制造精细化工产品:盐类水解可以用来制造精细化工产品,如涂料、油漆等,以改善人们的生活质量。
10、制造环保产品:盐类水解可以用来制造环保产品,如污水处理剂、污水处理设备等,以保护环境。
以上就是盐类水解的十大应用,它们在食品、医药、清洁剂、润滑剂、燃料、化妆品、染料、纸张、精细化工产品和环保产品等方面都有着重要的作用。
盐类水解的应用概念

盐类水解的应用概念盐类水解是指盐类在水中发生水解反应,产生酸性或碱性溶液的过程。
在化学中,盐类是由阳离子和阴离子组成的化合物,当盐类溶解在水中时,阳离子和阴离子会与水分子发生反应,形成酸性或碱性的溶液。
盐类水解在生活和工业中有着广泛的应用,下面将详细介绍盐类水解的应用概念。
1. 盐类水解在生活中的应用:a. 调节酸碱平衡:盐类水解可以用于调节酸碱平衡,例如在烹饪中,我们常常使用食盐(氯化钠)来调味,食盐溶解在水中会产生氯离子和钠离子,氯离子可以与水分子发生水解反应,产生酸性溶液,而钠离子则可以与水分子发生水解反应,产生碱性溶液,从而调节食物的酸碱度。
b. 调节水质:盐类水解可以用于调节水质,例如在游泳池中,我们常常使用氯化钠来消毒水质,氯化钠溶解在水中会产生氯离子和钠离子,氯离子可以与水中的有机物发生反应,起到消毒的作用,从而保证游泳池水的卫生安全。
c. 调节土壤酸碱度:盐类水解可以用于调节土壤的酸碱度,例如在农业中,我们常常使用石灰来调节土壤的酸碱度,石灰溶解在水中会产生氢氧根离子和钙离子,氢氧根离子可以与土壤中的酸性物质发生反应,中和土壤的酸性,从而改善土壤的肥力。
2. 盐类水解在工业中的应用:a. 制备酸碱溶液:盐类水解可以用于制备酸碱溶液,例如在化学实验室中,我们常常使用氯化氢溶液来调节实验的酸碱度,氯化氢溶液是由氯化氢盐类水解产生的酸性溶液。
b. 制备金属:盐类水解可以用于制备金属,例如在冶金工业中,我们常常使用氯化铝来制备铝金属,氯化铝溶解在水中会产生氯离子和铝离子,铝离子可以与水分子发生反应,生成氢气和氢氧根离子,氢氧根离子与铝离子反应生成氢氧化铝,进一步还原生成铝金属。
c. 制备化学品:盐类水解可以用于制备化学品,例如在化工工业中,我们常常使用氯化钠来制备氯气和氢氧化钠,氯化钠溶解在水中会产生氯离子和钠离子,氯离子可以与水分子发生反应,生成氯气,而钠离子则与水分子发生反应,生成氢氧化钠。
【知识解析】盐类水解的应用
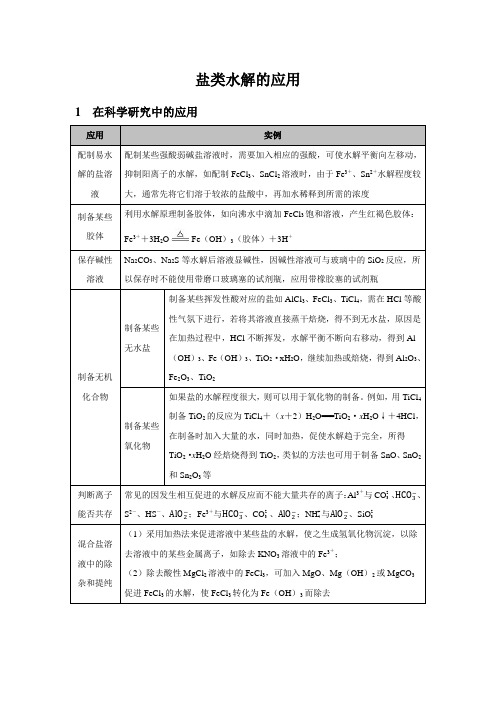
1在科学研究中的应用
应用
实例
配制易水解的盐溶液
配制某些强酸弱碱盐溶液时,需要加入相应的强酸,可使水解平衡向左移动,抑制阳离子的水解,如配制FeCl3、SnCl2溶液时,由于Fe3+、Sn2+水解程度较大,通常先将它们溶于较浓的盐酸中,再加水稀释到所需的浓度
制备某些胶体
利用水解原理制备胶体,如向沸水中滴加FeCl3饱和溶液,产生红褐色胶体:Fe3++3H2O Fe(OH)3(胶体)+3H+
判断离子能否共存
常见的因发生相互促进的水解反应而不能大量共存的离子:Al3+与CO2- 3、 、S2-、HS-、 ;Fe3+与 、CO2- 3、 ;NH+ 4与 、SiO2- 3
混合盐溶液中的除杂和提纯
(1)采用加热法来促进溶液中某些盐的水解,使之生成氢氧化物沉淀,以除去溶液中的某些金属离子,如除去KNO3溶液中的Fe3+;
(2)除去酸性MgCl2溶液中的FeCl3,可加入MgO、Mg(OH)2或MgCO3促进FeCl3的水解,使FeCl3转化为Fe(OH)3而除去
2在工农业生产和生活中的应用
应用
实例
明矾或FeCl3作净水剂
Al3+、Fe3+发生水解反应,产生的胶体能够吸附水中的悬浮物而起到净水的作用
用热的纯碱溶液去污效果更好
CO2- 3+H2O +OH-,水解反应为吸热反应,加热使平衡向右移动,溶液的碱性增强,去污效果更好
泡沫灭火器的原理
泡沫灭火器中使用的是Al2(SO4)3溶液和NaHCO3溶液,两者混合时,发生相互促进的水解反应,直至水解完全:Al3++3 ===Al(OH)3↓+3CO2↑,灭火器内压强增大,CO2、H2O、Al(OH)3一起喷出覆盖在着火物质上使火焰熄灭
盐类水解的应用

想一想:盐类水解在日常生活中有哪些应用?
应用1:明矾(KAl(SO4)2·12H2O)净水原理(胶体制备) Al3++3H2O Al(OH)3(胶体)+3H+,
Al(OH)3胶体可吸附水中悬浮杂质,达到净水目的.
如何制备氢氧化铁胶体?(84页)
问题1:为什么用沸水?加热到什么时候? 若持继加热会怎样?
D. 氨水
应用7:利用水解可除去溶液中某些水解能力较强的金 属离子,如Fe3+等
练习:为了同时对某农作物施用分别含有N、P、 K三种元素的化肥,对于给定的化肥: ①K2CO3 ②KCl ③Ca(H2PO4)2 ④(NH4)2SO4 ⑤氨水,最适合的组合是 B
A、①③④ C、①③⑤
B、②③④ D、②③⑤
应用6:加热蒸发盐溶液要考滤水解
盐不水解,得原溶质
盐水解的产物能脱离溶液体系(如盐酸,硝酸等 挥发性酸),则得另一水解产物,否则得原溶质。
注:同时要考虑加热物质是否会分解或被氧化。 练习4:FeCl3溶液蒸干灼烧,最后得到固体产物是什么?
FeCl3+3H2O
Fe(OH)3+3HCl
2Fe(OH)3 △ Fe2O3 + 3H2O
如何加热FeCl3溶液得到FeCl3固体? 在HCl气流中加热.
练习5:加热蒸干并灼烧下列物质的溶液,可以得
到该物质固体的是( C E )
A、氯化铝
B、碳酸氢钠
C、碳酸钠
D、亚硫酸钠
E 、硫酸铝溶液
练习6:为除去MgCl2溶液中少量FeCl3,可在加热搅拌下
加入( A )
A.氧化镁
B.氢氧化钠
C.碳酸钠
CO32-+H2O HCO3-+H2O
盐类水解原理的应用

盐类水解原理的应用
盐类水解是指盐在水中溶解后,离子会与水分子发生反应,水分子同时接受和释放H+离子,从而形成酸性或碱性溶液的化学反应。
盐类水解的应用包括:
1. 食品加工:盐类水解可调节食品溶液的pH值,增强食品的味道和保存时间。
2. 化学分析:盐类水解可用于分析化学实验中,测量酸性或碱性。
3. 工业生产:盐类水解可用于纺织、皮革、造纸、金属加工等工业生产中,调节反应环境,改变反应结果。
4. 医学应用:盐类水解可用于医学诊断与治疗上。
如碳酸氢钠的水解可使人体血液酸性度下降,有助于治疗酸中毒。
总之,盐类水解是化学领域中的一个重要现象,在许多领域都有广泛的应用。
盐类水解的应用

盐类水解的应用
盐类水解是指将盐类物质(如氯化钠)分解成其中的离子,这是一种重要的化学反应,在医药、食品、纺织和其他行业中都有着重要的应用。
盐类水解可以用来提取有用成分,例如,在医药行业,可以将有机物质分解成碳水化合物、氨基酸和其他有效成分,从而提取活性物质,用于制药、研究和生产药物。
此外,盐类水解还可以用于食品加工,以提取食品中的有效成分,例如蛋白质,以及制造食品添加剂,以增加食品的口感和营养价值。
此外,盐类水解还可以用于纺织行业。
纤维制成的衣物可以通过水解成碱性物质,通过这种方式来改善纤维的性能,使其更有弹性、耐磨性和耐腐蚀性。
另外,盐类水解还可以用于石油行业,将石油分解成烃类物质,从而制造汽油、柴油等燃料。
总之,盐类水解有着广泛的应用,可以用于医药、食品、纺织、石油等行业,为各行各业的发展提供了重要的帮助。
盐类的水解的应用

盐类水解的应用一、在生活中的应用1、去污:纯碱具有去污作用,加热后,去污能力增强,原因是碳酸钠溶液水解显碱性,且温度升高水解程度增大,碱性增强,油脂在碱性条件下水解为溶于水的高级脂肪酸盐和甘油。
2、泡沫灭火器原理:成分为NaHCO 3与Al 2(SO 4)3,发生反应的方程式为:3、明矾净水原理:明矾溶于水电离出的Al 3+水解 (写水解方程式),生成的Al(OH)3具有吸附性,可吸附水中杂质,达到净水的效果。
4、化肥的使用:铵态氮肥与草木灰(主要成分为K 2CO 3)不得混用,原因:CO 32-与NH 4+发生双水解 (写方程式),NH3挥发到空气中,氮元素损失,铵态氮肥肥效降低。
5、除锈剂:NH 4Cl 与ZnCl 2溶液可作焊接时的除锈剂,原因:NH 4Cl 与ZnCl 2溶液因NH 4+和Zn 2+水解而显酸性,铁锈(Fe 2O 3)会溶于该酸性溶液。
二、在实验中的应用1、配制或贮存易水解的盐溶液:加入相应的酸或碱抑制其水解eg :(1)配制CuSO 4溶液时,加入少量 ,防止Cu 2+水解;(2)贮存Na 2CO 3溶液、Na 2SiO 3溶液的试剂瓶要用 塞而不用磨口玻璃塞原因:(3)如何配制FeCl 3溶液?(4)保存FeCl 2溶液时,需要加入铁粉,目的是2、Fe(OH)3胶体的制备方法为: 方程式为:3、盐溶液蒸干所得产物的判断(1)蒸干后得原物质:强碱盐、弱碱的难挥发性酸盐eg :Na 2CO 3 (aq)――→蒸干( ) KAl(SO 4)2 (aq)――→蒸干( )(2)蒸干后得水解产物:弱碱的易挥发性酸盐,再灼烧得氧化物eg :AlCl 3(aq)――→蒸干 ( )――→灼烧( )。
FeCl 3(aq)――→蒸干 ( )――→灼烧( )。
(3)蒸干或灼烧后得分解产物:受热易分解的物质eg : Ca(HCO 3)2―→CaCO 3(CaO); NaHCO 3―→Na 2CO 3;KMnO 4―→K 2MnO 4+MnO 2; NH 4Cl ―→NH 3↑+HCl ↑。
盐类水解的应用

盐类水解的应用
1.判断盐溶液的酸、碱性时要考虑盐的水解。
2.判断溶液中离子能否大量共存时,有时要考虑盐的水解。
如Al3+、Fe3+与HCO3-、CO32-、AlO2-等不能大量共存。
3.盐在参加反应时,有时要考虑盐的水解。
如Mg加到NH4Cl溶液中,AlCl3与Na2S 溶液混合等。
4.加热浓缩某些盐溶液时,要考虑水解。
如浓缩FeCl3、AlCl3溶液。
盐溶液蒸干后,有的能得到原溶质,有的不能得到原溶质,而转化成其他物质,有的得不到任何物质,其规律如下:
①金属阳离子易水解的挥发性强酸盐得到氢氧化物,如FeCl3、AlCl3等。
②金属阳离子易水解的难挥发性强酸盐蒸干得到原溶质,如Al2(SO4)3。
③酸根阴离子易水解的强碱盐,如Na2CO3等蒸干后可得到原溶质。
④阴阳离子均易水解,其水解产物易挥发的盐蒸干后得不到任何物质,如(NH4)2S等。
⑤不稳定的化合物水溶液,加热在溶液中就能分解,也得不到原溶质,如Ca(HCO3)2 溶液,蒸干后得到CaCO3,Mg(HCO3)2蒸干后得到Mg(OH)2。
⑥易被氧化的物质,蒸干后得不到原溶质,如FeSO4、Na2SO3溶液等,蒸干后得到其氧化产物。
5.保存某些盐溶液时,有时要考虑盐是否水解。
如保存Na2CO3溶液不能用玻璃塞,保存NH4F溶液不能用玻璃瓶。
6.配制某些盐溶液时,要考虑盐的水解。
7.解释生活、生产中的一些化学现象,例如明矾净水原理,化肥施用问题等。
8.某些胶体的制备利用水解原理,如实验室制备Fe(OH)3胶体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
农业谚语 : “灰混粪,粪混灰,灰粪相混损肥分。”
思考:为什么会损肥分?
草木灰不宜与铵态氮肥混合施用:
草木灰的成分:K2CO3,水解呈碱性 CO32-+H2O HCO3- +OH-, HCO3-+H2O NH4++H2O H2CO3 +OH-, NH3· 2O+ H+, H
铵态氮肥——铵盐,水解呈酸性。
硬脂酸(C17H35COOH)是一种一元弱酸
C17H35COO-+H2O
△H>0
C17H35COOH+OH-
泡沫 灭火剂
制备胶体 明矾净水
混施化肥
盐类水解 的利用
判断溶液
酸碱性
盐溶液 的蒸发 溶液配制 试剂贮存
离子浓度 比较
练习:
1、科学使用化肥,是农作物高产的有利保证, 为了同时对农作物施用分别含N、P、K三 种元素的化肥,对于给定的化肥:
炸油条或油饼时必须要放明矾与纯碱 当矾与碱放入水中时,它们之间会发生化学变 化,产生大量CO2和絮状物。与面合在一起时, 絮状物Al(OH)3与面产生膜状物,将CO2气体 包住。油条放入热油锅中, CO2受热膨胀,使 油条胀大。这就是炸油条要放矾、碱的原因。 但其间的配比一定要掌握好,明矾多了,水解 产生的Al(OH)3就多,使油条遇热产生硬、脆、 多泡现象,而且耗油量大。若碱放多了,则会 使油条颜色发黄,增加其苦涩味。矾与碱之比 以2.5:3.5较为合适。
盐类的水解(第三课时)
思考:
1.日常生活中,我们经常用纯碱去油污. 冷纯碱水和热纯碱水哪个去油污效果好? 答: 热
2.实验室在配置FeCl3溶液时,需加入一种 试剂,你知道加入的试剂是什么吗? 答:HCl
盐类水解的利用
三、盐类水解的应用:
⒈判断盐溶液的酸碱性和溶液酸碱 性强弱
思考判断下列水溶液的酸碱性
Mg+ 2H+ = Mg2+ + H2↑ △ NH3•H2O = NH3 ↑ + H2O
NH4++ H2O
NH3· 2O + H+ H
Mg + 2H+ ═ Mg2+ + H2↑ NH3· 2O ═ NH3↑+ H2O H Mg2++2NH3· 2O═Mg(OH)2↓+2NH4+ H
△
7.解释生产、生活中的一些现象
用明矾净水
科学施肥:铵态氮肥不能和草木
灰(K2CO3)混施 泡沫灭火器的原理:Al2(SO4)3和 NaHCO3
灭 火 器 原 理
塑料筒里面放入 的是什么药品?
外筒放入的是什么药品?
泡沫灭火器里的药品是NaHCO3溶液和Al2(SO4)3溶液。
泡沫灭火器的原理应用双水解
药品:Al2(SO4)3溶液、NaHCO3溶液
练习:25℃ 浓度均为 1mol/L 的下列 溶液 中 ① NH4Cl ② NH4HSO4 ③ CH3COONH4 ④ ( NH4 )2Fe(SO4)2 判断C(NH4+)由大到小的顺序是: ②④①③ ________(填序 号)
3.配制和保存易水解的盐溶液
实验:热水配制CuCl2溶液
实验现象:溶液出现浑浊
△
亚硫酸钠溶液蒸干后得到什么固体 物质?
碳酸钾溶液加热蒸干后得到什么物 质?
①K2CO3
④ (NH4)2SO4
②KCl
⑤氨水
③Ca(H2PO4)2
最适宜的组合是: (填序号) ②③④
4、把AlCl3溶液蒸干后再灼烧,最后 得到的产物主要成分是? Al2O3
1 .AlCl3 +3H2O Al(OH)3+3HCl
2 .AlCl3 +3H2O △ Al(OH)3↓+3HCl↑ ═ 2Al(OH)3 ═ Al2O3 +3H2O
油条的制作口诀是“一碱、二矾、三 钱盐”,其中碱、矾、 盐分别是指: NaHCO3、KAl(SO4)2· 2O和NaCl,请分析制 12H 作油条的原理是什么? 在面团中Al3+和HCO3-发生双水解反应, Al3++3HCO3-=Al(OH)3+3CO2 当面团被投入到沸腾的油中时,面团受热,其中 的CO2体积增大, 致使面团膨胀为油条。
室 温 25℃
6.某些活泼金属与水解显酸性盐溶液的反应
【实验】 把Mg粉放入NH4Cl溶液 实验现象:剧烈反应有气体放出,有刺激性气味
[思考]检验NH3方法? 用湿润的红色石蕊试纸或蘸有浓盐酸的玻璃棒 检验结果:湿润的红色的石蕊试纸变蓝,说明刺激 性气味的气体是NH3 。
NH4++H2O
NH3•H2O + H+
Ba(OH)2>NaOH>Na2CO3>NaHCO3>NaAc>Na2SO4 >NH4Cl> (NH4)2SO4>NaHSO4>H2SO4
2、比较盐溶液中各离子浓度的相对大
小时,当盐中含有易水解的离子,需 考虑盐的水解。 练:25℃时,在浓度均为1mo/L的 (NH4)2SO4、(NH4)2CO3 2种溶液中, 若测得其中[NH4+]分别为a、b、(单 位为mo/L),则下列判断正确的是( ) A.a=b B. a>b C.b>a D.a>b
△
⑵HCl挥发
2Fe(OH)3 = Fe2O3 + 3H2O 思考:Al2(SO4)3溶液加热蒸发后得到固体是 什么?
尽管Al3+水解生成Al(OH)3和H2SO4,但由 于H2SO4是高沸点酸,不易挥发,加热最 终只是把水蒸去,因此仍得Al2(SO4)3固体。
3H2SO4+2Al(OH)3=Al2(SO4)3+6H2O
混施后,OH-与H+中和成水,使两种盐的 水解平衡强烈地向右移动,以至生成大量的 NH3· 2O,进一步分解成NH3 逸出了,从而降 H 低了肥效。 双水解
热纯碱水去油污能力强: 在碱性条件下去油污能力强
CO32-+H2O
HCO3-+H2O
HCO3- +OH- △H>0
H2CO3 +OH△H>0
[生活常识] 为什么用肥皂洗衣服时用温水比 冷水洗得干净一些? 肥皂主要成分:硬脂酸钠(C17H35COONa)
4、判断溶液中离子能否大量共存。 当弱碱阳离子和弱酸阴离子之间 发生彻底双水解反应,则不能在溶 液中大量共存。
双水解:弱酸根离子和弱碱离子同时存在于
溶液中,互相促进水解,使水解程度 显著增 大(甚至进行到底)
弱酸根离子与弱碱阳离子双水解配对情况
Al3+与AlO2- 、 CO32 - 、 HCO3 - 、 S2 - 、 HS Fe3+与AlO2- 、 CO32 - 、 HCO3 - 、
例:
下列微粒在溶液中能大量共存的( A. Na+, Fe 2+, SO42-, NO3 B. Al 3+, K+, Cl-, AlO2 C. Fe 3+, Na+, SO42-, S2 D. Ca 2+, H+, NO3-, SO32-
A
)
5.加热蒸发可水解的盐溶液 产物的判断
例:把FeCl3溶液蒸干灼烧,最后得到的固体 产物是Fe2O3. , 为什么?? FeCl3+3H2O Fe(OH)3+3HCl ⑴加热促进水解
原因:
CuCl2+2H2O >0
或Cu2++2H2O
Cu(OH)2+2HCl △H
Cu(OH)2+2H+ △H>0
热水:升温能够促进水解
配制CuCl2溶液,为防止出现浑浊,应加少量的
稀盐酸 _______
Na2CO3溶液保存时注意: 试剂瓶用( 橡胶 )塞
NH4F溶液保存时注意: 不能用( 玻璃 )瓶
Al3++3H2O
Al(OH)3+3H+,
HCO3-+H2O
H2CO3 +OH-,
总式:Al3++3HCO3- = Al(OH)3↓+3CO2↑;
为什么不能用溶解度大的Na2CO3代 替NaHCO3? 原因是:与等物质的量的Al2(SO4)3
产生的CO2少且生成CO2的速率慢。
Al3+ + 3HCO3- ═ Al(OH)3↓+3CO2↑ 2Al3+ + 3CO32- +3H2O═2 Al(OH)3↓+3CO2↑
(1)NaHCO3(2)KCl
(3) Cu(NO3)2 (5)NaF (4)KClO
相同条件,相同物质的量浓度的下列几 种溶液:Na2CO3、NaAc、Na2SO4、 NaHCO3、 NaOH 、Ba(OH)2、 (NH4)2SO4、NH4Cl、H2SO4、NaHSO4 等溶液,PH值由大到小的顺序为:
