癌胚抗原定量测定试剂盒(化学发光免疫分析法)的临床性能评价
罗氏CobasE601全自动电化学发光免疫分析仪检测癌胚抗原(CEA)的研究分析

罗氏Cobas E601全自动电化学发光免疫分析仪检测癌胚抗原(CEA)的研究分析发布时间:2022-11-21T01:39:17.158Z 来源:《医师在线》2022年19期作者:秦英杰[导读] 目的:研究分析罗氏Cobas E601全自动电化学发光免疫分析仪对CEA的检测性能秦英杰锡山人民医院东亭分院江苏无锡 214000【摘要】目的:研究分析罗氏Cobas E601全自动电化学发光免疫分析仪对CEA的检测性能。
方法:从我院2021年1月~2021年6月的体检人员中选择120例,将血液样本作为分析对象,通过罗氏Cobas?E601分析仪对CEA的检测结果进行分析。
结果:在不同浓度、不同批次、批内下,SV(变异系数)结果符合规定范围,检测值在认定范围。
结论:罗氏Cobas?E601全自动电化学发光免疫分析仪对CEA的检测准确性、精密度能够得到保证,值得应用。
【关键词】全自动电化学发光免疫分析仪;癌胚抗原;精密度;准确度【中图分类号】 R446.6 【文献标识码】ACEA属于肿瘤标志物的一种,除了胃癌以外,在乳腺癌、肺癌等癌症中也表现为CEA水平升高。
为此,以CEA指标为基础进行检测能有效判断肿瘤发展程度,利于病情诊断检测[1]。
全自动电化学发光免疫分析仪作为现阶段技术较为成熟的检测仪器,具有处理样本及检测速度快的特点[2]。
为此,本研究将严格按照实验室质量要求,对罗氏Cobas?E601全自动电化学发光免疫分析仪检测性能进行探究分析,现报道内容如下。
1 资料与方法1.1一般资料1.1体检人员资料选择我院2021年1月~2021年6月期间内体检的人员共120名,所有送检的标本均无溶血、无脂血情况,为新鲜标本。
其中,男性体检人员共63例、女性共57例,年龄均值范围:[28~76(48.55±5.13)]岁。
纳入标准:①年龄≥18岁;②自愿参加此研究;③入院基本资料完全。
排除标准:①凝血功能障碍;②妊娠期、哺乳期患者。
癌胚抗原化学发光法参考范围

癌胚抗原化学发光法参考范围【原创实用版】目录1.癌胚抗原化学发光法的概念2.癌胚抗原化学发光法的参考范围3.癌胚抗原化学发光法与其他肿瘤标志物的区别4.癌胚抗原化学发光法在诊断癌症中的作用5.癌胚抗原化学发光法结果的解读正文癌胚抗原化学发光法是一种检测癌症的常用方法,它通过测量血液中癌胚抗原(CEA)的含量来判断患者是否患有癌症。
癌胚抗原是一种蛋白质,正常情况下只存在于胚胎和胎儿组织中。
当人体内出现癌细胞时,癌胚抗原的含量会明显升高。
癌胚抗原化学发光法的参考范围因检测方法和仪器不同而有所差异。
通常情况下,癌胚抗原化学发光法的参考范围为 0-5ng/mL。
如果检测结果超出这个范围,可能意味着患者体内存在癌细胞。
但是,单凭癌胚抗原化学发光法的结果并不能确诊癌症,因为它只是一个筛查指标,而不是诊断指标。
癌胚抗原化学发光法与其他肿瘤标志物的区别在于,它是一种特异性较高的肿瘤标志物。
所谓特异性,是指它只对某种类型的癌细胞敏感。
例如,大肠癌、胰腺癌和肺癌患者的癌胚抗原含量通常会明显升高。
但是,这并不意味着癌胚抗原化学发光法的结果可以用来确诊这些类型的癌症,因为它的敏感度和特异性仍然有限。
癌胚抗原化学发光法在诊断癌症中的作用是辅助诊断。
当医生怀疑患者可能患有癌症时,可以通过检测患者的癌胚抗原含量来判断患者是否真的患有癌症。
如果癌胚抗原含量明显升高,医生可能会建议患者进一步接受检查,如 CT 扫描或病理检查,以确诊癌症。
癌胚抗原化学发光法结果的解读需要综合考虑多个因素,包括检测方法、仪器和参考范围。
如果检测结果超出参考范围,并不能直接判断为癌症,而需要进一步检查。
同时,癌胚抗原化学发光法的结果也受其他因素的影响,如胃肠道炎症、进食等。
化学发光法测定CEA 的方法学性能评价

化学发光法测定CEA 的方法学性能评价摘要】目的通过对化学发光仪测定癌胚抗原(CEA)的方法学性能评价,验证其性能是否与厂家声明一致。
方法按照美国国家临床实验室标准化委员会(CLSI)推荐的方法测定CEA 的精密度、正确度、分析测量线性范围、分析灵敏度、生物参考区间等指标进行验证。
结果CEA 的方法学评价结果均与厂家提供的数据一致。
结论化学发光分析仪检测系统的性能能满足临床需求。
【关键词】癌胚抗原方法学性能评价【中图分类号】R446 【文献标识码】A 【文章编号】1672-5085(2013)36-0161-02近年来随着I S O15189 医学实验室质量和能力认证工作在国内大中型医院的开展,检验医学界更重视对临床实验室开展的项目的检测系统或方法的分析性能进行验证确认或评价。
现在就本实验室化学发光仪测定CEA 的方法学性能评价报道如下。
1 材料与方法1.1 仪器与试剂雅培ARCHITECT i2000 全自动免疫分析仪,配套试剂、校准品和质控品。
1.2 评价方案和实验方法1.2.1 精密度评价根据CLSI EP15-A[1] 文件,选择每天分析1个批次,2 个浓度,每个浓度重复测定4 次,连续5 天。
样本为美国伯乐公司生产的免疫复合血清低、高2 个浓度质控品。
常规IQC 在控后,分别进行批内、批间精密度测定,计算均值(x-)、标准差( S ) 和变异系数(CV)。
1.2.2 正确度评价根据C L S I E P15-A[1] 文件,采用卫生部临检中心2012 年至2013 年发放的20 份室间控制品进行检测,检测结果与已知“靶值”和可接受限进行比对,计算相对偏倚( B i a s ) , 公式:Bias=( 测定值一靶值)/ 靶值×100,可接受范围±25%。
1.2.3 分析测量线性范围(AMR) 评价按照CLSI EP6-A2[2] 文件,选择低浓度( L ) 和高浓度( H ) 标本各1 份,浓度覆盖仪器给定范围,用6 点法进行稀释(L,0.8L+0.2H,0.6L+0.4H,0.4L+0.6H,0.2L+0.8H,H),每个样品重复测定2 次,取均值,做回归统计分析,将实测值与预期值进行比较,计算回归方程Y=bX+a,确定检测项目的AMR。
化学发光试剂临床意义

名 称:人垂体泌乳素(PRL)诊断试剂盒(化学发光免疫分析法) 临床意义:人垂体泌乳素(PRL)是由垂体前叶产生的,由 198 个氨基酸组成的单链多肽,分子量 22kD,其结构与生物学方面与生长激素、胎泌乳素属同类激素。PRL 直接作用于体细胞,促进乳 腺生长、发育和乳液形成。此外,尚有促进卵巢分泌甾体激素 、黄体形成与溶解的作用。非妊娠 妇女与男性 PRL 水平相当,妊娠后 PRL 水平逐渐增加,至分娩前达到高峰,哺乳期进一步增加。 PRL 测定对垂体疾病,特别是垂体瘤和各种原因引起的高泌乳素血症及月经异常和不孕症的病因 诊断与鉴别有重要意义。
2
北京华科泰生物技术有限公司
化学发光各项目的临床意义
名 称:高灵敏人促甲状腺激素(TSH)诊断试剂盒(化学发光免疫分析法) 临床意义:促甲状腺激素(TSH)的分泌受血清中 T3 和 T4 浓度的负反馈调节。TSH 主要作用于甲 状腺,它能增加甲状腺合成并分泌甲状腺激素 T3 和 T4。测定血清中 TSH 的含量,是诊断甲状腺功 能和研究下丘脑-垂体-甲状腺轴的重要指标之一。在甲状腺功能评估中,可鉴别原发性和继发性 (垂体性或下丘脑性)甲状腺功能低下症,并可作为对甲低症疗效观察的指标。此外,可观察垂体 TSH 的储存功能,进一步区别下丘脑和垂体的病变;与 T4 联合使用是目前诊断新生儿先天性甲低 的唯一方法。
磁微粒子化学发光法测定AFP

磁微粒子化学发光法测定AFP、CEA的应用关键词】癌胚抗原【摘要】目的研究磁微粒子化学发光酶免疫法检测的可靠性及方法学评价。
方法利用磁微粒子化学发光法检测血清AFP、CEA,并进行精密度、灵敏度、特异性、回收率方面的探讨。
结果化学发光法测定AFP的线性范围0.30~1380μg/L,CEA的线性范围0.51~1067μg/L。
测定AFP的批内精密度CV值为1.16%~3.53%,批间为1.49%~4.67%;CEA的批内精密度CV值为0.87%~4.47%,批间为1.92%~4.71%。
AFP的最低检测限度0.30μg/L;CEA 的最低检测限度0.51μg/L。
AFP的回收率97.7%~99.0%;CEA的回收率98.4%~101.65%。
黄疸、脂血、溶血对AFP、CEA的测定无明显影响。
结论磁微粒子化学发光酶免疫法在病人结果可报告范围宽、精密度好、灵敏度高、特异性高、抗干扰能力强。
【关键词】磁微粒子化学发光甲胎蛋白癌胚抗原近十年来通过不断改进和发展,使化学发光免疫分析成为非放射性标记免疫分析中最有前途的方法之一。
测定时间短,无放射污染等特点,广泛应用在临床和科研[1]。
甲胎蛋白(AFP)和癌胚抗原(CEA)是最常用的肿瘤标志物之一。
它们的测定有助于肿瘤病人的诊断、治疗及术后疗效观察。
BECKMAN COULTER公司生产的ACCESS型免疫分析仪,即全自动微粒子化学发光免疫分析系统。
我们用此法对血清中的AFP和CEA的测定,作了精密度、分析灵敏度、回收试验及干扰试验等实验,现报告如下。
1 材料与方法1.1 仪器美国BECKMAN COULTER公司生产的ACCESS型全自动化学发光免疫分析仪。
1.2 试剂 AFP和CEA试剂盒由BECKMAN COULTER公司提供配套试剂。
1.3 方法按仪器操作手册,用配套试剂盒测定定值、样品。
数值在标定值允许的范围内,继续做精密度、灵敏度、回收试验和干扰试验等相关实验。
癌胚抗原项目性能验证方案

癌胚抗原(CEA) 检测方法学性能验证评价报告验证内容:正确度、重复精密度、中间精密度、线性范围、临床可报告范围及参考区间的确认验证人员:王绮华、杨俊一检测系统信息项目:CEA仪器名称: 全自动免疫分析仪仪器型号: I2000SR试剂及厂商:雅培公司检测方法:化学发光微粒子免疫检测法二厂商提供的相关参数三验证过程1 正确度1.1 目的:评价仪器测试结果与接受参考值之间的一致程度。
通过实验室检测数据的偏倚从而评价和验证实验室检测结果的准确性。
1.2 评价方法:参加卫生部临检中心的室间质评,本组参加室间质评的项目一律用回报结果作为评价标准,最近一次参加卫生部室间质评卫生部质控值。
1.3 结果判断:<1/2 CLIA’88正确度验证试验数据记录表2 精密度2.1 重复精密度2.1.1 目的:考察仪器检测方法的随机误差2.1.2 原理:在检测系统处于优良的条件下,连续测定20个结果,判断这20个独立结果间的一致程度2.1.3 方法:选择新鲜混合血清标本(病人高值、低值)各20份,测量前先定标,再做质控,质控结果在控制范围内,连续重复测定20次,计算SD,CV,得到重复性精密度。
2.1.4 标本来源:高、低值标本均为混合血清。
2.1.5 结果判断:<1/4C LIA’ 88 6.25%重复性精密度验证试验数据记录表2.2 中间精密度:2.2.1 目的:考察目前实验室检测方法中间精密度。
2.2.2 原理:在检测系统处于优良的条件下,连续测定20天,取得20个结果,判断这20个独立结果间的一致程度。
2.2.3 方法:取一个月的室内质控值(高值、低值)计算CV、SD,得到批间精密度。
2.2.4 结果判断方式:<1/3 CLIA’ 88 8.33%中间精密度验证试验数据记录表3 线性范围(Linearity range, AMR)3.1 目的:在确定某项目检测上限的同时检测其上下限是否呈线性关系,从而保证该浓度范围检测结果的准确性。
癌胚抗原化学发光免疫分析方法学研究

王 高生 , 李立和 , 魏 荣华 , 应希堂 , 胡 国茂 , 李振 甲 , 王建梅 (1.天津 市宝坻 区人 民医 院 ,天津 301800;2.北京科 美东雅 生物技 术有 限公 司 ,北 京 100094)
பைடு நூலகம்
摘要 :目的 研制化学发光免疫分析法 (CLIA)癌胚抗 原 (CEA)检测试剂盒。方法 采 用双抗体夹心法用 2种不同的单克隆抗体分别与 CEA分子上不同的抗原决定簇发生反应。用 1株单抗包被微孑L板制成 固相抗 体 , 用另 1株单抗标记碱性 磷酸酶(ALP)制成 酶标抗体 。在 包被微孑L中加入 CEA校 准品或待 测血清及酶标抗 体 , 温育后即形成 固相抗体一抗原一酶标抗体 的复合物 ,充分洗涤后加入化学发光底物液 ,于 30~90 min内测定其发光 强度 (RLU),根据标准 曲线即可算 出标 本中 CEA的含量。结果 该试剂盒 其敏感性 可达0.058 ng/mL;批 内和 批 间变异系数(CV)分别为 5.5% 一9.3%和 10.2% 一12.2% 。经实 验表明 ,CLIA与免疫放射分 析法 (IRMA)和 酶联免疫吸附试验 (ELISA)分别呈高度相关 ,相关系数 (r)分别 为 0.991、0.984;平均 回收率 为 97.3% 。结 论 新 研 制 的 CEA CLIA试 剂盒 各 项 技 术 指 标 均 达 到 了 国外 同类 产 品 水 平
关键词 :癌胚抗原 ;化学发光免疫分析法 ;微孔板
cea化学发光法参考值

cea化学发光法参考值【原创版】目录1.CEA 化学发光法的基本概念2.CEA 化学发光法的参考值3.CEA 化学发光法的应用领域4.CEA 化学发光法的优势与局限性正文CEA 化学发光法,全称为癌胚抗原化学发光法,是一种临床常用的肿瘤标志物检测方法。
这种方法主要通过检测人体内癌胚抗原(CEA)的含量,来辅助诊断肿瘤疾病。
一、CEA 化学发光法的基本概念癌胚抗原(CEA)是一种在正常情况下只存在于胚胎和胎儿体内的蛋白质。
在成人体内,CEA 的含量通常很低。
然而,当人体内发生肿瘤时,CEA 的含量会明显升高。
因此,CEA 被认为是一种重要的肿瘤标志物。
CEA 化学发光法是利用化学发光原理来检测 CEA 的一种方法。
这种方法具有高灵敏度、高特异性和高准确性等优点,因此在临床检测中得到了广泛应用。
二、CEA 化学发光法的参考值CEA 化学发光法的参考值通常根据不同的检测方法和仪器设备而有所不同。
一般来说,正常人的 CEA 含量应该在 2.5ng/mL 以下。
如果 CEA 含量超过 5.0ng/mL,就有可能是肿瘤疾病的表现。
然而,CEA 含量的升高并不一定意味着患有肿瘤,还需要结合其他检查结果和临床表现来综合判断。
三、CEA 化学发光法的应用领域CEA 化学发光法主要应用于以下几个领域:1.肿瘤疾病的早期诊断:通过检测 CEA 含量的升高,可以帮助医生早期发现肿瘤疾病。
2.肿瘤疾病的疗效监测:在治疗过程中,通过检测 CEA 含量的变化,可以评估治疗效果。
3.肿瘤疾病的预后判断:对于已经确诊的肿瘤患者,通过定期检测CEA 含量,可以预测疾病的进展和预后。
四、CEA 化学发光法的优势与局限性CEA 化学发光法具有以下优势:1.高灵敏度:可以检测到非常低浓度的 CEA,有利于早期发现肿瘤疾病。
2.高特异性:与其他肿瘤标志物相比,CEA 的特异性较高,不易出现假阳性或假阴性。
3.高准确性:化学发光法具有较高的测量准确性,可以提供较为可靠的检测结果。
化学发光微粒子免疫分析法和酶联免疫吸附分析法检测癌胚抗原的效果

化学发光微粒子免疫分析法和酶联免疫吸附分析法检测癌胚抗原的效果王海生【期刊名称】《临床医学研究与实践》【年(卷),期】2018(3)36【摘要】目的比较化学发光微粒子免疫分析法(CMIA)和酶联免疫吸附分析法(ELISA)检测癌胚抗原(CEA)的效果。
方法分别采用CMIA和ELISA检测临床标本中CEA的水平,分析其灵敏度、检测范围、精密度、准确度及相关性。
结果 CMIA 法和ELISA法的灵敏度分别为0.5、1.8 ng/mL。
CMIA法检测范围为0.5~1 336 ng/mL,ELISA法的检测范围为1.8~90 ng/mL。
CMIA法高、中、低值混合血清的批内和批间精密度均小于5%,而ELISA法的均小于15%。
CMIA法高、中、低的回收率分别为95.9%、103.1%、106.2%,平均为101.7%;ELISA法分别为93.8%、97.4%、94.6%,平均为95.3%。
CMIA法和ELISA法检测CEA水平的线性回归方程为Y=0.9244X+3.1739(r=0.967,P<0.01)。
结论 CMIA法检测CEA水平的灵敏度、检测范围、精密度及准确度均优于ELISA法,但ELISA法检测CEA的结果也能满足临床要求,适用于大批量体检标本检测。
【总页数】2页(P151-152)【关键词】化学发光微粒子免疫分析法;酶联免疫吸附分析法;癌胚抗原【作者】王海生【作者单位】常州市武进中医医院检验科【正文语种】中文【中图分类】R446.6【相关文献】1.化学发光微粒子免疫分析法与酶联免疫吸附法检测感染性疾病抗原抗体的比较[J], 李琦;尚晓泓2.酶联免疫吸附测定与化学发光微粒子免疫分析法检测抗-HBc IgM的一致性 [J], 冯艺;吕静静;颜丙玉;刘甲野;徐爱强;纪峰;宋立志;张丽3.化学发光微粒子免疫分析法与酶联免疫吸附法检测血清乙型肝炎表面抗体的比对[J], 周双艳;赵克斌;杨泽华4.化学发光微粒子免疫分析法与酶联免疫吸附法检测感染性疾病抗原抗体的比较[J], 周德众5.化学发光微粒子免疫分析法、酶联免疫吸附法在丙肝病毒抗体检测中的应用对比观察 [J], 薛海玲; 曾昭伟; 孙兰菊; 常艳敏因版权原因,仅展示原文概要,查看原文内容请购买。
癌胚抗原测定195发光法

癌胚抗原测定195发光法摘要:1.癌胚抗原测定简介2.195发光法原理3.195发光法在临床中的应用4.195发光法的优势与局限5.总结正文:癌胚抗原测定是一种检测肿瘤标志物的方法,通过对癌胚抗原(CEA)的测定,可以帮助医生评估患者的癌症风险。
在众多的检测方法中,195发光法具有较高的准确性和可靠性,被广泛应用于临床实践中。
195发光法是一种基于放射免疫分析的方法,其主要原理是将CEA抗原与放射性同位素125I标记的抗CEA抗体结合,再通过发光剂195发光信号的强度来推测CEA抗原的水平。
该方法具有高灵敏度、高特异性和短检测时间等优点,使得检测结果更加准确可靠。
在临床应用中,195发光法主要用于肿瘤的筛查、诊断、疗效监测和预后评估。
对于高危人群,如年龄大于40岁、有肿瘤家族史、吸烟史等人群,定期进行CEA测定有助于早期发现肿瘤风险。
对于已确诊患者,195发光法可以用于监测病情变化,评估治疗效果。
此外,195发光法在肺癌、结直肠癌、胃癌等肿瘤的诊断和筛查中具有较高的临床价值。
尽管195发光法在肿瘤标志物检测中具有明显优势,但仍然存在一定的局限性。
首先,CEA水平的升高并不一定意味着肿瘤的存在,还可能与其他疾病如炎症、肠道疾病等有关。
其次,部分肿瘤患者CEA水平升高不明显,可能导致检测结果阴性,从而延误病情。
因此,在实际应用中,195发光法需与其他检测方法如CA125、CA19-9等联合应用,以提高检测的准确性。
总之,195发光法作为一种癌胚抗原测定方法,在肿瘤诊断、筛查和监测方面具有较高的临床价值。
然而,单一使用195发光法仍存在一定的局限性,需与其他检测方法联合应用,以提高检测的准确性和可靠性。
癌胚抗原(CEA)测定试剂盒(化学发光免疫分析法)产品技术要求北方生物
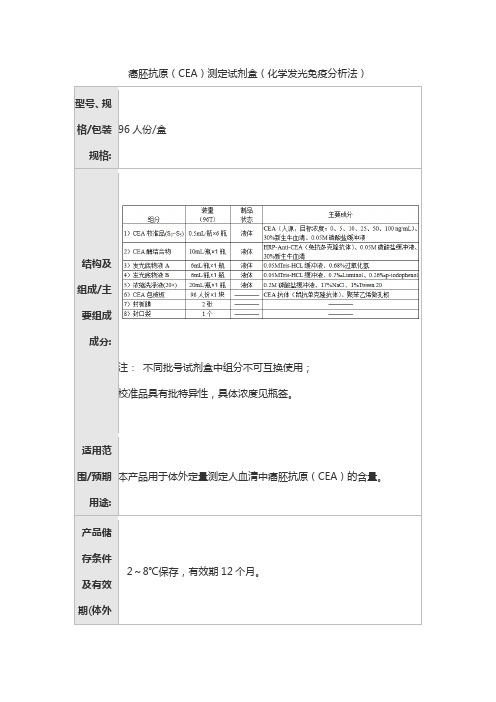
癌胚抗原(CEA)测定试剂盒(化学发光免疫分析法)
注:不同批号试剂盒中组分不可互换使用;
校准品具有批特异性,具体浓度见瓶签。
2.1外观
试剂(盒)各组分应齐全、完整,液体无渗漏;中文包装标签应清晰,无磨损。
2.2溯源性
根据GB/T21415-2008及有关规定,提供试剂盒内校准品的来源、赋值过程以及测量不确定度等内容,溯源至中国食品药品检定研究院提供的国家标准品(编号:150541)。
2.3准确度
用国家标准品(编号:150541)作为样本进行检测,其测量结果的相对偏差应在±10%范围内。
2.4线性
用Log-Log数学模型拟合,在[4~100]ng/mL范围内,相关系数(r)应不低于0.9900。
2.5重复性
用10ng/mL±2ng/mL和100ng/mL±20ng/mL的样本各重复检测10次,其变异系数(CV)应不大于15%。
2.6批间差
用3个批号试剂盒检测同一份样本,则3个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.7空白限
应不大于0.5ng/mL。
2.8特异性
与其它相关物质的交叉反应数据
2.9稳定性
37℃放置7天,或2~8℃放置12个月,测定结果应符合上述2.3、2.4、2.5、2.7项要求。
癌胚抗原(CEA)测定(化学发光法测定)

4 操作步骤
1 开机前检查
a 察看电源是否正常安全通电
b 推主机下部的前门,打开后检查洗净水与分注液的用量是否满足当日
用量废试样杯与废吸嘴是否丢弃
2 开机
a更换75%酒精,放置基质液
b 打开电脑主机及AIA-1800电源, 点击主业面进入root
c 试样吸嘴的设置及酶标识试剂,检体稀释液的设置,按主机操作版面
Reagent/Tip键,LED指示灯变为绿色,打开试剂吸嘴护罩,将酶
标识试剂,检体稀释液设置在试剂托架上,将条形码
标识面朝前
d 试剂杯的设置,按主机操作版面的Cup Sorter键,LED指示灯
变为绿色,拉开分类器抽屉将试剂托盘设置在分类器托盘上,将分类器
抽屉推到底
3 开机日检
4 日检通过后,进行标本检测,在树形菜单上进入界面设置标
本检测项目,Assay键点击开始测定
5 测定完毕后,按主机操作版面的Cup Sorter及Reagent/Tip键,LED指
示灯变为绿色,打开试剂吸嘴护罩及分类器抽屉,收集试剂放入冰箱,
更换基质液,放置75%酒精
6 点击关机,待窗口消失,关闭AIA-1800电源,在关闭电脑及主电
源
5 质量控制:
每批试剂都要使用东曹公司标准品作质量控制,请参见AIA-1800仪器操作手。
cea免疫组化判读标准

cea免疫组化判读标准
免疫组化(Immunohistochemistry,IHC)是一种用于检测组织样本中特定蛋白质表达的技术。
在临床诊断中,免疫组化广泛应用于肿瘤诊断和分子病理学研究。
CEA(癌胚抗原)是一种用于肿瘤诊断的免疫组化标记物,通常用于肝、结肠和直肠癌等恶性肿瘤的诊断和预后评估。
在免疫组化判读CEA时,通常会根据细胞膜和细胞浆中CEA的染色程度和范围进行评估。
具体的判读标准可能会因实验室和临床实践而有所不同,但一般来说,可以从以下几个方面进行评估:
1. 染色强度,CEA的染色强度通常被分为无、弱阳性、中等阳性和强阳性。
强阳性的染色表示CEA的高表达,可能与恶性肿瘤相关。
2. 染色范围,除了染色强度,还需要评估CEA的染色范围,即CEA阳性细胞在组织样本中的分布情况。
如果CEA阳性细胞呈现弥漫性分布,可能与肿瘤的浸润和转移有关。
3. 与临床病理特征的关联,最终的CEA免疫组化判读需要结合
患者的临床病理特征进行综合评估,包括肿瘤类型、分级、浸润深度、淋巴结转移等,以确定CEA的表达与肿瘤的临床意义。
总的来说,CEA免疫组化的判读标准是一个综合性的评估过程,需要综合考虑染色强度、染色范围和临床病理特征等多个因素。
这
些判读标准的制定和应用有助于指导临床医生进行肿瘤诊断和治疗
决策,提高肿瘤患者的预后和生存质量。
CEA

癌胚蛋白(CEA)化学发光
试剂盒
使 用 说 明 书
济南杏恩生物科技有限公司
癌胚蛋白(CEA)化学发光试剂盒说明书
【临床意义】
通过化学发光酶免疫法定量分析人血清中癌胚抗原(Carcinoembryonic Antigen,CEA)的浓度。
血清CEA升高主要见于结肠直肠癌、胰腺癌、胃癌、肝癌、肺癌、乳腺癌等。
【原理】 酶免疫分析测试
【试剂存放方式】(所有试剂保存在2-8℃)
【试剂盒组成】
1.CEA 包被板:可拆板,8×12孔。
2.CEA 标准品: 6小管,0.3ml/管,各个标准品浓度分别为 0,3, 12,30, 60, 120ng /ml。
3.CEA 标记偶合液:1瓶,10ml/瓶。
4. CEA低质控对照品:0.3ml/管
5. CEA高质控对照品:0.3ml/管
6.发光底物 1:5ml/瓶,含有H2O2的缓冲液。
7.发光底物 2:5ml/瓶,含有冷光酶的缓冲液。
8.产品说明书一份。
适用机器: 国内外所有板式化学发光仪 .
【样本采集】
本测试的样品为血清或血浆。
样品可保存在2-8℃下48小时,如需长期保存需冷冻在-20℃。
样品在解冻后需混合均匀后再进行测试
简易操作步骤
样品
化学发光标记偶合液
反应时间 15分钟 (室温25+/-2度)
洗板
Mediators PHL TM 选定程序 机器自动加底液
发光底物1
反应时间5分钟(室温25+/-2度
发光底物2
立即测读(1秒钟之内)
计算样品浓度。
癌胚抗原化学发光法参考范围

癌胚抗原化学发光法参考范围
癌胚抗原(CEA)是一种在正常情况下存在于胚胎和胎儿体内的糖蛋白,随着胎儿的生长发育,CEA水平逐渐下降。
然而,在某些疾病状态下,如结肠癌、乳腺癌等肿瘤患者体内,CEA水平会升高。
因此,检测CEA对于肿瘤的筛查、诊断及病情监测具有重要临床价值。
化学发光法是一种灵敏、准确的CEA检测方法。
它基于抗原抗体反应原理,通过测定抗原与抗体结合后产生的化学发光信号强度,从而推算出CEA的水平。
与其他检测方法相比,化学发光法具有较高的灵敏度和特异性,能有效降低假阳性及假阴性的发生。
在实际应用中,CEA化学发光法的参考范围为0-5.0ng/ml。
这个范围可以用于评估个体患肿瘤的风险。
若CEA水平低于参考范围,说明患肿瘤的风险较低;若CEA水平高于参考范围,需进一步进行相关检查,如影像学、病理学等,以确认是否存在肿瘤。
当CEA检测结果异常时,患者不必过于担忧。
首先,要明确CEA升高并不一定意味着患有肿瘤,还可能与其他疾病如炎症、感染等有关。
其次,需结合其他临床资料,如病史、症状、影像学检查等,综合评估病情。
在必要时,可进行进一步的实验室检查,如肿瘤标志物组合检测、基因检测等,以明确诊断。
总之,CEA化学发光法作为一种有效的肿瘤筛查工具,可以帮助临床医生及时发现患者的风险。
然而,CEA检测结果的解释需结合临床资料综合判断,避免过度诊断和治疗。
在面临异常结果时,保持冷静,寻求专业医生的建议是
关键。
cea化学发光法参考值

cea化学发光法参考值化学发光法是一种测定化学物质浓度的分析方法,利用物质在化学反应中释放能量发出的光进行测量。
该方法通过控制反应条件和测量光的强度来确定待测物质的浓度。
化学发光法利用化学反应中发生的放射性衰变或化学反应释放的光来测量物质的浓度,是一种非常灵敏的分析方法。
这种方法的主要原理是待测物质与特定试剂进行化学反应,发生放射性衰变或化学发光反应,产生的光通过光学仪器测量。
测量出的光强度与待测物质的浓度成正比关系。
化学发光法在环境监测、医学诊断和生物技术等领域有广泛的应用。
例如,在环境监测中可以通过化学发光法测定空气中有毒气体浓度,以及水中污染物的含量。
在医学诊断中,化学发光法可以用于血液中肿瘤标志物的检测、病毒感染的诊断,以及药物代谢产物的测定等。
在生物技术领域,化学发光法可以用于核酸杂交、蛋白质定量和酶活性测定等。
化学发光法的核心是发光媒介。
常用的发光媒介有化学荧光剂、化学放射性测荧剂和化学固相发光材料等。
这些发光媒介在特定的条件下释放能量产生光,通过测量光的强度可以确定物质的浓度。
化学发光法的灵敏度和选择性取决于发光媒介的性能和与待测物质的反应。
因此,选择合适的发光媒介至关重要。
化学发光法的操作步骤相对简单,但仪器设备较为复杂。
通常,需要配备光源、光学系统、控制系统和数据处理系统。
光源可以是激光器、发光二极管或者荧光灯。
光学系统包括滤光片、光电倍增管等,用于选择和接收发出的光。
控制系统用于调节反应温度、反应时间和光源强度等参数。
数据处理系统通过计算机软件实现光强的计算、数据处理和结果输出。
化学发光法具有许多优点。
首先,化学发光法可以测量极低浓度的物质。
其灵敏度可以达到亚微摩尔甚至飞摩尔的级别。
其次,化学发光法反应时间短,可在短时间内得到准确的测量结果。
此外,化学发光法对待测物质的选择性较高,可以通过选择合适的发光媒介和反应条件来实现。
最后,化学发光法操作简便,由于不需要进行染色或标记,因此避免了误差的引入。
癌胚抗原的实验报告

癌胚抗原的实验报告1. 引言癌胚抗原(Carcinoembryonic antigen,CEA)是一种产生于癌胚组织及恶性细胞中的糖蛋白,广泛存在于许多癌症类型的细胞表面。
CEA在临床上常用作肿瘤标志物,用于辅助肿瘤的诊断、预测预后以及监测治疗效果。
本实验旨在确定CEA在肿瘤细胞株中的表达情况,并通过免疫组织化学染色和ELISA方法对其进行定性和定量分析。
2. 材料与方法2.1 实验材料- 人肺癌细胞株A549- 兔抗人CEA抗体- 辅助抗体:羊抗兔IgG-HRP- DAB染色盒- 免疫组织化学染色常用试剂- 细胞培养基- 96孔ELISA板- CEA标准品- 人CEA酶联免疫吸附试剂盒2.2 方法2.2.1 免疫组织化学染色1. 培养肺癌细胞株A549至密集细胞层,并用PBS洗涤细胞。
2. 使用PFA固定细胞片,冷冻切片。
3. 样品脱脂:用xylene处理、以乙醇递降浓度处理、最后用PBS洗涤。
4. 阻断非特异性结合:在切片上滴加5%的牛血清白蛋白,静置30分钟。
5. 兔抗人CEA抗体处理:将兔抗人CEA抗体稀释至适当浓度,在切片上滴加抗体,室温孵育2小时。
6. 三次PBS洗涤:每次5分钟。
7. 辅助抗体处理:将羊抗兔IgG-HRP稀释至适当浓度,并在切片上滴加。
室温孵育1小时。
8. 三次PBS洗涤:每次5分钟。
9. 使用DAB染色盒按说明书进行染色。
10. 用水清洗切片,封片后显微镜观察。
2.2.2 酶联免疫吸附实验(ELISA)1. 培养肺癌细胞株A549至密集细胞层,并在96孔ELISA板上接种细胞悬液。
2. 收集细胞上清液,离心去除细胞碎片。
3. 在ELISA板上设置标准品组和待测组。
4. 将标准品和待测样品加入板孔中,孵育一段时间后洗涤孔。
5. 加入辅助抗体孵育,再次洗涤。
6. 加入底物,反应一定时间后停止反应。
7. 用ELISA酶标仪测量吸光度。
3. 结果与讨论3.1 免疫组织化学染色结果通过免疫组织化学染色,观察到肺癌细胞株A549中CEA的表达情况。
光激化学发光法定量测定AFP和CEA的性能评价

光激化学发光法定量测定AFP和CEA的性能评价荣扬;赵强元;刘敏;齐永志;王珍光;李娜【摘要】目的探讨光激化学发光法(LiCA)和酶促化学发光法测定甲胎蛋白(AFP)和癌胚抗原(CEA)结果的可比性,评估LiCA AFP和CEA检测试剂的分析性能.方法依据美国临床实验室标准化委员会(NCCLS)和《体外诊断试剂临床研究指导原则》,评估LiCA AFP和CEA检测试剂的分析灵敏度、不精密度和线性;分别用2种系统定量检测血清AFP(406例)和CEA(442例),对结果进行统计学分析.结果 LiCA AFP和CEA检测试剂分析灵敏度分别为0.112和0.05 ng/mL;批内变异系数(CV)分别为4.32%和4.56%;批间CV分别为5.89%和6.47%;线性范围分别为2.6~950.2和1.2~862.6 ng/mL.与酶促化学发光法测定AFP和CEA的相关系数(r)均>0.99.结论 LiCA检测AFP和CEA具有较好的分析性能,与酶促化学发光法高度相关,能满足临床检测要求.%Objective To investigate the comparability of the results of alpha fetoprotein ( AFP) and carcinoembryonic antigen ( CEA) measured by light initiated chemiluminescence ( LiCA) and enzyme-enhanced chemiluminescence, and evaluate the clinical performances of LiCA AFP and CEA kits. Methods According to the documents of National Committee for Clinical Laboratory Standards ( NCCLS) and In Vitro Diagnostic Products Clinic Research Guideline, the analytical sensitivity, imprecision and linearity of LiCA AFP and CEA kits were evaluated, and 406 AFP serum samples and 442 CEA serum samples were detected by LiCA and enzyme-enhanced chemiluminescence respectively. The data were analyzed statistically. Results The analytical sensitivities of AFP and CEA by LiCA were 0.112 and 0. 05 ng/mL. The within-run and between-runcoefficients of variation ( CV) of AFP and CEA by LiCA were 4.32% ,4. 56% and 5. 89% ,6. 47% respectively. The linearities of AFP and CEA by LiCA were 2. 6-950. 2 and 1.2-862.6 ng/mL. The correlation coefficients (r) of 2 chemiluminescence systems for AFP and CEA were >0. 99. Conclusions The clinical performances of LiCA AFP and CEA are satisfied to clinical measurement. There is a correlation between the 2 systems for AFP and CEA.【期刊名称】《检验医学》【年(卷),期】2013(028)002【总页数】4页(P146-149)【关键词】光激化学发光法;酶促化学发光法;甲胎蛋白;癌胚抗原;性能分析;对比【作者】荣扬;赵强元;刘敏;齐永志;王珍光;李娜【作者单位】海军总医院检验科,北京100048【正文语种】中文【中图分类】R446.1纵观标记免疫分析的发展史,近年来,化学发光免疫分析已占据了免疫分析的主导地位,尤其是进口的化学发光试剂占据了相当的份额。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
q u nt a i t a i t v e d e t e r mi n a t i o n k i t( E C L ) w e r e u s e d a s c o n t r o l a g e n t s , a n d A b b o t t c a r c i n o e mb r y o n i c a n t i g e n
临床性 能评价 。
方法
定 量测定试 剂盒 ( 电化学发 光法 ) 为对 照试剂 , 雅 培公 司癌胚抗 原测定试 剂盒 ( 化学发 光微 粒子免 疫检测 法) 作 为复核试剂 , 对 自制试剂 盒的一致性 和相关性 等指标进行 计算分析 。 结果 自制试 剂盒 异常符 合率 达 9 6 . 1 %, 正常符 合率 达 9 7 . 8 %, 总符合 率达 9 7 . 3 %, Ka p p a值达 0 . 9 3 1 ( P < O . 0 1 ) 。 从 定量测 定值 分析 , 与罗 氏试 剂盒 测值 相 比 , 自制试 剂盒测 值 的线性 回归方 程为 Y= O . 0 9 1 + 1 . 0 0 9 X, 相关 系数为 0 . 9 8 7 ( P < 0 . 0 1 ) , 相关 性 良好 。 结论 本试 剂盒检测性 能满足 临床应用 的需 要 。 [ 关键 词] 癌胚抗原 ;临床 研究 ;化 学发 光免疫 分析法 T h e c l i n i c r e s e a mh o f t h e c a r c i n o e mb r y o n i c a n t i g e n( CE A )q u a n t i t a t i v e d i a g n o s t i c k i t b y c h e mi l u mi n e s -
( 1 .Da r u i Bi o t e c h n o l o g y Co . ,Lt d . ,Gu a n g z h o u ,Gu a n g d o n g ,Ch i n a ,5 1 0 6 6 5 ;2 .S c h o o l o f Bi o t e c h n o l o g y ,
梁丽萍 ・ 李志雄 1 董志宁 李明 吴英松 。
[ 摘 要] 目光免 疫分 析法 ) 进行 临床 应用研 究及 用 自制试 剂盒检测采 集到 的血 清 l 1 5 6例和 1 0 1 例 血浆 , 以罗 氏公 司癌胚抗 原 同罗 氏试剂盒相 比,
d e t e r mi n a t i o n it ( k CMI A) we r e u s e d a s a r e a g e n t i n r e v i e w. Co n s i s t e n c y a n d c o r r e l a t i o n we r e c lc a u l a t e d .
.
3 1 8.
分 子诊 断与治疗杂 志
2 0 1 5年 9月
第 7 卷
第 5期
J Mo l D i a g n T h e r ,S e p t e m b e r 2 0 1 5 , Vo 1 . 7 N o . 5
・
论 著 ・
癌胚抗原定量测定试剂盒 ( 化学发光免疫分析法 ) 的 临床性能评价
c e n t i mmu n o a s s a y( CL I A )
L I ANG L i p i n g ,LI Z h i x i o n g ,DONG Z h i n i n g , LI Mi n g 。 , W U Yi n g s o n g 。
Re s u l t s T h e p o s i t i v e a c c o r d a n t r a t i o , t he n e g a t i v e a c c o r d a n t r a i t o , he t Ka p p a v lu a e wa s 9 6 . 1 %, 9 7 . 8 %, 0 . 9 3 1
q u a n i t t a i t v e d i a g n o s i t c k i t b y c h e mi l u mi n e s c e n t i mmu n o a s s a y( C L I A)( C E A — C L I A) . Me t h o d s l 1 5 6 c a s e s
S o u t h e r n Me d i c a l Un i v e r s i t y ,Gu a n g z h o u ,Gu a n g d o n g , Ch i n a ,5 1 0 5 1 5 )
【 A B S T R A C T ]Ob j e c t i v e T o i n v e s i t g a t e he t c l i n i c r e s e a r c h o f he t c a r c i n o e mb r y o n i c a n i t g e n( C E A)
