国家食品药品监管总局关于印发医疗器械经营环节重点监管目录及现场检查重点内容的通知-国家规范性文件
新版《医疗器械监督管理条例》解读分析
新版《医疗器械监督管理条例》--解读分析
新《条例》修订思路
在此次修订过程中,国务院法制办和食品药品监管总局在总体思路上把握了以下 几点:
第一,以分类管理为基础,确定医疗器械研制、生产、经营、使用各环节的具体 制度,突出管理的科学性。
第二,以风险高低为依据,在保证产品安全有效的前提下,管放结合、宽严有别, 给高风险产品生产经营企业“加压”,给低风险产品生产经营企业“松绑”,促 进医疗器械生产经营企业做大做强。
第三,遵循推进政府职能转变和深化行政审批制度改革的精神和要求,适当减少 事前许可,重点强化过程监管和日常监管,提高监管的有效性。
普门科技 SHENZHEN LIFOTRONIC TECHNOLOGY CO.,LTD
新版《医疗器械监督管理条例》--解读分析
新《条例》概述
《医疗器械监督管理条例》已经2014年2月12日国务院第39次常务会议修订通 过;
3月31日,国家食品药品监督管理总局与国务院法制办在京联合召开宣传贯彻 《医疗器械监督管理条例》 (国务院令 第650号)新闻发布会。现将修订后的 《医疗器械监督管理条例》公布,自2014年6月1日起施行; 自施行之日起,代替已经于1999年12月28日国务院第24次常务会议通过, 2000年4月1日起施行的《医疗器械监督管理条例》(国务院令 第276号)。
普门科技 SHENZHEN LIFOTRONIC TECHNOLOGY CO.,LTD
新版《医疗器械监督管理条例》--解读分析
新《条例》概述
为确保《条例》的贯彻实施工作,国家食品药品监管总局于2014年04月11日 印发《食品药品监管总局关于认真贯彻实施<医疗器械监督管理条例>的通知》 (食药监法〔2014〕31号),要求各直属单位/部门: ——充分认识《条例》的重要意义; ——积极开展《条例》的学习、宣传和培训; ——抓紧制定、完善相关配套规章和制度; ——加强医疗器械监管能力建设; ——以贯彻实施《条例》为重要契机,扎实做好医疗器械专项整治工作;
医疗器械经营环节国家重点监管目录六个类别

类 别品种(类)目录一、无菌类
1.一次性使用无菌注射器(含自毁式、胰岛素注射、高压造影用)
2.一次性使用无菌注射针(含牙科、注射笔用)
3.一次性使用输液器(含精密、避光、压力输液等各型式)
4.一次性使用静脉输液针
5.一次性使用静脉留置针
6.一次性使用真空采血器
7.一次性使用输血器
8.一次性使用塑料血袋
9.一次性使用麻醉穿刺包10.人工心肺设备辅助装置(接触血液的管路、滤器等)11.血液净化用器具(接触血液的管路、过滤/透析/吸附器械)12.氧合器13.血管内造影导管14.球囊扩张导管15.中心静脉导管16.外周血管套管17.动静脉介入导丝、鞘管18.血管内封堵器械(含封堵器、栓塞栓子、微球)19.医用防护口罩、医用防护服二、植入材料和人工器官类 1.普通骨科植入物(含金属、无机、聚合物等材料的板、钉、针、棒、丝、填充、修复材料等)2.脊柱内固定器材3.人工关节4.人工晶体5.血管支架(含动静脉及颅内等中枢及外周血管用支架)6.心脏缺损修补/封堵器械7.人工心脏瓣膜8.血管吻合器械(含血管吻合器、动脉瘤夹)9.组织填充材料(含乳房、整形及眼科填充等)10.医用可吸收缝线11.同种异体医疗器械12.动物源医疗器械三、体外诊断试剂类 1.人传染高致病性病原微生物(第三、四类危害)检测相关的试剂2.与血型、组织配型相关的试剂3.其他需要冷链储运的第三类体外诊断试剂
四、角膜接触镜类软性角膜接触镜五、设备仪器类 1.人工心肺设备2.血液净化用设备3.婴儿保育设备(含各类培养箱、抢救台)4.麻醉机/麻醉呼吸机5.生命支持用呼吸机6.除颤仪7.心脏起搏器8.一次性使用非电驱动式输注泵9.电驱动式输注泵10.高电位治疗设备六、计划生育类避孕套(含天然胶乳橡胶和人工合成材料)医疗器械经营环节国家重点监管目录(六个类别)。
国家食品药品监管总局关于印发医疗器械经营环节重点监管目录及现场检查重点内容的通知

国家食品药品监管总局关于印发医疗器械经营环节重点监管目录及现场检查重点内容的通知
文章属性
•【制定机关】国家食品药品监督管理总局(已撤销)
•【公布日期】2015.08.17
•【文号】食药监械监〔2015〕159号
•【施行日期】2015.08.17
•【效力等级】行业规定
•【时效性】失效
•【主题分类】检验监管
正文
食品药品监管总局关于印发医疗器械经营环节重点监管目录
及现场检查重点内容的通知
食药监械监〔2015〕159号各省、自治区、直辖市食品药品监督管理局:
为加强医疗器械经营监管,根据《医疗器械经营监督管理办法》(国家食品药品监督管理总局令第8号)和《医疗器械经营企业分类分级监督管理规定》(食药监械监〔2015〕158号),总局组织制定了《医疗器械经营环节重点监管目录及现场检查重点内容》,现印发给你们,请按照《医疗器械经营企业分类分级监督管理规定》对《医疗器械经营环节重点监管目录及现场检查重点内容》中所列品种的经营实施重点监管。
附件:医疗器械经营环节重点监管目录及现场检查重点内容
食品药品监管总局
2015年8月17日。
医疗器械经营环节重点监管目录及现场检查重点内容
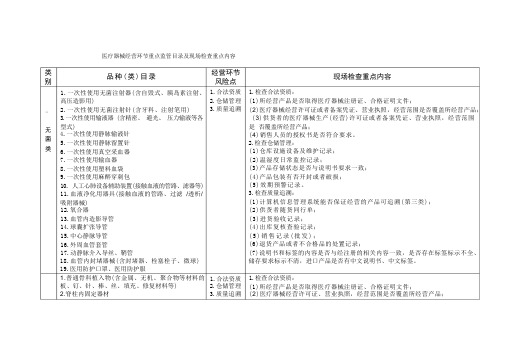
医疗器械经营环节重点监管目录及现场检查重点内容一品种(类)目录1.一次性使用无菌注射器(含自毁式、胰岛素注射、高压造影用)2.一次性使用无菌注射针(含牙科、注射笔用)3.一次性使用输液器 (含精密、避光、压力输液等各型式)4.一次性使用静脉输液针5.一次性使用静脉留置针6.一次性使用真空采血器7.一次性使用输血器8.一次性使用塑料血袋9.一次性使用麻醉穿刺包10. 人工心肺设备辅助装置(接触血液的管路、滤器等)11.血液净化用器具(接触血液的管路、过滤/透析/吸附器械)12.氧合器13.血管内造影导管14.球囊扩张导管15.中心静脉导管16.外周血管套管17.动静脉介入导丝、鞘管18.血管内封堵器械(含封堵器、栓塞栓子、微球)19.医用防护口罩、医用防护服1.普通骨科植入物(含金属、无机、聚合物等材料的板、钉、针、棒、丝、填充、修复材料等)2.脊柱内固定器材经营环节风险点1.合法资质2.仓储管理3.质量追溯1.合法资质2.仓储管理3.质量追溯现场检查重点内容1.检查合法资质:(1)所经营产品是否取得医疗器械注册证、合格证明文件;(2)医疗器械经营许可证或者备案凭证、营业执照,经营范围是否覆盖所经营产品;(3)供货者的医疗器械生产(经营)许可证或者备案凭证、营业执照,经营范围是否覆盖所经营产品;(4)销售人员的授权书是否符合要求。
2.检查仓储管理:(1)仓库设施设备及维护记录;(2)温湿度日常监控记录;(3)产品存储状态是否与说明书要求一致;(4)产品包装有否开封或者破损;(5)效期预警记录。
3.检查质量追溯:(1)计算机信息管理系统能否保证经营的产品可追溯(第三类);(2)供货者随货同行单;(3)进货验收记录;(4)出库复核查验记录;(5)销售记录(批发);(6)退货产品或者不合格品的处置记录;(7)说明书和标签的内容是否与经注册的相关内容一致,是否存在标签标示不全、储存要求标示不清,进口产品是否有中文说明书、中文标签。
国家药监局综合司关于印发2024年国家医疗器械抽检产品检验方案的通知

国家药监局综合司关于印发2024年国家医疗器械抽检产品检验方案的通知文章属性•【制定机关】国家药品监督管理局•【公布日期】2024.03.18•【文号】药监综械管〔2024〕32号•【施行日期】2024.03.18•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】医疗管理正文国家药监局综合司关于印发2024年国家医疗器械抽检产品检验方案的通知药监综械管〔2024〕32号各省、自治区、直辖市和新疆生产建设兵团药品监督管理局,中国食品药品检定研究院、相关检验机构:根据《国家药监局综合司关于开展2024年国家医疗器械质量抽查检验工作的通知》(药监综械管〔2024〕14号),现将2024年国家医疗器械抽检产品检验方案印发给你们,请认真组织实施并提出以下要求:一、检验工作要求各省、自治区、直辖市和新疆生产建设兵团药品监督管理局、中国食品药品检定研究院应当按照2024年国家医疗器械抽检品种检验方案(见附件1),组织相关检验机构按照医疗器械强制性标准、经注册或者备案的产品技术要求开展检验工作。
检验机构应当加强对未能依照检验方案完成全部适用项目检验情况的收集。
对于注册人备案人或者进口产品代理人未能提供完成检验所需全部资料和配套必需品的,以及产品技术要求不完善导致无法完成检验的,应当向注册人备案人或者进口产品代理人所在地省级药品监督管理部门出具国家医疗器械抽检缺项检验提示函,该提示将通过国家医疗器械抽检信息系统传递,省级药品监督管理部门应当对相关情况及时调查处理。
对于无正当理由不配合医疗器械质量抽查检验工作的,应当将调查结果记入企业信用档案,并通过其他形式加强对企业和相关产品的监督管理,增加监督检查强度和频次。
对于产品技术要求不完善的,应当监督企业尽快完善产品技术要求,并依法依规完成变更。
相关调查处理结果应当在提示函印发后30个工作日内录入国家医疗器械抽检信息系统。
二、复检工作要求2024年国家监督抽检的复检受理部门为医疗器械注册人备案人或者进口产品代理人所在地省级药品监督管理部门。
国家药监局关于发布医疗器械经营质量管理规范的公告

国家药监局关于发布医疗器械经营质量管理规范的公告文章属性•【制定机关】国家药品监督管理局•【公布日期】2023.12.04•【文号】国家药监局公告2023年第153号•【施行日期】2024.07.01•【效力等级】部门规范性文件•【时效性】尚未生效•【主题分类】医疗质量正文国家药监局公告2023年第153号关于发布医疗器械经营质量管理规范的公告为加强医疗器械经营质量管理,规范医疗器械经营行为,促进行业规范发展,保障公众用械安全有效,根据相关法规规章规定,国家药监局修订了《医疗器械经营质量管理规范》,现予发布,自2024年7月1日起施行,原国家食品药品监督管理总局《关于施行医疗器械经营质量管理规范的公告》(2014年第58号)同时废止。
特此公告。
附件:医疗器械经营质量管理规范国家药监局2023年12月4日附件医疗器械经营质量管理规范第一章总则第一条为了加强医疗器械经营质量管理,规范医疗器械经营活动,保证医疗器械安全、有效,根据《医疗器械监督管理条例》《医疗器械经营监督管理办法》等法规规章的规定,制定本规范。
第二条本规范是医疗器械经营质量管理的基本要求。
从事医疗器械经营活动,应当在医疗器械采购、验收、贮存、销售、运输、售后服务等全过程采取有效的质量管理措施,确保医疗器械产品在经营过程中的质量安全与可追溯。
第三条医疗器械经营企业应当严格执行本规范。
医疗器械注册人、备案人销售其注册或者备案的医疗器械,以及医疗器械流通过程中其他涉及贮存与运输医疗器械的,应当符合本规范的相关要求。
第四条医疗器械注册人、备案人依法对上市医疗器械的安全、有效负责,医疗器械经营企业(以下简称企业)对本企业的经营行为负责。
第五条从事医疗器械经营活动,应当按照所经营医疗器械的风险程度实行风险管理,并采取相应的质量管理措施。
第六条企业及其从业者应当诚实守信、依法经营,禁止任何虚假、欺骗行为。
第七条鼓励企业使用信息化手段传递和存储相关政府管理部门制作的电子证照。
医疗器械注册员必备法规

医疗器械注册员必备法规《医疗器械监督管理条例》(国务院令第650号)自2014年6月1日正式实施,条例配套的规章及规范性文件陆续密集出台。
新法规的出台意味着医疗器械企业面临新的机遇和挑战,作为医疗器械注册人熟悉这些必备的法规,对企业正常运行、产品如期顺利上市起到至关重要的作用国家食品药品监督管理总局已经发布和正在征求意见的系列法规文件目录如下,具体内容参见国家食品药品监督管理总局网站。
行政法规1. 医疗器械监督管理条例(国务院令第650号)2. 国务院关于修改《医疗器械监督管理条例》的决定(国务院令第680号)部门规章1. 医疗器械注册管理办法(CFDA局令第4号)2. 体外诊断试剂注册管理办法(CFDA局令第5号)3. 医疗器械说明书和标签管理规定(CFDA局令第6号)4. 医疗器械生产监督管理办法(CFDA局令第7号)医疗器械生产监督管理办法(修正版)(2017年11月21日发布)5. 医疗器械经营监督管理办法(CFDA局令第8号)医疗器械经营监督管理办法(修正版)(2017年11月21日发布)6. 药品医疗器械飞行检查办法(CFDA局令第14号)7. 医疗器械分类规则(CFDA局令第15号)8. 医疗器械使用质量监督管理办法(CFDA局令第18号)9. 医疗器械通用名称命名规则(CFDA局令第19号)10. 医疗器械临床试验质量管理规范(CFDA 国家卫计委令第25号)11. 医疗器械召回管理办法(CFDA局令第29号)12. 体外诊断试剂注册管理办法修正案(CFDA局令第30号)13. 关于调整部分医疗器械行政审批事项审批程序的决定(CFDA局令第32号)14. 医疗器械标准管理办法(CFDA局令第33号)15. 医疗器械网络销售监督管理办法(CFDA局令第38号)产品分类界定1. 关于可降解泪道栓子等53个产品分类界定的通知(食药监办〔2013〕11号)2. 关于体外高频治疗机等47个产品分类界定的通知(食药监办械管〔2013〕31号)3. 关于血细胞分离机用耗材等11个产品分类界定的通知(食药监办械管〔2013〕68号)4. 关于自体富血小板凝胶制备用套装等23个产品分类界定的通知(食药监办械管〔2013〕69号)5. 关于重症及麻醉临床信息系统等9个产品分类界定的通知(食药监办械管〔2013〕109号)6. 关于基因分析仪等3个产品分类界定的通知(食药监办械管〔2014〕8号)7. 关于生物电导扫描仪等11个产品分类界定的通知(食药监办械管〔2014〕10号)8. 关于角膜治疗仪等12个产品分类界定的通知(食药监办械管〔2014〕103号)9. 关于电子宫腔观察镜等30个产品分类界定的通知(食药监办械管〔2014〕149号)10. 关于交联胺化聚乙烯醇泡沫封堵肺减容系统等34个产品分类界定的通知(食药监办械管〔2014〕177号)11. 关于腹腔镜手术用内窥镜自动调控定位装置等61个产品分类界定的通知(食药监办械管〔2014〕198号)12. 关于乳腺摄影立体定位装置等153个产品分类界定的通知(食药监办械管〔2015〕49号)13. 关于人工血管接环等172个产品分类界定的通知(食药监办械管〔2015〕69号)14. 关于恒温核酸扩增检测仪等22个产品分类界定的通知(食药监办械管〔2015〕75号)15. 关于多功能超声骨刀等127个产品分类界定的通知(食药监办械管〔2015〕104号)16. 关于阴茎增大增粗拉伸器具产品分类界定事项的复函(食药监办械管函〔2016〕480号)通告1. 关于发布第一类医疗器械产品目录的通告(CFDA通告2014年第8号)2. 关于发布医疗器械产品技术要求编写指导原则的通告(CFDA通告2014年第9号)3. 关于发布免于进行临床试验的第二类医疗器械目录的通告(CFDA通告2014年第12号)4. 关于发布免于进行临床试验的第三类医疗器械目录的通告(CFDA通告2014年第13号)5. 关于发布需进行临床试验审批的第三类医疗器械目录的通告(CFDA通告2014年第14号)6. 关于医疗器械生产质量管理规范执行有关事宜的通告(CFDA通告2014年第15号)7. 关于发布体外诊断试剂临床试验技术指导原则的通告(CFDA通告2014年第16号)8. 关于发布体外诊断试剂说明书编写指导原则的通告(CFDA通告2014年第17号)9. 关于发布禁止委托生产医疗器械目录的通告(CFDA通告2014年第18号)10. 关于发布医疗器械生产企业供应商审核指南的通告(CFDA通告2015年第1号)11. 关于发布医疗器械临床评价技术指导原则的通告(CFDA通告2015年第14号)12. 关于发布医疗器械产品出口销售证明管理规定的通告(CFDA通告2015年第18号)13. 关于贯彻落实小微企业行政事业性收费优惠政策的通告(CFDA通告2015年第31号)14. 关于生产一次性使用无菌注、输器具产品有关事项的通告(CFDA通告2015年第71号)15. 关于发布医疗器械注册证补办程序等5个相关工作程序的通告(CFDA通告2015年第91号)16. 关于发布医疗器械注册指定检验工作管理规定的通告(CFDA通告2015年第94号)17. 关于发布医疗器械工艺用水质量管理指南的通告(CFDA通告2016年第14号)18. 关于第三类医疗器械生产企业实施医疗器械生产质量管理规范有关事宜的通告(CFDA通告2016年第19号)19. 关于发布《医疗器械临床试验伦理审查申请与审批表范本》等六个文件的通告(CFDA通告2016年第58号)20. 关于发布医疗器械生产企业质量管理体系年度自查报告编写指南的通告(CFDA 通告2016年第76号)21. 关于发布第二批免于进行临床试验医疗器械目录的通告(CFDA通告2016年第133号)22. 关于发布2016年第二批医疗器械临床试验监督抽查项目的通告(CFDA通告2016年第143号)23. 总局关于发布医疗器械生产企业质量控制与成品放行指南的通告(CFDA通告2016年第173号)24. 总局关于发布医疗器械审评沟通交流管理办法(试行)的通告(CFDA通告2017年第19号)25.总局关于发布第三批免于进行临床试验医疗器械目录的通告(CFDA通告2017年第170号)26. 总局关于需审批的医疗器械临床试验申请沟通交流有关事项的通告(CFDA通告2017年第184号)27. 总局关于发布医疗器械注册单元划分指导原则的通告(CFDA通告2017年第187号)28. 总局关于发布移动医疗器械注册技术审查指导原则的通告(CFDA通告2017年第222号)29. 总局关于发布接受医疗器械境外临床试验数据技术指导原则的通告(CFDA通告2018年第13号)政策解读1. 医疗器械抽验和不良事件监测部分(一)(2015年01月22日发布)2. 《医疗器械经营监督管理办法》部分(一)(2015年01月22日发布)3. 《医疗器械生产监督管理办法》部分(一)(2015年01月22日发布)4. 医疗器械注册管理法规解读之一(《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》部分)(2015年02月05日发布)5. 医疗器械注册管理法规解读之二(《医疗器械说明书和标签管理规定》部分)(2015年02月05日发布)6. 关于《药品医疗器械飞行检查办法》的说明(2015年07月08日发布)7. 医疗器械注册管理法规解读之三(关于《医疗器械分类规则》的修订说明)(2015年07月16日)8. 医疗器械注册管理法规解读之四(2015年11月02日发布)9. 医疗器械注册管理法规解读之五(2015年11月19日发布)10. 医疗器械不良事件监测的主要目的和意义(2015年11月25日发布)11. 关于《医疗器械使用质量监督管理办法》的说明(2015年11月30日发布)12. 医疗器械注册管理法规解读之六(2016年01月07日发布)13. 关于《医疗器械通用名称命名规则》的说明(2016年01月27日发布)14. 《医疗器械临床试验质量管理规范》解读(2016年03月23日发布)15. 关于《医疗器械优先审批程序》的说明(2016年10月26日发布)16. 《医疗器械质量管理体系用于法规的要求》标准解读(一)(2017年02月04日发布)17. 《医疗器械质量管理体系用于法规的要求》标准解读(二)(2017年02月04日发布)18. 《医疗器械召回管理办法》解读(2017年02月08日发布)19. 《体外诊断试剂注册管理办法修正案》解读(2017年02月08日发布)20. 《医疗器械网络安全注册技术审查指导原则》解读(2017年03月02日发布)21. 《关于调整部分医疗器械行政审批事项审批程序的决定》解读(2017年04月06日发布)22. 《医疗器械标准管理办法》解读(2017年04月26日发布)23. 《医疗器械召回管理办法》解读之二(2017年05月24日发布)24. 图解政策:2017年器械注册管理改革有这4项重要举措(2017年07月14日发布)25. 图解政策:体外诊断试剂注册管理办法修正案(2017年07月28日发布)26. 创新医疗器械特别审批程序相关问题解读(2017年07月31日发布)27. 医疗器械临床试验质量管理相关问题解读(2017年07月31日发布)28. 《医疗器械标准管理办法》解读之一(2017年08月09日发布)29. 《医疗器械标准管理办法》解读之二(2017年08月09日发布)30. 《医疗器械网络安全注册技术审查指导原则》解读(2017年08月09日发布)31. 《医疗器械临床试验机构条件和备案管理办法》解读(2017年11月24日发布)32. 《医疗器械网络销售监督管理办法》解读(2017年12月22日发布)33. 《移动医疗器械注册技术审查指导原则》解读(2017年12月29日发布)通知性文件1. 关于进一步做好医疗器械产品分类界定工作的通知(食药监办械〔2013〕36号)2. 关于小型医用吸氧器监管有关问题的通知(食药监办法〔2013〕63号)3. 关于实施避孕套出口备案管理的通知(食药监办械监〔2013〕72号)4. 关于进一步加强医疗器械不良事件监测体系建设的指导意见(食药监械监〔2013〕205号)5. 关于印发医疗器械质量监督抽查检验管理规定的通知(食药监械监〔2013〕212号)6. 关于加强省级医疗器械技术审评能力建设的指导意见(食药监械管〔2013〕220号)7. 关于印发医疗器械生产日常监督现场检查工作指南的通知(食药监办械监〔2014〕7号)8. 关于印发创新医疗器械特别审批程序(试行)的通知(食药监械管〔2014〕13号)9. 关于认真贯彻实施《医疗器械监督管理条例》的通知(食药监法〔2014〕31号)10. 关于进一步做好医疗器械召回信息公开工作的通知(食药监办械监〔2014〕107号)11. 关于实施《医疗器械生产监督管理办法》和《医疗器械经营监督管理办法》有关事项的通知(食药监械监〔2014〕143号)12. 关于实施《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》有关事项的通知(食药监械管〔2014〕144号)13. 关于实施第一类医疗器械备案有关事项的通知(食药监办械管〔2014〕174号)14. 关于印发医疗器械检验机构开展医疗器械产品技术要求预评价工作规定的通知(食药监械管〔2014〕192号)15. 关于印发境内第三类和进口医疗器械注册审批操作规范的通知(食药监械管〔2014〕208号)16. 关于印发境内第二类医疗器械注册审批操作规范的通知(食药监械管〔2014〕209号)17. 关于印发医疗器械生产企业分类分级监督管理规定的通知(食药监械监〔2014〕234号)18. 关于印发国家重点监管医疗器械目录的通知(食药监械监〔2014〕235号)19. 关于启用医疗器械生产经营许可备案信息系统的通知(食药监办械监函〔2014〕476号)20. 关于加强避孕套质量安全管理的通知(食药监械监〔2015〕30号)21. 关于印发体外诊断试剂质量评估和综合治理工作方案的通知(食药监办械监〔2015〕55号)22. 关于印发境内第三类医疗器械注册质量管理体系核查工作程序(暂行)的通知(食药监械管〔2015〕63号)23. 关于对取消和下放行政审批事项加强事中事后监管的意见(食药监法〔2015〕65号)24. 关于印发医疗器械经营企业分类分级监督管理规定的通知(食药监械监〔2015〕158号)25. 关于印发医疗器械经营环节重点监管目录及现场检查重点内容的通知(食药监械监〔2015〕159号)26. 关于印发医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知(食药监械监〔2015〕218号)27. 关于印发医疗器械经营质量管理规范现场检查指导原则的通知(食药监械监〔2015〕239号)28. 关于执行医疗器械和体外诊断试剂注册管理办法有关问题的通知(食药监械管〔2015〕247号)29. 关于印发医疗器械检验机构资质认定条件的通知(食药监科〔2015〕249号)30. 关于成立医疗器械分类技术委员会的通知(食药监械管〔2015〕259号)31. 关于进一步加强医疗器械抽验工作的通知(食药监办械监〔2016〕9号)32. 关于切实做好第三类医疗器械生产企业实施医疗器械生产质量管理规范有关工作的通知(食药监办械监〔2016〕12号)33. 关于医疗器械产品技术要求有关问题的通知(食药监办械管〔2016〕22号)34. 总局关于实施《医疗器械通用名称命名规则》有关事项的通知(食药监械管〔2016〕35号)35. 总局关于印发一次性使用无菌注射器等25种医疗器械生产环节风险清单和检查要点的通知(食药监械监〔2016〕37号)。
国家食品药品监督管理总局关于施行医疗器械经营质量管理规范的公告(2014年第58号)

国家食品药品监督管理总局关于施行医疗器械经营质量管理规范的公告(2014年第58号)2014年12月12日发布国家食品药品监督管理总局公告2014年第58号关于施行医疗器械经营质量管理规范的公告为加强医疗器械经营质量管理,规范医疗器械经营管理行为,保证公众用械安全,国家食品药品监督管理总局根据相关法规规章规定,制定了《医疗器械经营质量管理规范》,现予公布,自公布之日起施行。
特此公告。
附件:医疗器械经营质量管理规范国家食品药品监督管理总局2014年12月12日附件医疗器械经营质量管理规范第一章总则第一条为加强医疗器械经营质量管理,规范医疗器械经营管理行为,保证医疗器械安全、有效,根据《医疗器械监督管理条例》和《医疗器械经营监督管理办法》等法规规章规定,制定本规范。
第二条本规范是医疗器械经营质量管理的基本要求,适用于所有从事医疗器械经营活动的经营者。
医疗器械经营企业(以下简称企业)应当在医疗器械采购、验收、贮存、销售、运输、售后服务等环节采取有效的质量控制措施,保障经营过程中产品的质量安全。
第三条企业应当按照所经营医疗器械的风险类别实行风险管理,并采取相应的质量管理措施。
第四条企业应当诚实守信,依法经营。
禁止任何虚假、欺骗行为。
第二章职责与制度第五条企业法定代表人或者负责人是医疗器械经营质量的主要责任人,全面负责企业日常管理,应当提供必要的条件,保证质量管理机构或者质量管理人员有效履行职责,确保企业按照本规范要求经营医疗器械。
第六条企业质量负责人负责医疗器械质量管理工作,应当独立履行职责,在企业内部对医疗器械质量管理具有裁决权,承担相应的质量管理责任。
第七条企业质量管理机构或者质量管理人员应当履行以下职责:(一)组织制订质量管理制度,指导、监督制度的执行,并对质量管理制度的执行情况进行检查、纠正和持续改进;(二)负责收集与医疗器械经营相关的法律、法规等有关规定,实施动态管理;(三)督促相关部门和岗位人员执行医疗器械的法规规章及本规范;(四)负责对医疗器械供货者、产品、购货者资质的审核;(五)负责不合格医疗器械的确认,对不合格医疗器械的处理过程实施监督;(六)负责医疗器械质量投诉和质量事故的调查、处理及报告;(七)组织验证、校准相关设施设备;(八)组织医疗器械不良事件的收集与报告;(九)负责医疗器械召回的管理;(十)组织对受托运输的承运方运输条件和质量保障能力的审核;(十一)组织或者协助开展质量管理培训;(十二)其他应当由质量管理机构或者质量管理人员履行的职责。
2014-2018医疗器械法规文件大汇总

2014年1.国家食品药品监督管理总局关于发布医疗器械生产质量管理规范的公告(2014年第64号)/WS01/CL0087/111642.html2.《国家食品药品监督管理总局关于施行医疗器械经营质量管理规范的公告》(2014年第58号)/WS01/CL1294/110920.html3.关于医疗器械(含体外诊断试剂)注册申报有关问题的公告(2014年第129号)/WS01/CL0068/109780.html4.食品药品监管总局关于印发国家重点监管医疗器械目录的通知食药监械监〔2014〕235号/WS01/CL0845/107405.html5.食品药品监管总局关于印发医疗器械生产企业分类分级监督管理规定的通知食药监械监〔2014〕234号/WS01/CL0845/107404.html6.国家食品药品监督管理总局关于发布禁止委托生产医疗器械目录的通告(2014年第18号)/WS01/CL0087/107065.html7.食品药品监管总局办公厅关于实施第一类医疗器械备案有关事项的通知食药监办械管〔2014〕174号/WS01/CL0845/106435.html8.食品药品监管总局关于印发境内第二类医疗器械注册审批操作规范的通知食药监械管〔2014〕209号/WS01/CL0845/106258.html9.食品药品监管总局关于印发境内第三类和进口医疗器械注册审批操作规范的通知食药监械管〔2014〕208号/WS01/CL0845/106257.html10.国家食品药品监督管理总局关于发布体外诊断试剂说明书编写指导原则的通告(2014年第17号)/WS01/CL0087/106242.html11.国家食品药品监督管理总局关于发布体外诊断试剂临床试验技术指导原则的通告(2014年第16号)/WS01/CL0087/106241.html12.国家食品药品监督管理总局关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告(2014年第44号)/WS01/CL0087/106096.html13.国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)/WS01/CL0087/106095.html14.国家食品药品监督管理总局关于医疗器械生产质量管理规范执行有关事宜的通告(2014年第15号)/WS01/CL0087/106114.html15.国家食品药品监督管理总局关于发布需进行临床试验审批的第三类医疗器械目录的通告(2014年第14号)/WS01/CL0087/105374.html16.食品药品监管总局关于印发医疗器械检验机构开展医疗器械产品技术要求预评价工作规定的通知(食药监械管〔2014〕192号)/WS01/CL0845/105194.html17.国家食品药品监督管理总局关于发布免于进行临床试验的第三类医疗器械目录的通告(2014年第13号)/WS01/CL0087/105225.html18.国家食品药品监督管理总局关于发布免于进行临床试验的第二类医疗器械目录的通告(2014年第12号)/WS01/CL0087/105224.html19.食品药品监管总局关于实施《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》有关事项的通知(食药监械管〔2014〕144号)/WS01/CL0845/103802.html20.食品药品监管总局关于实施《医疗器械生产监督管理办法》和《医疗器械经营监督管理办法》有关事项的通知(食药监械监〔2014〕143号)/WS01/CL0845/103801.html21.《医疗器械说明书和标签管理规定》(总局令第6号)/WS01/CL0053/103758.html22.《体外诊断试剂注册管理办法》(总局令第5号)/WS01/CL0053/103757.html23.《医疗器械注册管理办法》(总局令第4号)/WS01/CL0053/103756.html24.国家食品药品监督管理总局关于发布医疗器械产品技术要求编写指导原则的通告(2014年第9号)/WS01/CL0087/100814.html25.国家食品药品监督管理总局关于发布第一类医疗器械产品目录的通告(2014年第8号)/WS01/CL0087/100815.html26.国家食品药品监督管理总局关于第一类医疗器械备案有关事项的公告(2014年第26号)/WS01/CL0087/100816.html27.国家食品药品监督管理总局关于医疗器械生产经营备案有关事宜的公告(2014年第25号)/WS01/CL0087/100800.html28.国家食品药品监督管理总局关于贯彻实施《医疗器械监督管理条例》有关事项的公告(2014年第23号)/WS01/CL0087/100480.html29.《医疗器械监督管理条例》(国务院令第650号)/WS01/CL0784/97814.html30.总局关于印发创新医疗器械特别审批程序(试行)的通知(食药监械管〔2014〕13号)/WS01/CL0845/96654.html2015年1.《医疗器械通用名称命名规则》(总局令第19号)/WS01/CL0053/139000.html2.国家食品药品监督管理总局关于发布医疗器械注册指定检验工作管理规定的通告(2015年第94号)/WS01/CL0087/136660.html3.国家食品药品监督管理总局关于发布医疗器械注册证补办程序等5个相关程序的通告(2015年第91号)/WS01/CL0087/135860.html4.国家食品药品监督管理总局关于规范含银盐医疗器械注册管理有关事宜的公告(2015年第225号)/WS01/CL0087/134580.html5.食品药品监管总局关于执行医疗器械和体外诊断试剂注册管理办法有关问题的的通知(食药监械管〔2015〕247号)/WS01/CL0845/134021.html6.国家食品药品监督管理总局关于境内医疗器械生产企业跨省新开办企业时办理产品注册及生产许可有关事宜的公告(2015年第203号)/WS01/CL0087/133069.html7.《医疗器械使用质量监督管理办法》(总局令第18号)/WS01/CL0053/132880.html8.食品药品监管总局关于印发医疗器械医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知(食药监械监〔2015〕218号)/WS01/CL0845/130869.html9.关于体外诊断试剂临床试验机构盖章有关事宜的公告(2015年第154号)/WS01/CL0068/128860.html10.《医疗器械分类规则》(总局令第15号)/WS01/CL0053/124222.html11.国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录体外诊断试剂的公告(2015年第103号)/WS01/CL0087/124119.html12.国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录植入性医疗器械的公告(2015年第102号)/WS01/CL0087/124118.html13.国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录无菌医疗器械的公告(2015年第101号)/WS01/CL0087/124117.html14.国家食品药品监督管理总局关于发布医疗器械临床试验备案有关事宜的公告(2015年第87号)/WS01/CL0087/123460.html15.食品药品监管总局关于印发境内第三类医疗器械注册质量管理体系核查工作程序(暂行)的通知(食药监械管〔2015〕63号)/WS01/CL0845/121049.html16.《国家食品药品监督管理总局关于发布药品、医疗器械产品注册收费标准的公告》(2015年第53号)/WS01/CL1294/120201.html17.国家食品药品监督管理总局关于发布医疗器械临床评价技术指导原则的通告(2015年第14号)/WS01/CL0087/119643.html18.国家食品药品监督管理总局关于发布医疗器械生产企业供应商审核指南的通告(2015年第1号)/WS01/CL0087/112629.html2016年1.总局关于发布医疗器械生产企业质量控制与成品放行指南的通告(2016年第173号)/WS01/CL1294/168287.html2.总局关于发布医疗器械优先审批程序的公告(2016年第168号)/WS01/CL0087/165582.html3.总局关于发布第二批免于进行临床试验医疗器械目录的通告(2016年第133号)/WS01/CL0087/164956.html4.总局办公厅关于体外诊断试剂说明书文字性变更有关问题的通知(食药监办械管〔2016〕117号)/WS01/CL0845/161645.html5.总局办公厅关于贯彻实施《医疗器械临床试验质量管理规范》的通知(食药监办械管〔2016〕41号)/WS01/CL0845/149540.html6.总局关于实施《医疗器械通用名称命名规则》有关事项的通知(食药监械管〔2016〕35号)/WS01/CL0845/148881.html7.《医疗器械临床试验质量管理规范》(总局、卫计委令第25号)/WS01/CL0053/148101.html8.总局关于发布《医疗器械临床试验伦理审查申请与审批表范本》等六个文件的通告(2016年第58号)/WS01/CL0087/148126.html9.总局办公厅关于医疗器械产品技术要求有关问题的通知(食药监办械管〔2016〕22号)/WS01/CL0845/145601.html10.总局关于第三类医疗器械生产企业实施医疗器械生产质量管理规范有关事宜的通告(2016年第19号)/WS01/CL1294/144100.html2017年1.总局办公厅关于做好医疗器械检验有关工作的通知(食药监办械管〔2017〕187号)/WS01/CL0845/221407.html2.总局关于过敏原类、流式细胞仪配套用、免疫组化和原位杂交类体外诊断试剂产品属性及类别调整的通告(2017年第226号)/WS01/CL1294/220850.html3.《医疗器械网络销售监督管理办法》(总局令第38号)/WS01/CL1101/220098.html4.国家食品药品监督管理总局国家卫生和计划生育委员会关于发布医疗器械临床试验机构条件和备案管理办法的公告(2017年第145号)/WS01/CL0087/217367.html5.总局办公厅关于做好医疗器械临床试验机构备案工作的通知(食药监办械管〔2017〕161号)/WS01/CL0845/217380.html6.《医疗器械经营监督管理办法》(总局令第8号)(2017-11-21修订)/WS01/CL0053/217162.html7.《医疗器械生产监督管理办法》(总局令第7号)(2017-11-21修订)/WS01/CL1101/217161.html8.总局关于需审批的医疗器械临床试验申请沟通交流有关事项的通告(2017年第184号)/WS01/CL0087/216841.html9.总局关于进口医疗器械注册申请人和备案人名称使用中文的公告(2017年第131号)/WS01/CL0087/216229.html10.总局关于医疗器械经营备案有关事宜的公告(2017年第129号)/WS01/CL0050/216296.html11.总局办公厅关于规范医疗器械产品分类有关工作的通知(食药监办械管〔2017〕127号)/WS01/CL0845/177958.html12.总局关于发布聚氯乙烯输液输血器具中荧光物质识别及定量补充检验方法的公告(2017年第110号)/WS01/CL1294/177496.html13.总局关于实施《医疗器械分类目录》有关事项的通告(2017年第143号)/WS01/CL0087/177087.html14.总局关于发布医疗器械分类目录的公告(2017年第104号)/WS01/CL0087/177089.html15.总局办公厅关于印发2017年医疗器械行业标准制修订项目的通知(食药监办械管〔2017〕94号)/WS01/CL0845/174746.html16.总局关于贯彻实施《国务院关于修改〈医疗器械监督管理条例〉的决定》有关事项的公告(2017年第78号)/WS01/CL0087/174096.html17.《医疗器械标准管理办法》(总局令第33号)/WS01/CL0053/172049.html18.总局办公厅关于印发国家食品药品监督管理总局医疗器械分类技术委员会工作规则的通知(食药监办械管〔2017〕56号)/WS01/CL0845/171682.html19.《国家食品药品监督管理总局关于调整部分医疗器械行政审批事项审批程序的决定》(总局令第32号)/WS01/CL0053/171404.html20.总局关于成立医疗器械分类技术委员会专业组的通知(食药监械管〔2017〕27号)/WS01/CL0845/171324.html21.总局关于发布医疗器械技术审评专家咨询委员会管理办法的公告(2017年第36号)/WS01/CL0087/171212.html22.总局关于发布医疗器械优先审批申报资料编写指南(试行)的通告(2017年第28号)/WS01/CL0087/169620.html23.《体外诊断试剂注册管理办法修正案》(总局令第30号)/WS01/CL0053/169364.html24.《医疗器械召回管理办法》(总局令第29号)/WS01/CL0053/169345.html25.总局关于发布医疗器械审评沟通交流管理办法(试行)的通告(2017年第19号)/WS01/CL0087/169361.html2018年(截至5月7日)1. 总局办公厅关于实施《医疗器械网络销售监督管理办法》有关事项的通知(食药监办械监〔2018〕31号)/WS01/CL0050/225541.html2. 关于发布《自行取消进口第一类医疗器械备案工作程序》的公告(第206号)/WS01/CL0068/224399.html3. 国家药品监督管理局办公室关于公开征求《创新医疗器械特别审批程序(修订稿征求意见稿)》的意见/WS04/CL2051/227922.html。
北京市食品药品监督管理局关于落实《医疗器械经营企业分类分级监督管理规定》的指导意见

北京市食品药品监督管理局关于落实《医疗器械经营企业分类分级监督管理规定》的指导意见文章属性•【制定机关】北京市食品药品监督管理局•【公布日期】2016.05.05•【字号】•【施行日期】2016.05.05•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】卫生医药、计划生育其他规定正文北京市食品药品监督管理局关于落实《医疗器械经营企业分类分级监督管理规定》的指导意见各区局,各直属分局:为建立以分类管理为基础、以风险高低为导向、以过程监督为重点的工作机制,根据《医疗器械监督管理条例》(国务院令第650号)、《医疗器械经营监督管理办法》(国家食品药品监督管理总局令第8号)、《食品药品监管总局关于印发医疗器械经营企业分类分级监督管理规定的通知》(食药监械监〔2015〕158号),现就我市医疗器械经营企业分类分级监督管理工作提出如下指导意见。
一、监管级别划分(一)三级监管三级监管(以下简称“Ⅲ级”)为风险最高级别的监管,对下列医疗器械经营企业实施三级监管:1.经营国家食品药品监督管理总局《医疗器械经营环节重点监管目录及现场检查重点内容》(以下简称《重点监管目录》)所列品种的;2.为其他医疗器械生产经营企业提供贮存、配送服务的;3.上年度被行政处罚且整改不到位的;4.存在不良信用记录的。
(二)二级监管二级监管(以下简称“Ⅱ级”)为风险一般级别的监管,对Ⅲ级以外的从事第二、三类医疗器械批发经营的企业实施二级监管。
(三)一级监管一级监管(以下简称“Ⅰ级”)为风险较低级别的监管,对Ⅲ级、Ⅱ级以外的从事其他类医疗器械经营的企业实施一级监管。
对涉及多个监管级别的经营企业实施最高级别的监管。
二、监督管理措施(一)三级监管措施1.对经营《重点监管目录》无菌类、植入材料和人工器官类、体外诊断试剂类、设备仪器类中所列品种的企业,每年现场检查不得少于一次,按照《北京市医疗器械经营质量管理规范现场检查评定细则》(以下简称《检查评定细则》),以《重点监管目录》列出的检查内容为重点,逐条检查。
食品药品监管总局关于印发医疗器械经营质量管理规范现场检查指导原则的通知

※2.7
企业质量管理机构或者质量管理人员应当履行以下职责:
(一)组织制订质量管理制度,指导、监督制度的执行,并对质量管理制度的执行情况进行检查、纠正和持续改进;
(二)负责收集与医疗器械经营相关的法律、法规等有关规定,实施动态管理;
(三)督促相关部门和岗位人员执行医疗器械的法规、规章及规范;
(四)负责对医疗器械供货者、产品、购货者资质的审核;
医疗器械经营质量管理规范
现场检查指导原则
章节
条款
内容
职
责
与
制
度
2.5.1
企业法定代表人或者负责人是医疗器械经营质量的主要责任人,全面负责企业日常管理。
重点查看企业相关制度文件或职责权限文件,确认文件内容是否明确企业法定代表人或者负责人是医疗器械经营质量的主要负责人;查看法定代表人或者负责人履行职责的相关记录(如法定代表人或者负责人授权文件、任命文件签发,资源配置批准,重大事项决定等),确认其是否全面负责企业日常管理工作。
(十)医疗器械召回规定(包括医疗器械召回记录等);
(十一)设施设备维护及验证和校准的规定(包括设施设备相关记录和档案等);
(十二)卫生和人员健康状况的规定(包括员工健康档案等);
(十三)质量管理培训及考核的规定(包括培训记录等);
(十四)医疗器械质量投诉、事故调查和处理报告的规定(包括质量投诉、事故调查和处理报告相应的记录及档案等);
重点监管目录及措施
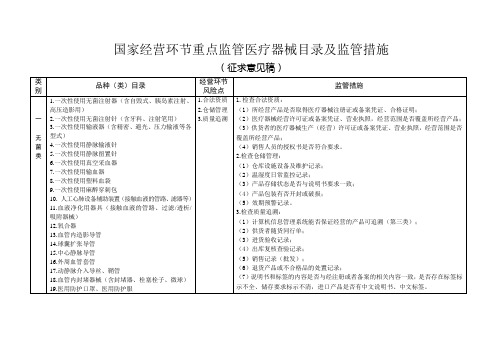
4.售后管理
1.检查合法资质:
(1)所经营产品是否取得医疗器械注册证或备案凭证.合格证明;
(2)医疗器械经营许可证或备案凭证、营业执照,经营范围是否覆盖所经营产品;
(3)供货者的医疗器械生产(经营)许可证或备案凭证、营业执照,经营范围是否覆盖所经营产品;
(4)销售人员的授权书是否符合要求。
2.脊柱内固定器材
3.人工关节
4.人工晶体
5.血管支架(含动静脉及颅内等中枢及外周血管用支架)
6.心脏缺损修补/封堵器械
7.人工心脏瓣膜
8.血管吻合器械(含血管吻合器、动脉瘤夹)
9.组织填充材料(含乳房、整形及眼科填充等)
10.医用可吸收缝线
11.同种异体医疗器械
12.动物源医疗器械
1.合法资质
2.仓储管理
(3)供货者的医疗器械生产(经营)许可证或备案凭证、营业执照,经营范围是否覆盖所经营产品;
(4)销售人员的授权书是否符合要求。
2.检查仓储管理:
(1)仓库设施设备及维护记录;
(2)温湿度日常监控记录;
(3)产品存储状态是否与说明书要求一致。
3.检查质量追溯:
(1)计算机信息管理系统能否保证经营的产品可追溯;
4.检查验光专业要求:
(1)是否配备验光专业或有职业资格的人员;
(2)是否设有检查区(门店、不含角膜塑形镜);
(3)是否配备电脑验光仪、裂隙灯显微镜等仪器设备,查看使用维护记录(门店、不含角膜塑形镜)。
五
设
备
仪
器
类
1.人工心肺设备
2.血液净化用设备
3.婴儿保育设备(含各类培养箱、抢救台)
4.麻醉机/麻醉呼吸机
2.检查仓储管理:
医疗器械重点监管产品目录

医疗器械重点监管产品目录
1.一次性使用无菌医疗器械(输注器具、塑料血袋、采血器等)
2.植入(介入)性等高风险医疗器械(心脏起搏器、心脏瓣膜、心血管支架、导管导丝导鞘、骨科内固定器械、栓塞器械、人工血管、宫内节育器等)、医用可吸收缝合线;
3.体外诊断试剂(用于微生物鉴别或药敏试验的微生物培养基,血液配型、艾滋病、梅毒、甲肝、乙肝、丙肝、结核、甲胎蛋白、癌胚抗原等检测试剂);
4.医用分子筛制氧设备、婴儿培养箱、血液透析设备、呼吸机、输注泵;
5.超声诊断仪、X射线设备。
6.注射用透明质酸钠、角膜接触镜(含装饰性平光隐形眼镜、角膜塑形镜)、避孕套;
7.体验式销售的物理康复治疗设备、高电位治疗仪、电场治疗仪、光波康复理疗仪;
附件2:
2019年无菌和植入性等医疗器械经营企业自查要点企业名称(盖章):
自查人员:自查日期:
质量负责人签名:联系方式:企业法定代表人或企业负责人签名:联系方式:
附件3:
2019年医疗器械使用质量管理自查表单位名称(盖章):
自查人员:自查日期:
质量负责人签名:联系方式:
单位法定代表人或负责人签名:联系方式:
2019年无菌和植入性等医疗器械经营使用单位监督检查情况汇总表上报单位(公章)
填表人:联系电话:
2019年经营角膜接触镜类检查情况统计表报送单位(盖章):填报年度:年度
填表人:填表时间:年月日
2019年避孕套质量安全管理工作统计表报送单位(盖章):填报年度:年度
填表人:填表时间:年月日。
2015出台的医疗器械政策汇总表

完整版:2015医疗器械政策汇总一、分类界定序号分类界定颁发机构日期1 食品药品监管总局办公厅关于乳腺摄影立体定位装置等153个产品分类界定的通知(食药监办械管〔2015〕49号)最新15个Ⅲ类医疗器械分类界定总局 3.31最新58个Ⅱ类医疗器械分类界定最新51个Ⅰ类医疗器械分类界定最新29个非医疗器械分类界定2 食品药品监管总局办公厅关于人工血管接环等172个产品分类界定的通知(食药监办械管〔2015〕69号))总局受理中心5.183 食品药品监管总局办公厅关于恒温核酸扩增检测仪等22个产品分类界定的通知(食药监办械管〔2015〕75号)总局受理中心6.114 食品药品监管总局办公厅关于多功能超声骨刀等127个产品分类界定的通知(食药监办械管〔2015〕104号)总局受理中心7.2二、政策法规序号法规名称颁发机构日期1 食品药品监管总局关于加强避孕套质量安全管理的通知(食药监械监〔2015〕30号)总局 3.232 食品药品监管总局办公厅关于印发体外诊断试剂质量评估和综合治理工作方案的通知(食药监办械监〔2015〕55号)总局 4.073 主动脉覆膜支架系统临床试验审评要点医疗器械技术审评中心4.234 全降解冠状动脉药物洗脱支架临床试验审评要点医疗器械技术审评中心4.235 国务院关于印发《中国制造2025》的通知(国发〔2015〕28号)国务院 5.86 国家发展改革委、财政部关于印发《药品、医疗器械产品注册收费标准管理办法》的通知(发改价格[2015]1006号)国家发展改革委5.127 食品药品监管总局关于印发境内第三类医疗器械注册质量管理体系核查工作程序(暂行)的通知(食药监械管〔2015〕63号)总局 6.088 食品药品监管总局关于对取消和下放行政审批事项加强事中事后监管的意见(食药监法〔2015〕65号)总局 6.99 《药品医疗器械飞行检查办法》(国家食品药品监督管理总局令第14号)总局 6.2910 《医疗器械分类规则》(国家食品药品监督管理总局令第15号)总局7.1411 食品药品监管总局办公厅关于经营免验配耳背式数字助听器有关问题的复函(食药监办械监函〔2015〕414号)总局7.1412 欧洲通过医疗器械和体外诊断器械新法规提案的普遍方法商务部7.213 食品药品监管总局关于进一步加强药品医疗器械保健食品广告审查监管工作的通知(食药监稽〔2015〕145号)总局7.3114 国家卫生计生委医政医管局关于印发《药物代谢酶和药物作用靶点基因检测技术指南(试行)》和《肿瘤个体化治疗检测技术指南(试行)》的通知国家卫生计生委7.3115 食品药品监管总局发布医疗器械软件注册技术审查指导原则总局8.716 食品药品监管总局关于印发医疗器械经营企业分类分级监督管理规定的通知(食药监械监〔2015〕158号)总局8.1717 食品药品监管总局关于印发医疗器械经营环节重点监管目录及现场检查重点内容的通知(食药监械监〔2015〕159号)总局8.1718 国务院关于改革药品医疗器械审评审批制度的意见(国发〔2015〕44号)国务院8.1819 食品药品监管总局介绍药品医疗器械审评审批制度改革情况中国政府8.1820 食品药品监管总局办公厅关于个体工商户从事医疗器械经营活动有关问题的复函(食药监办械监函〔2015〕533号)总局9.0221 食品药品监管总局办公厅关于启用医疗器械注册管理信息系统备案子系统的通知(食药监办械管函〔2015〕534号)总局9.0222 食品药品监管总局关于印发医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知(食药监械监〔2015〕218号)总局9.2523 食品药品监管总局印发《医疗器械生产质量管理规范现场检查指导原则》等4个现场检查指导原则总局10.124 食品药品监管总局等部门关于印发开展打击非法制售和使用注射用透明质酸钠行为专项行动工作方案的通知(食药监械监〔2015〕236号)总局10.1425 食品药品监管总局关于印发医疗器械经营质量管理规范现场检查指导原则的通知(食药监械监〔2015〕239号)总局10.1526 《医疗器械使用质量监督管理办法》(国家食品药品监督管理总局令第18号)总局10.2127 食品药品监管总局办公厅关于经营体外诊断试剂相关问题的复函(食药监办械监函〔2015〕646号)总局10.2228 食品药品监管总局发布医疗器械使用质量监督管理办法总局10.2329 医疗器械注册管理法规解读之四总局11.230 食品药品监管总局关于执行医疗器械和体外诊断试剂注册管理办法有关问题的通知(食药监械管〔2015〕247号)总局11.431 食品药品监管总局关于印发医疗器械检验机构资质认定条件的通知(食药监科〔2015〕249号)总局11.432 医疗器械注册管理法规解读之五总局11.1933 关于《医疗器械使用质量监督管理办法》的说明总局11.334 《医疗器械通用名称命名规则》(国家食品药品监督管理总局令第19号)总局12.21三、公告/通知/通告/通报序号公告、通知、通告、通报颁发机构日期1国家食品药品监督管理总局关于发布医疗器械生产企业供应商审核指南的通告(2015年第1号)总局 1.192关于调整行政许可事项申报资料接收方式的公告(第133号)总局受理中心 1.303关于采用签收方式接收申报资料的公告(第136号)总局受理中心 2.124关于医用电气设备受理有关问题的公告(第137号)总局受理中心 2.275关于国家食品药品监督管理总局食品安全监管三司、医疗器械注册管理司咨询安排的公告(第139号)总局受理中心 2.286关于调整行政受理、制证咨询服务电话接听安排的公告(第140号)总局受理中心 2.287国家食品药品监督管理总局关于批准发布YY 0572-2015《血液透析及相关治疗用水》等90项医疗器械行业标准的公告(2015年第8号)总局 3.028国家食品药品监督管理总局药物临床试验机构资格认定复核检查公告(第4号)总局 3.199关于调整注册申报资料接收方式的公告(第141号)总局受理中心 3.2010关于医疗器械(含体外诊断试剂)延续注册申报资料有关问题的公告(第144号)总局受理中心 3.3111关于医疗器械延续注册申请过渡期相关问题的公告(第143号)总局受理中心 3.3112关于印发《体外诊断试剂抽验工作方案》的通知(食药监械监便函〔2015〕37号)总局器械监管司4.813国家食品药品监督管理总局关于发布生物制品稳定性研究技术指导原则的通告(2015年第10号)总局 4.1514国家食品药品监督管理总局关于发布雌激素受体、孕激素受体抗体试剂及检测试剂盒技术审查指导原则的通告(2015年第11号)总局 4.1715国家食品药品监督管理总局关于注销医疗器械注册证书的公告(2015年第12号)总局 4.1716国家食品药品监督管理总局关于发布医疗器械临床评价技术指导原则的通告(2015年第14号)总局 5.1917第一批优秀国产医疗设备品目遴选顺利完成国家卫生计生委5.2118国家食品药品监督管理总局关于发布药品、医疗器械产品注册收费标准的公告(2015年第53号)总局 5.2719国家食品药品监督管理总局关于发布医疗器械产品出口销售证明管理规定的通告(2015年第18号)总局 6.0120国家食品药品监督管理总局关于发布《中华人民共和国药典》(2015年版)的公告(2015年第67号)总局 6.0521关于执行《国家食品药品监督管理总局关于发布医疗器械产品出口销售证明管理规定的通告》有关事宜的公告(第148号)总局受理中心 6.2422关于调整注册申报资料接收方式的公告(第150号)总局受理中心7.0123国家卫生计生委关于取消第三类医疗技术临床应用准入审批有关工作的通知国家卫生计生委7.224关于发布《前列腺特异性抗原检测前列腺癌临床应用》等4项推荐性卫生行业标准的通告国家卫生计生委7.225国家食品药品监督管理总局关于医疗器械临床试验备案有关事宜的公告(2015年第87号)总局7.0326国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录体外诊断试剂的公告(2015年第103号)总局7.127国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录无菌医疗器械的公告(2015年第101号)总局7.128国家食品药品监督管理总局关于发布医疗器械生产质量管理规范附录植入性医疗器械的公告(2015年第102号)总局7.129国家发展改革委关于实施增强制造业核心竞争力重大工程包的通知(发改产业[2015]1602号)国家发展改革委7.1330国家食品药品监督管理总局关于贯彻落实小微企业行政事业性收费优惠政策的通告(2015年第31号)总局7.1431国家食品药品监督管理总局关于发布乙型肝炎病毒基因分型检测试剂技术审查指导原则的通告(2015年第32号)总局7.1532国家食品药品监督管理总局关于发布影像型超声诊断设备新技术注册技术审查指导原则的通告(2015年第33号)总局7.1533关于办理受理和领取批件等行政许可事项的公告(第151号)总局受理中心7.1634食品药品监管总局办公厅关于印发2015年国家医疗器械抽验产品检验方案的通知(食药监办械监〔2015〕100号)总局7.1635国家医疗器械不良事件监测年度报告(2014年度)总局7.236第二批优秀国产医疗设备产品遴选工作启动国家卫生计生委7.23372014年度食品药品监管统计年报总局7.2438国家医疗器械质量公告(2015年第1期,总第6期)总局7.2439关于发布医疗器械软件注册技术审查指导原则的通告(2015年第50号)总局8.0540国家医疗器械质量公告(2015年第2期,总第7期)总局9.241食品药品监管总局办公厅关于启用医疗器械注册管理信息系统备案子系统的通知(食药监办械管函〔2015〕534号)总局9.242关于体外诊断试剂临床试验机构盖章有关事宜的公告(第154号)总局受理中心9.0943国家食品药品监督管理总局关于发布结核分枝杆菌复合群核酸检测试剂注册技术审查指导原则的通告(2015年第65号)总局9.2144关于对部分发补未回的申报资料进行退审的公告医疗器械技术审评中心9.2245国家食品药品监督管理总局关于境内医疗器械生产企业跨省新开办企业时办理产品注册及生产许可有关事宜的公告(2015年第203号)总局10.2146国家食品药品监督管理总局关于规范含银盐医疗器械注册管理有关事宜的公告(2015年第225号)总局11.947国家食品药品监督管理总局关于发布药物临床试验数据现场核查要点的公告(2015年第228号)总局11.148关于药品注册审评审批若干政策的公告(2015年第230号)总局11.1149医疗器械不良事件信息通报(2015年第1-3期)总局11.1250国家食品药品监督管理总局关于征求《关于解决药品注册申请积压实行优先审评审批的意见(征求意见稿)》意见的公告(2015年第227号)总局11.1351国家食品药品监督管理总局关于发布丙型肝炎病毒核糖核酸测定试剂等4个医疗器械技术审查指导原则的通告(2015年第93号)总局11.2652医疗器械不良事件监测的主要目的和意义总局11.2653国家食品药品监督管理总局关于发布医疗器械注册指定检验工作管理规定的通告(2015年第94号)总局11.2754国家食品药品监督管理总局首次组织开展对境外医疗器械生产企业生产现场检查总局12.255食品药品监管总局办公厅关于医疗器械检验机构资质认定条件有关事项的通知(食药监办科函〔2015〕775号)总局12.756广东省探索试行《第二类创新医疗器械特别审批程序》总局12.1157食品药品监管总局办公厅关于启用医疗器械注册管理信息系统受理和制证、技术审评、行政审批子系统的通知(食药监办械管函〔2015〕804号)总局12.1558国家食品药品监管总局出台食品药品领域主要信访事项法定办理途径及相关法律依据总局12.2159广东省率先实施医疗器械注册无纸化审评审批总局12.2260关于征求加强医疗器械监督抽验复检工作有关意见的函(食药监械监便函〔2015〕137号)总局12.2461国务院关于同意建立药品医疗器械审评审批制度改革部际联席会议制度的批复国务院12.2462国家食品药品监督管理总局发布2015年第3期国家医疗器械质量公告总局12.25四、征求意见序号征求意见颁发机构日期1关于征求医疗器械生产质量管理规范无菌医疗器械附录和植入性医疗器械附录意见的函(食药监械监便函〔2015〕6号)总局器械监管司 2.092关于征求《医疗器械生产质量管理规范体外诊断试剂附录》意见的函(食药监械监便函〔2015〕10号)总局器械监管司 2.163关于征求《出具医疗器械出口销售证明管理规定》意见的函(食药监械监便函〔2015〕14号)总局器械监管司 3.134关于征求医疗器械临床试验备案有关事宜意见的函(食药监械管便函〔2015〕25号)总局器械注册司 4.285关于《腹腔内置疝修补补片动物实验技术审评要点》第一次征求意见的通知医疗器械技术审评中心4.36关于对《动物源性医疗器械产品注册申报资料指导原则(修订版)》征求意见的通知医疗器械技术审评中心6.17关于《人红细胞反定型试剂技术审查指导原则》(征求意见稿)公开征求意见的通知医疗器械技术审评中心6.188关于征求《医疗器械经营企业分类分级监督管理规定(征求意见稿)》意见的函(食药监械监便函〔2015〕89号)总局器械监管司7.039国家食品药品监督管理总局关于公开征求《医疗器械命名规则(试行)》﹙征求意见稿﹚意见的通知总局7.110国家食品药品监督管理总局关于公开征求《医疗器械临床试验机构资质认定管理办法》﹙征求意见稿﹚意见的通知总局7.211关于征求《医疗器械生产质量管理规范现场检查指导原则》等四个指导原则意见的函(食药监械监便函〔2015〕98号)总局器械监管司7.2412关于《主动脉覆膜支架系统的临床试验指导原则》(修订稿)公开征求意见的通知医疗器械技术审评中心9.2213关于《α-氰基丙烯酸酯类医用粘合剂产品注册申报资料指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心9.2214关于征求相关医疗器械注册事项办理程序意见的函(食药监械管便函〔2015〕61号)总局器械注册司9.2815关于对《软性接触镜上市前临床试验指导原则》征求意见的通知医疗器械技术审评中心9.2816关于对《脊柱后路内固定系统产品注册技术审查指导原则》征求意见的通知医疗器械技术审评中心9.2817关于《影像型超声诊断设备(第三类)产品注册技术审查指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心9.318国家食品药品监督管理总局器械监管司公开征求《医疗器械工艺用水质量管理指南》意见总局器械监管司10.0919关于《粒子束治疗系统注册申报资料指导原则》&《一次性使用脑积水分流器注册技术审查指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心10.1920关于《植入式心脏起搏器注册申报资料指导原则(征求意见稿)》征求意见的通知医疗器械技术审评中心10.2621关于《医用X射线诊断设备(第三类)产品注册技术审查指导原则(征求意见稿)》&《离心式血液成分分离设备非临床注册技术审查指导原则(征求意见稿)》征求意见的通知征求意见的通知医疗器械技术审评中心10.2622关于《可吸收性外科缝线产品注册技术审查指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心10.2723关于《治疗呼吸机注册技术审查指导原则》征求意见的通知医疗器械技术审评中心11.224关于《脉搏血氧仪设备临床评价技术审查指导原则》征求意见的通知医疗器械技术审评中心11.325关于《高频手术设备注册技术审查指导原则》&《强脉冲光治疗仪产品注册技术审查指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心11.626关于《牙科基托聚合物材料注册技术审查指导原则》(征求意见稿)征求意见的通知医疗器械技术审评中心11.627关于对《无源植入类骨关节产品说明书编写指导原则》及《常见无源植入类骨关节产品说明书示例》征求意见的通知医疗器械技术审评中心11.1228食品药品监管总局办公厅国家卫生计生委办公厅关于公开征求医疗器械不良事件监测和再评价管理办法(征求意见稿)意见的函(食药监办械监函〔2015〕723号)医疗器械技术审评中心11.1229关于对《髋关节假体注册技术审查指导原则—临床试验部分》征求意见的通知医疗器械技术审评中心11.2430关于征求对《椎间融合器技术审查指导原则(征求意见稿)》意见的通知医疗器械技术审评中心11.2731关于征求对《免于进入临床试验的第二类医疗器械目录(第二批)(征求意见稿)和《免于进行临床试验的第三类医疗器械目录(第二批)(征求意见稿)意见的通知医疗器械技术审评中心12.1432关于征集“胎儿染色体非整倍体(T21、T18、T13)检测试剂盒(高通量测序法)”生产企业信息的通知医疗器械技术审评中心12.23来源:奥咨达整理。
国家药监局关于调整《医疗器械分类目录》部分内容的公告-国家药监局公告2022年第30号

国家药监局关于调整《医疗器械分类目录》部分内容的公告正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家药监局公告2022年第30号关于调整《医疗器械分类目录》部分内容的公告为进一步深化医疗器械审评审批制度改革,依据医疗器械产业发展和监管工作实际,按照《医疗器械监督管理条例》《医疗器械分类目录动态调整工作程序》有关要求,国家药监局决定对《医疗器械分类目录》部分内容进行调整。
现将有关事项公告如下:一、调整内容对27类医疗器械涉及《医疗器械分类目录》内容进行调整,具体调整内容见附件。
二、实施要求(一)对于附件中调整涉及的09-07-02射频治疗(非消融)设备中射频治疗仪、射频皮肤治疗仪类产品,自本公告发布之日起,可按《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)的规定申请注册。
自2024年4月1日起,射频治疗仪、射频皮肤治疗仪类产品未依法取得医疗器械注册证不得生产、进口和销售。
射频治疗仪、射频皮肤治疗仪类产品相关注册人、生产企业应当切实履行产品质量安全主体责任,全面加强产品全生命周期质量管理,确保上市产品的安全有效。
自本公告发布之日起,射频治疗仪、射频皮肤治疗仪类产品相关注册人、生产企业应当主动向所在地(进口产品为代理人所在地)省级药品监督管理部门报告产品按医疗器械研制注册计划、适用的安全性标准承诺、生产质量管理体系及运行情况、顾客投诉处置及不良事件制度和执行情况等。
省级药品监督管理部门应当建立企业信用档案,加强对该类产品注册人、生产企业的检查,督促企业落实主体责任、加快完成产品注册,健全质量管理体系。
自2024年4月1日起,未取得医疗器械生产、经营许可(备案)的企业,不得从事相关产品的生产和销售。
医疗器械经营重点监管品种目录

12-03-01
Ⅲ
骨接合植入物
13-01
Ⅲ
运动损伤软组织修复重建及置换植入物
13-02
Ⅲ
脊柱植入物
13-03
Ⅲ
关节置换植入物
13-04
Ⅲ
骨科填充和修复材料
13-05
Ⅲ
神经内/外科植入物
13-06
Ⅲ
心血管植入物
13-07
Ⅲ
耳鼻喉植入物
13-08
Ⅲ
整形及普通外科植入物
13-09
Ⅲ
组织工程支架材料
Ⅲ
心肺转流器具
10-06
Ⅲ
注射、穿刺器械中的第三类产品
14-01
Ⅲ
血管内输液器械-输液泵
14-02-01
Ⅲ
血管内输液器械-无源输注泵
14-02-04
Ⅲ
血管内输液器械-输液器
14-02-05
Ⅲ
血管内输液器械-静脉输液针
14-02-06
Ⅲ
血管内输液器械-血管内留置针
14-02-07
Ⅲ
动静脉采血针
22-11-01
Ⅲ
二、植入材料和人工器官类
用于血管的吻合器(带钉)
02-13-01
Ⅲ
可吸收缝合线
02-13-06
Ⅲ
外固定及牵引器械中的第三类产品
04-13
Ⅲ
骨水泥定型模具(包含植入体内的组件)
04-16-01
Ⅲ
植入式心脏起搏器
12-01-01
Ⅲ
植入式心律转复除颤器
12-01-02
Ⅲ
植入式神经刺激器
12-02-01
Ⅲ
16-06-01
Ⅲ
医疗器械经营质量管理规范内容及现场检查重点

医疗器械经营质量管理规范内容及现场检查重点1.法律及管理体系:明确医疗器械经营者应依法取得相关经营许可证书,并建立健全质量管理体系,明确质量管理职责和关键环节,确保各项管理活动符合法律法规的要求。
2.采购管理:明确医疗器械经营者在进行医疗器械采购时,需要履行的程序与要求,包括经营者的采购合同、入库验收、合格供货者的评审等。
3.储存管理:明确医疗器械的储存条件、储存期限、储存设备和设施的管理要求、储存区域的划分、储存管理的责任制等,确保储存的医疗器械安全、有效。
4.销售管理:明确医疗器械的销售程序、销售合同的要求、售后服务等,确保销售的医疗器械符合规定的质量标准。
5.质量监控与追溯:明确医疗器械经营者应建立并严格执行产品质量监控与追溯体系,及时发现和处理不良反应和不良事件,确保产品质量和使用安全。
1.采购管理:检查医疗器械采购的合同、进货验收记录、供应商评审等,确保采购程序符合规定。
2.储存管理:检查储存设施和设备是否符合要求,检查储存区域的划分是否合理,检查医疗器械的储存记录和有效期限,确保储存条件符合规定。
3.销售管理:检查销售合同的签订与执行情况,检查售后服务的落实情况,确保销售程序和服务符合规定。
4.质量监控与追溯:检查医疗器械经营者的质量监控与追溯体系是否建立并有效执行,核查不良反应和不良事件的处理情况。
5.记录管理:检查医疗器械经营者的质量管理相关记录的完整性和准确性,包括采购记录、销售记录、储存记录和质量监控记录等。
综上所述,医疗器械经营质量管理规范的内容及现场检查重点主要涉及采购管理、储存管理、销售管理、质量监控与追溯以及记录管理等方面,通过严格执行相关规定和要求,能够确保医疗器械经营过程中的质量安全。
医疗器械相关法规与标准清单
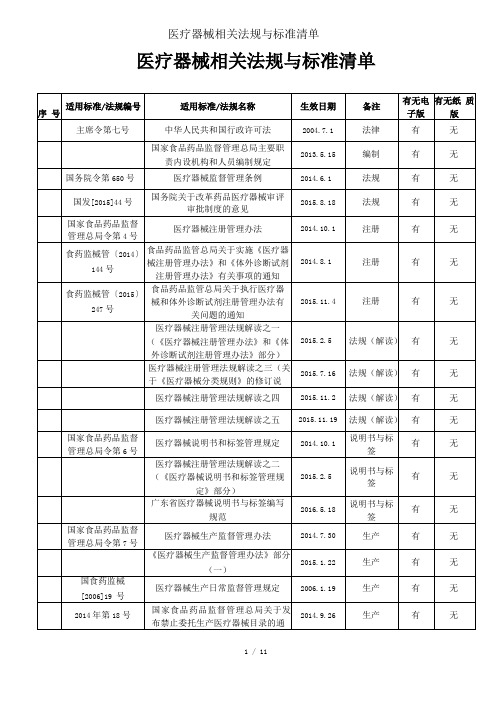
命名
有
无
医疗器械注册管理法规解读之六(命 名)
2016.1.7
命名
有
无
国家食品药品监督 管理总局令第29号
医疗器械召回管理办法
2017.2.8
召回
有
无
《医疗器械召回管理办法》解读
2017.2.8
召回
有
无
《医疗器械召回管理办法》解读之二
2017.5.24
召回
有
无
总局办公厅关于实施《医疗器械召回 管理办法》有关事项的通知
则(2017年修订版)
主清单
2017.4.27
注册
有
无
国食药监械
[2008]409号
关于印发进一步加强和规范医疗器 械注册管理暂行规定的通知
2008.7.23
(已废止)
有
无
总局关于印发一次性使用塑料血袋 等21种医疗器械生产环节风险清单 和检查要点的通知
2017.2.10
注册
有
无
食药监械监〔2016〕
分类
有
无
5 / 11
国家食品药品监督 管理总局令第15号
医疗器械相关法规与标准
医疗器械分类规则
主清单
2015.7.14
分类
有
无
医疗器械分类目录
分类
有
无
国家食品药品监督 管理总局公告2014年第26号
国家食品药品监督管理总局关于第 一类医疗器械备案有关事项的公告
2014.10.1
备案
有
无
食药监办械管
[2014]174号
2015.2.5
说明书与标 签
有
无
医疗器械生产重点监管品种目录

医疗器械生产重点监管品种目录医疗器械是指用于预防、诊断、治疗、矫正人类疾病、损伤或残疾的设备、器具、仪器和其他物品,包括其组成部分、附属品和配件。
为了确保医疗器械的安全性和有效性,各国都采取了相应的监管措施。
医疗器械生产重点监管品种目录是指在医疗器械安全监管中,针对部分具有较高风险的医疗器械品种进行重点监管,并对其生产、销售和使用进行规范。
医疗器械生产重点监管品种目录的制定是根据医疗器械的特殊性以及相关法律法规的要求,结合实际情况进行的。
目录中的医疗器械品种通常具有较高的风险,其不合理的生产、销售和使用可能对人体健康产生危害。
因此,制定重点监管品种目录,加强对这些医疗器械的监管力度,可以保护公众的健康安全。
1.诊断类医疗器械:包括各种用于临床诊断、疾病筛查、健康检查等的医疗器械,如影像设备、试纸、生化分析仪器等。
2.治疗类医疗器械:包括各种用于治疗疾病、手术操作等的医疗器械,如手术器械、激光设备、电疗仪等。
3.体外辅助类医疗器械:包括各种用于辅助人体内器官或系统功能的医疗器械,如呼吸机、心脏起搏器、假肢等。
4.输送类医疗器械:包括各种用于输送药物、液体或气体的医疗器械,如注射器、输液器、氧气瓶等。
5.植入类医疗器械:包括各种植入人体的医疗器械,如人工关节、心脏支架、人工器官等。
6.诊疗一体化设备:包括一体化的医疗设备,如CT、MRI等多功能影像设备。
以上只是医疗器械生产重点监管品种目录的一部分,具体的品种和范围根据不同国家和地区的法律法规以及实际监管需要而定。
监管机构通常会根据医疗器械的特殊性、市场需求和风险评估的结果,对重点监管品种目录进行动态调整,以适应不断发展的医疗器械市场。
对于医疗器械生产企业和销售机构而言,重点监管品种目录的制定对其生产和销售活动产生了一定的约束和规范。
企业需要严格按照相关法律法规的要求,确保生产的医疗器械质量稳定、安全可靠,遵守相关的生产和质量管理规范。
销售机构则需要确保销售的医疗器械合法、真实、有效,不得违规进行虚假宣传和销售欺诈行为。
国家重点监管医疗器械目录

国家重点监管医疗器械目录医疗器械是指用于预防、诊断、治疗疾病,以及调节人体结构和生理功能的器械。
它在医疗领域具有重要作用,可以帮助医生进行准确的诊断和治疗,提高治疗效果,提升患者的生活质量。
然而,由于市场竞争激烈和监管缺失等原因,一些低质量、不安全的医疗器械也存在于市场上,给病患和医疗机构带来了潜在的健康风险。
为了解决这一问题,国家制定了国家重点监管医疗器械目录。
这个目录是根据医疗器械的风险等级和临床需求来确定的,主要包括高风险、高频次使用、重复使用、使用范围广、临床应用广泛等方面需要重点监管的医疗器械。
这些医疗器械具有较大的风险和社会影响,因此需要加强质量监管,确保它们的质量和安全性。
目前,国家重点监管医疗器械目录主要包括以下几个方面的医疗器械:1.高风险医疗器械:主要包括植入类医疗器械、介入类医疗器械、影像诊断类医疗器械等。
这些医疗器械使用不当可能会对人体造成严重的损害,因此需要严格的监管。
2.高频次使用医疗器械:主要包括一次性使用医疗器械。
这些器械在医疗过程中使用较频繁,一旦出现质量问题可能对患者造成较大危害。
3.重复使用医疗器械:主要包括手术器械、内窥镜等需要反复使用的医疗器械。
这些器械在使用过程中容易受到污染,如果清洗和消毒不彻底就可能会导致交叉感染。
4.使用范围广医疗器械:主要包括呼吸机、血液透析机等适用于多个科室的医疗器械。
这些器械在临床上应用广泛,一旦出现质量问题可能会对多个科室的患者造成危害。
通过对这些医疗器械的重点监管,国家可以加强对其质量和安全性的监督,提高监管效能,尽早发现和防范潜在的风险,保障患者的生命安全和身体健康。
同时,通过规范市场秩序,有助于提升医疗器械行业的整体竞争力,促进医疗器械技术的创新和发展。
总之,国家重点监管医疗器械目录的建立是一项重要的措施,旨在加强对医疗器械质量和安全的监管。
通过对高风险、高频次使用、重复使用、使用范围广等方面需要重点监管的医疗器械的监管,可以有效提高医疗器械的质量和安全性,保障患者的利益和权益。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
国家食品药品监管总局关于印发医疗器械经营环节重点监管目录及
现场检查重点内容的通知
各省、自治区、直辖市食品药品监督管理局:
为加强医疗器械经营监管,根据《医疗器械经营监督管理办法》(国家食品药品监督管理总局令第8号)和《医疗器械经营企业分类分级监督管理规定》(食药监械监〔2015〕158号),总局组织制定了《医疗器械经营环节重点监管目录及现场检查重点内容》,现印发给你们,请按照《医疗器械经营企业分类分级监督管理规定》对《医疗器械经营环节重点监管目录及现场检查重点内容》中所列品种的经营实施重点监管。
附件:医疗器械经营环节重点监管目录及现场检查重点内容
国家食品药品监管总局
2015年8月17日
附件:
医疗器械经营环节重点监管目录及现场检查重点内容
来源:/fg/detail2008242.html。
