最新北京课标版九年级化学上册《第一节 原子》习题2及答案
《第一节 原子结构》(同步训练)高中化学选择性必修2_人教版_2024-2025学年

《第一节原子结构》同步训练(答案在后面)一、单项选择题(本大题有16小题,每小题3分,共48分)1、下列关于原子核外电子排布的说法中,正确的是()。
A. 每个能层最多可容纳的电子数为(2n2)(n为能层序数)B. 电子在核外是按亚层次序排列的,即1s, 2s, 2p, 3s, 3p…C. 每个亚层中的电子数为2n+1D. s亚层只能容纳1个电子2、在卢瑟福α粒子散射实验中,绝大多数α粒子能直接穿过金箔,而少数α粒子被大角度散射。
这说明()A. 原子内部是空的B. 原子核带正电,且带电量远小于原子中的电子C. 原子核内的质子和中子的质量远小于电子的质量D. 原子核的体积非常小3、下列关于原子结构的说法中,正确的是()A、电子在原子核外的运动轨迹是固定的B、原子的质量主要集中在原子核上,而原子核又由质子和中子构成C、原子核的体积比原子体积小很多,但核外电子运动区域却很大D、原子的化学性质主要由电子层结构决定4、已知某元素的原子序数为15,下列关于该元素的原子结构描述正确的是()A、原子电子排布为1s²2s²2p⁶3s²3p⁵B、原子电子排布为1s²2s²2p⁶3s²3p⁶C、该元素属于第IIA族D、该元素的最外层电子数为15、以下物质形成离子键时,原子半径相对较大的是:A. Na⁺与Cl⁻B. Ca²⁺与O²⁻C. K⁺与Cl⁻D. Mg²⁺与F⁻6、下列关于原子结构的说法中,正确的是:A. 原子核由质子和中子组成,核外电子绕核做圆周运动。
B. 原子的化学性质主要取决于原子核中的质子数。
C. 同位素是指具有相同质子数但中子数不同的原子。
D. 原子核的电荷数等于核外电子的电荷数。
7、根据电子排布规则,下列原子序数的原子中,最外层电子数为3的是()。
A、6B、11C、13D、158、下列说法正确的是:A. 卢瑟福提出的原子结构模型中,原子核是空间空虚的。
最新北京课标版九年级化学上册《第一节 初步认识化学元素》习题1及答案

《第一节初步认识化学元素》习题一.选择题(每小题有1~2个选项符合题意)1.不同种元素的本质区别是()A.相对原子质量不同B.中子数不同C.电子数不同D.质子数不同2.元素在自然界里分布并不均匀,如智利富藏铜矿、澳大利亚多铁矿、山东的黄金储量居我国首位,但从整个地壳含量的多少分析,最丰富的金属元素是()A.Fe B.Si C.O D.Al3.某全麦饼干部分营养成分的含量如下表所示,表中的“铁、镁、锌、钙”是指()营养成分铁镁锌钙含量(mg/100g)4.5 ~ 590 ~1003 ~ 4280 ~300A.分子B.原子C.元素D.非金属4.一瓶气体经过化验和其中只有一种元素,则该气体是()A.一种单质B.一种化合物C.单质、化合物的混合物D.既可能是一种单质,也可能是几种单质的混合物5.下图是表示气体分子的示意图,图中“●”和“○”分别表示两种不同质子数的原子,其中表示化合物的是()6.下列说法错误..的是()A.物质能呈三态(固、液、气)是由于分子间有一定的间隔B.由同种分子构成的物质是纯净物C.化合物是由不同种元素组成的物质D.物质跟氧气发生的化学反应叫氧化反应7.加热装有少量高锰酸钾和氯酸钾的试管待完全反应后,试管中剩余固体物质中共有()A.两种化合物B.两种化合物,两种单质C.两种单质D.三种化合物8.蒸馏水中不宜养鱼,是因为蒸馏水中几乎不含..()A.氧原子B.氧元素C.氧气分子D .矿物质9.科学技术的发展,使人们操纵单个原子和分子成为可能,从而可以直接用原子来制造分子。
若能用这种方法制造葡萄糖(C 6H 12O 6),下列原子中不需要...的是( ) A .碳原子 B .氢原子 C .氮原子D .氧原子10.元素周期表是学习化学的重要工具,右图是元素周期表中的一格,从该图中,我们获取的相关信息中错误..的是( ) A .该元素的名称是镁 B .该元素的原子序数为12C .该原子的相对原子质量是24.31D .该元素在地壳中的含量为24.31%二.填空题11.填表:元素名称氧 铝 氮 氯 镁 铜 铁 硫 元素符号 C P Z n Na C a H12.请把下列物质的序号写在其所属类别的后面:a .氧气b .空气c .水d .氯酸钾 12 Mg 镁24.31(1)化合物_______;(2)混合物_______;(3)单质_________;(4)纯净物_______;13.物质的分类标准有多种,请你自拟两个分类标准,将水、氢气、氧气和二氧化碳四种物质中的三种物质包括在标准内,而另外一种物质不在标准内。
初中 化学北京版九年级上册第一章第一节-普通用卷

初中化学北京版九年级上册第一章第一节同步练习一、单选题1.已知碘原子的核外电子数为53,其相对原子质量为131,则下列关于碘131原子说法正确的是()A. 质子数为53B. 中子数为53C. 核电荷数为78D. 原子质量为131g2.下列关于相对原子质量的说法正确的是()A. 相对原子质量就是原子的实际质量B. 相对原子质量是原子质量与一种碳原子质量的比值C. 原子质量越大,相对原子质量就越大D. 相对原子质量的单位为“g”3.最近科学家制造出了原子序数为114号的新元素,其相对原子质量为289,下列有关114号元素的说法正确的是()A. 该元素的中子数为114B. 该元素的原子核外电子数为114C. 该元素的核电荷数为175D. 该元素的质子数为2894.已知一种锶原子的相对原子质量为88,其中子数为50,则这种锶原子的核外电子数为()A. 38B. 50C. 88D. 1265.一个重水分子是由两个重氢原子和一个氧原子构成的,重氢原子的核电荷数是1,相对原子质量是2.则下列说法中正确的是()A. 重氢原子核外有两个电子B. 重氢原子核内有一个质子C. 重氢原子中没有中子D. 水分子和重水分子的质量相同6.2006年10月6日,美国科学家劳伦斯⋅利费莫尔宣布他与俄罗斯科学家成功合成了一种核外电子数为ll8,中子数为179的超重元素原子,该元素的相对原子质量和质子数分别是()A. 297 118B. 118 297C. 118 179D. 179 1187.已知某原子核电荷数为a,该原子中核内有b个质子和c个中子,核外有d个电子.则()A. a=b=cB. b=c=dC. a=c=dD. a=b=d8.2019年12月15日,中国铀矿3000米科学深钻开钻仪式在江西相山铀矿田顺利举行。
铀是重要的核工业原料,原子序数为92,某铀原子的相对原子质量为238.则该原子的中子数为()A. 238B. 92C. 330D. 1469.疫情期间,同学们用眼增多,容易引发近视。
最新北京课标版九年级化学上册《第一节 初步认识化学元素》习题2及答案

《第一节初步认识化学元素》习题一.选择题(每小题有1~2个选项符合题意)1.下列各组物质中,前一种是单质,后一种是混合物的是()A.铝、二氧化硫B.冰、水蒸气C.水银,食盐水D.氮气、空气2.下列物质中,属于化合物的是()A.水B.食盐水C.氮气D.红磷3.下列物质中,不属于...氧化物的是()A.高锰酸钾(KMnO4)B.五氧化二磷(P2O5)C.水(H2O)D.氧化镁(MgO)4.地壳中含量最多的金属元素是()A.氧元素B.铁元素C.硅元素D.铝元素5.下列各组元素符号第一个字母相同的是()A.铁、锌、钠B.钙、铝、铜C.铝、银、镁D.碳、钙、氯6.下列关于元素的叙述中,正确的是()A.同种原子的统称叫元素B.同种元素的原子结构和质量完全相同C.元素的种类取决于该元素原子的核外电子数D.不同种元素的根本区别是核内质子数不同7.地壳中各元素所占质量分数从小到大的顺序是()A.O,Si,Al,Fe B.Al,Fe,Si,O C.Fe,Al,Si,O D.Si,O,Fe,Al 8.下列说法中,正确的是()A.空气是一种单质B.空气是一种化合物C.空气是几种元素的混合物D.空气是几种单质和几种化合物的混合物9.化合物()A.至少含有两种元素B.指所含两种或两种以上的元素的物质C.一定是纯净物D.可以是混合物10.水是由()A.1个氢分子和1个氧原子组成的B.1个氧原子和2个氢原子构成的C.2个氢元素和1个氧元素组成的D.氢元素和氧元素组成的二.填空题11.写出下列符号表示的意义:“H”表示;“2H”表示。
12.水是由和组成的;一个水分子是由和构成的。
13.书写元素符号时,第一个字母应(填“大”或“小”)写,第二个字母应(填“大”或“小”)写。
例如:镁和锰的元素符号分别为和,其元素符号的共同点是,不同点是。
14.写出下列元素符号:氢氧氮氯碳硫磷钾钙钠镁铝锌铜参考答案:1.C、D 2.A 3.A 4.D5.答案:D 点拨:本题考查对常见元素符号的识记能力。
最新北京课标版九年级化学上册《第一节 碳的单质》习题2及答案

《第一节 碳的单质》习题
1.化学物质中有一种由多个五边形和六边形组成的形似足球的笼状分子,称为“足球烯”(如右图),化学式为C 60。
关于C 60的说法正确的是( ) A.属于单质。
B.属于混合物。
C.碳元素的化合价为+4。
D.足球烯是实心的。
2.金刚石和石墨都是( ) A.有金属光泽的无色透明晶体。
B.电的良导体。
C.非常坚硬的物质。
D.由碳元素形成的单质。
3.下列实验能证明金刚石和石墨是由同种元素形成的不同单质的是( ) A.测量其密度。
B.测量其熔点。
C.用水溶解。
D.分别燃烧验证燃烧产
物。
4.活性炭或木炭能使红墨水的红色褪去,是因为( ) A.它们的主要成分是碳。
B.它们具有多管道的疏松结构而有吸附作用。
足球烯结构模型
C.它们的化学性质在常温下很活泼。
D.它们的颗粒很细小,而且是黑色的。
5.清代著名画家郑板桥所作的字画至今仍不褪色,是因为墨汁中的碳()
A.具有可燃性。
B.在常温下稳定。
C.具有氧化性。
D.具有还原性。
6.下列关于碳的几种单质的组成和用途的说法,错误的是()
A.璀璨夺目的天然钻石是由碳元素组成的。
B.长期未用而难开启的铁锁,可在锁孔中加入少量铅笔芯来作润滑剂。
C.铅笔芯主要是用铅和少量碳粉制成的。
D.活性炭可作防毒面具的滤毒剂。
参考答案:
1.A
2.D
3.D
4.B
5.B
6.C。
最新北京课标版九年级化学上册《第一节 空气》习题2及答案

《第一节空气》习题1、19世纪末,物理学家瑞利在研究中发现,从空气中分离得到的氮气密度,与从含氮物质制得的氮气密度有0.0064 kg/m3的差异,他没有放过这一差异,在化学家拉姆塞的合作下,经过十几年的努力,于1894年发现了空气中的氩气。
下列说法正确的是填序号①氩是一种化学性质极不活泼的气体②瑞利从空气中分离的氮气是纯净物③19世纪末以前,人们认为空气由氧气和氮气组成④瑞利发现,从含氮物质制得的氮气密度大于从空气中分离的氮气的密度2、在一个锥形瓶里放一段镁带,点燃镁带,用塞子将瓶口塞紧,等镁带燃烧后并冷却,开启瓶塞非常费劲。
其原因是。
3、右图是利用红磷在空气中燃烧测定氧气含量的实验装置图,在实验中,钟罩内的水为什么先下降后上升?4、2008年北京奥运会申办成功,为了让世界各国朋友有一个清新的比赛和旅游观光环境,北京市应提高空气质量,你认为可以采取哪些措施:①②③④5、空气质量监测报告提醒人们要关心环境、保护环境。
2002年十月某一天,首都北京、全国重工业基地重庆、海滨城市大连空气质量监测数据如下:注意各分指标与污染分指数之间关系:一级<50,二级50~100,三级100~200,四级200~300,五级300~400,六级400~500。
请按要求分析:①空气质量最差的城市是______________;②空气质量标准确定依据是以下三项中的(填序号)___________。
A.三项数据综合考虑B.看最大的数据C.看最小的数据参考答案:1、①③2、因为镁条与空气中的氧气反应生成了白色的氧化镁固体,锥形瓶中的气体减少,压强变小,所以打不开了。
3、因为反应时放出大量的热,使钟罩内压强增大,所以水面下降;当反应结束温度降低时,由于氧气参加了反应,钟罩内压强减小,所以水面又上升。
4、①搞好环境卫生②汽车尾气要处理后再排放③植树造林,增大绿化面积④工厂废气先处理后排放5、重庆B。
初中九年级化学上册《原子的结构》课后练习题 附加答案

3.2.1原子的结构1.某些花岗岩石材中含有放射性元素氡。
一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为()A.50B.86C.136D.2222.下列说法正确的是()A.原子不能再分B.原子核都是由质子和中子构成的C.相对原子质量只是一个比,没有单位D.原子可以构成分子,也可以直接构成物质3.有两种原子,一种原子核内有17个质子和18个中子,另一种原子核内有17个质子和19个中子,则它们不相等的是()A.核电荷数B.核外电子数C.原子质量D.原子的带电荷量4.“神舟”五号不仅将杨利伟送上太空,实现了亿万中国人的梦想,同时还承担着其他的科研任务。
比如探索宇宙中可能存在完全由反粒子构成的物质——反物质。
物质与反物质相遇会发生“湮灭”现象,释放出巨大的能量,在能源研究领域中前景可观。
正电子、负质子等都是反粒子。
它们与通常所说的电子、质子相比较,质量相等但电性相反。
请你推测,反氢原子的结构可能是()A.由一个带正电荷的质子与一个带负电荷的电子构成B.由一个带负电荷的质子与一个带正电荷的电子构成C.由一个带正电荷的质子与一个带正电荷的电子构成D.由一个带负电荷的质子与一个带负电荷的电子构成5.居里夫人是著名科学家,两次获得诺贝尔奖。
她首先发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。
一种元素的原子经过放射变成了另一种元素的原子,据此可推断放射出的粒子是()A.电子B.中子C.质子D.原子核6.英国科学家道尔顿最先确立了原子学说,他的中心论点主要有:①原子是不能再分的粒子;②原子是微小的实心球;③同种元素的原子,其性质和质量都相同。
而现代科学实验表明:同种元素的原子内部有相同的质子数和不一定相同的中子数。
从现代的观点看,你认为道尔顿的三个论点中,不确切的是()A.①B.①③C.②③D.①②③7.科学研究发现:氮气不活泼,在3000 ℃时仅有0.1%的分子分裂。
在0 ℃常压条件下,向密闭容器M中充入一定量氮气,而后升高温度(不超过300 ℃,压强不变),若该密闭容器的体积增大了一倍,几位同学设想了四种M内分子变化示意图,你认为合理的是哪一种?图4-18.(经典回放)为形象展示水分解的微观过程,某同学制作了一些模型,表示相应的微观粒子。
初三化学上册《原子的结构》初三练习题 含答案

课题2 原子的结构一、选择题(每小题只有一个选项符合题意)1.下列关于原子的叙述正确的是( )A.原子由原子核和核外电子构成B.原子由原子核和中子构成C.原子由质子和电子构成D.原子由质子和中子构成2.核能已经成为一种重要的能源,氘和氚都是未来生产核能的燃料。
氚是氢元素的一种原子,氚原子的核电荷数是( )A.1B.2C.3D.43.下列原子各1×1021个,总质量最大的是( )A.氧原子B.氯原子C.氢原子D.铁原子4.下列关于原子的叙述中,错误的是( )A.原子呈电中性B.原子是实心球体C.原子由原子核与核外电子构成D.原子可以构成分子5.最近科学家发现了一种与天体中的中子星构成类似的,只由四个中子构成的粒子,这种粒子称为“四中子”,也称为“零号元素”。
有关这种粒子的说法正确的是( )A.易失去电子B.相当于一个氢分子的质量C.不显电性D.在周期表中可与氢元素占同一位6.2010年2月19日德国重粒子研究中心宣布第112号元素的符号位Cn,它的中文名称为鎶。
已知Cn的相对原子质量为277,其质子数是112,则这种原子的核外电子数为( )A.112B.165C.277D.3897.从下列图片中不能..获取的信息是( )A.分子之间有间隔B.硅原子是由原子核和电子构成的C.受热水分子运动速率加快D.构成物质的粒子有分子、原子和离子8.中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我国在该领域的研究处于世界前列。
氘和氚是核聚变的原料(氘、氚原子核内都只有1个质子,但含不同数目的中子),聚变发生后,氘、氚原子核转变为氦原子核。
根据以上叙述,下列说法正确的是( )A.核聚变是化学变化B.氘原子和氚原子属于不同元素C.氘原子和氚原子是氢元素的两种不同原子D.氘原子和氚原子的相对原子质量相同9.英国科学家道尔顿最先确立了原子学说,他的中心论点主要有:①原子是不能再分的粒子;②原子是微小的实心球;③同种元素的原子,其性质和质量都相同。
最新北京课标版九年级化学上册《第一节 原子》习题1及答案

《第一节原子》习题一.选择题(每小题有1~2个选项符合题意)1.在原子中,质子数等于()A.中子数B.核外电子总数C.相对原子质量D.中子数和电子数之和2.一滴水能分成许许多多个水分子,分子又可分成原子,原子又由中子、质子、电子等构成,这些微粒中,一定能保持水的化学性质的是()A.水分子B.构成水分子的原子C.中子和质子D.电子3.下列关于原子的说法错误..的是()A.原子是化学变化中的最小微粒B.原子是最小的微粒C.原子核带正电荷,但原子不显电性D.分子能直接构成物质而原子不能4.原子中决定相对原子质量大小的是()A.质子数和中子数B.质子数和电子数C.中子数和电子数D.核电荷数和电子数5.表示两个氢原子的是()A.2H B.H2C.2H2D.2H+6.碳的相对原子质量是()A.12 g B.12 C.1.993×10-26 kg D.1/12 g7.下列关于原子的叙述正确的是()A.物质都是由原子直接构成的B.原子是由质子和电子构成的C.原子是由质子和中子构成的D.原子是由原子核和核外电子构成的8.据中央电视台6月3日对云南抚仙湖湖底古城考古的现场报道,科学家曾通过测定古生物遗骸中的碳-14含量来推断古城年代。
碳-14原子的核电荷数为6,相对原子质量为14。
下列关于碳-14原子的说法中,错误..的是()A.中子数为6 B.质子数为6 C.电子数为6 D.质子数和中子数之和为14二.填空题9.将分子、原子、原子核、质子、中子和电子,分别填入下列有关空格内。
(1)构成物质的微粒有多种,有的物质是由构成的,如氦气,汞,有的物质是由构成的,如氮气、水等。
(2)氧化汞是保持氧化汞化学性质的微粒,在化学变化中,氧化汞分解成,汞直接构成汞,每两个氧构成一个氧。
(3)氧原子虽然在化学反应里不能再分,但原子中心有一个带8个单位正电荷的,其外有8个作高速运动,由于每一个带一个单位负电荷,不带电,所以整个不显电性。
北京课改版化学-九年级上册-《原子》同步练习1
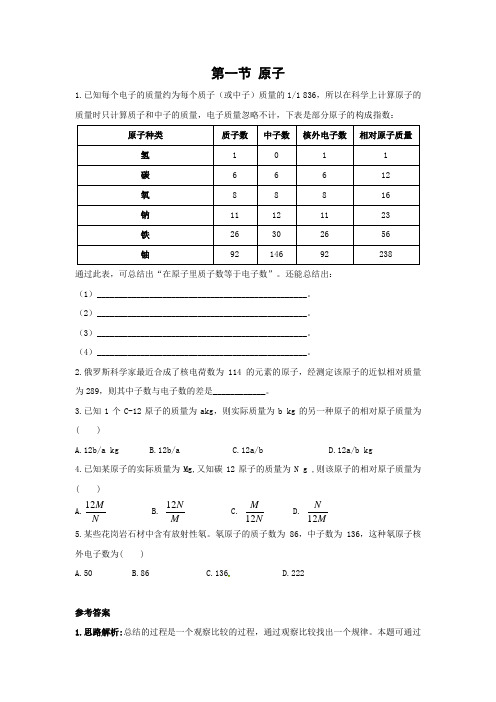
第一节 原子1.已知每个电子的质量约为每个质子(或中子)质量的1/1 836,所以在科学上计算原子的质量时只计算质子和中子的质量,电子质量忽略不计,下表是部分原子的构成指数:原子种类 质子数 中子数 核外电子数 相对原子质量 氢 1 0 1 1 碳 6 6 6 12 氧 8 8 8 16 钠 11 12 11 23 铁 26 30 26 56 铀9214692238通过此表,可总结出“在原子里质子数等于电子数”。
还能总结出: (1)________________________________________________。
(2)________________________________________________。
(3)________________________________________________。
(4)________________________________________________。
2.俄罗斯科学家最近合成了核电荷数为114的元素的原子,经测定该原子的近似相对质量为289,则其中子数与电子数的差是____________。
3.已知1个C-12原子的质量为akg ,则实际质量为b kg 的另一种原子的相对原子质量为( )A.12b/a kgB.12b/aC.12a/bD.12a/b kg4.已知某原子的实际质量为Mg,又知碳12原子的质量为N g ,则该原子的相对原子质量为 ( ) A.N M 12 B. M N 12 C. N M 12 D. MN12 5.某些花岗岩石材中含有放射性氡。
氡原子的质子数为86,中子数为136,这种氡原子核外电子数为( )A.50B.86C.136D.222 参考答案1.思路解析:总结的过程是一个观察比较的过程,通过观察比较找出一个规律。
本题可通过观察比较横行数据和纵列数据找出原子构成的一些规律。
观察比较每一横行数据不难发现:相对原子质量=质子数+中子数;原子核内不一定都有中子;原子核内质子数不一定等于中子数。
初中化学北京课改版九年级上册第3章 构成物质的微粒第一节 原子-章节测试习题(2)

章节测试题1.【答题】下列四种粒子的结构示意图中,表示Na+的是()A.B.C.D.【答案】C【分析】本题考查离子的结构示意图,根据离子的形成过程解答。
【解答】原子中,质子数=核外电子数,失去最外层电子数得到阳离子,使质子数大于核外电子数。
Na+表示的是钠离子带一个单位的正电荷。
钠原子的质子数为11,钠原子失去一个电子形成带一个单位正电荷的钠离子,核外电子数为10。
故选C。
2.【答题】钠、镁、铝、铁的相对原子质量分别为:23、24、27、56,相同质量的四种金属含有的原子个数最少的是()A.钠B.镁C.铝D.铁【答案】D【分析】本题考查相对原子质量、原子个数、物质质量的关系。
【解答】相对原子质量×原子个数=物质质量。
物质的质量相同时,相对原子质量越大,原子个数越少。
钠、镁、铝、铁的相对原子质量分别为:23、24、27、56,相对原子质量钠<镁<铝<铁,那么原子个数的关系是:钠>镁>铝>铁,故所含原子数最少的是铁。
故选D。
3.【答题】某微粒的结构示意图如右图所示,下列有关该微粒的说法不正确的是()A.该微粒的原子核内有17个质子B.该微粒的原子核外有3个电子层C.该图表示的微粒是一种离子D.该微粒在化学反应中易得到1个电子【答案】D【分析】本题考查微粒的结构示意图,最外层电子数与元素化学性质的关系。
【解答】A、根据结构示意图,该微粒的原子核内有17个质子,正确;B、根据结构示意图,该微粒的原子核外有3个电子层,正确;C、当质子数=核外电子数,为原子,当质子数≠核外电子数,为离子,该图表示的微粒中质子数17≠核外电子数18,是一种离子,正确;D、根据结构示意图,该微粒的最外层电子数为8,故在化学反应中比较稳定,错误。
故选D。
4.【答题】氦-3原子核里有2个质子,1个中子,相对原子质量为3,下列表示氦-3原子的结构示意图中正确的是()A.B.C.D.【答案】D【分析】本题考查微粒结构示意图。
北京课改版化学-九年级上册-《原子》同步练习2

第一节 原子一.我会选择1、绝大多数原子的原子核中含有( )A .质子、中子、电子B .质子、电子C .中子、电子D .质子、中子2、下列对原子结构的认识错误的是( )A.原子核体积很小B.原子核带正电C.原子内部有很大的空间D.原子是实心的球体3、在原子的原子核里,质子数等于( )A.核外电子数B.中子数C.中子数和电子数之差D.中子数和电子数之和4、居里夫妇在1898年从几吨铀盐废料中提炼出0.3g 镭。
镭具有放射性,镭原子会分裂,变成一个质子数为86、中子数为136的氡原子和一个具有2个中子和2个电子的氦原子,并放出能量。
试推测镭原子的核电荷数与相对原子质量分别是 ( )A 、88、138B 、86、14C 、88、226D 、84、1685、氢是新型清洁能源,但难储运。
研究发现,镧和镍的一种合金是储氢材料。
下列有关57号元素镧(La)的说法不正确的是 ( )A .该元素原于的质子数为57B .该元素原子的核电荷数为57C .该元素原于的核外电子数为57D .该元素为非金属元素6、1992年,我国科学家首次发现了汞元素的一种新原子。
这种汞原子的相对原子质量为208,核电核数为80,这种汞原子的中子数为 ( )A 、80B 、128C 、208D 、2887、甲原子与乙原子的质量比为a :b ,而乙原子与碳原子的质量比为c :d ,则甲原子的相对原子质量为 ( )A 、B 、C 、D 、 8、1999年度诺贝尔奖获得者艾哈德•泽维尔开创了化学研究新领域,他使运用激光光谱技术观察化学反应时分子中原子运动成为可能。
你认为该技术不能观察到的是 ( )ad 12bc 12bdac bc 12ad 12ac bdA、原子中原子核的内部结构B、化学反应中原子的运动C、化学变化中生成物分子的形成D、化学反应中反应物分子的分解二.我会填空9、“嫦娥一号”是我国自主研制、成功发射的第一个月球探测器。
“嫦娥一号”的发射过程包括火箭发射、入轨、变轨、奔月、绕月等过程。
2019年精选北京课改版初中化学九年级上册第3章 构成物质的微粒第一节 原子课后练习[含答案解析]八十六
![2019年精选北京课改版初中化学九年级上册第3章 构成物质的微粒第一节 原子课后练习[含答案解析]八十六](https://img.taocdn.com/s3/m/d451d23beff9aef8941e06a6.png)
2019年精选北京课改版初中化学九年级上册第3章构成物质的微粒第一节原子课后练习[含答案解析]八十六第1题【单选题】下列有关说法中,正确的是( )A、原子不显电性,是因为原子中不存在带电的粒子B、热胀冷缩,说明分子的大小随温度的升降而改变C、在化学反应中,反应前后原子的种类没有改变,数目没有增减D、化学反应前后,催化剂的质量不会改变,化学性质改变【答案】:【解析】:第2题【单选题】一种铁原子的原子核内有26个质子和30个中子,该原子的核外电子数为( )A、26B、30C、56D、4【答案】:【解析】:第3题【单选题】2014年5月,科学家们在粒子加速器中,用钙离子轰击放射性元素锫(元素符号为Bk,原子序数为97),成功生成了一种新元素﹣117号元素.下列说法正确的是( )A、钙离子的符号为Ca^+2B、锫元素原子核外电子数为97C、新元素原子的核内中子数为117D、新元素的相对原子质量为117【答案】:【解析】:第4题【单选题】建立模型是学习化学的重要方法,下列化学模型中正确的是( )A、铝原子结构B、地壳中元素含量C、物质的分类D、不饱和溶液、稀溶液关系模型【答案】:【解析】:第5题【单选题】下面是九年级化学学习过程中一些学生的认识,其中正确的是( )A、原子核内中子数决定了元素的种类B、如果物质的组成元素相同,化学性质也一定相同C、二氧化碳的含量:人体呼出气体﹥吸入空气D、最外层电子数为8的粒子一定是稀有气体元素的原子【答案】:【解析】:第6题【单选题】朝核问题引发了国际关注,核问题的关键是核能的如何利用,已知某种核原料的原子核中含有1个质子和2个中子,那么( )A、该原子是一种氢原子B、该原子的相对原子质量是2C、该原子核外有3个电子D、该原子核带2个单位的正电荷【答案】:【解析】:第7题【单选题】由我国著名科学家、中国科学院院士张青莲教授主持测定了钢、铱、锑、铂等几种元素的相对原子质量新值,其中他测定核电荷数为63的铂元素的相对原子质量的新值为152,则下列说法正确的是( )A、铂元素的原子核内的质子数为63B、铂元素的原子核内的中子数为63C、铂元素的原子核外电子数为89D、铂元素的原子的质量为152g【答案】:【解析】:第8题【综合题】“见著知微,见微知著”是化学思维方法.从宏观知微观①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为______;②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是______和______(填符号).从微观知宏观①微粒A最外层电子数是______,在化学反应中容易______(填“得”或“失”)电子;②微粒A,B,C,D,E中,对应单质化学性质最稳定的是______(填编号,下同),属于同一种元素的是______和______.【答案】:【解析】:第9题【综合题】在①分子②原子③原子核④质子⑤中子⑥电子等粒子中,选择合适粒子填空(填序号):保持物质化学性质的粒子是______化学变化中的最小粒子是______带正电荷的粒子是______不显电性的粒子是______质量最小的粒子是______在同一原子中数目相等的粒子是______【答案】:无【解析】:第10题【综合题】我国科学家最近成功合成了世界.上首个五氮阴离子盐[(H3O)3(NH4)4(N5)6Cl],占领了超高能材料研究的国际制高点。
北京版化学-九年级上册第3章第1节原子同步练习

《原子》同步练习1.从右图水分子分解示意图中获得以下信息,其中不正确...的是A.水是由氢元素和氧元素组成B.化学反应前后元素的种类不变C.在化学变化中,分子可分,原子也可分D.1个水分子由2个氢原子和1个氧原子构成2.对一个问题要多方面深入分析,用这样的思想方法对下面的问题作出判断,经测定某物质只含有一种原子,则下列推断正确的是()A.该物质中一定只含同种分子B.该物质一定是纯净物C.该物质中可能含不同种分子D.该物质一定是混合物3.碳﹣12、碳﹣13、碳﹣14都是碳元素的原子,它们的主要差别在于()A.电子数目不同B.中子数目不同C.质子数目不同D.化学性质不同4.下列对如图所示4个实验的分析不正确的是()A.甲实验说明铁丝在氧气中燃烧生成氧化铁B.乙实验说明二氧化碳不燃烧,也不支持燃烧,密度比空气大C.丙实验b烧杯中的酚酞溶液变红色,说明NH3分子运动到酚酞溶液中D.丁实验中,白磷能在水下燃烧,说明它具备了燃烧的二个条件5.下列四种离子的结构示意图中,化学性质最稳定的元素的原子是()A.B.C.D.6.(5分)A元素的原子结构示意图为:,A元素在化学反应中容易_电子变成______________(填离子符合),属_______________元素(填金属或非金属);B元素的离子结构示意图为:,该离子带____________个单位正电荷,该元素的原子核外总共有___________个电子。
7.水是生命之源,也是人类宝贵的自然资源。
(1)下列各种水中,属于纯净物的是(填序号)。
A.苏打水B.矿泉水C.蒸馏水D.自来水(2)饮用硬度过大的水不利于人体健康,因此人们常采用的方法将硬水软化。
(3)小刚为了净化收集到的雨水,自制了一个如图所示的简易净水器,其中小卵石、石英砂和彭松棉的作用相同,它们的作用是。
(4)自来水消毒时发生的化学反应中有下图所示的微观过程:(表示氯原子,表示氧原子,表示氢原子)该反应中化合价发生变化的元素是。
精选2019-2020年北京课改版化学九年级上册第一节 原子练习题九十八

精选2019-2020年北京课改版化学九年级上册第一节原子练习题九十八第1题【单选题】关于原子质量,下列叙述正确的是( )A、原子的质量几乎全部集中在质子上B、一个碳12原子的质量是akg,氧的相对原子质量为16,则一个氧原子的实际质量为有误kgC、氮原子的相对原子质量为14,氧原子的相对原子质量为16,则氮原子与氧原子的实际质量之比为8:7D、国际上统一采用相对质量来计量原子的质量为了方便书写、记忆和运算【答案】:【解析】:第2题【单选题】铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )A、24B、58C、82D、140【答案】:【解析】:第3题【单选题】下列各种粒子,不带电的是( )A、原子核B、质子C、中子D、电子【答案】:【解析】:第4题【单选题】氧元素与氢元素的本质区别是( )A、中子数不同B、质子数不同C、相对原子质量不同D、中子数与核外电子数不同【答案】:【解析】:第5题【单选题】下列说法正确的是( )A、原子不能再分B、原子核都是由质子和中子构成的C、原子可以构成分子,也可以直接构成物质D、相对原子质量只是一个比,没有单位【答案】:【解析】:第6题【单选题】一个铁原子中共有82个粒子,其中30个粒子不带电,则铁原子的相对原子质量为( )A、26B、30C、56D、82【答案】:【解析】:第7题【单选题】随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知。
下图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图。
下列说法错误的是A、碘的相对原子质量为126.9,原子核内质子数为53B、碘原子核外共有53个电子,最外层有7个电子C、碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为-1价D、碘元素属于非金属元素,碘原子在化学反应中容易得到电子【答案】:【解析】:第8题【单选题】氚是氢的一种同位素,氚原子含有1个质子和2个中子。
九年级化学上册 3.1.1 原子同步练习 (新版)北京课改版

3.1.1原子同步练习【基础题型】1、原子相对质量的测量方法是:()A、用精密天平称量,取其质量的近似值B、经过精密的仪器和实验测出C、根据原子体积的大小排列顺序D、以一种碳原子质量的1/12为标准,取其相对比值2、电子质量很小,仅相当于质子或中子质量的1/1836,所以原子的质量主要集中在原子核上。
镁原子核有12个质子和12个中子。
则镁的相对原子质量是()A、 12B、 24C、 12克 D 、24克3、已知一种碳原子质量为1.993×10-26kg,一个A原子质量是6.64×10-26kg。
则A的相对原子质量是()A、 40B、 24 C 、65 D 、6.64×10-26kg4、下列有关原子的说法中,错误的是()A.原子的质量和体积都很小B.原子在不停地运动着C.原子可以构成物质D.原子很小,不可再分【能力提升】5、下列关于原子的叙述中不正确的是()A.原子是化学变化中的最小粒子B.原子是构成物质的一种粒子C.原子中都含有质子、中子和电子D.原子的质量主要集中在原子核上英国科学家道尔顿最先确立了原子学说,他的中心论点主要有:①原子是不能再分的粒子;②原子是微小的实心球;③同种元素的原子,其性质和质量都相同.而现代科学实验表明:同种元素的原子内部有相同的质子数和不一定相同的中子数.从现代的观点看,你认为道尔顿的三个论点中,不确切的是()A.① B.①③ C.②③ D.①②③7、为形象展示水分解的微观过程,某同学制作了一些模型,表示相应的微观粒子.其中表示水分解过程中不能再分的微粒是()A. B. C. D.【对接中考】8.(重庆)同一原子中,下列说法错误的是()A.质子和电子的数目相同B.原子和中子的电性不同C.原子核和电子的质量不同D.原子核和原子的体积不同9.(荆州)下列说法中正确的是()A.原子核内的质子数与其核电荷数相等B.原子核中的质子数与中子数一定相等C.原子核一定由质子和中子构成D.元素的化学性质取决于原子核内的质子数10、(常州)下列关于原子的叙述中,正确的是()A.是带电的微粒 B.是实心球体C.可分解为分子 D.可转变成离子参考答案D 2、B 3、A 4、D 5、C 6、D 7、C 8、B 9、A 10、D。
京改版九年级化学上册第3章 第一节 原子 同步练习

第一节原子1.构成原子核的粒子一般是( )A.质子、中子和电子B.电子和中子C.质子和中子D.质子和电子2.已知一种碳原子可以用来测定文物的年代,该原子的原子核内含有6个质子和8个中子,则该原子的核外电子数为( )A.2B.14C.8D.63.原子的质量主要集中在( )A.质子B.中子C.电子D.原子核4. 根据相对原子质量的定义,判断铁原子的相对原子质量为( )A.56 gB.9.288×10-26 kgC.56D.112 g5.原子的相对原子质量( )A.是原子的真实质量B.可以用“kg”作为单位C.是比值,没有单位D.在数值上约等于质子数与中子数的和6.已知氦3的原子核是由1个中子和2个质子构成的,则其核外电子数和相对原子质量分别为( )A.1和2B.2和3C.3和1D.3和37.下列关于原子的叙述中正确的是( )①物质都是由原子构成的②原子是不能再分的③原子是实心的球体④同种原子的质量和性质都相同⑤原子在永远不停地运动着⑥由原子构成的物质,其化学性质由构成该物质的原子保持A.④⑤⑥B.①②③④⑥C.①③D.②④⑤8.下列各种粒子中带负电荷的是( )A.电子B.中子C.质子D.原子核9.已知一种氧原子,原子核内有8个质子和10个中子,则该氧原子中,核电荷数为( )A.18B.2C.10D.810. 据英国《自然》杂志报道,科学家已研制成功以锶原子做钟摆的“光晶格钟”,成为世界上最精确的钟。
已知一种锶原子的相对原子质量为88,其原子核外电子数为38,则这种锶原子的中子数为( )A.126B.88C.50D.3811.钛被称为航空金属,国产C919大飞机的钛合金用量达到9.3%。
已知一种钛原子核内有22个质子和26个中子,该原子的核外电子数为( )A.4B.22C.26D.4812. 原子的构成示意图如图3-1-1所示,下列叙述正确的是 ( )图3-1-1A.原子是实心球体B.质子、中子、电子均匀分布在原子中C.电子与质子的质量相等D.整个原子的质量主要集中在原子核上13 原子中的质子数等于( )A.中子数B.电子数C.最外层电子数D.相对原子质量14 考古学家通过测定碳14的含量等方法将人类生活在黄土高原的历史推前至距今212万年。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《第一节原子》习题
一.选择题(每小题有1~2个选项符合题意)
1.已知一个质子数和中子数都是6的碳原子的质量是1.993×10-26 kg,则一个氧原子的质量是()
A.16 g B.16
C.12×16×1.993×10-26 kg D.1.993×10-26÷12×16 kg
2.相同质量的下列原子,所含原子个数最多的是()A.氧原子B.铁原子C.氢原子D.氯原子
3.在原子中()
A.质子数一定等于中子数B.质子数一定等于电子数
C.质子数、中子数、电子数三者都相等D.原子核所带电量跟核外电子的电量相等
4.1803年,英国科学家道尔顿提出了原子学说,其主要论点有:①物质都是由原子构成的;②原子是微小的不可分割的实心球体;③同类原子的性质和质量都相同。
从现代观点看,这三个观点中不正确的是()
A.②B.①、②C.②、③D.①、②、③
5.如下图是水分子在一定条件下分解的示意图,从中获得的信息中不正确的是()
A.一个水分子由二个氢原子和一个氧原子构成
B.水分解后生成氢气和氧气的分子个数比为2∶1
C.水分解过程中,分子的种类不变
D.水分解过程中,原子的数目不变
6.我国“嫦娥工程”探月计划的一个重要目标是开发月球新能源——“氦—3”,10吨氦—3就能满足我国一年所有的能源需求。
关于氦原子的说法正确的是()
A.质子数为3,电子数为3 B.质子数为2,电子数为2 C.质子数为2,电子数为3 D.质子数为3,电子数为2
7.科学家设想宇宙中可能存在完全由反粒子构成的物质——反物质;物质反物质相遇会释放出巨大的能量,在能源研究领域中前景可观,正电子、负质子等都是反粒子,它们跟通常所说的电子、质子相比较,质量相等但电性相反,请您推测,反氢原子的结构可能是()A.由1个带正电荷的质子和1个带负电荷的电子构成
B.由1个带负电荷的质子和1个带正电荷的电子构成
C.由1个带正电荷的质子和1个带正电荷的电子构成
D.由1个带负电荷的质子和1个带负电荷的电子构成
二.填空题
8.下图中,表示氧原子,表示氢原子。
(1)根据此图,试分别从物质组成、分子构成的角度各说出一种观点:
a.;
b.。
(2)根据此图,说明化学反应的本质:。
9.原子是由原子核和电子构成的。
原子核在原子中所占体积极小,其半径在约为原子半径的十万分之一,因此,相对而言,原子里有很大空间,α粒子是带两个单位正电荷的氦原子。
1911年,科学家用一束平行高速运动的α粒子轰击金箔时(金原子的核电核数为79,相对原子质量为197),发现三种实验现象:
(1)有一小部分α粒子改变了原来的运动路径。
原因是α粒子途经原子核附近时,受到斥力而稍微改变了运动方向。
(2)大多数α粒子不改变原来的运动方向,原因是____________________。
(3)极少数α粒子被弹了回来,原因是_____________________________。
参考答案
一.选择题
1.D 2.C
3.答案:B D 点拨:质子数不一定等于中子数。
如氢原子有1个质子而无中子,所以A、C不正确。
在原子中核电荷数=质子数=电子数。
原子不显电性就是由于质子数=电子数。
所以B、D正确。
4.提示:(1)原子是构成物质的一种微粒,有些物质由原子直接构成,如稀有气体,而有些物质则由分子(或其他微粒)构成,如水、食盐等;(2)现代结构理论表明物质可无限分割,原子只是物质无限分割层次上的一个微粒,它还可以再分为原子核和核外电子;(3)同类原子(核电荷数相同)化学性质相同,但质量不同(因其核中质子数相同而中子数不同)。
所以,从现代观点看,以上三点都不正确,应选D。
5.答案:C
6.答案:B
7.答案:B
二.填空题
8.(1)a.物质由分子构成;b.在化学变化中,分子不是最小的微粒
(2)在化学变化中,分子分解成原子,原子重新组合成新的分子,原子总数不变。
9.(2)原子核的体积极小,原子核外有相对很大的空间
(3)α粒子撞击了带正电荷、质量大的金原子核而弹回。
