文献质量评价工具
常用的期刊评价的检索工具

3、常用于文献评价的权威检索工具有哪些?答:目前,大多数高校科研管理部门将下列四种数据库作为文献评价的权威检索工具:SCI (科学引文索引)、ISTP(科学技术会议录索引)、EI(工程索引)和CSCD(中国科学引文数据库)。
评价期刊最常用的检索工具: 美国《期刊引文报告JCR》、《中国科技论文统计源期刊目录》、《中文核心期刊要目总览》。
还有一些重要的检索工具也可作为文献评价的数据源:国外文献检索工具---美国《科学评论索引ISR》、美国《社会科学引文索引SSCI》、美国《艺术与人文科学引文索引A&HCI》、美国《化学文摘CA》、英国《科学文摘SA》、日本《科学技术文献速报CBST》、俄罗斯《文摘杂志AJ》、德国《数学文摘Zbl Math》、美国《数学评论MA》、法国《文摘通报BS》、美国《生物学文摘BA》等。
国内文献检索工具---《中国科学引文数据库CSCI或CSCD》、《中文社会科学引文索引CSSCI》、《中国人民大学书报资料中心复印报刊资料索引》。
《期刊引文报告》(SCI Journal Citation Reports,JCR)期刊引用报告(JournalCitation Reports)简称JCR,是由美国科学信息研究所(ISI)编制出版、国际上一种权威的用于期刊评价的重要工具。
JCR从1975开始,ISI在《科学引文索引》(SCI)年度累积本中,增加“期刊引用报告”部分。
JCR提供的信息包括:每种期刊在当前年被引用的总次数(Total Cites)、每种期刊的影响因子(即该刊前两年发表的文章在当前年的平均被引次数(Impact Factor))、每种期刊当前年发表的文章在当前年的平均被引次数(Immediacy Index)、每种期刊当前年的文章总数(Articles)、每种期刊论文研究课题的延续时间(Cited Half-life)、每种期刊的引用期刊列表(Citing Journal)、每种期刊的被引用期刊列表(Cited Journal)、每种期刊的影响因子在近几年的变化情况(Trends)、每种期刊的来源数据情况(Source Data)等。
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版

交替或循环
出生日期
病历号
其它明确的非隐藏过程
风险未知
没有足够信息判断为低风险或高风险。通常因分配隐藏的方法未描述或描述不充分。例如描述为使用信封分配,但为描述信封是否透明?密封?顺序编号?
对参与者和实施者的盲法
因参与者和实施者了解干预情况而导致实施偏倚
低风险判断标准
参与者以及纳入参与者的研究者因以下掩盖分配的方法或相当的方法,事先不了解分配情况
中心分配(包括电话,网络,药房控制随机)
相同外形的顺序编号的药物容器;
顺序编号、不透明、密封的信封
高风险判断标准
参与者以及纳入参与者的研究者可能事先知道分配,因而引入选择偏倚,譬如基于如下方法的分配:
使用摊开的随机分配表(如随机序列清单)
Selectionbias(biasedallocationtointerventions)duetoinadequateconcealmentofallocationspriortoassignment.
Performancebias.
BlindingofparticipantsandpersonnelAssessmentsshouldbemadeforeachmainoutcome(orclassofoutcomes).?
可能存在偏倚风险,但存在以下两种中的一种
没有足够信息评估是否存在其它重要的偏倚风险
没有足够的证据认为发现的问题会引入偏倚
summaryassessmentsoftheriskofbiasforeachimportantoutcome(acrossdomains)withinandacrossstudies
cochrane文献评价手册

Cochrane文献评价手册在医学和健康领域,Cochrane文献评价手册是一个备受推崇的参考资料。
它是一个致力于提供高质量、广度和深度兼具的文献评价和系统评价信息的权威评台。
通过对临床试验和其他医学研究进行全面评估和分析,Cochrane文献评价手册为医生、医学研究者和患者提供了宝贵的参考意见。
在Cochrane文献评价手册中,我们可以查找到各种主题的文献评价和系统评价,涵盖了从疾病预防到治疗、康复的各个方面。
无论是针对特定疾病、特定干预措施或特定人群的研究,Cochrane文献评价手册都提供了可靠的信息和意见,帮助人们做出更明智的医疗决策。
对于医学研究者来说,Cochrane文献评价手册提供了一个值得借鉴和学习的标准。
他们可以通过查阅Cochrane文献评价手册,了解到如何进行高质量的文献评价和系统评价,以及如何准确地汇总和分析研究结果。
这有助于提高他们的学术水平,促进医学研究的发展和进步。
对于医生和医疗工作者来说,Cochrane文献评价手册则是一个宝贵的临床参考工具。
他们可以在这里找到与自己临床实践相关的最新研究成果和最可靠的证据,以指导自己的临床决策。
这有助于提高临床实践的质量,保证患者获得更好的医疗服务。
对于患者和公众来说,Cochrane文献评价手册提供了一个可靠的信息来源。
他们可以在这里了解到关于自己健康问题的最新研究成果和治疗建议,从而更好地了解自身疾病,做出更明智的健康决策。
Cochrane文献评价手册是一个对医学研究、临床实践和健康决策都具有重要意义的权威评台。
它以其高质量、深度和广度兼具的文献评价和系统评价信息,为医学领域的各个参与者提供了宝贵的帮助和指导。
相信随着医学研究的不断进步和发展,Cochrane文献评价手册将为我们带来更多的惊喜和启发。
Cochrane文献评价手册作为权威评台,其对医学领域具有重要意义的确无庸置疑。
在现代医学研究中,由于信息的爆炸性增长和研究成果的不断涌现,医生和研究者需要一个可靠的参考工具来指导他们的决策和实践。
分析性横断面研究的文献质量评价工具

分析性横断面研究的文献质量评价工具澳大利亚JBI循证卫生保健中心(2016)对分析性横断面研究(analytical cross-sectional study)的质量评价工具包含8个评价项目(下表)。
评价者需对每个评价项目做出“是”、“否”、“不清楚”、“不适用”的判断,并最终经过小组讨论,决定该研究是纳入、排除,还是需获取进一步的信息。
澳大利亚JBI循证卫生保健中心对分析性横断面研究的真实性评价评价项目评价结果1. 是否清晰界定了研究对象的纳入标准?是否不清楚不适用2. 是否详细描述研究对象及研究场所?是否不清楚不适用3. 是否采用有效、可信的方法测评暴露因素?是否不清楚不适用4. 是否采用客观、标准的方法测评健康问题?是否不清楚不适用5. 是否明确了混杂因素?是否不清楚不适用6. 是否采取措施控制了混杂因素?是否不清楚不适用7. 是否采用有效、可信的方法测评结局指标?是否不清楚不适用8. 资料分析方法是否恰当?是否不清楚不适用条目解读:一是否清晰界定了研究对象的纳入标准论文中应清晰描述研究对象的纳入和排除标准,纳入和排除标准应具体。
二是否详细描述研究对象及研究场所论文中应详细描述研究对象的来源及特征,包括人口学资料、场所、取样时间。
三是否采用有效、可信的方法测评暴露因素论文中应清晰描述对暴露因素的测评方法。
判定其效度时需有金标准;信度通常包括内部一致性信度、评定者间信度。
四是否采用客观、标准的方法测评健康问题判断该研究纳入的患者是否依据公认的诊断标准或定义;如果没有使用公认的诊断标准或定义,应阐述是依据什么关键特征来匹配研究对象的。
五是否明确了混杂因素除了要研究的暴露因素不同外,各组间的其他因素也不同,会对结果带来干扰,这些因素就是混杂因素。
典型的混杂因素包括各组研究对象的基线特征、预后因素、与要验证的暴露因素同时存在的其他暴露因素。
高质量的研究应识别出这些潜在的混杂因素,并尽可能对其进行测评。
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版
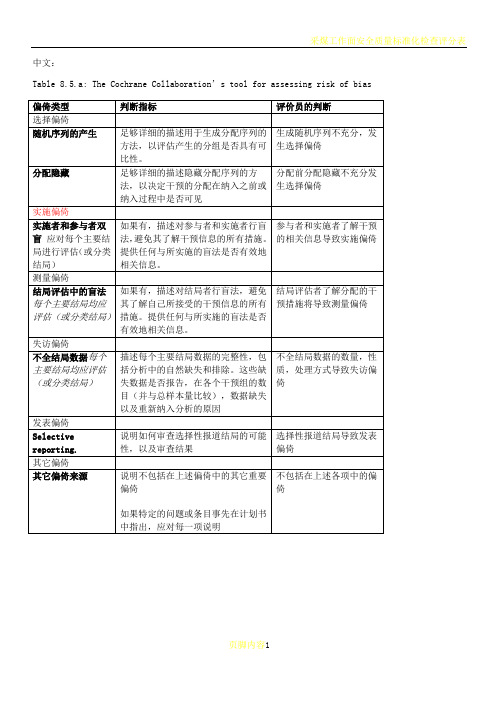
中文:Table 8.5.a: The Cochrane Collaboration’s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias’ assessment tool研究者描述随机序列产生过程譬如:参考随机数字表使用计算机随机数字生成器扔硬币洗牌的卡片和信封掷骰子抽签最小化*最小化,可实现无随机元素,被认为相当于是随机的。
研究者描述序列的产生使用的是非随机的方法。
通常是系统的非随机方法,例如:通过奇偶或出生日期产生序列通过入院日期产生序列通过类似住院号或门诊号产生序列相对于上面提到的系统方法,其它非随机的方法少见的多,也更明显。
通常包括对参与者进行判断或非随机的方法,例如:临床医生判断如何分配参与者判断如何分配基于实验室检查或系列测试的结果分配基于干预的可获取性进行分配中心分配(包括电话,网络,药房控制随机)相同外形的顺序编号的药物容器;顺序编号、不透明、密封的信封参与者以及纳入参与者的研究者可能事先知道分配,因而引入选择偏倚,譬如基于如下方法的分配:使用摊开的随机分配表(如随机序列清单)分发信封但没有合适的安全保障(如透明、非密封、非顺序编号)交替或循环出生日期病历号其它明确的非隐藏过程任何如下标准:无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破任何如下标准:无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况任何如下标准:无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破任何如下标准:无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况任何如下标准:无缺失数据缺失数据的产生不大可能与真实结局相关(对于生存数据,删失不大可能引入偏倚)缺失数据的数目在各干预组相当,且各组缺失原因类似对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;缺失的数据用合适的方法进行估算任何如下标准:缺失数据的产生很大可能与真实结局相关, 缺失数据的数目及缺失原因在各干预组相差较大对二分类变量,与观察事件的发生风险相比,缺失比例足以影响预估的干预效应对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)足以影响观察的效应规模;意向治疗分析中存在实际干预措施与随机分配的干预相违背的情况对缺失数据进行简单的不合适的估算任何如下标准:没有报道缺失或排除的情况,无法判断高风险或低风险(如未说明随机的数量,未提供数据缺失的原因)研究未描述此情况任何如下标准:实验的计划书可获取,系统评价感兴趣的所有首要或次要结局均按计划书预先说明的方式报道实验计划书不可得,但很明显发表的报告包括所有的结局,包括预先说明的结局(这种性质的有说服力的文字可能少见)任何如下标准:不是所有的预先说明的首要结局均被报道一个或多个首要结局为采用预先说明的测量方法、分析方法或数据子集来报道系统评价感兴趣的一个或多个首要结局报道不全,以至于不能纳入meta分析研究未报道此研究应当包含的主要关键结局具有与特殊试验设计相关的潜在偏倚来源或被指欺诈或其它问题可能存在偏倚风险,但存在以下两种中的一种没有足够信息评估是否存在其它重要的偏倚风险没有足够的证据认为发现的问题会引入偏倚Table 8.7.a: Possible approach for summary assessments of the risk of bias for each important outcome (across domains) within and across studies英文:Table 8.5.a: The Cochrane Collaboration’s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias’ assessment toolprocess such as:Referring to a random number table;Using a computer random number generator;Coin tossing;Shuffling cards or envelopes;Throwing dice;Drawing of lots;Minimization*.*Minimization may be implemented without a random element, and this isconsidered to be equivalent to being random.judgement The investigators describe a non-random component in the sequence generation process. Usually, the description would involve somesystematic, non-random approach, for example:Sequence generated by odd or even date of birth;Sequence generated by some rule based on date (or day) of admission;Sequence generated by some rule based on hospital or clinic recordnumber.Other non-random approaches happen much less frequently than thesystematic approaches mentioned above and tend to be obvious. Theyusually involve judgement or some method of non-random categorization ofparticipants, for example:Allocation by judgement of the clinician;Allocation by preference of the participant;Allocation based on the results of a laboratory test or a seriesof tests;Allocation by availability of the intervention.Criteria for a judgement Participants and investigators enrolling participants could not foreseeassignment because one of the following, or an equivalent method, was usedto conceal allocation:Central allocation (including telephone, web-based andpharmacy-controlled randomization);Sequentially numbered drug containers of identical appearance;Sequentially numbered, opaque, sealed envelopes.judgement Participants or investigators enrolling participants could possiblyforesee assignments and thus introduce selection bias, such as allocationbased on:Using an open random allocation schedule (e.g. a list of randomnumbers);Assignment envelopes were used without appropriate safeguards(e.g. if envelopes were unsealed or nonopaque or not sequentiallynumbered);Alternation or rotation;Date of birth;Case record number;Any other explicitly unconcealed procedure.Criteria for a judgement Any one of the following:No blinding or incomplete blinding, but the review authors judgethat the outcome is not likely to be influenced by lack of blinding;Blinding of participants and key study personnel ensured, andunlikely that the blinding could have been broken.judgementAny one of the following:No blinding or incomplete blinding, and the outcome is likely tobe influenced by lack of blinding;Blinding of key study participants and personnel attempted, butlikely that the blinding could have been broken, and the outcomeis likely to be influenced by lack of blinding.judgement ‘Unclear risk’ ofAny one of the following:Insufficient information to permit judgement of ‘Low risk’ or ‘High risk’;The study did not address this outcome.Criteria for a judgement Any one of the following:No blinding of outcome assessment, but the review authors judge thatthe outcome measurement is not likely to be influenced by lack ofblinding;Blinding of outcome assessment ensured, and unlikely that theblinding could have been broken.judgementAny one of the following:No blinding of outcome assessment, and the outcome measurement islikely to be influenced by lack of blinding;Blinding of outcome assessment, but likely that the blinding couldhave been broken, and the outcome measurement is likely to beinfluenced by lack of blinding.judgement ‘Unclear risk’ ofAny one of the following:Insufficient information to permit judgement of ‘Low risk’ or‘High risk’;The study did not address this outcome.Criteria for a judgement Any one of the following:No missing outcome data;Reasons for missing outcome data unlikely to be related to trueoutcome (for survival data, censoring unlikely to be introducingbias);Missing outcome data balanced in numbers across interventiongroups, with similar reasons for missing data across groups;For dichotomous outcome data, the proportion of missing outcomescompared with observed event risk not enough to have a clinicallyrelevant impact on the intervention effect estimate;For continuous outcome data, plausible effect size (difference inmeans or standardized difference in means) among missing outcomesnot enough to have a clinically relevant impact on observed effectsize;Missing data have been imputed using appropriate methods.judgement Any one of the following:Reason for missing outcome data likely to be related to trueoutcome, with either imbalance in numbers or reasons for missingdata across intervention groups;For dichotomous outcome data, the proportion of missing outcomescompared with observed event risk enough to induce clinicallyrelevant bias in intervention effect estimate;For continuous outcome data, plausible effect size (difference inmeans or standardized difference in means) among missing outcomesenough to induce clinically relevant bias in observed effect size;‘As-treated’ analysis done with substantial departure of theintervention received from that assigned at randomization;Potentially inappropriate application of simple imputation.judgement ‘Unclear risk’ ofAny one of the following:Insufficient reporting of attrition/exclusions to permit judgement of ‘Low risk’ or ‘High risk’ (e.g. number ran domized not stated,no reasons for missing data provided);The study did not address this outcome.Criteria for a judgement Any of the following:The study p rotocol is available and all of the study’spre-specified (primary and secondary) outcomes that are of interestin the review have been reported in the pre-specified way;The study protocol is not available but it is clear that thepublished reports include all expected outcomes, including thosethat were pre-specified (convincing text of this nature may beuncommon).judgementAny one of the following:Not all of the study’s pre -specified primary outcomes have beenreported;One or more primary outcomes is reported using measurements,analysis methods or subsets of the data (e.g. subscales) that werenot pre-specified;One or more reported primary outcomes were not pre-specified(unless clear justification for their reporting is provided, suchas an unexpected adverse effect);One or more outcomes of interest in the review are reportedincompletely so that they cannot be entered in a meta-analysis;The study report fails to include results for a key outcome thatwould be expected to have been reported for such a study.judgementThere is at least one important risk of bias. For example, the study: Had a potential source of bias related to the specific study designused; orHas been claimed to have been fraudulent; orHad some other problem.judgement ‘Unclear risk’ ofThere may be a risk of bias, but there is either:Insufficient information to assess whether an important risk of bias exists; orInsufficient rationale or evidence that an identified problem willintroduce bias.Table 8.7.a: Possible approach for summary assessments of the risk of bias for each important outcome (across domains) within and across studies。
文献评价指标sjr和hix

文献评价指标sjr和hixSJR是SCImago Joumal Rankings的缩写,是一个既考虑了期刊被引数量,又考虑了期刊被引质量的指标。
它采用Goode的PageRank算法,赋予高声望期刊的引用以较高的权重,并以此规则迭代计算直到收敛。
SNIP是Source Normalized Impact per Paper的缩写,是衡量期刊影响力的新工具。
SNIP是荷兰学者Moed 教授于2010年提出的全新期刊评价指标,旨在对不同主题领域的期刊影响力进行评价,为验证这一评价指标在期刊评价实践中的效用。
扩展资料文献检索方法:直接法又称常用法,是指直接利用检索系统(工具检索文献信息的方法。
它又分为顺查法、倒查法和抽查法。
顺查法顺查法是指按照时间的顺序,由远及近地利用检索系统进行文献信息检索的方法。
这种方法能收集到某一课题的系统文献,它适用于较大课题的文献检索。
例如,已知某课题的起始年代,需要了解其发展的全过程,就可以用顺查法从最初的年代开始查找。
倒查法倒查法是由近及远,从新到旧,逆着时间的顺序利用检索工具进行文献检索的方法。
使用这种方法可以最快地获得最新资料。
抽查法抽查法是指针对项目的特点,选择有关该项目的文献信息最可能出现或最多出现的时间段,利用检索工具进行重点检索的方法。
追溯法是指不利用一般的检索系统,而是利用文献后面所列的参考文献,逐一追查原文(被引用文献,然后再从这些原文后所列的参考文献目录逐一扩大文献信息范围,一环扣一环地追查下去的方法。
它可以像滚雪球一样,依据文献间的引用关系,获得更好的检索结果。
循环法又称分段法或综合法。
它是分期分交替使用直接法和追溯法,以期取长补短,相互配合,获得更好的检索结果。
参考资料来源:——文献检索。
cochrane纳入的RCT文献质量评价风险偏倚评价工具中英文对照版

分配隐藏
分配前不充足的分配隐藏导致选择偏倚
低风险判断标准
参与者以及纳入参与者的研究者因以下掩盖分配的方法 或相当的方法,事先不了解分配情况
•中心分配(包括电话,网络,药房控制随机)
•相同外形的顺序编号的药物容器;
•顺序编号、不透明、密封的信封
高风险判断标准
参与者以及纳入参与者的研究者可能事先知道分配,因
而引入选择偏倚,譬如基于如下方法的分配:
•使用摊开的随机分配表(如随机序列清单)
•分发信封但没有合适的安全保障(如透明、非密 封、非顺序编号)
•交替或循环
•出生日期
•病历号
•其它明确的非隐藏过程
风险未知
没有足够信息判断为低风险或高风险。通常因分配隐藏 的方法未描述或描述不充分。例如描述为使用信封分配, 但为描述信封是否透明?密封?顺序编号?
outcome assessors.
Attrition bias.
Incomplete outcome dataAssessments should be made for each main outcome (or class of outcomes).?
Describe the completeness of outcome data for each main outcome, including attrition and exclusions from the analysis. State whether attrition and exclusions were reported, the numbers in each intervention group (compared with total randomized participants), reasons for attrition/exclusions where reported, and any re-inclusions in analyses performed by the review authors.
JBI循证卫生保健中心关于不同类型研究的质量评价工具——干预性研究的质量评价

JBI循证卫生保健中心关于不同类型研究的质量评价工具——干预性研究的质量评价周英凤;顾莺;胡雁;邢唯杰【摘要】澳大利亚JBI循证卫生保健中心作为全球最大的循证协作中心之一,一直致力于推动循证资源的整合、传播和应用.在2016年11月,JBI推出了针对不同类型研究的质量评价工具,以帮助研究者科学评价研究的方法学质量.本文旨在对JBI 关于随机对照试验类的文献质量评价工具进行详细解读,该工具共包括13个条目,从随机化、对照、盲法的实施、研究对象的随访、结局指标收集及分析等方面全面评价RCT的研究质量.%The Joanna Briggs Institute (JBI) is an international,membership based research and development organization in Australia.The Institute specializes in promoting and supporting evidence-based resouces integration,dissemination and application November 2016,the Institute developed 13 critical appraisal tools for systematic reviews.This article focused on introducing the critical appraisal tool for randomized controlled trials.This tool consisted of 13 items and evaluated the methodological quality of RCT fromrandomization,concealment,blindness,followup,measurement and analysis.【期刊名称】《护士进修杂志》【年(卷),期】2018(033)001【总页数】3页(P24-26)【关键词】JBI循证卫生保健中心;文献质量评价;随机对照试验【作者】周英凤;顾莺;胡雁;邢唯杰【作者单位】复旦大学护理学院复旦大学JBI循证护理合作中心,上海200032;复旦大学附属儿科医院,上海200032;复旦大学护理学院复旦大学JBI循证护理合作中心,上海200032;复旦大学护理学院复旦大学JBI循证护理合作中心,上海200032【正文语种】中文【中图分类】R471Joanna Briggs循证卫生保健中心(JBI)是目前全球规模最大的循证卫生保健协作网之一,成立于1996年,总部设在澳大利亚阿德莱德大学。
XXX纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版

XXX纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版根据XXX的“偏倚风险评估工具”,表8.5.a列出了评估偏倚类型的指标。
其中,选择偏倚包括评估随机序列的产生,以及对分组可比性的评估。
需要提供足够详细的描述,以便判断分组的产生是否具有可比性。
分配偏倚则需要提供足够详细的描述,以评估分配是否隐藏,并决定干预的分配是否可见。
实施偏倚则需要描述实施者和参与者是否采用了双盲方法,以避免其了解干预信息。
同时,需要提供与实施的盲法是否有效相关的信息。
测量偏倚则需要描述对结局者行盲法,避免其了解所接受的干预信息。
同时,需要提供与实施的盲法是否有效相关的信息。
失访偏差需要描述每个主要结局数据的完整性,以及缺失数据是否报告。
同时,需要说明重新纳入分析的原因。
发表偏差需要说明如何审查选择性报道结局的可能性,以及审查结果。
其他偏差则需要说明不包括在上述偏差中的其他重要偏差。
如果在计划书中指出了特定的问题或条目,需要对每一项进行说明。
表8.5.d列出了评估偏倚风险的标准。
其中,随机序列的产生不充分会导致选择偏差。
对于评判为低风险的标准,研究者需要描述随机序列产生的过程,例如参考随机数字表、使用计算机随机数字生成器、扔硬币、洗牌的卡片和信封、掷骰子、抽签、最小化等方法。
对于评判为高风险的标准,研究者需要描述使用的非随机方法,通常是系统的非随机方法,例如最小化,虽然可实现无随机元素,但被认为相当于是非随机的。
可能被打破,结局很可能受到缺乏盲法的影响风险未知任何如下标准:没有足够信息判断为低风险或高风险研究未描述此情况随机化是临床研究中重要的方法之一,但在实施随机化时,存在着一些潜在的风险和偏差。
在随机化的过程中,通常会采用系统方法或非随机的方法来产生序列。
其中,系统方法包括通过奇偶或出生日期、入院日期、住院号或门诊号等方式产生序列;非随机的方法则包括临床医生或参与者的判断、实验室检查或系列测试的结果、干预的可获取性等方式来分配。
cochrane文献质量评价分级

cochrane文献质量评价分级医学文献的定义及类别“文献”一词出现在中国已有2000多年的历史,从春秋战国时期就有关于文献的记载,最早见于《论语八佾》。
随着人类文明的发展,“文献”的概念也发生了巨大的变化,人们对文献的研究一直持续至今。
文献的具体定义尚缺乏统一的定论,《现代汉语词典》对文献的定义是“有历史价值或参考价值的资料”[1];《中华人民共和国国家标准—文献著录总则》将文献定义为“记载有知识的一切载体”[2]。
有学者将文献定义为“文献就是将知识、信息用文字、符号、图像、音频等记录在一定物质载体上的结合体”[3]。
有历史价值和研究价值的知识、一定的载体、一定的方法和手段、一定的意义表达和记录体系这4个方面构成文献的基本要素。
医学文献(medicalliterature)就是与医学有关的有参考价值的资料。
按照文献的研究类型分为:系统评价、随机对照临床试验、队列研究、病例对照研究、病例系列研究、病例报告和专家经验总结等。
决定文献质量的关键部分:研究有首创性或提供了新证据、研究对象的选择合理、科研设计合理、偏倚得到有效控制、研究样本量足够大和研究的时间足够长。
然而医学文献是如何发挥作用的,前提就是该文献必须有一定的价值,而且有可靠的等级评价体系。
医学文献的价值就是根据其文献内在及外在真实性及临床意义的重要性去评判,是根据医学研究的方向不同确定评价的原则和方法[4],其中内在真实性是文献评价的重点。
2西医文献评价体系2.1证据分级20世纪60年代,首次提出证据分级概念,将随机对照研究的质量定为最高,并引入内部真实性和外部真实性的概念。
证据分级为西医识别文献可靠性的准则。
最初3级标准:1级:设计良好的随机对照试验(RCT);2级:1级和3级中间的类型;3级:专家经验。
老5级标准:1级:收集所有质量可靠的RCT后做出的系统评价或Meta分析结果,大样本多中心随机对照试验;2级:单个大样本的RCT结果;3级:设有对照但未用随机方法分组的研究病例对照研究和队列研究;4级:无对照的系列病例观察;5级:专家意见、描述性研究和病例报告。
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版讲解学习

缺失数据的产生不大可能与真实结局相关(பைடு நூலகம்于生存数据,删失不大可能引入偏倚)
缺失数据的数目在各干预组相当,且各组缺失原因类似
对二分类变量,与观察事件的发生风险相比,缺失比例不足以影响预估的干预效应
对连续性结局数据,缺失数据的合理效应规模(均数差或标准均数差)不会大到影响观察的效应规模;
缺失的数据用合适的方法进行估算
因参与者和实施者了解干预情况而导致实施偏倚
偏倚低风险标准
任何如下标准:
无盲法或盲法不充分,但系统评价员判断结局不太可能受到缺乏盲法的影响
参与者和主要实施者均实施可靠的盲法,且盲法不太可能被打破
偏倚高风险标准
任何如下标准:
无盲法或盲法不充分,但系统评价员判断结局很可能受到缺乏盲法的影响
尝试对关键的参与者和实施者行盲法,但盲法很可能被打破,结局很可能受到缺乏盲法的影响
实验计划书不可得,但很明显发表的报告包括所有的结局,包括预先说明的结局(这种性质的有说服力的文字可能少见)
高风险判断标准
任何如下标准:
不是所有的预先说明的首要结局均被报道
随机序列的产生
随机序列产生不充分导致选择偏倚
判断为低风险的标准
研究者描述随机序列产生过程譬如:
参考随机数字表
使用计算机随机数字生成器
扔硬币
洗牌的卡片和信封
掷骰子
抽签
最小化
*最小化,可实现无随机元素,被认为相当于是随机的。
判断为高风险的标准
研究者描述序列的产生使用的是非随机的方法。通常是系统的非随机方法,例如:
其它偏倚
其它偏倚来源
说明不包括在上述偏倚中的其它重要偏倚
如果特定的问题或条目事先在计划书中指出,应对每一项说明
jbi文献质量评价工具英文版

jbi文献质量评价工具英文版Title: A Review of Quality Assessment Tools for Journal of Biomedical Informatics (JBI) Literature1. IntroductionThe Journal of Biomedical Informatics (JBI) is a renowned platform for research articles in the field of biomedical informatics. To ensure the reliability and validity of published articles, it is essential to have a sound evaluation process in place. The purpose of this paper is to review and analyze various tools employed for assessing the quality of JBI literature.2. MethodologyA comprehensive literature search was conducted using databases such as PubMed, Scopus, and Google Scholar. Keywords such as "JBI," "journal assessment," "literature quality," and "evaluation tools" were used to identify relevant articles. The inclusion criteria were articles that presented or discussed tools specifically designed for assessing the quality of JBI literature. Exclusion criteria included articles not published in English or those that did not focus on JBI literature.3. Findings3.1. PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses)PRISMA is a widely used tool for systematic reviews and meta-analyses. Although not explicitly designed for JBI literature, it serves as a valuable resource in assessing the quality of research articles. PRISMA provides a transparent reporting framework, emphasizing the inclusion of essential components in study design, conduct, and reporting. It consists of a 27-item checklist covering title, abstract, introduction, methods, results, discussion, and funding.3.2. CONSORT (Consolidated Standards of Reporting Trials)CONSORT is a guideline developed for reporting randomized controlled trials (RCTs). It consists of a 25-item checklist that addresses different aspects of RCT reporting, ensuring transparent and comprehensive reporting of study findings. While not exclusive to JBI literature, CONSORT aids in evaluating the quality of RCTs published in JBI.3.3. STARD (Standards for Reporting of Diagnostic Accuracy Studies)STARD is a tool designed for assessing the quality of diagnostic accuracy studies. It encompasses a 25-item checklist, covering all the necessary aspects of study design and reporting. By adhering to the STARD guidelines, authors can ensure the reliability and transparency of their research findings in the domain of diagnostic accuracy.3.4. PRISMA-ScR (PRISMA Extension for Scoping Reviews)PRISMA-ScR is an extension of the PRISMA tool specifically developed for scoping reviews. Scoping reviews are gaining popularity in the JBI field, and this tool assists in evaluating the quality and reliability of such reviews. PRISMA-ScR follows a 20-item checklist, ensuring a comprehensive and systematic approach to literature review.4. DiscussionWhile there is an absence of specific tools exclusively targeting the assessment of JBI literature, the aforementioned tools play a vital role in evaluating the quality of research articles published in JBI. These tools provide valuable frameworks and checklists to assess the transparency, reliability, and validity of research findings.It is imperative for authors, editors, and reviewers of JBI literature to familiarize themselves with these tools and incorporate them into the review process. By utilizing these assessment tools, the overall quality of JBI literature can be significantly enhanced, thereby facilitating evidence-based decision-making in the field of biomedical informatics.5. ConclusionIn conclusion, despite the lack of specific tools for quality assessment of JBI literature, existing tools such as PRISMA, CONSORT, STARD, and PRISMA-ScR can be effectively utilized. These tools offer valuable guidelines and checklists to ensure transparent reporting and enhance the overall quality of JBI literature. Authors, editors, and reviewers should actively employ these tools to maintain the credibility and reliability of research published in JBI. Future research should focus on developing tools specifically tailored to evaluate JBI literature, further advancing the field of biomedical informatics.。
cochrane纳入的RCT文献质量评价风险偏倚评估工具中英文对照
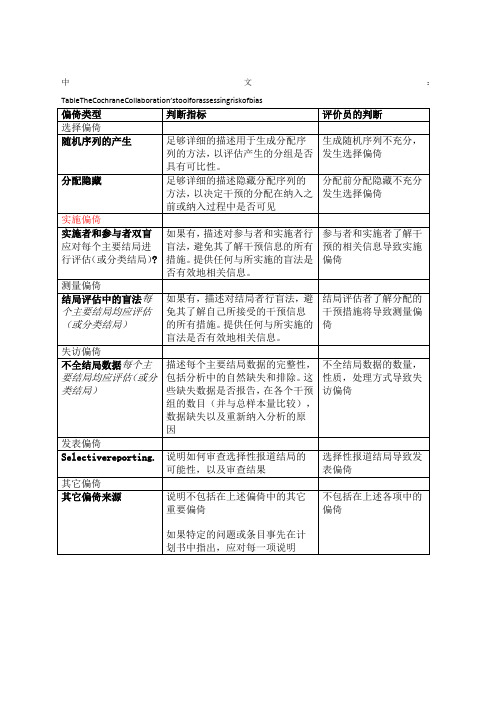
结局评估者了解分配的干预措施将导致测量偏倚
失访偏倚
不全结局数据每个主要结局均应评估(或分类结局)
描述每个主要结局数据的完整性,包括分析中的自然缺失和排除。这些缺失数据是否报告,在各个干预组的数目(并与总样本量比较),数据缺失以及重新纳入分析的原因
Selectionbias.
Randomsequencegeneration.
Describethemethodusedtogeneratetheallocationsequenceinsufficientdetailtoallowanassessmentofwhetheritshouldproducecomparablegroups.
基于实验室检查或系列测试的结果分配
基于干预的可获取性进行分配
偏倚风险不清楚的判断标准
没有足够的信息判断随机序列的产生存在高风险或低风险
分配隐藏
分配前不充足的分配隐藏导致选择偏倚
低风险判断标准
参与者以及纳入参与者的研究者因以下掩盖分配的方法或相当的方法,事先不了解分配情况
中心分配(包括电话,网络,药房控制随机)
Selectionbias(biasedallocationtointerventions)duetoinadequategenerationofarandomisedsequence.
Allocationconcealment.
Describethemethodusedtoconcealtheallocationsequenceinsufficientdetailtodeterminewhetherinterventionallocationscouldhavebeenforeseeninadvanceof,orduring,enrolment.
cochrane纳入的RCT文献质量评价(风险偏倚评估工具)中英文对照版..

cochrane纳⼊的RCT⽂献质量评价(风险偏倚评估⼯具)中英⽂对照版..中⽂:Table 8.5.a: The Cochrane s tool for assessing riskTable 8.5.d: Criteria for judging risk ofbias in the assessment tool Risk of bias分配隐藏分配前不充⾜的分配隐藏导致选择偏倚Table 8.7.a: Possible approach for summarya ssessments of the risk of bias for each important outcome (across domains) within and across studies英⽂:Table 8.5.a: The Cochrane Collaboration ' s tool for assessing risk of biasTable 8.5.d: Criteria for judging risk of bias in the ‘Risk of bias ' assessment toolriskorsOTHER BIASTable 8.7.a: Possible approach for summary assessments of the risk of bias foreach important outcome (across domains) within and across studiesthose that were pre-specified (convincing text of this naturemay be uncommon).Criteria for theudgement o f ‘Highrisk of bias. Any one of the following: ' Not all of the study'-spse pcrifeied primary outcomes havebeen reported; One or more primary outcomes is reported using measurements,analysis methods or subsets of the data (e.g. subscales) thatwere not pre-specified;One or more reported primary outcomes were not pre-specified(unless clear justification for their reporting is provided,such as an unexpected adverse effect);One or more outcomes of interest in the review are reportedincompletely so that they cannot be entered in a meta-analysis;The study report fails to include results for a key outcomethat would be expected to have been reported for such a study.Criteria for the udgement of ‘ Unclear isk ' of bias.Insufficient information to permit judgement of ‘Low risk ' or ‘Hi It is likely that the majority of studies will fall into this category. gh risk。
常用的meta分析文献质量评价量表:AHRQ文献质量评价--横断面研究

AHRQ横断面研究评价标准
美国卫生保健质量和研究机构(Agency for Healthcare Research and Quality,AHRQ)对观察性研究的质量评价标
准进行了推荐,其中推荐NOS量表作为评价队列研究和病例-对照研究的标准;推荐评价横断面研究(cross-sectional study)的标准包括11个条目,分别用“是”、“否”及“不清楚”作答:
(1)是否明确了资料的来源(调查,文献回顾)?
(2)是否列出了暴露组和非暴露组(病例和对照)的纳入及排除标准或参考以往的出版物?
(3)是否给出了鉴别患者的时间阶段?
(4)如果不是人群来源的话,研究对象是否连续?
(5)评价者的主观因素是否掩盖了研究对象其他方面情况?
(6)描述了任何为保证质量而进行的评估(如对主要结局指标的检测/再检测);(7)解释了排除分析的任何患者的理由;
(8)描述了如何评价和(或)控制混杂因素的措施;
(9)如果可能,解释了分析中是如何处理丢失数据的;
(10)总结了患者的应答率及数据收集的完整性;
(11)如果有随访,查明预期的患者不完整数据所占的百分比或随访结果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
■ r■■ I ■ r ■■■■■ r■■ i ■ r■■ i ■■■■■ i ■ r■■ i ■■■■■ i ■ r■■ i ■■■■■ i ■ r■■ i ■ r ■■■■■ r■■ i ■ r ■溟大利亚JBI循证为证保健中心对类实验性研宪的真实性评价(2004)
作者(年份〉、標期刊(名稱、卷期■ Mtt)
研完方法(Deriga)
研丸Wlt(ParticQam)
介入措施(Intes'vention)
比IMtttCCoirparison)
成果指fll(Outtome)
■ r
■ ■ I ■ r ■
■ ■ ■ ■ r
■ ■ i ■ r ■ ■ i ■ ■ ■ ■ ■ i ■ r ■ ■ i ■ ■ ■ ■ ■ i ■ r ■ ■ i ■ ■ ■ ■ ■ i ■ r ■ ■ i ■ r ■
■ ■ ■ ■ r
■ ■ i ■ r ■
评析理目 结果 评析依据
瞬丸目的是否明确■立題依据是否充分? 清
是
否不
胃料分析方法是否恰当? I
主丸成果
i • ** > ■ i * * > ■ ■ i * * > ■ i * * > ■ ■ * * * > ■ i * > ■ ■ * * ■
否 不清楚
f t
英H 牛津大学«证医学中心对病例对照研完的真实性评价 篇
名 AU>U<UMU<iUtl<AU*UtU*»HaUU<4A>JU>/>UUMd<44l*U4
研丸方法(Deriga )
研 ^WXParticpant)
/hAJtttCIntervenlion)
xtf la
Ulf
QU
比 <5WSJI(Comparison)
成果指 fil(Outtome)
imtniruiHavuuuvntvnivnmtvumtHimifMiuiriuiitMiimmtrfiiiiiMititim lU ■UtlUUfWIUUlUMU
IIIUK
RMfi 的M 入方法和样本量是否怡当.ft 否代表硏宪祥体
I
评析琐目 结果 评析依据
作# (年份)•標《、期刊(名卷期-頁ft )
illllUIIIOIIIIIIIIIIIKtlllllllllllKIIKIUIIIIIIIIIIIIKIIIIIII
一
是否不
&.PP
甘黒但的M 入方法和样本■是否恰当,能否代《总体•与病例粗是 曹 FCS. I 制鼻*因索的测量是否准确•病例姐和对照组的測■方式是否一敦・ 是 否 不清楚 !□不清殖
庄研完设计和责料分析中.是否考虑到了所有■要的鴻杂因素 楚
清
是否不 h F E —
I 隹9m 完成果
I
「
「
英国牛津大学循证医学中心对队列研兄的真实性评价
研丸方法(Deriga)
研^WXParticpant)
/hAJtttCIntervenlion)
比<5WSJI(Comparison)
成果指fil(Outtome)
评析琐目结果评价依据
牌*的第入方湛t否恰瓠能否代表研克髀体? 1
□是
□否□不清楚
篇
UAAUU*UUA>1UWi>A^U.U UAUU ** ** * **^
作者(年份八標乐期刊(名稱、卷期、頁ft)
等級
I
i«ii»iiiVM<ii«ii»»iiiMiii«iiBn«ia«ii»iuii«ii«>tt«iiii*tiii<iniuiiniiaiii<iimi<iaiiiiiiityivaiifiiiiHViiiviiriiivairiiivnitminiiif»irnviiifimiifiiitnvmviiviipUHB»mimimiun»uimitmiwuuui«nimfm«tn» I tt
果 |l
较好的代豪
上整凹鯉5 ___
f
评价依IK
•■MH*
■SMHBUJUUV的可比 ft Wfttt
(ttitW分析輪段〉
M*
■«n)attt
■否(时m«*・參豊耒发生庚研几的鬚需》 —h ------------------------------- L ■访9UL 对折有的研欢Um 访
《详价己可ufiie —个M 访*》•少 央«小井对喪旳着进厅了||述分析•
|1
于•MUJI* 自同一人 «•
自不 M 人 VI
F 秦ffft 耒・
乍产iMjfen 记录〈鈿外科tt£»)• btt 梅式问《1■畫
r 自己的记录 **««
卜的69*诊1»分併对《•
p««其«的・«69* (fltaS-SSH«> AIMD 分併对 |» (可以9W 为ft 否对SV 的■*因f»S 行了視正〉
11独立的盲法《«和秤估• 卜««可靠的记录• Icene*
__________
kitt*
jCB访«VtMU对失访《我有进疗播
述k林述
注,毎,项研兜花“选斤-和“估ar上的何,个条【1«多可以和•个“锹而在"M比竹「上的条可以育两个.。
