用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质C的含量
特殊杂质检查法

2.阿司匹林中检查游离水杨酸 游离水杨酸来源:a.生产中未 反应完全;b、贮存中水解 影响:游离水杨酸酸性较强, 对胃粘膜43;Fe3+一不反应 SA+Fe3+一紫堇色
检查方法:样品管:取样品0.1g,加乙醇 1ml溶解 1ml 加水至50m1 标准管:水杨酸0.1g加水溶解,加醋酸 加水至1000m1,取出1.0m1加 乙醇1ml,水48ml。 样品管、标准管均加新制成稀硫酸铁铵 lml,摇匀30"内如显色,比较不得更深。
③加校正因子的主成分自身对照法 将供试溶液稀释成与杂质限度相 当浓度作为对照溶液,分别取供试溶 液和对照溶液进样分析,供试液中各 杂质峰面积总和与校正因子相乘后与 对照溶液主成分峰面积比较,计算供 试品中杂质的含量。
校正因子(f) =
AS / CS AR / CR
(C x) f × =
Ax ′ AS / C'S
例如ChP2000枸橼酸乙胺嗪中检查N-甲 基哌嗪。 板:硅胶G薄层板 点样:供试品(50mg/ml甲醇液, 对照品(N-甲基哌嗪50μg/ml甲醇液), 各10μl 展开剂:氯仿:甲醇:氨水(13: 5:1) 显色剂:置碘蒸气中显色。 规定:供试品液所显与对照品液 相应的杂质斑点,颜色不得深于对照 品液主斑点。
L = 杂质量/ 供试品量×100% = 2×10 ×100% = 0.06%
0.05 453× 100 −3
3)吸附或分配性质的差异(色谱差异) (1)TLC:根据药物与杂质对吸附剂 的吸附或展开剂的解析能力不同,加以 分离和检查。 ①利用待检杂质的纯品作对照:用待 检杂质纯品(或可能存在的杂质纯品) 作为对照液,与供试液点于同一薄层板 上,展开和定位后进行检查。
②不加校正因子的主成分自身对照法
(完整版)药物分析简答题

1.药物分析的任务是什么?①.药物成品的化学检验工作②。
药物生产过程的质量控制③。
药物贮存过程的质量考察④。
临床药物分析工作2.高效液相色谱法检查药物的杂质方法有几种?①。
内标法加校正因子测定供试品中某个杂质含量②.外标法测定供试品中某个杂质含量③。
加校正因子的主成分自身对照法④。
不加校正因子的主成分自身对照法⑤。
面积归一法3。
杂质有哪些来源和途径?来源;①。
从药物生长过程中引入②.由药物储藏过程中引入途径:在合成药的生产过程中,未反应完全的原料、反应的中间体和副产物,在精致时未能完全出去,就会成为产品中的杂质。
药品在储藏过程中,在外界条件的影响下,或因微生物的作用,可能发生水解、氧化、分解、异构化、晶型转变、聚合、潮解和发霉等变化,产生有光的杂质。
具有酚羟基、巯基、亚硝基、醛基以及长链共轭多烯等结构的药物,在空气中易被氧化,引起药物变色、失效甚至产生毒性的氧化产物等。
4。
铁盐检查法中加入硫酸铵的目的是什么?加入氧化剂过硫酸铵,一方面可以氧化供试品中Fe²+成Fe³+,同时可防止光线导致的硫氰酸铁还原货分解褪色.5。
为什么标准铅液、标准铁液、标准砷液都要事先配制成储备液存放,用时稀释?铅离子、铁离子和亚砷酸根离子在低浓度、近中性溶液中易水解,故先配成高浓度的酸性储备液,使其稳定。
用时稀释即可。
6。
薄层色谱法检查杂质的类型有哪几种?①.选用实际存在的待检杂质对照品法②.选用可能存在的某种物质作为杂质对照品③.高低浓度对比法④.在检查条件下,不允许有杂质斑点。
7。
用对照法检查杂质,应注意哪些方面的平行?供试液的处理和对照液的处理在所用试剂、反应条件、反应时间、实验顺序登方面要相同,以保证结果的可比性。
8.重金属检查的常用四种方法反别在什么情况下应用?第一法(硫代乙酰胺法):适用于无需有机破坏,在酸性条件下可溶解的,无色的药物的重金属检查。
第二法(炽灼破坏后检查重金属):适用于含芳香环、杂环以及不溶于水稀酸及乙醇的有机药物的重金属检查.第三法(硫化钠法):适用于溶于碱而不溶于稀酸或在稀酸中生成沉淀的药物。
药物分析--期末试卷和答案

B.氧化物、聚合物
C.降解物、水解物
D.分解物、霉变物
E.异构体、残留溶剂、重金属
6. 用高氯酸滴定时,常用的溶剂有
A.二甲基甲酰胺
B.无水甲酸
C. 醋酐
D.乙二胺
E.冰醋酸
7.HPLC 测定中,为达到系统适用性试验要求,可适当改变色谱条件,但不能改变
A. 固定相种类
B. 流动相组成
C. 色谱柱长度
A. 碘化铋钾 B. 三氯化铁 C. 碘化钾 D. 硫酸亚铁 E. 亚铁氰化钾 4. UV 测定药物含量时,溶液的吸光度应控制在 误差最小。
A. 0.2~0.8 B. 0.3~1.0 C. 0.00~2.00 D. 0.3~0.7 E. 0.1~1.0 5. 可以以信噪比 S/N=10 时相应的浓度或量预测的分析方法的效能指标是 A. 线性 B. 检测限 C. 定量限 D. 精密度 E. 专属性 6. 中药制剂的质量分析是指 A.对中药制剂的定性鉴别 B.对中药制剂的性状鉴别 C.对中药制剂的检查 D.对中药制剂的含量测定 E.对中药制剂的鉴别、检查和含量测定等方面的评价 7. 鉴别是
D.测定易损成分 E.测定专属性成分
11. 可用于硫酸链霉素鉴别的显色反应有
A.与茚三酮反应
B.葡萄糖胺反应
C.Molisch 反应 D.板口反应
(Sakaguchi Reaction) E.麦芽酚反应(Maltol Reaction)
12. 紫外光谱法鉴别药物时常用的测定方法有
A 测定λmax,λmin
D. 流动相流速
E. 检测器类型
3
8. 可用作气相色谱法的载气有
A. 空气
B. 氧气
C. 氮气
D. 氢气
E. 氦气
HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量

HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量1. 引言1.1 研究背景高效液相色谱(HPLC)是一种高效、精确的分析方法,已广泛应用于药物分析领域。
在HPLC分析过程中,由于色谱柱的运用、温度变化等因素,可能会导致色谱峰的漂移,造成定量分析的误差。
为了解决这一问题,加入校正因子及主成分自身对照法成为一种常用的校正方法。
本研究旨在利用HPLC加校正因子的主成分自身对照法,对盐酸特拉唑嗪片中有关物质的含量进行准确测定,以提高药物质量的控制水平,保证药物的安全有效使用。
通过本研究,将为药物检测方法的改进与发展提供参考,并推动相关领域的研究进展。
1.2 研究目的研究目的是为了建立一种可靠、准确的方法来测定盐酸特拉唑嗪片中有关物质的含量,以确保药品质量符合标准要求。
通过使用HPLC 加校正因子的主成分自身对照法,可以提高测定的准确性和精确度,为药物生产和质量控制工作提供有力支持。
本研究旨在探讨该方法在实际药品分析中的应用前景,为相关领域的研究和实践提供参考和借鉴,推动药品检验技术的不断创新与提高。
通过深入研究盐酸特拉唑嗪片中的有关物质含量测定方法,可以为进一步优化药品生产工艺、提高产品质量和安全性提供科学依据,促进药品行业的可持续发展和健康发展。
1.3 研究意义盐酸特拉唑嗪片是一种常用的药物,用于治疗胃酸过多引起的胃溃疡、十二指肠溃疡等消化系统疾病。
而在药品生产和质量控制中,准确测定药物中的活性成分含量是至关重要的。
研究如何准确、快速地测定盐酸特拉唑嗪片中有关物质的含量具有重要的意义。
HPLC加校正因子的主成分自身对照法是一种常用的药物含量测定方法,具有高灵敏度、高分辨率和高准确性的特点。
通过该方法可以有效地对药物中的活性成分进行定量分析,为药品的生产质量提供有力支持。
本研究拟通过HPLC加校正因子的主成分自身对照法,对盐酸特拉唑嗪片中的活性成分进行含量测定,旨在为药品质量控制提供更加可靠的分析方法,并为相关药物的生产和质量管理工作提供参考。
《药物分析》杭太俊第8版 第三章 药物的杂质检查

比较法: 取一定量的 供试品,测 定待检、杂 质与规定的 限量比较。
第三章 药物的杂质检查
• 1、标准对照法
• 取一定量 (C·V) 与被检杂质相同的纯品或对照品配成对照 品溶液,与一定量(S)药物供试溶液在相同条件下处理后, 比较反应结果,以确定杂质含量是否超过规定。
操作:
平行试验比较两比色管的 颜色或浊度,判断杂质限量 是否符合规定。
和疗效,甚至对人体健康有害的微量物质(ChP规定) 。
杂质包括: 对人体健康有毒副作用的物质; 本身无毒副作用,但影响药物的稳定性和疗效的物质; 本身无毒副作用,也不影响药物的稳定性和疗效,但影响药 物的科学管理。 为保证药品质量,确保用药安全、有效,必须检查杂质,控 制药物纯度。
第三章 药物的杂质检查
• 药物的纯度(Purity):指药物的纯净程度。 • 其中杂质是影响药物纯度的主要因素,可
使得药物的外观性状、物理常数发生变化, 影响药物的稳定性,使药物的活性降低、 毒副作用增加。
第三章 药物的杂质检查
• 如氧氟沙星(右旋为杂质),地高辛(洋地黄毒苷)等。
• 盐酸哌替啶(Pethidine Hydrochloride)
稀释液对照品 供试品
第三章 药物的杂质检查
• ③ 对照药物法 当无适合的杂质对照 品,尤其是供试品显示 的杂质斑点颜色与主成 分斑点颜色有差异,难 以判断限量时,可用与 供试品相同的药物作为 对照品,此对照物中所 含待检杂质需符合限量 要求,且稳定性好。
供试品 符合要求药物
2 、HPLC法
主要方法
• 1、显色反应(如5-氯水杨酸的鉴别):
• 方法:取本品0.5g,加水10ml,煮沸2分钟,放冷,滤过, 滤液加三氯化铁试液数滴,不得显红色或紫色。
药物分析复习

二、填空题1、银量法测定巴比妥类是。
【答案】巴比妥类药物首先生成一银盐,当巴比妥类药物完全形成一银盐后,稍过量的银离子就与巴比妥类药物形成难溶性的二银盐,使溶液混浊,以此指示终点。
2、芳酸类药物的酸性强度与有关。
【答案】苯环、羧基或取代基的影响3、酰胺类药物基本结构为。
【答案】4、Vitali反应鉴别硫酸阿托品或氢溴酸东莨菪碱的原理为。
【答案】阿托品水解成莨菪酸,可与发烟硝酸共热,生成黄色硝基衍生物。
5、用高氯酸的冰醋酸滴定液滴定生物碱硫酸奎宁盐时,将硫酸盐只能滴定至。
【答案】硫氢酸盐6、取某吡啶类药物约2滴,加水1 ml,摇匀,加硫酸铜试液2滴与硫氰酸铵试液3滴,即生成草绿色沉淀。
该药物应为。
【答案】尼克刹米7、芳胺类药物适量,加水溶解,加氢氧化钠试液使溶液呈碱性,即生成白色沉淀,加热沉淀则变为油状物,继续加热,则产生可使红色石蕊试纸变蓝的气体。
该药物应为。
【答案】盐酸普鲁卡因8、药典采用溴量法测定盐酸去氧肾上腺素及其注射液的含量时,1 ml溴滴定液(0.1 mol/L)相当于盐酸去氧肾上腺素(其分子量为203.7)的量为。
9、三点校正法测定维生素A含量中,第二法测定的是,以为溶剂。
【答案】维生素A醇,异丙醇10、古蔡氏检砷法的原理为金属锌与酸作用产生________,与药物中微量砷盐反应生成具挥发性的________,遇溴化汞试纸,产生黄色至棕色的砷斑,与一定量标准砷溶液所产生的砷斑比较,判断药物中砷盐的含量。
【答案】新生态氢,砷化氢11.引起中药制剂结块、霉变或有效成分分解的主要原因是,检查方法有、和。
【答案】水分过多,甲苯法,烘干法,气相色谱法。
【答案】生产和储存过程中引入的杂质14. 中国药典(2000版)规定盐酸氯丙嗪原料药的含量测定中采用非水滴定法,而注射剂则采用紫外分光光度法,其原因是。
【答案】防止抗氧化剂的干扰三、简答题(15%)1、根据下列药物的结构,请简要设计其鉴别和含量测定的方法。
杂质测定中加校正因子的主成分自身对照法的校正因子测定问题

杂质测定中加校正因子的主成分自身对照法的校正因子测定问题杂质测定中加校正因子的主成分自身对照法:在杂质研究中,因某一杂质与主成分在某一波长下的响应因子不在0.9-1.1范围内,可考虑采用加校正因子的主成分自身对照法。
此校正因子可直接载入各品种项下,用于校正杂质的实测峰面积。
这些需做校正因子的杂质,通常以主成分为参照,采用相对保留时间定位,其数值一并载入各品种项下。
(可以理解为校正因子具有法律效应的作用)关于校正因子的理论知识如下:色谱定量分析的依据是被测组分量与检测器的响应信号(峰面积或峰高)成正比。
但是同一种物质在不同类型检测器上往往有不同的响应灵敏度;同样,不同物质在同一检测器上的响应灵敏度也往往不同,即相同量的不同物质产生不同值的峰面积或峰高。
这样,各组分峰面积或峰高的相对百分数并不等于样品中各组分的百分含量。
色谱的检测器对不同物质有不同的响应,换句话说,1mg化合物A在检测器上能产生1000mAu的响应,但同样是1mg的化合物B在该检测器上也许就只能产生847mAu的响应,所以我们不能在检测器输出1000mAu的响应时就认定样品中一定含有1mg化合物,这时就必须引入定量校正因子。
校正后的峰面积或峰高可以定量地代表物质的量,校正因子的作用就是反映某物质的量与检测器响应之间的关系。
定量校正因子分为两种:1、绝对定量校正因子f;f=M/A,(其中M代表被测物质的量,A代表检测器信号响应,可以是峰面积或峰高),其意义为单位响应所反映的物质量。
绝对定量校正因子,即单位峰面积所代表的物质量。
这是以峰面积表示的定量校正因子,也可以用峰高来表示定量校正因子。
此外,也有用它们的倒数来表示的,简称为响应值。
绝对定量校正因子的值随色谱实验条件而改变,因而很少使用。
2、相对定量校正因子f';f'=fi/fs=(Mi/Ai)/(Ms/As)=(Mi*As)/(Ms*Ai),(其中i代表被测定物质,s代表选定的基准物质)。
HPLC-加校正因子的主成分自身对照法同时测定奥美沙坦酯氢氯噻嗪片中4种有关物质含量
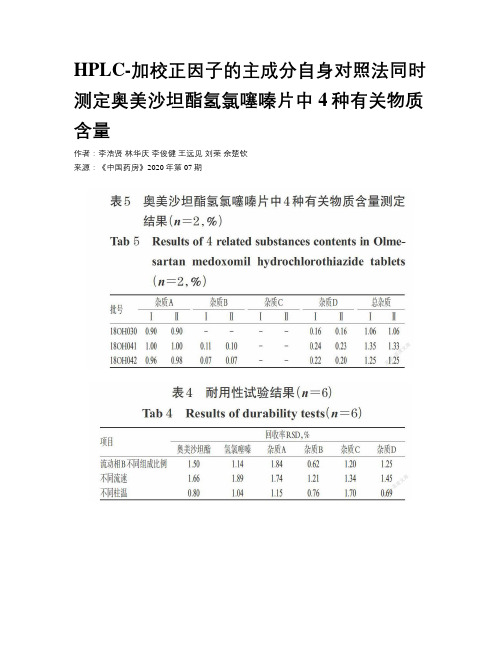
HPLC-加校正因子的主成分自身对照法同时测定奥美沙坦酯氢氯噻嗪片中4种有关物质含量作者:李浩贤林华庆李俊健王远见刘荣余楚钦来源:《中国药房》2020年第07期摘要目的:建立同时测定奥美沙坦酯氢氯噻嗪片中4种已知有关物质(奥美沙坦、奥美沙坦酯二聚体、奥美沙坦酯烯、苯并噻二嗪杂质,简称杂质A、B、C、D)的方法。
方法:采用高效液相色谱(HPLC)-加校正因子的主成分自身对照法进行测定。
色谱柱为YMC-Triart C8;流动相A为乙腈-0.015 mol/L磷酸二氢钾溶液(用磷酸调节pH至2.8)(70 ∶ 30,V/V),流动相B为乙腈-0.015 mol/L磷酸二氢钾溶液(用磷酸调节pH至2.8)(15 ∶ 85,V/V),梯度洗脱;流速为0.8 mL/min;检测波长为265 nm;柱温为25 ℃;自动进样器温度为4 ℃;进样量为10 μL。
结果:杂质A、B、C、D的校正因子分别为1.42、1.17、0.89、0.92。
奥美沙坦酯、氢氯噻嗪和杂质A、B、C、D的质量浓度线性范围分别为0.252 7~7.580 0、1.152 1~4.562 9、0.244 0~18.299 0、0.244 7~3.670 8、0.265 2~3.978 3、 0.149 9~4.497 3 μg/mL(r 均不低于0.999 7),检测限分别为0.084 2、0.050 7、0.081 3、0.081 6、0.088 4、0.050 0μg/mL,定量限分别为0.252 7、0.152 1、0.244 0、0.244 7、0.265 2、0.149 9 μg/mL,中间精密度、稳定性(24 h)、重复性试验结果均符合相关要求,平均回收率分别为104.00%~108.04%、102.00%~104.94%、100.99%~106.89%、92.00%~95.18%、102.00%~105.06%、103.90%~107.00%(n=3)。
药物分析 药物的杂质限量及检查方法

9
(一)
化 学 方 法
1 杂质与一定试剂反应产生沉淀
盐酸肼屈嗪中游离肼的检查.
2 杂质与一定试剂反应产生颜色
氯硝柳胺中2-氯-4-硝基苯胺和5-氯水杨酸的 检查
3 杂质与一定试剂反应产生气体
盐酸乙基吗啡中胺盐检查.
4 滴定法
10
(二)
比较法:取供试品一定量依法检查,测定特定的杂质 参数,与规定的限量相比,不得更大。
三、杂质的限量(Limit Test)
杂质限量计算法如下:
杂质限量(%) 杂质最大允许量 100% 供试品量
标准溶液的浓度 标准溶液的体积 100% 供试品量
CV
L(%)
100%
S
注意单位统一!
四、杂质的常用检查法
按毒性分类 毒性杂质和信号杂质
按理化性质 有机杂质、无机杂质、残留
分类
溶剂
三、杂质的限量(Limit Test)
药物中所含杂质的最大允许量。
通常用百分之几或百万分之几 (parts per million, ppm )
杂质 限量 控制
限量检查
对照法 灵敏度法 比较法
定量测定杂质含量
注意平行原则
三、杂质的限量(Limit Test)
(二)
色 谱 方 法
3.气相色谱法(GC) ——用于药物中挥发性杂质的检查,
如药物中残留溶剂、农药残留量等.
检查方法:同高效液相色谱法. 标准溶液加入法
19
(二)
色 谱 方 法
4.毛细管电泳法 —
20
(三)
光 谱 方 法
1. 可见-紫外分光光度法 2. 红外分光光度法 3. 原子吸收分光光度法
2017年药物分析在线作业标准答案解析

1.【第1-3章】药物中有关物质的检查,一般采用()。
A 滴定法B 色谱法C 紫外光谱法D 比色法E 热重分析法正确答案:B单选题2.【第1-3章】在砷盐检查中,为除去反应液中可能存在的微量硫化物干扰,在检砷装置的导气管中需填充什么?()A 碘化钾试纸B 硝酸铅棉花C 溴化汞试纸D 醋酸汞棉花E 醋酸铅棉花正确答案:E单选题3.【第1-3章】由信噪比S/N=10测得的最低浓度或量()。
A 准确度B 定量限C 检测限D 精密度E 线性范围正确答案:B单选题4.【第1-3章】具有直接三氯化铁反应的药物是()。
A 地西泮B 乙酸水杨酸C 醋氨苯砜D 对乙酰氨基酚E 链霉素正确答案:D单选题5.【第1-3章】一个药品的质量标准的主要内容包括()。
A 名称、正文、用法与用途B 名称与结构、正文、贮藏、附录C 性状、鉴别、检查、含量测定D 取样、鉴别、检查、含量测定、稳定性E 取样、检验(鉴别、检查、含量测定)、记录与报告正确答案:C单选题6.【第1-3章】澄清度检查( )。
A 红外分光光度法B 比色C 气相色谱法D 比浊度法E 原子吸收分光光度法正确答案:D单选题7.【第1-3章】阿托品()。
A 氟离子的茜素氟蓝反应B 重氮化-偶合反应C Vitali反应D 硝酸银反应E 硫色素反应正确答案:C单选题8.【第1-3章】药物分析中的原始纪录()。
A 是实验研究的原始档案,一般检验报告发出后可以销毁B 通常要有检验人和委托人签名C 一般应在检验报告发出后一个月内销毁D 是实验研究的第一手资料,应妥善保管E 是实验研究的技术档案,内容应完整,若有遗漏可以插页,但字迹要清楚正确答案:D单选题9.【第1-3章】用回收率表示()。
A 准确度B 定量限C 检测限D 精密度E 线性范围正确答案:A单选题10.【第1-3章】药物的杂质限量是指()。
A 杂质的定量限B 杂质的最小允许量C 杂质的最大允许量D 杂质的检测限E 杂质的含量正确答案:C单选题11.【第1-3章】铁盐检查,实验条件下被检杂质的适宜浓度为():A 0.0002mgB 0.002mgC 0.01~0.05mgD 0.1~0.5mgE 0.01~0.02mg正确答案:C单选题12.【第1-3章】在碱性水溶液中被铁氰化钾氧化后溶于正丁醇显蓝色荧光的药物是()。
HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量

HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量作者:周燕丽余永华马佳丽顾超群谢明华来源:《中国药房》2019年第05期中图分类号 R927.2;O657.72 文献标志码 A 文章编号 1001-0408(2019)05-0627-05DOI 10.6039/j.issn.1001-0408.2019.05.10摘要目的:建立测定盐酸特拉唑嗪片中有关物质含量的方法。
方法:采用高效液相色谱加校正因子的主成分自身对照法。
色谱柱为Agilent Zorbax Eclipse XDB C18,流动相为乙腈-高氯酸溶液(20 ∶ 80,V/V),流速为1.0 mL/min,检测波长为246 nm,进样量为20 μL,柱温为50 ℃;绘制盐酸特拉唑嗪和杂质A、B、C的线性方程,以斜率计算各杂质相对于盐酸特拉唑嗪的校正因子,用相对保留时间确定各杂质位置,测定3批盐酸特拉唑嗪片中杂质A、B、C的含量,并与杂质对照品法测得的结果进行比较。
结果:盐酸特拉唑嗪杂质A、B、C的相对保留时间分别为0.39、0.74、2.77,检测质量浓度线性范围均为0.25~3.0 μg/mL,校正因子分别为0.75、1.09、0.84,检测限分别为0.35、0.51、0.43 ng,定量限分别为0.70、1.02、0.86 ng。
3批盐酸特拉唑嗪片中杂质A、B、C的含量分别为0.11%~0.13%、0.03%、0.09%~0.12%,杂质B未检出;与杂质对照品法测定结果一致。
结论:该方法简便快速,可准确测定盐酸特拉唑嗪片中有关物质的含量。
关键词盐酸特拉唑嗪片;有關物质;高效液相色谱法;校正因子Determination of Related Substance in Terazosin Hydrochloride Tablets by HPLC and Principal Component Self-control with Correction FactorZHOU Yanli1,YU Yonghua2,MA Jiali3,GU Chaoqun3,XIE Minghua1(1.Dept. of Pharmacy,Hangzhou Yuhang District First People’s Hosp ital, Hangzhou 311100, China;2.Hangzhou SINOVO Pharmaceutical Co., Ltd., Hangzhou 310015, China;3.College of Pharmacy, Zhejiang College of TCM, Hangzhou 310403, China)ABSTRACT OBJECTIVE: To establish the method for the content determination of related substance in Terazosin hydrochloride tablets. METHODS: HPLC and principal component self-control with correction factor were adopted. The determination was performed on Agilent Zorbax Eclipse XDB C18 column with mobile phase consisted of acetonitrile-perchloric acid solution (20 ∶80, V/V) at the flow rate of 1.0 mL/min. The detection wavelength was set at 246 nm, and sample size was 20 μL. The column temperature was 50 ℃. The linear equations of terazosin hydrochloride, impurity A, B, C were drawn. The correction factors of each impurity related to terazosin hydrochloride were calculated by slope, and relative retention time was used to determinethe position of impurities. The contents of impurity A, B and C in 3 batches of Terazosin hydrochloride tablets were determined and compared with the results of impurity control method. RESULTS: The relative retention time of impurity A, B, C was 0.39, 0.74, 2.77,respectively; the linear range of them were 0.25-3.0 μg/mL, respectively. The correction factors were 0.75, 1.09, 0.84, respectively. The detection limits were 0.35, 0.51, 0.43 ng, and the limits of quantification were 0.70, 1.02, 0.86 ng, respectively. The contents of impurity A, B and C in 3 batches of Terazosin hydrochloride tablets were 0.11%-0.13%, 0.03% and 0.09%-0.12%; impurity B did not detected. The results are consistent with the determination of impurity control method. CONCLUSIONS: The method is simple, rapid and accurate for the content determination of related substances A, B, C in Terazosin hydrochloride tablets.KEYWORDS Terazosin hydrochloride tablets; Related substances; HPLC; Correction factor特拉唑嗪是一种α-肾上腺受体拮抗药,临床上可用于治疗轻度或中度高血压,还适用于良性前列腺增生(BPH)和男性下尿路症状(LUTS)[1]。
加校正因子的主成分自身对照法测定盐酸苯海拉明片中有关物质的含量_郭福团

盐酸苯海拉明为组胺 H1 受体拮抗剂,主要用于治疗皮 肤黏膜的过敏 性 疾 病 和 晕 动 症。 中 国 药 典〔1〕和 英 国 药 典〔2〕 均有收载,为保证药品质量和临床用药的安全有效,盐酸苯海 拉明片在 2010 版《中国药典》〔1〕采用不加校正因子的主成分 自身对照法测定其有关物质,但是二苯酮在 258nm 波长紫外 吸收强度显著大于盐酸苯海拉明〔3〕,约为 30 倍,从而造成有 关物质检查项最大杂质( 二苯酮) 和总杂质均超过限度要求, 产生误判。为更加准确地控制酸苯海拉明片中有关物质的含 量,根据相关文 献〔4〕,本 文 建 立 了 加 校 正 因 子 的 主 成 分 自 身 对照法测定盐酸苯海拉明片中二苯酮杂质和总杂质的含量。 1 仪器和试药 1. 1 仪器 Agilent1290 高 效 液 相 色 谱 仪 和 Agilent 氰 基 柱 ( 250mm × 4. 6mm,5μm) 组成仪器系统 1,Agilent1100 高效液
便、准确可靠,适用于盐酸苯海拉明片中有关物质的控制。
关键词: 盐酸苯海拉明; 校正因子;自身对照; 有关物质; 二苯酮
中图分类号: R927. 2 文献标识码: B 文章编号: 1006-3765( 2013) -10-0047-03
Correction Factor for Determination of Content of Related Substances in Diphenhydramine Hydrochloride Tablet by HPLC
作者简介: 郭福团,男。职称: 主管药师。联系电话: 13805082979,Email: guofutuan@ 163. com
相色谱仪和 Waters 氰基柱( 250mm × 4. 6mm,5μm) 组成仪器 系统 2,Milli-QA 超纯水器( Millipore) ,ALP-204 电子天平( 梅 特勒) 。 1. 2 药品和试剂 二苯酮( 国药集团化学试剂有限公司,批 号 20091211,纯度: 99. 5% ) ,盐酸苯海拉明( 中国药品生物制 品检定研究院,批号 100066-200807,纯度: 99. 9% ) ,盐酸苯海 拉明 片 ( 临 汾 宝 珠 制 药 有 限 公 司,批 号: 100102、100103、 100301) ,乙腈为色谱纯; 水为超纯水,其他试剂均为分析纯。 2 方法和结果 2. 1 色谱条件 色谱柱: Agilent 氰基柱 ( 250mm × 4. 6mm, 5μm) 、Waters 氰基柱( 250mm × 4. 6mm,5μm) ; 流动相: 乙腈水-三乙胺( 50∶ 50∶ 0. 5) ( 用冰醋酸调节 pH 值至 6. 5) ; 柱温: 25℃ ; 检 测 波 长: 258nm; 流 速: 1. 0mL · min - 1 ; 进 样 量: 20μL ( 自动进样) 。 2. 2 对照品储备液、供试品溶液与空白辅料样品溶液的制备 2. 2. 1 对照品贮备液的制备: 精密称取盐酸苯海拉明对照品 适量,加流动相制成每 1mL 含盐酸苯海拉明 1. 081mg 的溶
答案中国医科大学2020年12月《药物分析》作业考核试题

中国医科大学 2020 年 12 月考试《药物分析》作业考核试题试卷总分:100 得分:100一、单选题(共20道试题,共20分)1.药物纯度符合规定系指:()A项.含量符合药典的规定B 项.纯度符合优级纯试剂的规定C 项.绝对不存在杂质D 项.对患者无不良反应E 项.杂质含量不超过限度规定答案:E2.在检查酸不溶性或在酸中析出沉淀的药物中的重金属时,所用的显色剂是:() A项.硫代乙酰胺试液B项.硫化氢试液C项.硫化钠试液D项.醋酸汞试液E项.以上都不是答案:C3.在下列药物中,对氨基酚是其中存在的特殊杂质的是?() A项.对氨基水杨酸钠B项.盐酸普鲁卡因C项.盐酸利多卡因D项.对乙酰氨基酚E项.阿司匹林答案:D4.用铈量法测定硝苯地平的含量时,常用的指示剂是:() A项.甲基橙B 项.曙红C 项.荧光黄D 项.淀粉指示剂E 项.邻二氮菲指示液答案:E5.紫外分光光度法测定盐酸氯丙嗪注射液的含量,下列说法中不正确是:() A项.可采用双波长法和吸收系数法测定药物含量B 项.可以在最大吸收波长254nm 附近处直接测定盐酸氯丙嗪的含量C项.可以在299nm附近处直接测定盐酸氯丙嗪的含量D项.可以在254nm和277nm波长处采用双波长法测定E项.采用百分吸收系数法测定含量时不需要对照品答案:B6.与硝酸作用产生红色的是:()A项.异烟肼B 项.尼可刹米C项.氯丙嗪D项.地西泮E 项.奥沙西泮答案:C7.异烟肼的特殊杂质为:()A项.戊烯二醛反应B 项.银镜反应C 项.游离肼D 项.亚硝酸钠E 项.香草醛答案:C8.具有共轭多烯侧链的药物为:()A项.司可巴比妥B项.阿司匹林C项.苯佐卡因D项.维生素A E项.维生素E答案:D9.维生素A具有的结构为:() A项.氨基嘧啶环和噻唑环B 项.共轭多烯侧链C 项.二烯醇和内酯环D项.β-内酰氨环和氢化噻唑环E项.β-内酰氨环和氢化噻嗪环答案:B10.可与碘化汞钾生成淡黄色沉淀的药物为:()A 项.维生素EB 项.维生素AC项.维生素C D项.维生素B1 E项.维生素D答案:D11.用1,2 - 二氯乙烷溶解后,与三氯化锑试液反应,生成橙红色,逐渐变为粉红色的药物为:()A项.维生素E B项.维生素A C项.维生素C D项.维生素B1 E项.维生素D答案:E12.具有C17-α-醇酮基的药物是:() A项.维生素B1B项.雌二醇1 C项.地塞米松D项.黄体酮答案:C13.青霉素在碱性或青霉素酶的作用下,易发生水解,生成:() A项.青霉酸B项.青霉胺C项.青霉醛D 项.青霉烯酸E 项.青霉噻唑酸答案:E14.片剂中常使用的赋形剂不包括:()A项.糖类B 项.硬脂酸镁C 项.滑石粉D 项.淀粉E 项.维生素C答案:E15.片重在0.3g或0.3g以上的片剂的质量差异限度为:() A项.7.5%B项.±5.0%C项.5.0%D项.7.0%答案:B16.6.2750修约后要求保留3位有效数字:() A项.6.27B项.6.20C项.6.28D项.6.24E项.6.25答案:C17.采用法定的化学方法确定某已知药物的真实性属于:()A项.含量测定B项.效价测定C项.鉴别反应D项.杂质检查E项.t检验答案:C18.用非水碱量法测定含量时需采用电位滴定法指示终点的生物碱盐类药物是:() A项.盐酸盐B 项.氢溴酸盐C项.硫酸盐D项.硝酸盐E 项.马来酸盐答案:D19.可用于雌二醇含量测定的方法是:()A项.异烟肼比色法B项.硫色素荧光法C项.四氮唑比色法D 项.凯氏定氮法E 项.Kober 反应比色法答案:E20.用三点校正法(三波长校正法)测定维生素A醋酸酯含量时,下列叙述中正确的是:() A项.原理是维生素A可与三氯化锑反应显色B 项.杂质吸收在测定波长范围内为线性,且随波长增加吸收度增强C 项.当最大吸收波长在326~329nm 之间时,不一定不需皂化处理D 项.当校正吸收度与未校正吸收度之差在未校正吸收度的±3.0%以内时,用校正吸收度计算含量E 项.换算因数为 0.1939答案:B 判断题21.药物分析是收载药品质量标准的典籍正确错误答案:错误22.无机金属盐焰色反应中钠离子显紫色;钾离子显鲜黄色;钙离子显砖红色。
药物分析在线

1.下列药品标准中属于法定标准的是()。
D 国家药典2.银量法测定巴比妥类药物,终点指示的原理是()。
B 过量1滴的滴定剂使巴比妥类形成难溶性的二银盐沉淀3.细菌内毒素检查采用的方法()。
B 鲎试剂法4.减少分析测定中偶然误差的方法为()。
B 增加平行试验次数5.原料药的含量测定宜选()。
C 容量分析法6.非水碱量法测定生物碱的硝酸盐()。
E 电位法指示终点7.中国药典规定紫外测定中,溶液的吸光度应控制在()。
C 0.3~0.78.具有怎样结构的甾体激素类药物可用四氮唑比色法测定()。
B C17-a- 醇酮基9.药品稳定性考察中加速试验的条件和所需样品批次是()。
C 40℃、RH75%,6个月,3批样10.下列哪一项不属于色谱系统适用性试验内容?() A 准确度11.拖尾因子表示()。
E 峰对称性12.荧光分析法适合于()。
D 低浓度溶液的测定13.一个药品的质量标准的主要内容包括()。
C 性状、鉴别、检查、含量测定14.澄清度检查()。
D 比浊度法15.维生素C中铜的检查()。
E 原子吸收分光光度法16.亚硝酸钠滴定法中,加KBr的作用是()。
E 生成NOBr以加速反应17.由信噪比S/N=10测得的最低浓度或量()。
B 定量限18.甲苯咪唑中无效晶型的检查()。
A 红外分光光度法19.在碱性水溶液中被铁氰化钾氧化后溶于正丁醇显蓝色荧光的药物是()。
B 维生素B120.对于毒性或贵重药材,应尽量采用()。
C 显微鉴别法21.盐酸去氧肾上腺素的溴量法原理()。
A 取代反应22.色谱法适合于多组分的分离分析,中药鉴别中最常用的方法是()。
E 薄层色谱法23.实验条件下被检杂质的适宜浓度,重金属为()。
E 0.01~0.02mg24.拆分酮康唑外消旋体的方法()。
B 手性流动相添加法25.用高氯酸滴定液直接滴定硫酸奎宁,1摩尔硫酸奎宁需消耗几摩尔高氯酸()。
执业西药师药学专业知识【药物分析部分】(模拟试卷四)

执业西药师药学专业知识(一)【药物分析部分】(模拟试卷四)一、最佳选择题1、《中国药典》的现行版本为A.2000年版B.2004年版C.2005年版D.2010年版E.2013年版【正确答案】:D【答案解析】:《中国药典》的现行版本为2010年版,常识性知识。
2、《中国药典》凡例中规定密闭系指A.将容器密闭,以防止尘土及异物进入B.将容器熔封,以防止空气及水分的侵入并防止污染C.将容器密封,以防止风化、吸潮、挥发或异物进入D.将容器用适宜的材料严封,以防止空气及水分的侵入并防止污染E.用不透光的容器包装,例如棕色容器或黑纸包裹的无色透明、半透明容器【正确答案】:A【答案解析】:本题考察密闭的概念,密闭系指将容器密闭,以防止尘土及异物进入。
C是密封;BD是熔封和严封;E是避光;所以此题选择A。
3、取样量为101mg时应选用的天平感量为A.0.001mgC.0.1mgD.1mgE.0.0001mg【正确答案】:C【答案解析】:药物分析实验室使用的分析天平的感量有0.1mg、0.01mg和0.001mg三种。
为了保证称量的相对误差小于千分之一,当取样量大于100mg 时,选用感量为0.1mg的分析天平;当取样量为100~10mg时,选用感量为0.01mg的分析天平;取样量小于10mg时,选用感量为0.001mg的分析天平。
4、线性的相关系数(r)的值A.越小越好B.越大越好C.在0和1之间较好D.在0和-1之间较好E.越接近1越好【正确答案】:E【答案解析】:相关系数(r)在0~±1之间。
越接近1,线性关系越好,r=±1时,各点在一条直线上。
当r>0,称正相关;r<0,称负相关;r=0,无线性关系。
5、熔点大致为220℃左右的物质测定熔点使用的传温液正确的是A.水B.乙醇D.黏度60mm2/s的硅油E.黏度110mm2/s的硅油【正确答案】:E【答案解析】:除另有规定外,熔点在80℃以下者,用水;熔点介于80~200℃之间者,用黏度不小于50mm2/s的硅油;熔点高于200℃者,用黏度不小于100mm2/s的硅油。
药分问答分离题

问答题1、杂质的来源途径有哪些?杂质包括哪些种类?一,生产过程中引入的杂质。
二,储藏过程中引入的杂质。
按来源分:一般杂质,特殊杂质。
工艺杂质,降解产物,外来杂质。
按毒性分:毒性杂质,信号杂质。
按化学性质分:无机杂质,有机杂质,残留溶剂。
2、药物中重金属检测方法有哪几种?各适用于什么药物的检测?一、硫代乙酰胺法:适用于溶于水,稀酸,乙醇的药物二、炽灼后的硫代乙酰胺法:适用于含有芳环,杂环以及难溶于水,稀酸,乙醇的药物三、硫化钠法:适用于溶于碱性水溶液而难溶于稀酸或在稀酸中即生成沉淀的药物。
3、砷盐检查的方法有哪些?古蔡氏法。
二乙基二硫代氨基甲酸银法(DDC -A g )。
白田道夫法。
次磷酸法。
4、简述薄层色谱法检查杂质时的具体方法及适用情况。
1.杂质对照品法:适用于已知杂质并能制备杂质对照品的情况。
2.供试品溶液的自身稀释对照法:无杂志对照品且杂质斑点与主成分斑点相近3.两法并用。
当药物中存在多个杂质点,有的有杂质对照品,有的没有杂质对照品4.对照药物法:无杂质对照品,杂质斑点和主成分斑点有差异5、简述高效液相色谱法检查杂质时的具体方法及适用情况。
1.外标法(杂质对照品法)适用于有杂质对照品,而且进样量能够精确控制(以定量环或自动进样器进样。
)情况。
2.加校正因子的主成分自身对照法,该法仅适用于没有杂质对照品已知杂质的控制,杂质的校正因子和相对保留时间载入质量标准中3.不加校正因子的主成分自身对照法,适用于没有杂质对照品的情况且杂质与主成分相应因子相近4.面积归一化法,通常只适用于供试品中结构相似,相对含量较高且限度范围较宽的杂质含量的粗略考察6、简述凯氏定氮法的原理与应用。
凯氏定氮法:本法是将含氮有机物与硫酸共热,药物分子中有机结构被氧化分解成二氧化碳和水,有机结合的氮转变为无机氮,过滤并与过量的硫酸结合为硫酸氢氨,经氢氧化钠分解释放出氨,后者借水蒸气被蒸出,用硼酸溶液或定量的酸滴定液吸收后,再用酸或碱滴定液滴定。
加校正因子的主成分自身对照法测定复方奥美拉唑咀嚼片相关物质含量的分析

加校正因子的主成分自身对照法测定复方奥美拉唑咀嚼片相关物质含量的分析张茁【摘要】目的:通过加校正因子的主成分加校正因子的主成分自身对照法测定复方奥美拉唑咀嚼片相关物质含量。
方法分别配制浓度为0.2 mg/mL 的杂质对照液、浓度为1 g/L 的奥美加唑对照品储备液、浓度为0.2 mg/L 的供试品溶液、浓度为2 mg/L 的对照溶液、浓度为0.2 mg/L 的供试品溶液、浓度为0.2 mg/L 的系统适用性溶液、浓度为2 mg/L 的对照溶液和浓度为0.2 mg/L 的阴性对照液,然后根据需要取适量溶液注入仪器中进行检测和计算,测定 A、B、C、D、E 五种杂质的含量。
结果校正因子分别为1.45、0.66、1.21、1.39、0.8测得奥美拉唑的杂质含量分别为0.9、3.4、0.8、0.4,其中杂质 D 的含量均为0。
结论通过加校正因子的主成分加校正因子的主成分自身对照法测定复方奥美拉唑咀嚼片相关物质含量简洁快捷而且准确率高。
【期刊名称】《中国医药指南》【年(卷),期】2016(014)006【总页数】2页(P38-39)【关键词】校正因子;自身对照;奥美拉唑;相关物质【作者】张茁【作者单位】黑龙江省佳木斯市中心医院药剂科,黑龙江佳木斯 154002【正文语种】中文【中图分类】R917奥美拉唑是一种在酸性环境容易分解的弱碱性物质,其作用是有效地抑制H+-K+-ATP酶的活性,进而降低胃酸的分泌,目前在市面上流通的大多数奥美拉唑达到药效顶峰的时间很长,复方奥美拉唑咀嚼片的特点是降减和胃溶的量减少,药效快[1-5]。
为了保障药物的安全性,需对药物中的杂质进行检测,结合各国药典的经验,本文选择用加校正因子的主成分加校正因子的主成分自身对照法测定复方奥美拉唑咀嚼片中杂质的含量,以提高检验的精度和实现对杂质的有效控制,本次检测中涉及的杂质有五种。
1.1 一般资料:本次检测工作择用加校正因子的主成分加校正因子的主成分自身对照法,对复方奥美拉唑咀嚼片中的五中杂质进行检测,需要用到的仪器分别系统1(Agilent XDB C8(4.6 mm×150 mm,5 μm)色谱柱和HITACHI Chromaster高效液相色谱仪),系统2 (Kromasil C8(4.6 mm×150 mm,5 μm)色谱柱和HITACHI L-2000型高效液相色谱仪),需要用到的检测药品有乙腈、磷酸氢二钠、磷酸、蒸馏水、复方奥美拉唑咀嚼片数粒。
用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质 C 的含量

用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质 C 的含量徐亮亮;朱小林;苏丽【摘要】目的:建立加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质 C 的含量。
方法采用 C18柱(4.6 mm ×250 mm,5μm),以乙腈:0.325%磺酸钠(用磷酸调节 pH 值为2.8)(10:90)为流动相,梯度洗脱,流速为1.5 mL·min -1,柱温为45℃,检测波长为215 nm,进样量为20μL。
测定杂质 C 相对于盐酸去氧肾上腺素的相对出峰时间及校正因子,并计算其含量。
结果杂质 C 在0.0651~1.6269μg·mL -1,盐酸去氧肾上腺素在0.0647~1.6184μg·mL -1浓度范围内,峰面积与浓度呈良好的线性关系;杂质 C 相对于盐酸去氧肾上腺素的相对保留时间为1.3,校正因子为0.50。
结论本方法专属性强,结果准确可靠,无需提供杂质对照品,能够准确测定盐酸去氧肾上腺素中杂质 C 的含量。
%Objective To establish a method for the determination of impurity C in phenylephrine hydrochloride by main constituent own control method with correction factor. Methods The assay was carried out on a C18 column(4. 6 mm × 250 mm,5 μm)with the mobile phase of acetonitrile - 0. 325% sodium sulfonate solution(with phosphoric acid to adjust pH value of 2. 8)(10:90)at a flow rate of 1. 5 mL·min - 1. The column temperature,the detection wave length and the in-jection volume were set at 45 ℃,215 nm,and 20 μL. The relative retention time and the correction factor between impurity C and phenylephrine hydrochloride were determined. Results The linear ranges of impurity C and phenylephrine hydro-chloride were 0. 065 1 ~ 1. 626 9 μg·mL - 1 ,0. 064 7 ~ 1. 618 4 μg·mL -1 ,respectively. The relative retention time be-tween impurity C and phenylephrine hydrochloride was 1. 3,the correction factor between impurity C and phenylephrine hydrochloride was 0. 50. Conclusion This method was simple,accurate and reliable to determine impurity C in phenyleph-rine hydrochloride. without standard substances.【期刊名称】《药学研究》【年(卷),期】2015(000)012【总页数】4页(P706-708,718)【关键词】盐酸去氧肾上腺素;杂质 C;校正因子【作者】徐亮亮;朱小林;苏丽【作者单位】江苏先科药业有限公司,江苏南通226200;江苏先科药业有限公司,江苏南通 226200;江苏先科药业有限公司,江苏南通 226200【正文语种】中文【中图分类】R927.11盐酸去氧肾上腺素为拟肾上腺素药物,用于防治脊椎麻醉、全身麻醉、外科手术延长局疗麻醉时间,鼻黏膜充血的消炎、眼科的扩瞳以及急性低血压的升压、感冒等,为急救常备药品[1~3]。
加校正因子的主成分自身对照法同时测定非那雄胺片中2个杂质

加校正因子的主成分自身对照法同时测定非那雄胺片中2个杂质刘光敏【期刊名称】《中国药品标准》【年(卷),期】2018(019)005【摘要】目的:建立加校正因子的主成分自身对照法测定非那雄胺片中有关物质的含量.方法:CAPCELLPAK C18色谱柱(4.6 mm×250 mm,5μm),流动相乙腈-水(45:55),流速1.0 mL·min-1,检测波长210 nm,进样量20μL,柱温30℃.测定非那雄胺与杂质Ⅰ、Ⅱ的标准曲线方程,以斜率计算杂质相对于非那雄胺的校正因子,用相对保留时间确定各杂质的位置.结果:非那雄胺杂质Ⅰ、Ⅱ的相对保留时间分别为0.85与1.30,相对校正因子分别为2.40与0.69.结论:本方法可用于非那雄胺片中有关物质的定性及定量分析,采用加校正因子的主成分自身对照法可以更准确的反映其有关物质的含量.【总页数】6页(P353-358)【作者】刘光敏【作者单位】淄博职业学院,淄博255314【正文语种】中文【中图分类】R921.2【相关文献】1.加校正因子的主成分自身对照法测定盐酸苯海拉明片中有关物质的含量 [J], 郭福团2.用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质C的含量 [J], 徐亮亮;朱小林;苏丽;3.用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质 C 的含量 [J], 徐亮亮;朱小林;苏丽4.HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量[J], 周燕丽;余永华;马佳丽;顾超群;谢明华5.HPLC-加校正因子的主成分自身对照法同时测定奥美沙坦酯氢氯噻嗪片中4种有关物质含量 [J], 李浩贤; 林华庆; 李俊健; 王远见; 刘荣; 余楚钦因版权原因,仅展示原文概要,查看原文内容请购买。
用加校正因子的自身对照法检测兰索拉唑的有关物质的含量

用加校正因子的自身对照法检测兰索拉唑的有关物质的含量谭宏宇;高丽【期刊名称】《黑龙江医药》【年(卷),期】2012(025)006【摘要】目的:建立加校正因子的主成分自身对照法测定兰索拉唑的有关物质的含量.方法:采用C18色谱柱(250 mm×4.6 mm,5μm),以水-A液*(A液*:乙腈-水-三乙胺(160∶40∶1)混合液,用磷酸调节pH值至7.0)(60∶40)为流动相,柱温30℃,检测波长285nm.测定杂质A、B、E相对于兰索拉唑的相对保留时间及校正因子,并计算其含量.结果:兰索拉唑、杂质A、B、E质量浓度分别在0.0904μg/ml ~2.892μg/ml,0.0992μg/ml ~1.650μg/ml,0.0966μg/ml~3.255μg/ml,0.1426μg/ml~2.468μg/ml范围内线性关系良好,r均达到0.999.杂质A、B、E相对于主成分兰索拉唑的相对保留时间分别为0.42,1.17,0.23.杂质A、B的校正因子均在0.9~1.1范围,杂质E校正因子为0.39.结论:本方法操作简单、准确可靠,重现性、分离效果好,灵敏度高,无需提供杂质对照品就能准确测定兰索拉唑杂质的有关物质.【总页数】3页(P821-823)【作者】谭宏宇;高丽【作者单位】黑龙江省食品药品监督管理局;北京科信必成医药科技发展有限公司哈尔滨分公司【正文语种】中文【中图分类】R927.1【相关文献】1.加校正因子的主成分自身对照法测定奥硝唑片和胶囊中有关物质含量 [J], 耿庆光;王发2.加校正因子的主成分自身对照法测定盐酸苯海拉明片中有关物质的含量 [J], 郭福团3.加校正因子的主成分自身对照法测定奥美拉唑肠溶胶囊中有关物质的含量 [J], 刘虹;李源;陈燕;赵海鹏4.HPLC加校正因子的主成分自身对照法测定盐酸特拉唑嗪片中有关物质的含量[J], 周燕丽;余永华;马佳丽;顾超群;谢明华5.HPLC-加校正因子的主成分自身对照法同时测定奥美沙坦酯氢氯噻嗪片中4种有关物质含量 [J], 李浩贤; 林华庆; 李俊健; 王远见; 刘荣; 余楚钦因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药学研究·J o u r n a l o f P h a r m a c e u t i c a l R e s e a r c h 2 0 1 5V o l . 3 4 , N o . 1 2
用加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中 杂质 C的含量
徐亮亮, 朱小林, 苏 丽
j e c t i o nv o l u n d 2 0μ L T h e r e l a t i v e r e t e n t i o nt i m e a n dt h e c o r r e c t i o nf a c t o r b e t w e e ni m p u r i t y Ca n dp h e n y l e p h r i n eh y d r o c h l o r i d ew e r ed e t e r m i n e d R e s u l t s T h el i n e a r r a n g e so f i m p u r i t yCa n dp h e n y l e p h r i n eh y d r o
( 江苏先科药业有限公司, 江苏 南通 2 2 6 2 0 0 ) 摘要: 目的 建立加校正因子的主成分自身对照法测定盐酸去氧肾上腺素中杂质 C的含量。 方法 采用 C 1 8 柱( 4 . 6m m× 2 5 0m m , 5μ m ) , 以乙腈∶ 0 . 3 2 5 %磺酸钠( 用磷酸调节 p H值为 2 . 8 ) ( 1 0 ∶ 9 0 ) 为流动相, 梯度洗脱, 流速
A b s t r a c t : O b j e c t i v e T oe s t a b l i s ham e t h o df o r t h ed e t e r m i n a t i o no f i m p u r i t yCi np h e n y l e p h r i n eh y d r o c h l o r i d eb y Me t h o d s T h e a s s a y w a s c a r r i e do u t o na C o l u m n( 4 6m m m a i nc o n s t i t u e n t o w nc o n t r o l m e t h o dw i t hc o r r e c t i o nf a c t o r 1 8c × 2 5 0m m , 5μ m )w i t ht h e m o b i l e p h a s e o f a c e t o n i t r i l e - 0 3 2 5 %s o d i u ms u l f o n a t e s o l u t i o n ( w i t hp h o s p h o r i c a c i dt o a d j u s t
D e t e r mi n a t i o no f t h ei mp u r i t yCi np h e n y l e p h r i n eh y d r o c h l o r i d eb yma i nc o n s t i t u e n t o w nc o n t r o l me t h o dw i t hc o r r e c t i o nf a c t o r X UL i a n g l i a n g , Z H UX i a o l i n , S UL i ( J i a n g s uA s c e n d i aP h a r m a c e u t i c a l C o . , L t d . , N a n t o n g2 2 6 2 0 0 , C h i n a )
- 1 - 1 g ·m L , 0 0 6 47~ 1 6 1 84μ g ·m L , r e s p e c t i v e l y T h er e l a t i v er e t e n t i o nt i m eb e c h l o r i d ew e r e 0 0 6 51~ 1 6 2 69μ
对保留时间为 1 . 3 , 校正因子为 0 . 5 0 。结论 本方法专属性强, 结果准确可靠, 无需提供杂质对照品, 能够准确测定 盐酸去氧肾上腺素中杂质 C的含量。 关键词: 盐酸去氧肾上腺素; 杂质 C ; 校正因子 中图分类号: R 9 2 7 . 1 1 文献标识码: A 文章编号: 2 0 9 5- 5 3 7 5 ( 2 0 1 5 ) 1 2- 0 7 0 6- 0 0 4
- 1 p Hv a l u eo f 2 8 ) ( 1 0 ∶ 9 0 )a t a f l o wr a t e o f 1 5m L ·m i n T h e c o l u m nt e m p e r a t u r e , t h e d e t e c t i o nw a v e l e n g t ha n dt h e i n
t w e e ni m p u r i t yCa n dp h e n y l e p h r i n eh y d r o c h l o r i d ew a s 1 3 , t h ec o r r e c t i o nf a c t o r b e t w e e ni m p u r i t yCa n dp h e n y l e p h r i n e h y d r o c h l o r i d ew a s 0 5 0 C o n c l u s i o n T h i s m e t h o dw a s s i m p l e , a c c u r a t e a n dr e l i a b l e t o d e t e r m i n e i m p u r i t y Ci np h e n y l e p h r i n eh y d r o c h l o r i d e w i t h o u t s t a n d a r ds u b s t a n c e s K e yw o r d s : P h e n y l e p h r i n eh y d r o c h l o r i d e ; I m p u r i t yC ; C o r r e c t i o nf a c t o r
- 1 为1 . 5m L ·m i n , 柱温为 4 5℃, 检测波长为 2 1 5n m , 进样量为 2 0μ L 。测定杂质 C相对于盐酸去氧肾上腺素的相 - 1 . 0 6 51~ 1 . 6 2 69μ g ·m L , 盐酸去氧肾上腺素在 对出峰时间及校正因子, 并计算其含量。 结果 杂质 C在 0 - 1 0 . 0 6 47~ 1 . 6 1 84μ g ·m L 浓度范围内, 峰面积与浓度呈良好的线性关系; 杂质 C相对于盐酸去氧肾上腺素的相
