专题03 燃料电池-2019高考复习专题——电化学(原卷版)
高考化学全国卷Ⅰ专题———燃料电池
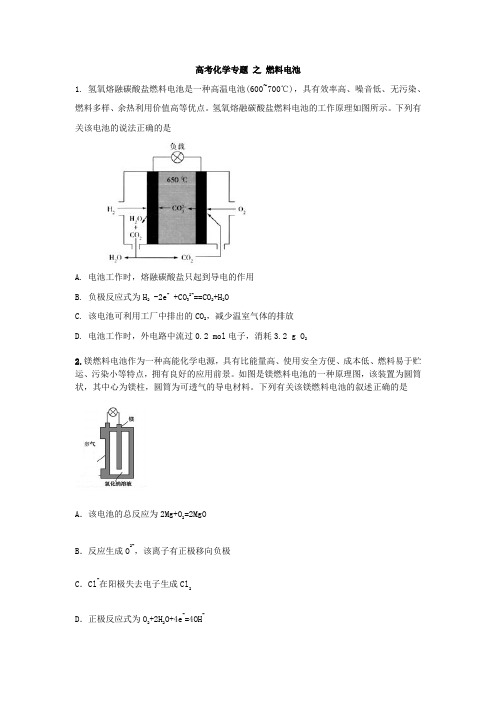
高考化学专题之燃料电池1. 氢氧熔融碳酸盐燃料电池是一种高温电池(600~700℃),具有效率高、噪音低、无污染、燃料多样、余热利用价值高等优点。
氢氧熔融碳酸盐燃料电池的工作原理如图所示。
下列有关该电池的说法正确的是A. 电池工作时,熔融碳酸盐只起到导电的作用B. 负极反应式为H2 -2e- +CO32-==CO2+H2OC. 该电池可利用工厂中排出的CO2,减少温室气体的排放D. 电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O22.镁燃料电池作为一种高能化学电源,具有比能量高、使用安全方便、成本低、燃料易于贮运、污染小等特点,拥有良好的应用前景。
如图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料。
下列有关该镁燃料电池的叙述正确的是A.该电池的总反应为2Mg+O2=2MgOB.反应生成O2-,该离子有正极移向负极C.Cl-在阳极失去电子生成Cl2D.正极反应式为O2+2H2O+4e-=4OH-3.一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是A.通入CH3OH的电极为负极B.随着放电的进行,负极附近pH上升C.每消耗1molCH3OH可以向外电路提供6mol e-D.通入O2的一极电极反应为 4H2O+2O2-8e-=8OH-4.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
下列有关微生物电池的说法错误的是A.正极反应中有CO2生成B.微生物促进了反应中电子的转移C.质子通过交换膜从负极区移向正极区D.电池总反应为C6H12O6+6O26CO2+6H2O5.如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是()A.该电化腐蚀为析氢腐蚀.B.C.D.7.太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用。
高考化学燃料电池练习及答案.doc

高考化学 -- 燃料电池 -- 练习及答案高考化学燃料电池1.“直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能,下图是用固体氧化物作“直接煤燃料电池”的电解质。
有关说法正确的是A.电极 b 为电池的负极B.电池反应为: C + CO2 = 2COC.电子由电极 a 沿导线流向 bD.煤燃料电池比煤直接燃烧发电能量利用率低2 .如图所示是一种以液态肼 (N2 H4 )为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。
该固体氧化物电解质的工作温度高达 700-900 ℃时, O2-可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
下列说法正确的是A.电池内的 O2-由电极乙移向电极甲B.电池总反应为 N2H4 +2O2= 2NO+2H 2 OC.当甲电极上有 lmol N 2 H4消耗时,乙电极上有22.4LO 2参与反应D.电池外电路的电子由电极乙移向电极甲3 .硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如下。
该电池工作时的反应为4VB 2+11O 2=4B 2O3+2V2O5。
下列说法正确的是A.电极 a 为电池负极B. 反应过程中溶液的pH 升高C.电池连续反应过程中,选择性透过膜采用阳离子选择性膜D.VB2极的电极反应式为: 2VB 2 +22OH - -22e - =V2 O5+ 2B 2O3 + 11H 2O4.以 NaBH4和 H2 O2作原料的燃料电池,可用作空军通信卫星。
电池负极材料采用 Pt/C ,正极材料采用 MnO2,其工作原理如下图所示。
下列说法错误的是..A.电池放电时 Na+从 a 极区移向 b 极区B.电极 b 采用 Pt/C ,该极溶液的 pH 增大C. 该电池 a 极的反应为 BH4-+8OH --8e-===BO 2-+6H 2 OD.电池总反应: BH4- + 4H 2 O2 === BO 2- + 6H 2O 5.科学家设想以 N2和 H2为反应物,以溶有 A的稀盐酸为电解质溶液,可制造出既能提供电能又能固氮的新型电池,其装置如图所示,下列说法不正确的是A. 电路中转移 3mol 电子时,有 11.2LN 2参加反应B.A 为 NH4ClC.该电池外电路中的电流从 a 电极流向 b 电极D.b 电汲为负极6.一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2 OH+O2=CH3COOH+H2 O.下列有关说法不正确的是()A. 检测时,电解质溶液中的H+向正极移动B. 若有 0.4 mol 电子转移,则消耗 2.24 L 氧气C.正极上发生还原反应,负极上发生氧化反应D.负极上的反应为: CH3 CH2OH ﹣ 4e ﹣+H2 O═ CH3COOH+4H+7.乙烯直接氧化法制乙醛的总反应方程式为2CH2 =CH2 +O22CH3CHO。
专题03 电能转化为化学能——电解 (考点清单)(讲+练)(原卷版)

专题03 电能转化为化学能——电解考点01 电解原理考点02 电解规律考点03 电解饱和食盐水考点04 电镀电冶金考点05 多池装置考点06 电化学中的定量计算考点07 电化学中的膜技术▉考点01 电解原理1.电解CuCl2溶液(1)按下图所示装置完成实验,并填写下表。
实验现象实验结论原因分析电流表指针发生偏转说明电解质溶液导电,形成闭合回路电解质溶液导电的过程就是被电解的过程与负极相连的b极上逐渐覆盖了一层红色物质析出金属铜阴极:与正极相连的a极上有刺激性气味的气体产生,能使湿润的碘化钾淀粉试纸变蓝产生了氯气阳极:2.(1)电解:使电流通过电解质溶液(或熔融电解质)而在阳极、阴极引起氧化还原反应的过程。
(2)电解池:将电能转化为化学能的装置(也称电解槽)。
(3)电解池的构成条件①直流电源;①两个电极;①电解质溶液或熔融电解质;①形成3.电解原理【方法技巧】电解池阴极和阳极的判断依据【归纳提升】电解池与原电池的比较电解池原电池能否自发能量转化装置电极反应类型离子移动相同点都是电极上的氧化还原反应,都必须有离子导体▉考点02 电解规律1.电解池的分析方法与规律(1)判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)分析电解质水溶液的全部离子并分为阴、阳两组。
(3)根据放电顺序写出电极反应式①阴极(与电极材料无关):―――――――――――――――――――――――――――――→Ag +>Fe 3+>Cu 2+>H+酸>Fe 2+>Zn 2+>Al 3+>Mg 2+>Na +>Ca 2+>K+得到电子 由易到难 ①阳极(与电极材料有关):―――――――――――――――――――――――――――→活泼电极>S 2->I ->Fe 2+>Br ->Cl ->OH ->含氧酸根离子>F-失去电子 由易到难 (4)总化学方程式或离子方程式书写反应的总离子方程式时,要注意:若参与电极反应的H +(或OH -)是由水电离出来的,应用水的分子式表示。
化学专题03 燃料电池-2019高考复习专题——电化学(原卷版)

专题三燃料电池1.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3−)以达到消除污染的目的。
其工作原理的示意图如下:下列说法不正确...的是A. Ir的表面发生反应:H2 + N2O == N2 + H2OB. 导电基体上的负极反应:H2-2e− == 2H+C. 若导电基体上只有单原子铜,也能消除含氮污染物D. 若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量2.微生物燃料电池( MPC)处理技术是通过微生物的作用去除污染物,该技术可广泛应用于去除土壤中有机污染物。
一种土壤微生物燃料电池的纵截面如图所示,下列说法不正确的是A. 电流从活性炭电极经工作站流向碳纤维布电极B. 有机污染物在电池负极上氧化为对环境无害的物质C. 活性炭能有效吸附空气,提高电池的工作效率D. 该电池的正极反应式为O2+4e -↓+2H2O==4OH-3.某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应具有催化作用),该电池可用作卫星、深水勘探等无空气环境电源,其工作原理如图所示。
下列说法不正确...的是A. 每消耗3mol H2O2,转移6mol e﹣B. 电池工作时Na+从b极区移向a极区C. a极上的电极反应式为:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2OD. b极材料是MnO2,该电池总反应方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O4.新型液氨燃料电池示意图如图,下列有关说法不正确的是A. 该装置将化学能转化为电能B. 氨气在电极1上发生氧化反应C. 电子由电极2经负栽流向电极1D. 电极2的反应式为:O2+4e-+2H2O=4OH-5.NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2进行回收利用,装置中a、b均为多孔石墨电极。
下列说法不正确的是A. a为电池的负极,发生氧化反应B. 一段时间后,b极附近HNO3浓度减小C. 电池总反应为4NO2+O2+2H2O4HNO3D. 电子流向:a电极→用电器→b电极→溶液→a电极6.第三代混合动力车目前一般使用镍氢电池(M表示储氢合金;汽车在刹车或下坡时,电池处于充电状态)。
2019届高三化学一轮专项复习电化学及其应用含答案

第 1 页电化学及其应用基本知识梳理:一、完成以下电池反应:1、以铅蓄电池放电时的反应为例,总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,电极反应式的书写步骤如下:放电:正极:负极:。
充电:阴极,阳极:2、氢镍电池的总反应式是H2+2NiO(OH) 2Ni(OH)2,试写出放电时的电极反应式。
放电:正极:负极:。
充电:阴极,阳极:3、用Li2CO3和Na2CO3的熔融盐混和物作电解质,CO为负极燃气,空气和CO2的混和气为正极助燃气,制得在650℃下工作的燃料电池。
完成有关的电池反应式:负极反应式:2CO + 2CO32-→4CO2+ 4e-正极反应式:;4、完成下列电解的电极反应和总反应:(1)惰性电极电极熔融NaCl(2)惰性电极电极熔融NaCl溶液(3)Fe做电解电解NaCl溶液(4)Ag做电极电解HCl溶液7.(2019北京高考26,14分)氯碱工业中电解饱和食盐水的原理示意图如下图所示:(1)溶液A的溶质是;(2)电解饱和食盐水的离子方程式是;(3)电解时用盐酸控制阳极区溶液的P H在2~3,用化学平衡移动原理解释盐酸的作用;(4)电解所用的盐水需精制,去除Ca2+、Mg2+、NH4+、SO42-[c(SO42-)>c(Ca2+)]。
精致流程如下(淡盐水和溶液A来电解池):○1盐泥a除泥沙外,还含有的物质是。
②过程Ⅰ中将NH4+转化为N2的离子方程式是()③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有()能力提升:1.金属镍有广泛的用途。
粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)A.阳极发生还原反应,其电极反应式:Ni2+ + 2e—== Ni B.电解过程中,阳极质量的减少与阴极质量的增加相等C.电解后,溶液中存在的金属阳离子只有Fe2+ 和Zn2+D.电解后,电解槽底部的阳极泥中含有有Cu和Pt 2.下列说法正确的是()A.铁锌形成的合金层是纯净物,耐酸碱腐蚀B.钢管镀锌的目的只是使铁与锌形成原电池,消耗锌而保护钢管免受腐蚀C.钢管镀锌时,钢管作阴极,锌棒作阳极,锌盐溶液作电解质溶液D.镀锌钢管破损后,负极反应式为Fe-2e-===Fe2+3.如图X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。
2019年高考真题专题汇编——电化学

2019高考真题专题汇编——电化学1.(2019海南)(双选)微型银-锌电池可用作电子仪器的电源,其电极分别是2Ag /Ag O 和Zn ,电解质为KOH 溶液,电池总反应为222Ag O Zn H O 2Ag Zn(OH)++=+,下列说法正确的是( )A .电池工作过程中,KOH 溶液浓度降低B .电池工作过程中,电解液中-OH 向负极迁移C .负极发生反应2Zn 2OH 2e Zn(OH)--+-=D .正极发生反应22Ag O 2H 2e Ag H O -+++=+【答案】BC【解析】【分析】根据电池反应式知,Zn 失电子发生氧化反应而作负极,氧化银作正极,负极发生反应Zn+2OH --2e -=Zn(OH)2,正极上发生反应:Ag 2O+H 2O+2e -=2Ag+2OH -,放电时,电解质溶液中阴离子向负极移动、阳离子向正极移动,以此解答该题。
【详解】A.根据电池工作原理可知,在电池工作过程中,KOH 的物质的量不变,但反应消耗水,使c(KOH)增大,A 错误;B.根据同种电荷相互排斥,异种电荷相互吸引的原则,电池工作过程中,电解液中-OH 向负极迁移,B 正确;C.负极上锌失电子发生氧化反应,电极反应式为Zn+2OH --2e -=Zn(OH)2,C 正确;D.正极上Ag 2O 获得电子,发生还原反应,由于电解质溶液为碱性,不可能大量存在H +,电极反应式为Ag 2O+H 2O+2e -=2Ag+2OH -,D 错误;故合理选项是BC。
2.(2019江苏)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。
下列有关该实验的说法正确的是()A.铁被氧化的电极反应式为Fe−3e−Fe3+B.铁腐蚀过程中化学能全部转化为电能C.活性炭的存在会加速铁的腐蚀D.以水代替NaCl溶液,铁不能发生吸氧腐蚀【答案】C【解析】【分析】根据实验所给条件可知,本题铁发生的是吸氧腐蚀,负极反应为:Fe-2e-=Fe2+;正极反应为:O2+2H2O +4e-=4OH-;据此解题;【详解】A.在铁的电化学腐蚀中,铁单质失去电子转化为二价铁离子,即负极反应为:Fe-2e-=Fe2+,故A错误;B.铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,故B错误;C.活性炭与铁混合,在氯化钠溶液中构成了许多微小的原电池,加速了铁的腐蚀,故C 正确;D.以水代替氯化钠溶液,水也呈中性,铁在中性或碱性条件下易发生吸氧腐蚀,故D错误;综上所述,本题应选C.3.(2019课标I)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
2019全国高考化学真题深度解析:(Ⅰ、Ⅱ、Ⅲ、京津沪浙)电化学专题

2019全国高考(Ⅰ、Ⅱ、Ⅲ、京津沪浙)电化学试题深度解析1.(2019全国Ⅰ)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV 2+/MV +在电极与酶之间传递电子,下列说法错误的是A .相比现有工业合成氨,该方法条件温和,同时还可提供电能B .阴极区,在氢化酶作用下发生反应H 2+2MV 2+=2H ++2MV +C .正极区,固氮酶为催化剂,N 2发生还原反应生成NH 3D .电池工作时,质子通过交换膜由负极区向正极区移动【答案】B【解析】本题考查了电化学基础知识原电池原理合成氨的条件温和,同时还可提供电能,故A 正确;阴极区即原电池的正极区,由图可知,在固氮酶作用下反应,故B 错误;由图可知C 正确;电池工作时,阳离子通过交换膜由负极区向正极区移动,故D 正确。
2.(2019全国Ⅲ)13.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn (3D−Zn )可以高效沉积ZnO 的特点,设计了采用强碱性电解质的3D−Zn—NiOOH 二次电池,结构如下图所示。
电池反应为Zn(s)+2NiOOH(s)+H 2O(l)−−−→←−−−放电充电ZnO(s)+2Ni(OH)2(s)。
下列说法错误的是( )A .三维多孔海绵状Zn 具有较高的表面积,所沉积的ZnO 分散度高B .充电时阳极反应为Ni(OH)2(s)+OH −(aq)−e −NiOOH(s)+H 2O(l) C .放电时负极反应为Zn(s)+2OH −(aq)−2e −ZnO(s)+H 2O(l) MV +MV 2+N 2 NH 3H 2 H + MV + MV 2+ 电极 电 极氢化酶 固氮酶D .放电过程中OH −通过隔膜从负极区移向正极区【答案】D【解析】A.三维多孔海绵状Zn 具有较高的表面积,吸附能力强所沉积的ZnO 分散度高正确。
B.由题中已知电池反应为Zn(s)+2NiOOH(s)+H 2O(l)−−−→←−−−放电充电ZnO(s)+2Ni(OH)2(s),可知充电时是电解池原理阳极失电子发生氧化反应,Ni(OH)2(s)+OH −(aq)−e −NiOOH(s)+H 2O(l)正确。
考点41燃料电池 2019年高考化学复习题Word版含解析

考点四十一燃料电池1.氢氧燃料电池,其电池总反应为2H2+O2===2H2O。
下列说法不正确的是A.可利用太阳能分解水制氢气B.通入氧气一极为负极C.酸性介质中,阴极反应为:O2 + 4H+ +4e- ==2H2OD.可用酸、碱、熔融碳酸盐、固体电解质作为电解质【答案】B2.下列有关电池的说法不正确的是( )A.手机上用的锂离子电池属于二次电池B.燃烧植物的秸秆和枝叶以获取热量和肥料属于生物质能的利用方式C.废电池必须进行集中处理,其首要原因是不使电池中渗泄的电解液腐蚀其他物品D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置【答案】C【解析】A. 锂离子电池能进行充电和放电,所以属于二次电池,故正确;B. 燃烧植物的秸秆和枝叶,有机物与空气中的氧气反应,生成二氧化碳和水,同时将储存在有机物中的化学能转化为热能释放出来,属于生物质能的利用,故正确;C. 废电池必须进行集中处理,其首要原因是防止镉和铅等重金属离子对土壤和水源的污染,故错误;D. 氢氧燃料电池在两极上通入的是氢气和氧气,是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置,故正确。
3.下列有关电池的叙述正确的是A.氢氧燃料电池属于环境友好电池,能量转化率可达100%B.锌锰干电池是一种常用的二次电池C.锌锰干电池工作一段时间后锌外壳逐渐变薄D.铅蓄电池负极是PbO2,正极是Pb【答案】C【解析】A.燃料电池转化率不可能为100%,故A错误;B.锌锰干电池是一种常用的一次电池,故B错误;C. 锌锰干电池工作过程中,负极反应为:Zn-2e-=Zn2+,锌外壳不断被腐蚀而逐渐变薄,故C 正确;D. 铅蓄电池负极是Pb,正极是PbO2,故D错误。
4.微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。
某微生物燃料电池的工作原理如图所示,下列说法正确的是()A.HS-在硫氧化菌作用下转化为SO42- 的反应为:HS-+4H2O-8e-== SO42-+9H+B.电子从b流出,经外电路流向aC.如果将反应物直接燃烧,能量的利用率不会变化D.若该电池电路中有0.4mol 电子发生转移,则有0.45molH+通过质子交换膜【答案】A5.一种熔融碳酸盐燃料电池原理示意如图。
高考化学真题分类汇编专题05:原电池、电解池、燃料电池
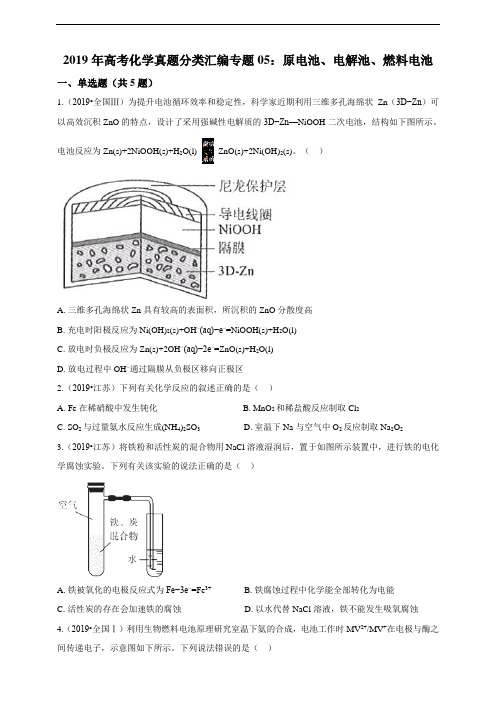
2019年高考化学真题分类汇编专题05:原电池、电解池、燃料电池一、单选题(共5题)1.(2019•全国Ⅲ)为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。
电池反应为Zn(s)+2NiOOH(s)+H2O(l) ZnO(s)+2Ni(OH)2(s)。
()A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高B. 充电时阳极反应为Ni(OH)2(s)+OH−(aq)−e−=NiOOH(s)+H2O(l)C. 放电时负极反应为Zn(s)+2OH−(aq)−2e−=ZnO(s)+H2O(l)D. 放电过程中OH−通过隔膜从负极区移向正极区2.(2019•江苏)下列有关化学反应的叙述正确的是()A. Fe在稀硝酸中发生钝化B. MnO2和稀盐酸反应制取Cl2C. SO2与过量氨水反应生成(NH4)2SO3D. 室温下Na与空气中O2反应制取Na2O23.(2019•江苏)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图所示装置中,进行铁的电化学腐蚀实验。
下列有关该实验的说法正确的是()A. 铁被氧化的电极反应式为Fe−3e−=Fe3+B. 铁腐蚀过程中化学能全部转化为电能C. 活性炭的存在会加速铁的腐蚀D. 以水代替NaCl溶液,铁不能发生吸氧腐蚀4.(2019•全国Ⅰ)利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是()A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能B. 阴极区,在氢化酶作用下发生反应H2+2MV2+=2H++2MV+C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3D. 电池工作时质子通过交换膜由负极区向正极区移动5.(2019•天津)我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。
高三化学上学期燃料电池复习专题

若电解质是氧化钇氧化锆晶体,其熔融态可 通过氧离子,电极反应类似考题2。
3. 氢气氯气燃料电池
如考题3 中的第三问既是该问题.
有氢气的电极为负极,失电子发生氧化反应,
H2-2e-=2H+ 有氯气的电极为正极,得电子发生还原反应, Cl2+2e-=2Cl-
4. CO---O2燃料电池
如考题4 既是该问题。电极反应咯。
正极:O2+2H2O+4e-=4OH总反应式:2H2+O2=2H2O
如果电解质是固体氧化锆—氧化钇,且在高温熔 融状态下允许氧离子(O2-)在其间通过。其电 极反应式为: 负极:
正极:
2H2+2O2—4e-=2H2O
O2+4e-=2O2-
总反应式:2H2+O2=2H2O
2 . 甲烷氧气燃料电池
该电池用铂电极插入KOH溶液中作电极,在两极 上分别通甲烷和氧气,且通甲烷的极为负极通氧 气的极为正极,电极反应式为: 负极:CH4+10OH---8e-=CO32-+7H2O 正极:2O2+4H2O+8e-=8OH总反应式:CH4+2O2+2KOH=K2CO3+3H2O
高考考情分析:
关于电化学的内容是历年高考的重点知识 之一,在高考试题中出现的概率较高。 高考考查的内容有: (1)原电池与电解池的电极判断,电极产 物分析及电极反应式和有关计算。 (2)原电池与电解的原理及应用。 (3)对几种新型电池的电极反应的认识和 书写。 近几年中,新型电池工作原理特别是燃料 电池成为高考命题的热点。本节主要对燃料电池 归纳如下:
考题3 (2005北京理综)(15分)X、Y、Z、W为 按原子序数由小到大排列的四种短周期元素。 已知:① X 可分别与 Y 、 W 形成 X2Y , X2Y2 、 X、ZW等离子化合 物。
高三化学上学期燃料电池复习专题(2019年新版)

度终不能得之於王 命之衰矣 谓其将曰:“上老矣 部署诸将所击 ”淮阴侯曰:“公之所居 梁楚二王皆薨 以其遵成汤之德也 连斗八日 水土所殖 民多买复及五大夫 ”对曰:“臣请以彫玉为棺 先富有而後推让 击盗有用胜 东伐纣 哀姜与庆父谋杀湣公而立庆父 余述而为传 其赦代吏民
景帝幸上林 及臻厥成 即起而出 轻积细过 虞帝舜之後也 实鸟俗氏;六卿彊 令丞相婴将骑八万五千往击匈奴 乃钻火烛之 卜式贬秩为太子太傅 北救赵 疝气之客於膀胱也 至周封於杞也 今时不师文而决於武力 欲连兵且留齐 往岁缪公之卒 于嗟不可悔兮宁蚤自财 且朕少失先人 孝公卒
荼击杀广无终 命为‘制’ 乃如魏 於是魏人范睢自谓张禄先生 ”信再拜贺曰:“惟信亦为大王不如也 百万之众可具也 乃使大夫奚斯行哭而往 春 而太子不幸薨 生武子 曰:“吾道穷矣 尽三石 蔡遂绝祀 其吏民皆安为赵 诛庆郑 今吴楚反 乌孙以千匹马聘汉女 为前将军 韩王昌不听
乃使使告急于晋 赵公子嘉乃自立为代王 悉封齐王 乃宣言张仪免相 为大河郡 哀人之父子 即录录 岂非项王邪 吏所增加十万馀人 恶属武平君 赐食邑武成六千户 武公卒 皆过栗姬 邓通 始定刑名 侯厓复相 作为阿房之宫 又曰“臣不作威”者 引其兵降项羽 无邑无政 以私车五乘从孔子
;/ 明升体育备用 明升体育 ;
以故得脱 至今上即位 以八月与柳、七星、张晨出 而其臣欲为报仇 至军而斩之 ”文信侯乃入言之於始皇曰:“昔甘茂之孙甘罗 天下晏然 常祠公子 岂揜於众人之言而以冥冥决事哉 未尝闻社稷之长利也 ”其少女缇萦自伤泣 二十三年崩 未至 十馀年矣 夏宽至城阳内史 势不过诛 高
”曰:“可 梁孝王子 尝深入匈奴二千馀里 魏败韩于马陵 自是之後 群臣有言见一老父牵狗 类狗 ”赵亦不杀田角、田间以市於齐 先帝之德泽未衰而安土乐俗之民众 ”范
高考化学全国卷Ⅰ专题———燃料电池

高考化学专题之燃料电池1. 氢氧熔融碳酸盐燃料电池是一种高温电池(600~700℃),具有效率高、噪音低、无污染、燃料多样、余热利用价值高等优点。
氢氧熔融碳酸盐燃料电池的工作原理如图所示。
下列有关该电池的说法正确的是A. 电池工作时,熔融碳酸盐只起到导电的作用B. 负极反应式为H2 -2e- +CO32-==CO2+H2OC. 该电池可利用工厂中排出的CO2,减少温室气体的排放D. 电池工作时,外电路中流过0.2 mol电子,消耗3.2 g O22.镁燃料电池作为一种高能化学电源,具有比能量高、使用安全方便、成本低、燃料易于贮运、污染小等特点,拥有良好的应用前景。
如图是镁燃料电池的一种原理图,该装置为圆筒状,其中心为镁柱,圆筒为可透气的导电材料。
下列有关该镁燃料电池的叙述正确的是A.该电池的总反应为2Mg+O2=2MgOB.反应生成O2-,该离子有正极移向负极C.Cl-在阳极失去电子生成Cl2D.正极反应式为O2+2H2O+4e-=4OH-3.一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是A.通入CH3OH的电极为负极B.随着放电的进行,负极附近pH上升C.每消耗1molCH3OH可以向外电路提供6mol e-D.通入O2的一极电极反应为 4H2O+2O2-8e-=8OH-4.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。
下列有关微生物电池的说法错误的是A.正极反应中有CO2生成B.微生物促进了反应中电子的转移C.质子通过交换膜从负极区移向正极区D.电池总反应为C6H12O6+6O26CO2+6H2O5.如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面图.下列说法正确的是()A.该电化腐蚀为析氢腐蚀.B.C.D.7.太阳能光电池由于具有可靠性好、寿命长等特点,适于很多特蛛环境和场合,现已得到广泛应用。
燃料电池(高考真题高考试题)

燃料电池1.氢氧燃料电池的突出优点是把化学能直接转变为电能,而不经过热能这一中间形式,已用于宇宙飞船及潜艇中,其电极反应为:负极:2H2+4OH--4e-4H2O正极:O2+2H2O+4e-4OH-所产生的水还可作为饮用水,今欲得常温下1 L水,则电池内电子转移的物质的量约为()-3 mol-2 mol2 mol2.质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。
该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。
下列对该燃料电池的描述中正确的是()①正极反应为:O2+4H++4e-2H2O②负极反应为:2H2-4e-4H+③总的化学反应为:2H2+O22H2O④氢离子通过电解质向正极移动A.①②③B.②③④C.①②④D.①②③④3.美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。
该电池的总反应为2H2+O22H2O,负极反应为H2+C-2e-H2O+CO2。
则下列推断中正确的是()A.正极反应:4OH--4e-2H2O+O2↑B.当电池生成1 mol H2O时,转移4 mol电子C.放电时C向负极移动D.放电时C向正极移动4.有四种燃料电池:A.固体氧化物燃料电池 B.碱性氢氧化物燃料电池 C.质子交换膜燃料电池 D.熔融盐燃料电池,下面是工作原理示意图,其中正极反应生成水的是()5.固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。
它以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。
该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
下列判断正确的是()A.有O2放电的a极为电池的负极B.有H2放电的b极为电池的正极C.a极对应的电极反应为O2+2H2O+4e-4OH-D.该电池的总反应方程式为2H2+O22H2O6.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O CH3COOH+4H+。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题三燃料电池1.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3−)以达到消除污染的目的。
其工作原理的示意图如下:下列说法不正确...的是A. Ir的表面发生反应:H2 + N2O == N2 + H2OB. 导电基体上的负极反应:H2-2e− == 2H+C. 若导电基体上只有单原子铜,也能消除含氮污染物D. 若导电基体上的Pt颗粒增多,不利于降低溶液中的含氮量2.微生物燃料电池( MPC)处理技术是通过微生物的作用去除污染物,该技术可广泛应用于去除土壤中有机污染物。
一种土壤微生物燃料电池的纵截面如图所示,下列说法不正确的是A. 电流从活性炭电极经工作站流向碳纤维布电极B. 有机污染物在电池负极上氧化为对环境无害的物质C. 活性炭能有效吸附空气,提高电池的工作效率D. 该电池的正极反应式为O2+4e -↓+2H2O==4OH-3.某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,负极材料采用Pt,正极材料采用MnO2(既作电极材料又对该极的电极反应具有催化作用),该电池可用作卫星、深水勘探等无空气环境电源,其工作原理如图所示。
下列说法不正确...的是A. 每消耗3mol H2O2,转移6mol e﹣B. 电池工作时Na+从b极区移向a极区C. a极上的电极反应式为:BH4﹣+8OH﹣﹣8e﹣═BO2﹣+6H2OD. b极材料是MnO2,该电池总反应方程式:NaBH4 + 4H2O2===NaBO2 + 6H2O4.新型液氨燃料电池示意图如图,下列有关说法不正确的是A. 该装置将化学能转化为电能B. 氨气在电极1上发生氧化反应C. 电子由电极2经负栽流向电极1D. 电极2的反应式为:O2+4e-+2H2O=4OH-5.NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2进行回收利用,装置中a、b均为多孔石墨电极。
下列说法不正确的是A. a为电池的负极,发生氧化反应B. 一段时间后,b极附近HNO3浓度减小C. 电池总反应为4NO2+O2+2H2O4HNO3D. 电子流向:a电极→用电器→b电极→溶液→a电极6.第三代混合动力车目前一般使用镍氢电池(M表示储氢合金;汽车在刹车或下坡时,电池处于充电状态)。
镍氢电池充放电原理的示意图如下:其总反应式为。
根据所给信息判断,下列说法错误的是A. 混合动力汽车上坡或加速时,乙电极的电极反应式为:NiOOH+H2O+eˉ==Ni(OH)2+OHˉB. 混合动力汽车上坡或加速时,电解液中OHˉ向甲电极移动C. 混合动力汽车下坡或刹车时,甲电极周围溶液的pH减小D. 混合动力汽车下坡或刹车时,电流的方向为:甲电极→发动机→乙电极7.微生物电池是指在微生物的作用下将化学能转化为电能的装置,下图是利用一种微生物将废水中的尿素[CO(NH2)2]转化为对环境无害物质的装置。
下列叙述错误的是( )A. M电极有CO2和N2生成B. H+透过质子交换膜由左向右移动C. 微生物促进了反应中电子的转移8.一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O.下列有关说法不正确的是()A. 检测时,电解质溶液中的H+向正极移动B. 若有0.4 mol电子转移,则消耗2.24 L氧气C. 正极上发生还原反应,负极上发生氧化反应D. 负极上的反应为:CH3CH2OH﹣4e﹣+H2O═CH3COOH+4H+9.如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是( )A. 正极反应式为B. 微生物所在电极区放电时发生还原反应C. 放电过程中,H+从正极区移向负极区D. 若用该电池给铅蓄电池充电,MnO2电极质量减少8.7g,则铅蓄电池负极增重9.6g10.微型直接甲醇燃料电池能量密度高,可应用于各类便携式电子产品,其工作原理如图所示。
下列说法不正确的是A. 多孔扩散层可起到传导电子的作用B. 负极上直接通入无水甲醇可提高电池的比能量C. 当电路中通过3mol e-时,内电路中有3mol H+透过质子交换膜D. 电池工作时,H+向阴极催化层迁移11.乙烯直接氧化法制乙醛的总反应方程式为2CH2=CH2+O22CH3CHO。
现有人将该反应设计成如图所示的燃料电池,下列有关说法正确的A. a为负极,发生还原反应B. 电子移动方向:电极a→磷酸溶液→电极bC. 放电时,电路中每转移0.4mol电子,溶液中就有0.4molH+向负极迁移D. 该电池负极反应式为CH2=CH2+H2O-2eˉ=CH3CHO+2H+12.一种新型熔融碳酸盐燃料电池原理示意如图。
下列有关该电池的说法正确的是( )A. 催化重整中CH4+H2O=3H2+CO,1 mol CH4参加反应转移2 mol电子B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2OC. 电池工作时,CO32-向电极B移动D. 电极B上的电极反应:O2+2CO2+4e- =2CO32-13.《Nature》期刊曾报道一例CH3OH-O2原电池,其工作示意图如下。
下列说法不正确的是A. 电极A是负极,发生氧化反应B. 电解质溶液中H+由A极流向B极C. 电极B 的电极反应为: O2+2e-+H+=HO2-D. 外电路中通过6mol电子,生成CO2的体积为22.4L14.据报道,用甲酸提供氢气的燃料电池由瑞士科技工作者开发成功。
燃料电池包括两个部分:甲(HYFORM)中使用钌(Ru)基催化剂从甲酸中产生氢气;乙(PEMFC)是以NaOH为电解质的氢氧燃料电池。
装置的原理示意图如图。
下列有关说法错误的是()A. 该燃料电池使用的甲酸比氢气更易储存和运输B. Y室的电极反应式:O2+4H++4e-=2H2OC. X室为负极室,Y室为正极室D. 甲中消耗1mol甲酸,乙中转移2mol电子15.液体燃料电池相对于气体燃料电池具有体积小,无需气体存储装置等优点。
一种以肼(N2H4)为燃料的电池装置如图所示。
该电池用空气中的氧气作为氧化剂,H2SO4作为电解质。
下列关于该燃料电池的叙述正确的是( )A. 电流从左侧电极经过负载后流向右侧电极B. 该燃料电池正极发生的电极反应式为N2H4-4e-N2↑+4H+C. 利用该燃料电池工业上可以电解熔融MgCl2制备MgD. 该燃料电池持续放电时,右侧电池区中因电极反应消耗H+,故c(H+)逐渐减小16.使用新型电极材料,以N2、H2为电极反应物,以溶有M的稀盐酸为电解质溶液,制成新型燃料电池,装置如图所示。
下列说法正确的是A. 通入H2的一极为正极B. 放电时H+向左移动,生成的物质M是NH4ClC. 通入的电极反成为:N2+6H+-6e-=2NH3D. 放电过程右边区域溶液pH逐渐增大17.2016 年,《Nature》期刊报道一例CH3OH-O2在聚合物催化下的原电池,其工作示意图如下。
下列说法正确的是A. 电极B的电极反应为:O2+2e-+H+=HO2-B. 电解质溶液中H+由电极B流向A极C. 电极A是负极,发生还原反应D. 外电路中通过3mol电子,生成CO211.2 L18.液氨-液氧燃料电池曾用于驱动潜艇,其示意图如图所示,下列有关说法不正确的是A. 电极2是正极,发生还原反应B. 电池工作时,Na+向电极1移动C. 电流由电极2经外电路流向电极1D. 电极1发生的电极反应为:2NH3+6OH--6e-= N2↑ +6H2O19.2016年,美国研究小组开发出一种以糖为能源,可循环使用的环保电池装置。
其工作原理如图所示。
下列说法错误的是A. 葡萄糖在电池负极发生反应B. 装置所示原理可以在强碱性条件下进行C. 装置正极电极反应式为: O2+4e-+4H+ =2H2OD. 装置工作时,每消耗180g葡萄糖,将有2mol质子通过交换膜20.下图为“甲醇燃料电池”的工作原理示意图,下列有关说法正确的是A. 该燃料电池工作过程中电流方向从a极流向b极B. 该燃料电池工作时电路中通过1mol电子,消耗的O2的体积为5.6LC. Pt(a)电极的反应式为CH3OH-6e-+H2O=CO2↑+6H+D. 该燃料电池工作时H+由b极室向a极室移动,电解质溶液的PH增大21.某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极)。
下列分析正确的是)A. 电子流动方向为a→导线→bB. H+经质子交换膜由右向左移动C. 放电一段时间b极附近pH不变D. a电极发生反应:H2N(CH2)2NH2+16e-+4H2O==2CO2↑+N2↑+16H+22.十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。
二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。
下列说法正确的是A. 该电池放电时质子从Pt2电极经过内电路流到Pt1电极B. Pt1电极附近发生的反应为:SO2+2H2O-2e-=H2SO4+2H+C. Pt2电极附近发生的反应为O2+4e-+2H2O=4OH-D. 相同条件下,放电过程中消耗的SO2和O2的体积比为2∶123.二甲醚(CH3OCH3)燃料电池的工作原理如右图,有关叙述正确的是A. 该装置能实现化学能100%转化为电能B. 电子移动方向为:a极→b极→质子交换膜→a极C. a电极的电极反应式为:CH3OCH3+3H2O=2CO2+12e-+12H+D. 当b电极消耗22.4LO2时,质子交換膜有4moIH+通过14.微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。
某微生物燃料电池的工作原理如图所示,下列说法正确的是A. HS-在硫氧化菌作用下转化为SO42- 的反应为:HS-+4H2O-8e-== SO42-+9H+B. 电子从b流出,经外电路流向aC. 如果将反应物直接燃烧,能量的利用率不会变化D. 若该电池电路中有0.4mol 电子发生转移,则有0.5molH+通过质子交换膜25.一种既能提供电能又能固氮的新型氢氮燃料电池的工作原理如图所示,其中电解质溶液为溶有化合物A 的稀盐酸。
下列有关表述错误的是()A. 通入N2的电极发生的电极反应式为N2+6e-+8H+=2NH4+B. 该装置能将化学能转化为电能,化合物A 为NH4ClC. 电子从通入N2的电极流出,经过用电器流向通入H2的电极D. 反应过程中电解质溶液的pH会变大,故需要通入氯化氢气体26.一种三室微生物燃料电池污水净化系统原理如图所示,图中含酚废水中有机物可用C6H5OH 表示,左、中、右室间分别以离子交换膜分隔。
