福州大学-乙酸正丁酯
乙酸正丁酯的制备实验报告

乙酸正丁酯的制备实验报告乙酸丁酯的合成与精制实验方案乙酸正丁酯的合成与精制专业实验预习报告实验名称: 乙酸正丁酯的合成及精制实验姓名: 学号: 联系方式: 组员: 专业:化学工程与工艺乙酸正丁酯的合成与精制一、实验目的(1)初步了解和掌握化工产品开发的研究思路和实验研究方法。
(2)学会组织全流程实验,并获得高纯度的产品。
(3)学会分析实验流程及实验结果,提出实验改进方案。
二、实验原理乙酸正丁酯是一种无色的液体。
具有比乙酸戊酯略小的水果香味。
它可与醇,酮,酯和大多数常用的有机溶剂混溶。
特别是当它预先与活性溶剂或是惰性溶液混和时是硝化纤维素和纤维素醚的一种溶剂。
天然品存在于苹果、香蕉、樱桃、葡萄等植物中,易挥发,难溶于水,能溶解油脂莘脑,树胶,松香等,有麻醉作用,有刺激性[1]。
乙酸正丁酯是一种重要的化工产品,也是一种重要的有机合成中间体,广泛用于涂料、制革、制药等工业。
它是化工、医药等行业的主要溶剂之一,是清漆、人造革等的良好溶剂,还可用于部分化妆品、添加剂、防腐防霉剂等合成中,用以调配食用香精,也可用做日化香精及酒用香精。
因此,乙酸正丁酯具有广泛的应用价值和发展前景。
现代工业中多采用间歇法,以浓硫酸作为催化剂生产,但此法存在着以下缺点:1) 由于浓硫酸有强脱水性和氧化性,可能产生乙醚、乙烯等副产物,同时可能由于局部过热出现碳化,影响产品的分离;2) 硫酸腐蚀性强,对设备的要求比较高;3) 反应后的产品要经过多次碱洗、水洗才能出去硫酸等杂质,后处理复杂,产生的废水多,污染环境,给环境保护带来很大的压力。
随着人们充分利用资源、简化工艺流程、提高经济效益、保护生存环境的意识不断增强和环保法规的日益完善,用环境友好催化剂替代浓硫酸催化合成酯类化合物已成为探索方向。
对于乙酸正丁酯合成实验方案的改进中,绝大多数还是以酸、醇为原料的,只是所采用的催化剂不同而已,但是大多数均为固体酸。
先将所查到的文献的部分方案简要叙述如下:?蔡新安[2]等人利用廉价易得的硫酸氢钾催化剂来制备乙酸正丁酯,酯化产率较高,催化剂可重复使用,后处理简单,效果良好。
乙酸正丁酯的实验室合成条件优化研究

乙酸正丁酯的实验室合成条件优化研究
邹静
【期刊名称】《化学工程师》
【年(卷),期】2024(38)3
【摘要】以冰醋酸和正丁醇为原料,浓H_(2)SO_(4)作催化剂,无水Mg SO4为干燥剂合成乙酸正丁酯,研究了投料比、反应时间、反应温度、浓H_(2)SO_(4)用量等对产率和纯度的影响。
得出最佳反应条件为:冰醋酸与正丁醇的物质的量之比为1∶1.05,冰醋酸的用量为14.00g,浓H_(2)SO_(4)用量为1.00m L,回流反应时间为40min。
在该条件下合成乙酸正丁酯,纯度超过98%,产率可达80%以上。
【总页数】5页(P14-18)
【作者】邹静
【作者单位】陕西国防工业职业技术学院化学工程学院
【正文语种】中文
【中图分类】O623
【相关文献】
1.乙酸正丁酯合成条件探讨
2.醋酸正丁酯合成中几种催化剂催化性能的研究及最优催化剂催化条件的优化
3.探索合成乙酸正丁酯的最佳条件
4.催化合成乙酸正丁酯实验条件的优化研究
5.反应精馏合成乙酸乙酯/乙酸丁酯联产优化研究(英文)
因版权原因,仅展示原文概要,查看原文内容请购买。
乙酸正丁酯制备实验报告

乙酸正丁酯制备实验报告乙酸正丁酯制备实验报告引言:乙酸正丁酯是一种常用的有机溶剂和香料成分,广泛应用于化学工业和食品工业中。
本实验旨在通过酯化反应制备乙酸正丁酯,并探究反应条件对产率的影响。
实验材料与方法:实验所需材料包括正丁醇、乙酸、浓硫酸和酸性酯化催化剂。
实验装置为圆底烧瓶、冷凝器、反应釜和磁力搅拌器。
首先,取一定量的正丁醇和乙酸,按照摩尔比1:1加入反应釜中。
然后,加入适量的酸性酯化催化剂,如硫酸。
接下来,将反应釜连接至冷凝器,并在烧瓶中加入冷却水。
最后,开启磁力搅拌器,开始反应。
实验结果与分析:在实验过程中,我们注意到反应温度对乙酸正丁酯产率的影响较大。
当反应温度过高时,反应速率会加快,但同时也会导致副反应的发生,从而降低产率。
实验中我们选择了适宜的反应温度并进行了多次实验,最终得到了较高的产率。
此外,我们还观察到反应时间对产率的影响。
较长的反应时间有助于提高产率,但过长的反应时间则会导致产率下降。
因此,在实验中我们控制了适宜的反应时间,以获得最佳的产率。
实验中我们使用了酸性酯化催化剂来促进反应的进行。
酸性催化剂可以提供质子,从而加速酯化反应的进行。
硫酸是一种常用的酸性催化剂,具有良好的催化效果。
在实验中,我们选择了适量的硫酸作为催化剂,并进行了多次实验以确定最佳的催化剂用量。
结论:通过本实验,我们成功制备了乙酸正丁酯,并探究了反应条件对产率的影响。
实验结果表明,适宜的反应温度、反应时间和催化剂用量是获得高产率的关键因素。
此外,我们还发现反应温度和反应时间的选择需要在速率和副反应之间进行权衡。
乙酸正丁酯作为一种常用的有机溶剂和香料成分,在化学工业和食品工业中具有广泛的应用前景。
通过本实验的实施,我们不仅获得了制备乙酸正丁酯的实际操作经验,还深入了解了酯化反应的原理和影响因素。
这对于我们进一步探索有机合成和化学工艺具有重要的意义。
实验的成功进行离不开实验人员的精心操作和仔细观察。
在今后的实验中,我们将进一步探索不同反应条件下的乙酸正丁酯制备,并寻求优化反应条件以提高产率。
乙酸正丁酯的制备实验报告

乙酸正丁酯的制备实验报告一、实验目的1、学习并掌握通过酯化反应制备乙酸正丁酯的原理和方法。
2、熟悉分水器的使用,了解共沸除水的原理。
3、巩固回流、蒸馏、洗涤和干燥等有机化学基本操作。
二、实验原理乙酸正丁酯是由乙酸和正丁醇在浓硫酸的催化作用下发生酯化反应而制得。
主反应:CH₃COOH + CH₃CH₂CH₂CH₂OH ⇌CH₃COOCH₂CH₂CH₂CH₃+ H₂O由于反应是可逆的,为了提高酯的产率,需要将反应生成的水及时从反应体系中除去。
本实验利用正丁醇、水和乙酸正丁酯形成共沸物(沸点 907℃),通过分水器不断将水从反应体系中分出,使反应向生成酯的方向进行。
三、实验仪器与药品1、仪器圆底烧瓶(250mL)、分水器、回流冷凝管、蒸馏烧瓶(100mL)、直形冷凝管、接引管、锥形瓶(100mL、50mL)、分液漏斗、量筒(10mL、50mL)、温度计(150℃)、电热套、铁架台、玻璃棒等。
2、药品冰醋酸(分析纯)、正丁醇(分析纯)、浓硫酸、饱和碳酸钠溶液、饱和氯化钠溶液、无水硫酸镁。
四、实验步骤1、加料在 250mL 干燥的圆底烧瓶中,加入 185mL 正丁醇、154mL 冰醋酸和 3~4 滴浓硫酸,摇匀后加入几粒沸石。
2、安装回流分水装置按从下到上、从左到右的顺序安装好回流分水装置。
将分水器装满水至支管处,然后放出 32mL 水,记录水的体积。
3、加热回流用电热套缓慢加热,保持回流速度为 1~2 滴/秒,回流约 15h。
当分水器中的水层不再增加,表明反应基本完成。
4、冷却停止加热,稍冷后拆除回流装置。
5、洗涤将反应液倒入分液漏斗中,用 25mL 饱和碳酸钠溶液洗涤至中性,然后再用 25mL 饱和氯化钠溶液洗涤一次,以除去碳酸钠。
6、干燥将有机层倒入干燥的锥形瓶中,加入约 3g 无水硫酸镁干燥 15~20分钟。
7、蒸馏安装蒸馏装置,先蒸出正丁醇,再收集 124~126℃的馏分,即为乙酸正丁酯。
五、实验现象与记录1、加料时,溶液为无色透明液体。
乙酸正丁酯的合成实验实训报告实例 .docx

乙酸正丁酯的合成实验实训报告实例 .docx一、实验目的:1.了解、掌握酯的合成方法和反应机理。
2.学习并掌握分液、提取、洗涤的基本操作技能。
3.掌握分子式相似的化合物的气相色谱的分析方法,加深对实验原理的理解。
二、实验原理:乙酸正丁酯的合成反应方程式:CH3COOH + CH3(CH2)3OH →CH3COO(CH2)3CH3+ H2O三、实验步骤:1.在干燥仪上干燥反应管1-2h,然后称取2g异丙醇加入到反应管中,加入10mL乙酸。
2.将反应管置于水浴中,加热反应1-1.5h,同时加入3-4滴浓硫酸作为催化剂。
3.反应罐中加入20mL的水,将反应液中的乙酸正丁酯过硫酸并入罐中,用水浴将反应罐加热,直到溶液完全沸腾。
4.离心筛滤去上层的油脂,用20mL二甲苯重复溶解和过湿含硫酸铁,然后将双层观察瓶中的橘黄色液体分离并保存。
5.通过加热反应液、过筛滤、分质提取和分子筛去表面有机杂质,然后用气相色谱法分析样品纯度。
四、实验结果:根据测得的实验数据,乙酸正丁酯是通过上述方法合成的。
经过气相色谱的分析,实验中合成的酯物质含量为98.5%,证实此方法非常有效。
本次实验旨在熟悉酯的合成方法和反应机理,熟练掌握分液、提取、洗涤的基本技能以及分子式相似的化合物的气相色谱分析方法。
本次实验的结果证明了该方法的有效性,合成纯度达到了98.5%。
通过本次实验,我意识到合成实验中需要仔细严谨,并且反应条件参数的调节是非常重要的,这个实验也展示了反应罐在整个反应过程中的重要作用。
在后续的研究中将会更加深入地探究这种配方和反应条件的优化方法,以尽可能地提高实验效率和结果的准确度。
乙酸正丁酯的制备

乙酸正丁酯的制备乙酸正丁酯是一种常用的有机溶剂,也常用于制备其他有机物。
本文将详细介绍乙酸正丁酯的制备过程。
一、实验原理乙酸正丁酯的制备是通过乙酸和正丁醇的酯化反应实现的。
酯化反应需要催化剂和水的存在。
其中催化剂可以使用浓硫酸或氯化铵二乙酰。
反应的化学方程式如下:CH3COOH + C4H9OH → CH3COOC4H9 + H2O二、实验步骤1、实验器材准备(1) 长颈漏斗(2) 三角瓶(4) 滴管(5) 沸石(6) 醋酸纤维素膜2、制备反应混合液取长颈漏斗中部填充沸石,加入30mL干正丁醇,并在230C油浴内充分加热,使其中加入的干正丁醇完全蒸发为无色清澈液体,冷却至室温,将三角瓶秤重,加入1.5mL浓硫酸,加至室温,将称量的浓硫酸慢慢倒入三角瓶中,瓶口用醋酸纤维素膜密封,将三角瓶放入劳森几上。
将加热后的沸石取出,将其余皆加入在长颈漏斗中已装有滴管的三口瓶中,用膜密封它的口,预热它的全体于油浴内,并反复秒数,直至温度平稳,出水珠完整,达到平衡,称取38.5mL的干乙酸加入三口瓶内,离心,取出水层不要。
3、进行酯化反应将加入浓硫酸的三角瓶立放于沙浴中,将三口瓶的支管以1小时每滴2-3滴的速度,加入全部乙酸,期间温度应维持在35-40℃,反应结束后,分别预加入去离子水、10%的氢氧化钠溶液,由于氢氧化钠溶液与未反应的乙酸起切断反应的作用,所以先加少量氢氧化钠溶液,离心,沉淀物一般为白色或带黄色,水中有些残渣,取上清液,加入适量无水氯化钠溶液,均匀混合,将其均匀装在蒸馏球中止,进行精馏至瓶温为90℃止即可,回收组分收集在含2-3g干氢氧化钠的干彼岸瓶内,并用干燥管通入干燥剂干燥,得到无色透明的液体。
三、注意事项1、实验过程中应注意安全,避免酸性物质对皮肤的损伤。
2、加热操作要进行缓慢,避免反应过程中温度过高。
3、实验中使用的器材应干燥无水,以免影响反应结果。
4、收集精馏的乙酸正丁酯时应加入干燥剂干燥,以去除其中的水份。
乙酸正丁酯合成实验的改进

渤海大学本科毕业论文乙酸正丁酯合成实验的改进Improvement of n-butyl acetate synthesis experiment学院(系):化学化工与食品专业:应用化学学号:0904015学生姓名:王亚彬入学年度:2009.09指导教师:王敏完成日期:2013年5月29 日渤海大学Bohai University乙酸正丁酯合成实验的改进王亚彬化学化工与食品安全学院摘要乙酸正丁酯是一种具有水果香味的无色液体,广泛应用于化工、制药、制革、香料等行业。
是一种优良的有机溶剂和化工原料。
在国内市场供不应求。
以往合成采用浓硫酸作催化剂,但存在以下缺点:(1)醇易失水成醚并产生焦质,影响产品质量。
(2)废酸污染环境并严重腐蚀设备。
本次实验针对乙酸正丁酯的制备方法进行了改进。
根据绿色化学的原则,对正丁醇、乙酸、环己烷和催化剂的用量进行了优化,得出较佳反应条件,采用甲基磺酸钙作催化剂,环己烷作共沸溶剂,在回流分水条件下反应2.5 h,酯化率可达93%。
反应结束后,催化剂经简单的相分离就可重复使用。
此方法具有污染小,收率高,经济环保等优点。
关键词:乙酸正丁酯;甲基磺酸钙;酯化反应;绿色化学Improvement of n-butyl acetate synthesis experimentWang YabinCollege of Chemistry and Food SafetyAbstractN-butyl acetate is a colorless liquid with fruit flavor, widely used in chemical, pharmaceutical, leather, spices and other industries. It is an excellent organic solvents and chemical raw materials. The need of it is large.Conventional synthesis using concentrated sulfuric acid as a catalyst, but has the following disadvantages: (1) Alcohols easily the loca into ether and produce coke quality, affect product quality. (2) The waste acid pollution of the environment and severe corrosion of equipment. The experimental method for the preparation of n-butyl acetate has been improved. Calcium with methyl sulfonic acid as catalyst and cyclohexane as an azeotropic solvent, the reaction was carried out under refluxing conditions. N-butanol, acetic acid, cyclohexane, and the amount of catalyst to draw the preferred reaction conditions, under the reaction conditions, the esterification rate up to 93%. After completion of the reaction, the catalyst by simple phase separation can be reused.Keywords: N-butyl acetate; Methyl sulfonic acid calcium; Esterification; Green Chemistry目录一、引言 (1)(一)绿色化学简介 (1)(二)已报道合成乙酸正丁酯的方法 (2)1. 氨基磺酸催化剂合成法 (2)2. 固体超强酸催化剂合成法 (3)3. 活性炭固载氯化铁催化合成法 (5)4.硫酸铈铵催化合成法 (6)5.固体超强酸催化剂 (7)6杂多酸作催化剂液相合成乙酸正丁酯 (7)(三)本论文选题及方向 (8)二、实验部分 (9)(一)反应方程式 (9)(二)仪器和试剂 (9)1. 实验仪器 (9)2. 实验试剂 (9)(三)甲基磺酸钙制备 (9)(四)乙酸正丁酯的合成 (9)(五)酯化率的测定 (10)(六)产品的分离及表征 (10)三、结果与讨论 (10)(一)醇酸摩尔比对酯化率的影响 (10)(二)溶剂用量对酯化反应的影响 (11)(三)催化剂用量对酯化率的影响 (11)(四)反应时间对酯化率的影响 (11)(五)甲基磺酸钙的重复使用性能 (12)(六)甲基磺酸盐对其他酯的催化作用 (12)(七)酯化反应机理 (12)四、结论 (13)五、参考文献 (13)六、致谢 (14)渤海大学本科毕业论文一、引言(一)绿色化学简介当今世界科技的迅猛发展,人们越来越意识到对环境保护的重要性。
乙酸正丁酯的制备实验流程详细解析

乙酸正丁酯的制备实验流程详细解析一、实验目的掌握酯化反应的基本原理和实验操作技术;学习使用分液漏斗、冷凝管等实验仪器;了解乙酸正丁酯的物理化学性质及其在工业上的应用;培养实验操作的严谨性和实验数据处理的能力。
二、实验原理乙酸正丁酯的制备是通过酯化反应实现的,酯化反应是一种醇与酸(有机或无机)作用生成酯和水的反应。
在本实验中,我们使用乙酸和正丁醇作为原料,通过加热和催化作用,使它们发生酯化反应生成乙酸正丁酯。
酯化反应是一个可逆反应,为了提高乙酸正丁酯的产率,通常需要加入浓硫酸作为催化剂,同时采用加热回流的方法,使反应向生成酯的方向进行。
反应方程式如下:CH3COOH + CH3(CH2)3OH ⇌CH3COOCH2CH2CH2CH3 + H2O三、实验步骤实验准备(1)仪器准备:圆底烧瓶、冷凝管、分液漏斗、接收瓶、温度计、磁力搅拌器、恒温水浴锅、电子天平、量筒等。
(2)试剂准备:乙酸、正丁醇、浓硫酸、饱和碳酸钠溶液、无水硫酸钠等。
实验操作(1)称取一定量的乙酸和正丁醇,按照摩尔比1:1.2的比例混合,放入圆底烧瓶中。
(2)加入少量浓硫酸作为催化剂,摇匀。
(3)安装实验装置,将圆底烧瓶置于恒温水浴锅中,连接冷凝管,冷凝管下端连接接收瓶。
(4)开启磁力搅拌器,使反应物充分混合。
(5)开启恒温水浴锅,设定反应温度,开始加热回流。
(6)观察反应现象,记录反应过程中的温度变化。
(7)反应结束后,关闭加热和搅拌,待反应液冷却至室温。
(8)将反应液倒入分液漏斗中,加入饱和碳酸钠溶液进行洗涤,以去除剩余的酸和催化剂。
(9)静置分层后,分离出有机层,再用饱和食盐水洗涤数次,以去除剩余的碳酸钠。
(10)将有机层转移至干燥的接收瓶中,加入无水硫酸钠进行干燥。
(11)通过蒸馏方法,收集乙酸正丁酯的馏分。
四、实验结果与数据分析实验结果实验结束后,我们收集到了一定量的乙酸正丁酯馏分。
通过称重和测定折射率等方法,我们可以计算出乙酸正丁酯的产率和纯度。
乙酸正丁酯实验报告

乙酸正丁酯实验报告实验目的:通过合成乙酸正丁酯的实验,了解酯化反应的基本原理及实验方法,掌握实验操作技能。
实验原理:酯化反应是指醇和酸在催化剂的作用下发生酯的生成反应,如乙醇与乙酸反应生成乙酸乙酯。
在本次实验中,正丁醇和乙酸在硫酸的催化下发生酯化反应,生成乙酸正丁酯。
反应方程式为:CH3COOH + CH3(CH2)3OH → CH3COOCH2CH2CH2CH3 + H2O实验步骤:1. 准备涂层玻璃反应器、超声波浴、导管、冷凝管、漏斗、称量器等实验器材和试剂。
2. 在涂层玻璃反应器中加入16.0mL正丁醇,并且用称量器精确称量4.5mL乙酸加入反应器中。
3. 在反应器中加入0.6mL浓硫酸,并将反应器放入超声波浴中。
4. 打开超声波浴开关,超声震荡2h。
5. 将超声波浴中的反应物倾入漏斗中,过滤得到沉淀物。
6. 用纯水冲洗出滤液中的杂质,再用这些水将过滤纸中的产物清洗干净,直至没有味道为止。
7. 将产物放在烤箱中烘干(Oven100℃,1h)。
按目标量,称取一定量干净的产品,记录质量。
8. 计算理论产物质量及产率;根据产物的理论产量和实际产量来计算产率。
实验结果:1. 所制备的乙酸正丁酯样品纯度较高,呈现为无色透明的液体,无异味。
2. 称取7.5g产物,实际产率为85.2%。
3. 理论产物的质量为8.6g。
实验结论:本次实验的实际产率较高,表明实验操作技能熟练,反应条件良好。
通过本次实验,我们深入了解了酯化反应的基本原理及实验操作技能,对于实验室的化学实验有所帮助。
参考文献:鲁炜译.《有机化学实验》[M].高等教育出版社,1991.。
乙酸正丁酯的制备实验报告思考题

乙酸正丁酯的制备实验报告思考题乙酸正丁酯的制备实验报告思考题乙酸正丁酯(Ethyl Butyrate)是一种常见的有机酯,具有香蕉和苹果味道,被广泛应用于食品和香料工业中。
在这篇实验报告中,我将讨论乙酸正丁酯的制备实验以及相关的思考题。
1. 实验步骤:1.1 准备器材和试剂:我们需要一支反应瓶、冷却管、溶液和试剂,如正丁醇、乙酸和浓硫酸。
1.2 预冷冷却管:我们将冷却管放入冰水中,以使其冷却。
1.3 添加试剂:向反应瓶中加入适量的正丁醇和乙酸,然后加入少量的浓硫酸作为催化剂。
1.4 进行酯化反应:将反应瓶放入加热器中,加热至较高温度。
将预冷的冷却管连接到反应瓶的开口,并将另一端放入收集瓶中。
1.5 收集产物:乙酸正丁酯会在加热过程中蒸发,并通过冷却管重新液化在收集瓶中。
2. 实验思考题:2.1 为什么需要添加浓硫酸作为催化剂?答:浓硫酸可以作为酸催化剂加速酯化反应的进行。
在酯化反应中,乙酸和正丁醇会经历酸催化下的缩合反应生成乙酸正丁酯。
2.2 为什么要预冷冷却管?答:预冷冷却管的目的是将反应物中的蒸汽冷却、液化,避免溢出并保证产物的收集。
正丁酯的沸点较低,通过冷却管的冷却作用,可以促使蒸发的乙酸正丁酯在冷凝后回到液体状态,从而收集到液体产物。
2.3 有没有其他方法制备乙酸正丁酯?答:是的,除了酸催化下的酯化反应外,还可以使用其他催化剂或反应条件制备乙酸正丁酯。
可以使用酶催化剂或酶催化反应,并且可以采用更温和的条件来进行制备,这样可以避免对反应物的破坏。
2.4 除了乙酸正丁酯的香蕉和苹果味道,还有其他哪些酯具有特殊的香味?答:酯类化合物常常具有特殊的香味。
除了乙酸正丁酯的香蕉和苹果味道,还有丁酸异丁酯(香蕉味)、乙酸异戊酯(香梨味)、乙酸己酯(葡萄味)等。
3. 总结和回顾:乙酸正丁酯的制备实验中,我们通过酸催化酯化反应来合成该有机酯。
这个实验两个重要的步骤是添加浓硫酸催化剂和预冷冷却管来保证反应进程和产物的收集。
乙酸正丁酯的制备

实验六乙酸正丁酯的制备一、实验目的1、认识酯化反应原理,掌握乙酸正丁酯的制备方法。
2、掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
3、学习有机物折光率的测定方法。
二、实验重点、难点1、重点:掌握乙酸正丁酯的制备方法。
掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
2、难点:掌握共沸蒸馏分水法的原理和分水器(油水分离器)的使用。
三、实验学时4学时四、实验原理酸与醇反应制备酯,是一类典型的可逆反应:为提高产品收率,一般采用以下措施:1、使某一反应物过量;2、在反应中移走某一产物(蒸出产物或水);3、使用特殊催化剂用酸与醇直接制备酯,在实验室中有三种方法。
第一种是共沸蒸馏分水法,生成的酯和水以沸臃物的形式蒸出来,冷凝后通过分水器分出水,油层回到反应器中。
第二种是提取酯化法,加入溶剂,使反应物、生成的酯溶于溶剂中,和水层分开。
第三种是直接回流法,一种反应物过量,直接回流。
制备乙酸正丁配用共沸蒸馏分水法较好。
为了将反应物中生成的水除去,利用酯、酸和水形成二元或三元恒沸物,采取共沸蒸馏分水法。
使生成的酯和水以共沸物形式逸出,冷凝后通过分水器分出水层,油层则回到反应器中。
五、仪器、试剂与装置仪器蒸馏装置玻璃磨口仪器、球形冷凝管、分水器、圆底烧瓶(50ml)、温度计(150℃)、锥形瓶(50ml)、烧杯(400ml)、电热套、分液漏斗、量筒(10ml、50ml)、电热套、铁架台、铁夹及十字头、铁圈、橡胶水管、天平试剂正丁醇(11.5ml)、冰醋酸(7.2ml)、浓硫酸、10%碳酸钠溶液、无水硫酸镁、冰块、沸石、甘油、pH试纸装置六、实验步骤1、50 mL圆底烧瓶中,加11.5 mL (0.125 mol) 正丁醇, 7.2 mL冰醋酸(0.125 mol) 和3~4d浓H2SO4(催化反应), 混匀,加2颗沸石。
2、接上回流冷凝管和分水器。
在分水器中预先加少量水至略低于支管口(约为1~2 cm),目的:使上层酯中的醇回流回烧瓶中继续参与反应,用笔作记号并加热至回流,不需要控制温度,控制回流速度1~2d/s。
乙酸正丁酯的理化性质及危险特性
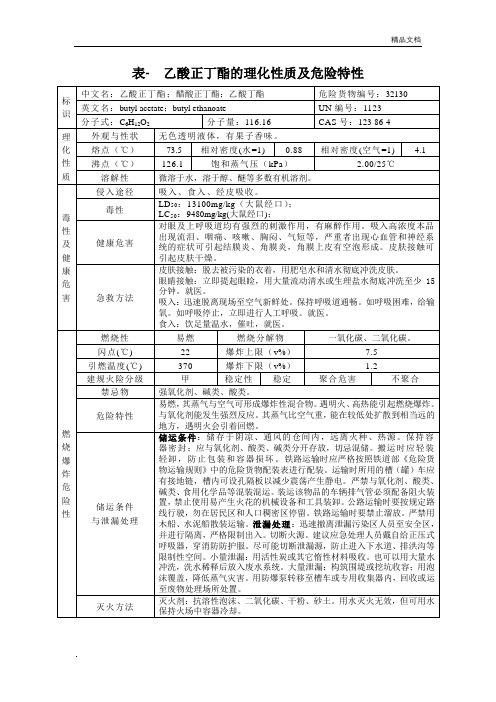
与泄漏处理
储运条件:储存于阴凉、通风的仓间内,远离火种、热源。保持容器密封;应与氧化剂、酸类、碱类分开存放,切忌混储。搬运时应轻装轻卸,防止包装和容器损坏。铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。运输时所用的槽(罐)车应有接地链,槽内可设孔隔板以减少震荡产生静电。严禁与氧化剂、酸类、碱类、食用化学品等混装混运。装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。铁路运输时要禁止溜放。严禁用木船、水泥船散装运输。泄漏处理:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源,防止进入下水道、排洪沟等限制性空间。小量泄漏:用活性炭或其它惰性材料吸收。也可以用大量水冲洗,洗水稀释后放入废水系统。大量泄漏:构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。
0.88
相对密度(空气=1)
4kPa)
2.00/25℃
溶解性
微溶于水,溶于醇、醚等多数有机溶剂。
毒性及健康危害
侵入途径
吸入、食入、经皮吸收。
毒性
LD50:13100mg/kg(大鼠经口);
LC50:9480mg/kg(大鼠经口);
健康危害
对眼及上呼吸道均有强烈的刺激作用,有麻醉作用。吸入高浓度本品出现流泪、咽痛、咳嗽、胸闷、气短等,严重者出现心血管和神经系统的症状可引起结膜炎、角膜炎,角膜上皮有空泡形成。皮肤接触可引起皮肤干燥。
一氧化碳、二氧化碳。
闪点(℃)
22
爆炸上限(v%)
乙酸正丁酯的制备实验报告思考题

乙酸正丁酯的制备实验报告思考题标题:乙酸正丁酯的制备实验报告思考题引言:乙酸正丁酯是一种重要的有机化合物,在化学实验中常用于有机合成和有机溶剂。
本文将探讨乙酸正丁酯的制备实验,并进一步思考与该实验相关的问题和概念。
1. 实验方法:在制备乙酸正丁酯实验中,可采用碱催化酯化反应。
将正丁醇与乙酸在催化剂存在下进行反应,生成乙酸正丁酯和水。
催化剂通常使用无水NaOH或酸性树脂,反应在适当的温度和时间条件下进行。
2. 实验步骤和条件:详细描述实验的步骤和条件,包括反应容器的选择、反应温度、反应时间、催化剂的用量等。
对于每个步骤,说明其重要性以及可能出现的注意事项。
3. 乙酸正丁酯生成的原理与机理:深入探讨乙酸正丁酯生成的原理和机理。
解释酯化反应的基本原理,包括醇和酸或酸酐反应产生酯的机制。
考虑可能的反应动力学因素和平衡条件,以帮助读者更好地理解反应过程。
4. 实验结果与分析:列出实验中所得到的乙酸正丁酯产率和纯度数据。
进一步分析可能影响产率和纯度的因素,如反应温度、催化剂用量、反应时间等。
讨论可能存在的产物副反应和影响产率的废弃物生成等问题。
5. 乙酸正丁酯的应用:介绍乙酸正丁酯的常见应用领域,如溶剂、香料等。
讨论其物理化学性质和特点,以及为什么它在这些领域中被广泛使用。
6. 实验中遇到的问题和解决方案:讨论实验过程中可能遇到的问题,如催化剂选择、反应达到平衡的时间等。
提供解决这些问题的可能方法和建议。
7. 思考题:7.1 乙酸正丁酯可以用于有机溶剂,那么在有机合成过程中,为什么要选择乙酸正丁酯作为溶剂?7.2 在酯化反应中,酸和醇的摩尔比对乙酸正丁酯产率有何影响?为什么?总结与回顾:通过本次乙酸正丁酯的制备实验,我们深入研究了酯化反应的原理和机制,同时了解了乙酸正丁酯的应用领域。
本文总结了实验结果的分析与讨论,并就可能遇到的问题提供了解决方案。
观点和理解:作者认为乙酸正丁酯的制备实验是有效的,因为我们通过探索它的原理和机制来加深对酯化反应的理解。
乙酸正丁酯的制备实验原理

乙酸正丁酯的制备实验原理1. 前言大家好,今天我们来聊聊一个有趣的实验,那就是乙酸正丁酯的制备。
听起来是不是有点高大上?别担心,咱们用简单的语言来解释一下,绝对让你听得懂、记得住。
乙酸正丁酯可不是个陌生的角色,它在香水、食品和医药等领域都有身影,算是个多才多艺的家伙。
话不多说,咱们赶紧深入一下这个实验的原理。
2. 实验的基本原理2.1 酯化反应那么,乙酸正丁酯究竟是怎么来的呢?其实,它是通过一种叫“酯化反应”的过程制造出来的。
想象一下,乙酸和正丁醇就像两对情侣,彼此吸引,经过一番“热恋”,最终结合成一个新的分子。
这种反应其实挺简单的,主要是乙酸中的羧基和正丁醇中的醇基发生了化学反应,水分子从中溜走,留下了咱们想要的乙酸正丁酯。
2.2 反应条件当然,光有化学反应可不够,我们还得提供一些条件来助它一臂之力。
一般来说,我们会加点酸催化剂,比如硫酸。
它就像是派对上的DJ,让气氛更热烈。
催化剂的作用是加速反应,但本身并不会消耗掉,真是个聪明的小家伙。
反应的温度通常控制在一个合适的范围,过高或过低都不太行,得让它在“舒适区”里活动,才能保证反应顺利进行。
3. 实验步骤3.1 材料准备好啦,接下来我们聊聊实验的具体步骤。
首先,你得准备好材料,乙酸、正丁醇和催化剂。
别小看这几样东西,都是大牌角色。
通常,乙酸的比例要稍微多一点,这样才能推动反应朝着咱们想要的方向发展。
听起来是不是有点像买菜?对啊,好的材料是成功的关键!3.2 反应过程然后,咱们就把这些材料混合在一起,加热搅拌。
哇,这个过程可真是妙不可言,就像煮一锅美味的汤。
随着温度的升高,气味开始弥漫,这时你会觉得心里乐开了花,感觉快要出好东西了。
等到反应结束,水分子也被“请”走了,咱们的乙酸正丁酯就诞生啦!最后,咱们还得进行分离和纯化,确保产品的质量,别让杂质捣乱。
4. 结尾说到这里,乙酸正丁酯的制备实验原理就基本介绍完啦!这个过程虽然听上去有点复杂,但其实充满了乐趣。
乙酸正丁酯的制备 毕业论文

中文摘要乙酸正丁酯的合成有许多种方法,有对甲苯磺酸、钨钛杂多酸盐、浓H2S04一K Cr2 07、改性煤基活性炭、固体超强酸、浓硫酸等作催化剂的合成。
本实验以浓硫酸作催化剂,以冰乙酸和正丁醇为原料合成乙酸正丁酯,考察醇与酸物质的量比、反响时间、催化剂用量等因素对酯化率的影响。
得出反响的最正确条件为: V(正丁醇):V(冰乙酸)=1.6:1.0,催化剂用量为冰乙酸,质量的3%,反响温度124℃~126℃,反响时间45min左右,用浓硫酸作催化剂时,乙酸正丁酯的收率为69%~76%。
关键词:乙酸正丁酯;酯化反响;催化剂ABSTRACTSynthesis of butyl acetate There are many ways for acid, titanium tungsten heteropoly acid, concentrated H2S04—KCr207, modified coal-based activated carbon, solid super acid, concentrated sulfuric acid as catalyst. In this experiment, concentrated sulfuric acid as catalyst to acetic acid and butanol to butyl acetate was synthesized to study alcohol and acid molar ratio, reaction time, catalyst amount on esterification rate. The optimal reaction conditions were: V (n-butyl alcohol): V (acetic acid) = 1.6:1.0, catalyst and acetic acid, with 3%, reaction temperature 124 ℃~ 126 ℃, reaction 45min time around, with concentrated sulfuric acid catalyst and butyl acetate the yield was 69% ~ 76%.Keywords:butyl acetate; esterification ;catalyst目录目录 (1)第一章前言 (4)乙酸正丁酯的简介 (4)乙酸正丁酯的性质 (4)乙酸正丁酯的用途 (4)羧酸酯的生产现状与开展趋势 (5)对环境的影响 (5)第二章实验内容 (6)2.1 仪器及试剂 (6)仪器 (6)2.1.2 试剂 (7)实验内容 (7)2.3 乙酸正丁酯性能测试方法 (8)2.4 实验结果与讨论 (9)醇酸质量比的不同对产物的影响 (9)反响时间不同对产物的影响 (9)催化剂用量不同对产物的不同 (10)第三章总结 (10)参考文献 ................................................................................................... .. (11)致谢 ........................................................................................................... .. (12)第一章前言乙酸正丁酯的简介乙酸正丁酯,英文名:n-Butyl acetate 别名:醋酸正丁酯,结构式:CH3COO(CH3)3CH3 。
毕业论文-年产1500吨乙酸正丁酯工艺设计

本科毕业设计说明书(论文)(2013届)题目:年产1500吨乙酸正丁酯工艺设计专业班级化学工程与工艺所在学院化学工程与材料学院学生姓名学号指导教师提交日期2013年4月年产5000吨乙酸正丁酯工艺设计摘要乙酸正丁酯(n-Butyl acetate)是一种无色透明,具有可燃性的,水果香味的液体[1],它可以作为溶剂,应用于清漆、塑料等行业中,在化工、制药、香料等行业,也充当着重要的角色。
在实验室中,乙酸正丁酯有多种合成方法,在工业生产中,当下主要是以乙酸和正丁醇为原料,用硫酸做催化剂的传统工艺。
但是该工艺生产工序繁杂,能耗高,产品损失多,设备腐蚀严重,并产生大量的废水,污染环境。
本次设计用固体对甲苯磺酸作为催化剂,运用反应精馏技术,进行年产1500吨乙酸正丁酯的工艺设计。
期间还用Aspen Plus软件进行了一系列数据模拟计算,使得设计更为精确可靠。
设计中,原料以醇酸摩尔比0.98:1混合方式进料,进料量为244kg/hr。
反应精馏塔中用到塔板20块,在第七块板上进料,温度为120℃。
塔顶的混合液经冷凝分水后,去除水相,有机相与塔顶的粗酯混合后,再进入常规精馏塔中进行反应。
常规精馏塔用到40块塔板,在第14块板上进料。
塔顶产物经冷凝后回流,塔釜得到93.9%含量的酯。
得到的产品最后经过固体碱干燥,达到GB/T3729-2007优等品要求。
通过Aspen中的模拟数据,进行物料和热量衡算,还有设备的选型。
在经济这一块,有投资估算,成本估算和收入估算,分析其利润及经济效益。
得到该工厂的投资回收期是3.3年,净现值为231.92万元,内部收益率是19.99%,大于10%(基准收益率),因此该项目是经济合理的。
关键词:乙酸正丁酯,Aspen Plus模拟,固体对甲苯磺酸,反应精馏THE PROCESS DESIGN OF N-BUTYL ACETATE WITH ANNUAL OUTPUT OF 1500 TONSABSTRACTN-butyl acetate (n-Butyl acetate) is a kind of liquid, which is colorless, flammable and transparent, with fruit flavor. Widely used as a solvent in varnish, plastic, it also plays an important role in chemical, pharmaceutical and perfume industries. There are a variety of methods to synthesis n-butyl acetate in the laboratory, however, the industrial method now is mainly traditionally conventional process, make acetic acid and n-butanol as raw material, using sulfuric acid to catalyze. But this process is of much shortcoming, like complication, high energy consumption, product loss, severe corrosion of the equipment, and large amounts of waste water production.The process using the technology of reactive distillation with solidp-toluenesulfonic acid as catalyzer, was designed for annual production capacity of 1500 tons of butyl acetate. Aspen Plus software was also used to conduct a series of data simulation, to make the results more accurate.In this design, the raw material, acetic acid and n-Butyl alcohol, were mixed with molar ratio 0.98:1 and 244 kg/hr feed amount. Total tray 20 was used in the reactive distillation column, and the feed plate was the seventh with temperature 120℃. After condensation, there was nearly no water left, the organic phase was mixed with the crude ester from bottom, entering the nomal distillation tower for reaction. Using 40 trays and feed board 14th, ester content of 93.9% product was gained, and the top liquid refluxed to the first tower after condensed again. Then the final product after solid base dry was acquired, which achieved the requirement GB/T3729-2007.Material and heat balance was calculated by the Aspen Plus data, and equipments were also selected. In the economical field, investment, cost andrevenue estimate were made to analyse the economic benefits. After calculation, the plant payback period was 3.3 years, the net present value is of 2,319,200 yuan, and the internal rate of return is 19.99%, which was greater than 10%(the benchmark rate of return). All in all, the the project is economically reasonable.Key Words: n-Butyl acetate, Aspen Plus simulation,solidp-toluenesulfonic acid,reactive distillation目录摘要 (II)ABSTRACT (III)第一章总论 (1)1.1 产品概述 (1)1.2 生产方法及特点 (1)第二章市场需求 (3)2.1 全球生产状况 (3)2.2 我国生产与贸易状况 (5)2.2.1 国内生产情况 (5)2.2.2 全球市场份额 (5)2.2.3 进出口情况 (6)2.2.4 发展趋势及措施 (6)第三章工艺设计方案 (7)3.1 概述 (7)3.2 硫酸作催化剂间歇生产 (8)3.3 反应精馏技术生产 (8)5.2.1 固体酸——反应精馏 (9)5.2.2 无机盐——反应精馏 (10)5.2.3 有机盐——反应精馏 (10)5.2.4 离子交换树脂——反应精馏 (10)3.4 热泵精馏的应用 (11)3.5 小结 (11)第四章生产工艺流程 (12)4.1 原料路线 (12)4.2 采用的生产方法及特点 (12)4.3 工艺流程示意图 (13)4.4 工艺流程描述 (14)第五章物料衡算 (15)5.1 物料衡算的原理方法及步骤 (15)5.1.1 原理 (15)5.1.2 方法 (15)5.1.3 步骤 (15)5.2 物料衡算过程 (16)5.2.1 原料及产品的物性数据 (16)5.2.2 反应精馏物料衡算 (17)5.2.3 油水分离物料衡算 (18)5.2.4 常规精馏塔物料衡算 (19)5.2.5 反应精馏总流程物料衡算 (21)5.3 后期精制物料衡算 (22)5.4 原材料消耗定额及消耗量 (22)第六章热量衡算 (23)6.1 热量衡算的原理 (23)6.2 热量衡算过程 (23)6.2.1 原料预热器热量衡算 (24)6.2.2 反应精馏塔热量衡算 (25)6.2.3 分水冷却器热量衡算 (26)6.2.4 常规精馏塔热量衡算 (27)6.2.5 产品冷却器热量衡算 (28)6.2.6 产品精制热量衡算 (29)6.3 能量调配 (30)6.4 动力消耗定额及消耗量 (30)第七章主要设备 (31)7.1 反应精馏塔设计 (31)7.1.1 Aspen模拟设计 (31)7.1.2 反应精馏塔总体结构 (32)7.1.3 反应精馏塔填料 (33)7.2 常规精馏RadFrac塔设计 (33)7.2.1 精馏塔设计原则 (33)7.2.2 精馏塔类型选择 (33)7.2.3 Aspen模拟设计 (34)7.2.4 常规精馏塔总体结构 (34)7.3 固体碱干燥器 (35)7.4 其他设备选型 (36)7.4.1 储罐的选型 (36)7.4.2 泵的选型 (37)7.4.3 换热器的选型 (38)第八章厂址选择与环境安全保护 (41)8.1 厂址选择 (41)8.2 执行的环境质量标准及排放标准 (41)8.3 三废产生情况分析及处理方式 (42)8.3.1 废气 (42)8.3.2 废液 (42)8.3.3 废渣 (42)8.4 厂区供电 (42)8.5 存储安全 (43)(3)防雷防静电措施 (44)第九章投资估算 (44)9.1 编制依据 (44)9.2 固定资产 (44)9.2.1 工程费用 (44)9.2.2 固定资产投资估算表 (47)9.3 无形资产 (47)9.4 递延资产 (47)9.5 预备费用 (48)9.6 流动资产 (48)9.7 总投资估算表 (49)9.8 资金筹集 (49)第十章成本估算及财务评价 (50)10.1 估算依据 (50)10.2 成本估算 (50)10.2.1 原料辅料费 (50)10.2.2 动力费及污水处理费 (50)10.2.3 工资及福利 (51)10.2.4 车间经费 (52)10.2.5 其他费用 (52)10.2.6 成本估算表 (53)10.3 销售收入和税金估算 (54)10.3.1 销售收入估算 (54)10.3.2 税金估算 (55)10.4 财务评价 (55)10.4.1 损益表 (55)10.4.2 现金流量表 (56)10.4.3 投资回收期 (57)10.4.4 净现值 (57)10.4.5 内部收益率 (58)第十一章总结与展望 (60)11.1 设计总结 (60)11.2 前景展望 (60)参考文献 (61)致谢 (63)附录 ................................................... 错误!未定义书签。
乙酸正丁酯实验原理

乙酸正丁酯实验原理嘿,朋友!今天咱们就来好好唠唠乙酸正丁酯这个实验原理。
这可有意思着呢!我先给你讲讲啥是乙酸正丁酯。
你可以把它想象成一个小小的化学精灵,在化学世界里有着独特的地位。
乙酸正丁酯是一种有香味的液体,它的分子就像一群小伙伴手拉手一样组合在一起。
从结构上看,它是由乙酸和正丁醇发生反应得来的。
这就好比两个人合作创造出一个新的东西一样神奇。
那这个反应是怎么发生的呢?这就是我们实验原理要探讨的重点啦。
在这个反应里,我们用到的是酯化反应的原理。
什么是酯化反应呢?简单来说,就是酸和醇反应生成酯和水。
就像一场化学舞会,酸和醇这两位舞者,在合适的条件下,交换彼此的一部分,然后形成新的组合。
想象一下这个场景:乙酸就像一个带着特殊标志(羧基)的小团体,正丁醇呢,也带着自己的独特标识(羟基)。
当把它们放在一起的时候,在催化剂的作用下,就像是有一个魔法棒在指挥。
乙酸的羧基中的羟基( - OH)和正丁醇羟基( - OH)上的氢原子(H)就像是两个互相吸引的小磁铁,它们结合在一起,变成了水(H₂O)。
而剩下的部分就组合成了我们的乙酸正丁酯。
这就像是两个小伙伴各自拿出自己的一部分,然后把剩下的部分拼接在一起,创造出了一个全新的小伙伴。
我和我的实验室小伙伴们在做这个实验的时候,那可真是状况百出啊。
我的一个同学小明,一开始就特别自信地说:“这有啥难的,不就是把东西放一起反应嘛。
”结果呢,他没有控制好反应条件,就像厨师做菜没有掌握好火候一样。
温度过高或者过低,都会影响这个化学舞会的进程。
温度低了,乙酸和正丁醇就像两个懒家伙,反应慢吞吞的,半天都看不到什么成果。
温度高了呢,又像是一群疯狂的舞者,乱了节奏,可能会产生一些我们不想要的副反应,就像原本是一场优雅的舞会,结果变成了一场混乱的闹剧。
还有用量的问题呢。
另一个同学小红就特别纠结这个。
她总是问:“到底乙酸和正丁醇该用多少比例才好呢?”这就像是在调配一种特殊的药水,比例不对,最后的结果可就大相径庭了。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
冷凝液组成% 上层 下层
沸点℃
即是反应物、产物, 也是除水剂
118 117
126
98.8/1.2
0.68/99.32
90.7
55.5/44.5
32.8/67.2
79.9/20.1
7.7/92.3
93.0
/
/
117.6
63.0/8.0/29
86/11/3.0
1.0/2.0/97.0
90.7
三、实验装置
移至分液漏斗中分液
10mL 水 10mL 10%Na2CO3 10mL 水
1、注意分液漏斗的使用 2、各步各洗去什么 如有酸性怎么处理? 干燥剂的量与放置的时间 无水硫酸 镁干燥 1、所用仪器需干燥 2、若有前馏分117 ℃左右的,是 什么?
蒸馏,收集 124~126 ℃馏分
提纯流程图
n-C4H9OH CH3COOC4H9 n-C4H9OH CH3COOH H2SO4 H 2O 有机层 10ml水 水层 CH3COOH H2SO4 H 2O CH3COOC4H9 CH3COOH H2O n-C4H9OH H2SO4 CH3COONa 水层 Na2SO4 n-C4H9OH NaHCO3 H 2O 水层 CH3COOC4H9 10ml水 NaHCO3 n-C4H9OH H2O NaHCO3 n-C4H9OH H 2O 10ml10%Na2CO3
有机层
有机层
CH3COOC4H9 无水MgSO4 CH3COOC4H9 n-C4H9OH n-C4H9OH H2 O 干燥
加入沸石蒸馏 收集124-126℃馏分
R
CH3COOCH2(CH2)2CH3 + H2O
OH C O
+
H
+
OH
R C OH
R C OH
R'OH
R'
OH H
+OH
OH R C
+ OH
Hale Waihona Puke O2R'
R
C
O
-H+
R' +
H2O
O
可逆反应; 需要酸催化; 常用催化剂:浓硫酸,对甲苯磺酸,强酸 型离子交换树脂,过渡金属氧化物……
R
C
O
R'
三、实验原理
一、实验目的
学习羧酸和醇的酯化反应原理,了解三元共沸原理及 其应用。
掌握利用分水器进行共沸蒸馏的脱水方法,训练萃取、 洗涤、蒸馏等纯化技术。
二、 羧酸的化学性质
脱羧反应
H R C H
O C
取代
O
H
酸性
α-H的反应
酯化反应(-OH被取代)
CH3COOH + CH3(CH2)2CH2OH
O
+
H2SO4
CH3COOH + CH3(CH2)2CH2OH 0.125mo1 0.125mo1
H+
CH2COOCH2(CH2) 2CH3+H2O
除去产物水! 如何实现?
如何使反应趋于完成?
蒸气组成% 乙酸 正丁醇 乙酸丁酯 乙酸正丁酯/水 正丁醇/水 乙酸正丁酯 /正丁醇 乙酸正丁酯 /正丁醇 /水 72.9/27.1
乙酸正丁酯
1.加入硫酸后为什么要混合均匀,加热反应液出
现黑色是什么原因?
2.为什么说正丁醇和乙酸正丁酯即是反应物、产
物,也是除水剂?
3.如何正确使用分水器?怎样标记生成的水量? 4. 反应终点如何判断? 5.在蒸馏分离阶段,如果水没有干燥完全,会出 现什么情况?
化学合成与制备实验B
乙酸正丁酯的制备
分水器
约1cm
四. 实验步骤及注意事项
圆底烧瓶 11.5mL 正丁醇 7.2mL 冰醋酸 3~4滴浓硫酸 注意分水器先要预先装好水,离支管 口1cm左右 滴加硫酸注意混合均匀
沸石
反应40 min左右 不再有水生成 装好装置
分水器水层的高度要维持不变 记录分出的水量
反应瓶和分水器中的上层都应移入
反应结束
