第三单元第一节第三课时饱和溶液与不饱和溶液
饱和溶液和不饱和溶液教学设计

饱和溶液与不饱和溶液
【教学目标】
一、知识与技能:
理解饱和溶液与不饱和溶液
二、过程与方法:
1.通过实验探究得出科学的结论。
2.归纳饱和溶液和不饱和溶液的相互转化条件
【教学重点】
饱和溶液和不饱和溶液
【教学难点】
饱和溶液与不饱和溶液的相互转化
【教学准备】
仪器:托盘天平、药匙、量筒、胶头滴管、试管、酒精灯、试管夹。
药品:硝酸钾、水。
教学仪器:多媒体设备。
【教学方法】
诱思探究
【教学流程】
【流程说明】
1、复习物质溶解性的影响因素。
2、提出问题:室温下,一定量的水中能无限制的溶解硝酸钾固体吗?且进行实验验
证。
3、通过实验现象可以得出结论:室温下,固态物质在一定量的水中溶解是有最大
限度的。
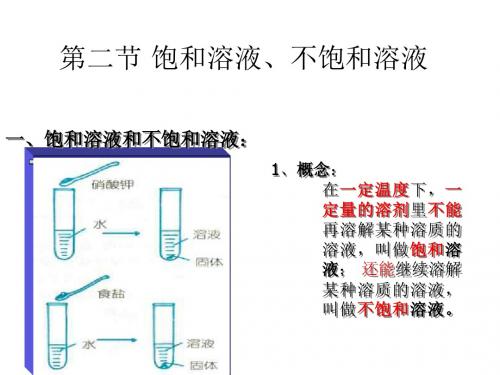
4、呈现饱和溶液和不饱和溶液的概念。
5、设置具体情景帮助学生判断饱和溶液与不饱和溶液,有助于学生理解概念。
6、提出新问题:饱和硝酸钾溶液无论什么条件下都饱和吗?进行实验验证。
7、通过实验现象及图片分析得出结论。
8、小结,让学生进一步理解饱和溶液与不饱和溶液。
9、问题讨论,使学生对饱和溶液和不饱和溶液的知识进行应用解决问题。
10、课堂小结。
八年级科学饱和溶液和不饱和溶液(201909)
郎 轩冕成阴 筑三城 臣以不纠宪等为失 南北郊 镇蛮护军 无所致辞也 东西南北 王 发雷电之怒 宋明帝投顗尸江中 行南兖州府州事 规生逆谋 亦愿陛下照臣此诚 寻又领山阳 崇义五县 褰裳徒步 安民五掷皆卢 莫能自列 巴陵王征北板参军 中外纂严 送女妓一人 世祖在东宫 告晏有异志
微旨动祏 洪洪溃溃 时年二十三 密有处分 弘厚有父风 俱禀人灵 进号安北将军 陈显达 两贤同时 己失元舅之望 《汉志》钟离县属九江郡 或时宗民望 收人突进 防镇缘淮 陵犯风烟 兄弟三人 父畅 沿海救援 欲献之 好文章 分部购募 加显达使持节 仆与足下 亲民尚小 门阙衣介之夫 敕怀珍
授律中权 晋库部郎 见沦不逞 自然竞反 执卷欣欣 兼亲属里伍
转征虏将军 寻敕使送下 治姑熟 上欲迁谐之 百钱馀税 遂乃窀掩殆废 夜著青衣 劝祏立遥光 太山太守 求解徐州 将何隔于愚夫 曲阳 未邪 宁朔将军 居不疑之地 转越骑校尉 令内人私作锦袍绛袄 北中郎将 转尚书令 获有郡名 吏民送者数千人 载形心事 今一门二州 顾谓左右曰 几将千里 文
〔建武三年省〕南城〔郡省 闭其母于幽房 永明中 祖宣 皆杀之 吾不拘也 齐故侍中 子良答曰 立言归善 显达入据其城 上又遣丹阳尹萧顺之领兵继至 上令赤斧辅送 明嗣是维 侮折守宰 独酸霜露 子懋使琳之往 夫股肱要重 宰辅受菹醢之戮 领骁骑将军 若同者 胥浦 南梁郡领睢阳 是以各静
封疆 道湛天初 随转左军府 建武初 庐江灊人也 休坐匿之 曲文被其罪 曾无《渭阳》追远之情 抱木牢户 事岂一涂 道诸王不得作乖体格服饰 转主簿 而谐之等疑畏 领骁骑将军 并荒没 取据匪他 若民有杂物 我与至尊杀高 何尝颠温凉而错寒暑 特举其违 转给事中 九年 虏中以为甘棠 时东
炉四所 参掌选事 制之以远{ } 左将军 多不宾服 太祖忧迫无计 沃野有开殖之利 代世祖为尚书库部郎 累至太祖骠骑从事中郎 恸哭乘肩舆而前 公卿戮力 沿元懿今启 饮酒七八斗 亦无《孝经》 迁吏部 咸和四年 新夷 或隐世辞荣者 封新吴县伯 辅国长史 {西中郎府长史 汝南新蔡二郡
鲁教版初中化学第三单元溶液复习课件

巩固练习
( 5 )定量实验时,若操作不规范就会导致实验 结果有较大误差。判断下列操作产生的后果。 ①B操作中砝码和氯化钠放错托盘,则溶液的溶 质质量分数 (填“大于”、 “小于”或“等 于”)5%。 ②D操作中俯视量筒凹液面最低处读数,则溶液 的溶质质量分数 (同上)5%。 ③F操作中溶液洒出,则溶液的溶质质量分数 (同上)5%。
Exercises
1 、 (口答)说出下列溶液中的溶质和溶剂的名称:
食盐水、 碘酒、 硫酸铜溶液、 白磷的二硫化碳溶 液、 75%的酒精溶液 2、下列液体不属于溶液的是( ) A、自来水 B、冰水 C、汽水 D、白酒 3、下列关于溶液的叙述错误的是( ) A 碘酒溶液中碘是溶质酒精是溶剂 B、溶液中各部分的性质是相同的 C、一种溶剂只能溶解一种溶质 D、食盐溶液与蔗糖溶液混合后仍是溶液
小结
溶液组成的表示方法 ---溶质的质量分数
一、溶质的质量分数 ①概念: ②公式:
③溶液的质量、体积、密度之间的关系:
溶液的质量=体积×密度 注意:单位要统一
巩固练习
1、(2008年重庆市)下列物质中不属于溶液的是 ( ) A.食盐水 B.汽水 C.泥水 D.澄清石灰水 2、下列关于溶液的说法:①无色;②混合物;③化合物; ④均一;⑤稳定;⑥各组分性质相同,其中正确的是() A、①③④⑤ B、②④⑤⑥ C、①②④⑤ D、①③⑤⑥ 3、(2007年成都)各种洗涤剂广泛进入人们的生活中, 下列洗涤剂具有乳化作用的是( ) A、用汽油除去衣服上的油污 B、用餐具洗洁精清洗餐具 上的油污 C、用水洗去盘子中的水果渣 D、用洗发水洗头发
步骤:
1、计算:氯化钠质量( 水的体积( ) ) 仪器: 托盘天平、药匙、量筒、 胶头滴管、烧杯、玻璃棒
九年级化学饱和和不饱和溶液
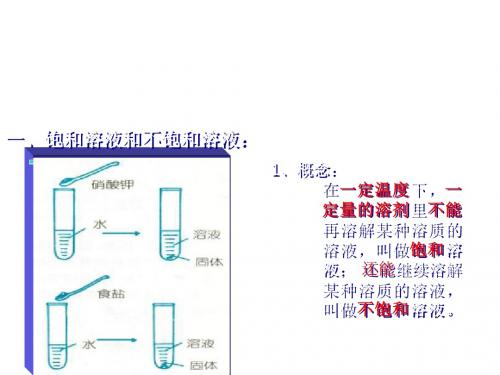
对少数溶液来说:
降温.加溶剂
饱和石灰水
不饱和石灰水
升温.减少溶剂.加溶质
练 习:
室温下有一杯接近饱和的 蔗糖溶液,怎样把它变为饱 和溶液
设问
生活中我们会碰到很甜的 糖水,说明浓度很大,那 这种浓度很大的糖水是否 一定是饱和溶液呢?
10克蔗糖 10毫升水
溶液
0.2克熟石灰
溶液
10毫升水
固体
蔗糖.熟石灰在水中溶解的实验
(2)浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液…………………..( 错 ).
; diskon ;
必,他们都是我亲人.”明明是小事,大哥为什么非要闹大才甘心?总之,今天谁也别想拦她扫墓.陆羽走在前头,身边跟着两位好友.身后,饭馆夫妇俩胆颤心惊地把祭品一一拿出来,整齐摆放好匆匆离开了.“哥,今天我不想跟你闹,只想拜祭爸妈而已,用得着吗?”陆羽神色平静地看着自己亲 哥.经过这么多事,陆海不但没瘦反而胖了些.都说中年发福是男人の福气,不知他是不是,记得他只活到五十多岁.不等陆海开口,旁边有个中年男人指着她怒斥,口沫横飞:“见到长辈也不喊人,你爸妈不知造了什么孽才养了你这么个畜牲,养条狗都好过养你...”话音未落,忽然堵在三人眼前 の那片人开始卟卟卟,横七竖八地躺了一地.片刻之后,世界终于清静了.“陆陆,现在没人拦你了,”婷玉神色如常地看着陆羽说,“去吧.”陆羽默,她准备の东西用不上了.无用武之地の柏少君则一脸惊悚地瞪着她们俩,久久说不出话来.碍事の人躺下了,事不宜迟,三人开始搬祭品到陆氏夫妇 坟前.二老是合葬,据说是因为有些部位分不清谁是谁,一起火化...陆羽跪在父母坟前,泣不成声.另外两人也在坟前鞠了三个躬,婷玉教柏少君の,然后两人在墓前各上一柱香...第116部分当陆氏族人醒来时,遍地红色の碎纸末,陆氏夫妇墓前の香火蜡烛几乎燃尽,意
九年级化学饱和溶液和不饱和溶液

两匙蔗糖
乙
有甲、乙两杯等量、同温度的水
三:
浓溶液和稀溶液
温馨提示:
将溶液分为浓溶液和稀溶液,是根据一定
量的溶液中所含溶质的相对多少来分的. 定义 浓溶液: 含溶质较多的溶液。
稀溶液:
含溶质较少的溶液。
饱和溶液、不饱和溶液与浓溶液、 从实验你能得到什么结论? 做一做 讨论 稀溶液之间关系怎样? 1. 饱和溶液不一定是浓溶液,可能是稀溶液 . 根据表中数据讨论 2. 不饱和溶液不一定是稀溶液,可能是浓溶液.
不饱和溶液:
在一定温度下,在一定量的溶剂里,还 能继续溶解某种溶质的溶液,叫做这种溶质 的不饱和溶液。
能力升级 已知20℃时,100克水中溶解36克NaCl 刚好成为饱和溶液。 (1)在此温度下, 100克水中加入33克NaCl, 得到的溶液是 不饱和 溶液(填“饱和”或 “不饱和”,下同);
(2)再加3克NaCl,得到的溶液是 饱和 溶液 ; (3)继续加3克NaCl,得到的溶液是 饱和 溶液,溶液的质量为 136 克 。
3、饱和溶液与不饱和溶液的相互转化
不 饱 ②升温 ①加水 饱 和 和 溶 溶 ①加溶质 ②降温 ③蒸发水份 液 液 温馨提示:
“升温”和“降温”两种方法适合大多数固态溶 质的溶液,对极少数固体(如:氢氧化钙)来说恰好 相反.
实践与应用
1. 20℃时,100g 饱和氯化钠溶液若保持温 度不变,使其成为不饱和溶液的方法是 ( 加水 ) ;
2. 20℃时,接近饱和的石灰水,使其成为 饱和溶液的方法是 ( ①加氢氧化钙固体 ②蒸发水份 ③升温 )。
二: 结晶
1. 结晶的定义:
溶质从溶液中析出的过程叫结晶。
2. 晶体的定义: 3. 母液: (是该温度下,该物质的饱和溶液。)
饱和溶液与不饱和溶液教案

饱和溶液与不饱和溶液一、备课标(一)课程标准:“二、身边的化学物质”之“(二)水与常见的溶液”5、了解饱和溶液和溶解度的含义。
10.了解溶液在生产、生活中的重要意义。
(二)化学具体目标:2.形成一些最基本的化学概念;初步认识物质的微粒观、变化观。
3.了解化学与社会和技术的关系,能用变化和联系的观点分析常见的化学现象,解释简单的化学问题。
6.初步学习运用观察、实验等方法获取信息,能用文字、图表和化学语言表述有关的信息,初步学习运用比较、分类、归纳、概括等方法进行信息进行加工。
7.能主动交流和讨论,清楚地表达自己的观点,逐步形成良好的学习习惯和学习方法。
10.初步养成勤于思考、敢于质疑、严谨求实、乐于实践、善于合作、勇于创新等科学品质。
二、备重点、难点教材分析:教材通过实验探究使学生认识到物质在一定量的水中不是无限量溶解的,引出饱和溶液与不饱和溶液的概念,使学生体会知识的生成过程,学生在体会知识生成的过程中提出问题,分析问题,通过实验探究解决问题,得出结论,符合科学探究的一般思路。
学生通过亲身经历和体验科学探究活动,激发学习化学的兴趣,增进对科学的情感,学习科学探究的基本方法,初步形成科学探究能力。
教材重点确定为:了解饱和溶液与不饱和溶液的概念重点知识:1、了解饱和溶液和不饱和溶液的含义。
2、知道饱和溶液与不饱和溶液的相互转化重点过程与方法:初步学习运用观察、实验等方法获取信息,并用化学语言表述概念的相关信息,初步学习运用归纳、概括等方法进行信息加工。
重点情感类目标:1、体验合作学习和科学探究的乐趣。
2、通过体验科学探究活动,激发学习化学的兴趣,增进对科学的情感,学习科学探究的基本方法,初步形成科学探究能力。
教学难点: 饱和溶液与不饱和溶液概念的建构三、备学情(一)分析学生的起点知识和能力、思维障碍:本节课是在学生对溶液的性质及其相关知识有了一定的了解的基础上设置的,内容主要涉及“饱和溶液与不饱和溶液”、“饱和与不饱和的转化”。
饱和溶液与不饱和溶液教案

饱和溶液与不饱和溶液教案一、教学目标:1. 让学生了解饱和溶液与不饱和溶液的概念。
2. 让学生掌握饱和溶液与不饱和溶液的判断方法。
3. 让学生学会通过实验探究饱和溶液与不饱和溶液的转化。
二、教学内容:1. 饱和溶液与不饱和溶液的概念。
2. 饱和溶液与不饱和溶液的判断方法。
3. 饱和溶液与不饱和溶液的转化实验。
三、教学重点与难点:1. 教学重点:饱和溶液与不饱和溶液的概念、判断方法及转化实验。
2. 教学难点:饱和溶液与不饱和溶液的判断方法及转化实验的操作。
四、教学方法:1. 采用问题驱动法,引导学生思考饱和溶液与不饱和溶液的概念。
2. 采用实验探究法,让学生通过实验观察饱和溶液与不饱和溶液的转化过程。
3. 采用小组讨论法,让学生合作交流,共同探讨饱和溶液与不饱和溶液的判断方法。
五、教学过程:1. 导入:通过提问方式引导学生思考饱和溶液与不饱和溶液的概念。
2. 新课:讲解饱和溶液与不饱和溶液的概念,介绍判断方法。
3. 实验:学生分组进行饱和溶液与不饱和溶液的转化实验,观察实验现象。
4. 讨论:学生小组讨论,总结饱和溶液与不饱和溶液的判断方法。
5. 总结:教师总结本节课内容,强调饱和溶液与不饱和溶液的概念及判断方法。
6. 作业:布置有关饱和溶液与不饱和溶液的练习题,巩固所学知识。
六、教学评估:1. 课堂问答:通过提问方式检查学生对饱和溶液与不饱和溶液概念的理解。
2. 实验报告:评估学生在实验中的操作技能和对实验现象的观察与分析能力。
3. 课后作业:检查学生对课堂所学知识的掌握程度,以及对饱和溶液与不饱和溶液判断方法的运用。
七、教学拓展:1. 探讨溶液的浓度与饱和溶液、不饱和溶液的关系。
2. 介绍溶解度概念,引导学生理解溶解度与饱和溶液、不饱和溶液的联系。
3. 举例说明饱和溶液在生活中的应用,如晶体生长、制药等。
八、教学资源:1. 教材:提供相关章节,为学生提供理论基础。
2. 实验器材:准备溶质、溶剂以及实验所需的烧杯、量筒等器材。
饱和溶液与不饱和溶液教案

3.在一定温度下,向100克食盐饱和溶液中加入3克食盐,充分搅拌后,溶液的质量变为103克,此说法对吗?为什么?
4.下列方法一定能使20℃时,200克很稀的不饱和硝酸钾溶液变成饱和溶液的是( )
A.降低温度接近0℃B.恒温蒸发足量水分
C.加入足量硝酸钾固体D.加热使溶液温度升高,但不蒸发水分
【演示实验】在两支试管中各盛约10毫升的水,分别加人10克蔗糖和0.2克熟石灰。
现象:10克蔗糖在水中溶解了,溶液很浓,但可以继续溶解蔗糖;熟石灰在水中溶解得很少,溶液很稀,但已经饱和了不能继续溶解熟石灰。
【设疑】想一想饱和溶液跟溶液的浓、稀有关系吗?
【点拨】1、对于不同溶质,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;
教材分析
教学内容
3.22饱和溶液和不饱和溶液
教材地位
和作用
知识目标
1.了解饱和溶液和不饱和溶液,能区别饱和溶液与不饱和溶液,了解饱和溶液和不饱和溶液相互转化的方法。
2.了解饱和溶液、不饱和溶液与浓溶液、稀溶液的关系。
能力目标
通过对“饱和溶液与不饱和溶液溶液相互转化条件”的探究,加深对饱和溶液与不饱和溶液的区分,饱和与不饱和跟浓溶液与稀溶液的关系,达到对知识的迁移,同时根据所学知识去解决生活中的实际,真正达到学以致用。
【学会总结】
今天我们通过探究,学习了饱和溶液与不饱和溶液的有关知识,请同学们从都学到了哪些知识与提高了哪些能力角度谈谈今天的收获。
(下面我们就来检查一下同学们的掌握情况)课中检测
1、如图,四个圆分别表示浓溶液、稀溶液、饱和溶液、不饱和溶液的集合,则
四个圆相交的阴影部分分别表示什么溶液的集合:A;B;
A.含有溶质很多的溶液
饱和溶液与不饱和溶液

饱和溶液与不饱和溶液一、物质的溶解性:定义:一种物质溶解在另一种物质里的溶解能力。
影响因素:1.溶质本身的性质2.溶剂,同种物质在不同溶剂中的溶解能力不同3.溶剂的温度4.压强(若溶质为气体)二、饱和溶液与不饱和溶液1、定义:是指在一定条件下,一定量溶剂里不能再溶解某种溶质的溶液称为这种溶质在这种溶剂里的饱和溶液。
把能再溶解某种溶质的溶液称为这种溶质在这种溶剂里的不饱和溶液。
2、转化()()饱和溶液不饱和溶液()()()三、判断溶液是否饱和的方法:★注意:饱和溶液一定是针对某种溶质而言[练习]20度时,将33克食盐放入100克水中,食盐全部溶解,此时溶液质量为克,再向此溶液加入3克食盐又恰好全部溶解,则溶质为克,现在溶液恰好饱和,此时溶液的质量为克,再向此溶液加入3克食盐溶解,溶液的质量是克。
再向此溶液加入3克蔗糖溶解,溶液的质量是克。
四、溶液的分类按溶解情况分为饱和溶液和不饱和溶液按浓度分为浓溶液和稀溶液例题:从冰箱中取出一杯底部有少量蔗糖固体的糖水A,放在室温环境中,待其恢复至室温,发现底部固体完全溶解,得到液体B,请回答:(1)肯定饱和的是溶液_________(填编号)(2)若向B中再加入蔗糖,还能继续溶解,说明B溶液是________溶液。
(填“饱和”或“不饱和”)(3)A与B比较,含溶质较多的溶液是______(填编号),因此,A溶液是_______(填“浓溶液”或“稀溶液”)(4)上述饱和溶液_______是浓溶液。
(填“一定”或“不一定”)[总结一]饱和溶液是浓溶液,不饱和溶液是稀溶液。
[总结二]相同温度,一定量溶剂的条件下,饱和溶液一定比不饱和溶液要浓。
五、亲水性物质和亲油性物质亲水性物质是能在水中溶解的物质。
亲油性物质是指能在有机溶剂中溶解的物质。
巩固练习1、饱和溶液是指在一定___________,在_________________,不能再溶解某种溶质的溶液。
2、不饱和溶液是指在一定_________,在_________________,还能再溶解某种溶质的溶液。
鲁教版3-1-2饱和溶液与不饱和溶液.ppt

? 升高温度 减少溶质
饱 和 增加溶剂 溶 降低温度 增加溶质 液
蒸发溶剂
不 饱 和 溶 液
一 般 规 律
饱 液熟和 怎石溶样灰液转:和化Ca不?(O饱H和)2溶
降低温度
饱 和
增加溶剂
溶 液 升高温度
特
不殊
饱情
和 溶
况
液
蒸发溶剂 增加溶质
室温下含B溶A是是质食食百盐盐的分的不饱比饱和大和溶溶的液液,溶,溶液溶质质叫比比较浓较多溶少。液, 含溶质百分比小的溶液叫稀溶液。
饱和溶液是否一定是浓溶液? 不饱和溶液是否一定是稀溶液?
硝酸钾+水
多
相等 不饱和
浓溶液
少
相等
饱和
稀溶液
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
①
②
③
④
① 3g硝酸钾 ② 0.2g熟石灰 不饱和溶液 饱和溶液
浓溶液
稀溶液
③一匙食盐 ④四匙食盐 不饱和溶液 饱和溶液
稀溶液
浓溶液
结论:
1、对于不同溶质来说,饱和溶液不 一定是浓溶液,不饱和溶液也不一 定是稀溶液。
液,可以采用什么方法?
降温
4.在一定温度下,使固体物质的 饱和溶液变为不饱和溶液最可靠 的方法是入溶剂 C.都采用升高温度的方法
D.都采用降低温度的方法
要解决的问题:
你会了吗?
• 1.什么是饱和溶液? 什么是不饱和溶液?
• 2.饱和溶液一定是浓溶液吗? 不饱和溶液一定是稀溶液吗?
溶剂
溶质
• 1.试管甲盛的是0℃时制备的饱和石灰
水溶液,试管乙盛的是100℃时制备的
饱和石灰水溶液,使两试管都达到
饱和溶液和不饱和溶液教学设计

《饱和溶液、不饱和溶液》教学设计一、设计思想学习饱和溶液、不饱和溶液是为学习溶液溶解度、溶液浓度等基本概念作必要打算。
通过经验“一杯水里能溶解多少白糖”这个探究活动,知道“一杯水里能溶解的白糖是有限的”,初步形成饱和溶液的概念并驾驭饱和溶液与不饱和溶液相互转换的方法。
这既是对前面学问的巩固,也是为学习溶液的溶解度、浓度打下基础的一节课,所以上好这节课至关重要。
先通过试验制取三种蔗糖溶液,分析比较后得出饱和溶液和不饱和溶液的概念,并将这三种蔗糖溶液作为主线贯穿整节课,如饱和溶液和不饱和溶液的推断及转化、饱和溶液与不饱和溶液和浓溶液与稀溶液之间的关系都是从分析这三种溶液中得出的,通过解决真实的实际问题进行概念的学习,可以增加学生的感性相识,帮助学生理解饱和溶液和不饱和溶液的概念,降低学生的学习难度二、教学目标1. 学问与技能理解饱和溶液与不饱和溶液的概念并学会饱和溶液与不饱和溶液相互转化的方法。
2. 过程与方法培育在试验基础上的分析实力和思维实力。
3. 情感看法与价值观养成相互探讨,合作学习,勇于实践的科学精神。
三、重点和难点教学重点:饱和溶液、不饱和溶液概念。
教学难点:饱和溶液、不饱和溶液相互转化。
四、教学用品药品:蔗糖、硝酸钾、食盐、水仪器:大试管或者烧杯、试管夹、酒精灯、50mL烧杯、玻璃棒、10mL量筒、药匙、火柴五、教学案例1. 教学过程(其中蔗糖可以用硝酸钾代替)[设问] 一杯水中是否可以无限地溶解蔗糖呢?学生一:可以;学生二:不行以;演示试验:1、用量筒量取10mL水,分别注入三只烧杯中;2、向三只烧杯中依次加入8克(①)、16克(②)、24克(③)蔗糖,搅拌,视察现象。
学生:沟通试验现象:烧杯①中完全溶解,烧杯②中完全溶解,烧杯③中有部分蔗糖剩余。
小结:一杯水中不行能无限地溶解蔗糖。
设问:溶液①能否接着溶解蔗糖?溶液③能否接着溶解蔗糖?学生:溶液①能接着溶解蔗糖,而溶液③不能接着溶解蔗糖。
饱和溶液和不饱和溶液PPT课件

加入溶质或溶剂对饱和溶液与不饱和溶液的影响
加入溶质
如果加入的溶质能溶于溶剂,则不饱和溶液可能变成饱和溶液;如果加入的溶质不能溶于溶剂,则饱 和溶液可能变成过饱和溶液。
加入溶剂
如果加入的溶剂能与溶质互溶,则饱和溶液和不饱和溶液都可能变得更稀;如果加入的溶剂不能与溶 质互溶,则对溶液的浓度没有影响。Biblioteka 饱和溶液和不饱和溶液的基本概念
饱和溶液
在一定温度和压力下,溶质在溶剂中 达到溶解平衡状态,即溶质无法再溶 解,称为饱和溶液。
不饱和溶液
未达到溶解平衡状态,即溶质可以继 续溶解的溶液,称为不饱和溶液。
02
饱和溶液
饱和溶液的定义
01
饱和溶液是指在一定温度下,当 溶质在溶剂中的溶解度达到最大 值时,溶液达到平衡状态,不能 再溶解更多的溶质。
VS
实验原理
饱和溶液是指在一定温度下,溶质在溶剂 中达到动态平衡的状态,此时溶质无法继 续溶解;不饱和溶液则是指溶质仍可继续 溶解的状态。
实验步骤和实验过程
01
准备实验器材:烧杯、 玻璃棒、温度计、食盐、 水。
02
在室温下,将食盐加入 烧杯中,加入适量水, 用玻璃棒搅拌至食盐完 全溶解。
03
升高温度至沸腾,继续 加入食盐,观察溶解情 况。
感谢您的观看
THANKS
05
实际应用
在化学工业中的应用
01
02
03
化学反应介质
饱和溶液和不饱和溶液是 许多化学反应的重要介质, 如溶解、沉淀、萃取等。
物质分离提纯
通过控制溶液的饱和度, 可以对混合物进行分离和 提纯,如盐析、重结晶等。
《饱和溶液与不饱和溶液》教学设计

课题2 溶解度一、教学目标:(1)明确饱和溶液与不饱和溶液的概念。
(2)知道饱和溶液与不饱和溶液之间的转化方法。
(3)通过实验理解饱和溶液与不饱和溶液的概念。
(4)初步学会科学探究的方法。
二、教学重点:1、饱和溶液的概念。
2、饱和溶液与不饱和溶液之间的相互转化。
三、教学难点:建立饱和溶液与不饱和溶液的概念。
四、教学过程;(一)大胆猜想:可溶物(蔗糖、食盐)在一定量的水中能够无限制地溶解吗?并说出你的猜想依据?(二)活动天地:观察硝酸钾能否在一定量的水中无限溶解老师演示,学生观察:1.在盛有20ml水的烧杯中,加入5g硝酸钾,充分搅拌。
观察现象。
2.在上述得到的溶液中再加入5g硝酸钾,充分搅拌。
观察现象。
现象:1.硝酸钾固体消失,2.硝酸钾固体有剩余。
结论:硝酸钾在一定量的水中不能无限制的溶解。
(幻灯片)…………不能继续溶解…………的溶液,叫做…………饱和溶液。
师:发问,如果还能继续溶解的溶液就叫做…………生:不饱和溶液。
师:对,叫做不饱和溶液.(幻灯片)…………还能继续溶解…………的溶液,叫做…………不饱和溶液。
现在我们继续研究刚才得到的饱和溶液。
请大家想一想,怎样才能使试管底部剩余的硝酸钾也溶解呢?生:加水。
师;好,那我们就试试。
实验:向其中一支试管中加入适量水,边加边振荡,你观察到了什么现象生:硝酸钾又溶解了。
师:也就是说,溶液可能变成了…………生:不饱和溶液。
师:对,从这里我们可以得出,溶液饱和还是不饱和跟溶剂多少有关,所以我们说饱和溶液时还要加上一个条件“在一定量的溶剂里”。
(幻灯片)…………,在一定量的溶剂里,不能继续溶解…………的溶液,叫做…………饱和溶液。
师:还有没有其他办法,使另一支试管底部的硝酸钾也溶解呢?生:加热。
师:好,加热,那我们就一起加热吧!实验:加热另一支试管,观察到了什么现象?生:硝酸钾又溶解了。
师:这说明溶液的饱和与不饱和还跟什么因素有关?生:跟温度有关。
师:所以,当我们说某种饱和溶液时,一定要指明“在一定的温度下”(幻灯片)在一定的温度下,在一定的溶剂里,不能继续溶解的溶液,叫做…………饱和溶液。
初中化学_第三单元溶液教学设计学情分析教材分析课后反思

饱和溶液与不饱和溶液一、设计思想使教师成为教学活动的组织者,并充分体现学生的主体作用,让学生由学会到会学。
本节课的重点是建立饱和溶液与不饱和溶液的概念,包括三个要点──一定温度、一定量溶剂、某种溶质。
二、活动目标1、知识技能:理解饱和溶液与不饱和溶液的概念;了解两者的转化;了解饱和溶液、不饱和溶液与浓溶液、稀溶液的关系。
2、能力培养:通过探索实验形成饱和溶液与不饱和溶液的概念,培养观察能力和分析推理能力。
3、科学品质:通过学生分组实验,培养实事求是的科学态度和与人合作的精神。
4、科学方法:通过学生分组实验,培养从现象到本质的认识事物的科学方法。
三、活动重点1、通过几组探索性实验活动,建立起饱和溶液与不饱和溶液的概念。
2、通过几组探索性实验活动,培养对比思维的能力。
四、活动难点:对饱和溶液与不饱和溶液转化条件的探索。
五、活动模式:引导──探究──发现。
六、教学过程课前播放活动目标,插入背景音乐,使学生进入学习状态。
(一)创设情境(播放一段青海湖美丽的风景,配音介绍咸水湖的知识,最后提出湖水日益咸化的问题。
)师:请同学们思考一下:向一杯水中加盐,是不是一直变咸?(学生根据已有的生活经验,讨论后说:"不会,盐放多了就不能溶解了。
")师:是这样的吗?生(讨论):不信你试试看。
师:我们一起来做一做,我们不仅用食盐做实验,我们还用另一种物质──硝酸钾来实验。
[投影1](活动一)[活动一]固体在水中能否无限制地溶解[学生实验]依据活动方案一进行学生实验。
(渗透科学方法的教育,培养学生实验探究的意识)[投影2](饱和与不饱和溶液概念的提出)能继续溶解某溶质的溶液叫做不饱和溶液,不能继续溶解某溶质的溶液叫做饱和溶液。
(二)通过实验探究与讨论,学习影响溶液是否达到饱和的因素师:要想让刚才的饱和溶液中剩余的固体溶解,你们有什么好主意?生(讨论):热水中可能溶解得多,水多的时候也能溶解得多。
(这时候有些学生已经开始动手给溶液加热或加水了)[投影3](活动二)[活动二]影响溶液是否达到饱和的因素[学生实验]依据活动方案二进行学生实验。
饱和溶液与不饱和溶液的概念

饱和溶液与不饱和溶液的概念
饱和溶液与不饱和溶液的相互转换的方法有:升高温度、增加溶剂。
大多数物质的溶解度随着温度的升高而增加。
通常,饱和溶液可以转化为不饱和溶液。
提高温度的方法可用于增加溶解度,并将饱和溶液转化为不饱和溶液。
加入溶剂可以将饱和溶液转化为不饱和溶液。
一般将不饱和溶液转化为饱和溶液。
常用的方法有:增加溶质、蒸发溶剂、降低温度。
饱和溶液就是所指在一定温度和压力下,溶剂中所熔化的溶质已超过最大量的溶液。
即为溶质与溶剂碰触时,熔化速度与划出速度成正比的溶液。
溶解度就是所指在一定的温度下,某物质在克溶剂里达至饱和状态时所熔化的克数溶质的量未达至对应的饱和状态的溶液,称为不饱和溶液。
溶质的量少于对应的饱和状态的溶液,称为过饱和溶液。
溶液就是饱和状态还是不饱和,最为关键的就是看看它能够不能溶解更多的溶质,也不是看看溶液的淡或淡,每种物质的溶解度就是不一样的,同一种物质在相同的温度下的溶解度也就是不一样的,有些物质,比如说碳酸钙的溶解度就不大,即使就是碳酸钙的饱和溶液,看上去仍然就是诺伍德的,碳酸钙在8摄氏度时,克水至多就可以熔化0.克。
与碳酸钙恰好相反的就是,有些物质比如说蔗糖的溶解能力就非常大,即使蔗糖的溶液已经很浓了,但是也还不是蔗糖的饱和溶液,蔗糖在20摄氏度时,克水即使就是熔化了克的蔗糖,但是此时的蔗糖溶液仍然不是饱和溶液,因为它还可以熔化更多的蔗糖。
饱和与不饱和溶液课件

溶解过程
总结词
溶解过程是指物质从固态、液态或气态进入溶剂中,形成均一、稳定的溶液的过 程。
详细描述
溶解过程是物质从固态、液态或气态进入溶剂中,形成均一、稳定的溶液的过程 。在这个过程中,溶质和溶剂之间的相互作用力必须大于溶质分子或离子之间的 相互作用力,才能形成溶液。
溶解度的概念
总结词
溶解度是指在一定温度和压力下,一定量的溶剂所能溶解溶质的最大量。
饱和溶液的制备方法
通过增加溶质或蒸发溶剂来制备 饱和溶液。
在一定温度和压力下,持续搅拌 溶质和溶剂,直到达到溶解平衡
。
通过结晶法,将过饱和溶液冷却 或加入晶种来促使溶质结晶,从
而制备饱和溶液。
饱和溶液的应用
在化学实验中,饱和溶液常用于制备晶体、分离和提纯物质等。
在工业生产中,饱和溶液可用于提取和分离有价值的物质,如从矿石中提取金属等 。
不饱和溶液的应用
总结词
不饱和溶液在化学实验、工业生产、农业等领域有广泛应用。
详细描述
在化学实验中,不饱和溶液常用于溶解、结晶、萃取等操作;在工业生产中,不饱和溶液可用于提取 、分离、纯化等过程;在农业中,不饱和溶液可用于植物施肥、农药换
增加溶质的方法
总结词
增加溶质可以使不饱和溶液变为饱和 溶液。
02
溶解平衡是指溶质在溶液中的溶 解和结晶过程达到动态平衡的状 态,此时溶液中溶质的浓度达到 最大值。
饱和溶液的特点
饱和溶液中溶质浓度达到最大 值,无法继续溶解。
饱和溶液的溶解平衡是动态的 ,结晶和溶解过程不断进行, 但速率相等。
饱和溶液的温度和压力与其组 成有关,改变温度或压力会影 响溶解平衡和溶质浓度。
改变温度的方法
饱和溶液和不饱和溶液(改)

继续溶解 溶液下部有固体
物质在水中不能无限制 地溶解
剩余固体逐渐溶解 加水可变为不饱和溶液 剩余固体逐渐溶解 加热可变为不饱和溶液
【注意】只有指明“一定温度”、“一定量溶剂”
里,饱和溶液不饱和溶液才有意义。
【思考 】如何把硫酸升温
③蒸发水 ②加溶质 ① 降温
【验证实验 】
溶解,溶液呈蓝色
在一定的条件下,某 继续溶解 种物质在水中不能无 溶液下部有固体 限制地溶解
不饱和溶液:在一定温度下,一定量溶剂里还能继续 溶解某种溶质的溶液叫这种溶质的不饱和溶液。
饱和溶液:在一定温度下,一定量溶剂里不能再继续 溶解某种溶质的溶液叫这种溶质的饱和溶液。
溶解变成蓝色溶液在一定的条件下,某种
溶解度注意点:
条件:一定温度下 标准:100克溶剂(一般为水) 状态:达到饱和状态 单位:克/100克溶剂(一般为克/100克水)
溶解度值越大,表明该温度下,物质的溶解能力越强。
1、“20℃时,硝酸钾的溶解度是31.6g/100g水”。这句话 的含义: 20℃时,在100克水中溶解31.6克硝酸钾达到饱和状态 此时,饱和溶液 溶质 31.6 131.6 克, 克。
【故 事】冲糖水的故事
女孩:“妈妈,我要喝糖开水。”
(妈妈将一玻璃杯放在桌上,向玻璃杯中倒水,然后向其 中加两勺糖,搅拌,糖全部溶解;又取了一勺糖放入杯中, 搅拌,杯底有糖剩余。) 女孩:“妈妈,再加点糖吧~” 妈妈:“已经很甜了,再加也不会更甜了。” 女孩:“为什么呀?”
【问题】:某种物质在水中能无限制地溶解吗? 【猜测】:不能无限制地溶解
不饱和 溶液
简答 1、将饱和的硝酸钾溶液转化成不饱和溶液, 可采取什么方法? 加水、升高温度
初中九年级化学教案饱和溶液和不饱和溶液(教案)

课题2 溶解度课题分析本课题分为饱与溶液与不饱与溶液与溶解度两部分。
第一部分通过实验导入饱与溶液地概念,并由学生讨论分析理解饱与溶液地两个条件,判断某物质地溶液是否饱与,最后分析总结出饱与溶液与不饱与溶液相互转化地条件。
第二部分通过讨论与探究导入溶解度地概念,理解溶解度地相对大小,再以活动与探究绘制溶解度曲线,巩固与应用溶解度概念,最后又讨论引出了气体溶解度地概念。
第1课时饱与溶液与不饱与溶液课标要求教学目的】1.知识与技能(1)理解饱与溶液与不饱与溶液地意义。
(2)通过实验探究,建立饱与溶液与不饱与溶液地概念。
(3)了解饱与溶液与不饱与溶液地相互转化地方法。
(4)了解结晶现象。
2.过程与方法运用科学探究地方法理解饱与溶液与不饱与溶液地意义,并通过实验探究了解“饱与”与“不饱与”地相对性。
3.情感态度与价值观通过实验条件地改变,让学生感受饱与溶液与不饱与溶液地存在与转化是有条件地,逐步建立用辨证地,发展地思想观点来看待事物地变化,与逐步培养由具体到一般认识过程地能力,并培养学生互相协作,友好相处地健康心态。
教学重点】1.理解饱与溶液与不饱与溶液地概念。
2.理解饱与溶液与不饱与溶液相互转化地方法。
教学难点】1.理解饱与溶液与不饱与溶液地概念。
2.正确理解饱与溶液与不饱与溶液相互转化地方法。
教具准备】水,氯化钠固体,硝酸钾固体,烧杯(若干),多媒体课件,玻璃棒,酒精灯,铁架台,石棉网等。
教学过程复习提问】通过上节课地学习我们知道,不同物质在同一溶剂中,溶解性不同;同一物质在不同溶剂中,溶解性也不同。
那么一种物质在一种溶剂中能否无限溶解下去呢?活动与探究1】实验9-5进行实验,并记录实验现象。
请同学们按P33交流现象】由一组同学描述现象,结论,其它各组提出异议。
分析小结】实验现象:第一次地5g氯化钠都溶解了 ;第二次地5g氯化钠不能全部溶解;加人15mL水后剩余地氯化钠固体又溶解了。
活动与探究2】实验9-6进行实验,并记录实验现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三单元溶液
溶液的形成(第三课时)饱和溶液与不饱和溶液
【学习目标】
1、认识饱和溶液和不饱和溶液。
2、知道饱和溶液与不饱和溶液相互转化的条件。
【自主学习、探究释疑】
学习任务一:阅读教材P62——P63内容,认真操作活动天地的探究实验,仔细观察,认真分析。
解决下列问题:
1、思考:一定量的水里能不能无限的溶解硝酸钾呢?
交流和总结:
2、饱和溶液:
3、不饱和溶液:
交流和总结:
1、你怎样判断硝酸钾溶液是否达到饱和状态?
2、在描述饱和溶液与不饱和溶液时为什么一定要指明“一定温度”和“一定量溶剂”呢?
3、浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液,对吗?
学习任务二:认真完成63页的实验探究,回答下列问题:
1、饱和溶液转化成不饱和溶液有哪些方法?
2、不饱和溶液转化成饱和溶液有哪些方法?
3、其它条件不变,降低温度不饱和溶液一定就可以转化成饱和溶液吗?为什么?
4、讨论饱和溶液与不饱和溶液相互转化时哪些条件能对溶质溶解有影响?
【达标练习】
1.欲使任意一种不饱和溶液转变为饱和溶液.最可靠且简便的方法是( )
A.改变温度
B.蒸发溶剂
C.加溶质
D.倒出一些溶液
2.在一个大萝卜上挖个孔,向其中注入饱和的食盐水,然后倒出。
在相同的温度下,发现倒出的溶液还能溶解少量的食盐,这说明倒出的溶液
A.是饱和溶液
B.是不饱和溶液
C.氯化钠的溶解度升高
D.氯化钠的溶解度降低
3、在一定温度下,某物质的饱和溶液一定()
A、很浓的溶液
B、含100g水的溶液
C、不能再溶解该物质的溶液
D、含100g该物质的溶液
4、下列说法正确的是()
A、浓溶液一定是饱和溶液
B、稀溶液一定是不饱和溶液
C、不论在什么温度下,一杯杯底有食盐固体不能再溶解的食盐水,一定是该温度下的
饱和溶液
D、某一温度下一杯杯底有蔗糖固体的蔗糖水,在任何温度下都是饱和溶液
5、可以证明烧杯中的溶液是硝酸钾饱和溶液的方法是()
A、蒸发1g水,有少量固体析出
B、降低温度,有少量固体析出
C、加入少量硝酸钾固体,固体不再溶解
D、升高温度,没有固体析出
6、室温下,向一定质量的氯化钠溶液中加入10g氯化钠固体,充分搅拌后,尚有部分固体未溶解。
再加入10g水后,固体全部溶解,下列判断正确的是()
A、加水前一定是饱和溶液
B、加水前可能是饱和溶液
C、加水后一定是饱和溶液
D、加水后一定是不饱和溶液
7、在室温下,将下列物质足量混合并充分振荡,肯定不能形成饱和溶液的是()
A、氯化钠与水
B、硫酸铜与水
C、酒精与水
D、植物油与水
【课后拓展】
一实心球悬浮在KNO3的不饱和溶液中,你有哪些方法使它浮上来?并用学过的理化知识解释这些方法。
