不同标准溶液浓度的温度补正值(以MLLJI计)
标准溶液温度体积校正值
不同温度下标准滴定溶液的体积的补正值

+1.1
+4.2
+0.50 +0.6 +0.6
+0.6
+0.7
+0.8
+0.8
+3.1
+0.34 0.4 +0.4
+0.4
+0.5
+0.6
+0.6
+2.1
+0.18 +0.2 +0.2
+0.2
+0.2
+0.3
+0.3
+1.0
0.00
0.00 0.00
0.0
0.0
0.0
0.0
0.0
-0.18 -0.2 -0.2
-2.6
-2.8
-3.2
-3.1
-10.6
31
-2.58 -2.7 -2.7
32
-2.86 -3.0 -3.0
33
-3.04 -3.2 -3.3
34
-3.47 -3.7 -3.6
35
-3.78 -4.0 -4.0
36
-4.10 -4.3 -4.3
-2.9
-3.1
-3.5
-3.2
-3.4
-3.9
-3.5
+1.38
0.1mol/l 和
0.2mol/l 以下的 各种水 溶液
+1.7
盐酸溶液 c(HCl)=0.5mol /l
+1.9
盐酸溶液 c(HCl)=1m ol/l
+2.3
硫酸溶液 硫 酸 溶 液
c(1/2H2SO4 c(1/2H2SO4)=1 )=0.5mol/l, mol/l,氢氧化钠
(完整word版)不同温度下标准滴定溶液的体积的补正值.doc
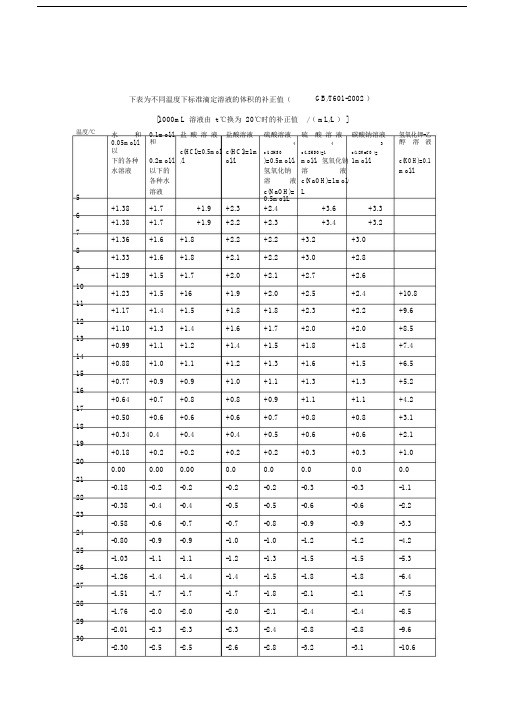
温度/℃56789101112131415161718192021222324252627282930下表为不同温度下标准滴定溶液的体积的补正值(GB/T601-2002 )[1000mL 溶液由 t ℃换为 20℃时的补正值/( mL/L ) ]水和0.1mol/l 盐酸溶液盐酸溶液硫酸溶液硫酸溶液碳酸钠溶液氢氧化钾-乙0.05mol/l以和c(HCl)=0.5mol c(HCl)=1m4 4 3 醇溶液c(1/2HSO c(1/2HSO)=1 c(1/2NaCO )=下的各种0.2mol/l /l ol/l )=0.5mol/l,mol/l,氢氧化钠1mol/l c(KOH)=0.1 水溶液以下的氢氧化钠溶液mol/l 各种水溶液c(NaOH)=1mol/溶液c(NaOH)= L+1.38 +1.7 +1.9 +2.30.5mol/L+3.6 +3.3+2.4+1.38 +1.7 +1.9 +2.2 +2.3 +3.4 +3.2+1.36 +1.6 +1.8 +2.2 +2.2 +3.2 +3.0+1.33 +1.6 +1.8 +2.1 +2.2 +3.0 +2.8+1.29 +1.5 +1.7 +2.0 +2.1 +2.7 +2.6+1.23 +1.5 +16 +1.9 +2.0 +2.5 +2.4 +10.8+1.17 +1.4 +1.5 +1.8 +1.8 +2.3 +2.2 +9.6+1.10 +1.3 +1.4 +1.6 +1.7 +2.0 +2.0 +8.5+0.99 +1.1 +1.2 +1.4 +1.5 +1.8 +1.8 +7.4+0.88 +1.0 +1.1 +1.2 +1.3 +1.6 +1.5 +6.5+0.77 +0.9 +0.9 +1.0 +1.1 +1.3 +1.3 +5.2+0.64 +0.7 +0.8 +0.8 +0.9 +1.1 +1.1 +4.2+0.50 +0.6 +0.6 +0.6 +0.7 +0.8 +0.8 +3.1+0.34 0.4 +0.4 +0.4 +0.5 +0.6 +0.6 +2.1+0.18 +0.2 +0.2 +0.2 +0.2 +0.3 +0.3 +1.00.00 0.00 0.00 0.0 0.0 0.0 0.0 0.0-0.18 -0.2 -0.2 -0.2 -0.2 -0.3 -0.3 -1.1-0.38 -0.4 -0.4 -0.5 -0.5 -0.6 -0.6 -2.2-0.58 -0.6 -0.7 -0.7 -0.8 -0.9 -0.9 -3.3-0.80 -0.9 -0.9 -1.0 -1.0 -1.2 -1.2 -4.2-1.03 -1.1 -1.1 -1.2 -1.3 -1.5 -1.5 -5.3-1.26 -1.4 -1.4 -1.4 -1.5 -1.8 -1.8 -6.4-1.51 -1.7 -1.7 -1.7 -1.8 -2.1 -2.1 -7.5-1.76 -2.0 -2.0 -2.0 -2.1 -2.4 -2.4 -8.5-2.01 -2.3 -2.3 -2.3 -2.4 -2.8 -2.8 -9.6-2.30 -2.5 -2.5 -2.6 -2.8 -3.2 -3.1 -10.631 -2.58 -2.7 -2.7 -2.9 -3.1 -3.5 -11.632 -2.86 -3.0 -3.0 -3.2 -3.4 -3.9 -12.633 -3.04 -3.2 -3.3 -3.5 -3.7 -4.2 -13.734 -3.47 -3.7 -3.6 -3.8 -4.1 -4.6 -14.835 -3.78 -4.0 -4.0 -4.1 -4.4 -5.0 -16.036 -4.10 -4.3 -4.3 -4.4 -4.7 -5.3 -17.0注: 1 .本表数值是以20 ℃为标准温度以实测法测出。
(完整word版)不同温度下标准滴定溶液的体积的补正值
+1.36
+1.6
+1.8
+2.2
+2.2
+3.2
+3.0
8
+1.33
+1.6
+1.8
+2.1
+2.2
+3.0
+2.8
9
+1.29
+1.5
+1.7
+2.0
+2.1
+2.7
+2.6
10
+1.23
+1.5
+16
+1.9
+2.0
+2.5
+2.4
+10.8
11
+1.17
+1.4
+1.5
+1.8
+1.8
+2.3
+2.2
+9.6
12
+1.10
+1.3
+1.4
+1.6
+1.7
+2.0
+2.0
+8.5
13
+0.99
+1.1
+1.2
+1.4
+1.5
+1.8
+1.8
+7.4
14
+0.88
+1.0
+1.1
+1.2
+1.3
+1.6
+1.5
+6.5
溶液温度校正值计算公式

溶液温度校正值计算公式引言:在科学研究和实验中,温度是一个重要的参数,对于溶液的浓度测量也是至关重要的。
然而,溶液的浓度在不同的温度下可能会发生变化,因此需要进行温度校正。
本文将介绍一种常用的溶液温度校正值计算公式,以帮助读者更好地理解和应用这一概念。
一、温度校正的背景和意义在实验室中,我们经常需要测量溶液的浓度。
然而,溶液的浓度在不同的温度下会发生变化,这是由于温度对溶液中化学物质的溶解度有影响。
为了保证浓度测量的准确性,我们需要进行温度校正。
温度校正是通过计算溶液温度校正值来修正浓度的方法,以确保在不同温度下获得准确的浓度值。
二、溶液温度校正值计算公式溶液温度校正值的计算公式如下:温度校正值 = (测量浓度 - 校正浓度) / 校正因子其中,测量浓度是在实验中测得的溶液浓度,校正浓度是在标准温度下测得的溶液浓度,校正因子是校正浓度与标准温度下的溶液浓度之间的比例关系。
三、温度校正值计算示例为了更好地理解温度校正值的计算过程,我们来看一个实际的示例。
假设我们在实验室中测得某溶液在25摄氏度下的浓度为2mol/L,而在标准温度下(通常为20摄氏度)的浓度为1.8mol/L。
校正因子为0.9。
那么,我们可以使用上述公式计算出温度校正值:温度校正值 = (2 - 1.8) / 0.9 = 0.2 / 0.9 ≈ 0.222mol/L因此,校正后的溶液浓度为1.8 + 0.222 ≈ 2.022mol/L。
四、温度校正值的应用温度校正值可以用于各种实验和应用中,特别是在需要准确测量溶液浓度的情况下。
通过使用温度校正值,我们可以消除温度对浓度测量的影响,从而获得更准确的结果。
在实际应用中,温度校正值可以应用于各种溶液浓度测量的方法,如比色法、光谱法和电化学法等。
通过在测量过程中考虑温度校正值,可以提高浓度测量的准确性和可靠性。
五、总结温度校正是保证溶液浓度测量准确性的重要步骤。
通过使用溶液温度校正值计算公式,我们可以修正温度对浓度测量的影响,从而获得更准确的结果。
(完整word版)不同温度下标准滴定溶液的体积的补正值
-13.7
34
—3.47
—3.7
-3.6
—3。8
—4。1
—4.6
—14。8
35
—3。78
-4。0
—4。0
-4。1
-4。4
—5.0
—16.0
36
-4。10
—4。3
—4.3
-4.4
—4.7
—5.3
—17.0
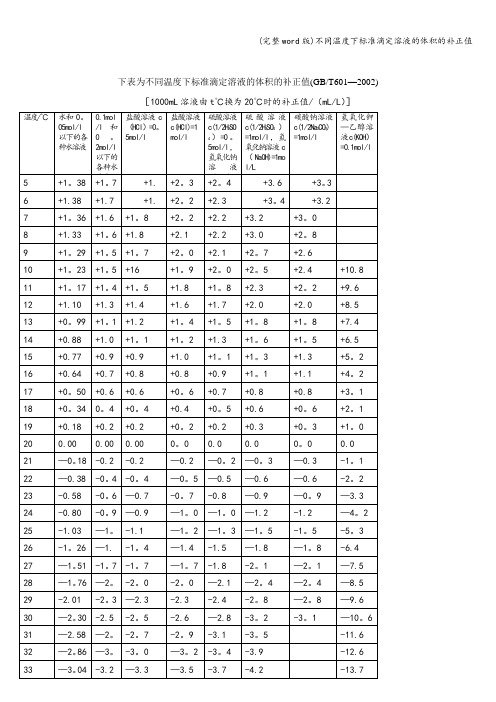
注: 1 .本表数值是以20 ℃为标准温度以实测法测出。
2 .表中带有“ + ”、“-”号的数值是以20 ℃为分界.室温低于20 ℃的补正值为“ + ” ,高于20 ℃的补正值为“—"。
-2。3
—2.3
-2.3
-2.4
-2。8
—2。8
—9.6
30
—2。30
-2.5
-2。5
-2.6
—2.8
-3。2
-3。1
—10。6
31
—2.58
—2。7
-2。7
-2。9
-3.1
-3。5
-11.6
32
—2。86
—3。0
-3。0
—3。2
-3。4
-3.9
-12.6
33
—3。04
-3.2
—3.3
—3.5
-3.7
硫酸溶液c(1/2H2SO4)=1mol/l,氢氧化钠溶液c(NaOH)=1mol/L
碳酸钠溶液c(1/2Na2CO3)=1mol/l
氢氧化钾—乙醇溶液c(KOH)=0.1mol/l
5
+1。38
+1。7
+1.9
+2。3
+2。4
常用标准溶液的配制

容量标准溶液的配制凡制备的标准溶液的浓度均指20℃时的浓度。
在标定和使用时,如温度有差异,应按附表[不同标准溶液浓度的温度补正值(以ml/L计)]补正。
“标定”或“比较”标准溶液浓度时,平行试验不得少于八次,两人各作四平行,每人四平行测定结果的极差与平均值之比不得大于0.1%,两人测定结果平均值之差不得大于0.1%,结果取平均值.浓度值取四位有效数字.凡规定用”标定”和”比较”两种方法测定浓度时,不得略去其中任何一种,且两种方法测得的浓度值之差不得大于0.2%,以标定结果为准.制备的标准溶液浓度与规定浓度相对误差不得大于5%.配制浓度等于或低于0.02mol/L标准溶液时,应于临用前将浓度高的标准溶液用煮沸并冷却的水稀释,必要时重新标定.碘量法反应时,溶液的温度不能过高,一般在15--20℃之间进行滴定.滴定分析(容量分析)用标准溶液在常温(15--20℃)下,保存时间一般不得超过两个月.1.氢氧化钠标准滴定溶液[c(NaOH)=1mol/L、0.5mol/L、及0.1mol/L](1)配制称取100g氢氧化钠,溶于100ml水中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮,使用前以塑料管虹吸上层清液(饱和氢氧化钠溶液).氢氧化钠标准滴定溶液[c(NaOH)=1mol/L]:量取52ml饱和氢氧化钠溶液,注于1000ml新经煮沸并冷却的水中,摇匀.氢氧化钠标准滴定溶液[c(NaOH)=0.5mol/L]:量取26ml饱和氢氧化钠溶液,注于1000ml新经煮沸并冷却的水中,摇匀.氢氧化钠标准滴定溶液[c(NaOH)=0.25mol/L]:量取13ml饱和氢氧化钠溶液,注于1000ml新经煮沸并冷却的水中,摇匀.氢氧化钠标准滴定溶液[c(NaOH)=0.1mol/L]:量取5ml饱和氢氧化钠溶液,注于1000ml新经煮沸并冷却的水中,摇匀.(2)标定(i)测定方法:氢氧化钠标准滴定溶液[c(NaOH)=1mol/L]:称取6g于105--110℃烘至恒重的基准邻苯二甲酸氢钾(精确至0.0001g).溶于80ml新经煮沸并冷却的水中,加2滴酚酞指示液(10g/L),用氢氧化钠标准滴定溶液[c(NaOH)=1mol/L]滴定至溶液呈粉红色,同时作空白试验.氢氧化钠标准滴定溶液[c(NaOH)=0.5mol/L]:称取3g于105--110℃烘至恒重的基准邻苯二甲酸氢钾(精确至0.0001g).溶于80ml新经煮沸并冷却的水中,加2滴酚酞指示液(10g/L),用氢氧化钠标准滴定溶液[c(NaOH)=0.5mol/L]滴定至溶液呈粉红色,同时作空白试验.氢氧化钠标准滴定溶液[c(NaOH)=0.25mol/L]:称取1.5g于105--110℃烘至恒重的基准邻苯二甲酸氢钾(精确至0.0001g).溶于60mL新经煮沸并冷却的水中,加2滴酚酞指示液(10g/L),用氢氧化钠标准滴定溶液[c(NaOH)=0.25mol/L]滴定至溶液呈粉红色,同时作空白试验.氢氧化钠标准滴定溶液[c(NaOH)=0.1mol/L]:称取0.6g于105--110℃烘至恒重的基准邻苯二甲酸氢钾(精确至0.0001g).溶于50ml新经煮沸并冷却的水中,加2滴酚酞指示液(10g/L),用氢氧化钠标准滴定溶液[c(NaOH)=0.1mol/L]滴定至溶液呈粉红色,同时作空白试验.(ii)计算:mc(NaOH)=(V1-V2)×0.2042式中V1—滴定邻荐二甲酸氢钾耗用氢氧化钠标准滴定溶液的体积,ml;V2—空白试验耗用氢氧化钠标准滴定溶液的体积,ml;m---邻苯二甲酸氢钾质量,g;c(NaOH)--氢氧化钠标准滴定溶液之物质的量浓度,mol/L;0.2042—与1.00ml氢氧化钠标准滴定溶液[c(NaOH)=1000mol/L]相当的以克表示的邻苯二甲酸氢钾的质量。
