007 生物指示剂试验记录
洁净区(间)空气消毒效果及周期验证

—验证文件—工艺验证文件名称: 洁净室(区)空气消毒效果及周期再验证文件编号: SX/YZ6.4-06版本号: 2013版本编制: 日期:年月日审核: 日期:年月日批准: 日期:年月日实用标准文案目录1概述 (1)2验证目的 (1)3验证范围 (1)4验证方案制定的依据 (1)5验证人员职责分工 (1)6验证仪器设备 (2)6.1验证所需仪器设备仪表 (2)6.2仪器仪表校验记录确认 (2)7验证材料 (2)7.1材料的选取 (2)7.2材料的用量 (2)7.3材料的主要用途 (2)7.4材料的确认 (2)8验证方法 (2)8.1熏蒸消毒方法 (2)8.2熏蒸参数 (3)8.3熏蒸时间周期 (3)8.4生物指示剂试验方法 (3)8.5物体表面菌试验方法 (4)8.6沉降菌试验方法 (4)9验证环境 (4)9.1无菌实验室检测环境确认 (4)9.2洁净车间环境确认 (5)9.3洁净车间的清洁 (5)10验证检测 (5)10.1生物指示剂检测 (5)10.2物体表面菌检测 (5)10.3沉降菌检测 (5)10.4 验证标准 (6)11验证结果的综合评价 (6)12 再验证周期 (6)目录附件1 人员资格确认表附件2 计量器具确认记录附件3 洁净车间空气消毒剂的确认记录附件4 洁净车间空气消毒剂的确认记录附件5 洁净车间熏蒸消毒方法确认记录附件6 消毒试验方法确认记录附件7 检测环境确认报告附件8 生物指示剂检测记录附件9 洁净车间消毒后物体表面菌检测记录附件10 洁净室消毒30天后物体表面菌检测记录附件11 洁净车间消毒后沉降菌检测记录附件12 洁净车间消毒后30天沉降菌检测记录附件13 验证结果附件14 验证结果分析及评价附件15 验证结论附件16 验证报告附件17 验证证书天台县双星医疗器械厂编号SX/YZ6.4-06洁净室(区)空气消毒效果及周期再验证版本2013验证方案页数第1页共6页1概述甲醛是常用的消毒剂,其3~5%的水溶液或乙醇溶液能破坏细菌繁殖体及许多芽孢、真菌和病毒,使其蛋白质、酶类变性。
生物实验流程记录单

生物实验流程记录单下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by the editor. I hope that after you download them, they can help yousolve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, our shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts,other materials and so on, want to know different data formats and writing methods, please pay attention!在生物学研究中,实验流程记录单是极为重要的工具,它用于记录实验过程中的关键步骤和结果,有助于研究人员追溯和分析实验数据。
生物指示剂挑战性实验记录140g

生物指示剂挑战性实验记录检验依据:《臭氧发生系统验证》O3-V-VP-01一、实验器具:二、实验方法:1、测试前的准备工作:1.1将JK401机组新风阀关闭,启动风机运行,设定频率在40HZ;1.2四楼洁净区卫生已清洁完毕,岗位已在无人状态下,并且洁净区的温度<24℃,相对湿度>70%(臭氧消毒所需温湿度条件);1.3检查洁净区内应无暴露的物料、中间产品、成品和易被臭氧氧化、腐蚀的橡胶、塑料等制品,应采取防护措施,防止臭氧氧化破坏;1.4按臭氧发生系统操作规程操作。
检查并全开臭氧发生器中的O3出气阀门和冷却水出水阀门,以保证O3气体出气和冷却水排放全部畅通;1.5检查臭氧发生器的冷却水进水压力和进水温度,应控制进水温度<35℃,进水压力0.1~0.3MPa,打开HVAC机组和臭氧发生器的冷却水进水控制阀门;1.6检查臭氧发生单元的“电流调节”按钮,并应使其在最小处(mix),相对应的电流表应显示为0;1.7接通臭氧发生系统电源,“富氧关”按钮上的红灯指示灯应正确显示(亮),电源电压应正常显示(220V);1.8将臭氧发生器的时间设定为3.5H,以免在测试不同杀菌时间与杀菌率关系时,造成自动停机;1.9在药检中心无菌室内超净工作台上,将枯草芽胞杆菌黑色变种芽胞菌片放置于无菌培养皿(无培养基)中,每个培养皿放置1片,共放 7 个培养皿(培养皿应预先进行编号,以确定杀菌时间),盖上平皿盖,用牛皮纸包扎好;2、杀菌实验:2.1将包扎好的枯草芽胞杆菌黑色变种芽胞菌片培养皿,通过传递窗传入洁净区,放置在内包间正中央地面上;2.2全部移开平皿盖(注意防止对培养基平皿污染),人员撤离出洁净区,准备臭氧消毒;2.3按下绿色“富氧开”启动按钮,“富氧开”绿色按钮指示灯亮,相应的“富氧关”红色按钮指示灯灭,“臭氧关”红色按钮指示灯亮,“时间定时器”通电开始计时;2.4打开外接压缩空气阀门,调节并控制气源静态压力应≤0.25MPa(气源静态压力是指臭氧发生单元未工作时,压缩空气压力。
七年级下册生物实验七年级生物上实验记录

七年级下册生物实验七年级生物上实验记录蚯蚓的运动目的要求:1、设置一个适于蚯蚓生存的环境并饲养蚯蚓。
2、观察蚯蚓的外部形态,3、观察蚯蚓的运动。
教学用具蚯蚓、蜗牛、蚯蚓横切片、显微镜、硬纸板、玻璃板实验过程:(1)分组实验:给出学生实验用具,自己设计实验,观察蚯蚓的运动方式特点,以其运动与身体结构的关系。
将蚯蚓放在硬纸板上,观察它的运动。
当蚯蚓运动时,它的身体形状发生什么变化?把耳朵贴近蚯蚓仔细地听,能听到声音吗?用手摸一摸蚯蚓的身体表面,有什么感觉?用放大镜观察蚯蚓身体的每一节,会发现有什么结构?将蚯蚓放在玻璃板上,观察它的运动速度与在硬纸板上是否一样?这时能否听到声音?将观察到的结果填入下表,并分析其原因。
(2)按照课本上给出的程序进行实验,得出实验结论。
前进的距离(cm)蠕动次数/分钟1分钟2分钟3分钟1cm2cm3cm在硬纸板上1cm1cm1cm在玻璃板上蚯蚓在粗糙的纸板上爬行,可听到轻微的沙沙声,这是蚯蚓体表的刚毛与纸板磨擦发出的声音。
刚毛在运动中起支撑和结果及分析固定身体的作用。
当蚯蚓在玻璃板上时只见它的身体在蠕动,变粗变细,却不能前进,这是因为玻璃的表面光滑摩擦力小刚毛无法固定支撑身体。
实验说明刚毛有协助运动的作用(3)在显微镜下观察蚯蚓的横切片,对照图4-2-1,观察蚯蚓体壁上的环形肌和纵肌,并分析蚯蚓在运动时,身体的变化及运动产生的原因。
总结归纳:动物之所以能够运动并能做出各种复杂的动作,都与自身的形态结构密切相关。
蚯蚓通过体壁内的肌肉交替收缩和舒张,并与刚毛的伸缩相互配合在土壤中蠕动。
练习使用显微镜目的要求:1.练习使用显微镜,学会规范的操作方法。
2.能够独立操作显微镜。
3.能够将标本移动到视野中央,并看到清晰的图象。
材料用具:显微镜,写有“上”字的玻片,动、植物玻片标本,擦镜纸,纱布。
方法步骤1.右手握住镜臂,左手托住镜座。
2.把显微镜放在实验台距边缘7厘米左右处,略偏左。
微生物限度检验记录

微生物限度检验记录一、检验目的:确认产品是否满足微生物限度要求,保证产品的安全性和质量。
二、检验项目:1.总大肠菌群:用于评估产品是否受到粪便污染。
2.霉菌和酵母菌:用于评估产品是否受到霉菌和酵母菌的污染。
3.沙门氏菌:用于评估产品是否受到沙门氏菌的污染,沙门氏菌是一种常见的食源性病原菌。
4.铜绿假单胞菌:用于评估产品是否受到铜绿假单胞菌的污染,铜绿假单胞菌是一种常见的致病菌。
5.谷氨酰胺酶阳性菌:用于评估产品是否受到谷氨酰胺酶阳性菌的污染,谷氨酰胺酶阳性菌是一种常见的致病菌。
三、检验步骤:1.样品准备:从产品中取得一定量的样品,确保样品的代表性。
2.样品处理:根据产品的不同特性,选择适当的方法进行样品处理,如水解、稀释等。
3.培养基制备:根据所需的检验项目,制备相应的培养基。
4.培养基接种:将处理后的样品接种到相应的培养基中,利用无菌技术确保操作的无菌。
5.培养:将接种过的培养基培养在适宜的温度和湿度条件下,培养一定的时间,一般为24-72小时。
6.检查结果:观察培养基上是否有菌落形成,记录菌落的数量和形态特征。
7.鉴定:对培养出的菌落进行进一步的鉴定,如形态学观察、生理生化特性测试等。
8.统计和分析:根据检查结果,统计并分析微生物的数量,计算出产品的微生物限度。
四、检验结果:1.总大肠菌群:每克不超过100个。
2.霉菌和酵母菌:每克不超过10个。
3.沙门氏菌:每克不得检出。
4.铜绿假单胞菌:每克不得检出。
5.谷氨酰胺酶阳性菌:每克不得检出。
五、检验记录样例:日期:2024年4月1日样品名称:XXX产品检验员:XXX检验项目:1.总大肠菌群结果:每克10个,符合微生物限度要求。
2.霉菌和酵母菌结果:每克2个,符合微生物限度要求。
3.沙门氏菌结果:未检出,符合微生物限度要求。
4.铜绿假单胞菌结果:未检出,符合微生物限度要求。
5.谷氨酰胺酶阳性菌结果:未检出,符合微生物限度要求。
六、结论:根据检验结果,XXX产品符合微生物限度要求,产品安全可靠。
生物实验室使用记录

11.7
2.4
叶绿体中色素的提取和分离
烧杯、研钵、小玻璃漏斗、尼龙布、毛细吸管、剪刀、小试管、天平等
新鲜的绿色叶片、丙酮、层析液、二氧化硅、碳酸钙
损坏3根毛细吸管
11.18
3.4
学习微生物培养的基本技术
天平、药勺、200mL的烧杯、试管、漏斗、量筒、玻璃棒、滴管、胶管、三脚架
质量浓度为03g/mL的蔗糖溶液、清水
11.24
2.4
观察植物细胞的质壁分离与复原
刀片、镊子、滴管、载玻片、盖玻片、吸水纸、显微镜
质量浓度为03g/mL的蔗糖溶液、清水
11.25
2.3
观察植物细胞的质壁分离与复原
刀片、镊子、滴管、载玻片、盖玻片、吸水纸、显微镜
质量浓度为03g/mL的蔗糖溶液、清水
生物实验室使用记录
10.18
2.4
比较H2O2酶和Fe3+的催化效率
试管、大烧杯、量筒、滴管、温度计、试管架、试管夹、三脚架、石棉网
质量分数为20%的淀粉酶溶液、质量分数为3%的可溶性淀粉溶液、质量分数为3%的蔗糖溶液
10.19
2.5
比较H2O2酶和Fe3+的催化效率
试管、大烧杯、量筒、滴管、温度计、试管架、试管夹、三脚架、石棉网
斐林试剂、苏丹Ⅲ/Ⅳ染液、双缩脲试剂、苹果、花生种子、生鸡蛋等
损坏两支试管
9.9
2.5
生物组织中还原糖、脂肪、蛋白质的鉴定
剪刀、解剖刀、双面刀片、试管、试管夹、大、小烧杯、火柴、毛笔等
斐林试剂、苏丹Ⅲ/Ⅳ染液、双缩脲试剂、苹果、花生种子、生鸡蛋等
9.10
2.3
生物组织中还原糖、脂肪、蛋白质的鉴定
灭菌方法与生物指示剂

❖ 化学指示剂验证:物品包外用化学指示剂用于验证物品是 否经过灭菌处理,物品包内中心部位的化学指示剂才可作 为物品是否达到灭菌的参考标志。
❖ 生物指示剂验证:将已知其耐热性的生物指示剂直接接种 在产品溶液或相似溶液中进行验证, 是评判灭菌工艺杀灭 效果最直观有效的方法, 也是灭菌工艺验证必不可少的试 验。
生孢梭菌孢子 Clostridium sporogenes
枯草芽孢杆菌 Bacillus subtilis
保藏号
NCTC 10007 NCIMB 8157 ATCC 7953
NCTC 8594 NCIMB 8053 ATCC 7955
NCIMB 8058 ATCC 9372
短小芽孢杆菌 Bacillus pumilus
置于放射剂量25kGy条件下,D值约3kGy。
harmony
过滤除菌法
系利用细菌不能通过致密具孔滤材的原理以 除去气体或液体中微生物的方法。
适用范围:
对热不稳定的药物溶液、气体、水或原料的除菌。
harmony
常用生物指示剂
➢ 滤膜孔径为0.22μm的滤器 :缺陷假单胞菌 (Pseudomonas diminuta, 如ATCC19 146)
无菌保证水平 一批物品的无菌特性只能相对地通过物品中活微 生物的概率低至某个可接受水平来表述,即SAL (sterility assurance level)。
我国及欧美药典都把SAL不得大于百万分之一 作为最终灭菌产品无菌保证的要求,即 SAL≤10-6
harmony
灭菌工艺验证
❖ 验证一个灭菌工艺系统能否使产品灭菌后达到无菌要求, 通常认为灭菌后微生物残存概率小于1×10-6。
灭菌设备的灭菌效果验证记录(湿热生物指示剂法).

灭菌设备的
灭菌效果验证记录
方法:生物指示剂法
设备名称:立式压力蒸汽灭菌锅
型号:YXQ-LS-50S11
福建闽东力捷迅药业有限公司
福建闽东力捷迅药业有限公司
灭菌设备验证记录
编号:REC-ZK009-(00)
验证日期:年月日报告日期:年月日灭菌设备负载:(空载、满载)灭菌参数温度:℃,时间: min
培养条件:温度:℃,时间: h
2支管均显黄色,判定该此灭菌效果合格;灭菌锅内任意一个测试点的培养结果显黄色,即判定为灭菌不合格;若阳性对照2支中有一支培养结果显紫色,说明生物指示剂质量存在问题,实验重做。
结论:
复核人:检验人:。
药品微生物限度检验记录

起草/修订审核批准微生物限度检查记录物料描述批号请验单位取样日期年月日检验依据分样日期年月日1. 供试品处理实验:供试品处理方法(在相应对应项前的□中划“√”)操作规范(在相应对应项前的□中划“√”)□气/喷雾剂供试液的制备取供试品支,置冰冻室冰冻约1小时,取出迅速消毒供试品开启部位,用无菌钢锥在该部位钻一小孔,放置室温,并轻轻转动容器,使抛射剂缓缓全部释出,用无菌注射器吸出全部药液,加批号为PH7.0无菌氯化钠-蛋白胨缓冲液ml,震荡混匀稀释制成比例为的供试液。
□水溶性供试液的制备取供试品,用批号为PH7.0无菌氯化钠-蛋白胨缓冲液ml,混匀并倍比稀释制成比例为的供试液。
□非水溶性供试液的制备取供试品,用ml 表面活性剂/乳化剂,按照□研钵法□匀浆法转/分匀浆min □保温振荡法℃水浴保温min,加批号为PH7.0无菌氯化钠-蛋白胨缓冲液,制成比例为的供试液。
□其他供试液的制备2. 细菌总数的计数实验:取上述1: 的供试液ml,按照(在相应计数方法前划“√”)□平皿法□薄膜过滤法:以PH7.0无菌氯化钠-蛋白胨缓冲液ml 冲洗遍。
进行计数操作,操作完成后将培养皿倒置放置于温度为30~35℃的培养箱进行培养,并逐日观察点记菌落数。
培养箱型号/编号:培养基名称:营养琼脂培养基微生物限度检查记录批号:培养基批号:滤膜批号:滤杯批号:检验人:时间:年月日时检验结果见下表:天数编号实验组阴性对照观察人观察时间1 1年月日时22 1年月日时23 1年月日时2结果cfu/ ( 标准规定:cfu/ )结论□符合规定□超标结果3.霉菌酵母菌总数计数实验:取上述1: 的供试液ml,按照(在相应计数方法前划“√”)□平皿法□薄膜过滤法:以PH7.0无菌氯化钠-蛋白胨缓冲液ml 冲洗遍。
进行计数操作,操作完成后将培养皿倒置放置于温湿度为23~28℃、75%~85% 的霉菌培养箱进行培养,并逐日观察点记菌落数。
培养箱型号/编号:培养基名称:玫瑰红钠琼脂培养基培养基批号:滤膜批号:滤杯批号:检验人:时间:年月日时检验结果见下表:天数编号实验组阴性对照观察人观察时间1 1年月日时22 1年月日时23 1年月日时2微生物限度检查记录批号:4 1年月日时25 1年月日时2结果cfu/ ( 标准规定:cfu/ )结论□符合规定□超标结果4.控制菌检查实验培养箱型号/编码:培养温度:30~35℃培养箱(阳性对照)型号/编码:培养温度:30~35℃阳性菌来源:阳性菌代次:阳性菌操作人:4.1大肠埃希菌检查增菌培养:取1:供试液,mL(在相应计数方法前划“√”),□直接接种□薄膜过滤:以PH7.0无菌氯化钠-蛋白胨缓冲液ml 冲洗遍,将滤膜接种至ml 的胆盐乳糖培养基中,混匀,30~35℃增菌培养小时。
生物指示剂验证检验报告s

xxxxx 医疗股份有限公司
W-PZ-140
生物指示剂检验报告
检验员: 复核人:
产品名称 一次性喉镜叶片
批号 批量 抽检数 10 生产日期
检验日期
2016.5.6
判断标准
灭菌的培养结果均为绿色,阳性对照管均显黄色,判定该此灭菌效
果合格
操作方法及参考标准 生物指示剂无菌测试指引
灭菌时间
半周期
培养温度
35℃
编号 培养前 培养时间 记录 培养时间
记录 1 绿
24H
绿
48H
绿 2 绿 绿 绿 3 绿 绿 绿 4 绿 绿 绿 5 绿 绿 绿 6 绿 绿
绿
7 绿 绿 绿 8 绿 绿 绿 9 绿 绿 绿 10 绿 绿 绿 空白组
绿
黄
黄
使用相关仪器的仪器设备:生物培养箱
检测结论:通过检验,产品的灭菌效果在半周期就灭菌完全,则产品
符合规定要求。
(详情检验记录见附页)。
生物指示剂相关参考资料

保证产品无菌是注射剂产品质量保证的核心问题。
无菌生产工艺是保障注射剂产品无菌的关键手段。
而只有经过充分验证后的灭菌(无菌)生产工艺,才能保证生产出无菌的产品。
微生物挑战试验是无菌生产工艺验证的重要环节。
而选择适当的生物指示剂则是微生物挑战试验结果获得认可的关键。
本文将围绕如何为终端灭菌工艺(过度杀灭和残存概率法)选择适当的生物指示剂进行讨论。
灭菌是指杀灭所有形式微生物的过程。
在业界,常用“无菌保证水平”(Sterility Assurance Level,SAL)概念来评价灭菌(无菌)工艺的效果,SAL的定义为产品经灭菌/除菌后微生物残存的概率。
该值越小,表明产品中微生物存在的概率越小。
为了保证注射剂的无菌安全性,国际上一致规定,采用湿热灭菌法的SAL不得大于10-6,即灭菌后微生物存活的概率不得大于百万分之一。
生物指示剂就是为了保证整个灭菌过程达到SAL 水平而应用的,它能综合反映影响灭菌效果的各种因素。
因此为了保证验证结果的重复性,生物指示剂应当采用标准化的菌株(即变异性小,各项生物学特征均一性好的菌种),并且应当具备合乎要求的抗力。
更重要的是,参照USP的要求“It must be esta blished that the biological indicator system provides a challenge to the sterilization process that exceeds the challenge of the natural microbial burden in or on the product.”,我们应当选择比现有生产线自然环境下所发现的菌株更难杀灭的菌株来作为生物指示剂。
举例来说,比如通过对现有车间环境,生产线,人员,物料两年的的连续观测,发现在现有生产条件下所发现的菌株的D 值最高不超过0.8,则选择D值在0.8~1.5之间的生孢梭菌( Clostridium sporogenes;ATCC7955)为生物指示剂进行验证就是不合适的。
007.PSMV-11088水浴式灭菌器验证方案讲解

安徽捷众生物化学有限公司PSM 水浴式灭菌柜验证方案编号 QY·TS·01·007-00 页 数共 34 页 制定人 制定日期 年 月 日 修订日期 年 月 日 审核人 审核日期 年 月 日 颁发部门 质量管理部 批准人批准日期年 月 日 生效日期年 月 日分发部门相关部门1.概述1.1 PSM 水浴式灭菌柜是山东新华医疗器械股份有限公司生产安装的,用于大容量注射剂的灭菌处理,灭菌柜采用过热水淋浴方式对输液软袋进行加热灭菌,灭菌控制系统主要由现场控制系统和上位机两部分组成。
现场控制系统通过采集相应的输入信号和温度等数据,然后输出相应的控制信号,实现对灭菌柜运行过程的控制。
上位机接收现场控制系统(PLC )送出的数据,对数据进行分析、显示和记录,同时根据所记录的数据输出报表和趋势,以达到对灭菌过程的监控和数据处理。
工艺流程: 工艺流程图1.2主要技术参数: a.容器类别:Ⅰ类b. 设计工作压力:0.30Mpac. 最高工作压力:0.27 Mpad. 最高设计温度:150℃e. 最高工作温度:134℃f.工作温度范围:70-121℃g.蒸汽压力:0.3-0.5 Mpah.去离子水源:0.15-0.3Mpa i 冷却水源:0.2-0.4Mpa j.压缩空气源:0.4-0.6Mpa k.循环周期;≤90min L.耐压试验压力:0.38Mpa M .容积:32.04m3 1.3验证目的:升温进料 排水排汽灭菌冷却出料1.3.1检查并确认PSM水浴式灭菌器的安装符合设计要求,资料及文件符合GMP规定。
1.3.2检查并确认PSM水浴式灭菌器的运行性能,看空载情况灭菌器的温度分布情况,检查标准操作规程是否符合设备的实际操作。
1.3.3验证装载情况下灭菌器不同位置的热量分布状况及产品的预定灭菌程序确保灭菌冷点的产品达到F0>8的要求。
1.4验证项目及要求1.4.1灭菌器概况检查并确认灭菌器的随机文件和资料以及附件符合使用和管理要求。
压力灭菌用生物指示剂的使用方法

压力灭菌用生物指示剂1262该压力蒸汽灭菌生物培养指示剂用于压力蒸汽灭菌效果的生物监测包括下排气锅和预真空锅;通过培养基颜色变化;反应嗜热脂肪杆菌芽孢是否存活;从而判断压力蒸汽灭菌生物监测结果..1.将压力蒸汽灭菌生物培养指示剂放于一标准测试包中;2.按照国家规范;分别将测试包放于锅内不同位置;3.灭菌完毕;取出该生物指示剂;4.挤破内含的安瓿;与一支对照管一起放于56℃培养锅内培养;48小时后阅读结果..结果阅读:1.培养后指示管不变色呈紫色;表示灭菌通过;2.培养后指示管变色呈黄色;表示灭菌不通过;必须及时查出灭菌失败原因..3.同时培养的对照管应为阳性呈黄色;如阴性;可能的原因为:培养条件不符合要求;生物指示剂有问题;应及时查出阴性原因..注意事项:1.灭菌完毕;含生物指示剂的包裹很热并有一定压力;需至少冷却10分钟以上;否则可能引起塑料管内的安瓿破裂;飞溅的碎片导致损伤;2.只有对照管为阳性;其生物监测结果才算有效..3.贮存于室温:15-30℃;相对湿度为35-60%;避免靠近灭菌器和化学消毒剂..1292该生物指示剂可用以121℃下排气和132℃预真空压力蒸汽灭菌锅..3MATTESTTM压力蒸汽灭菌生物培养指示剂快速在与3MATTEST290培养锅共用时;通过酶活性的灭活与否;探测嗜热脂肪杆菌芽孢是否存活;从而判断压力蒸汽灭菌结果..使用方法:1、在生物指示剂标签上注明灭菌器锅号;负荷数量;灭菌日期;不要在指示剂的瓶或盖上另贴一个标签..将生物指示剂放于一个标准测试包内;并置于最难灭菌的位置..2、将含有生物指示剂的测试包放在灭菌器最难灭菌的位置;通常是灭菌器底层;近门或排气口上面..3、正常装载..4、灭菌循环完毕;取出生物指示剂..5、灭菌结束后;从灭菌器内取出含有生物指示剂的测试包;打开散热5分钟后才能取出生物指示剂..同时在压碎安瓿之前;让生物指示剂在培养锅外再冷却10分钟后才能压碎;然后进行生物培养..6、检查生物指示剂标签上的化学指示剂;颜色由玫瑰色变成棕色证明生物指示剂经过压力蒸汽灭菌过程的处理..该颜色的变化并非表明该处理达到灭菌的目的;如果化学指示剂没有变化;请检查灭菌过程..7、戴上防护眼镜;挤碎安瓿;然后培养生物指示剂..详细步骤请参阅3MATTEST290培养锅操作说明..8、每次培养须同时培养一个未灭菌过的生物指示剂进行阳性对照;阳性对照生物指示剂与经过灭菌处理的生物指示剂为相同生产日期和批号..阳性对照的目的是保证:1正确的培养条件2指示剂的活性不适当的贮存条件可能影响有效期内的指示剂活性33MATTEST290培养锅功能完好9、在3MATTEST290培养锅培养温度62+/-20C内;培养阳性对照和已处理的指示剂3小时;读出最终结果..阳性对照必须得出荧光阳性结果阅读器显示为红灯或+;如阳性对照读出荧光阴性绿灯或-;应检查培养锅温度和操作过程;直至阳性对照为阳性结果;生物监测的结果才是有效的..对于经过灭菌处理的指示剂;荧光阳性红灯或+表明灭菌过程失败;荧光阴性绿灯或-表明灭菌过程合格..10、如果需要通过颜色变化检测生物监测结果;应将生物指示剂放在培养锅内继续培养..同时随时监测阳性结果的出现;如8、12、24;直至168小时7天;最终视觉效果应在168小时7天得出..黄色表明细菌生长;灭菌过程失败..168小时7天没有颜色变化培养基为紫色表明灭菌过程合格..11、对任何为阳性生物监测结果应立即采取行动;如追回同锅次的灭菌物品;和寻找原因..直至生物指示剂的结果呈阴性..注意事项:冷却之前压碎或过度处理生物指示剂可能导致玻璃安瓿的破碎;飞溅的碎屑会使人员受伤;因此建议在从灭菌器内取出生物指示剂时戴防护眼镜和手套;在压碎生物指示剂时也需要戴防护眼镜..禁忌:该生物指示剂不能用于121℃预真空和132℃下排气压力蒸汽灭菌锅;及干热、化学蒸汽、环氧乙烷和其他的低温灭菌过程的生物监测..。
生物指示剂的选择

生物指示剂菌液浓度的计算(阴性分数法)
假设F0=8,用D121℃=0.7的枯草芽孢杆菌计算: SLRbi=F0/ Dbi=11.43 (SLR为孢子对数下降值) SLRbi=lgN0-lgN (N0和N分别为灭菌前后孢子数) 根据阴性分数法,N=2.303×lg(n/q),其中n为挑战性试验 样品总数,q为试验结果呈阴性的瓶数。如试验结果20瓶 挑战瓶均呈阴性,在计算时可假设只有19只瓶呈阴性(因 为q=n,lg(n/q)=0,代入公式SLRbi=lgN0-lgN时,数学式 无意义),则可得出: N=2.303×lg(n/q)=0.0513 lgN=-1.29 lgN0=SLRbi+lgN=11.43-1.29=10.14 N0= 1010.14=1.4×1010(cfu/瓶)
生物指示剂菌种的选择 08年年度回顾,车间洁净区最耐热菌株D100℃值为 14.2, 09年年度回顾,车间洁净区最耐热菌株 D100℃值为16.7。连续两年,车间洁净区最耐热菌 株D100℃值最高为16.7 ,换算成D121℃约为0.12。 因此,我们应该选择D121℃值比0.12大的菌株。 由于菌株的D值受介质影响,因此,我们需要测定 在各介质中的实际的D值,确保生物指示剂适合我 们公司使用。
USP-55 生物指示剂-抗性测试解读

USP 55BIOLOGICAL INDICATORS—RESISTANCE PERFORMANCE TESTS生物指示剂-抗性测试TOTAL VIABLE SPORE COUNT活孢子数总数计数Remove three specimens of the relevant biological indicator from their original individual containers. Disperse the paper into component fibers by placing the test specimens in a sterile 250-mL cup of a suitable blender containing 100 mL of chilled, sterilized Purified Water and blending for 3 to 5 minutes to achieve a homogeneous suspension. Transfer a 10-mL aliquot of the suspension to a sterile, screw-capped 16- × 125-mm tube.从生物指示剂的原包装袋中取出3支作为样本。
把待测样品放入一个已灭菌的250mL有搅拌器的杯子里,杯子内装100 mL放冷的灭菌纯化水。
把杯子里的纸片磨碎成纤维状,并混合3~5min使之成为均一的悬浮液。
转移10ml的整数倍的悬浮液至一个已灭菌的16 × 125mm的螺盖管中。
For Biological Indicator for Steam Sterilization, Paper Carrier, heat the tube containing the suspension in a water bath at 95to 100for 15 minutes (heat shock), starting the timing when the temperature reaches 95.如果是纸载的蒸汽灭菌生物指示剂,则把装有悬浮液的管放入95℃~100℃水浴15min (热休克),在悬浮液温度达到95℃时开始计时。
药品微生物限度检查实验记录
供试品瓶(盒)1直接检查法2集螨法
结果(规定不得检出)
结论:检验者:校对者:报告日期:
大肠埃希菌检查(阳性菌加入CFU/ml)大肠菌群检查(阳性菌加入CFU/ml)
方法:
供试液
阳性
阴性
方法:
供试液
阳性
阴性
10-1
10-2
10-3
BL
MUG培养管
胆盐乳糖发酵管
靛基质
EMB
EMB或MacC
MacC平板
革兰染色、镜检
革兰染色、镜检
IMVic
乳糖发酵管
乳糖发酵
结果(规定不得检出)
结果(限度规定:)
文件编号:
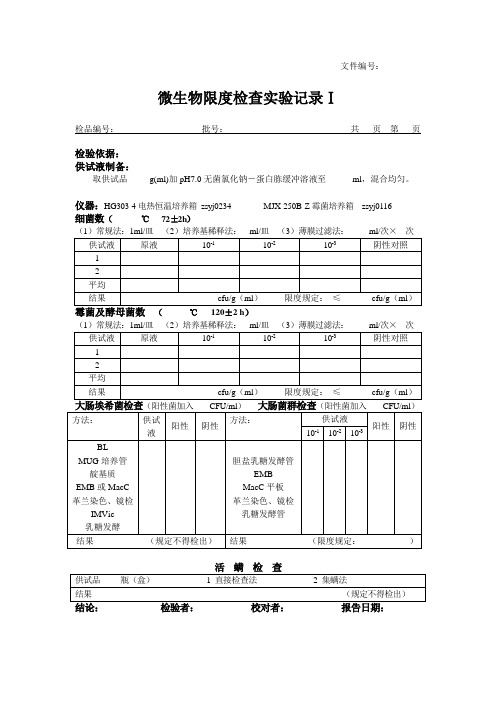
微生物限度检查实验记录Ⅰ
检品编号:批号:共页页
检验依据:
供试液制备:
取供试品g(ml)加pH7.0无菌氯化钠-蛋白胨缓冲溶液至ml,混合均匀。
仪器:HG303-4电热恒温培养箱zsyj0234MJX-250B-Z霉菌培养箱zsyj0116
细菌数(℃72±2 h)
(1)常规法:1ml/皿(2)培养基稀释法:ml/皿(3)薄膜过滤法:ml/次×次
供试液
原液
10-1
10-2
10-3
阴性对照
1
2
平均
结果
cfu/g(ml)限度规定:≤cfu/g(ml)
霉菌及酵母菌数(℃120±2 h)
(1)常规法:1ml/皿(2)培养基稀释法:ml/皿(3)薄膜过滤法:ml/次×次
供试液
原液
10-1
10-2
10-3
阴性对照
1
2
平均
结果
cfu/g(ml)限度规定:≤cfu/g(ml)
生物化学实验记录和实验报告的书写

第二节实验记录和实验报告的书写正确记录实验过程及书写实验报告,是训练学生进行正规实验训练的重要内容。
实验是在理论指导下的科学实践,目的在于经过实践,掌握科学观察的基本方法和技能,培养学生的科学思维、分析判断和解决实际问题的能力。
也是培养探求真知、尊重科学事实和真理的学风,以及培养科学态度的重要环节。
为此,要求学生在实验前必须预习、理解从基本原理和实验基本操作步骤、注意事项,列出所需试剂和仪器,实验中组织安排好时间,严肃认真地执行操作,细致观察变化,如实作好记录、书写实验报告等。
一、实验记录实验记录要整洁、字迹清楚。
实验中观察到的现象、结果和数据,耍及时地直接记在记录本。
原始记录必须准确简练、详尽、清楚。
记录时,应做到如实正确记录实验结果,不可夹杂主观因素。
在实验条件下观察到的现象,也应如实仔细地记录下来。
在定量实验中观测到的数据,如称量物的重量、滴定管的读数、光电比色计的光密度值等,都应设计一定的表格准确记录。
并应根据仪器的精确度准确记录有效数字。
要求对实验的每个结果都应正确无遗漏地做好记录。
实验中使用仪器的类型、试剂的规格、化学反应式、分子量、浓度等,都应记录清楚。
实践过程中,应一丝不苟,努力培养严谨的科学作风。
完整的实验记录应包括日期、实验题目、目的、操作、结果。
二、实验报告实验结束后,应及时整理和总结实验结果及记录,写出实验报告。
实验报告应包括实验名称、实验日期、目的要求、原理、试剂配制、仪器设备、操作方法;实验结果、讨论等项内容。
书写实验报告时,目的和要求、原理以及操作方法部分应作简单扼要的叙述,但对实验条件和操作的关键环节必须写清楚。
对于实验结果部分,应根据实验的要求,把所得的实验结果和数据进行整理、归纳、分析和对比,并尽量总结成各种图表,如标准曲线图以及实验组与对照组实验结果的比较表等。
还应针对实验结果进行必要的说明和分析。
讨论部分不是对结果的重述,而是对实验方法,实验结果和异常现象进行探讨和评论,以及对于实验设计的认识、体会和建议。
