食品化学复习资料
食品化学复习

一、掌握的基本概念1.水分活度2.单分子层水3.结合水4.体相水5.等温吸着曲线6.分子流动性7.吸湿性8.保湿性9.转化糖10.果胶酯化度11.淀粉的老化12.淀粉糊化13.α-淀粉14.美拉德反应15.蛋白质变性16.单纯蛋白17.蛋白质共凝胶作用18.蛋白质的持水能力19.盐溶20.调温21.固体脂肪指数22.油脂的塑性23.脂肪同质多晶现象24.乳化25.HLB值26.皂化值27.POV28.抗氧化剂29.褐变30.酶促褐变31.非酶褐变32.风味33.风味前体34.味觉阈值35.香气值36.AH/B 生甜团学说37.食品添加剂38.防腐剂39.ADI值40.MNL值二、回答问题1)你认为食品化学有哪些新的研究方向?2)试论述水分活度与食品的安全性的关系?3)水在食品中的重要作用?4)水分活度、分子移动性和Tg在预测食品稳定性中的作用?并举行比较。
5)食品中水的存在状态?结合水与体相水的区别?6)糖类的吸湿性和保湿性在食品中的作用?7)食品的质量属性包括哪些方面?8)多糖在食品中的增稠特殊性与哪些因素有关?9)亚硫酸盐在食品中有哪些作用?10)油脂的常温储藏对其品质产生什么影响?如何防止?11)油脂的高温热加工对其品质产生什么影响?如何防止?12)为什么水果从未成熟到成熟是一个由硬变软的过程?13)β—环状糊精特征及用途?14)简述果蔬制品护绿的方法?15)味感的相互作用有哪些,试举例说明?16)对食品进行热加工的目的是什么?热加工会对蛋白质有何不利影响?17)试述食品中香气形成的途径,并举例说明。
18)试分别论述油脂在不同氧化机理下氢过氧化物的形成过程,并用化学反应式表示?19)蛋白质具有哪些功能性质,它们与食品加工有何关系?20)写出某种脂肪酸的写出速记符号和名称?21)什么是糊化?影响淀粉糊化的因素有那些?22)什么是老化?影响淀粉老化的因素有那些?如何在食品加工中防止淀粉老化?23)非酶褐变的作用机理主要有哪几种?24)乳化剂的HBL与其适用范围之间有什么关系?25)味感的相互作用有哪些,试举例说明?26)主要的甜味、酸味、苦味、鲜味物质有哪些27)基本味感包括哪几种?28)多酚类衍生物天然色素有哪几种?29)防腐剂必须具备的条件是什么?30)大豆的有毒物质有哪几种?31)影响面团的两种主要蛋白质是什么?32)导致水果和蔬菜中色素变化有三个关键性的酶是什么?33)同一种油脂以下列哪种结晶方式存在时,其塑性最好?34)葱、蒜、韭菜等蔬菜中的香辛的主体成分是什么?啤酒中主要苦味物质是什么?35)抑制酶促褐变的的方法有哪些?36)油脂自动氧化历程中的氧是什么态?油脂光敏氧化历程中的氧是什么态?哪种历程对油脂酸败的影响更大?37)油脂的精制有哪几个步骤,它的作用是什么?38)什么是食品添加剂?对食品添加剂又说明要求?39)什么是食品添加剂的MNL值?什么是ADI值?以实例推断食品添加剂的添加量的确定?40)简述食品添加剂亚硝酸盐对食品的利与弊。
《食品化学》复习资料

《食品化学》期末复习资料1 简要概括食品中的水分存在状态。
食品中的水分有着多种存在状态,一般可将食品中的水分分为自由水(或称游离水、体相水)和结合水(或称束缚水、固定水)。
其中,结合水又可根据被结合的牢固程度,可细分为化合水、邻近水、多层水;自由水可根据这部分水在食品中的物理作用方式也可细分为滞化水、毛细管水、自由流动水。
但强调的是上述对食品中的水分划分只是相对的。
2 简述食品中结合水和自由水的性质区别?食品中结合水和自由水的性质区别主要在于以下几个方面:⑴食品中结合水与非水成分缔合强度大,其蒸汽压也比自由水低得很多,随着食品中非水成分的不同,结合水的量也不同,要想将结合水从食品中除去,需要的能量比自由水高得多,且如果强行将结合水从食品中除去,食品的风味、质构等性质也将发生不可逆的改变;⑵结合水的冰点比自由水低得多,这也是植物的种子及微生物孢子由于几乎不含自由水,可在较低温度生存的原因之一;而多汁的果蔬,由于自由水较多,冰点相对较高,且易结冰破坏其组织;⑶结合水不能作为溶质的溶剂;⑷自由水能被微生物所利用,结合水则不能,所以自由水较多的食品容易腐败。
3 比较冰点以上和冰点以下温度的αW差异。
在比较冰点以上和冰点以下温度的αW时,应注意以下三点:⑴在冰点温度以上,αW是样品成分和温度的函数,成分是影响αW的主要因素。
但在冰点温度以下时,αW与样品的成分无关,只取决于温度,也就是说在有冰相存在时,αW不受体系中所含溶质种类和比例的影响,因此不能根据αW值来准确地预测在冰点以下温度时的体系中溶质的种类及其含量对体系变化所产生的影响。
所以,在低于冰点温度时用αW值作为食品体系中可能发生的物理化学和生理变化的指标,远不如在高于冰点温度时更有应用价值;⑵食品冰点温度以上和冰点温度以下时的αW值的大小对食品稳定性的影响是不同的;⑶低于食品冰点温度时的αW不能用来预测冰点温度以上的同一种食品的αW。
4 MSI在食品工业上的意义MSI即水分吸着等温线,其含义为在恒温条件下,食品的含水量(每单位干物质质量中水的质量表示)与αW的关系曲线。
食品化学复习资料

第一章绪论名词解释1.食品化学:用化学的理论和方法研究食品本质的科学,它通过对食品营养价值、安全性和风味特征的研究,阐明食品的组成、性质、结构和功能以及食品成分在贮藏、加工和运输过程中可能发生的化学、物理变化和生物化学变化的科学。
2.营养素:指那些能维持人体正常生长发育和新陈代谢所必需的物质。
P2第二章水分名词解释1.结合水:指存在于溶质或其他非水组分附近的、与溶质分子之间通过化学键结合的那一部分水,可分为化合水、邻近水和多层水。
P212.体相水:指食品中除了结合水以外的那一部分水,它分为不移动水或滞化水、毛细管水和自由流动水。
P223.水分活度:指食品中水的蒸汽压与同温下纯水的饱和蒸汽压的比值。
P234.水分的吸附(吸湿)等温线:在恒定温度下,食品的水分含量与它的水分活度之间的关系图称为吸附等温线(MSI)。
P265.等温线的滞后现象:一种食物一般有两条吸附等温线;一条是吸附等温线,是食品在吸湿时的吸附等温线;一条是解吸等温线,是食品在干燥时的吸附等温线;往往这两条曲线并不完全重叠,在中低水分含量部分张开了一细长的眼孔,把这种现象称为等温线的滞后现象。
6.玻璃态:指既像固体一样具有一定的形状和体积,又像液体一样分子间排列只是近似有序,因此它是非晶态或无定形态。
7.玻璃化转变温度:指非结晶态的食品体系从玻璃态到橡胶态的转变时的温度。
8. 分子移动性:又称分子流动性,是分子的旋转移动和平动移动的总度量。
问答题1.水分活度与食品稳定性的关系。
答:食品的贮藏稳定性与水分活度之间有着密切的联系。
一)水分活度与微生物生命活动的关系:各类微生物生长都需要一定的水分活度,只有食物的水分活度大于某一临界值时,特定的微生物才能生长。
一般说来:细菌为Aw>0.9;酵母为Aw>0.87;霉菌为Aw>0.8。
(一些耐渗透压微生物除外。
)在Aw<0.60时,绝大多数微生物就无法生长。
二)水分活度与食品化学变化的关系:1)、从酶促反应与食物水分活度的关系来看:水分活度对酶促反应的影响是两个方面的综合,一方面影响酶促反应的底物的可移动性,另一方面影响酶的构象。
食品化学复习资料全

1、酶活力:就是酶催化能力,用酶催化反应的速度来表示。
在25℃及其他酶最适条件下,在1min内1μmol的底物转化为产物的酶量称为酶的国际单位(IU)。
单位时间内催化反应生成产物的量称为比活力。
每毫克酶蛋白含有的酶活力单位酶活力单位。
2、影响酶促反应速度的因素:1.底物浓度的影响。
在低底物浓度时, 反应速度及底物浓度成正比。
当底物浓度达到一定值,几乎所有的酶都及底物结合后,反应速度达到最大值(Vmax),此时再增加底物浓度,反应速度不再增加。
2、酶浓度的影响。
在底物浓度充足、反应条件适宜时,反应速度及酶浓度成正比。
3. 温度的影响。
酶促反应的最适温度高于酶活力的最适温度。
4. pH 的影响。
在一定的pH 下, 酶具有最大的催化活性,通常称此pH 为最适pH。
3、米氏常数Km的意义:不同的酶具有不同Km值,它是酶的一个重要的特征物理常数。
Km值只是在固定的底物,一定的温度和pH条件下,一定的缓冲体系中测定的,不同条件下具有不同的Km值。
Km值表示酶及底物之间的亲和程度:Km 值大表示亲和程度,酶的催化活性4、不可逆抑制作用:抑制剂及酶的必需活性基团以非常牢固的共价键结合而引起酶活力的丧失,不能用透析、超滤等物理方法除去抑制剂而使酶恢复活性,称为~。
5、可逆的抑制作用:抑制剂通过非共价键及酶和(或)酶-底物复合物进行可逆结合而使酶活性降低或失活,可采用透析、超滤等方法将抑制剂除去而使酶恢复活性,称为~。
分为:竞争性、非竞争性、反竞争性6、食品酶研究的内容和意义:研究食品原料体内酶的变化及作用。
通过控制来减少食物贮藏时成分的损失,同时使食品具有更好的品质。
研究酶学原理及酶制剂在食品工中的应用。
达到控制和改善品质及贮藏性的目的。
7、酶促褐变:当果蔬受到损伤时,组织和氧接触,由酶催化造成变色的作用。
8、酶促褐变的控制:控制: 针对酶促褐变的三个条件:酚类物质,氧和氧化酶类。
(1)热处理法:理论值70~95℃7s。
食品化学复习资料

食品化学复习资料食品化学复习资料食品化学作为食品科学的重要学科之一,研究的是食品中的化学成分、化学变化以及与人体健康的关系。
在食品安全和营养方面,食品化学的知识是必不可少的。
本文将从食品的组成、食品加工过程中的化学反应以及食品添加剂等方面,为大家提供一些食品化学复习资料。
一、食品的组成食品由许多不同的化学成分组成,包括水分、碳水化合物、脂肪、蛋白质、维生素、矿物质等。
水分是食品中最基本的成分,它不仅是食品的溶剂,还能影响食品的质地和口感。
碳水化合物是食品中的主要能量来源,包括单糖、双糖和多糖。
脂肪是食品中的另一种重要能量来源,同时也是维生素的溶剂和传递体。
蛋白质是构成人体组织和维持生命所必需的,它们由氨基酸组成。
维生素和矿物质是人体所需的微量元素,对于人体的正常生长和发育至关重要。
二、食品加工过程中的化学反应食品加工过程中会发生许多化学反应,这些反应不仅会影响食品的质地和口感,还会对食品的营养价值产生影响。
例如,烹调过程中的加热反应会导致食物中的维生素和蛋白质的损失。
此外,食品中的糖类和氨基酸在高温下会发生糖胺反应和美拉德反应,产生有机化合物的香气和色素。
这些反应不仅能够改善食品的风味,还能增加其诱人的色泽。
三、食品添加剂食品添加剂是指为了改善食品质量、延长食品保质期、增加食品的色泽、口感和营养价值而加入的物质。
常见的食品添加剂包括防腐剂、色素、甜味剂、增稠剂等。
防腐剂可以抑制微生物的生长,延长食品的保质期。
色素可以改变食品的色泽,增加食欲。
甜味剂可以替代糖类,减少热量的摄入。
增稠剂可以增加食品的黏稠度,改善食品的质地。
然而,食品添加剂也存在一定的风险。
一些食品添加剂可能会引起过敏反应,甚至对人体健康产生不良影响。
因此,在选择食品时,我们应该尽量选择不含或含量较低的食品添加剂,避免长期过量摄入。
四、食品化学与健康食品化学与人体健康密切相关。
食品中的营养成分和化学物质可以影响人体的生理功能和健康状况。
食品化学复习资料含答案(全)

食品化学复习资料一、单项选择题在每小题列出的四个备选项中只有一个是符合题目要求的,未选、错选或多选均无分。
1.牛乳中含量最高的蛋白质是( )A、酪蛋白B、β-乳球蛋白C、α-乳清蛋白D、脂肪球膜蛋白2.在食品生产中,一般使用浓度的胶即能产生极大的粘度甚至形成凝胶。
( )A、<0.25%B、0.25~0.5%C、>0.5%3.奶油、人造奶油为()型乳状液。
A、O/WB、W/OC、W/O/WD、O/W或W/O4.油脂的性质差异取决于其中脂肪酸的()。
A、种类B、比例C、在甘三酯间的分布D、在甘三酯中的排列5.下列哪一种酶不属于糖酶()。
A、α-淀粉酶B、转化酶C、果胶酶D、过氧化物酶6.下列何种不属于催化果胶解聚的酶()。
A、聚甲基半乳糖醛酸酶B、果胶裂解酶C、果胶酯酶D、果胶酸裂解酶7.下列不属于酶作为催化剂的显著特征为()。
A、高催化效率B、变构调节C、高专一性D、酶活的可调节性8.虾青素及( )结合时不呈红色,及其分离时则显红色。
A、蛋白质B、糖C、脂肪酸D、糖苷9.肉中()含量增高,则肉变得僵硬。
A.肌球蛋白 B.肌动蛋白 C. 肌动球蛋白 D. 肌原球蛋白10.DE为的水解产品称为麦芽糖糊精。
A、<20B、>20C、≦20,D、=2011.为W/O型的食品是()。
A、牛乳B、淋淇淋C、糕点面糊D、人造奶油12.食品工业中常用的乳化剂硬酯酰乳酸钠(SSL)为()。
A、离子型B、非离子型C、O/W型D、W/O型13.一般认为及果蔬质构直接有关的酶是()。
A、蛋白酶B、脂肪氧合酶C、果胶酶D、多酚氧化酶14.导致水果和蔬菜中色素变化有三个关键性的酶,但下列()除外。
A、脂肪氧合酶B、多酚氧化酶C、叶绿素酶D、果胶酯酶15.下列何种蛋白酶不属于酸性蛋白酶()。
A、真菌蛋白酶B、凝乳酶C、胃蛋白酶D、胰蛋白酶16.活性氧法是用以测定油脂的抗氧化的能力;所测得的数值的单位为()。
食品化学复习资料

⾷品化学复习资料氨基酸和蛋⽩质第⼀部分⼀、概述 Protein 蛋⽩质蛋⽩质是⼀种复杂的巨型分⼦,其组成元素有碳、氢、氧、氮、硫、磷、碘及铁、锌等⾦属元素。
蛋⽩质是由不同氨基酸通过肽键相互连接⽽成的。
由于这些氨基酸的侧链各不相同,当它们互相连接时,就使不同的蛋⽩质具有不同的化学性质和多种多样的⼆级和三级结构蛋⽩质的⽣物功能1、酶蛋⽩作为⽣物催化剂2、代谢和代谢调节物质(例如胰岛素)3、免疫活性成分(例如抗体)4、物质转运和储存(例如⾎红蛋⽩)5、运动与⽀持作⽤(例如肌纤维蛋⽩)6、参与细胞间信息传递(例如膜蛋⽩、糖蛋⽩)7、营养蛋⽩、结构蛋⽩和毒素蛋⽩蛋⽩质⽣物功能举例1、⾓蛋⽩、胶原和弹性蛋⽩构建结缔和组织结构。
2、酶是具有⾼度专⼀性的催化剂。
3、胰岛素和⽣长激素等蛋⽩质能调节代谢反应。
4、收缩蛋⽩质(肌球、肌动和微管蛋⽩)为产⽣运动所需。
5、免疫球蛋⽩能抵抗脊椎动物感染。
6、胰蛋⽩酶抑制剂等蛋⽩质具有抗营养性质。
7、⼀些蛋⽩质会导致⾷物过敏。
8、⾁毒杆菌毒素、葡萄球菌毒素等外源蛋⽩质对⾼等动物有毒。
⾷品蛋⽩质在⾷品体系中的功能作⽤⼆、分类、结构和基本性质(⼀)蛋⽩质的分类◆根据组成成分分类:简单蛋⽩质仅含有氨基酸的蛋⽩质结合蛋⽩质氨基酸+辅基还有⼀类是⽤化学或酶学⽅法适当处理蛋⽩质得到的化合物,称为衍⽣蛋⽩质。
辅基:结合蛋⽩质中的⾮蛋⽩部分,绝⼤部分辅基是通过共价键与蛋⽩部分相连,辅基与蛋⽩质的功能密切相关。
包括糖、脂、核酸、磷酸、⾊素和⾦属离⼦等。
◆根据分⼦形状分类:球状蛋⽩质:分⼦长轴:短轴<10,多数可溶于⽔。
亲⽔基团位于分⼦表⾯,疏⽔基团位于分⼦内部。
纤维状蛋⽩质:分⼦长轴:短轴>10,难溶于⽔简单蛋⽩质的分类:1.清蛋⽩:溶于⽔及稀盐、稀酸或稀碱溶液。
为饱和硫酸铵所沉淀。
⼴泛存在于⽣物体内,如⾎清清蛋⽩、乳清蛋⽩等。
2.球蛋⽩:为半饱和硫酸铵所沉淀。
不溶于⽔⽽溶于稀盐溶液的称优球蛋⽩;溶于⽔的称拟球蛋⽩,普遍存在于⽣物体内。
食品化学 复习资料

水自由水:是指食品中与非水成分有较弱作用或基本没有作用的水。
水分子可以自由运动,但在宏观上它是被束缚的。
结合水:又称为束缚水,是指存在于食品中的与非水成分通过氢键结合的水,是食品中与非水成分结合的最牢固的水。
笼形水合物:是冰状包合物,其中水为主体物质,通过氢键形成了笼状结构,物理截留了另一种被称为客体的分子,主体由20~74个水分子构成,客体是低分子量化合物。
水分活度:水分活度表示食品中水分可以被微生物所利用的程度在数值上,食品水分活度等同于空气的平衡相对湿度单分层水:指与食品中非水成分的强极性基团如:羧基、氨基、羟基等直接以氢键结合的第一个水分子层。
在食品中的水分中它与非水成分之间的结合能力最强,很难蒸发,与纯水相比其蒸发焓大为增加,它不能被微生物所利用。
一般说来,食品干燥后安全贮藏的水分含量要求即为该食品的单分子层水。
若得到干燥后食品的水分含量就可以计算食品的单分子层水含量。
吸湿等温线:在恒温条件下,以食品的含水量(用每单位干物质质量中水的质量表示)对Aw(水活性)绘图形成的曲线滞后现象:回吸:把水加到干的样品中解吸:先使样品吸水饱和,再干燥。
回吸与解吸所得的等温线不重叠现象即为“滞后现象”一般来说,当Aw一定时,解吸过程中食品的水分含量大于回吸过程中水分含量。
解吸线在上方(滞后环)滞后环形状取决于食品品种,温度。
水分活度与食品稳定性的关系:(1)水分活度与微生物的生长水分活度在0.91以上,食品的微生物变质以细菌为主,水分活度降低到0.91以下就可以抑制一般细菌的生长,水分活度在0.9以下时,食品微生物腐败主要是酵母菌和霉菌引起,食品中有害微生物生长的最低水分活度是0.86~0.97,所以真空包装的水产品和畜产加工制品,水分活度要低于0.94(2)水分活度与酶促反应水分能使蛋白质膨润,体积增大,暴露出长链中可氧化的基团,Aw的增大会加速蛋白质的氧化,破坏蛋白质的结构,导致其变性。
食品在较高Aw(30-60%)的情况下,淀粉老化速度最快;如果降低Aw,则老化速度减慢,若含水量降至于10%-15%,则食品中水分多呈结合态,淀粉几乎不发生老化.(3)水分活度与非酶褐变、赖氨酸损失非酶褐变反应可发生在中、低水分含量的食品中低Aw(0.2),反应速度极低或不反应,中等至高Aw,反应速度可达到最高,水是一个产物,水含量继续增加,会稀释中间产物的浓度,导致产物抑制作用。
食品化学复习资料(食安用)

第二章水1.1 水分子的结构单个水分子的结构特征:①H2O 分子的四面体结构有对称型。
②H-O 共价键有离子性。
③氧的另外两对孤对电子有静电力。
④H-O 键具有电负性。
水分子的缔合●形成三维氢键能力:水分子具有在三维空间内形成许多氢键的能力可充分地解释水分子间存在大的引力。
●水分子缔合的原因:①H-O 键间电荷的非对称分布使H-O 键具有极性,这种极性使分子之间产生引力。
②由于每个水分子具有数目相等的氢键供体和受体,因此可以在三维空间形成多重氢键。
③静电效应。
●水与溶质间的相互作用2.2 结合水是存在于非水组分邻近的水,与同一体系中的体相水相比,它们呈现出与同一体系中体相水显著不同的流动性及其他性质;结合水由构成水、邻近水和多层水所组成。
邻近水:是指水-离子和水-偶极的缔合作用,于非水组分的特定亲水位置发生强烈相互作用的那部分水。
◆在-40℃下不结冰◆无溶解溶质的能力◆与纯水比较分子平均运动大大减少◆不能被微生物利用此种水很稳定,不易引起Food 的腐败变质体相水:距离非水组分位置最远,水-水氢键最多的那部分水。
⏹结冰,但冰点有所下降⏹溶解溶质的能力强,干燥时易被除去⏹与纯水分子平均运动接近,很适于微生物生长和大多数化学反应,易引起食品的腐败变质,但与食品的风味及功能性紧密相关2.3 水与离子及离子基团的相互作用⏹水-离子键的强度大于水-水氢键的强度,但是远小于共价键的强度。
⏹加入可以离解的溶质会打破纯水的正常结构。
⏹水和简单的无机离子产生偶极-离子相互作用。
⏹离子和有机分子的离子基团在阻碍水分子流动的程度上超过其他类型的溶质。
(1)水和简单的无机离子产生偶极-离子相互作用(2)一些离子在稀水溶液中具有净结构破坏效应●净结构破坏效应溶液比纯水具有较高的流动性●净结构形成效应溶液比纯水具有较低的流动性(3)一种离子改变水的净结构的能力与它的极化半径(电荷除以半径)或电场强度紧密相关。
(4)离子效应——离子通过它们不同程度的水合能力:改变水的结构; 影响介电常数;决定胶体粒子周围双电层的厚度;影响水对其它非水溶质和悬浮物质的相容程度;影响蛋白质的构象和胶体的稳定性。
食品化学复习资料

食品化学一、科学名词1. 食品化学:用化学的理论和方法研究食品本质的科学,它通过食品营养价值、安全性和风味特征的研究,阐明食品的组成、性质、结构和功能以及食品成分在贮藏、加工和运输过程中可能发生的化学、物理变化和生物化学变化的科学。
2. 滞后现象:采用向干燥样品中添加水(回吸作用)的方法绘制水分吸着等温线和按解吸过程绘制的等温线并不相互重叠,这种不重叠性称为滞后现象。
3. 吸湿等温线:在恒定的温度下,食品的水分含量(用单位干物质质量中水的质量表示,g水/g 干物质)与它的水分活度之间的关系图称为吸附等温线(简称MSI)。
4. 水分活度:水分活度是指食品中水的蒸汽压和该温度下纯水的饱和蒸汽压的比值。
5. 单分子层水:它是处在非水组分亲水性最强的基团周围的第一层位置,与离子或离子基团缔合的水。
主要结合力是水-离子和水-偶极缔合作用,其次是水和溶质之间的氢键。
6. 淀粉糊化:淀粉粒在适当温度下,在水中溶胀,分裂,形成均匀的糊状溶液的过程被称为糊化。
其本质是微观结构从有序到无序。
7. 淀粉老化:淀粉溶液经缓慢冷却或淀粉凝胶经长期放置,会变为不透明甚至产生沉淀的现象,被称为淀粉的老化。
8. 改性淀粉:天然淀粉经适当的化学处理、物理处理或酶处理,使某些加工性能得到改善,以适应特定的需要,这种淀粉被称为变性淀粉。
9. 低聚糖:又称寡聚糖,由2~10个单糖通过糖苷键连接形成的直连或支链的低聚合度的糖类,有甜味,溶于水,普遍存在于自然界。
10.蛋白质的一级结构:又称化学结构,是指氨基酸在肽链中的排列顺序及二硫键的位置。
11. 必须氨基酸:人体必不可少,而机体内又不能合成的,必须从食物中补充的氨基酸,称必需氨基酸蛋白质的变性12. 蛋白质变性:由于外界因素的作用,使天然蛋白质分子的构象发生了异常变化,从而导致生物活性的丧失以及物理、化学性质的异常变化,不包括一级结构上肽键的断裂。
13. 同质多晶: 是化学组成相同而晶体结构不同的一类化合物,但融化时可生成相同的液相。
食品化学复习
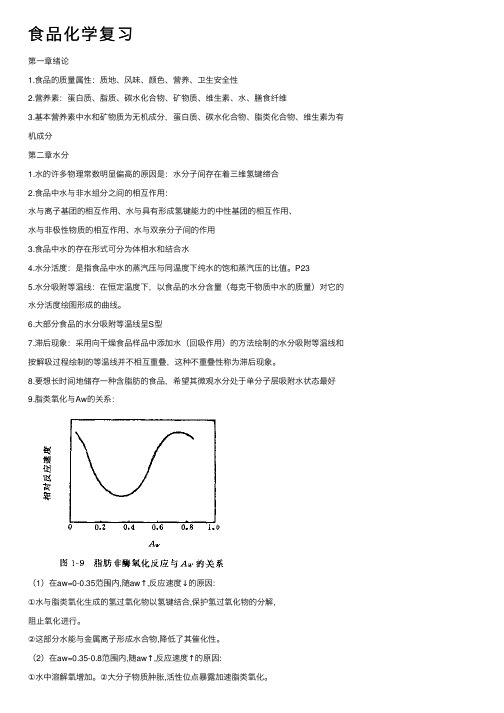
⾷品化学复习第⼀章绪论1.⾷品的质量属性:质地、风味、颜⾊、营养、卫⽣安全性2.营养素:蛋⽩质、脂质、碳⽔化合物、矿物质、维⽣素、⽔、膳⾷纤维3.基本营养素中⽔和矿物质为⽆机成分,蛋⽩质、碳⽔化合物、脂类化合物、维⽣素为有机成分第⼆章⽔分1.⽔的许多物理常数明显偏⾼的原因是:⽔分⼦间存在着三维氢键缔合2.⾷品中⽔与⾮⽔组分之间的相互作⽤:⽔与离⼦基团的相互作⽤、⽔与具有形成氢键能⼒的中性基团的相互作⽤、⽔与⾮极性物质的相互作⽤、⽔与双亲分⼦间的作⽤3.⾷品中⽔的存在形式可分为体相⽔和结合⽔4.⽔分活度:是指⾷品中⽔的蒸汽压与同温度下纯⽔的饱和蒸汽压的⽐值。
P235.⽔分吸附等温线:在恒定温度下,以⾷品的⽔分含量(每克⼲物质中⽔的质量)对它的⽔分活度绘图形成的曲线。
6.⼤部分⾷品的⽔分吸附等温线呈S型7.滞后现象:采⽤向⼲燥⾷品样品中添加⽔(回吸作⽤)的⽅法绘制的⽔分吸附等温线和按解吸过程绘制的等温线并不相互重叠,这种不重叠性称为滞后现象。
8.要想长时间地储存⼀种含脂肪的⾷品,希望其微观⽔分处于单分⼦层吸附⽔状态最好9.脂类氧化与Aw的关系:(1)在aw=0-0.35范围内,随aw↑,反应速度↓的原因:①⽔与脂类氧化⽣成的氢过氧化物以氢键结合,保护氢过氧化物的分解,阻⽌氧化进⾏。
②这部分⽔能与⾦属离⼦形成⽔合物,降低了其催化性。
(2)在aw=0.35-0.8范围内,随aw↑,反应速度↑的原因:①⽔中溶解氧增加。
②⼤分⼦物质肿胀,活性位点暴露加速脂类氧化。
③催化剂和氧的流动性增加。
(3)当aw>0.8时,随aw↑,反应速度增加很缓慢的原因:催化剂和反应物被稀释,继续加⽔表现为阻滞氧化。
在aw=0.3~0.4范围内,氧化速度最低10.MSI的实际意义:(1)从MSI图可以看出⾷品脱⽔的难易程度(2)如何组合⾷品才能避免⽔分在不同物料间的转移(3)测定包装材料的阻湿性(4)据MSI可预测含⽔量对微⽣物的影响(5)预测⾷品的化学与物理稳定性与⽔分的含量的关系(6)可以看出不同⾷品中⾮⽔组分与⽔结合能⼒的强弱11.图:⾷品在低⽔分含量范围内的吸湿等温(20℃)p26I区:⽔分⼦与羧基、氨基等离⼦基团以⽔-离⼦或⽔-偶极相互作⽤⽽牢固结合,是⾷品中最不易移动的⽔,主要为化合⽔和邻近⽔II区:主要靠⽔-⽔和⽔-溶质的氢键与邻近的分⼦缔合;主要为多分⼦层结合⽔III区:⾷品中结合最不牢固、最易移动的⽔;主要为体相⽔12.为什么不能根据冰点以下温度Aw预测冰点以上温度的Aw(⾷品在冰点点温度上下⽔分活度的⽐较):(1)在冰点以上,Aw是样品成分与温度的函数,前者是主要的因素;在冰点以下,Aw与样品的成分⽆关,仅与温度有关。
(完整版)食品化学复习(详细版)

食品化学江西科技师范大学授课老师:赵利谭政第一章引论1.食品化学:从化学的角度和分子水平研究食品的化学组成、结构、物理化学性质、功能性质、安全性质及食品加工贮藏过程中的变化。
2.食品的特点:安全无毒;有营养物质;赋有一定的色、香、味;内部组分之间不断发生反应和变化;容易受外界环境影响而发生变质。
食品的定义:是可供人类食用或饮用的物质。
3.食品的主要特性:颜色、风味、质构、营养价值。
第二章水1.水在食品中的作用?水对食品的外观形态、色泽、硬度、风味、鲜度等性质具有重要的影响。
水是微生物生长繁殖和生物体内化学反应的必需条件,关系到食品腐败变质的问题,影响到食品的耐贮性。
水是食品加工中的重要原料,水在食品中起着膨润、浸透、溶解、分散、均匀化等多种作用。
水可以除去食品加工中的部分有害物质。
水在食品加工制造中作为反应和传热的介质。
大多数食品加工的单元操作都与水有关2.为什么水冻结比解冻快?在0℃时,冰的导热率约为同温下水的导热率的4 倍,这意味着冰传导热能比非流动水(如食品原料组织中的水)快得多。
冰的热扩散率比水近乎大9 倍,这表明在一定的环境中,冰经受温度变化的速率比水快得多。
3.水分子为什么有强烈的缔合倾向?水分子呈V字样的形状,同时0-H键具有极性,这就是造成不对称的电荷分布和纯水在蒸汽状态时具有1.84D的偶极距。
水分子的极性产生了分子间吸引力,因而水分子具有强烈的缔合倾向。
4.水的三种结构模型:混合模型、连续模型、填隙式模型。
5.结合水的分类:化合水:结合最强的水,已成为非水物质的整体部分;邻近水:占据着非水成分的大多数亲水基团的第一层位置;多层水:占有第一层中剩下的位置以及形成了邻近水外的几层。
6.疏水水合和疏水相互作用以及笼状水合物及其作用:疏水水合:谁与非极性物质混合时,在这些不相容的非极性实体临近处,水形成了特殊结构,使得熵下降的过程。
疏水相互作用:如果存在两个分离的非极性基团,那么不相容的水环境将促进它们之间的缔合,从而减少H2O----非极性实体界面面积,这个热力学熵有力的过程就叫做疏水相互作用。
食品化学复习资料资料

第一章1食品化学:用化学的理论和方法研究食品本质的科学,它通过食品营养价值、安全性和风味特征的研究,阐明食品的组成、性质、结构和功能以及食品成分在贮藏、加工和运输过程中可能发生的化学、物理变化和生物化学变化的科学。
2食品化学的研究内容(1)研究食品的化学组成(2)揭示食品在加工、贮藏中发生的化学变化。
(3)研究食品贮藏、加工新技术,开发新产品和新的食物资源(4)研究化学反应的动力学行为和环境因素影响食品化学的实验应包括理化实验和感官实验。
第二章水1单个水分子的结构特征○1H2O分子的四面体结构有对称型○2H-O共价键有离子性○3氧的另外两对孤对电子有静电力○4H-O键具有电负性水分子在三维空间形成多重氢键键合—每个水分子具有相等数目的氢键给体和受体,能够在三维空间形成氢键网络结构。
2水分子缔合的原因由于每个水分子具有相等数目的氢键给体和受体,能够在三维空间形成氢键网络结构。
○1H-O键间电荷的非对称分布使H-O键具有极性,这种极性使分子之间产生引力。
○2由于每个水分子具有数目相等的氢键供体和受体,因此可以在三维空间形成多重氢键。
○3静电效应。
3水分子的结构特征○1水是呈四面体的网状结构。
○2水分子之间的氢键网络是动态的。
○3水分子氢键键合程度取决于温度(连续模型:分子间氢键均匀地分布于整个水样, 水分子的连续网络结构成动态平衡。
)水的结构模型:混合模型;连续结构模型;填隙结构模型4冰的结构○1冰是水分子有序排列形成的晶体。
○2水结冰时分子之间氢键连接在一起形成低密度(非常疏松)的刚性结构。
5冰的分类(按冷冻速度和对称要素分)冰有11种结晶类型,普通冰的结晶属于六方晶系的双六方双锥体。
另外,还有9种同质多晶和1种非结晶或玻璃态的无定型结构,在常压和温度0℃时,这11 种结构中只有六方型冰结晶才是稳定的形式。
○1六方型冰晶○2不规则树枝状结晶○3粗糙的球状结晶○4易消失的球状结晶及各种中间体6水与离子基团的相互作用由于水中添加可解离的溶质,使纯水靠氢键键合形成的四面体排列的正常结构遭到破坏。
食品和化学复习内容

Ⅱ 复习要点第一章 绪论食品化学定义:是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储藏和运销中的变化及其对食品品质和安全性影响的学科。
食品化学的研究范畴、研究方法食品化学主要包括食品营养成分化学、食品色香味化学、食品工艺中的化学、食品物理化学和食品有害成分化学及食品分析技术。
根据研究内容的物质分类,食品化学主要包括食品碳水化合物化学、食品油脂化学、食品蛋白质化学、食品酶学、食品添加剂、维生素化学、食品矿质元素化学、调味品化学、食品风味化学、食品色素化学、食品毒物化学和食品保健成分化学。
一般的研究方法为:①确定代表优质食品特征的相关性质②找出影响这些食品质量与安全的化学与生物化学反应 ③弄清相关的化学与生物化学反应是如何影响食品质量与安全的④将这些知识应用于食品加工与贮藏过程中。
第二章 水分水在食品中的作用:1 起着溶解、分散蛋白质、淀粉等水溶性成分的作用2 对食品的新鲜度、硬度、风味、流动性、色泽、耐贮性和加工适应性有影响3 是食品的的组成成分4 水起着膨润、浸透、均匀化等功能;食品体系中水的存在类型、定义与特点1结合水:又称束缚水或固定水,通常是指存在于溶质或其它非水组分附近的、与溶质分子之间通过化学键的力结合的那部分水。
【具有“被阻碍的流动性”,而不是“被固定化的”占总水量很小的一部分 】化合水,又称组成水是指与非水物质结合得最牢固并构成非水物质整体的那些水。
【1在-40℃下不结冰 2 无溶解溶质的能力 3 与纯水比较分子平均运动为0 4 不能被微生物利用】邻近水(单分子层水)是指处在非水组分亲水性最强的基团周围的第一层位置,与离子或离子基团缔合的水。
【1 在-40℃下不结冰 2 无溶解溶质的能力 3与纯水比较分子平均运动大大减少 4 不能被微生物利用】多层水是指位于上述所说的第一层的剩余位置的水和单分子层水的外层形成的另外几层水。
主要靠水-水,水-溶质氢键作用。
食品化学复习材料

1、食物:含有营养素的可食性物料。
食品:经特定方式加工后供人类食用的食物。
2、食品的基本营养成分:糖类、蛋白质、脂质、维生素、矿物质、水3、食品化学研究内容:(1)研究食品化学组成(2)揭示食品在加工贮藏中发生的化学变化(3)研究食品贮藏、加工新技术,开发新产品和新的食物资源(4)研究化学反应的动力学行为和环境因素的影响4、食品在加工储藏的变化(有哪些期望、哪些需要控制、举例)(1)苹果削皮、香蕉拨皮后变色:酚类化合物外溢,酚类很不稳定,在溢出过程中与多酚氧化酶接触,在多酚氧化酶的催化下,迅速氧化成褐色的醌类物质和水。
(2)在食品加工或储藏中可发生的变化分类(3)决定食品在储藏加工中稳定性重要因素①产品自身的因素: 各组成成分(包括氧化剂)的含量与化学性质、氧气含量,pH、水分活度(Aw)、玻璃化温度(Tg)玻璃化温度时的水含量(Wg)②环境因素: 温度(T)、处理时间(t)、大气成分、经受的化学、物理处理、见光、污染、极端的物理环境5、影响食品化学反应因素内在:自身组成成分影响;外在:温度、pH、光照、加工过程中所有仪器中所包含的金属离子等。
6、研究化学反应的动力学行为和环境因素的影响:淀粉糊化、老化、油脂的氧化、丙烯酰胺(丙烯酰胺:丙烯酰胺的危害是急性毒性,神经毒性和生殖发育毒性,遗传毒性,致癌性。
)1、水分子的缔合(小知识点)①H-O键间电荷的非对称分布使H-O键具有极性,这种极性使分子之间产生引力②由于每个水分子具有数目相等的氢键供体和受体,因此可以在三维空间形成多重氢键。
③静电效应。
另:a.由于每个水分子上有四个形成氢键的位点,因此每个水分子的可以通过氢键结合4个水分子;b.水分子之间还可以以静电力相互结合,因此缔合态的水在空间有不同的存在形式;c.不同的缔合形式,可导致水分子之间的缔合数大于4。
2、一般食品中的水均是溶解了其中可溶性成分所形成的溶液,因此其结冰温度均低于0℃。
3、按照食品中的水与其他成分之间相互作用强弱可将食品中的水分成:结合水和体相水水多层水化合水邻近水结合水体相水自由水滞化水4、结合水和体相水(又称:自由水、游离水)的区别5、水分活度:是指食品中水的蒸汽压与同温下纯水的饱和蒸汽压的比值,可用下式表示(水分活度比水分含量更能体现食物的稳定性)纯水:Aw =P/P0=1 食品:P<P0,0<Aw<1P为某种食品在密闭容器中达到平衡状态时的水蒸汽分压p0为在同一温度下纯水的饱和蒸汽压。
食品化学复习资料

食品化学复习资料①什么是食品化学?它的研究内容是什么?1.食品的化学组成及理化性质2.是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储藏和运销中的变化及其对食品品质和安全性影响的学科。
②试述食品中主要的化学变化及对食品品质和安全性的影响。
属性质地风味颜色营养价值安全性变化失去溶解性、失去持水性、质地变坚韧、质地柔软出现酸败、出现焦味、出现异味、出现美味和芳香褐变(暗色)、漂白(褪色)、出现异常颜色、出现诱人色彩蛋白质、脂类、维生素和矿物质的降解或损失及生物利用改变产生毒物、钝化毒物、产生有调节生理机能作用的物质③你希望从这门学科中学到什么以及对这门课程的教学有何建议?第二章1.名词解释:水分活度、水分吸附等温线、结合水、疏水水合作用、疏水相互作用、笼形水合物、滞后现象。
水分活度(wateractivity)是指食品中水的蒸汽压与该温度下纯水的饱和蒸汽压的比值,可用下式表示:Awppo水分吸附等温线(Moitureorptioniotherm,MSI)在恒定温度下,使食品吸湿或干燥,所得到的食品水分含量(每克干物质中水的质量)与Aw的关系曲线。
疏水水合(Hydrophobichydration):向水中添加疏水物质时,由于它们与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,使得熵减小,此过程称为疏水水合。
疏水相互作用(Hydrophobicinteraction):当水与非极性基团接触时,为减少水与非极性实体的界面面积,疏水基团之间进行缔合,这种作用称为疏水相互作用。
笼形水合物(Clathratehydrate):是象冰一样的包含化合物,水为“宿主”,它们靠氢键键合形成象笼一样的结构,通过物理方式将非极性物质截留在笼内,被截留的物质称为“客体”。
一般“宿主”由20-74个水分子组成,较典型的客体有低分子量烃,稀有气体,卤代烃等。
滞后现象(Hyterei):回吸与解吸所得的水分吸附等温线不重叠现象即为“滞后现象”(Hyterei)。
食品化学复习资料

绪论1:食品化学:是一门研究食品中的化学变化与食品质量相关性的科学。
2:食品质量属性(特征指标):色、香、味、质构、营养、安全。
第一章:水一:名词解释1:AW:指食品中水分存在的状态,即水分与食品结合程度(游离程度)。
AW=f/fo (f,fo 分别为食品中水的逸度、相同条件下纯水的逸度。
)2:相对平衡湿度(ERH): 不会导致湿气交换的周围大气中的相对湿度。
3:过冷现象:由于无晶核存在,液体水温度降到冰点以下仍不析出固体。
4:异相成核:指高分子被吸附在固体杂质表面或溶体中存在的未破坏的晶种表面而形成晶核的过程(在过冷溶液中加入晶核,在这些晶核的周围逐渐形成长大的结晶,这种现象称为异相成核。
)5:吸湿等温线(MSI):在一定温度条件下用来联系食品的含水量(用每单位干物质的含水量表示)与其水活度的图6:解吸等温线:指在一定温度下溶质分子在两相界面上进行的吸附过程达到平衡时它们在两相中浓度之间的关系曲线。
7:单层值(BET):单分子层水,量为BET,一般食品(尤为干燥食品)的水分百分含量接近BET时,有最大稳定性,确定某种食品的BET对保藏很重要。
8:滞后环:是退汞曲线和重新注入汞曲线所形成的圈闭线。
它反映了孔隙介质的润湿及结构特性。
9:滞后现象:MSI的制作有两种方法,即采用回吸或解吸的方法绘制的MSI,同一食品按这两种方法制作的MSI图形并不一致,不互相重叠,这种现象称为滞后现象。
二:简述题1:食品中水划分的依据、类型和特点。
答:以水和食品中非水成分的作用情况来划分,分为游离水(滞化水、毛细管水和自由流动水)和结合水【化合水和吸附水(单层水+多层水)】。
结合水:流动性差,在-40℃不会结冰,不能作为溶剂。
游离水:流动性强,在-40℃可结冰,能作为溶剂。
2:冰与水结构的区别答:水:由两个氢原子的s的轨道与一个氧原子的两个sp3杂化轨道形成两个σ共价键。
冰:由水分子构成的非常“疏松”的大而长的刚性结构,相比液态水则是一种短而有序的结构。
食品化学复习资料(全)

食品化学复习资料第一章引论一、名词解释:1、营养素:指那些能维持人体正常生长发育和新陈代谢所必需的物质。
2、食物:可供人类食用的含有营养素的天然生物体。
3、食品:经特定方式加工后供人类食用的食物。
4、食品化学:是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储存和运销过程中的变化及其对食品品质和安全性影响的科学。
二、问答题:1、食品在加工贮藏过程中发生的化学变化有那些?答:①、一般包括生理成熟和衰老过程中的酶促变化;②、水份活度改变引起的变化;③、原料或组织因混合而引起的酶促变化和化学反应;④、热加工等激烈加工条件引起的分解、聚合及变性;⑤、空气中的氧气或其它氧化剂引起的氧化;⑥、光照引起的光化学变化及包装材料的某些成分向食品迁移引起的变化。
2、为什么生物工程在食品中应用紧紧依赖于食品化学?答:①、生物工程必须通过食品化学的研究来指明原有生物原料的物性有哪些需要改造和改造的关键在哪里,指明何种食品添加剂和酶制剂是急需的以及它们的结构和性质如何;②、生物工程产品的结构和性质有时并不和食品中的应用要求完全相同,需要进一步分离、纯化、复配、化学改性和修饰,在这些工作中,食品化学具有最直接的指导意义;③、生物工程可能生产出传统食品中没有用过的材料,需由食品化学研究其在食品中利用的可能性、安全性和有效性。
3、食品化学的主要研究内容?答:研究食品中营养成分、呈色、香、味成分和有害成分的化学组成、性质、结构和功能;阐明食品成分在生产、加工、贮藏、运销中的变化,即化学反应历程、中间产物和最终产物的结构及其对食品的品质和卫生安全性的影响;研究食品贮藏加工的新技术,开发新的产品和新的食品资源以及新的食品添加剂等,构成了食品化学的主要研究内容。
4、食品化学研究方法与一般化学研究方法的区别?答:是把食品的化学组成、理化性质及变化的研究同食品的品质和安全性研究联系起来。
因此,从实验设计开始,食品化学的研究就带有揭示食品品质或安全性变化的目的,并且把实际的食品物质系统和主要食品加工工艺条件作为实验设计第二章水一、填空题1、冰的导热系数在0℃时近似为同温度下水的导热系数的 4 倍,冰的热扩散系数约为水的 5 倍,说明在同一环境中,冰比水能更快的改变自身的温度。
食品化学复习资料

在没有氨基化合物存在的条件下,将糖和糖浆直接加热熔融,在温度超过100℃时,糖分解变化形成黑褐色的焦糖,称为焦糖化反应。
由少数必须基团组成的能与底物分子结合并完成特定催化作用的空间小区域是酶的活性中心防腐剂是凡具有杀死微生物或抑制其增殖作用的物质。
.肉的成熟是动物屠宰后经僵直到软化,使肉产生最佳食用状态的过程脂肪酸通过酶催化α与β碳原子间的断裂、β-碳原子上的氧化,相继切下二碳单位而降解的方式称为脂肪酸的β氧化。
水分活度一个食品样品中水蒸气分压P与同一温度下纯水的饱和蒸气压P之比。
Aw=P/P无催化活性的酶分子称为酶原EMP途径葡萄糖无氧分解为丙酮酸的一系列化学变化过程,又称葡萄糖的酵解途径氨基酸的α-氨基与酮酸的α-酮基在转氨酶的作用下相互交换,使原来的α-氨基酸变为相应的α-酮酸,α-酮酸转变为相应的α-氨基酸,这个过程称为转氨基作用。
食品添加剂为改善食品品质和色、香、味,以及为防腐和加工工艺的需要而加入食品中的化学合成的或者天然的物质。
生色基能够在紫外可见区内吸光的基团当氧合肌红蛋白或血红蛋白在有氧的条件下加热,因珠蛋白变性,血红素的二价铁变为三价铁,生成黄褐色的变肌红蛋白,称为肌色质。
食品溶液或食品中可溶性成分溶于唾液中,刺激味蕾,进而刺激味觉神经传递到异化作用通过物质分解,将自身物质转化为外部物质的过程。
淀粉溶液在室温或者低于室温的条件下,硬度会变大,体积会减小,会变得不透明,甚至凝结而沉淀,这种现象称为淀粉的老化。
必需氨基酸人体不能合成而只能由食物供给的氨基酸。
分别是Lys Phe Val Met Trp Leu Ile Thr(His)酶的必需基团是酶蛋白中只有少数特定的氨基酸残基的侧链基团和酶的催化活性有直接关系,这些官能团称为酶的必需基团生物氧化糖类、脂肪和蛋白质等有机物质在生物体类的氧化分解,又叫细胞呼吸血色质是在缺氧的条件下,肌色质的中的三价铁还原为二价铁,生成粉红色的物质,称为血色质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
① 什么是食品化学?它的研究内容是什么?1. 食品的化学组成及理化性质2. 是从化学角度和分子水平上研究食品的化学组成、结构、理化性质、营养和安全性质以及它们在生产、加工、储藏和运销中的变化及其对食品品质和安全性影响的学科。
② 试述食品中主要的化学变化及对食品品质和安全性的影响。
③ 你希望从这门学科中学到什么以及对这门课程的教学有何建议?第二章1. 名词解释:水分活度、水分吸附等温线、结合水、疏水水合作用、疏水相互作用、笼形水合物、滞后现象。
水分活度(water activity)是指食品中水的蒸汽压与该温度下纯水的饱和蒸汽压的比值,可用下式表示: op p Aw 水分吸附等温线 (Moisture sorption isotherms,MSI)在恒定温度下,使食品吸湿或干燥,所得到的食品水分含量(每克干物质中水的质量)与Aw 的关系曲线。
疏水水合(Hydrophobic hydration):向水中添加疏水物质时,由于它们与水分子产生斥力,从而使疏水基团附近的水分子之间的氢键键合增强,使得熵减小,此过程称为疏水水合。
疏水相互作用( Hydrophobic interaction):当水与非极性基团接触时,为减少水与非极性实体的界面面积,疏水基团之间进行缔合,这种作用称为疏水相互作用。
笼形水合物(Clathrate hydrates):是象冰一样的包含化合物,水为“宿主”,它们靠氢键键合形成象笼一样的结构,通过物理方式将非极性物质截留在笼内,被截留的物质称为“客体”。
一般“宿主”由20-74个水分子组成,较典型的客体有低分子量烃,稀有气体,卤代烃等。
滞后现象(Hysteresis):回吸与解吸所得的水分吸附等温线不重叠现象即为“滞后现象”(Hysteresis)。
2. 请至少从4个方面分析Aw与食品稳定性的关系。
1.除脂肪氧化在Aw<时有较高反应外,其它反应均是Aw愈小反应速度愈小。
也就是说,对多数食品而言,低Aw有利于食品的稳定性。
2.Aw:范围内,水与脂类氧化生成的氢过氧化物以氢键结合,保护氢过氧化物的分解,阻止氧化进行。
水与金属离子水合,降低了催化性。
随A w↑,反应速度↓过分干燥,食品稳定性下降3.Aw:范围内,水中溶解氧增加,大分子物质肿胀,活性位点暴露加速脂类氧化,催化剂和氧的流动性增加,随Aw↑,反应速度↑4. Aw >随Aw↑,反应速度增加很缓慢,原因 : 催化剂和反应物被稀释,阻滞氧化3.简要说明水分与溶质的相互作用。
随着离子种类及所带电荷的不同,与水之间的相互作用也有所差别。
大致可以分作两类:1、有助于水分子网状结构的形成,水溶液的流动性小于水,如:Li+、Na+、H3O+、Ca2+、Ba2+、Mg2+、Al3+、OH-等。
2、能阻碍水分子之间网状结构的形成,其溶液的流动性比水大,此类离子如:K+、Rb+、Cs+、NH4+、Cl-、Br-、I-、NO3-、BrO3-等;实际上,从水的正常结构来看,所有的离子对水的结构都起破坏作用,因为它们能阻止水在0℃下结冰。
4.概括食品中的水分存在状态。
体相水(自由水,截流水):以毛细管力结合的水结合水(构成水,邻近水,多层水):以氢键结合力结合的水5.解释脂质氧化与水分活度的关系并说明原因。
脂质在Aw小于时,反应速度随着Aw增大而减小。
原因:水与脂类氧化生成的氢过氧化物以氢键结合,保护氢过氧化物的分解,阻止氧化进行。
水与金属离子水合,降低了催化性。
6.简要说明水分吸附等温线滞后现象产生的主要原因。
7.图中各区水的名称和性质。
区Ⅰ的水的性质:最强烈地吸附,最少流动,水-离子或水-偶极相互作用,在-40℃不结冰,不能作为溶剂,看作固体的一部分,占总水量极小部分区Ⅱ多层水大多数多层水在-40℃不结冰,其余可结冰,但冰点大大降低。
有一定溶解溶质的能力。
与纯水比较分子平均运动大大降低。
不能被微生物利用。
区Ⅰ和区区Ⅲ的水的性质:体相水被物理截留或自由的。
宏观运动受阻。
性质与稀盐溶液中的水类似。
占总水分的95%以上8.比较高于和低于冻结温度下的Aw时应注意的两个重要差别?9.为什么植物的种子和微生物的孢子能保持其生命力?是因为后者不含水分因此不受温度的影响吗?10.冰冻果蔬的伤害是低温使果蔬的代谢受阻所致。
第三章1. 名词解释:碳水化合物、糖的吸湿性(保湿性)、甜度、淀粉糊化(老化)、单糖、低聚糖、多糖、乳糖不耐症、变性淀粉、焦糖化反应、 Maillard反应、HM果胶、LM果胶、葡萄糖当量碳水化合物(Carbohydrates):多羟基醛或多羟基酮及其衍生物和缩合物。
吸湿性(糖在空气湿度较高情况下吸收水分的性质)顺序果糖>葡萄糖保湿性(糖在空气湿度较低条件下保持水分的性质)顺序葡萄糖>果糖甜度:是一个相对值,以蔗糖(非还原糖)为基准物,一般以10%或15%的蔗糖水溶液在20 ℃时的甜度为1。
影响甜度的因素:分子量越大溶解度越小,则甜度也小糖的不同构型(α、β型)淀粉的糊化:淀粉粒在适当温度下,破坏结晶区弱的氢键,在水中溶胀,分裂,胶束则全部崩溃,形成均匀的糊状溶液的过程被称为糊化。
本质:微观结构从有序转变成无序,结晶区被破坏。
老化:α-淀粉溶液经缓慢冷却或淀粉凝胶经长期放置,会变为不透明甚至产生沉淀的现象。
实质:是糊化后的分子又自动排列成序,形成高度致密的结晶化的不溶解性分子粉末。
单糖——不能再被水解的多羟基醛、酮,是碳水化合物的基本单位。
单糖又分为醛糖和酮糖。
低聚糖——由2-10个单糖分子缩合而成,水解后生成单糖。
多糖——由10个以上单糖分子缩合而成。
根据组成多糖的单糖种类,又分为均多糖和杂多糖。
乳糖不耐症:乳糖保留在小肠肠腔内,由于渗透压的作用,乳糖有将液体引向肠腔的趋势,产生腹胀和痉挛。
乳糖不耐症随着年龄增大而加重。
有两种方法可以克服乳糖酶缺乏的影响:一种方法是通过发酵如在生产酸奶和乳制品时除去乳糖;另一种方法是加入乳糖酶减少乳中乳糖。
变性淀粉:天然淀粉经适当的化学处理、物理处理或酶处理,使某些加工性能得到改善,以适应特定的需要,这种淀粉被称为改性淀粉或变性淀粉。
焦糖化反应:糖类物质在没有氨基化合物存在的情况下,加热到熔点以上(蔗糖200℃)时,糖发生脱水与降解并生成黑褐色物质的反应。
美拉德反应(Maillard Reaction) :食品中的还原糖与氨基化合物发生缩合、聚合生成类黑色素物质的反应,又称羰氨反应。
反应物三要素:氨基化合物、还原糖和水酯化度(DE):酯化的半乳糖醛酸残基(羧基)数占半乳糖醛酸残基总数的百分数。
高甲氧基果胶— HM DE>50%低甲氧基果胶— LM DE<50%葡萄糖当量:2. 试述Maillard 反应及其影响因素,并举一例说明其在食品中的应用。
抑制不期望的Maillard 反应有哪些措施?在食品中的作用? 始和引发阶段: a. 氨基和羰基缩合——葡基胺 b. Amadori 分子重排——醛糖中间阶段 c. 糖脱水d. 糖裂解e. 氨基酸降解后期阶段f. 醇、醛缩合g. 胺-醛缩合——褐色色素影响因素:糖的种类:戊糖 > 已糖 > 双糖, 半乳糖 > 甘露糖 > 葡萄糖 > 果糖, 醛糖 > 酮糖 氨基酸:胺类 > 氨基酸、肽 > 蛋白质;碱性氨基酸(末端)的氨基易褐变,如赖AA 、精AA 、组AA 。
温度:T ↑,速度↑,每增加10℃,速度↑3-5倍。
30℃以上加快,20℃以下变慢,故低温可防止褐变。
氧气:室温下氧能促进褐变,氧促进V C 、脂肪氧化褐变。
水分:10-15%含水量最易褐变,干燥食品,褐变抑制,如冰淇淋粉的含水量<3%,不易褐变。
pH :pH>3时,pH ↑,速度↑,pH= ,速度增加快 pH ≤6,速度增加慢。
金属:催化Maillard 反应,速度↑(Fe 3+ ,Fe 2+ ) 亚硫酸盐:阻止生成N-葡萄糖基胺抑制美拉德:稀释或降低水分含量,注意选择原料:如土豆片,选氨基酸、还原糖含量少的品种,一般选用蔗糖。
降低pH :常加酸,如柠檬酸,苹果酸。
降低温度,除去一种作用物:如热水烫漂,除去部分可溶固形物,降低还原糖含量。
加入葡萄糖转化酶,除去糖,减少褐变色素形成早期加入还原剂(如亚硫酸盐),可起到脱色效果。
用来衡量淀粉转化为D-葡萄糖的程度定义:还原糖(按葡萄糖计)在玉米糖浆中的百分比DE 反映水解程度大小的指标 当DE ↑,更多的寡糖,更少的多糖当DE ↑,更甜和粘性更小的产品美拉德反应对食品的影响:色泽——希望和不希望风味——美拉德反应产品能产生牛奶巧克力的风味。
当还原糖与牛奶蛋白质反应时,美拉德反应产生乳脂糖、太妃糖及奶糖的风味。
营养——还原糖与氨基酸的反应破坏氨基酸,特别是必需氨基酸L-赖氨酸所受的影响最大,赖氨酸含有ε-氨基,即使存在于蛋白质分子中也能参与美拉德反应。
安全——已从烧煮和油炸的肉和鱼以及牛肉的浸出物中分离得到诱变杂环胺。
3. 简要说明淀粉糊化的三个阶段及其特点。
4. 简述碳水化合物、单糖、低聚糖和多糖之间的相互关系。
碳水化合物从结构上定义为多羟基醛或多羟基酮及其聚合物或衍生物的总称,包括单糖、低聚糖和多糖。
单糖,是糖类物质最基本的单位,不能进一步水解,从分子结构上看,它们是含有一个自由醛基或酮基的多羟基醛或多羟基酮类化合物;低聚糖,又称寡糖,是由2~10个单糖通过糖苷键连接形成的直链或支链低聚合度糖类;多糖,是由10个以上的单糖通过糖苷键连接而成的一类化合物。
5. 影响淀粉的糊化、老化的因素有哪些?结构:直链淀粉<支链淀粉。
Aw:Aw提高,糊化程度提高。
糖:高浓度的糖水分子,使淀粉糊化受到抑制。
盐:高浓度的盐使淀粉糊化受到抑制;低浓度的盐存在,对糊化几乎无影响。
温度:温度越高,糊化程度越大。
6. HM、LM果胶的胶凝机理。
条件:(糖-酸-果胶凝胶)糖>55%,~,果胶=~%,室温~100℃机理:酸的作用——阻止羧基离解,中和电荷,胶束结晶、凝聚而形成凝胶。
糖的作用——脱水以减少胶粒表面的吸附水。
促进形成链状胶束,形成果胶分子间氢键。
胶束失水后而凝聚(结晶沉淀),形成一种具有一定强度和结构类似海绵的凝胶体。
空隙处吸附着糖—水分子。
7.简述食品中单糖、多糖的作用及功能。
单糖:(1)甜味剂(2)亲水功能(吸湿性或保湿性)(3)防腐功能(4)结晶功能(5)其他功能多糖:生理功能:(1)膳食纤维:①很高的持水力;②对阳离子有结合交换能力;③对有机化合物有吸附螫合作用;④具有类似填充的容积;⑤可改变肠道系统中的微生物群组成。
(2)真菌多糖:增强免疫,降血糖,降血脂,抗肿瘤,抗病毒。
如香菇多糖,人参多糖,灵芝多糖和茶叶多糖等水的结合功能:增稠剂,胶凝剂,澄清剂等8.豌豆在贮藏过程中甜度降低的原因是?香蕉贮藏后变甜,为什么?淀粉是豌豆种子中最重要的贮藏性多糖,豌豆等豆类中的淀粉含量与其老熟程度成正比,豌豆在贮藏过程中可溶性糖大量合成淀粉使其甜度降低,香蕉富含淀粉,在贮藏过程中,淀粉在酶的作用下不断水解,从而使可溶性糖的含量增加,甜度增加。
