有机化学考研知识点总结
有机化学考研知识点总结

H
B 消去
2)水合反应
CC
H 2O, H 2SO 4 H2SO 4
CC H OH
X
含有吸电子基团,
为反马氏产物
【特点】反式共平面加成、
马氏加成物、重排
3) 加X2反应
X2
CC
CC XX
【特点】反式加成、马 氏加成产物
16
第二节 有机化学的基本反应
4)加XOH反应
CC
X OH
5)硼氢化-氧化反应
CC
3. 考虑反应的区域选择性问题:消除反应:扎依切夫规则还是霍夫 曼规则; 加成反应:马氏规则还是反马氏规则; 重排反应:哪个基团迁移、 不对称酮的反应:热力学控制还是动力学控制等。
4. 考虑立体选择性问题:消除反应:顺消还是反消、加成反应:顺 加还是反加、重排反应:构型保持还是构型翻转、SN1:重排、SN2:构型 翻转等。
歧化反应
按电荷行协为同:反亲应电—反—应周环亲反核应反应
D-A反应
9
第二节 有机化学的基本反应
一、取代反应 ——自由基取代、亲电取代和亲核取代 1.自由基取代 【特点】有自由基参与、光照、加热或过氧化物存在 【注意】 ①烷烃的卤代一卤代较差,溴卤代的选择性较好
hv
CH3CH 2CH 3 + Cl2
13
RONO 2 + AgX
第二节 有机化学的基本反应
2) 羰基化合物亲核加成-消除反应
O
O
C + Nu H R R' 亲核试剂
R C Nu + HR'
F
3) 重氮盐取代反应 【特点】低温环境,强酸介质
【应用】制备芳香族亲电取代 反应难制备的化合物
有机化学70条必考知识点

有机化学70条必考知识点1. 有机化合物的结构与性质2. 有机化合物的命名3. 共轭体系和共轭结构4. 反应机理和反应类型5. 键的构成和键的性质6. 分子结构的立体化学7. 共价键和离子键的区别8. 化学平衡和化学反应速率9. 酸碱性和电离常数10. 功能团和官能团11. 有机反应的官能团转化12. 手性和光学异构体13. 利用IR、NMR等光谱技术进行结构分析14. 醇、酚和醚的结构和性质15. 醛、酮和酸的结构和性质16. 烯烃和炔烃的结构和性质17. 脂肪族和芳香族化合物的结构和性质18. 卤代烃的结构和性质19. 胺和氨基酸的结构和性质20. 脂类和类固醇的结构和性质21. 环状化合物的结构和性质22. 多官能团化合物的结构和性质23. 羧酸和酰氯的结构和性质24. 酯和醚的结构和性质25. 脂肪酸和脂肪酰胺的结构和性质26. 酰胺和酰亚胺的结构和性质27. 杂环化合物的结构和性质28. 聚合物的结构和性质29. 核磁共振谱和质谱的基本原理和应用30. 红外光谱和紫外-可见光谱的基本原理和应用31. 加成反应和消除反应32. 反应活化能和反应速率常数33. 亲电试剂和亲核试剂的选择性34. 高分子合成的反应机理和方法35. 环加成和开环反应的机理36. 键的断裂和键的形成37. 光化学反应和自由基反应机理38. 自由基取代反应和自由基加成反应39. 卤代烃的亲核取代反应40. 消除反应的机理和方法41. 酮醇互变和糖的结构和性质42. 羧酸衍生物的反应性和应用43. 脂肪酸的氧化反应和酯的加水反应44. 胺的取代反应和胺的碱性45. 光化学和热化学反应的比较46. 共轭体系和共轭结构的形成47. 有机金属化合物的结构和性质48. 有机催化剂的种类和应用49. 有机合成的策略和方法50. 稠环化合物的合成和反应51. 化学反应的立体选择性52. 共轭双键的反应性和应用53. 置换反应和消除反应的比较54. 共轭体系的光电性质55. 烯烃的环加成反应和环开合反应56. 键的极性和官能团的电子效应57. 氨基酸和多肽的结构和性质58. 鸟苷和核苷酸的结构和性质59. 生物大分子的结构和性质60. 有机化学在药物合成中的应用61. 有机化学在农药合成中的应用62. 有机化学在材料科学中的应用63. 有机化学在能源领域中的应用64. 有机化学在环境保护中的应用65. 有机化学在食品科学中的应用66. 合成方法的优化和反应条件的选择67. 有机化合物的分离和提纯技术68. 有机化合物的催化反应和催化剂的设计69. 有机合成中的手性识别和手性选择性控制70. 有机化学的前沿领域和新发展。
有机化学考研超强总结(知识点精要-例题)

1 _ 戊烯 _ 4 _ 炔
CH=CH2
1
C1 H3C2
CCH
34
CH
5
2C6 H
C7 HC8 H3
5 _ 乙烯基 _ 2 _ 辛烯 _ 6 _ 炔
4 取代基的书写位置按取代基的“优先次序”规 则,即根据与主链所连原子的原子序数大小, 原子序数小的放前面,原子序数大的放后面
关于“最低系列” :
所谓“最低系列”是指当碳链以不同方向编 号,得到两种或两种以上不同的编号序列时,则 顺次逐项比较各序列的不同位次,首先遇到位次 最小者,定为“最低系列”。
例如:
OH
1
2
3 4 56
C6H3C5HC4 H2C3 HC2 HC1 H3
OH OH 2,3,5_ 己三醇 不叫2,4,5 _ 己三醇
O CH
醛基 甲酰基
O C
羰基
OH
羟基
SH
巯基
OOH
C=C
C=C
NH2 > -R
氢过氧基 碳碳叁键 碳碳双键 氨基 烷基
OR
烷氧基
X(F , Cl , Br , I)
卤原子
NO2
硝基
2 选择含有母体官能团的最长碳链作主链 3 对主链进行编号,首先保证母体官能团所对
应的碳位号最小,然后使取代基的位号最小, 遵循“最低系列”原则
2°当最小基团位于竖线时,若其余三个基团由大→中→小为反 时针方向,则此投影式的构型为R,反之为S。
含两个以上C*化合物的构型或投影式,也用同样方法对每一个 C*进行R、S标记,然后注明各标记的是哪一个手性碳原子。
例如:
CH3 2
C HO
H
3 CH3 C
有机化学知识点总结超全

有机化学知识点总结超全完整版
一、有机化学基础:
1. 元素组成:有机物主要由C、H、O、N、S等元素组成。
2. 元素的相互作用:有机物中的各种元素之间可以通过键的形成而形成不同的化合物,如单键、双键、三键等。
3. 化学键的强弱:根据原子间的相互作用,分为共价键和非共价键,其中共价键是最强的,非共价键较弱。
4. 分子的结构:有机物的分子结构包括碳链、环状结构和含氧结构等。
5. 稳定性:有机物的稳定性取决于其分子结构,稳定性越高,则该物质的活性越低。
二、有机反应:
1. 加成反应:一种有机反应,是一种常见的有机反应,两个有机物聚合在一起,结果是新物质,也就是反应物质。
2. 氧化还原反应:有机物构成的复杂反应,它是有机物之间改变氧化状态的反应,氧化反应会使有机物的氧化状态变高,而还原反应则会降低有机物的氧化状态。
3. 酯化反应:酯化反应是将一个有机物和一个醇或羟基反应,生成一个酯化物的反应。
4. 水解反应:利用水对有机物进行水解反应,生成物质的反应,此反应可以将水分子分解成两个离子:氢离子和氧离子。
5. 还原反应:有机物的还原反应是指将氧的氧化状态从氧的高氧化状态还原为氧的低氧化状态,以达到物质变化的目的。
化学考研有机化学重点知识点

化学考研有机化学重点知识点有机化学作为化学考研的重要一部分,是许多考生需要重点关注的内容。
本文将介绍化学考研有机化学的重点知识点,以帮助考生有针对性地进行学习和复习。
一、有机化学的基本概念与原理有机化学是研究碳和碳的化合物的科学,其中包括了有机物的结构、性质、合成和反应等内容。
有机化合物的特点是含有碳元素,具有丰富多样的结构和性质。
有机化学所研究的反应主要包括取代、加成和消除等。
二、有机化合物的命名与结构有机化合物的命名是有机化学中非常重要的一部分,正确的命名可以准确地表示化合物的结构和性质。
常见的命名方法包括系统命名法、功能团命名法和摩尔命名法等。
在进行命名时,需要熟悉常见的有机官能团和它们在结构中的位置、数量等信息。
三、有机反应的类型和机理有机反应可以分为取代反应、加成反应、消除反应和重排反应等几种类型。
每种反应都有其特定的机理和条件,需要考生熟悉常见的有机反应类型、反应条件以及反应机理等。
掌握反应的机理有助于理解有机反应的规律和特点。
四、官能团的转化和合成在有机化学中,官能团的转化和合成是重要的知识点。
通过不同的反应可以将一个官能团转化为另一个官能团,实现有机化合物的合成。
考生需要掌握官能团之间的相互转化关系,具体的合成方法和途径,以及一些重要有机化合物的合成方法。
五、有机化学的分析方法有机化学的分析方法主要包括光谱分析、质谱分析和色谱分析等。
光谱分析包括紫外可见光谱、红外光谱和核磁共振等;质谱分析主要用于确定化合物的相对分子质量和分子结构;色谱分析常用于分离和检测化合物。
考生需要了解各种光谱和色谱的基本原理和应用,以及如何正确地解读和分析光谱数据。
六、有机化学的应用领域有机化学广泛应用于生物医药、材料科学、环境保护等领域。
生物医药方面,有机化合物常用于药物的合成和结构修饰;材料科学中,有机聚合物和高分子材料的合成是重要的研究内容;环境保护方面,研究有机化合物在环境中的存在和归趋对于环境修复和保护非常重要。
(完整版)【非常详细】有机化学知识点归纳

有机化学知识点归纳一、有机物的结构与性质1 、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
原子: —X官能团 原子团(基): —OH 、—CHO (醛基) 、—COOH (羧基) 、C 6H 5— 等化学键: C=C 、—C≡C—2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无 ;通式: C n H 2n+2;代表物: CH 4B) 结构特点:键角为 109°28′,空间正四面体分子。
烷烃分子中的每个 C 原子的四个价键也都如此。
C) 物理性质: 1.常温下,它们的状态由气态、液态到固态,且无论是气体还是液体,均为无色。
一般地, C1~C4 气态, C5~C16 液态, C17 以上固态。
2.它们的熔沸点由低到高。
3.烷烃的密度由小到大,但都小于 1g/cm^3 ,即都小于水的密度。
4.烷烃都不溶于水,易溶于有机溶剂D) 化学性质:①取代反应(与卤素单质、在光照条件下)CH 4 + Cl 2 CH 3Cl + HCl , CH 3Cl + Cl 2 CH 2Cl 2 + HCl ,……。
点燃②燃烧 CH 4 + 2O 2 CO 2 + 2H 2O高温C 16H 34 催化剂C 8H 18 + C 8H 16加热、加压④烃类燃烧通式: C x H t + (x +y )O 2 点———燃 xCO 2 + y H 2O 4 2⑤烃的含氧衍生物燃烧通式 : C x H y O z + (x +y - z )O 2 点———燃 xCO 2 + yH 2O 4 2 2E) 实验室制法:甲烷: CH 3 COONa + NaOHOCH 4 个 +Na 2 CO 3△注: 1.醋酸钠:碱石灰=1: 3 2.固固加热 3.无水(不能用 NaAc 晶体) 4.CaO :吸水、稀释 NaOH 、不是催化剂(2)烯烃:A) 官能团: C=C ;通式: C n H 2n (n≥2);代表物: H 2C=CH 2B) 结构特点:键角为 120° 。
有机化学考研复习知识点总结

有机化学考研复习知识点总结●一、有机化合物命名●1、系统命名法●饱和碳原子和氢原子的分类:碳原子(伯、仲、叔、季),氢原子(伯、仲、叔)●烃基的名称:常用烃基的名称及缩写,如:甲基(Me-)、乙基(Et-)、正丁基(n-Bu-)、苯基(Ph-)、芳基(Ar-)等。
●系统命名法原则及各类有机化合物的命名:选择含特征官能团的最长碳链作主链,从靠近官能团的一端开始编号,取代基命名时排序按“次序规则”。
●2、顺、反异构体命名●顺、反命名法:两个相同基团在双键同侧的为顺式,异侧的为反式。
●Z、E命名法:按‘次序规则’,优先基团在双键同侧的为Z型,异侧的为E型。
●3、含手性碳原子的手性分子命名● R、S命名法:手性碳原子(C*)构型的确定,先将连在手性碳原子上的四个原子或基团按“次序规则”排序,将次序最低的基团远离观察者,其余三个基团的次序由大到小为顺时针排列时,记为‘R构型’,逆时针排列记为‘S构型’。
●4、多官能团化合物的命名●当化合物中含有多个官能团时,应选取其中的一个作为母体官能团,其余的官能团作为取代基(个别有例外)。
●一些母体官能团按以下出现的先后顺序进行选择:—COOH,—SO3H,—COOR,—COCl,—CONH2,—CN,—CHO,-C=O,—OH,—SH,—NH2,—C≡C—,—C=C—,—OR,—R,—X,—NO2。
●例如:CH3COCH2CH2CH2CH2OH 6-羟基-2-己酮;CH2=CHCH2CH2C≡CH1-己烯-5-炔。
●5、一些常用见化合物的习惯名称(俗名)或名称缩写●如:氯仿、季戊四醇、肉桂醛、苦味酸;THF、NBS、TNT、DMSO、DMF等。
●二、有机化合物结构●1、同分异构●异构体类型:构造异构(碳链、官能团位置、官能团);立体异构(构象、顺反、对映)。
●异构体书写:常见或结构较为简单化合物的同分异构体。
如写分子式为C5H10、C5H12的同分异构体等。
●互变异构现象:酮式—烯醇式结构的互变异构、糖类链状与环状结构互变异构等。
非常详细有机化学知识点归纳

非常详细有机化学知识点归纳【非常详细有机化学知识点归纳】一、烃类化合物1. 烷烃:碳原子间只有单键,可以分为直链烷烃和环烷烃。
2. 烯烃:碳原子间存在一个或多个双键,可以分为直链烯烃和环烯烃。
3. 炔烃:碳原子间存在一个或多个三键。
4. 芳香烃:由苯环(六个碳原子呈六角形相连)及其衍生物组成,具有芳香性质。
二、官能团与功能团1. 羟基(-OH):醇是含有羟基的有机化合物,按照羟基的数量可分为一元醇、二元醇等。
2. 卤素(-X):取代烃中的氢原子,可以产生卤代烃(如氯代烷、溴代烷等)。
3. 羰基(C=O):酮和醛都含有羰基,区别在于酮羰基连接在碳链中间,而醛羰基连接在碳链末端。
4. 羧基(-COOH):羧酸是含有羧基的有机酸,包括脂肪酸、芳香酸等。
5. 氨基(-NH2):胺是含有氨基的有机化合物,可以分为一级胺、二级胺和三级胺。
6. 脂肪族取代基:以烷基为代表,如甲基(-CH3)、乙基(-C2H5)等。
7. 芳香族取代基:以芳香环为代表,如苯基(-C6H5)等。
三、立体化学1. 手性:分子的非对称性,手性分子可分为左旋体和右旋体。
2. 手性中心:一个碳原子上连接了四个不同取代基,产生手性分子。
3. 光学异构体:在手性分子中,左旋体和右旋体互为光学异构体。
4. 构象异构体:分子在空间中构象上的不同,如顺反异构体和环状异构体。
四、反应类型1. 加成反应:两个或多个分子结合而形成一个新分子,可分为电子亲和性和亲核性加成反应。
2. 消除反应:一个分子分解为两个或多个产物,产物中一些原子或基团结合成新键。
3. 取代反应:一个基团被另一个基团取代,分为亲电取代和自由基取代。
4. 氧化还原反应:电子的转移导致氧化态和还原态的变化。
五、反应机理1. 亲电加成机理:亲电试剂攻击亲核试剂中的部分,形成新的化学键。
2. 亲核加成机理:亲核试剂攻击亲电试剂中的部分,形成新的化学键。
3. 酸催化机理:酸性催化剂作用下,转移质子或更强的亲电基团被引入反应中。
有机化学考研超强总结(知识点精要例题)

蒸馏法
萃取法
结晶法
色谱法
利用物质沸点的不同,通过加热和冷 凝的方法将不同沸点的物质分离。
通过控制温度等条件使物质在溶剂中 结晶析出,再通过过滤和洗涤得到纯 品。
有机化合物的结构鉴定方法
核磁共振波谱法
通过分析原子核自旋磁矩的共振信号,确 定物质分子结构中的氢原子类型和数目。
有机合成
通过一系列有机反应,将 简单原料转化为复杂有机 化合物的过程。
有机化学中的键与分子结构
共价键
原子之间通过共享电子形 成的化学键,决定了分子 的基本结构。
分子轨道
分子中的电子在运动过程 中所处的空间位置,决定 了分子的电子结构和性质。
分子构型
分子中原子的排列方式, 决定了分子的立体结构和 性质。
烷烃的取代反应机理
自由基取代反应
在光、热或自由基引发剂的作用 下,烷烃分子中的氢原子被其他 基团取代。
离子型取代反应
烷烃在强酸或强碱的作用下,先 形成碳正离子或碳负离子,然后 与试剂发生取代反应。
协同反应
烷烃在某些条件下,可以经过过 渡态直接进行取代反应,不需要 经过自由基或离子中间体。
烯烃的加成与消除反应机理
A 红外光谱法
通过分析物质对红外光的吸收特征, 确定物质中存在的官能团和化学键 的类型。
B
C
D
X射线衍射法
通过分析X射线在晶体中的衍射现象,确 定物质分子中原子的排列方式和空间构型。
质谱法
通过分析带电粒子在电场和磁场中的运动 规律,确定物质分子量和官能团的结构信 息。
05
有机化学考研例题解析
有机化学选择题解析
有机化学知识点总结归纳(全)

催化剂加热、加压有机化学知识点归纳一、有机物的结构与性质1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 结构特点:键角为109°28′,空间正四面体分子。
烷烃分子中的每个C 原子的四个价键也都如此。
C) 物理性质:1.常温下,它们的状态由气态、液态到固态,且无论是气体还是液体,均为无色。
一般地,C1~C4气态,C5~C16液态,C17以上固态。
2.它们的熔沸点由低到高。
3.烷烃的密度由小到大,但都小于1g/cm^3,即都小于水的密度。
4.烷烃都不溶于水,易溶于有机溶剂 D) 化学性质:①取代反应(与卤素单质、在光照条件下) , ,……。
②燃烧 ③热裂解C 16H 34 C 8H 18 + C 8H 16④烃类燃烧通式:O H 2CO O )4(H C 222y x y x t x +++−−−−→−点燃⑤烃的含氧衍生物燃烧通式: O H 2CO O )24(O H C 222y x z y x z y x +-++−−−−→−点燃E) 实验室制法:甲烷:3423CH COONa NaOH CH Na CO +→↑+注:1.醋酸钠:碱石灰=1:3 2.固固加热 3.无水(不能用NaAc 晶体) 4.CaO :吸水、稀释NaOH 、不是催化剂(2)烯烃:A) 官能团:;通式:C n H 2n (n ≥2);代表物:H 2C=CH 2 B) 结构特点:键角为120°。
双键碳原子与其所连接的四个原子共平面。
CH 4 + Cl 2CH 3Cl + HCl 光CH 3Cl + Cl 2CH 2Cl 2 + HCl 光CH 4 + 2O 2CO 2 + 2H 2O 点燃CH 4C + 2H 2高温 隔绝空气C=C 原子:—X原子团(基):—OH 、—CHO (醛基)、—COOH (羧基)、C 6H 5— 等化学键: 、—C ≡C — C=C 官能团CaO △催化剂C) 化学性质:①加成反应(与X 2、H 2、HX 、H 2O 等)②加聚反应(与自身、其他烯烃) ③燃烧 ④氧化反应 2CH 2 = CH 2 + O 2 2CH 3CHO⑤烃类燃烧通式:O H 2CO O )4(H C 222y x y x y x +++−−−−→−点燃 D) 实验室制法:乙烯:CH 3CH 2OH CH 2CH 2浓H 2SO 4+↑H 2O 170℃注:1.V 酒精:V 浓硫酸=1:3(被脱水,混合液呈棕色)2. 排水收集(同Cl2、HCl )控温170℃(140℃:乙醚) 3.碱石灰除杂SO2、CO2 4.碎瓷片:防止暴沸E) 反应条件对有机反应的影响:CH 2=CH -CH 3+HBr CH3CH CH 3Br(氢加在含氢较多碳原子上,符合马氏规则)CH 2=CH -CH 3+HBrCH 3-CH 2-CH 2-Br (反马氏加成)F )温度不同对有机反应的影响:CH 2CH CH CH 280℃CH 2CH CH CH 2Br Br+ Br 2CH 2CH CH CH 260℃CH 2CHCH CH 2BrBr + Br 2(3)炔烃:A) 官能团:—C≡C— ;通式:C n H 2n —2(n ≥2);代表物:HC≡CHB) 结构特点:碳碳叁键与单键间的键角为180°。
有机化学考研超强总结知识点精要_例题

有机化学考研超强总结知识点精要_例题有机化学是考研化学的难点之一,因此要想在考试中取得好成绩,必须充分掌握有机化学的知识点和解题技巧。
本文将从例题的角度出发,对有机化学考研超强总结知识点进行精要概括,希望对考生有所帮助。
一、反应机理在有机化学中,反应机理是非常重要的一个环节。
掌握反应机理不仅有助于理解反应的过程和特点,还能够快速判断反应中心和键的断裂方式,从而更好地解决问题。
1.加成反应的机理加成反应是有机化学中比较常见的一种反应。
通常情况下,加成反应的机理可以分为两类:电子亲和反应机理和电子供给反应机理。
其中,电子亲和反应机理指的是亲电试剂核心攻击亲核试剂上的电子,而电子供给反应机理则是亲核试剂攻击亲电试剂上的电子。
举个例子,当我们将一分子HBr加入到乙烯中时,那么此时HBr中的H+离子就会通过电子亲和反应机理攻击乙烯中的双键电子。
随后,Br-离子会通过电子供给反应机理将电子输送到H+和乙烯生成物之间,从而形成1-溴乙烷。
2.消除反应的机理在消除反应中,通常会涉及到两个相邻的碳原子之间的反应。
在反应中,首先会发生质子酸性的离子负载,随后将会发生碳-碳键的断裂,最终形成不同的分子。
例如,在进行加热时,丁烷可以发生β消除反应。
在反应中,首先丁烷将失去两个相邻的氢原子,随后将发生碳-碳键的断裂。
最终,丁烯和H2气体会形成。
二、Fischer 折叠Fischer 折叠是有机化学中一种非常重要的工具,它可以直接确定有机分子的立体结构。
因此,掌握 Fischer 折叠的基本知识和方法非常必要。
1. Fischer 折叠法Fischer 折叠法是将平面上的分子折叠成它们的三维结构,这种折叠通常涉及到并列的平面环或垂直的平面环。
具体方法是,我们可以首先将分子折叠成一个所谓的反Y形,随后立体化学环节可以通过一系列的折叠来实现。
2. Fischer 行列式符号Fischer 行列式符号是一种表示具有对称和反对称兄弟关系的立体中心的方式,即 b、d、h 和 v 等。
(完整版)有机化学主要考点

有机化学主要考点第一部分 烃一、烷烃。
通式C n H n 2+2能发生取代反应,例如CH 4+Cl 2 光 CH 3Cl +HCl 。
(条件:C12、Br 2、光照) 二、烯烃。
通式:C n H n 2 二烯烃通式为C n H 22-n 官能团: C=C (碳碳双键)、CH 2=CH 2六个原子共面。
性质:①氧化反应:烯烃能使KM n O 4(H +)的紫红色褪去。
②加成反应:烯烃能使溴的四氯化碳红棕色褪去。
(或溴水) CH 2=CH 2+B 2r →③加聚反应:烯烃能发生加聚反应。
例如:n CH 2=CH 2催化剂[2-CH 2]n三、炔烃。
通式:C n H 22-n HC ≡CH 四个原子共直线,官能团:-C ≡C-性质:与烯烃的性质类似,比如能发生 ①氧化反应 ②加成反应 ③加聚反应 四、芳香烃。
苯和苯的同系物的通式:C n H 62-n (n ≥6) 分子中12个原子共平面。
苯的性质:①取代反应 +B 2r (l ))(Fe 催 –B r +HB r (B 2r 的水溶液不发生此反应)+HO-NO 242SO H 浓 -NO 2+H 20 (也叫硝化反应)鉴别②加成反应: +3H 2催苯的同系物的性质,比如甲苯3CH ①氧代反应:能使KM n O 4(H +)溶液褪色②取代反应3CH +3HONO 242SO H 浓 +3H 20第二部分 烃的衍生物一、卤代烃。
(官能团-B r )性质:①取代反应(水解反应)C 2H 5-B r +H-OH NaOH C 2H 5-OH+HB r 或C 2H 5B r +N a ON C 2H 5OH +N a B r 。
②消去反应:C 2H 5 B r + N a ON 醇 C 2H 4(CH 2= CH 2)+ N a B r +H 2O或写成:C 2H 5 B r醇/NaOH CH 2=CH 2 +HB r二、醇。
官能团:-OH 饱和一元醇的通式:C n H 22+n O 。
化学考研有机化学重要知识点总结

化学考研有机化学重要知识点总结一、有机化学的基本概念有机化学是研究碳及其化合物的科学,是近代化学的重要分支。
有机化合物的特点是含有碳元素,并且通常与氢、氧、氮等元素形成共价键。
有机化学中的基本概念包括原子、分子、化学键、官能团等。
二、有机化学的反应类型有机化学的反应类型丰富多样,常见的有加成反应、消除反应、置换反应、酸碱反应等。
这些反应类型时化学考研中重要的知识点,需要掌握其反应机理和实际应用。
三、有机化学键的构成有机化学中的化学键主要由共价键构成。
共价键是通过原子之间的电子共享形成的,共价键的形成与电子排布、轨道杂化等有关。
对于不同的原子,其化学键具有不同的稳定性和能量。
四、有机物的结构与命名有机物的结构与命名是有机化学非常重要的一部分。
有机化合物的结构由分子式、结构式、立体式等表示。
对于复杂的有机化合物,通常需要使用系统命名法进行正规命名。
五、有机物的共轭体系共轭体系是一种特殊的电子结构,可以影响有机化合物的性质和反应。
共轭体系的形成与电子的共轭排布有关。
六、有机反应的机理化学考研中重要的一个知识点是有机反应的机理。
有机反应的机理是指反应物转变为产物的步骤和中间体的形成。
掌握有机反应的机理有助于理解反应的本质和规律。
七、有机功能团与官能团的化学性质有机功能团是有机化合物中具有特定化学性质的团体。
不同的官能团具有不同的化学性质和反应类型,例如醇、醚、醛、酮等。
八、有机化学中的重要实验技术和仪器在化学考研中,实验技术和仪器也是重要的知识点。
有机化学中常用的实验技术包括重结晶、提取、蒸馏等,而常用的仪器有红外光谱仪、质谱仪等。
九、有机化学的应用领域有机化学在生物医药、材料科学、环境保护等领域具有重要应用价值。
掌握有机化学的基本知识和实际应用有助于在相关领域的研究和开发工作中取得积极的成果。
总结:有机化学是化学考研中的重要内容,需要掌握基本概念、反应类型、化学键构成、结构与命名、共轭体系、反应机理、功能团与官能团的化学性质、实验技术和仪器以及应用领域等知识点。
有机化学复习知识点超强总结

(一)反应题的重要考点:(1)烷烃的卤代反应,反应活性:①氟氯溴碘(F2>Cl2>Br2>I2);②活泼H原子的类型3〫>2〫>1°>CH3。
注意:药大考研常考察碳正离子稳定性,也会考察环烷烃的卤代开环(2)单烯烃的主要反应:①加成反应:催化加氢(注意:顺式加成)、亲电加成(X2、HX、H2SO4、H2O、BH3)、自由基加成(药大考研常考:HBr/ROOR(唯一));②氧化烯烃的反应(常用氧化剂总结:KMnO4/OH-(OsO4,药大考研官网推荐王积套课本有此氧化剂)、KMnO4/H+、O3、过氧酸、O2/Ag);③ɑ-H卤代(自由基取代反应);④聚合反应。
中国药科大学考研辅导南药人研路提示:马氏比较常考,但是反马加成也常涉及。
(3)炔烃和二烯烃的主要反应:①加成反应(林德拉、NaNH2/NH3(l)、亲电加成、自由基加成、亲核加成,这些加成反应类似烯烃的加成);②氧化反应;③炔氢的反应(注意);④聚合(一般不会考察);⑤D-A反应(多年考研真题中出现,重点掌握);⑥周环反应(开环和关环相应的条件下的顺旋和对旋)。
中国药科大学考研辅导南药人研路提示:2019年710真题第一次出现此知识点考查,注意掌握(常考炔烃部分加氢、与H2O加成生成醛酮;D-A反应等)(4)芳烃的主要反应:①亲电取代(注意:卤代、磺化、硝化、傅克反应、氯甲基化反应);②氧化反应;③α-H卤代(自由基);④加成反应。
中国药科大学考研辅导南药人研路提示:芳环上亲电取代的定位效应在药大考研中常考察,这个主要根据环上的电子云密度来判断;还有α-H的卤代。
(5)卤代烃的主要反应:①亲核取代、AgNO3(SN1);SN2的瓦尔登转化是药大历年重点!);②消除反应(HX(扎伊采夫规则,E2反式消除【特变注意】)、X2);③与金属反应(烷基铜锂,注意位阻,是1,2加成还是1,4加成,非常重要!);④还原产物为烃,常用还原剂:LiAlH4、NaBH4、Zn+HCL,醋酸等。
有机考研知识点总结

有机考研知识点总结一、有机化合物的结构有机化合物是由碳、氢、氧、氮、硫等元素构成的化合物,具有碳骨架和碳碳键,其结构具有多样性和复杂性。
有机化合物的结构包括了分子式、结构式、立体结构、杂化轨道等内容。
1. 分子式分子式是反映化合物中元素种类和相对原子数的表示法。
有机化合物的分子式可以通过元素符号和下标表示,如C6H12O6表示葡萄糖的分子式。
2. 结构式结构式是用化学连接线表示有机分子中原子的连接方式,包括了键的类型、化学键的方向以及原子之间的空间关系。
3. 立体结构立体结构是有机分子中空间构型的表示,包括了空间立体异构体和光学异构体。
4. 杂化轨道杂化轨道是描述有机分子中碳原子的杂化状态,通过杂化轨道可以解释有机分子的化学性质和反应机理。
二、有机化合物的性质有机化合物的性质包括了物理性质和化学性质两个方面。
1. 物理性质有机化合物的物理性质包括了熔点、沸点、密度、溶解度等内容,这些物理性质可以反映有机分子内部的相互作用和分子结构的稳定性。
2. 化学性质有机化合物的化学性质包括了酸碱性、还原性、氧化性、亲电性、亲核性等内容,这些化学性质决定了有机化合物在化学反应中的表现和反应路径。
三、有机化合物的合成有机化合物的合成是有机化学研究的重要内容,也是化学工业生产的基础。
有机化合物的合成包括了有机反应的研究以及有机合成的方法。
1. 有机反应有机反应是有机化合物在特定条件下发生的化学变化,包括了加成反应、消除反应、取代反应、重排反应等多种类型。
2. 有机合成有机合成是有机化合物的化学合成方法和技术,包括了合成路线的设计、合成步骤的优化以及合成产物的纯化和结构表征。
四、有机化合物的反应机理有机化合物的反应机理是揭示有机反应过程中原子和分子变化的规律和规则,有助于我们理解有机反应的特点和反应路径。
1. 亲电取代反应亲电取代反应是有机化合物中碳原子与亲电试剂发生取代反应的过程,包括了亲电试剂的攻击和碳原子的离子中间体的生成。
有机化学知识整理(全版)
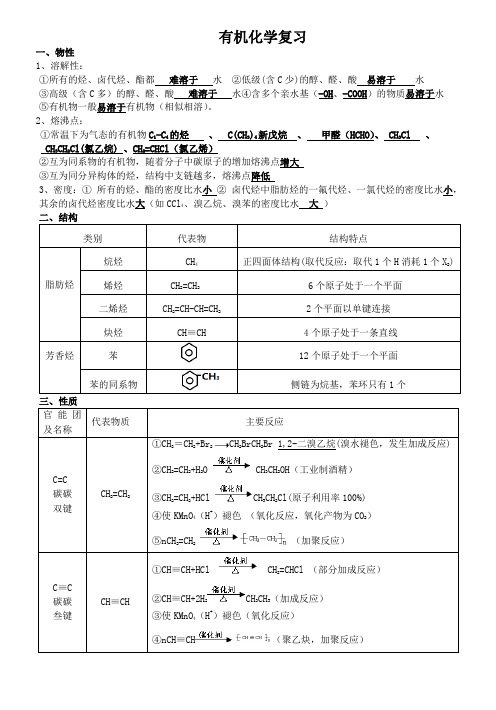
有机化学复习一、物性1、溶解性:①所有的烃、卤代烃、酯都难溶于水②低级(含C少)的醇、醛、酸易溶于水③高级(含C多)的醇、醛、酸难溶于水④含多个亲水基(-OH、-COOH)的物质易溶于水⑤有机物一般易溶于有机物(相似相溶)。
2、熔沸点:①常温下为气态的有机物C1-C4的烃、 C(CH3)4新戊烷、甲醛(HCHO)、 CH3Cl 、CH3CH2Cl(氯乙烷) 、CH2=CHCl(氯乙烯)②互为同系物的有机物,随着分子中碳原子的增加熔沸点增大③互为同分异构体的烃,结构中支链越多,熔沸点降低3、密度:① 所有的烃、酯的密度比水小② 卤代烃中脂肪烃的一氟代烃、一氯代烃的密度比水小,其余的卤代烃密度比水大(如CCl4、溴乙烷、溴苯的密度比水大)二、结构类别代表物结构特点脂肪烃烷烃CH4正四面体结构(取代反应:取代1个H消耗1个X2) 烯烃CH2=CH2 6个原子处于一个平面二烯烃CH2=CH-CH=CH22个平面以单键连接炔烃CH≡CH 4个原子处于一条直线芳香烃苯12个原子处于一个平面苯的同系物侧链为烷基,苯环只有1个三、性质官能团及名称代表物质主要反应C=C碳碳双键CH2=CH2①CH2=CH2+Br2 CH2BrCH2Br 1,2-二溴乙烷(溴水褪色,发生加成反应)②CH2=CH2+H2O CH3CH2OH(工业制酒精)③CH2=CH2+HCl CH3CH2Cl(原子利用率100%)④使KMnO4(H+)褪色(氧化反应,氧化产物为CO2)⑤nCH2=CH2(加聚反应)C≡C碳碳叁键CH≡CH①CH≡CH+HCl CH2=CHCl (部分加成反应)②CH≡CH+2H2CH3CH3(加成反应)③使KMnO4(H+)褪色(氧化反应)④nCH≡CH(聚乙炔,加聚反应)苯环(不是官能团)苯(易取代难加成能氧化)+ HBr(取代反应)① + Br2② +HO-NO2 + H2O③ + 3H2 (环己烷)(加成反应)苯不能使酸性KMnO4和溴水褪色,但可以萃取溴使原溴水层褪色苯的同系物能使酸性KMnO4褪色(氧化反应)不能使溴水褪色但能萃取溴-X CH3H2Br ①CH3CH2Br +NaOH CH2=CH2↑+ NaBr + H2O②CH3CH2Br +NaOH CH3CH2OH + NaBr③X检验:先加NaOH加热、再加过量HNO3,最后加AgNO3,根据沉淀的颜色确定X是什么-OH (羟基)CH3CH2OH①2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ 2-OH~2Na~H2②2CH3CH2OH+O2 2CH3CHO(乙醛)+2H2O③2CH3CH(OH)CH3+O22CH3COCH3(丙酮)+2H2O(结构要求:α-C上有2个H(-CH2OH)氧化为醛;有1个H氧化为酮;无H不能氧化)④CH3CH2OH CH2=CH2↑+H2O(结构要求:β-C上有H)⑤2CH3CH2OH CH3CH2OCH2CH3+H2O⑥CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O⑦CH3CH2OH+HBr CH3CH2Br+H2O (工业制卤代烃)苯酚①弱酸性:+NaOH→+H2O②+Na2CO3→+NaHCO3③+CO2→+NaHCO3(CO2少量或过量)④(邻对位取代,浓溴水过量)⑤易被氧化⑥遇Fe3+显紫色-CHO (醛基)CH3CHO-CHO → -CH2OH (与H2反应)-CHO → -COOH(与O2、KMnO4(H+)、溴水、银氨溶液、新制Cu(OH)2)①CH3CHO+H2 CH3CH2OH②CH3CHO+2Ag(NH3)2OH CH3COONH4+H2O +2Ag↓+3NH3(-CHO ~ 2Ag)③CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O(-CHO ~Cu2O)(羰基)CH3COCH3(丙酮)CH3COCH3+H2 CH3CH(OH)CH3-COOH (羧基)CH3COOH酸性(与Na、与NaOH、与Na2CO3、与NaHCO3)、酯化反应(2-COOH ~CO32-~CO2)(-COOH ~HCO3-~CO2)-COO- (酯基)CH3COOCH2CH3①CH3COOCH2CH3+H2O CH3COOH+CH3CH2OH (可逆)②CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH (不可逆)(-COOR ~NaOH)葡萄糖和多糖:①CH2OH(CHOH)4 CHO+ H2 CH2OH(CHOH)4CH2OH②CH2OH(CHOH)4CHO + 2Ag(NH3)2OH CH2OH(CHOH)4COONH4 + 2Ag↓ + 3NH3 + H2O③CH2OH(CHOH)4CHO + 2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O④C6H12O62CH3CH2OH + 2CO2⑤C12H22O11(蔗糖) + H2O C6H12O6(葡萄糖) + C6H12O6(果糖)⑥C12H22O11(麦芽糖) + H2O 2C6H12O6(葡萄糖)⑦(C6H10O5)n(淀粉) + nH2O n C6H12O6(葡萄糖)⑧(C6H10O5)n (纤维素) + nH2On C6H12O6(葡萄糖)⑨(硝酸纤维素酯) 油脂(油脂的氢化或硬化)(皂化反应)三、重要的反应类型反应类型反应特征典型反应名称取代反应有进有出(类似复分解)卤代反应、硝化反应、酯化反应、水解反应、醇分子间脱水成醚加成反应有进无出C=C、C≡C(与H2、HX、X2、H2O)苯环、羰基、醛基(与H2)消去反应无进有出醇(浓硫酸,170℃)、卤代烃(NaOH醇溶液,加热)氧化反应有机物得O或失H 燃烧、 C=C、C≡C、-CHO、-OH等被KMnO4(H+)、O2等氧化还原反应有机物失O或得H 与H2加成加聚反应打开不饱和键含双键、叁键就能发生加聚。
有机化学知识点总结

有机化学知识点总结1. 有机化学概述1.1 定义:研究含碳化合物的化学性质、结构、合成及其应用的科学。
1.2 特点:碳的四价性、碳链结构、官能团的存在。
2. 有机化合物的分类2.1 烃类:仅含碳氢元素的有机化合物。
2.1.1 饱和烃:碳原子之间全为单键,如烷烃。
2.1.2 不饱和烃:含有双键或三键,如烯烃、炔烃。
2.2 衍生物:由烃类通过取代或加成反应生成的化合物。
2.2.1 醇、酚:含羟基的化合物。
2.2.2 醛、酮:含羰基的化合物。
2.2.3 羧酸、酯:含羧基的化合物。
2.2.4 胺、酰胺:含氨基的化合物。
3. 有机化学反应类型3.1 取代反应:化合物中的一个原子或基团被另一个取代。
3.1.1 核式取代:如卤代反应。
3.1.2 亲核取代:如醇的生成。
3.2 加成反应:不饱和化合物与另一个分子结合形成饱和化合物。
3.2.1 电子对受体与亲电试剂的反应。
3.3 消除反应:化合物中的两个原子或基团脱离形成不饱和化合物。
3.4 重排反应:分子内部原子的重新分布。
3.5 聚合反应:单体分子通过重复的化学反应形成大分子链。
4. 有机分子的结构4.1 碳原子的杂化:sp、sp2、sp3杂化。
4.2 立体化学:手性、对映体、消旋体。
4.3 分子轨道理论:分子的电子结构。
5. 有机化学中的分析技术5.1 光谱分析:红外光谱、核磁共振光谱、紫外-可见光谱。
5.2 色谱分析:气相色谱、液相色谱、薄层色谱。
6. 有机合成策略6.1 逆合成分析:目标分子的合成路径设计。
6.2 保护基策略:对活性官能团的保护与去保护。
6.3 绿色化学:环保、可持续的合成方法。
7. 有机化学的应用7.1 药物合成:药物分子的设计、合成与改良。
7.2 材料科学:高分子材料、生物材料的开发。
7.3 能源化学:生物质能源、太阳能转换。
8. 有机化学的发展趋势8.1 新合成方法的开发。
8.2 新材料的设计与合成。
8.3 生物有机化学的交叉研究。
有机化学复习要点

有机化学复习要点有机化学是研究有机物(含碳的化合物)的合成、结构、性质和反应的科学。
下面是有机化学复习的重点要点:1.有机化合物的分类:根据碳的连接方式,有机化合物可分为链状、环状和支链状化合物。
根据它们的官能团,化合物可以被进一步分类为醇、酮、酯、醛、酸、胺等等。
2.有机化合物的命名:有机化合物的命名是有机化学的基础。
在命名时,需要确定主链、编号碳原子、标记官能团和提供适当的前缀和后缀。
3.有机化合物的构造:有机化合物的构造表示确定其分子的原子结构,包括原子的类型、化学键的类型(单键、双键、三键)和宇称等。
4.共价键的极性:共价键是由两个原子之间共享电子形成的,极性共价键指电子不均匀地共享。
这导致一侧带有部分正电荷,而另一侧带有部分负电荷,形成极性分子。
5.引入官能团:官能团是有机化合物中特定原子或原子组合的集合,确定化合物的性质和反应。
常见官能团有羟基(-OH)、醛基(-CHO)、酮基(-C=O)、羧基(-COOH)、胺基(-NH2)等等。
6.有机反应的基本原理:有机反应是有机化学的核心,包括加成反应、消除反应和取代反应。
加成反应是指在化合物中添加一个原子或基团;消除反应是指分子中的两个基团消除,形成一个双键或三键;取代反应是指一个基团被替换成另一个基团。
7.重要的有机反应:有机化学有许多重要的反应,其中一些包括酯化、醇酸化、加氢、亲电取代、亲核取代、还原和氧化等等。
了解这些反应及其机理对于理解有机化学非常重要。
8.常见的有机化学术语:在有机化学中,有许多常见的术语和概念,例如:轴手性、对映体、立体异构体、环状化合物等等。
了解这些术语可以帮助理解和解决有机化学问题。
9.溶剂的选择:在有机化学实验中,溶剂的选择非常重要。
常见的有机溶剂包括乙醇、丙酮、乙醚、二甲基甲酰胺等等,选择合适的溶剂可以促进反应的进行。
10.立体化学:立体化学涉及分子和化合物的空间构型和对称性。
手性和立体异构体是立体化学的重要概念,影响分子的性质和化学反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NH 2
N 2Cl
HCl, NaNO 2
50% H 3PO 2
5℃以下
, SO
Cu
3
Na 2
SO 3 Na
1)
CuCN, K CN
HB 4F,
2) N
SnC2l ,HCl
CH 3CH 2CH 2Cl + CH3CHClCH 3
43%
57%
hv
CH3CH2CH 3 + Br2
CH 3CH 2CH 2Br + CH 3CHBrCH 3
3%
97%
10
第二节 有机化学的基本反应
②烯丙基氢和苄基位氢卤代选择性好——NBS
CH 3
CH 2Br
+ NBS
2.亲电取代——芳环的“四化”(卤化、硝化、磺化、烷基化和酰基化) 【注意】 ①定位规律 I类定位基:负电荷、孤对电子、饱和键 II 类定位基:正电荷、不饱和键 III 类定位基:卤素
a
C 'a
b
C b'
Z 构型
a
C 'a
b'
C b
E 构型
2. 对映异构——Fischer投影式
a>a' b>b'
同碳上下比较!
楔形式
透视式
Fischer投影式
5
第一节 有机化合物命名和结构书写
3. 构象异构——Newman投影式
交叉式构象
重叠式构象
6
第二节 有机化学的基本反应
考查内容 完成反应式考查一个反应的各个方面: 一、正确书写反应方程式(反应物、产物、反应条件)。 二、反应的区域选择性问题。 三、立体选择性问题。 四、反应机理,是否有活性中间体产生?会不会重排?
CH 3
OH
(官能团 )位置异构 CH 3CH 2CH 2OH 和CH 3CHCH 3
官能团异构
CH 3CH 2OH 和CH 3O CH 3
异
OH
OH
构 现 象
互变异构 CH 3C-CH— 和 CH 3C=CH—
酮式
烯醇式
顺反异构
构型异构
立体异构
对映异构
构象异构
4
1. 顺反异构
第一节 有机化合物命名和结构书写
1. 系统命名法: 选择官能团( 母体) → 确定主链→ 排列取代基顺序→ 写出化合物全称 构型 + 取代基 + 母体
2. 桥环和螺环烃的命名法
取代基 + 环数[大.中.小] + 母体 取代基 + 螺[小. 大] + 母体
2
第一节 有机化合物命名和结构书写
3. 芳香烃命名法:
CH 3
o
o邻
m
m间
p
R' -O-R + X- RC≡CR' + X- R-R'
R-I + X- R-CN + X- R'COOR + X- R-NH2 + X- RNHR'+ X-
RNR' 2 + X-
[RP3P]+Xh-
RSH + X- RSR'+ X- RCH(COOR') 2 + X- CH 3COCHRCOOR'+ X-
COOH Br
COOHO 2N来自HNO 3+H2SO 4
Br
87%
COOH
COOH
NO 2 +
Br 13%
Br O2N
0%
11
第二节 有机化学的基本反应
② 磺化反应可逆——占位 ③ 芳环上有吸电子取代基如-NO2,-CN, -COOH, -SO 3H不发生傅克反应
例如合成间乙基苯甲酸。 COOH
?
CH 2CH 3
7
第二节 有机化学的基本反应
一、解题的基础:熟悉和灵活掌握各类反应 二、解题的基本思路:
1. 确定反应类型(反应能不能发生?有哪几类反应能发生?哪一类 反应占主导?)要回答这三个问题,必须了解:反应物的多重反应性能; 试剂的多重进攻性能;反应条件对反应进程的控制等。
2. 确定反应的部位(在多官能团化合物中,判断反应在哪个官能团 上发生。)一般要考虑:选择性氧化、选择性还原、选择性取代、选择 性加成、分子内取代还是分子间取代等。
歧化反应
按电荷行协为同:反亲应电—反—应周环亲反核应反应
D-A反应
9
第二节 有机化学的基本反应
一、取代反应 ——自由基取代、亲电取代和亲核取代 1.自由基取代 【特点】有自由基参与、光照、加热或过氧化物存在 【注意】 ①烷烃的卤代一卤代较差,溴卤代的选择性较好
hv
CH3CH 2CH 3 + Cl2
第一节 有机化合物命名和结构书写
考查内容
一、母体烃的名称,官能团字首、字尾的名称,取 代基的名称。
二、选主链的原则,编号的原则,取代基排列次序 的原则。
三、命名的基本格式。 四、确定R、S、Z、E、顺、反的原则。 五、桥环和螺环化合物的命名原则。 六、立体结构的各种表达方式(构象和构型)
1
第一节 有机化合物命名和结构书写
3. 考虑反应的区域选择性问题:消除反应:扎依切夫规则还是霍夫 曼规则; 加成反应:马氏规则还是反马氏规则; 重排反应:哪个基团迁移、 不对称酮的反应:热力学控制还是动力学控制等。
4. 考虑立体选择性问题:消除反应:顺消还是反消、加成反应:顺 加还是反加、重排反应:构型保持还是构型翻转、SN1:重排、SN2:构型 翻转等。
13
RONO 2 + AgX
第二节 有机化学的基本反应
2) 羰基化合物亲核加成-消除反应
O
O
C + Nu H R R' 亲核试剂
R C Nu + HR'
F
3) 重氮盐取代反应 【特点】低温环境,强酸介质
【应用】制备芳香族亲电取代 反应难制备的化合物
Cl
HO
BF,2) 4
I
△
H
1)H
2 O,
CuCl KI
12
2.亲核取代 1) SN1和SN2
第二节 有机化学的基本反应
亲核试剂
OH -
H2O R'O -
R'C≡C -
R' 2CuLi I-
CN-
R'COO -
R-X
NH3
NH2R'
NHR' 2
PPh 3 SH-
SR'
[CH(CO2O]-R') [CH3COCHCOOR'] -
AgNO3
反应产物 ROH + X- ROH + HX
5. 考虑反应的终点问题:氧化:阶段氧化还是彻底氧化、还原:阶 段还原还是彻底还原、取代:一取代还是多取代、连续反应:一步反应 还是多步反应等。
8
第二节 有机化学的基本反应
均裂
自由基反应(A :B
A? + B?)
重排反应
有机反应 离子型反异应裂 (A :B A+ + B- )
取代反应 缩合反应 加成反应 降解反应 消去反应 氧化还原反应
对
4. 音译命名法
N H
Pyrrole 吡咯
N
Pyridine 吡啶
O
Furan 呋喃
S
Thiophene 噻吩
N
Quinoline 喹啉
杂原子不同时,遵循O>S>NH> N 的优先顺序
3
第一节 有机化合物命名和结构书写
二、结构书写
构造异构
碳链异构 CH 3CH 2CH 2CH 3和CH 3CHCH 3
