化学作业33
14次有机化学作业

14次有机化学作业;.1.与Lucas试剂反应速度最快的是 C.叔丁醇2. 下列说法正确的是: A.若分⼦中没有对称因素,就是⼿性分⼦3. 下列化合物中有p-π共轭的是答案C4. 下列化合物中能发⽣碘仿反应的是 C.丙酮5. 请从备选答案中选取⼀个最佳答案 B.(CH3)3COH6. 下列糖类化合物中能与溴⽔反应使其褪⾊的是 B.葡萄糖7.与CH3COOH酯化反应速度最慢的是 B.(CH3)3COH8. C.89. 正丁烷的构象中,能量最低的是 D.全重叠式C. Br210. 下列化合物中最易被开环的是:11. D.⼏何异构体A. 12. 下列化合物中进⾏卤代反应活性最⾼的是C.13. 下列化合物在浓硫酸作⽤下脱⽔速率最⼤的是: D. 14. 下列化合物中没有芳⾹性的是:D. 下列化合物中酸性最强的是:15.;. .;.B. 16. 果糖的半缩酮羟基是:C.下列化合物中能与银氨溶液作⽤⽣成⽩⾊沉淀的是:17.B.型的是:Z 18. 下列化合物中构型为 D. 下列分⼦在极性条件下最难⽣成碳正离⼦的是:19.D20. 下列化合物酸性最强的是: C 在芳⾹烃的亲电取代反应中属于邻对位定位基的基团是21.22. 下列化合物中能与NaHSO反应⽣成α-羟基磺酸钠的是:3D23. 下列条件下,能发⽣反应的是:B.氯⽓先⽤光照射后,在⿊暗中迅速与⼄烷混合24. 下列化合物中⽆顺反异构体的是 B.1-丁烯D. CHCOOH酯化反应速度最快的是与25. 3 B26. 下列化合物中不能使⾼锰酸钾褪⾊的是27. 列化合物中与⼄醇发⽣亲核取代反应速度最快的是:B.⼄酰氯28. 甲烷与氯⽓在光照下进⾏反应,其反应机理是:B.亲核取代29. 与Lucas试剂反应速度最慢的是:A.正丁醇C. 下列化合物在碱性条件下不能与重氮盐发⽣偶联反应的是30.A. 下列化合物最易脱羧的是31.32. 下列化合物中与⼄醇发⽣亲核取代反应速度最快的是 B.⼄酰氯下列化合物中属于单糖的是:C.葡萄糖1.在芳⾹烃取代反应中属邻位定位基的基团是A.-OH2.;. .;.下列糖类化合物中能与I2/KI溶液显蓝⾊的是C.蔗糖.3下列化合物能发⽣羟醛缩合反应的是B.⼄醛.4丁烷的构象中,能量最⾼的是:D.全重叠式.5下列化合物能和⼄醛⽣成肟的是:A.羟氨.6下列化合物酸性最弱的是:C.CHCOOH7.3丙烯与HBr反马式加成时,反应条件是:B.过氧化物存在下8.C. 下列化合物中没有旋光性的是.9 B. 下列化合物中构型为E型的是:10.11. 下列化合物在低温下和亚硝酸反应能得到稳定的重氮盐的是C.伯芳⾹胺12. 下列化合物在⽔溶液中碱性最弱的是 C.CHNH2 5613. 下列化合物具有旋光性的是D.CHCHClCOOH3 C. 下列化合物中具有芳⾹性的是14..15. B.互变异构体16. 下列化合物中能与Tollons试剂发⽣反应的是:D.CHCHO 317. 顺反异构的构型表⽰⽅法是:A.Z/E18. 下列化合物能使溴⽔褪⾊的是:C.⼄酰⼄酸⼄酯19. 环⼰烷的构象中,优势构象是:B.椅式构象20. 下列关于糖类化合物说法错误的是:C.果糖是酮糖,是⾮还原糖D. 共轭的是:π21. 下列化合物中有p-22.-丁酮酸⼄酯βB. 23. D.下列糖类中⽆还原性的是:蔗糖;. .;.B.2S, 3S24.=CH⽔溶液反应的是:C.CHKMnO25. 下列化合物中能与2 24 B.⼄醛26. 下列化合物能发⽣羟醛缩合反应的是:NOD.—27. 在芳⾹烃取代反应中起致钝作⽤的基团是:2D.淀粉I2/KI溶液显蓝⾊的是:28. 下列糖类化合物中能与29.共轭A.p-π30. 在芳⾹烃的亲电取代反应中属于间位定位基的基团是:A-NO231. 下列化合物中亲电取代反应活性最强的是:D.OH-32. 在芳⾹烃取代反应中属邻位定位基的基团是:A. 分⼦具有不对称性判断化合物是否具有旋光性的条件是:D.33.麦芽糖下列糖类化合物中属于还原糖的是:A.1.下列化合物不能与重氮盐发⽣偶联反应的是:B.2.CHOHCH下列化合物中能发⽣碘仿反应的化合物是:C.CH3. 3 3 : D.蔗糖4. 下列化合物中不能产⽣变旋现象的是 D.果糖5. 下列化合物中能产⽣变旋现象的是:甲酸KMnO4溶液褪⾊的化合物是:B.6. 能使:B.P-卤代反应中的催化剂是⼄酸α7.下列烯烃中最稳定的是:D. 8.C.Z/E9. 顺反异构的构型表⽰⽅法是:NHA.—10. 在芳⾹烃取代反应中起强致活作⽤的基团是:2苯胺11. 下列化合物中能与溴⽔反应产⽣⽩⾊沉淀的是:C. A.⼄醛12. 下列化合物能发⽣羟醛缩合反应的是:-反应⽣成下列化合物中能与13. NaHSO3α羟基磺酸钠的是:D.;. .;.14. 下列化合物在⽔溶液中碱性最⼩的是:D.CHNH265 A. 15. 下列化合物亲电取代⽐苯活性⾼的是:16. 下列化合物中有旋光性的是:A.CHCHClCOOH 317. 下列化合物中加成反应活性最⾼的是:C.2-丁烯18. 在芳⾹烃亲电取代反应中属邻对位定位基的基团是:D.-Cl19. 不能与⽔形成分⼦间氢键的化合物是:D.CHCHBr 2320. 下列化合物与AgNO⽔溶液反应最快的是:C.3-氯丙烯321. 在从茶叶中提取咖啡因的实验中,是利⽤咖啡因的来精制它的D.升华性22. 与CHCOOH酯化反应速度最快的是:C.CHOH 3323. 葡萄糖的半缩醛羟基是:A.COH124. 下列化合物酸性最弱的是:A.CHCHCOOH 2325. 鉴别⼄醛与⼄醇可采⽤的试剂是:C.多伦试剂26. ⼄酰⼄酸⼄酯与FeCl溶液呈紫红⾊是由于它具有:D.互变异构现象327. 化合物在浓KOH/⼄醇溶液中脱HCl速率最⼤的是D.(CH)CClCH(CH) 2 32328. ⼄烯和Br/CCl溶液褪⾊的反应属于B.亲电加成4229. 下列化合物中不能发⽣碘仿反应的化合物是B.CHCOOH3 D. 速率最⼤的是上述化合物在浓1.KOH/醇中脱HCl上述化合物在浓KOH/醇中脱HCl速率最⼩的是:A.CHCH=CHCHCHCHCl 2.2223上述化合物中酸性最强的是:C.ClCH3.COOH 2上述化合物中酸性最弱的是:D.CH≡CH 4.上述化合物中酸性最强的是 5.B.CHCOOH 3上述化合物中酸性最弱的是:D.CH ≡CH6.C. 7.上述化合物中酸性最强的是:A.上述化合物中酸性最弱的是:8.9.在芳⾹烃取代反应中起弱致钝作⽤的基团是:C.-Cl10.在芳⾹烃取代反应中是间位定位基的基团是:A.-SOH3;. .;.11. A.顺反异构C.12.碳链异构13.CHCHCHCHOH与CHCHOCHCH属于:C.官能团异构3223223214.CHCHCHCHOH与(CH)CHCHOH属于:A.碳链异构222233215.上述化合物在浓硫酸作⽤下发⽣分⼦内时脱⽔速率最⼤的是: D.A.上述化合物在浓硫酸作⽤下发⽣分⼦内时脱⽔速率最⼩的是:16.17.上述化合物中酸性最强的是:B.CHCOOH 318.上述化合物中酸性最弱的是:C.CH≡CH19.卤代烃⽔解反应速度最快的是:B.CH=CHCHCl 2220.卤代烃⽔解反应速度最慢的是:D.CHCH=CHCl 321.能与溴⽔反应令其褪⾊的是:B.葡萄糖22.能与I溶液显蓝⾊的是:D.淀粉223.与Lucas试剂反应速度最快的是:D.2-甲基-2-丁醇B. 反应时最活泼的是24.上述化合物中发⽣F-C C 25.上述化合物中发⽣磺化反应时最不活泼的是:26.上述取代基在定位效应中属间位定位基的是B.-COOH27.上述取代基在定位效应中属强活化基团的是:C.-OH上述化合物中酸性最强的是:28.上述化合物中酸性最弱的是:29.;. .;.30.下列化合物在⽔溶液中碱性最强的是B.(CH)NH2331.下列化合物在⽔溶液中碱性最弱的是:D.(CH)NH 25632.上述化合物中碱性最强的是A.(CHCH)NH 232上述化合物中碱性最弱的是:33.34.与CHCOOH酯化反应速度最快的是:D.CHOH 3335.在芳⾹烃取代反应中起弱致钝作⽤的基团是:C.-Cl36.在芳⾹烃取代反应中是间位定位基的基团是:A.-SOH 3 C. 下列化合物中最易发⽣亲电取代的是:37.A.p-π38.共轭。
高中化学竞赛培训专题作业

35. AlF3 不溶于液态 HF 中,但当 HF 中加入 NaF 时则可溶,为什么?若在此溶液中导入 BF3 时 AlF3 又沉淀出来,为什么?写出有关化学反应方程式。
36. 矾土中常含有氧化铁杂质,现将矾土和氢氧化钠共熔,用水浸取熔块,将得到的溶液过 滤,在滤液中通入二氧化碳,再次得到沉淀,过滤后将沉淀灼烧,便得到较纯的氧化铝,
14. 从结构的观点解释下列问题: ⑴ 氮在自然界以大量的游离态存在; ⑵ 氨极易溶于水,而 NO 难溶于水; ⑶ N2 为反磁性分子,而 NO 为顺磁性分子; ⑷ H3PO4 为三元酸,而 H3PO3 为二元酸,H3PO2 为一元酸。 ⑸ 为什么白磷在空气中可以自燃 ,而 N2 在空气中却可稳定存在?
3. 试用一种试剂将可溶性硫化物、多硫化物、亚硫酸盐、硫代硫酸盐和硫酸盐彼此区分开 来。写出反应方程式和反应现象。
4. 给出 SOCl2 分子的空间构型和成键情况,为什么 SOCl2 既可以作为路易斯酸,又可作为 路易斯碱?
5. 某液体物质 A 具有与 CO2 相似的结构,A 与 Na2S 反应生成化合物 B,B 遇酸能产生恶 臭的有毒气体 C 及物质 A,C 可使湿润的醋酸铅试纸变黑。A 与 Cl2 在 MnCl2 催化下作 用可生成一种不能燃烧的液体物质 D;A 与 Cl2O 作用则生成极毒气体 E 和透明液体 F。 试推断从 A 到 F 各代表什么物质?
25. 说明下列各实验中浓 HCl 的作用,并写出反应方程式。 ⑴ 配制 SnCl2 溶液时,将 SnCl2( s )溶于浓 HCl 中而后加水稀释; ⑵ 加热条件下,用 MnO2 与浓 HCl 作用制取氯气; ⑶ 用浓 HCl 配制王水以溶解金; ⑷ 在 Na3AsO4 溶液中加入浓 HCl 以制取 As2S5。
全品作业化学九年级上册33~34页

全品作业化学九年级上册33~34页摘要:一、问题的提出1.化学在生活中的应用2.化学知识的普及和重要性二、化学与生活的联系1.生活中的化学现象2.生活中的化学制品3.化学在生活中的重要作用三、化学知识的普及1.化学基本概念的普及2.化学实验在普及化学知识中的作用3.化学知识的实际应用四、化学的重要性1.化学在科学领域的重要性2.化学在工业领域的重要性3.化学在环境保护领域的重要性五、结论1.化学在生活中的应用和普及的必要性2.提高化学知识的重要性3.鼓励更多人学习化学知识正文:一、问题的提出化学,一门研究物质组成、性质、变化规律的科学,在我们日常生活中无处不在。
无论是食品、药品、化妆品还是家居用品,都离不开化学的身影。
然而,化学知识的普及和重要性却并未被人们所充分认识到。
因此,本文旨在探讨化学与生活的紧密联系,以及化学知识普及的重要性。
二、化学与生活的联系1.生活中的化学现象在我们日常生活中,有很多常见的化学现象。
例如,铁的生锈、水果的氧化、食物的烹饪等。
这些现象虽然常见,但背后的化学原理却很少被人了解。
2.生活中的化学制品我们生活中所使用的物品,如塑料、合成纤维、洗涤剂等,都是化学制品。
这些制品的制造、性质和用途,都离不开化学知识。
3.化学在生活中的重要作用化学在生活中的应用不仅体现在物质上,还体现在环境保护、能源开发、医药保健等方面。
例如,通过化学方法处理污水,可以防止水污染;通过化学方法开发新能源,可以缓解能源危机;通过化学方法研究药物,可以提高人类的健康水平。
三、化学知识的普及1.化学基本概念的普及普及化学知识,首先需要让人们了解化学的基本概念,如原子、分子、化学键、化学反应等。
这些概念是学习化学知识的基础。
2.化学实验在普及化学知识中的作用化学实验是普及化学知识的重要手段。
通过实验,学生可以直观地看到化学反应的发生,更好地理解化学原理。
3.化学知识的实际应用将化学知识应用到生活中,可以让人们更好地理解和接受化学。
吉林大学---有机化学作业题(含实验)

有机化学〔含实验〕一、单项选择题1. 以下物质有两性性质的是〔〕。
C. 氨基酸2. 苯酚与甲醛反应时,当酚过量,酸性催化条件下的将得到〔〕C. 热塑性酚醛树脂3. Walden转化指的是反应中()D. 生成对映异构体4. 以下化合物中的碳为SP2杂化的是:( )。
B. 乙烯5. 以下化合物能发生碘仿反应的是〔〕。
D. CH3COCH2CH36. 根据休克尔规则,判断以下化合物哪些具有芳香性〔〕。
B.7. 以下自由基中最稳定的是〔〕。
B.8. A. 环丙烷、B. 环丁烷、C. 环己烷、D. 环戊烷的稳定性顺序( ) A. C >D>B>A9. ( ) A. 对映异构体10. 有机化合物与无机化合物相比其结构上的特点是〔〕A. 结构复杂,多为共价键连接9. 卤烃的亲核取代反应中,氟、氯、溴、碘几种不同的卤素原子作为离去基团时,离去倾向最大的是( ) D. 碘11. 以下化合物不能使酸性高锰酸钾褪色的是〔〕C. 丙烷12. 在以下化合物中,偶极矩最大的是( ) A. H3CCH2Cl13. 以下各化合物中具有芳香性的是〔〕。
A.14. 以下化合物中酸性最强的是〔〕. B. 对硝基苯酚15. 以下化合物不能发生傅列德尔-克拉夫茨酰基化反应的有:( )。
B. 硝基苯16. 该化合物属于〔〕 B. 醌类17. 以下化合物具有旋光性的是〔〕。
B. ;18. 以下烯烃氢化热〔KJ/mol〕最低的是〔〕。
D.19. 以下化合物与FeCl3溶液发生显色反应的有?〔〕A. 对甲基苯酚20. 比较以下醛〔酮〕与HCN 反应的活性〔〕B. d>a>b>c1. 物质具有芳香性不一定需要的条件是( ) C. 有苯环存在2. 和互为互变异构体,在两者的平衡混合物中,含量较大的是〔〕B.3. 苯酚可以用以下哪种方法来检验?( )B. 加Br2水溶液8. 用异丙苯法来制备苯酚,每生产1吨苯酚可同时获得多少吨丙酮?〔〕C. 0. 89. 与之间的相互关系是( ) D. 构象异构体10. 以下化合物进行SN2反应的相对活性最大的是〔〕. C. 3-甲基-1-氯丁烷11. 以下化合物不存在共轭效应的是〔〕B. 叔丁基乙烯12. 和互为互变异构体,在两者的平衡混合物中,含量较大的是〔〕B.13. 以下化合物碱性最强的是〔〕。
药物化学作业

药物化学作业年级:专业:姓名:学号:填空题1、麻醉药根据作用和要求可分为麻醉药和麻醉药,根据给药途径不同可将全身麻醉药分为和2、利多卡因比普鲁卡因稳定,不易水解是由于和。
3、镇静催眠药最常见的结构类型和。
4、镇静催眠药地西泮又称氯氮卓又称、5、苯妥英钠水溶液呈性、露置吸收空气中的而析出、显。
6、阿司匹林又称,扑热息痛又称。
7、阿司匹林的合成是以为原料,在硫酸的催化下,经制得。
8、哌替啶的商品名,其作用机制属于阿片受体9、马来酸盐的消旋体称为,属于H受体。
110、钙拮抗剂又名;降血脂药又称。
11、经典的ß-内酰胺类抗生素包括和,前者的代表药,后者的代表药。
12、血压高低主要决定于和两个因素。
13、氨基甙类抗生素具有较大的神经毒性,主要损害,引起,因此临床使用应慎重14、药物的水解最常见的是、和的水解。
15、构效关系的英文缩写,电荷转移复合物的缩写。
16变质后的麻醉乙醚不得供药用,是因为发生自动氧化,生成和等杂质,对有刺激性。
17、苯巴比妥溶于甲醛后,与硫酸反应,在二层界面处显。
18、阿司匹林与碱溶液共热,可发生反应,酸化后产生的酸臭,并析出白色沉淀。
19、布洛芬又名,其含有结构在碱性条件下与试液生成羟肟酸,然后在酸性条件下与试液生成红色或暗红色物质。
20、氢氯噻嗪的水解产物为含有结构的化合物,经重氮化后,可与偶合,生成色的偶氮化合物。
21.心血管系统药物可分为(1)__________(2)(3)__________和抗心律失常药四大类。
22.甲丙氨酯又可称为__________。
23.盐酸哌替啶为__________类镇痛药。
24.去甲肾上腺素属于__________类拟肾上腺素药,其主要用途是__________。
25.6-APA的结构式为__________。
26.土霉素结构中含有__________显弱酸性,还含有显碱性,故为两性化合物。
27.甾类激素按化学结构可分为__________,__________和孕甾烷三类。
有机化学作业

1.与Lucas试剂反应速度最快的是 C.叔丁醇2. 下列说法正确的是: A.若分子中没有对称因素,就是手性分子3. 下列化合物中有p-π共轭的是答案C4. 下列化合物中能发生碘仿反应的是 C.丙酮5. 请从备选答案中选取一个最佳答案B.(CH3)3COH6. 下列糖类化合物中能与溴水反应使其褪色的是 B.葡萄糖7.与CH3COOH酯化反应速度最慢的是 B.(CH3)3COH8. C.89. 正丁烷的构象中,能量最低的是 D.全重叠式10. 下列化合物中最易被Br2开环的是:C.11. D.几何异构体12. 下列化合物中进行卤代反应活性最高的是 A.13. 下列化合物在浓硫酸作用下脱水速率最大的是:C.14. 下列化合物中没有芳香性的是:D.15. 下列化合物中酸性最强的是:D.16. 果糖的半缩酮羟基是:B.17. 下列化合物中能与银氨溶液作用生成白色沉淀的是:C.18. 下列化合物中构型为Z型的是:B.19. 下列分子在极性条件下最难生成碳正离子的是:D.20. 下列化合物酸性最强的是:D21. 在芳香烃的亲电取代反应中属于邻对位定位基的基团是C22. 下列化合物中能与NaHSO3反应生成α-羟基磺酸钠的是:D23. 下列条件下,能发生反应的是: B.氯气先用光照射后,在黑暗中迅速与乙烷混合24. 下列化合物中无顺反异构体的是 B.1-丁烯25. 与CH3COOH酯化反应速度最快的是 D.26. 下列化合物中不能使高锰酸钾褪色的是B27. 列化合物中与乙醇发生亲核取代反应速度最快的是:B.乙酰氯28. 甲烷与氯气在光照下进行反应,其反应机理是:B.亲核取代29. 与Lucas试剂反应速度最慢的是:A.正丁醇30. 下列化合物在碱性条件下不能与重氮盐发生偶联反应的是C.31. 下列化合物最易脱羧的是A.32. 下列化合物中与乙醇发生亲核取代反应速度最快的是B.乙酰氯1.下列化合物中属于单糖的是:C.葡萄糖2.在芳香烃取代反应中属邻位定位基的基团是A.-OH。
分析化学网上作业1、2、3——(中南大学)

分析化学网上作业1、2、3(一) 单选题1.下列措施可以减小随机误差的是()。
(C)增加平行测定次数2.化学分析是()。
(A)分析化学是化学学科的一个重要分支,是研究物质的化学组成、含量、结构及其分析方法的学科3.定量分析中,精密度与准确度之间的关系是()。
(C)高精密度是保证准确度的前提4.下列数据中包含三位有效数字的是()。
(A)5.4*1055.在滴定分析测定中,属偶然误差的是()。
(D)滴定管最后一位估读不准确6.n次测定结果平均值的标准偏差与单次测量结果的标准偏差s之间的关系是()。
(C)7.试样用量为0.1~10mg的分析称为()。
(C)微量分析8.测定试样中CaO的质量分数,称取试样0.9080g,滴定耗去EDTA标准溶液20.50毫升,以下结果表示正确的是()。
(C)10.08%9.下列有关随机误差的叙述中不正确的是()。
B)随机误差具有单向性10.下列表述中,最能说明随机误差小的是()。
(A)高精密度1.用Ca2+为沉淀剂,测定四草酸氢钾,最后灼烧烧成CaO,求CaO对KHC2O4?H2C2O4?2H2O的换算因数()。
(D)2.2662.用0.1mol/L的HCl溶液滴定同浓度的时,适宜的指示剂为()。
(C)甲基红(pkHIn=5.0)3.标定HCl可用的基准物质是()。
(B)Na2CO34.已知H3PO4的pKa1=2.12,pKa2=7.20,pKa3=12.36,今有一磷酸盐溶液,测得其pH=7.0,则其主要存在形式是()。
(B)H2PO4-+HPO42-5.下图滴定曲线的第一化学计量点适用的指示剂为()(B)甲基橙(pH变色范围为3.1~4.4)6.共轭酸碱对的Ka与Kb的关系是()。
(B)KaKb=Kw7.用25mL常量滴定管进行滴定分析时,耗用标准溶液的体积应控制在(单位:mL)()。
(C)20~258.在滴定分析中,一般用指示剂颜色的突变来判断化学计量点的到达,在指示剂变色时停止滴定。
化学作业32
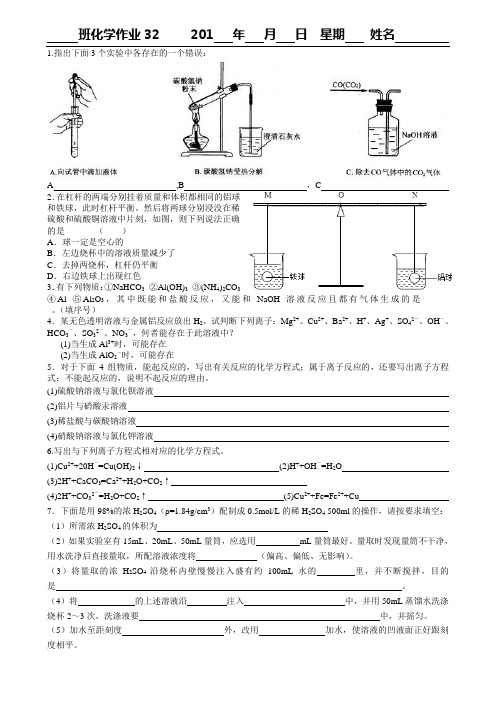
班化学作业32 201 年 月 日 星期 姓名1.指出下面3个实验中各存在的一个错误:A ,B ,C2.在杠杆的两端分别挂着质量和体积都相同的铝球和铁球,此时杠杆平衡。
然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,如图,则下列说法正确的是 ( )A .球一定是空心的B .左边烧杯中的溶液质量减少了C .去掉两烧杯,杠杆仍平衡D .右边铁球上出现红色3.有下列物质:①NaHCO 3 ②Al(OH)3 ③(NH 4)2CO 3④Al ⑤Al 2O 3,其中既能和盐酸反应,又能和NaOH 溶液反应且都有气体生成的是______ _。
(填序号)4.某无色透明溶液与金属铝反应放出H 2。
试判断下列离子:Mg 2+、Cu 2+、Ba 2+、H +、Ag +、SO 42-、OH -、HCO 3-、SO 32-、NO 3-,何者能存在于此溶液中?(1)当生成Al 3+时,可能存在________________________________(2)当生成AlO 2-时,可能存在_______________________________5.对于下面4组物质,能起反应的,写出有关反应的化学方程式;属于离子反应的,还要写出离子方程式;不能起反应的,说明不起反应的理由。
(1)硫酸钠溶液与氯化钡溶液(2)铝片与硝酸汞溶液(3)稀盐酸与碳酸钠溶液(4)硝酸钠溶液与氯化钾溶液6.写出与下列离子方程式相对应的化学方程式。
(1)Cu 2++20H -=Cu(OH)2↓ (2)H ++OH -=H 2O(3)2H ++CaCO 3=Ca 2++H 2O+CO 2↑(4)2H ++CO 32-=H 2O+CO 2↑ (5)Cu 2++Fe=Fe 2++Cu7.下面是用98%的浓H 2SO 4(ρ=1.84g/cm 3)配制成0.5mol/L 的稀H 2SO 4 500ml 的操作,请按要求填空:(1)所需浓H 2SO 4的体积为(2)如果实验室有15mL 、20mL 、50mL 量筒,应选用 mL 量筒最好。
药学物理化学作业

药学物理化学一、单项选择题:1、系统在可逆过程中做功(),环境在可逆过程中做功()。
(A) 最大最大(B) 最小最小(C) 最小最大(D) 最大最小2、以下各物理量属于强度性质的是()。
(A) 熵(B) 质量(C) 体积(D) 温度3、卡诺热机的效率取值范围是()。
(A) 1≥η≥0 (B) 1>η≥0(C) 1≥η>0 (D) 1>η>04、下列关于系统性质说法错误的是()。
(A) 广度性质的数值与系统的数量成正比。
(B) 强度性质的数值与系统的数量无关。
(C) 整个系统的某种广度性质是系统中各部分性质的总和。
(D) 强度性质在数学上是一次齐函数。
5、下列平衡不属于热力学平衡态的是()。
(A) 热平衡(B) 动态平衡(C) 力学平衡(D) 相平衡6、当系统的诸种性质不随时间而改变,则系统处于()。
(A) 热力学平衡状态(B) 动态平衡状态(C) 力学平衡状态(D) 化学平衡状态7、系统的某种广度性质与强度性质之间的关系是()。
(A)强度性质=广度性质/广度性质(B) 广度性质=强度性质/广度性质(C) 广度性质=强度性质/强度性质(D) 强度性质=强度性质/广度性质8、已知NaCO3和H2O可以形成三种水合物NaCO3•H2O(s)、NaCO3•7H2O(s)和NaCO3•10H2O(s),在293.15K时与水蒸气平衡共存的含水盐最多有()种。
(A) 1 ;(B) 2 ;(C) 3 ;(D) 4 。
9、对状态函数描述正确的是()。
(A) 状态是复值函数;(B) 改变量只与系统的始、终态有关;(C) 改变量只与变化途径有关;(D) 系统经历一个循环过程,状态值为1。
10、系统的状态发生变化时,它的某些性质的改变量只与系统的始态和终态有关,与系统的变化过程无关,这种特性的物理量叫做()。
(A) 广度性质;(B) 强度性质;(C) 状态函数;(D) 非状态函数。
11、孤立体系的能量与物质的交换情况是()。
33 共价晶体和分子晶体(分层作业)(解析版)2023学年高二化学(沪科版2020选择性必修2)

高二化学(沪科版2020选择性必修2 物质结构与性质)第三章晶体结构与性质3.3 共价晶体和分子晶体★基础过关练★1.下列关于分子晶体的说法不正确的是A.分子晶体中含有分子B.固态或熔融态时均能导电C.分子间以分子间作用力相结合D.熔、沸点一般比较低【答案】B【详解】A.分子晶体是由分子构成的,A正确;B.固态或熔融态时,分子晶体既不电离也没有自由移动的电子,均不能导电,B错误;C.分子间以分子间作用力相结合,C正确;D.分子晶体的熔、沸点一般比较低,D正确。
故选:B。
2.(2022·陕西·西安市阎良区关山中学高二阶段练习)下列物质属于分子晶体的是①冰;②二氧化硅;③碘;④铜;⑤固态的氩A.仅①③B.仅②③⑤C.仅⑤D.仅①③⑤【答案】D【分析】分子通过分子间作用力互相结合形成的晶体叫做分子晶体。
【详解】①冰、③碘、⑤固态的氩都是分子通过分子间作用力结合而成的晶体,属于分子晶体;②二氧化硅是共价晶体;④铜是金属晶体,故选D;答案选D。
3.(2022·天津市宁河区芦台第一中学高二阶段练习)下列叙述与范德华力无关的是A.气体物质加压或降温时能凝结或凝固B.白磷易自燃C.干冰易升华D.S8的熔、沸点较低【答案】B【详解】A.气体物质加压或降温时能凝结或凝固,克服了分子间的范德华力,A不符合题意;B.白磷易自燃,是其着火点较低,与范德华力无关,B符合题意;C.干冰易升华,是二氧化碳分子间的范德华力较弱,C不符合题意;D.S8是分子晶体,其熔、沸点较低,是由于其分子间的范德华力较弱,D不符合题意;故选B。
4.下列有关分子晶体的说法正确的有①分子晶体的构成微粒是分子,都具有分子密堆积的特征②冰融化时,分子中H-O键发生断裂③分子晶体在水溶液中均能导电④分子晶体中,分子间作用力越大,通常熔点越高⑤分子晶体中,共价键键能越大,该分子晶体的沸点一定越高⑥所有的非金属氢化物都是分子晶体⑦所有分子晶体中既存在分子间作用力又存在化学键A.1项B.2项C.3项D.4项【答案】B【解析】①分子晶体的构成微粒是分子,只含有分子间作用力的分子晶体具有分子密堆积的特征,而含有氢键的分子晶体不是密堆积,故①错误;②冰是分子晶体,熔化时只克服氢键和分子间作用力,不破坏化学键,水分子中H—O键没有断裂,故②错误;③分子晶体在水溶液中能电离的电解质,水溶液能导电,如硫酸,而在水溶液中不能电离的非电解质,水溶液不能导电,如蔗糖,故③错误;④分子晶体的熔点与分子间作用力的大小有关,通常分子间作用力越大,分子的熔、沸点越高,故④正确;⑤分子晶体熔化时,只破坏分子间作用力,不破坏分子内共价键,分子晶体的熔点高低与分子间作用力有关,与分子内共价键键能大小无关,故⑤错误;⑥所有的非金属氢化物都是由分子构成的分子晶体,故⑥正确;⑦并非所有的分子晶体中既存在分子间作用力又存在化学键,如稀有气体是单原子分子,分子中不存在化学键,故⑦错误;只有④⑥两项正确,故选B。
追俊学校高中化学 课时作业3 原子结构与元素周期表3高二3化学试题

皇泉州民德市追俊学校课时作业(三)A组—双基训练1.下列元素中,基态原子的外围电子排布不正确的是( )A.As 4s24p3B.Cr 3d44s2C.Ar 3s23p6D.Ni 3d84s2答案B解析能量相同的原子轨道在全充满(p6和d10)、半充满(p3和d5)和全空(p0和d0)状态时,体系能量较低,原子较稳。
故B项中Cr原子的外围电子排布为3d54s1。
2.元素周期表中共有18纵列,从左到右排为18列,第1列为碱金属元素(氢元素除外),第18列为稀有气体元素,则下列说法正确的是( )A.第9列元素中没有非金属元素B.第15列元素原子的最外层电子排布式是ns2np5C.最外层电子排布式为ns2的元素一在第2列D.第11、12列为d区元素答案A解析A项,第9列为第Ⅷ族,为金属元素。
B项,第15列为第ⅤA族,其元素原子的最外层电子排布式为ns2np3。
C项,He的最外层电子排布式为1s2,却在第18列。
D项,第11、12列元素原子的价电子排布式为(n-1)d10ns1~2,所以为ds区元素。
3.已知某元素+3价离子的电子排布式为1s22s22p63s23p63d5,该元素在周期表中的位置是( )A.第三周期第Ⅷ族,p区B.第三周期第ⅤB族,ds区C.第四周期第Ⅷ族,d区D.第四周期第ⅤB族,f区答案C解析某+3价离子的电子排布式为1s22s22p63s23p63d5,其原子核外电子数为23+3=26,为Fe元素,原子核外电子排布式为1s22s22p63s23p63d64s2,处于周期表中第四周期第Ⅷ族,电子最后排入的能级为3d,所以为d区元素,故选C项。
4.某主族元素的原子,4s能级上半充满,这种原子的质子数为( )A.只能是19 B.只能是24C.只能是29 D.24或29答案A5.最活泼的金属单质、最活泼的非金属单质、常温下呈液态的金属单质,其组成元素分别位于下列元素周期表中的( )A.s区、p区、ds区B.s区、p区、d区C.f区、p区、ds区D.s区、f区、ds区答案A解析理论上最活泼的金属单质是Fr,但由于其具有放射性,故一般认为最活泼的金属单质是Cs,而Cs 和Fr都属于第ⅠA族元素,位于s区;最活泼的非金属单质是F2,F位于p区;常温下呈液态的金属单质为Hg,Hg属于过渡元素,位于ds区。
上海市九年级上化学作业(答案版)

国庆化学作业姓名10月1日得分一、判断下列变化属于物理变化还是化学变化?(1)光合作用(化学变化)(2)蜡烛熔化(物理变化)(3)纸张燃烧(化学变化)(4)湿衣服晒干(物理变化)(5)火药爆炸(化学变化)(6)矿石粉碎(物理变化)(7)蜡烛燃烧(化学变化)(8)玻璃熔化(物理变化)二、区别下列属于什么性质?(1)液化气能燃烧(化学性质)(2)碳的单质在常温下性质很稳定。
(化学性质)(3)浓硫酸具有酸性。
(化学性质)(4)氨气是一种无色有刺激性气味的气体。
(物理性质)(5)浓盐酸具有挥发性(物理性质)(6)盐酸能与金属锌反应放出氢气。
(化学性质)三、写出下列实验的现象和符号表达式(1)大理石上滴盐酸现象:大理石逐渐溶解,有气泡产生符号表达式:CaCO3+ HCl →CaCl2+ H2O + CO2(2)往石灰水中吹气现象:澄清石灰水变浑浊(或有白色沉淀)符号表达式:Ca(OH)2+ CO2→CaCO3+ H2O(3)镁带燃烧现象:剧烈燃烧,耀眼白光,生成白色固体,放出热量符号表达式:Mg + O2MgO四、写出下列仪器的名称1.集气瓶 分液漏斗水槽 长颈漏斗锥形瓶 滴管 镊子 酒精灯 9. 10. 11. 12.药匙 漏斗 试管 量筒 13. 14. 15. 16.烧杯 玻璃棒 烧瓶 试管夹10月2日 得分一、写出下列仪器的名称1.(1) 铁圈 (2) 铁夹 (3) 铁架台 2.(1) 燃烧匙 (2) 毛玻璃片 (3) 集气瓶 3. 4.(1) 试管刷 (2) 试管架 (1) 蒸发皿二、实验室里所用的试剂,有的有毒,有的有腐蚀性,因此,取用时不能直接用手去拿,更不能尝药品的味道,也不要用鼻子靠近瓶口去闻试剂的气味。
三、浓硫酸沾在皮肤上,应先棉布抹去,立即用水冲洗,再用小苏打洗,最后用水冲洗;浓碱沾在皮肤上,先用水冲洗,再涂醋酸冲洗。
四、实验时,如果药品没有规定用量,液体一般取1-2mL,固体以盖满试管底部为宜。
有机化学作业

有机化学(含实验)交卷时间:2018-04-24 15:40:33 一、单选题1.(4分)醛、酮与肼类(H2N-NH2等)缩合的产物叫做( )。
• A. 羟基腈• B. 醛(或酮)肟• C. 羟胺• D. 腙得分:4知识点:有机化学(含实验)作业题展开解析答案D 解析2.(4分)下列化合物与氢气进行加成时,反应活性最小的是()• A. 乙烯• B. 丙烯• C. 2-丁烯• D. 2,3-二甲基-2-丁烯得分:4知识点:有机化学(含实验)作业题展开解析答案D 解析3.(4分)化合物和的关系是()• A. 同一化合物• B. 内消旋体• C. 对应异构体• D. 普通的同分异构体(非旋光性)得分:4知识点:有机化学(含实验)作业题展开解析答案C 解析4.(4分)和互为互变异构体,在两者的平衡混合物中,含量较大的是()• A.• B.• C. 两者差不多• D. 没法判断得分:4知识点:有机化学(含实验)作业题展开解析答案B 解析5.(4分)下列化合物能发生碘仿反应的是()。
• A. 2-甲基丁醛• B. 丁醇• C. 2-戊酮• D. 丙醇得分:4知识点:有机化学(含实验)作业题展开解析答案C 解析6.(4分)下列物质在1H NMR谱中出现两组峰的是()• A. 乙醇• B. 1-溴代丙烷• C. 1,3-二溴代丙烷• D. 正丁醇得分:4知识点:有机化学(含实验)作业题展开解析答案C 解析7.(4分)下列碳正离子中最不稳定的是()。
• A.• B.• C.• D.得分:4知识点:有机化学(含实验)作业题展开解析答案C 解析8.(4分)下列化合物没有芳香性的是();• A.• B.• C.• D.得分:0知识点:有机化学(含实验)作业题展开解析答案C 解析9.(4分)下列烯烃氢化热(KJ/mol)最低的是()。
• A.• B.• C.• D.得分:4知识点:有机化学(含实验)作业题展开解析答案D 解析10.(4分)下列羰基化合物对HCN加成反应速率最快的是()。
高中化学必修课时作业(3)

新教材•化学(RJ) 必修•第一册
新教材·化学(RJ) 必修·第一册
6.下列叙述正确的是 ( C ) A.液态氯化氢、固体氯化钾均不导电,故 HCl 和 KCl 均为非电解质 B.NH3、SO3 水溶液都能导电,故两者均为电解质 C.蔗糖、乙醇在水溶液里和熔融状态下都不导电,所以它们是非电解质 D.铜和石墨均能导电,所以它们都是电解质
新教材·化学(RJ) 必修·第一册
4.下列各组均为两种化合物溶于水时电离出的离子,其中由酸电离产生的是( B )
A.Na+、OH-、SO24-
B.H+、SO24-、Cl-
C.Na+、K+、OH-
D.K+、Na+、Cl-
解析:电离出的阳离子全部是 H+的化合物才是酸。B 正确。
新教材•化学(RJ) 必修•第一册
①溶液都是纯净物
新教材·化学(RJ) 必修·第一册
②含氧的化合物都是氧化物
③能电离出 H+的化合物都是酸 ④能电离出 OH-的化合物都是碱
⑤能电离出金属离子和酸根离子的化合物都是盐
⑥酸和碱的中和反应属于复分解反应
A.全部
B.⑤⑥
C.③④
D.①②
新教材•化学(RJ) 必修•第一册
新教材·化学(RJ) 必修·第一册
B.凡在水中能生成离子而能导电的物质
C.氧化钠溶于水能生成钠离子和氢氧根离子,尽管氧化钠是化合物,其水溶
液能导电,但溶液中的氢氧根离子并非氧化钠本身电离,因而氧化钠是非电解质
D.在水溶液里或熔融状态下本身能电离出阳离子和阴离子而能导电的化合物
新教材•化学(RJ) 必修•第一册
新教材·化学(RJ) 必修·第一册
新教材·化学(RJ) 必修·第一册
(1)通入 CO2 前,灯泡____亮____(填“亮”或“不亮”)。 (2)开始通入 CO2 时,灯泡的亮度___先__变__暗__后__熄__灭____。 (3)继续通入过量的 CO2,灯泡的亮度__熄__灭___后__又__逐__渐__变__亮___。 (4)下列四个图像中,____D____(填字母)能比较准确地反映出溶液的导电 能力和通入 CO2 的量的关系(x 轴表示通入 CO2 的量,y 轴表示导电能力)。
高中化学第一节第1课时作业

第一节第1课时作业题组一能层的理解与应用1.在基态多电子原子中,关于核外电子能量的叙述错误的是()A.最易失去的电子能量最高B.离核最远的电子能量最高C.p能级电子的能量一定高于s能级电子的能量D.在离核最近的区域内运动的电子能量最低2.在同一个原子中,M能层上的电子与Q能层上的电子的能量()A.前者大于后者B.后者大于前者C.前者等于后者D.无法确定3.下列说法中错误的是()A.某原子K层上只有一个电子B.某离子M层和L层上的电子数均为K层的4倍C.某原子M层上的电子数为L层电子数的4倍D.存在核电荷数与最外层电子数相等的离子题组二能层和能级4.下列有关能层和能级的叙述正确的是()A.M能层有s、p共2个能级,最多能容纳8个电子B.3d能级最多容纳5个电子,3f能级最多容纳7个电子C.无论哪一能层的s能级最多容纳的电子数均为2D.任一能层都有s、p能级,但不一定有d能级5.某一能层上n d能级最多所能容纳的电子数为()A.6 B.10 C.14 D.156.总共含有6个能级的能层符号为()A.M B.N C.P D.Q7.下列能级符号表示正确且最多容纳的电子数按照从少到多的顺序排列的是() A.1s、2p、3d B.1s、2s、3sC.2s、2p、2d D.3p、3d、3f题组三原子的基态、激发态与原子光谱8.下列关于同一种原子的基态和激发态的说法正确的是()A.基态时的能量比激发态时高B.激发态时比较稳定C.由基态转化为激发态的过程中吸收能量D.电子仅在激发态跃迁到基态时才会产生原子光谱9.(2022·成都高二期中)吸收光谱和发射光谱统称为原子光谱。
下列说法错误的是()A.同一种元素原子的吸收光谱和发射光谱的特征谱线相同B.霓虹灯光与原子核外电子发生跃迁释放能量有关C.光谱仪可以摄取元素的吸收光谱和发射光谱D.目前发现的元素都是通过原子光谱发现的10.元素Na的焰色试验呈黄色,从能量变化的角度其光谱类型属于()A.发射光谱B.吸收光谱C.连续光谱D.线状光谱11.对充有氖气的霓虹灯管通电,灯管发出红色光。
无机化学在线作业答案

单选题1.溶胶发生电泳时,向某一方向定向移动的是()。
• A 胶核• B 吸附层• C 胶团• D 胶粒正确答案:D单选题2.误差的正确定义是()。
• A 测量值与其算术平均值之差• B 含有误差之值与真值之差• C 测量值与其真值之差• D 错误值与其真值之差正确答案:C单选题3.属于随机误差的是()。
• A 滴定终点与化学计量点不一致• B 把滴定管的读数22.45读成22.46• C 用纯度为98%的CaCO3标定EDTA标准溶液的浓度• D 称量时把1g的砝码看成2g正确答案:B单选题4.称取同样质量的两种难挥发的电解质A和B,分别溶解在1升水中,测得A溶液的凝固点比B溶液的凝固点低,则()。
• A B的分子量小于A的分子量• B A的分子量和B的分子量相同• C B的分子量大于A的分子量正确答案:C单选题5.最易于形成配离子的金属元素位于周期表中的()。
• A p区• B d区和ds区• C s区和p区• D s区正确答案:B单选题6.两成键原子的原子轨道沿核间连线以“肩并肩”方式重叠形成()。
• A σ键• B 离子键• C Π键• D 氢键正确答案:C单选题7.从精密度好就可以断定分析结果可靠的前提是()。
• A 随机误差小• B 系统误差小• C 平均偏差小• D 标准偏差小正确答案:B单选题8.在配制FeCl3溶液时,为防止溶液产生沉淀,应采取的措施是()。
• A 加碱• B 加酸• C 多加水• D 加热正确答案:B单选题9.下列说法错误的是()。
• A 方法误差属于系统误差• B 系统误差又称可测误差• C 系统误差服从正态分布• D 系统误差具有单向性正确答案:C单选题10.在定量分析中,精密度与准确度之间的关系是()。
• A 精密度高,准确度必然高• B 准确度高,精密度也就高• C 精密度是保证准确度的前提• D 准确度是保证精密度的前提正确答案:C单选题11.HCl和H2O两分子间形成的分子间作用力有()。
普通化学第三阶段在线作业

∙普通化学第三阶段在线作业单选题 (共36道题)1.(2.5分)某元素A的原子属于第二周期,最外层有7个电子,它属于____ 族,___区,__ 属(填金或非金)。
∙ A、VIIA,p区,非金属∙ B、VIIA,s区,非金属∙ C、VIA,p区,金属∙ D、VIA,s区,金属我的答案:A 此题得分:2.5分2.(2.5分)元素甲的外层电子构型为3s23p5,则该元素的未成对电子数、周期、族、区分别为。
∙ A、1,3,VIIA,p∙ B、2,3,VIA,p∙ C、1,3,VIA,p∙ D、2,3,VIIA,s我的答案:A 此题得分:2.5分3.(2.5分)原子核外电子层结构为3d64S2的原子序数是,该元素位于周期表第周期,第族。
∙ A、25,3,VIII∙ B、25,4,VIIA∙ C、26,4,VIIA∙ D、26,4, VIII我的答案:D 此题得分:2.5分4.(2.5分)下列各组量子数哪个是不合理的____ 。
∙ A、n=1, 1=1, m=0∙ B、n=3, 1=2, m=1∙ C、n=2, 1=0, m=-1∙ D、n=4,1=2,m=-2我的答案:A 此题得分:2.5分5.(2.5分)磁量子数m描述核外电子运动状态的。
∙ A、电子能量高低;∙ B、电子自旋方向;∙ C、电子云形状;∙ D、电子云的空间伸展方向;我的答案:D 此题得分:2.5分6.(2.5分)某元素原子基态的电子构型为1s22s22p5,它在周期表中的位置是。
∙ A、p区ⅦA族∙ B、s区ⅡA族∙ C、ds区ⅡB族∙ D、p区Ⅵ族我的答案:A 此题得分:2.5分7.(2.5分)鲍林(pauli)原理的要点是。
∙ A、需用四个不同量子数来描述原子中每个电子∙ B、在同一原子中,不可能有四个量子数完全相同的两个电子存在∙ C、每一个电子层,可容纳8个电子∙ D、在一个原子轨道中可容纳自旋平行的两个电子我的答案:B 此题得分:2.5分8.(2.5分)在多电子原子中,轨道能级与。
无机及分析化学作业

1、指出下列配合物的名称、中心离子的氧化值和配位数、配离子的电荷。
[Pt(NH 3)2Cl 2] [Co(N 3)(NH 3)3]SO 4 Na 3[Ag(S 2O 3)2] [Pt(CN)4(NO 2)I]2- [Fe(CN)5(CO)]3- [Co(ONO)(NH 3)3(H 2O)2]Cl 2 K 2[Zn(OH)4] [Cr(en)3]3+ 注:NO 2代表以N 原子配位的硝基,ONO 代表以O 原子配位的亚硝酸根,en 代表乙二胺。
解:名称 氧化值 配位数 配离子电荷 (1)二氮·二氨合铂(Ⅱ) 2+ 4 0 (2)硫酸一叠氮酸根·三氨合钴(Ⅲ) 3+ 6 2+ (3)二硫代硫酸根合银(Ⅰ)酸钠 1+ 2 3- (4)一碘·四氰一硝酸合铂(Ⅵ)离子 4+ 6 2- (5)五氰·一碳基合铁(Ⅱ)离子 2+ 6 3- (6)二氯亚硝酸根·二水三氨合钴(Ⅲ) 3+ 6 2+ (7)四羟基合锌(Ⅱ)酸钾 2+ 4 2- (8)三乙二胺合铬(Ⅲ)离子 3+ 6 3+2、AgNO 3能从化合物Pt(NH 3)6C14的溶液中将所有的氯沉淀为AgCl ,但在Pt(NH 3)3Cl 4溶液中仅能沉淀1/4的氯。
试根据这些事实写出这两种配合物的结构式。
解:沉淀的是,不能沉淀配合物中作为配体的,配离子内界无法沉淀,配离子外界可以沉淀前者为后者为3、有两种配位化合物A 和B ,元素分析表明它们具有相同的组成:21.95%Co ,39.64%Cl ,26.08%N ,6.38%H ,5.95%O ,根据下列实验现象,确定它们的配离子,中心离子和配位数。
⑴、A 和B 的水溶液都呈微酸性,加入强碱并加热至沸腾时,有氨放出,同时析出Co 2O 3沉淀;⑵、向A 和B 的水溶液中加入AgNO 3溶液时都生成AgCl 沉淀;⑶、过滤除去上述两种溶液中的AgCl 后,再加AgNO 3均无变化,但加热至沸腾时,在B 的溶液中又有AgCl 生成,其质量为原来析出沉淀的一半。
2022化学新高考(双选版)课时作业(三十三) 分子结构与性质

课时作业(三十三)分子结构与性质1.下列化学式对应的结构式从成键情况看不合理的是()D[H、Se、N、C、Si形成的共用电子对数分别是1、2、3、4、4。
D选项中,C、Si 形成的共用电子对数分别为3、3,不合理。
]2.N2的结构可以表示为,CO的结构可以表示为,其中椭圆框表示π键,下列说法中不正确的是()A.N2分子与CO分子中都含有三键B.CO分子中有一个π键是配位键C.N2与CO互为等电子体D.N2与CO的化学性质相同D[由题意可知N2分子中N原子之间、CO分子中C、O原子之间均通过2个π键,一个σ键,即三键结合。
其中,CO分子中1个π键由O原子单方面提供孤电子对,C原子提供空轨道通过配位键形成。
N2化学性质相对稳定,CO具有比较强的还原性,两者化学性质不同。
]3.下表所列的是不同物质中氧氧键的键长和键能的数据,其中a和b未测出,根据一个原则可估计键能大小顺序为d>c>b>a,该原则是()O2-2O-2O2O+2键长/nm 149 128 121 112键能/(kJ/mol) a b c=494 d=628 AB.成键电子数越少,键能越大C.键长越短的键,键能越大D.以上都不是C[可以根据键长判断键能的大小。
]4.在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。
则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是() A.sp,范德华力B.sp2,范德华力C.sp2,氢键D.sp3,氢键C[由石墨的晶体结构知C原子为sp2杂化,故B原子也为sp2杂化,但由于B(OH)3中B原子与3个羟基相连,羟基间能形成氢键,故同层分子间的主要作用力为氢键。
] 5.CH+3、—CH3、CH-3都是重要的有机反应中间体,有关它们的说法正确的是() A.它们互为等电子体,碳原子均采取sp2杂化B.CH-3与NH3、H3O+互为等电子体,立体构型均为正四面体形C.CH+3中的碳原子采取sp2杂化,所有原子均共面D.CH+3与OH-形成的化合物中含有离子键C[A项,CH+3、—CH3、CH-3分别具有6个、7个和8个价电子,不是等电子体,且—CH3和CH-的碳原子采取sp3杂化,错误;B项,三者均为三角锥形,错误;C项,3CH+3中C的价电子对数为3,为sp2杂化,平面三角形,正确;D项,CH3OH中不含离子键,错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
班化学作业33 201 年 月 日 星期
姓名
1. 为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl (精盐)溶液,上图是该同学转移溶液
的示意图,图中的错误是___________________、_____________________。
2. 有NaCl 、FeCl 2、FeCl 3、MgCl 2、AlCl 3五种溶液,只用一种试剂就可把它们鉴别开来,这
种试剂是( )
A.盐酸
B.烧碱溶液
C.氨水
D.KSCN 溶液
3. 制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制
得.用以上两种方法都可制得的氯化物是( )
A.AlCl 3
B.FeCl 3
C.FeCl 2
D.CuCl 2 4. 某溶液中有Fe 3+、Mg 2+、Fe 2+和Al 3+四种阳离子,若向其中加入过量的氢氧化钠溶液,
搅拌后,再加入过量的盐酸,溶液中大量减少的阳离子是( )
A.Fe 3+
B.Mg 2+
C.Fe 2+
D.Al 3+
5.在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K +、Al 3+、Cl -、SO 2-4
B.含有0.1 mol·L -1 Fe 3+的溶液中:K +、Mg 2+、I -、NO -
3
C.含有0.1 mol·L -1 Ca 2+的溶液中:Na +、K +、CO 2-3、Cl -
D.室温下,pH =1的溶液中:Na +、Fe 3+、NO -3、SO 2-4
6. 除去下列物质中所含的杂质(括号内为杂质),将选用的试剂和分离方法填在题后的横线上,并写出有关反应的离子方程式。
(1)Fe 2O 3[Fe(OH)3] ;
(2)Fe 2O 3(Al 2O 3) ;
(3)FeCl 3(FeCl 2) ;
(4)FeCl 2(FeCl 3) ;
(5)FeCl 2(CuCl 2) ;
(6)Fe(Al) 。
7. 某同学为了检验家中的一瓶补铁药(成分为FeSO 4)是否变质,查阅了有关资料,得知Fe 2+能被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色,并结合已学的知识设计了如下实验:
将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,在一支试管中滴入酸性高锰酸钾溶液,在另一支试管中滴入KSCN 溶液。
请你填出该同学实验中出现以下现象时应得出的结论:
(1)若滴入酸性高锰酸钾溶液后褪色,滴入KSCN 溶液后不变红,结论是 。
(2)若滴入酸性高锰酸钾溶液后不褪色,滴入KSCN 溶液变红,结论是 。
(3)若滴入酸性高锰酸钾溶液后褪色,滴入KSCN 溶液变红,结论是 。
(4)能不能将KMnO 4和KSCN 滴入到同一试管中进行验证,为什么?试进行解释 ____________________________.
8. 向Ba (OH)2溶液中逐滴加入稀硫酸。
⑴ 写出反应的离子方程式_________________________________
⑵ 向盛有一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整
个过程中混合溶液的导电能力(用电流强度I 表示)近似地用右图的
曲线表示是( )
⑶ 在一烧杯中盛有Ba(OH)2溶液,同时有一表面光滑的塑料小球悬
浮于溶液中央,如右图所示。
向该烧杯里缓缓注入与稀H 2SO 4等密度
的Ba(OH)2溶液至恰好完全反应。
在此实验过程中小球将( )
A. 沉入水底
B. 上浮至水面
C. 不动
D. 上下浮动。
