羧酸银盐和溴或碘反应
华中科技大学有机化学第十二章 羧酸及其衍生物

用强酸酸化羧酸盐可使羧酸游离出来。由于羧酸的碱金属盐都 溶于水,因而可利用这个性质使羧酸与其它不溶于水的中性有机 物分离。一般的酚不溶于 NaHCO3 溶液,因而可以利用羧酸与 NaHCO3生成水溶性羧酸钠盐而与酚分离。 由于羧酸钠和钾盐的水溶性,制药工业常把含有羧基的药物 变成盐,使不溶于水的药物变成水溶性的。例如青霉素G分子中含 有羧基,一般将它制成钠盐或钾盐供临床注射。
由于负电荷分散在共轭体系中,羧酸根负离子与相应的烷氧基 负离子相比有大得多的稳定性,因此羧酸的酸性比醇强得多。但羧 酸仍是一种弱酸,一元饱和脂肪族羧酸的pKa值一般在3—5之间。
羧酸可与金属氧化物、氢氧化物作用生成盐。
利用羧酸和碱的中和反应,可以定量测定羧酸的含量和羧基的数目。 羧酸的酸性比碳酸强,因而羧酸能与碳酸盐或碳酸氢盐作用形成羧酸盐 并放出二氧化碳。
羧酸分子中去掉羟基后的基团(RCO)叫做酰基(acyl group),酰基 根据相应的羧酸来命名。例如:CH3CO-乙酰基,C6H5CO-苯甲酰基。 许多羧酸都有根据其来源的俗名,例如甲酸最初来自蚂蚁因而叫做 蚁酸,乙酸是食醋的主要成分,因而叫做醋酸等。
三、羧酸的物理性质 常见的一元羧酸的物理常数见下表。
六、二元羧酸受热的反应 二元羧酸受热易脱水、脱羧,生成产物的结构取决于两个 羧基的相对位置。无水草酸在加热时脱羧生成甲酸。
丙二酸及烃基取代的丙二酸加热到熔点以上时脱羧生成乙酸或取代乙酸;
丁二酸和戊二酸在单独加热或与乙酐共热时,脱水生成环酐
己二酸和庚二酸受热时同时发生脱水和脱羧,生成较为稳定的 五元环或六元环酮。
羧酸及其衍生物广泛存在于自然界,是生命活动的重要物质。 许多羧酸及其衍生物本身就是重要的临床药物、香料和日用化学品等, 同时它们也是医药工业和其它有机化学工业的原料或中间体。
《药物合成反应(闻韧主编第三版)》人名反应整理(新)

《药物合成反应(闻韧主编第三版)》人名反应整理一、卤化反应1、Hunsdriecke反应(汉斯狄克反应):羧酸银盐和溴或碘反应,脱去二氧化碳,生成比原反应物少一个碳原子的卤代烃。
☆☆☆☆☆2、Sandmeyer反应(桑德迈尔反应):用氯化亚铜或溴化亚铜在相应的氢卤酸存在下,将芳香重氮盐转化成卤代芳烃。
☆☆3、Gattermann反应(加特曼反应):将Sandmeyer反应条件改为铜粉和氢卤酸。
☆☆4、Schiemann反应(席曼反应):将芳香重氮盐转化成不溶性的重氮氟硼酸盐或氟磷酸盐,或直接将芳胺用亚硝酸钠和氟硼酸进行重氮化,此重氮盐再经热分解(有时在氟化钠或铜盐存在下加热),就可以制得较好收率的氟代芳烃。
☆二、烃化反应5、Willamson合成(威廉姆森合成):醇在碱(钠、氢氧化钠、氢氧化钾等)存在下与卤代烃反应生成醚的反应。
☆☆☆☆6、Gabriel合成(盖布瑞尔合成):将氨先制备成邻苯二甲酰亚胺,利用氮上氢的酸性,先与氢氧化钾形成钾盐,然后与卤代烃作用,得N-烃基邻苯二甲酰亚胺,再经过肼解或酸水解即可得纯伯胺。
☆☆☆☆☆7、Delepine反应(德勒频反应):用卤代烃与环六亚甲基四胺(乌洛托品Methenamine)反应得季铵盐,然后水解即可得伯胺。
8、Leuckart-Wallach反应(鲁卡特-瓦拉赫反应):用甲酸及其铵盐可对醛酮进行还原烃化,得各类胺。
☆9、Ullmann反应(沃尔曼反应):卤代芳烃与芳香伯胺在铜或碘化铜及碳酸钾存在并加热的条件下可得二苯胺及其同系物。
三、酰化反应10、Friedel-Crafts反应(傅列德尔-克拉夫茨反应,也称傅-克酰基化反应):羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
☆☆☆☆☆11、Hoesch反应(赫施反应):腈类化合物与氯化氢在Lewis酸催化剂ZnCl2等的存在下与烃基或烷氧基取代的芳烃进行反应可生成相应的酮亚胺,再经水解则得到羟基或烷氧基取代的芳香酮。
基础有机化学合成中增减一个碳原子的方法

基础有机化学合成中增减一个碳原子的方法作者:邹光龙来源:《教育教学论坛》2014年第31期有机化学作为大学化学、生物、医学、环境科学及材料学等专业开设的一门基础课,不仅要求掌握结构、反应、合成等方面的基本知识,而且要学会鉴定、表征有机化合物。
但是如何加深学生对有机化学基本概念、基本理论、基本反应的理解,提高学生分析和解决问题的能力?如何建立和培养学生的逻辑推理思维,找寻出貌似千差万别的各种反应的共同特征和规律?在有机化学的学习中,有机化学合成往往是学生感到头疼的难题,本文对一些典型的增减一个碳原子的合成方法进行了详细的总结,这在一定程度上为学生解开难题提供了一些可用的钥匙。
这样不仅能避免学生硬背书本,而且可以增强他们学习的兴趣。
一、有机化学反应种类繁多、反应机理复杂,内容庞杂因此本文对有机化学合成中增加和减少一个碳原子的合成方法进行了剖析。
常见的用于增加一个碳原子的试剂有:CO2,CO,HCN,NaCN,CH2I2,CHCl3,CH2Cl2,CH3OH,(CH3)2LiCu,HCHO,CH3MgI,Ph3P=CH2,(CH3)2SO4,CuCN,CO(NH2)2,氨基脲等。
下面我们具体举例说明如下:1.丙烯与四氯化碳在过氧化物存在下进行自由基加成反应生成比原料多一个碳原子的产物:2.乙炔在氯化铵-氯化亚铜水溶液中可与氢氰酸加成得到丙烯腈。
3.西蒙斯-斯密斯(Simons-Smith)于1959年提出了一个合成环丙烷的好方法,即在锌-铜合金存在下,二碘甲烷与烯作用生成环丙烷及衍生物,且其加成立体化学为顺式加成。
例如:4.卤代烃的氰解,即卤代烃与氰化钠在乙醇溶液中反应,卤原子被氰基取代而生成腈。
5.卡宾(:CCl2:和:CH2)作为一种重要的活泼中间体,对烯烃的插入反应,生成三元环化合物。
例如:6.二烷基铜锂与卤代烷反应生成烷烃,常用来合成各种结构的高级烷烃、烯烃和芳烃。
例如:二甲基铜锂与α,β不饱和醛、酮的反应以1,4-加成为主。
羧基与碘离子反应-概述说明以及解释

羧基与碘离子反应-概述说明以及解释1.引言1.1 概述概述部分可以介绍羧基与碘离子反应的背景及其在化学领域中的重要性。
可以包括以下内容:羧基与碘离子反应是一种重要的有机化学反应,它在有机合成和化学分析等领域具有广泛的应用。
羧基化合物是一类含有羧基(-COOH)官能团的有机分子,具有较高的反应活性和化学稳定性。
羧基化合物广泛存在于天然产物、药物和生物活性分子中,因此羧基反应的研究具有重要的理论和应用价值。
碘离子是一种带负电荷的离子,其化学性质活泼而多变,在有机合成反应中常被用作催化剂或试剂。
碘离子可以参与氧化、还原、取代、加成等多种反应,与羧基反应中的亲核试剂或电子云丰满的基团发生相应的反应。
羧基与碘离子反应是指羧基化合物与碘离子之间发生一系列化学反应,包括羧基取代、脱羧、羧酸酯形成等。
这些反应可以通过不同的条件和催化剂控制反应的选择性和产物的生成,实现有机合成中的底物转化和功能化。
本文主要对羧基与碘离子反应的机制、反应条件和影响因素等进行了系统的探讨和总结,并对其在有机合成和化学分析中的应用进行了归纳和展望。
通过深入研究羧基与碘离子反应,可以拓展有机化学的反应范围,提高化学合成的效率和选择性,也有助于揭示有机化合物的结构与功能之间的关系。
未来的研究可以进一步探索羧基与碘离子反应的新的应用领域和机制,开发新的催化剂和反应体系,提高反应的效率和产物的纯度,促进有机化学的发展和应用。
1.2文章结构文章结构部分可以包括以下内容:1.2 文章结构本文按照以下结构进行组织和论述:第一部分是引言部分,主要对本文的研究对象和目的进行概述,介绍羧基与碘离子反应的背景和重要性。
第二部分是正文部分,主要包括三个小节。
第一小节将对羧基的定义和性质进行详细介绍,包括其结构特点、物理化学性质和常见的功能和应用。
第二小节将对碘离子的定义和性质进行详细阐述,包括其电子结构、化学性质和常见的反应类型。
第三小节将重点探讨羧基与碘离子反应的机制,结合实验数据和理论研究结果,分析反应过程中的关键步骤和反应机理。
有机化学基础知识点整理羧酸的衍生物与反应

有机化学基础知识点整理羧酸的衍生物与反应羧酸的衍生物与反应羧酸是有机化学中常见的一类化合物,具有羧基(-COOH)的结构特征。
羧酸的衍生物是指通过对羧酸进行化学反应或者取代得到的相关化合物。
羧酸的反应涉及到许多重要的有机合成反应和应用,对于有机化学的学习非常重要。
本文将对羧酸的衍生物以及与之相关的反应进行整理和概述。
一、酯的合成酯是羧酸醇酯化反应的产物,也是羧酸衍生物中使用最广泛的一种化合物。
酯的合成通常通过将羧酸与醇在酸性条件下进行酯化反应而得到。
此反应是通过羧基中的羟基与醇发生酯化反应而形成的,其反应方程式如下所示:羧酸 + 醇→ 酯 + 水酯化反应可以在各种温度下进行,常见的催化剂有硫酸、盐酸等。
酯化反应是有机合成中的重要步骤,能够制备出许多重要的化合物,如乙酸乙酯、苯甲酸甲酯等。
二、酰氯的合成酰氯是羧酸与氯化物反应生成的一种衍生物。
酰氯是有机合成中常用的试剂,可以作为中间体参与进一步的化学反应。
羧酸与氯化物反应生成酰氯的反应方程式如下所示:羧酸 + 氯化物→ 酰氯 + 酸常见的氯化物有氯化亚砜、氯化磷等。
酰氯在合成中起到重要的作用,可以进一步发生亲核取代反应、缩合反应等。
三、酰亚胺的合成酰亚胺是羧酸与胺反应生成的衍生物,分子中含有酰基与氨基。
酰亚胺具有一定的稳定性和活性,可以作为有机化合物的合成中间体。
酰亚胺的反应方程式如下所示:羧酸 + 胺→ 酰亚胺 + 水酰亚胺的合成可以通过将羧酸与胺在酸性条件下反应而得到。
酰亚胺在有机合成中应用广泛,可以进行类似于酯的各种反应。
四、酰胺的合成酰胺是羧酸与氨反应生成的一种衍生物,分子中含有酰基与氨基。
常见的酰胺有酰胺与酰胺。
酰胺的合成通常通过将羧酸与氨在酸性或碱性条件下反应而得到。
酰胺的反应方程式如下所示:羧酸 + 氨→ 酰胺 + 水酰胺是许多药物和生物活性分子的结构基础,也是有机化学中重要的中间体。
综上所述,羧酸的衍生物包括酯、酰氯、酰亚胺和酰胺等,它们在有机合成和应用领域中具有广泛的应用。
羧酸及羧酸衍生物的重要反应及重要反应机理

资料范本本资料为word版本,可以直接编辑和打印,感谢您的下载羧酸及羧酸衍生物的重要反应及重要反应机理地点:__________________时间:__________________说明:本资料适用于约定双方经过谈判,协商而共同承认,共同遵守的责任与义务,仅供参考,文档可直接下载或修改,不需要的部分可直接删除,使用时请详细阅读内容第六章羧酸及羧酸衍生物的性质及重要反应机理一、羧酸的化学性质1.酸性羧酸具有酸性,诱导、共轭、场效应等对酸性强弱有影响。
利用羧酸的酸性可以制备羧酸酯和羧酸盐。
2.亲核取代反应这是羧酸在一定条件下转变成羧酸生物的反应。
大多数亲核取代反应是通过加成-消除历程完成的。
3.还原反应羧酸能被LiAlH4和B2H6还原成相应的伯醇。
4.α-H的卤化(Hell-Volhard-Zelinsky反应)通过控制卤素的用量可以制备一元或多元的卤代羧酸,并进一步制备羟基酸和氨基酸。
5.脱羧反应羧酸在适当的条件下,一般都能发生脱羧反应,这是缩短碳链的反应。
通常的脱羧反应表示如下:A为-COOH、-CN、-(C=O)R、-NO2、-CX3、-C=O、C6H5-等吸电子基团时,脱羧反应相当容易进行。
此外还有一些特殊的脱羧方法。
二元羧酸的脱羧规律是:乙二酸、丙二酸、加热失羧,丁二酸、戊二酸加热是水生成分子内酸酐,己二酸、庚二酸加热是水、失羧生成环酮。
根据以上反应可以得出一个结论,在有机反应中有成环可能时,一般易形成五元环或六元环。
这称为布朗克(Blanc)规则。
二、羧酸衍生物的化学性质1.亲核取代反应这是羧酸衍生物的转换反应。
转换的活性顺序为:RCOX>CRCOOOCR>RCOOR′>RCONR2酸和碱都能催化反应。
2.与有机金属化合物的反应选用空阻大的酰卤,反应能控制在酮的阶段。
选用甲酸酯,可以制备对称二级醇。
选用碳酸酯,可制备三个烃基相同的三级醇。
二元酸的环状酸酐可用来制备酮酸。
界限突破:无需过渡金属,芳香羧酸加点碱就能脱羧溴化

界限突破:无需过渡金属,芳香羧酸加点碱就能脱羧溴化羧酸在自然界中广泛存在,廉价易得。
将羧酸及其衍生物脱羧后转化为其他合成子不失为一种有效的策略来获取多种结构单元。
说起脱羧卤化过程,大家应该会想到Hunsdiecker反应。
早在1861年,俄国化学家A. Borodine便发现,CH3COOAg与Br2混合,在加热条件下可以消除一分子CO2得到脱羧溴化产物。
直至1942年,德国化学家H. Hunsdiecker才对该反应过程进行深入研究,将脂肪族羧酸转化为相应的银盐,引入Br2后加热得到减少一个碳原子的溴代烃。
Hunsdiecker反应(图片来源:参考资料[1])Hunsdiecker反应在20世纪后半叶得到了进一步拓展。
这种脱羧溴化过程不仅适用于烷基、烯基等脂肪族羧酸,部分芳香羧酸也能顺利参与反应。
Br2可换作Cl2、I2等其他卤素来源,甚至在反应条件改进后还能使用BrCCl3、CHI3等其他更加温和的卤化试剂完成以上过程。
反应所需的羧酸银盐通过相应的羧酸与Ag2O混合制得,并保证银盐干燥无水且纯度较高。
考虑到其热稳定性较差,有时人们还尝试将羧酸制备成亚铊(Tl I)盐、亚汞(Hg I)盐提高反应的可重现性。
尽管如此,Hunsdiecker反应仍旧存在一定的局限性。
该反应需借助化学计量的重金属氧化物方可实现,形成的亚铊盐与亚汞盐还具有较强的毒性。
除此之外,仅贫电子的芳香羧酸才能有效发生Hunsdiecker反应,富电子芳香羧酸则容易与卤素单质发生亲电芳香卤化,反应的选择性较差,由此限制了底物的适用范围。
脱羧溴化反应的发展历程(图片来源:参考资料[2])溴代芳香烃作为重要的芳基来源可参与过渡金属催化的交叉偶联反应,还能用于制备芳基锂、芳基格氏试剂等有机金属试剂。
为此,人们仍需要更为通用的手段,高效构建多种不同结构的溴代芳香烃满足有机合成反应中的需求。
今天我们要介绍的工作来自化学期刊Chem. Sci.,英国曼彻斯特大学(University of Manchester)的Igor Larrosa教授在2018年发展了一种不同于传统Hunsdiecker反应途径的脱羧溴化过程,反应规避了使用重金属氧化物及过渡金属催化剂,仅需加入廉价易得的无机碱K3PO4,便可打破富电子芳香羧酸反应困难的壁垒。
溴和硝酸银反应

溴和硝酸银反应溴和硝酸银反应是一种重要的化学反应,在化学实验中经常被用于检测卤素的存在。
这种反应是一种氧化还原反应,其反应方程式为: AgNO3 + Br2 → AgBr + HNO3在这个反应中,溴(Br2)被氧化为溴离子(Br-),硝酸银(AgNO3)被还原为银(Ag)和亚硝酸(HNO2)。
这个反应是可逆反应,可以逆向进行。
这个反应在实验室中经常被用于检测卤素的存在。
当溴与硝酸银反应时,会产生一种黄色的沉淀,这种沉淀就是溴化银(AgBr)。
如果溴化银的颜色出现,就可以证明样品中含有卤素。
这个反应也可以用于区分不同的卤素。
当氯(Cl2)与硝酸银反应时,会产生一种白色的沉淀,这种沉淀就是氯化银(AgCl)。
当碘(I2)与硝酸银反应时,会产生一种淡黄色的沉淀,这种沉淀就是碘化银(AgI)。
除了在实验室中用于检测卤素的存在,溴和硝酸银反应还有其他的应用。
例如,在摄影中,溴化银是一种常用的感光剂。
当溴化银暴露在光线下时,它会被光线激发,使其发生化学反应,从而形成影像。
此外,溴和硝酸银反应还可以用于制备其他化合物,如溴酸银(AgBrO3)和硝酸溴(HBrO3)等。
虽然溴和硝酸银反应在实验室和工业生产中有着广泛的应用,但它也有一些安全隐患。
首先,溴是一种有毒的化学物质,如果不小心吸入或摄入,会对人体造成严重的伤害。
此外,硝酸银也是一种有毒的化学物质,如果不小心接触到皮肤或眼睛,会引起化学灼伤。
因此,在进行溴和硝酸银反应时,必须要采取严格的安全措施,如佩戴防护眼镜和手套,保持实验室通风等。
总之,溴和硝酸银反应是一种重要的化学反应,在实验室和工业生产中有着广泛的应用。
它不仅可以用于检测卤素的存在,还可以用于制备其他化合物。
但是,在进行这个反应时,必须要注意安全,避免对人体造成伤害。
有机化学二各章小结

有机化学(二)各章小结第一章羧酸一、羧酸的分类与羧基相连的烃基不同:脂肪酸、芳香酸与羧基相连的烃基饱和程度不同:饱和酸、不饱和酸羧基的数目:一元酸、二元酸、多元酸二、命名1. 普通命名法(简单羧酸)2. 系统命名法(1)选含羧基的最长的碳链作为主链(有不饱和键的选含羧基和不饱和键的最长碳链)(2)从羧基开始编号(3)全名:取代基位次-取代基名称-主链碳数羧酸名称(酸、二酸等)(4)羧基与环相连,以脂环基或芳基的名称+甲酸,其他基团作为取代基命名(5)环上及侧链都有羧基者,则以脂肪酸为母体命名二、物理性质1. 物态(C-C—液态,C以上固体,二酸和芳酸晶状固体)10192. 水溶性C1-C4与水混溶(氢键)M增加水溶性减小3. 沸点(比分子量相同的醇高—分子间氢键,分子间双分子缔合)4. 熔点(锯齿状变化,偶数>相邻奇数)三、光谱性质IR:νC=O伸缩振动-1 -1cm二缔合体~RCOOH:单体 1770-1750 cm1710-1 1720 cm=CHCOOHCH:单体~2-1cm~1690 二缔合体1715-1 1680 cm二缔合体1700~ArCOOH:-1(单体)cm: 气态~3550 O-H伸缩振动-1-1cm~2500 二聚体3000 cm-11250 伸缩振动~cmC-O-1-1cmcm和~900O-H弯曲振动~1400 NMR:RCHCOOH R=2-2.6δCHCOOH 22RCOOH δ=10.5-13四、结构分析C—sp2杂化、三个σ键、键角120°C=O的构成:一个σ一个π键C=O键长0.123nm、C-O键长0.136nm-:C-O键长相等,均为COO0.127 nm-五、化学性质1. 酸性(1)弱酸一元酸:pKa =4~5比一般无机强酸弱,比碳酸强(pKa=6.36)二元酸:KaKa pKa112><pKa(吸电诱导和场效应)2(2)影响酸性的因素A. 诱导效应:吸电诱导效应酸性增强供电诱导效应酸性减弱(短程效应,离的越近作用越强)B. 共轭效应吸电共轭效应使酸性增强、供电共轭效应使酸性减弱(取代芳酸:邻位异构体大于间位和对位异构体)C. 场效应(3)成盐(4)酸性的应用:鉴别、分离、提纯、制备酯(S2) N 2. 酰化反应—羧酸衍生物的生成(1)酰卤的生成试剂:羧酸+无机酸的酰卤(PX 、PX 和SOCl ) 235(2)酸酐的生成 甲酸脱水生成一氧化碳脱水剂:PO 、乙酐等 52丁二酸、戊二酸、邻苯二甲酸加热生成五元环或六元环的酸酐还可用酰卤与无水羧酸盐共热制备(3)酯的生成及酯化反应机理A. 酯化反应试剂:羧酸、醇 催化剂:H SO 、HCl 、对甲苯磺酸等 42特点:可逆反应 也可用羧酸盐与卤代烃反应制备.B. 两种反应机理: (Ⅰ)酰氧键断裂双分子历程(大多数酯化反应的历程) (Ⅱ)烷氧键断裂单分子历程(叔醇酯化反应历程)+OOHOH +HR'OH R C OHR C OHR C OHHOR' +OHOH OH ?£-? +2R C OHR C OR'2 + OR'+OOH +H ??£-R C OR'R C OR'+H +OCRCOHH+R 233 O OO +R' C OHH +R' C OHR' C OCR +CR 3 3 CR 3(4)酰胺的生成试剂:羧酸、氨或胺→羧酸铵→加热→酰胺或取代酰胺3. 还原反应还原剂:LiAlH 产物:伯醇 4特点:产率高、不影响碳碳不饱和键4. 脱羧反应(1)饱和一元酸脱羧A. 低级羧酸盐与碱石灰共熔脱羧→烃B. α-碳原子连有吸电子基较易脱羧C. 邻、对位连有强吸电基团的芳酸比饱和一元酸易脱羧D. 羧酸盐电解脱羧(钾或钠盐)→阳极偶联→烃(Kolbe 电解法)F. 羧酸银盐与溴/四氯化碳溶液反应→少一个碳的溴代烃(Hunsdiecker 反应)(羧酸、氧化汞、溴/四氯化碳)(2)二元酸脱羧乙二酸、丙二酸→一元酸和CO 2.丁二酸、戊二酸→环状酸酐(加热脱水)己二酸、庚二酸→环酮(脱HO 和CO ) 225. α-H 的反应—卤代(C.Hell -J.V olhard -Zelinsky )反应试剂:有α-H 的羧酸、红磷、溴或氯(PX ) 3产物:α-卤代酸6. 与有机锂试剂反应试剂:羧酸、烃基锂 产物:酮(用于酮的制备)六、羧酸的制备1. 氧化法(1)烃氧化法A. 烷烃二氧化锰、高锰酸钾氧化→混合物羧酸(碳链断裂)B. 烯烃酸性高锰酸钾氧化(碳链断裂)C. 炔烃酸性高锰酸钾氧化(碳链断裂)D. 芳烃(有α-H)酸性高锰酸钾氧化(侧链断裂)(2)伯醇或醛氧化(碳数不变)(3)甲基酮卤仿反应(制备少一个碳的羧酸)2. 腈水解反应(碳链不变)3. Grignard试剂与CO反应(增加一个碳的羧酸)2常用:伯、仲、叔卤代烷,烯丙基型卤代烃、芳基卤。
羧酸衍生物的反应活性顺序原理

羧酸衍生物的反应活性顺序原理
羧酸衍生物是指有特定羧基的有机化合物。
它们的反应活
性有着特定的顺序,按照它们反应的速度排列的话,衍生物的
顺序是由氯酸钠至醋酸。
这一顺序可以用基本原理解释。
首先,由于氯酸钠比其他羧酸衍生物的pKa值更高,因此
在溶液中的结合性较弱,当其介质中添加更高结合性的衍生物时,它们很有可能会直接与氯酸钠结合,而其他衍生物则不太
可能,因此,氯酸钠结合性最低,因此位列衍生物反应活性的
最低位置。
其次,羧酸衍生物中的pKa值越高,它们发生反应
的能力就越强。
因此,醋酸具有最高的pKa值,反应活性处于
最高级别。
此外,羧酸衍生物之间还是有反应的,由于不同衍生物具
有不同的结构,它们之间发生反应的能力也就不同,从而引起
它们的反应活性差异。
由于其中的一些反应在反应活性上会超
过另一些,因此最终导致了羧酸衍生物的反应活性顺序,从而
形成这一顺序。
综上所述,羧酸衍生物反应活性的原理在于它们之间pKa
值的差异,比如说氯酸钠的pKa值最低,而醋酸的pKa值最高,另外,它们之间各自结构的不同也会影响它们的反应活性,进
而导致可以体现出预期的结果。
如上所述,羧酸衍生物的反应
活性顺序便由此产生。
羧酸银盐和溴或碘反应

Definition and Features
• 定义:有机化合物分子中引入卤素原子(X)的反应 (即分子中形成C-X的反应)称卤化反应。 – X = F, Cl, Br, I, etc.
• 特点:引入卤原子可改变有机分子中的性质,同 时能转化成其它官能团。
• 用途:作为特定活性化合物;作官能团转化的中 间体。
和影响因素 5 芳香环的卤置换反应的卤化剂种类、反应历程和影响因素 6 醛酮羰基α-位的卤置换反应的反应历程及其影响因素 7 用于醇酚羟基的卤置换反应的卤化剂的种类、反应历程及影
响因素 8 用于羧酸羟基的卤置换反应的卤化剂的种类、特点及条件
本章主要内容
• 不饱和烃的卤加成反应 • 卤取代反应 • 卤置换反应 • 卤化反应中的重排
Chapter 1 Halogenation Reaction
卤化反应
Fluorination,Chlorination, Bromination, Iodination, etc
Email: mengge@ :8080/web/mengge
• 2. What is the features of chemical pharmaceutical industry?
• 3. How many classifications for the organic reaction for drug synthesis?
• 4. How many classis in the scope of halogenation reaction?
第一节 不饱和烃的卤加成反应
不 饱 和+ 烃
• 和卤素的加成反应 • 和次卤酸(酯)的加成反应(卤内酯化)
• 和N-卤代酰胺的加成反应
大学有机化学反应总结
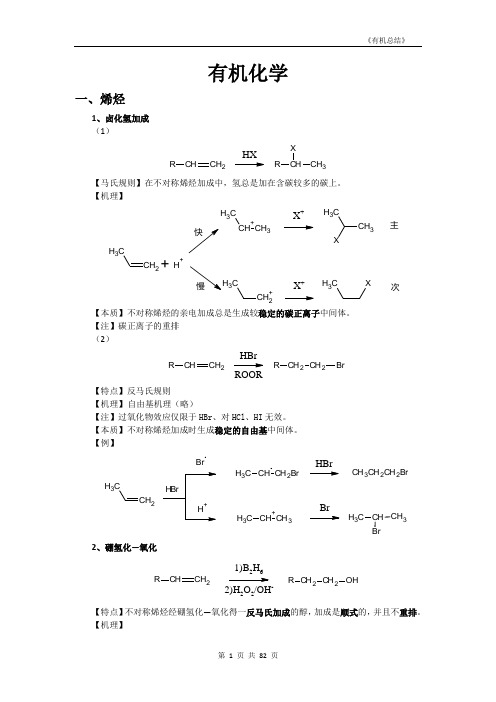
有机化学一、烯烃1、卤化氢加成 (1)CHCH 2RHXCH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3+CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】CH2CH 33H 323H 32CH CH 2CH 32CH CH=CH (CH 3CH 2CH 2)3-H 3CH 2CH 2C22CH 3CH 2B OCH 2CH 2CH 3H 3CH 2CH 2C2CH 2CH 3+OH -OHB-OC H 2CH 2CH 3CH 2CH 2CH 3H 3CH 2CH 2BOC H 2CH 2CH 3CH 2CH 2CH 3H 2CH 2CH 3HOO -B(OCH 2CH 2CH 3)3B(OCH 2CH 2CH 3)3+3NaOH 3NaOH3HOC H 2CH 2CH 33+Na 3BO 32【例】CH 31)BH 32)H 2O 2/OH -CH 3HH OH3、X 2加成C CBr /CClCC Br【机理】CCCC Br BrCBr +CC Br OH 2+-H +CC Br OH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
卤化反应(2)

3.4 醇、酚和醚的卤素置换反应3.4.1 醇的卤素置换反应醇的卤素置换反应是获得卤化物的重要方法,常用的卤化剂是氢卤酸和亚硫酰卤、磷酰卤及卤化磷等。
实际上,不论是哪种方法,不外乎是先将羟基变成更好的离去基团,然后用卤素进行亲核取代。
(1) 氢卤酸(卤化氢)作卤化剂醇与氢卤酸的反应一般为亲核取代反应。
能形成稳定碳正离子的底物可按SN1机理进行,其它反应通常为SN2机理。
醇的活性顺序为叔醇>仲醇>伯醇(SN1);氢卤酸(卤化氢)的活性顺序为HI>HBr>HCl>HF,低活性的卤化剂可加入Lewis酸催化。
叔胺也可催化这类反应。
see RU 2051889, Process for Preparing 2-Ethylhexyl Chloride-1(1993).(2) 亚硫酰卤(卤化亚砜)作卤化剂亚硫酰卤与醇反应生成卤代烷和二氧化硫与卤化氢,易分离,在醇的卤化中应用较广,如头孢哌酮钠中间体氧哌嗪甲酰氯的合成。
就氯化亚砜氯化而言,在不同的反应条件下,其反应机理不尽相同。
DMF和HMPA可催化醇与卤化亚砜的反应。
DMF可与SOCl2反应生成氯代烯铵盐:该烯铵盐可作为氯化剂实现醇的氯代。
类似地,HMPA与SOCl2的反应产物也是很好的氯化剂,其机理亦与DMF相同。
反应示例:HMPA催化的某伯醇的氯代。
有机碱,如吡啶,可以和卤化氢成盐而提高卤离子浓度,也能提高此类反应速度,该法尤其适用于对酸敏感的底物。
无取代或供电子基取代的芳醛与溴化亚砜共热,可得二溴苄。
反应物中存在的微量的溴化氢对醛羰基的加成是反应的第一步。
在无水DMF中,氯化亚砜可将芳醛转化为相应的二氯苄。
(3) 卤化磷作卤化剂三卤化磷和五卤化磷也是转化醇为卤代烷的常用试剂。
其反应活性较氢卤酸大,又较少发生重排反应。
常用的卤化磷是三氯化磷和三溴化磷,后者可由溴素与磷原位制备。
三卤化磷与醇反应可生成亚磷酸单、双和三酯,之后,卤离子对上述磷酸酯发生取代,置换掉氧亚磷酰片断,生成卤代烷。
羧基和溴反应

羧基和溴反应
1 羧基和溴的化学反应
化学反应是化学领域中最重要的一部分,它们可通过改变原子和分子之间的化学键来不断创造新的物质。
本文将讨论羧基和溴之间的化学反应。
2 什么是羧基和溴?
在学习羧基和溴的反应之前,我们需要了解它们是什么。
羧基是由碳和氧原子组成的化合物基团,通常在有机化合物中存在。
溴是一种卤素元素,具有强烈的加成反应性,常用于有机合成领域中。
3 羧基和溴的反应类型
当溴与羧基反应时,通常表现出加成反应的特性。
加成反应是一种将两个化学物质相加以形成单个产物的化学反应,其中的两种化学物质可以是元素或化合物。
4 羧基和溴的反应机理
羧基和溴的反应机理非常复杂,涉及多种反应步骤和中间体。
最初,酸性溴溶液和羧酸反应,产生溴酸和质子。
然后,一个新的亲电性溴离子与羧酸反应,同时释放出水分子,形成酰溴(RCOBr)。
酰溴是一种非常反应性的中间体,因为它既具有强烈的电子亲和力,又具有良好的离子极性。
之后,酰溴可能会与其他物质发生反应,产生不同的产物。
例如,在与胺或醇反应时,它可以生成酰胺或酯。
总之,羧基和溴之间的反
应具有重要的实际应用价值,并且为合成有机化合物提供了新的途径
和方法。
5 总结
本文描述了羧基和溴之间的反应类型、反应机理和实际应用。
这
种反应可用于产生各种不同种类的有机化合物,并且是有机合成领域
中非常常见的反应之一。
希望这篇文章能够帮助读者更好地理解羧基
和溴之间的化学反应,并且在实际的科学研究和实验中有所启发。
银催化脱羧

银催化脱羧
银催化脱羧是一种常用的有机化学反应,它利用银盐作为催化剂,使羧基(COOH)在特定条件下转化为相应的烃基(R)。
在银催化脱羧反应中,通常使用银盐(如硝酸银、氯化银等)作为催化剂,同时还需添加一种活化剂(如碘、溴等卤素元素或其化合物)。
在反应过程中,羧基首先与活化剂发生反应,形成活化态的羧基,然后该活化态的羧基与银盐发生反应,生成相应的烃基和银盐。
银催化脱羧反应具有较高的选择性,即能够将特定的羧基转化为相应的烃基,而不影响其他官能团。
此外,该反应条件温和,操作简单,因此在有机合成和药物合成等领域得到了广泛应用。
需要注意的是,银催化脱羧反应需要在特定的条件下进行,如控制温度、压力、反应时间等。
此外,对于不同的羧酸和活化剂,反应条件和结果也可能有所不同。
因此,在进行银催化脱羧反应时,需要仔细选择合适的催化剂、活化剂和反应条件,以确保获得最佳的转化率和选择性。
每天一个人名反应--Hunsdiecker反应

每天一个人名反应--Hunsdiecker反应
1939年化学家H.Hunsdiecker报道,干燥的脂肪酸银盐与单质溴反应可以得到相应的少一个碳的溴代烷。
这一脱羧溴代反应被称为Hunsdiecker反应。
除了单质溴,氯气和单质碘也能进行反应,生成相应的氯代烷和碘代烷。
羧酸盐不局限于银盐,更稳定和更易结晶的一价铊盐和汞盐还有利于产率的提高。
除了脂肪酸外,带有拉电子基团的芳香酸也可以作为反应底物。
反应机理
首先羧酸负离子进攻单质溴,形成O-Br键,由于该O-Br键键能比较低,很容易发生均裂,产生的酰氧自由基脱除一分子CO2,生成的烷基自由基再同溴自由基偶联或者进攻单质溴,则得产物溴代烷。
反应实例
参考文献
1. Borodine, B., Ann., 1861, 119, 121.
2. Hunsdiecker, H.; Hunsdiecker, C. Ber. 1942, 75, 291-297.
3. Sheldon, R. A.; Kochi, J. K. Org. React. 1972, 19, 326-421. (Review).
4. Barton, D. H. R.; Crich, D.; Motherwell, W. B. Tetrahedron Lett. 1983, 24, 4979-4982.
5. Das, J. P.; Roy, S. J. Org. Chem. 2002, 67, 7861-7864.
6. Ye, C.; Shreeve, J. M. J. Org. Chem. 2004, 69, 8561-8563.。
碘仿反应产物

碘仿反应产物碘仿反应是一种重要的有机合成反应,其产物具有广泛的应用领域。
碘仿反应的主要产物是碘代烷烃化合物,其结构特点使得它们可以用于医药、农药、染料和化学品等领域。
碘仿反应的产物主要有三种类型:碘代烷烃、碘代醇和碘代酸。
首先是碘代烷烃。
碘仿反应中,当碘醇与碱反应时,会生成碘代烷烃。
碘代烷烃是一类具有碘原子取代的烷烃化合物,其化学性质较为稳定。
碘代烷烃在医药领域有广泛的应用,例如碘仿是一种常用的外科消毒剂,具有抗菌和止血的作用。
其次是碘代醇。
碘仿反应中,当碘醇与醇反应时,会生成碘代醇。
碘代醇是一类具有碘原子取代的醇化合物,其具有一定的生物活性。
碘代醇在医药和农药领域有一定的应用,例如碘甲醇是一种常用的消毒剂,可以用于皮肤消毒和伤口消毒。
最后是碘代酸。
碘仿反应中,当碘醇与酸反应时,会生成碘代酸。
碘代酸是一类具有碘原子取代的羧酸化合物,其具有较强的酸性。
碘代酸在化学品和染料领域有着广泛的应用,例如碘乙酸是一种常用的染料中间体,可以用于染料的合成和着色。
除了以上三种主要的产物类型,碘仿反应还可能生成其他一些次要产物,如碘代醚和碘代酰胺等。
这些产物在特定的应用领域也有一定的价值和应用。
需要注意的是,碘仿反应中产物的种类和产率受到反应物的选择、反应条件的控制、反应时间的掌握等因素的影响。
合理选择反应物和优化反应条件可以提高产物的纯度和产率,从而提高产品的质量和应用价值。
碘仿反应的产物主要包括碘代烷烃、碘代醇和碘代酸等,这些产物在医药、农药、染料和化学品等领域具有广泛的应用。
通过合理选择反应物和优化反应条件,可以提高产物的质量和产率,进一步拓展碘仿反应的应用前景。
羧基盐的反应

羧基盐的反应
盐是我们生活中常见的化合物,它们有着丰富的性质和反应方式。
而羧基盐作为一类特殊的盐,也有着独特的反应和应用。
一、羧基盐的生成
羧基盐是由羧酸和碱反应生成的。
羧酸的通用结构为R-COOH,其中R代表有机基团。
当羧酸和碱反应时,羧基中的氢离子(H+)会被碱中的氢氧根离子(OH-)取代,生成羧基盐。
例如,乙酸(CH3COOH)和氢氧化钠(NaOH)反应,生成乙酸钠(CH3COONa)和水(H2O):
CH3COOH + NaOH → CH3COONa + H2O
二、羧基盐的性质
羧基盐既具有羧酸的特性,也具有盐的性质。
羧基盐是固体结晶,常温下多为白色结晶体。
它们在水中溶解度较高,可以与水形成稳定的溶液。
羧基盐还具有一定的酸性,能够与碱反应生成盐和水。
同时,羧基盐还可以与金属离子发生置换反应,生成相应的金属盐。
三、羧基盐的应用
羧基盐具有广泛的应用领域。
其中,乙酸盐是一种常见的羧基盐,被广泛应用于食品、制药、化妆品等行业。
乙酸钠作为食品酸化剂和防腐剂,在食品加工中起着重要作用。
羧基盐还可以用作染料、颜料、表面活性剂等化工产品的原料。
它们在化学合成中也扮演着重要的角色。
总结:
羧基盐是由羧酸和碱反应生成的化合物,具有盐和酸的特性。
它们在生活和工业中有着广泛的应用,如食品、化妆品、染料等领域。
羧基盐的反应性质和应用使其成为化学领域中不可或缺的重要物质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Examples
H
H
CC
Ph
CO2H
。Br2/CHCl3 0 r.t.20min
Br H H
O Ph + O
Br CH CH Ph
Br CO2H
69%
少量
三、不饱和烃和次卤酸(酯),N-卤代酰
胺的反应
机理 分析
R1
R3
CC
R2
R4
X-OH
HClO
HBrO
Cl--OH Br--OH
R1 OH R3
Br CC
R2
H
H
Me OS
Me
Br R2 H
H2O
R1 C C
H
O SMe2
-消除
BrR2 R1 C C H
OH H
Br R2
R1 C
C O
(在干燥D MSO中) H
Examples:
OAc
AcOCH2 AcOCH2
NBS/DMSO
O
r.t
(90%)
OgluAc4
OAc Br
O
O
OgluAc4
Products:
CH3 Br H H Br
CH3
CH3 H Br Br H
CH3
立 体 化 学 问 题
H Cl Cl2
H
H
ClCl
+
H Cl
与
Cl2加
成
产
物
同
向
加
成
,因
为 Cl不 H
易形 Br
成
桥
环
Br
H
H Br Br
H
Br2 +
Examples:
Me
HO
Br2 HO
Cl2 HO
Me
Br Br
Me
C
R4
R2
C
反向
H R3
反马氏规则
光
HBr
H + Br
R1 C
R4 Nu
R2
C
同向
R3 H
R
H
C C + Br
Chapter 1 Halogenation Reaction
卤化反应
Fluorination,Chlorination, Bromination, Iodination, etc
Email: mengge@ :8080/web/mengge
按照反应机理的类型
• 亲电加成 • 亲电取代 • 亲核取代 • 自由基反应
学习重点
1 不饱和烃与卤素加成反应的历程及其立体化学
2 次卤酸(酯)和N-卤代酰胺等化合物与不饱和烃反应的历程、
影响因素及其立体化学 3 卤化烃对不饱和烃加成反应的历程及影响因素 4 烯丙位、苄位的卤置换反应所用的卤化剂的种类、反应历程
OH
C
RC NH X
C
Nu
CC X
Nu CC
X
Nu=H2O, ROH, DMSO, DMF
Example:
Ph
CH
CH2
NBS/H2O 25 , 35min
Ph CH CH2Br
OH
82%
Special example: Dalton Reaction
R1 C C R2 NBS/DMSO
H
H
R1
OH H
NH
N
氯霉素
诺 氟 沙 星 C2H5
• 制备具有不同生理活性的含卤素的有机药物
O F
HN
5-氟尿嘧啶
ON H
Reviews
• 1. What is chemical drug? What is the classifications according to the its recourse?
• 酸性氧化剂,应用领域涉及面广:
• 消毒剂、石油、纺织印染助剂,游泳池和温泉等 水体的消毒处理、假牙的清洁、线路板的蚀刻、 纸浆和织物的低温漂白和脱浆、羊毛防缩处理、 贵重金属提炼、兽药消毒杀菌剂,碗盘清洗剂, 氧化淀粉,衣物的漂白剂、养殖业的供养剂。
• 有机物聚合反应的引发剂。
• 沉铜,化学镀,直接电镀,压膜和涂覆光阻剂的 板面预处理,阻焊绿油之前的板面预处理,内层 板面的预处理。
四、卤化氢对不饱和烃的加成反应
1 HX对烯烃的加成
R1
R4 HX
CC
R2
R3
H R1
C
R2
X
R4
C
+
R3
Cl
X R1
C
R2
H R4
C
R3
+ HCl
HCl CH3-CH=CH2
Cl CH2-CHCH3 只 有 HBr有反 马 氏 规 则
Ph-CH=CH2
HBr
Ph--C-CH3
Br
HBr
Ph-CH2CH2Br 反 马 氏 规 则
H XC
CH3 +
H XC
CH3
CX
X Ph H
CX H Ph
Cl 65%
35%
Br 88%
12%
Examples
X Br2/CCl4 X
H 2~5 H CH3
X=H X=OCH3
Br H C C CH3 + X H Br
Br CH3 CCH H Br
88% 63%
12% 37%
Examples
Example: Intermediates
• 如:制备药物中间体糖皮质激素醋酸可的松
CH3
CO OH
CH2I CO
OH
O CH2OCCH3
CO OH
I2/CaO
CH3COOK
CH3OH/CaCl2
DMF
O
O
O
Example: Medicines
H NHCOCHCl2
O
F
COOH
H2N
CC
CH2OH
2、卤素对炔的加成
Products: 反式二卤烯烃
ph C
C-CH3
Br2 LiBr
Cl2
HC C-CH2OH
I2
Br
ph C
C-CH3
E
Br
ph
Cl
C
C
E
Cl
CH3
I C
H
CH2OH
C
I
E
Examples
Ph C C CH3 HBOr2A/Lci/B25r。
Ph C
Br C
Ph +C
C CH3
Cl Cl
Examples
H3C
C
H
H AcOH/Cl2
C
C2H5 LiCl
Cl H3C
C H
Cl
Cl
+ H
C
H3C C
C2H5
H
OAc
H C
C2H5
I2/KIO3
CH3-CH=CH2
CH3-CH-CH2I 93%
OH
I2/AcOAg
H OAc
I
H
与卤素的加成
Examples
Ph
H
CC
H
CH3
X2/CCl4 0~5
HO
HO H
Me C16H30 Br2/AcOH
AcONa/Et2O
20-25
Me Br
Me C16H30 Br
HO
Br
H
Br
(84~85%)
Examples
H3C C
H
C
C2H5 H
Cl2/C2H5。3CO2H
CH3CH Cl
Cl CH
C2H5
52%*
添加 LiCl
69%*
OCOCH3
Cl
+ CH3CH CH C2H5 + CH3CH CH C2H5
Cl
33%*
OCOCH3
13%*
21%*
8%*
Examples
I2/AcOAg/Et2O
H
OAc I H
80%
Oxone + Sodium chloride
延伸知识: DPTBE
补充扩展:过一硫酸氢钾(复合盐)
Potassium monopersulfate
compound (PMPS,KMPS)
Br
CH3 Br
Br
98%*
0.2%*
二、不饱和酸的卤内酯化反应
I2/KI/NaHCO3
I
O
O
CH2COOH
H
H
CC
Ph
Br2
第二步 C OH
O
Br Ph
O
O
卤内酯化反应 Examples
I2/KI/N2O/r.t.4h
O
C
H2C
O
H
I
I HH
O
O
H
88%
和次卤酸(酯)的加成反应的改进
HClO水 中
Ar-CH CH2
收率较低
C OCl (有 机 溶 剂 中 )
AcOH
Ar-CH-CH2 70%
OH Cl
OH -
Ar-CH - CH2
+
Cl
EtO O
t-BuOCl/ROH
EtO O
Cl Cl ROH
OR
EtO O
不饱和炔烃的相关加成
次卤酸及其酯为卤化剂的反应
• 5. What is the main usages of halogenation reaction?
