XXX程序文件
采购管理流程控制程序文件

采购管理流程控制程序文件The document was finally revised on 2021封面页码:第1页,共5页深圳市XXXX有限公司XXX Storage & Multimedia Technology Co., Ltd.文件编号:XX-XX-XXX文件名称:采购管理控制程序版本:A/0生效日期:20XX年XX月XX日发行状态:(盖受控文件章)批准:___________________ 审核:___________________制定:__ XXX______封面页码:第2页,共5页1、目的为确保对影响采购质量的关键环节实施控制,保证采购产品的质量、性能、交期和服务等各方面,符合顾客、法律法规、职业健康安全和环境的要求,并满足公司生产和管理的需要,特制定本程序。
2、范围适用于公司在研发生产和生产准备过程中的所有产品或服务的采购控制。
3、职责负责公司所有产品(办公用品、大型机器等除外)所需求物料的采购。
总经理负责领导公司的采购管理,采购经理协助总经理负责领导公司的采购管理。
4、管理内容与要求采购的申请:4.1.1工程项目(打样)采购的申请由工程项目负责人填写《工程项目打样采购申请表》提出申请,项目主管提出初审意见,提交PMC,PMC提出审核意见,报公司领导批准后备案并进行采购管理工作。
需求物料采购申请4.2.1常用物料采购申请(需有安全库存的物料)由PMC部门填写《物料需求计划表》,经PMC部门主管签字审核后,下达给采购部,采购部按需求适时采购。
4.2.2订单物料采购申请由PMC部门依据订单需求情况,结合实际库存物料,作出计划后,填写《物料需求计划表》提出申请,经PMC负责人审核后,下达给采购部,采购部按需求适时采购,并进行采购管理。
生产性低值易耗品的采购申请4.3.1由生产部门填写《物料采购申请单》提出申请,部门主管提出初审意见,经PMC部门主管审核后,下达给采购部纳入采购计划,适时进行采购。
xxxxxx质量检测中心程序文件

文档从互联网中收集,已重新修正排版,word 格式支持编辑,如有帮助欢迎下载支持。
程序文件(第X 版)200Y-MM-DD 发布 200Y-MM-DD 实施分发号 : 受控状态: xxxxxx 质量检测中心文档从互联网中收集,已重新修正排版,word格式支持编辑,如有帮助欢迎下载支持。
目录 3HP0001-2001主任令 3HP0002-2001文件控制程序 3HP0301-2001检测用计算机、软件及网络控制程序 3HP0302-2001要求、标书和合同的评审程序 3HP0401-2001新项目评审程序 3HP0402-2001检测的分包程序 3HP0501-2001服务和供应品的采购程序 3HP0601-2001 服务客户程序 3HP0701-2001抱怨处理程序 3HP0801-2001不符合的检测工作控制程序 3HP0901-2001改进控制程序 3HP1101-2001记录的控制程序 3HP1201-2001内部审核程序 3HP1301-2001管理评审程序 3HP1401-2001人员培训程序 3HP1601-2001环境控制程序 3HP1701-2001检测方法及方法的确认程序 3HP1801-2001检测程序 3HP1802-2001测量不确定度评定与表述指南 3HP1803-2001设备管理程序 3HP1901-2001量值溯源程序 3HP2001-2001运行检查程序 3HP2002-2001抽样程序 3HP2101-2001样品管理程序 3HP2201-2001检测结果质量保证程序 3HP2301-2001结果报告程序 3HP2401-2001主任令文档从互联网中收集,已重新修正排版,word格式支持编辑,如有帮助欢迎下载支持。
本中心依据《质量手册》(第X版)重新编制了《程序文件》(第X版),经主任办公会批准,现予以颁布。
本手册自二O O一年九月一日起实施,以替代《质量体系程序文件》(第x版)。
程序文件封面标准模板

程序文件文件控制程序编号:XX-24-01编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件质量记录控制程序编号:XX-24-02编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件管理评审控制程序编号:XX-25-01编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件质量成本控制程序编号:XX-25-02编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件经营计划管理程序编号:XX-25-03编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件人力资源管理程序编号:XX-26-01编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件设备设施管理程序编号:XX-26-02编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件产品质量先期策划控制程序编号:XX-27-01编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件工程更改控制程序编号:XX-27-02编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件顾客需求管理程序编号:XX-27-03编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件服务控制程序编号:XX-27-04编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件产品和过程批准程序编号:XX-27-05编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件采购控制程序编号:XX-27-06编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件供应商管理程序编号:XX-27-07编制:审核:批准:版本号:受控状态:受控号:2012-07-28发布2012-08-01实施程序文件生产过程控制程序编号:XX-27-08编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件工装管理程序编号:XX-27-09编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件产品标识和可追溯性控制程序编号:XX-27-10编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件顾客财产管理程序编号:XX-27-11编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件产品防护和交付控制程序编号:XX-27-12编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件监视和测量装置控制程序编号:XX-27-13编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件内部质量体系审核程序编号:XX-28-01编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件内部过程审核程序编号:XX-28-02编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件内部产品审核程序编号:XX-28-03编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件检验和试验控制程序编号:XX-28-04编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件不合格品控制程序编号:XX-28-05编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件持续改进控制程序编号:XX-28-06编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施程序文件纠正和预防措施控制程序编号:XX-28-07编制:审核:批准:版本号:受控状态:受控号:XXXX-02-28发布XXXX-03-01实施。
程序文件(封面、签署页、目次)

XXX公司检测中心编号:CX01~30-2018受控状态:程序文件Procedure Documentation(V2.0版)[主要依据CNAS-CL01:2018编制]批准(签字):审核(签字):编制(签字):2018-08-01发布2018-09-01实施XXX股份有限公司批准《程序文件》签署页根据CNAS-CL01:2018《检测和校准实验室能力认可准则》(ISO/IEC 17025:2017)和实验室《质量手册》要求,为保证实验室正常开展检测、校准工作,特组织编制实验室V2.0版的CX01~30-2018《程序文件》,现予发布,本《程序文件》自2018年09月01日起开始实施。
质量主管(签字):二0一八年八月一日目次《程序文件》签署页1 CX01-2018 保证公正性的控制程序‥‥‥‥‥‥‥‥‥‥1-12 CX02-2018 保护秘密的控制程序‥‥‥‥‥‥‥‥‥‥‥2-13 CX03-2018 各部门各类人员职责与权限程序‥‥‥‥‥‥3-14 CX04-2018 内务管理程序‥‥‥‥‥‥‥‥‥‥‥‥‥‥4-15 CX05-2018 现场检测校准工作的控制程序‥‥‥‥‥‥‥5-16 CX06-2018 人力资源管理的控制程序‥‥‥‥‥‥‥‥‥6-17 CX07-2018 设施和环境条件的控制程序‥‥‥‥‥‥‥‥7-18 CX08-2018 测量设备使用和维护的管理程序‥‥‥‥‥‥8-19 CX09-2018 测量标准装置的管理程序‥‥‥‥‥‥‥‥‥9-110 CX10-2018 计量溯源性的控制程序‥‥‥‥‥‥‥‥‥10-111 CX11-2018 外部产品和服务的控制程序‥‥‥‥‥‥‥11-112 CX12-2018 要求、标书和合同评审的管理程序‥‥‥‥12-113 CX13-2018 检测和校准方法的验证和确认程序‥‥‥‥13-114 CX14-2018 开展新项目的评审程序‥‥‥‥‥‥‥‥‥14-115 CX15-2018 检测和校准物品处置的管理程序‥‥‥‥‥15-116 CX16-2018 记录的控制程序‥‥‥‥‥‥‥‥‥‥‥‥16-117 CX17-2018 测量不确定度和CMC评定的控制程序‥‥‥17-118 CX18-2018 检测和校准结果有效性的控制程序‥‥‥‥18-119 CX19-2018 证书和报告的编制和管理程序‥‥‥‥‥‥19-120 CX20-2018 印章和标识管理的控制程序‥‥‥‥‥‥‥20-121 CX21-2018 投诉的处理程序‥‥‥‥‥‥‥‥‥‥‥‥21-122 CX22-2018 不符合工作的控制程序‥‥‥‥‥‥‥‥‥22-123 CX23-2018 数据控制与信息管理程序‥‥‥‥‥‥‥‥23-124 CX24-2018 文件的控制程序‥‥‥‥‥‥‥‥‥‥‥‥24-125 CX25-2018 应对风险和机遇的控制程序‥‥‥‥‥‥‥25-126 CX26-2018 预防措施的控制程序‥‥‥‥‥‥‥‥‥‥26-127 CX27-2018 改进的控制程序‥‥‥‥‥‥‥‥‥‥‥‥27-128 CX28-2018 纠正措施的控制程序‥‥‥‥‥‥‥‥‥‥28-129 CX29-2018 内部审核的控制程序‥‥‥‥‥‥‥‥‥‥29-130 CX30-2018 管理评审的控制程序‥‥‥‥‥‥‥‥‥‥30-1。
航天XXX公司质量体系全套程序文件、记录表格DOC_101页.doc
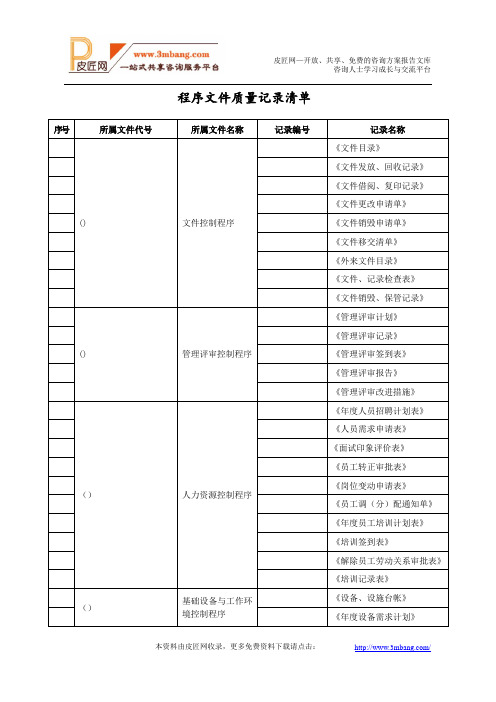
程序文件质量记录清单
文件目录
本资料由皮匠网收录,更多免费资料下载请点击:/
编制:日期:
文件发放、回收记录
本资料由皮匠网收录,更多免费资料下载请点击:/
文件借阅、复制记录
本资料由皮匠网收录,更多免费资料下载请点击:/
本资料由皮匠网收录,更多免费资料下载请点击:/
文件更改申请单
文件销毁申请单
皮匠网—开放、共享、免费的咨询方案报告文库
咨询人士学习成长与交流平台
皮匠网—开放、共享、免费的咨询方案报告文库
咨询人士学习成长与交流平台文件移交清单
皮匠网—开放、共享、免费的咨询方案报告文库
咨询人士学习成长与交流平台
外来文件目录
本资料由皮匠网收录,更多免费资料下载请点击:/
登记人:日期:本资料由皮匠网收录,更多免费资料下载请点击:/
文件、记录检查表
皮匠网—开放、共享、免费的咨询方案报告文库
咨询人士学习成长与交流平台
文件销毁、保存记录
本资料由皮匠网收录,更多免费资料下载请点击:/
本资料由皮匠网收录,更多免费资料下载请点击:/
管理评审计划
管理评审记录
记录人:日期:
管理评审签到表
四川航XX鑫玄武岩实业有限公司质量体系
管理评审报告
单位(盖章):
最高管理者: 管理者代表: 评审时间:
管理评审报告
一、评审目的:
二、评审时间:
三、评审范围:
四、评审内容:
管理评审改进措施。
程序文件范例

文件编号:02-HR-0000-A0 文件版本:A/0受控编号:受控印章:编制:审核:批准:2013年1月1日发布实施目录序号文件编号文件名称01 XX423 文件控制程序02 XX424 记录控制程序03 XX560 管理评审控制程序04 XX620 人力资源管理控制程序05 XX630/640 基础设施和工作环境控制程序06 XX720 与客户有关过程控制程序07 XX730 设计和开发控制程序08 XX740 采购控制程序09 XX751 生产提供控制程序10 XX755 产品防护控制程序11 XX760 监视和测量设备控制程序12XX821 客户满意度评定控制程序13XX822 内审控制程序14XX824-1 来料检验及定期确认检验控制程序15XX824-2 生产过程和过程控制16XX824-3 例行检验和确认检验控制程序17 XX830 不合格品控制程序18 XX850 改进控制程序19 XX-CP001 产品变更控制程序1.目的与适用范围对质量管理体系文件进行控制,确保相关部门及时得到并使用有效版本。
适用于本公司与质量管理体系有关的文件和资料的控制(包括外部提供的有关文件)。
2.职责2.1行政部负责公司文件总归口管理,负责组织对质量管理体系文件的定期评审。
2.2工程部负责技术文件归口管理。
2.3品管部负责检验文件归口管理。
2.4各部门负责相关文件的使用管理。
3.工作程序3.1文件的分类与编号3.1.1本公司受控的质量管理体系文件分类及编号为:a. 质量手册(包括质量方针、目标)编号为:QM-□□□□(为年份号)b. 程序文件;编号为:XX□□□(为标准要素代号)c. 技术性文件:操作规程编号为:MSP-□□□(为流水号);检验文件编号为:QCI-□□□(为流水号);工序指导书编号为:MEI-□□□(为流水号);d. 管理性文件(如管理制度、管理办法等)DOM-□□□:(为流水号);e. 记录WXYD-X□□□:(X为部门标号□为流水号);f. 外来文件WL-□□□(□□□为流水号);3.1.2:文件的版本采用A.0、A.1……A9、B.0、B.1……B.9的方式标识,如文件修改一次,其修改状态相应按0~9标识,当文件修改第5次或文件需大幅度更改时,文件需换版。
XXX程序文件格式模版

1.目的规范公司对人力资源合理配置、招募、管理等相关管理过程,有效的做好选才、育才、用才、留才之人力资源管理。
确保人力资源满足质量管理体系的要求。
2.适用范围适用于公司所有员工。
3.引用文件GB/T 18305-2010 ISO/TS 16949:2009 6.2 文件控制4.术语和定义4.1离职:包括公司辞退、公司开除、员工辞职、员工退休、员工自离五种类型。
4.2转岗:公司对考核评估不合格员工进行的岗位异动。
4.3调岗:员工对内部招聘的岗位异动,或公司对内部提拔员工的岗位异动。
5.职责5.1人力资源部:负责对人员的定编、定岗、招募、任用与规划管理工作,同时对各部门负责人的任职资格进行鉴定。
5.2各部门:负责用工申请,员工考核、评估。
6.流程图7.工作程序和内容7.1 人力资源规划7.1.1公司各部门经理根据本部门工作目标及本部门的岗位需求,于每年12月中旬,拟定部门下一年度《年度人力需求计划表》,报人力资源部汇总。
7.1.2人力资源部根据本公司发展计划、人力编制情况及各部门人力需求计划汇总,对现有人员的改进需求,能力需求等人力状况进行分析,编制《年度人力需求计划表》,《年度公司岗位编制表》,呈总经理核准。
7.2招聘实施7.2.1部门在编制内招聘,或职位出现空缺时,由各部门负责人填写《招聘申请单》,人力资源部按《岗位职务说明书》上的任职资格要求进行招聘。
招聘方式有外部招聘、内部招聘、内部提拔晋升三种类型。
7.2.2内部招聘:7.2.2.1人力资源部对需求岗位进行内部竞聘可行性进行分析,获得肯定后,发布《内部空缺职位竞聘公告》。
7.2.2.2公司里所有试用期满的人员,可参加内部竞聘。
参加工程师或组长(含)级以上岗位的竞聘,需经总经理批准。
7.2.2.3员工参加内部竞聘,到人力资源部填写《员工信息登记表》。
7.2.2.4人力资源部对竞聘人员依据《岗位工作说明书》要求进行资格审查,当应聘人员的岗位要求条件无法全部满足要求,而在某些方面具备较强能力时,可适当将某些条件如年龄、学历等要求经与用人部门面试审查确定。
检验科性能验证程序文件

检验科性能验证程序文件XXX人民医院检验科程序文件主题内容文件编号:JYK-02-CXWJ版本/修订号:A/0生效日期:性能验证性能验证1目的验证检测试剂在仪器上的性能指标。
2适用范围适用于检验科检验项目试剂的性能指标验证。
3职责3.1科主任:负责审批性能验证计划。
3.2技术负责人3.2.1负责制定性能验证方案和计划。
3.2.2负责组织性能验证的实施。
3.2.3负责定期对科室性能验证数据的统计、分析和总结。
3.2.4负责组织对上述活动的可行性和有效性评审。
3.3各专业组技术管理员3.3.1负责组织本组人员完成本组性能验证的验证工作。
3.3.2负责对本组性能验证数据的统计、分析和总结工作。
3.4检验人员3.4.1负责协助科室技术负责人和本组技术管理员完成本组的性能验证工作。
3.4.2负责完成本组性能验证工作中应承担的检验工作。
3.4.3卖力认真填写本组机能验证的检修记录。
4内容4.1生化生化室项目需要验证的参数包括批内精密度,批间精密度、正确度、线性范围、参考区间、可报告区间等,适用时,还要考虑分析灵敏度(仅对那些在接近的低值有临床意义的项目有必要进行确定,必要时,可引用说明书中给出的低值)和干扰试验。
4.1.1精密度4.1.1.1标本准备及要求可采用新鲜或冻存的样本。
当样本中待测物不稳定或样本不易得到时,也可考虑使用基质与实际待检样本相似的样本,如质控品。
应至少评估2个浓度水平样本的不精密度。
当2个浓度水平样本的不精密度有显著差异时,建议增加为3个浓度水平。
所选样本的被测物水平应在测量区间内,适宜时,至少有1个样本的被测物水平在医学决定水平左右。
注1:通常较高值样本的不精密度较小,较低值样本的不精密度偏大。
对低值有临床意义的检测项目,宜评判有判断代价的低程度样本的不精密度。
注2:如检测结果没有明确的医学决定水平,可在参考区间上限左右选1个浓度,再根据检验项目的特点在测量区间内选择另一个浓度。
XXX群众医院检修科程序文件主题内容文件编号:JYK-02-CXWJ版本/修订号:A/0见效日期:性能验证注3:如与厂商或文献报导的不精密度比较,所选样本水平宜与被比较的样本水平接近。
程序文件-人员管理程序

程序文件-人员管理程序XXX程序文件人员管理程序1目的文件编号:JY-QP-04-2017版次:第1版,第次修订页码:第1页,共4页采取有效的措施和程序,管理与检测任务相关的所有人员配备、能力确认等环节,保证人员素质、经历、技术和管理水平满足检测任务需要,制定本程序。
2范围适用于进入本单位场所的所有内外部人员活动管理的控制。
3职责3.1最高管理者负责人力资源的配备,任命技术负责人、质量负责人、资源负责人和提名授权签字人,并赋予其应有的权利和资源;任命(或授权任命)其他关键岗位人员。
3.2技术负责人组织,各部门负责人对本部门技术人员进行能力确认等。
3.3综合办公室负责人员技术档案的建立和管理。
4程序4.1人员招聘4.1.1在年度管理评审中或日常的内部沟通活动中,提出人力资源的引入要求。
4.1.2根据岗位职责要求通过招聘或内部升迁等方式引入满足需求的人员。
4.1.3最高管理者批准招聘、升迁、调入人员的资格条件。
4.2上岗前培训4.2.1培训内容包括法律、法规、管理体系文件、国家标准、检验检测实际和技术及科室半年岗位带培(见)等,质量监督员或科室负责人监督其从事的质量活动,经考核合格后领取上岗证。
调入员工如具有资质认定实验室一年以上工作经验,由质量负责人批准,进修与岗位带培三个月,并考核合格后发给上岗证。
只要持证上岗的人员,才能独立从事检验工作。
4.2.2最高管理者或其授权人员(质量负责人和技术负责人)分别负责对从事抽样、检验检测、签发报告、以及操作设备等工作的人员按要求根据相应的教育、培训、经验和可证明的技能进行资格确认,经考核合格颁发上岗证。
4.3人员基本要求本公司根据检测任务的技术要乞降工作量配备管理和技术人员,人员数量和能力均应满足请求,所有从事样品收罗、现场检测、样品制备、样品前处理、样品分析测试和数据XXX程序文件人员管理程序文件编号:JY-QP-04-2017版次:第1版,第次修订页码:第2页,共4页处理等检测人员必须持证上岗,与检测活动相关人员的能力均应获得确认。
社会责任程序文件

XXX工艺品有限公司社会责任程序文件编制:文件编制小组审批:受控编号:2.02020年1月2日发布 2020年1月2日实施程序文件目录序号文件名称页码1 法律法规收集和更新程序———————————————————————— 32 童工及未成年工控制程序————————————————————————4-53 教育训练控制程序———————————————————————————6-74 强迫劳动管理程序———————————————————————————85 健康与安全控制程序——————————————————————————9-116 基础设施及设备控制程序————————————————————————12-147 应急管理控制程序———————————————————————————15-168 工人代表及集体交涉管理程序——————————————————————179 歧视惩罚性措施管理程序————————————————————————1810 工资与补偿控制程序——————————————————————————19-2011 人力资源控制程序———————————————————————————21-2412 管理评审程序—————————————————————————————25-2613 社会责任管理体系审核程序————————————————————————27-2814 供应商评审及选择程序————————————————————————- 29-3015 纠正及预防措施控制程序————————————————————————31-3216 对外沟通管理程序———————————————————————————33一、法律法规收集和更新程序1、目的为了识别、获取、传达并更新适用于公司社会责任有关的法律、法规、标准及其它要求,特制定本程序。
2、范围本程序适用于公司识别、获取、传达并更新适用于公司的社会责任有关的法律、法规、标准及其它要求,以及评审确认其适用性。
工厂程序文件

XXXXXX有限公司质量管理体系程序文件Quality Mangement System Program Files版次:A/0制订:程序编制组审核:XXXX批准:XXXX受控:制订日期:2017年12月13日执行日期:2017年12月13日未经许可不得翻印程序文件目录文件更改一览表1目的使质量管理体系有关的文件和资料处于受控状态,防止丢失、误传,确保各场所使用的均为有效的文件和资料。
2适用范围适用于公司所有质量管理体系文件和资料的控制和管理。
3职责3.1行政部负责公司管理类文件和资料的编制、收发、编目、报审、用印、立卷、归档保存等的管理。
3.2生产部负责公司技术类文件和资料的归口管理。
3.3管理者代表负责组织文件编写小组编写质量管理手册、程序文件,并审核,报总经理批准。
3.4各职能部门负责本部门内部文件和资料的编写和修订,报管理者代表审批。
4工作程序4.1文件和资料的分类:1) 管理类文件:质量手册、程序文件、规章制度、作业指导文件。
2) 技术生产类文件:工艺技术/图纸/说明书/引用标准。
3)外来文件:国家、地区颁布的法律法规、规范、标准等文件。
4.1.1文件和资料分为受控和非受控两种。
受控文件为用于体系运行的所有相关文件,受控体系文件和资料加盖“受控”章进行管理,并进行跟踪控制;非受控文件为公司用于对外宣传,私人使用的参考文件,非受控文件和资料可进行登记,不跟踪控制。
4.1.2文件标识:内部体系文件以文件代号、版本号及“受控”印章进行标识,;国家标准、行业标准等质量管理体系所需的外来文件以原标准号标识;作为资料保留的作废文件,需加盖“保留资料”印章。
4.1.3公司行政部应编制《受控文件清单》,以备查公司的所有受控文件和最新的修订次数。
4.2文件的编写和审批4.2.1管理类文件由管理者代表组织文件编写小组进行集体编写,并由管理者代表组织会审,总经理批准后执行,包括以后新增的文件编写。
4.2.2技术类文件由生产部经理组织相关人员编写,经管理者代表批准执行。
XXX有限公司 WCA 社会责任程序文件-工作时间

[键入文字]XXX有限公司WCA 社会责任程序文件-工作时间管理程序本公司遵守适用法律,按《中华人民共和国劳动法》和《中华人民共和国劳动合同法》关于8小时,每周正常工作时间40小时。
保证员工每7天周期中至少休息一天;本公司如因生产需要,在保障劳动者身体健康及自愿每周工作时间最多不超过60小时。
一.发生下列情形之一,加班时间不受本程序限制。
1.发生自然灾害、事故或者因其它原因威胁劳动者生命健康和财产安全需紧急处理的;2.生产设备、交通运输路线、公共设施发生故障影响生产和公众利益必须及时抢修的;3.法律、行政法规定的其它情形。
二.本公司暂无有毒有害作业或繁重体力劳动,以后如有,每日正常工作时间相应缩短。
本公司若因生产情况或生产特点不能实行规定,经劳动行政部门批准可以实行综本公司依法安排员工享受下列休假待遇,假期内工资照发。
1法定节假日(11天)2元旦放假1天(1月1日);[键入文字]3春节放假3天(农历正月初一、初二、初三);4清明节放假1天(农历清明当日);5劳动节放假1天(5月1日);6端午节放假1天(农历端午当日);7中秋节放假1天(农历中秋当日);8国庆节放假3天(10月1日、10月2日、10月3日);9婚丧假(结婚或配偶、直系亲属死亡,婚丧假为3天)10到达法定年龄(男22周岁,女20周岁)可享受婚假3天;11员工的直系亲属(父母、配偶、子女)死亡给予3天丧假假期。
三.产假,女员工生育可享受产假1正常生育,女性员工可享受178天的产假(其中,符合法律、法规规定生育子女80天的奖励假;产前可以休15天),难产增加15天;2产假难产的,增加产假15天;生育多胞胎的,每多生育1个婴儿,增加产假15 天;[键入文字]3自然流产,女性员工怀孕未满4个月流产的,可享受假期15天,怀孕满4个月42天;工资照发;符合法律、法规规定生育子女的夫妻,男方享受15天的陪产假。
四.哺乳假有不满1周岁婴儿的女职工,其所在单位应当在每班劳动时间内给予其两次哺乳(含人)时间,每次30分钟。
45001管理体系手册和程序文件

xxx管理体系手册和程序文件是公司组织实施和维持xxx职业健康安全管理的重要文件,它包含了组织的健康安全管理体系的构建和运行所需的一切信息。
它是组织在ISO xxx认证中必备的重要文件,同时也是组织内部管理和持续改进的重要依据。
1. xxx管理体系手册的内容xxx管理体系手册是组织健康安全管理体系的核心文件,它包含了组织的健康安全管理政策、目标和愿景,以及管理体系的运行要求和相关流程。
具体来说,手册应包括以下内容:- 组织的健康安全管理政策和目标,以及对xxx标准的遵循承诺; - 组织结构和责任,包括组织内部的管理层次、职责和权限;- 组织各项健康安全管理程序的实施和控制要求;- 对xxx标准的遵循和持续改进的承诺;- 紧急情况应对计划和程序,以及危机管理和危险物质应对等内容。
2. xxx程序文件的编写和内容xxx程序文件是对xxx管理体系手册中各项要求的具体描述和实施细节,它具体规定了组织在执行xxx管理体系时应采取的具体步骤和管理措施。
程序文件的编写要求严格,内容应该满足以下基本要求:- 包含了组织的实际运营情况,能够指导组织内部各级管理人员和员工进行操作;- 具体规定了各项管理程序的执行要求和流程,包括健康安全管理的各项具体操作和实施步骤;- 对关键岗位和重要环节的作业流程和操作方式进行了明确规定,确保操作的一致性和标准化;- 注重风险控制和持续改进的要求,对各项健康安全风险的识别、评估和控制都有具体的规定。
3. 管理体系手册和程序文件的重要性管理体系手册和程序文件作为组织健康安全管理体系的核心文档,具有以下重要意义和作用:- 是组织健康安全管理的基础和依据,为组织内部的各项管理活动提供了有力支持;- 是组织对内外界传递健康安全管理承诺和要求的重要途径,提高了组织的管理透明度和公信力;- 在xxx认证评审和审核中具有重要作用,是xxx认证的必备文件; - 为组织内部的持续改进和风险控制提供了具体的操作指南和规定,对保障员工安全健康具有直接作用。
压力管道元件制造程序文件

压力管道元件制造程序文件Q/YT-B-2011版次/修订:A/0压力管道元件制造程序文件编制:审核:批准:持有者:受控编号:2011-06-01公布2011-06-10实施━━━━━━━━━━━━━━━━━━━━━━━━━━━━XXXXXXXXXXX公司1、公司依照TSG系列规范的要求,参照GB/T19001-2000标准的要求,结合我公司的实际情形,编制适宜的文件,以确保压力管道元件制造质保体系有效运行。
文件采纳纸张、运算机磁盘、光盘。
2、目的本公司质量体系所要求的文件进行操纵,确保在用文件的准确性、适宜性、有效性和可追溯性。
3、适用范畴适用于适用于本公司压力管道元件制造质量保证体系有效运行的所有文件(不包括质量记录)的操纵。
4 职责4.1 办公室是质量手册、质量治理体系程序性文件、技术标准、产品图样及设计文件的归口治理部门。
4.2 生产技术科负责工艺规程、工装图样等文件的治理。
4.3 各部门制定的内部治理文件由各部门参照本程序规定操纵。
5 工作程序5.1 文件的分类5.1.1按性质分为(1)技术性文件;(2)治理性文件。
5.1.2.按来源分为(1)外来文件,包括:1)国家及上级机关颁发的有关法规、法令、政策等文件;2)行业可直截了当引用或执行的规范、规则、技术标准等;3)顾客提供的资料、来函及件、记录等。
a、质量手册;b、质量程序性文件,包括质量体系程序文件和治理性作业文件;c、技术文件,包括产品图样、设计文件、工艺工装图样、工艺文件、检验规范等;d、过程策划所形成的文件如质量打算等;注:文件能够呈任何媒体,如磁盘、光盘、运算机软件及其他电子媒体。
5.1.3按操纵方式分为:5.1.3.1受控文件:凡与质量治理体系运行紧密相关的文件应为受控,受控文件的发放在文件上加盖“受控”印章,以便于识别。
(1)受控文件是由发放部门进行操纵并保持其有效状态的的文件,文件治理部门对本部门公布的受控文件都应制定并可随时提供能识别文件现行修订状态的受控文件清单,防止使用无效文件;受控文件应进行受控标识,标注受控编号。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XXX电子科技有限公司HY-CX-2010程序文件PROCEDURE DOCUMENT版本: A/0编制:审核:批准:发放编号:受控状态:2010-06-01发布2010-06-03实施版本号:A 修改码:0 章节号:0.1 页码:1/1程序文件目录1. 文件控制程序章节号 12. 记录控制程序章节号 23. 人力资源管理程序章节号 34. 质量信息控制程序章节号 45. 与顾客有关过程控制程序章节号 56. 设计和开发控制程序章节号 67. 新产品试制过程控制程序章节号78. 采购控制程序章节号89. 内部审核控制程序章节号910.不合格品控制程序章节号1011.纠正措施控制程序章节号1112.预防措施控制程序章节号1213.程序文件更改履历表章节号附录版本号:A 修改码:0 章节号:1 页码:1/61.文件控制程序HY/CX-4.2.3-2010 1 目的为使与质量管理体系有关的所有文件进行有效控制,防止使用无效版本的文件,确保与质量管理体系有关的所有文件处于受控状态,特制定并执行本程序。
2 范围本程序规定了质量管理体系文件控制的原则和方法。
本程序适用于公司与质量管理体系有关的所有文件的控制。
3 职责3.1 办公室负责质量手册、程序文件等体系文件及公司管理制度的编制,负责管理制度的起草及公司文件的监督管理。
3.2 生产技术部负责技术性文件的编写及文件的管理。
3.3 各部门负责本部门职能范围内管理业务文件的编写及部门文件的管理。
4 工作程序4.1 文件的分类4.1.1 按文件的描述对象不同分为:a) 管理性文件(如质量手册、程序文件、管理制度等);b) 技术性文件(如标准、图样、工艺、操作规程等方面的文件);c) 管理业务文件(如营销、采购、计划、培训、方面的文件);4.1.2 按文件的控制状态分为:a) 受控对文件的使用、修改、作废、换版进行跟踪管理。
b) 非受控对文件不进行跟踪管理。
4.1.3 按文件的来源分为:内部文件和外来文件。
对重要的外来文件应按照受控文件进行控制。
4.2 文件的编写与审批4.2.1 文件的编写a) 办公室负责组织质量手册等体系文件及公司管理制度的编写;b) 生产技术部负责技术性文件的编写并符合《技术文件管理规定》●图样和技术文件按规定进行审签、工艺和质量会签、标准化检查。
●图样、技术文件协调一致、现行有效●识别产品质量形成过程中需要保存的文件,并及时归档。
c) 各部门负责本部门职能范围内的业务文件的编写。
4.2.2 文件的审批a) 质量手册、岗位质量职责由管理者代表审核,报总经理批准后执行;b) 程序文件由各职能部门负责人会审后,报管理者代表审核,总经理批准后执行;c) 技术性或业务性文件部门负责人审批后执行,需要时报主管副经理批准后执行;d) 管理制度由办公室起草,经理办公会讨论通过后,总经理批准后执行。
4.3 文件的编号a) 除技术工艺文件、图样和合同外的所有与产品质量和质量管理体系有关文件的编号如下:A) 质量手册B) 程序文件C) 作业指导书D) 质量记录b) 技术工艺文件、图样和合同的编码按国家或行业标准执行;c) 质量管理体系文件类型采用汉语拼音字母缩写的方式,即质量手册:SC、程序文件:CX、作业指导书:ZY、质量记录:JL;公司汉语拼音缩写为:HY;d) 文件的版本采用英文字母A、B、C……的方式,修改状态采用数字0、1、2…表示,文件的版次用于质量手册、程序文件、作业指导书;质量记录不实行版次控制,每年对质量记录的格式进行确认;4.4 文件的发放4.4.1 文件发放实施签字控制,部门依据文件涉及部门和人员填写《文件发收登记表》,接受人员在接受文件后签字;受控文件发放前,要加盖红色“受控”标识,并填写发放编号,同一文件编号不得重复;4.4.2 发至本公司内部与质量体系有关的文件均为受控本,发给认证机构、军代表也为受控本,作为资料和信息发给顾客的文件为非受控文件,非受控文件由管理者代表审批后编号发放。
4.4.3 外来文件,由业务归口部门管理,需要时登记、编号后向有关部门和人员发放。
4.5 文件的评审、更改与回收4.5.1 每年应按照管理评审的要求对本公司现有质量管理体系文件的充分性和适宜性进行评审,各部门平时结合使用情况,对不合适的内容应及时进行调整和修订。
4.5.2 文件如需更改,应由更改提出部门提出书面更改建议,填写《文件更改申请单》,说明更改原因,报原编制部门审批;技术文件的更改按照《技术文件管理规定》相关要求执行。
若由其他部门人员进行审批时,需取得原审批部门相关背景资料。
文件的更改经审批后,由原编制部门组织更改或更换,并收回原作废文件。
文件的更改方式可采用划改、换页和换版;文件更改需在更改履历表上做出记录。
a) 划改:部分更改采用“划改”的方法,在原有文件相应条款处进行修改。
即在原有文字上划两道横线,并在原有文字的适当位置写出更改后的内容。
b) 换页:文件累计更改面积不得大于该页有效面积的1/4或划改次数不得超过4次,否则必须作换页处理。
c) 换版:文件有重大更改或重新排版时需要换版,新版文件生效时,原版文件同时作废。
文件的更改应该表明关联更改文件的信息,关联文件更改由编制单位进行更改修订,编制文件单位负责人负责监督和考核;内审过程中需要重点检查关联文件更改落实情况,办公室在检查文件过程中应检查关联文件更改情况;4.5.3 文件的回收文件管理人员对修订或作废文件应及时回收处理,文件回收时应填写“文件发收登记表”,文件提交人员在该表中签名,并填写有关文件回收的信息记录,为防止误填信息,文件回收人不得填写回收信息。
4.6 文件的作废4.6.1 作废的文件由发放部门负责收回,要及时处理作废文件,防止误用,文件销毁根据文件资料销毁记录内容履行有关程序,确保体系运行中的文件现行有效。
4.6.2 为法律和积累知识保留的作废文件,应征得原发放部门同意后登记并加盖“作废保留”标识后参考使用,不得作为正式文件使用,作废保留的文件不得多于两套。
4.7 文件日常管理4.7.1 各部门应指派专人(可兼职),负责本部门文件的日常收发、保管、存档等管理工作;文件要分类放置,使文件便于识别和检索。
4.7.2 文件的复制文件需要复制时,使用部门应经文件发放部门负责人同意。
其复制件经发放部门登记、编号并加盖红色“受控”印章后方可使用,否则复制件为无效文件。
4.7.3 因工作变更调离原岗位时,文件使用人不得带走文件,可同调入本岗位的人员一同到文件发放部门登记办理退还和交接手续。
4.7.4 当文件破损严重不能使用时,使用人应到文件发放部门以旧换新,新文件的分发号仍沿用原分发号,破损文件由发放部门销毁。
4.7.5 当文件丢失后,其使用人员应写出书面申请重新领用。
文件发放部门应给予补发文件新的分发号,同时在《文件发收登记表》上注明和通知各部门丢失的原分发号文件作废。
4.7.6公司内不得使用失效、作废的文件,一经发现,文件发放部门或办公室应立即收回并销毁。
4.7.7 需临时借阅文件的,须经发放部门负责人批准,并在《文件借阅登记表》中登记后方可借阅,借阅人应按时归还所借文件。
4.8 文件的归档和保存4.8.1 对产品质量控制的文件应由责任部门进行定期整理,一般以一个生产周期或一年为阶段进行整理,并按资料和文件的重要程度由部门负责人决定自行保存或归档。
4.8.2 需归档的文件,由发文部门负责将文件资料整理归档,并注明文件的名称、类别、存档要求。
4.8.3 档案管理员根据存档文件、资料的内容和档案管理的要求进行分类、组卷。
4.8.4 各部门对于如硬拷贝或电子媒体的文件需标明内容,单独存放或归档,加密保存,确保未经允许不被打印和拷贝,并保证其不受到损坏。
4.9 文件销毁4.9.1 在受控文件没有保留价值时,文件管理人员应填写《文件资料销毁记录》,经部门负责人批准后可以实施销毁,销毁时应有另一人监督,销毁人及监督人应在销毁记录上签字。
4.9.2 根据年度文件资料销毁记录,文件资料管理人员应整理登记年度文件销毁登记表,便于查找文件处理情况。
4.10 文件检查文件管理人员应检查所发放文件的控制情况,尤其是关联文件更改、回收和作废处理等情况,文件管理部门负责人要对该检查情况进行监督,防止出现不满足文件管理要求的情况。
5 相关/支持性文件5.1 HY/CX-4.2.4-2010 《记录控制程序》5.2 HY/ZY-09-2010《技术文件管理办法》版本号:A 修改码:0 章节号:1 页码:6/66 质量记录6.1 JL-4.2.3-01 《文件发收登记表》6.2 JL-4.2.3-02 《文件更改申请单》6.3 JL-4.2.3-03 《文件清单》6.4 JL-4.2.3-04 《文件借阅登记表》6.5 JL-4.2.3-05 《文件资料销毁记录》2、记录控制程序HY/CX-4.2.4-2010 1 目的对记录进行有效控制和管理,为质量管理体系有效运行和持续改进提供客观证据,特制定并执行本程序。
2 范围本程序对记录的设置、传递、保管、归档、借阅和销毁做出了具体规定。
本程序适用于与质量管理体系有关的所有记录的管理。
3 职责3.1 办公室负责质量记录的登记、审核、编号和备案,指导各部门建立、保存和管理有关的记录。
3.2 各部门分别对各自管辖范围内的记录的格式、正确性和完整性负责,并进行控制。
4工作程序4.1 记录的建立和编号4.1.1 记录所用的格式由各使用部门编制,报办公室审批统一编号、备案,特殊情况下需要时也可采用其它格式或随机记录,但必须在办公室登记备案;办公室编制本公司质量记录的总清单,各部门编制部门记录的清单。
4.1.2 各部门的记录格式需要增加、修改和作废时,应及时通知办公室登记备案。
4.1.3 记录的编号按照《文件控制程序》中的4.3条中d)项的规定执行。
4.2 记录表格的印制质量管理体系文件规定的记录表格及各部门自用的记录表格均由办公室负责印制。
办公室必须及时承制或外委印刷,满足各部门的使用要求。
4.3 质量记录的填写4.3.1 按质量记录设置的项目逐项填写,不得缺项。
某些项目不需要填写时,必须用“/”明示。
4.3.2 记录人员必须真实、及时记录各类质量活动和结果,不得后补、伪造,不得随意涂改,确认记录有误可划改不允许涂改,划改改后由记录者签字或盖章。
4.3.3 记录时应使用黑、蓝色钢笔、签字笔填写,字迹要清晰、规范,填写不漏项;签名时必须签全名。
4.3.4 记录中的计量单位和符号必须执行国家标准或或行业标准。
4.4 记录的传递、收集、编目4.4.2 记录由各业务主管部门指定专人负责收集、整理并按月度、季度、年度并按产品类型分类编目,装订成册,存放于专用橱柜内。
