制药行业术语和英文简称
制药行业术语和英文简称

制药行业术语和英文简称名词解释NDA : New Drug Application /新药生产上市申请INDA : Investigational New Drug Application/药品临床试验申报ANDA: Abbreviated New Drug Application/仿制药及改剂型申请提出申请快速通道资格认定(Request for Fast Track Designation)Accelerated Approval(加速审批): These regulations allowed drugs for serious conditions that filled an unmet medical need to be approved based on a surrogate endpoint.Breakthrough Therapy Designations(突破性疗法资格认定): A process designed to expedite the development and review of drugs which may demonstrate substantial improvement over available therapy.Fast Track Designation(快速通道资格认定): Fast track is a process designed to facilitate the development, and expedite the review of drugs to treat serious conditions and fill an unmet medical need.Priority Review(优先审核): A Priority Review designation means FDA’s goal is to take action on an application within 6 months.Orphan Drug Act(罕见疾病药物法案):也叫孤儿药注册1类和2类新药要进行新药临床试验申请(INDA);3类和4类要做验证性临床。
常用制药及GMP英文缩写

ISO(International Organization for Standardization):国际标准化组织日常办事机构是中央秘书处,设在瑞士日内瓦WHO(World Health Organization):世界卫生组织是联合国属下的专门机构,国际最大的公共卫生组织,总部设于瑞士日内瓦PIC/S(Pharmaceutical Inspection Convention/Pharmaceutical Inspection Cooperation Scheme):国际医药品稽查协约组织由欧洲自由贸易区(EFTA)组建ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use):人用药物注册技术要求国际协调会由欧盟(EU)、欧洲制药工业协会联合会(EFPIA)、日本厚生省(MHW)、日本制药工业协会(JPMA)、美国FDA、美国药物研究生产联合会(PRMA)等机构组成WHO、EFTA、加拿大卫生保健局(CHPB)为观察员ISPE(International Society for Pharmaceutical Engineering):国际制药工程协会是致力于培训制药领域专家并提升制药行业水准的世界最大的非盈利性组织之一,在美国坦帕州设有全球总部,在布鲁塞尔设有欧洲总部,亚洲总部在新加坡HHS(United States Department of Health and Human Services):美国卫生及公共服务部(美国卫生部)FDA(Food and Drug Administration):美国食品药品监督管理局(HHS下属机构)PDA(Parenteral Drug Association):美国注射剂协会EPA(Environmental Protection Agency):美国国家环境保护局CDER(Center for Drug Evaluation and Research):FDA药物评价与研究中心EMEA(The European Agency for the Evaluation of Medicinal Products):欧洲药物评审组织MHW(Ministry of Health and Welfare):日本厚生省,现改为厚生劳动省MHLW(Ministry of Health, Labor and Welfare),负责医疗卫生和社会保障的主要部门D&B(Dun & Bradstreet):邓白氏公司DUNS(Data Universal Numbering System):邓白氏公司提供的唯一的公司代号,用于信用评级等在SMF文件中会用到GMP(Good Manufacturing Practice):药品良好生产规范cGMP(Current Good Manufacture Practices):动态药品生产管理规范,即现行的GLP(Good Laboratory Practice):药物非临床研究质量管理规范,及优良实验室规范GSP(Good Supplying Practice):药品经营质量管理规范,及良好的药品供应规范GAP(Good Agricultural Practice for Chinese Crude Drugs):中药材生产质量管理规范GDP(Good Documentation Practice):良好文件管理GEP(Good Engineering Practice):工程设计规范GAMP(Good Automated Manufacturing Practice):优良自动化生产规范USP(united states pharmacopeia):美国药典EP(European Pharmacopeia):欧洲药典JP(Japanese Pharmacopoeia):日本药典CFR(Code of Federal Regulations):美国联邦法律CFR 21 Part 11(Code of Federal Registry Part11):联邦法规法律标题21第11部分CEP/COS(Certificate of Suitability to the monographs of European Pharmacopoeia):欧洲药典适应性认证证书CEP认证,COS证书CTD(Common Technical Document):国际注册用常规技术文件CTD文件是国际公认的文件编写格式,用来制作一个向药品注册机构递交的结构完善的注册申请文件EHS(Environment、Health、Safety):环境-健康-安全管理体系HACCP(Hazard Analysis and Critical Control Point):(保健食品)危害分析和关键控制点REACH(REGULATION concerning the Registration, Evaluation, Authorization and Restriction of Chemicals):欧盟规章《化学品注册、评估、许可和限制》,欧盟建立的,并于2007年6月1日起实施的化学品监管体系ICH-Q1A:新原料药和制剂的稳定性试验ICH-Q1B:稳定性试验:新原料药和制剂的光稳定性试验ICH-Q1C:稳定性试验:新剂型的要求ICH-Q1D:新原料药和制剂的稳定性试验的括号法和矩阵法设计ICH-Q1E:稳定性数据的评价ICH-Q1F:气候带Ⅲ和Ⅳ注册申请的稳定性数据ICH-Q2A:分析步骤验证:正文ICH-Q2B:分析步骤验证:方法学ICH-Q3A:原料药中的杂质ICH-Q3B:新制剂中的杂质ICH-Q3C:杂质;残留溶剂的指导原则ICH-Q4 :药典ICH-Q4A :药典的同一化ICH-Q4B:各地区使用的药典正文评估和建议ICH-Q5A:来源于人或动物细胞系的生物技术产品的病毒安全性评价ICH-Q5B:生物技术产品的质量:rDNA衍生蛋白质产品生产细胞的表达构建体分析ICH-Q5C:生物技术产品的质量:生物制品/生物技术产品的稳定性试验ICH-Q5D:用于生物技术产品及生物制品生产的细胞基质的来源和鉴定ICH-Q5E:生物技术产品/生物制品在工艺变更时的可比性ICH-Q6A:质量标准新原料药和制剂的检测以及可接受标准:化学物质ICH-Q6B:质量标准:生物技术产品及生物制品的检测方法和可接受标准ICH-Q7 :原料药良好制造规范(ICH-Q7A的新版)ICH-Q7A:原料药的GMP规范ICH-Q8 :药物研发指南ICH-Q9 :质量风险管理ICH- Q10(PQS):药物质量体系QA(Quality Assurance):质量保证QC(Quality Control):质量控制QRM(Quality Risk Management):质量风险管理IPC(Inproceics Quality Control):制程品质控制/中控OOS(Out of Specification):检验结果超标OOT(Out of Trend):超趋势结果OOL(Out of Limit):超出极限的结果,如温湿度等OOE(Out of Expectation):超期望结果SAL(Sterility Assurance Level):无菌保证水平灭菌后微生物的存活概率的负对数,要求≥6D值:杀灭90%的微生物所需要的时间,D值越大,微生物死亡越难,D值与细菌的耐热性成正比Z值:指灭菌时间减少到原来的10%所需要升高的温度或是相同的灭菌时间内杀死99%的微生物所需要提高的温度F值:为一定温度下,给定Z值所产生的灭局效果与参比温度T0下给定Z值所产生的灭菌效果相同时所相当的时间F值用于干热灭菌F0值:为一定温度下,Z值为10℃产生的灭菌效果与120℃,Z值为10℃时产生的灭菌效果相当的时间,t分钟内的灭菌效果相当于120℃下灭菌F0分钟的效果F0被称为标准灭菌时间,用于热压灭菌LRV:除菌过滤的对数下降值LRV=lgN0-lgNSOP(Standard Operation Procedure):标准操作规程DMF(Drug Master File):药品主文件SMF(Site Master File):工厂主文件URS(User Requirement Specification):用户需求标准FS(Functional Specification):功能标准DS(Design Specification):设计标准DQ(Design Qualification):设计确认IQ(Installation Qualification):安装确认OQ(Operational Qualification):运行确认PQ(Performance Qualification):性能确认RQ(Requalification):再确认CAPA(Corrective Action & Preventive Action):纠正预防系统,Q10的四大要素之一QbD(Quality by Design):质量源于设计COA(Certificate of Analysis):分析证书/检验报告书/检验报告单BPR(Batch Production Record):批生产记录API(Active Pharmaceutical Ingredients):药物活性成分,通常指的原料药。
制药行业常用英语词汇(缩写、中英文对照)

制药行业常用英语词汇(缩写、中英文对照)制药行业常用英语词汇(缩写、中英文对照)序号中文英文及缩写 1 药品生产质量管理规范 GMP:GoodManufacturingPractice 2 国家食品与药品监督管理局 State Food and Drug Administration 3 总则 GeneralProvisions 4 《中华人民共和国药品管理法》 the DrugAdministration Law of the People"s Republic of China 5 制剂Preparation 6 原料药 API: Active PharmaceuticalIngredient 7 成品finished goods 8 工序 process 9 机构与人员 organization and personnel 10 专业知识 professional knowledge 11 生产经验 production e_perience 12 组织能力 organizational skill 13 技术人员 technical staff 14 实施implementation 15 药品生产 pharmaceutical manufacturing 16 质量管理quality management 17 质量检验 quality inspection 18 专业技术培训professional and technicaltraining 19 基础理论知识 basic theoreticalknowledge 20 实际操作技能 practical operationskills 21 高生物活性 highly potent 22 高毒性 high to_icity 23 污染 contamination 24 考核评估 assessment25 厂房与设施 buildings and facilities 26 生产环境 production environment 27 空气洁净级别 clean air level 28 昆虫 insect 29 洁净室(区)clean room(area) 30 光滑 smooth 31 无裂缝 no cracks 32 无颗粒物脱落no particle shedding 33 耐受 endure 34 消毒 disinfection 35 无菌 sterile 36 交界处 junction, joint 37 弧形 arc 38 灰尘积聚 dues accumulation 39 储存区 store area 40 生产规模 production scale 41 设备 equipment 42 物料material 43 中间产品 intermediate product 44 待验品 quarantined material 45 交叉污染 cross-contamination 46 管道 pipeline, ductwork 47 风口 tuber 48 公用设施, 公用工程 utilities of publicservice 49 照明 lighting 50 照度 illumination 51 应急紧急情况 emergency 52 净化 purification, clean 53 微生物, 微生物学, 微生物 micro-organism,microbiology,microbiologic的 54 监测 monitoring 55 记录 record 56 天棚天花板 ceiling, roof 57 密封 seal 58 静压差 Static DifferentialPressure 59 温度 temperature 60 相对湿度 RH: Relative Humidity 61 低漏地漏 floor drainer 62 青霉素penicillin 63 分装室 separating room, fillingroom 64 相对负压 relative negativepressure 65 废气 waste gas,e_hausted air 66 β-内酰胺结构类药品 β-Lactasestructure drug, drugs of β-Lactic group 67 避孕药品 contraceptives 68 激素类 hormone 69 抗肿瘤类 anti-tumor, oncology 70 放射性药品 Radiopharmaceuticals 71 包装 packing, package 72 循环使用recycling 73 微粒 particles 74 辐射 radiation, irradiation 75 细菌bacteria 76 病毒 virus 77 细胞 cell 78 脱毒前后 pre and postdeto_ification 79 活疫苗与灭活疫苗 activevaccine/inactivatedvaccine 80 人血液制品 blood products 81 预防制品prevention products82 灌装 filling 83 中药 Chinesetraditional medicines 84 前处理pretreatment 85 提取 e_traction 86 浓缩 concentration 87 动物脏器viscera of animal,organ ofanimal 88 蒸、炒、炙、煅 ing, frying,sunburn, testing 89 炮制concocted 90 通风 ventilation 91 除烟 smoke removal 92 除尘 dust removal 93 降温设施 temperature-reducingestablishment,cooling 94 筛选 screening, sift 95 切片 slicing 96 粉碎 grinding 97 压缩空气 pressed air 98 惰性气体 noble gas 99 取样 Sling 100 称量室weighing room, dispensingroom 中药标本 Chinese herbalsle,e_emplar of TCM 102 检定鉴定 verification, identification 103 同位素 Isoe 104 设备 equipment 105 选型 model/type selection 106 耐腐蚀anticorrosion 107 吸附 adsorption, absorption 108 润滑剂, 润滑 lubricant, lubricate 109 冷却剂 coolant 110 流向 flow direction111 纯化水 PW: Purified Water 112 注射用水 WFI: Water for Injection 113 滋生 breeding 114 储罐 tank 115 死角 neglected portion 116 盲管blind pipe 117 纤维 fiber 118 疏水性 hydrophobicity 119 仪表instrumentation 120 量具 measuring tool 121 衡器 weighing instrument 122 精密度 precision 123 维修 maintenance 124 不合格 disqualified reject 125 物料 material 126 购买 purchasing 127 发放 releasing 128 产地 origin 129 入库 loading 130 固体 solid 131 液体 liquid 132 挥发性 volatile 133 净药材 medicine, TCM 134 麻醉药品 narcotics 135 精神药品 psychotropic drug 136 易燃 bustible 137 易爆 e_plosive 138 验收 acceptance 139 使用说明书instruction140 标签 label 141 卫生, 清洁/消毒 sanitation 142 车间, 辅房workshop 143 间隔时间 time interval 144 清洁剂 detergent 145 消毒剂disinfectant 146 废弃物 wastes 147 更衣室 changing room 148 工作服, work clothes 149 颗粒性物质, 颗粒剂 granules 150 耐药菌株 drug-resistantstrain 151 传染病 infectiousdisease 152 皮肤病 dermatitis 153 验证verification, validation 154 确认 qualification 155 安装 installation156 运行 running operation 157 性能 performance 158 原辅料 raw material and incipient 159 文件 document 160 投诉 plaint 161 报废 reject 162 品名product name 163 处方 preion, formula 164 技术参数 technicalparameter165 容器 container 166 半成品 semi-finished product,intermediate 167 申请 lication 168 稳定性 stability169 起草 draft 170 生产管理 production management,manufacturing control.171 事故 accident 172 混淆 mi_-up 173 喷雾 spray 174 合格证certificate 175 清场 clearance 176 质量管理 quality management 177 内控internal control,on-line test 178 滴定液 tartan 179 培养基 medium 180 有效期 validity, e_piry date,shelf life 181 产品销售与收回 product sales andrecovery/recall 182 投诉与不良反应报告 plaints and adversereaction 自检self-inspection 184 附则 schedule endi_ 185 平衡 balance 186 饮用水drinking water, potablewater 187 蒸馏法 distillation 188 离子交换法 ion e_change 189 反渗透法 RO: Reverse Osmosis 190 附加剂添加剂 additives 191 滞留 stranded resort 192 批 batch, lot 193 组分, 组成 ponent 194 无纤维脱落的过滤器 non-fiber-releasingfilter 195 活性成份 Active Ingredient 196 非活性成份 Inactive ingredient 197 中间产品 in-processproduct,intermediate product198 批号 batch number 199 药用物料 medicated feed 20__药用预混合料 medicated premi_ 201 质量控制部门 Quality control department 202 理论产量 Theoretical yield 203 实际产量 Actual yield 204 比率 Percentage, rate 205 验收标准可接受标准 Acceptance criteria 206 代表性样品 Representative sle 207 微粒状的 particulate 208 污染物contaminant 209 石棉 asbestos 210 诊断 diagnosis 211 缓解 mitigation 212 化学变化 chemical change 213 组分 ingredient, ponent 214 制备 fabricate preparation 215 复合 pound 216 混合 blend 217 加工 processing 218 浓度concentration 219 单位剂量 unit dose 220 药品包装容器 drug product containers 221 密封件, 封盖 closure 222 效价 Titer 223 纯度 purity 224 规格 strength 225 监督 supervise, monitor 226 实验室 laboratory 227 无菌操作 aseptic operation,sterileoperation 228 层流 laminar flow 229 湍流 turbulent air flow 230 空气过滤 air filtration 231 空气加热 air heating 232 预过滤器 profiler 233 排气系统 e_haust system 234 管件 plumbing 235 虹吸倒流 back-siphon age 236 污水 sewage 237 废料 refuse 238 盥洗设备 toilet facilities 239 空气干燥器 air drier 240 垃圾 trash 241 有机废料 organic waste 242 杀鼠剂rodenticides 243 杀昆虫剂 insecticides 244 杀真菌剂 fungicides 245 熏蒸剂 fumigating reagents 246 去垢剂 cleaning agents 247 消毒剂 sanitizing agents 248 滂沱剂 lubricant 249 自动化设备 automatic, mechanical,or electronic equipment 250 微型胶卷 microfilm 251 注射剂 injection 252 灭菌设备 sterilization equipment 253 无菌取样技术 aseptic sling techniques 254 显微镜 microscope 255 热, 内毒素 pyrogen, endoto_in 256 偏差 deviation 257 变更 change control 258 进料 charge-in 259 项目代码 item code 260 鉴别 identify 261 片剂 tablet 262 胶囊 capsule 263 颗粒剂 granule 264 溶解时间溶出时间 dissolution time 265 澄明度clarity 266 隔离系统 quarantinesystem, isolation system 267 返工reprocessing 268 发放 issuance, release 269 非处方药 OTC:over-the-counter 270 处方药 preed medicine 271 皮肤科药、牙粉、胰岛素、喉片dermatological,dentifrice,insulin, or throat lozenge product 272 保险包装 ter-resistant package 273 明胶硬胶囊 hard gelatin capsule 274 顺势治疗homeopathic 275 入库 warehousing 276 变质 deteriorate 277 准确性accuracy 278 灵敏性 sensitivity 279 特异性 specificity 280 重复性reproducibility, repeatability 281 变应原提取物 allergenic e_tracts 282 眼膏 ophthalmic ointment 283 粗糙或磨蚀物质 harsh or abrasivesubstances 284 控释制剂 controlled-releasedosage form 285 实验动物 laboratory animals 286 供应商 Supplier 287 光谱 spectrum 288 测量单位 units of measure 289 换算系数 conversion factors 290 试剂 reagent 291 安慰剂placebo 292 明确地 e_plicitly 293 取代 supersede 294 溶液 solution 295 批准 roval 296 (美国)食品药品监督管理局 FDA: Food and DrugAdministration 297 标准操作程序 SOP: StandardOperatingProcedure 298 质量保证 QA: Quality Assurance 299 质量控制QC:Quality Control 300 批生产记录 BPR: Batch ProductionRecord 301 批检验记录 BAR: Batch AnalysisRecord 302 工艺规程 PP: Process Procedure 303 健康,安全,环保 EHS: Environment,Health andSafe 304 美国联邦法规 CFR: Code of FederalRegulation 305 美国药典USP: The UnitedStatesPharmacopeia 306 欧洲药典 EP: European pharmacopeia 307 英国药典 BP: British pharmacopeia 308 药物主文件 DMF: Drug Master File 309 验证主计划 VMP: Validation MasterPlan 310 验证方案 VP: Validation Protocol 311 验证报告 : Validation Report 312 安装确认 IQ: Installation Qualification313 运行确认 OQ: Operation Qualification 314 性能确认 PQ: Performance Qualification 315 超出标准(限度) OOS: Out of Specification 316 冻干产品 freeze-dry product,lyophilizated product 317 工厂主述文件SMF: Site Master File。
最全的医药行业术语汇总

最全的医药行业术语汇总医药行业术语是指在医药领域中所使用的特定词汇和术语,用于描述医药研发、临床实践、制药、药学、药理学等领域的概念和操作。
以下是医药行业术语的一些常见和重要的词汇,供参考:1. 临床试验(Clinical trial):用于评估新药疗效、安全性和剂量等方面的研究。
2. 随机对照试验(Randomized controlled trial,RCT):一种临床试验设计,分为两组进行,一组接受治疗,另一组接受安慰剂或对照治疗,以评估新药的有效性。
3. 新药上市申请(New Drug Application,NDA):申请将新药提交给监管机构,以获得上市许可。
4. 药代动力学(Pharmacokinetics,PK):研究药物在体内的吸收、分布、代谢和排泄等过程。
5. 药物动力学(Pharmacodynamics,PD):研究药物对机体的作用和效应。
6. 目标药物(Targeted therapy):指通过选择性地作用于特定分子靶点,治疗患者疾病的药物。
8. 基因治疗(Gene therapy):通过向患者体内引入修复基因来治疗遗传性疾病的方法。
9. 帕金森病(Parkinson's disease):一种进展性神经系统疾病,特征是肌肉僵硬、震颤和运动障碍。
10. 阿尔茨海默病(Alzheimer's disease):一种神经系统疾病,影响认知能力和记忆功能。
11. 心脏病(Cardiovascular disease):一类影响心脏和血管的疾病,包括心脏病发作、心力衰竭和高血压等。
12. 癌症(Cancer):一类疾病,由异常细胞不受控制地生长和扩散而导致。
13. 肿瘤标志物(Tumor marker):指在体内或体液中检测到的与肿瘤相关的生物标记物。
14. 化疗(Chemotherapy):使用抗癌药物治疗癌症的方法。
15. 免疫疗法(Immunotherapy):通过激活或增强免疫系统来治疗疾病的方法。
常用制药及GMP英文缩写

ISO(International Organization for Standardization):国际标准化组织日常办事机构是中央秘书处,设在瑞士日内瓦WHO(World Health Organization):世界卫生组织是联合国属下的专门机构,国际最大的公共卫生组织,总部设于瑞士日内瓦PIC/S(Pharmaceutical Inspection Convention/Pharmaceutical Inspection Cooperation Scheme):国际医药品稽查协约组织由欧洲自由贸易区(EFTA)组建ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use):人用药物注册技术要求国际协调会由欧盟(EU)、欧洲制药工业协会联合会(EFPIA)、日本厚生省(MHW)、日本制药工业协会(JPMA)、美国FDA、美国药物研究生产联合会(PRMA)等机构组成WHO、EFTA、加拿大卫生保健局(CHPB)为观察员ISPE(International Society for Pharmaceutical Engineering):国际制药工程协会是致力于培训制药领域专家并提升制药行业水准的世界最大的非盈利性组织之一,在美国坦帕州设有全球总部,在布鲁塞尔设有欧洲总部,亚洲总部在新加坡HHS(United States Department of Health and Human Services):美国卫生及公共服务部(美国卫生部)FDA(Food and Drug Administration):美国食品药品监督管理局(HHS下属机构)PDA(Parenteral Drug Association):美国注射剂协会EPA(Environmental Protection Agency):美国国家环境保护局CDER(Center for Drug Evaluation and Research):FDA药物评价与研究中心EMEA(The European Agency for the Evaluation of Medicinal Products):欧洲药物评审组织MHW(Ministry of Health and Welfare):日本厚生省,现改为厚生劳动省MHLW (Ministry of Health, Labor and Welfare),负责医疗卫生和社会保障的主要部门D&B(Dun & Bradstreet):邓白氏公司DUNS(Data Universal Numbering System):邓白氏公司提供的唯一的公司代号,用于信用评级等在SMF文件中会用到GMP(Good Manufacturing Practice):药品良好生产规范cGMP(Current Good Manufacture Practices):动态药品生产管理规范,即现行的GLP(Good Laboratory Practice):药物非临床研究质量管理规范,及优良实验室规范GSP(Good Supplying Practice):药品经营质量管理规范,及良好的药品供应规范GAP(Good Agricultural Practice for Chinese Crude Drugs):中药材生产质量管理规范GDP(Good Documentation Practice):良好文件管理GEP(Good Engineering Practice):工程设计规范GAMP(Good Automated Manufacturing Practice):优良自动化生产规范USP(united states pharmacopeia):美国药典EP(European Pharmacopeia):欧洲药典JP(Japanese Pharmacopoeia):日本药典CFR(Code of Federal Regulations):美国联邦法律CFR 21 Part 11(Code of Federal Registry Part11):联邦法规法律标题21第11部分CEP/COS(C ertificate o f S uitability to the monographs of E uropean P harmacopoeia):欧洲药典适应性认证证书CEP认证,COS证书CTD(Common Technical Document):国际注册用常规技术文件CTD文件是国际公认的文件编写格式,用来制作一个向药品注册机构递交的结构完善的注册申请文件EHS(Environment、Health、Safety):环境-健康-安全管理体系HACCP(Hazard Analysis and Critical Control Point):(保健食品)危害分析和关键控制点REACH(REGULATION concerning the Registration, Evaluation, Authorization and Restriction of Chemicals):欧盟规章《化学品注册、评估、许可和限制》,欧盟建立的,并于2007年6月1日起实施的化学品监管体系ICH-Q1A:新原料药和制剂的稳定性试验ICH-Q1B:稳定性试验:新原料药和制剂的光稳定性试验ICH-Q1C:稳定性试验:新剂型的要求ICH-Q1D:新原料药和制剂的稳定性试验的括号法和矩阵法设计ICH-Q1E:稳定性数据的评价ICH-Q1F:气候带Ⅲ和Ⅳ注册申请的稳定性数据ICH-Q2A:分析步骤验证:正文ICH-Q2B:分析步骤验证:方法学ICH-Q3A:原料药中的杂质ICH-Q3B:新制剂中的杂质ICH-Q3C:杂质;残留溶剂的指导原则ICH-Q4:药典ICH-Q4A:药典的同一化ICH-Q4B:各地区使用的药典正文评估和建议ICH-Q5A:来源于人或动物细胞系的生物技术产品的病毒安全性评价ICH-Q5B:生物技术产品的质量:rDNA衍生蛋白质产品生产细胞的表达构建体分析ICH-Q5C:生物技术产品的质量:生物制品/生物技术产品的稳定性试验ICH-Q5D:用于生物技术产品及生物制品生产的细胞基质的来源和鉴定ICH-Q5E:生物技术产品/生物制品在工艺变更时的可比性ICH-Q6A:质量标准新原料药和制剂的检测以及可接受标准:化学物质ICH-Q6B:质量标准:生物技术产品及生物制品的检测方法和可接受标准ICH-Q7:原料药良好制造规范(ICH-Q7A的新版)ICH-Q7A:原料药的GMP规范ICH-Q8:药物研发指南ICH-Q9:质量风险管理ICH- Q10(PQS):药物质量体系QA(Quality Assurance):质量保证QC(Quality Control):质量控制QRM(Quality Risk Management):质量风险管理IPC(Inproceics Quality Control):制程品质控制/中控OOS(Out of Specification):检验结果超标OOT(Out of Trend):超趋势结果OOL(Out of Limit):超出极限的结果,如温湿度等OOE(Out of Expectation):超期望结果SAL(Sterility Assurance Level):无菌保证水平灭菌后微生物的存活概率的负−lgN0对数,要求≥6SAL=−lg存活率=F0DD值:杀灭90%的微生物所需要的时间,D值越大,微生物死亡越难,D值与细菌的耐热性成正比Z值:指灭菌时间减少到原来的10%所需要升高的温度或是相同的灭菌时间内杀死99%的微生物所需要提高的温度F值:为一定温度下,给定Z值所产生的灭局效果与参比温度T0下给定Z值所产生的灭菌效果相同时所相当的时间F值用于干热灭菌F0值:为一定温度下,Z值为10℃产生的灭菌效果与120℃,Z值为10℃时产生的灭菌效果相当的时间,t分钟内的灭菌效果相当于120℃下灭菌F0分钟的效果F0被称为标准灭菌时间,用于热压灭菌LRV:除菌过滤的对数下降值LRV=lgN0-lgNSOP(Standard Operation Procedure):标准操作规程DMF(Drug Master File):药品主文件SMF(Site Master File):工厂主文件URS(User Requirement Specification):用户需求标准FS(Functional Specification):功能标准DS(Design Specification):设计标准DQ(Design Qualification):设计确认IQ(Installation Qualification):安装确认OQ(Operational Qualification):运行确认PQ(Performance Qualification):性能确认RQ(Requalification):再确认CAPA(Corrective Action & Preventive Action):纠正预防系统,Q10的四大要素之一QbD(Quality by Design):质量源于设计COA(Certificate of Analysis):分析证书/检验报告书/检验报告单BPR(Batch Production Record):批生产记录API(Active Pharmaceutical Ingredients):药物活性成分,通常指的原料药PMC(Product Material Control):生产物料控制PC生产控制;MC物料控制CMC(Chemistry and manufacture control):生产和化学控制APR(Annual Products Review):年度质量回顾KPI(Key Performance Indicators):关键业绩指标P&ID(Piping and Instrument Diagram):工艺管道仪表流程图PFD(Process Flow Diagram):工艺流程图UFD(Utility Flow Diagram):公用工程流程图CIP(Cleaning in Place):原位清洗(全自动,如针剂配制系统)WIP(Washing in Place):在线清洁(半自动,需要手动的拆卸,如流化床)SIP(Sterilization in Place):在线灭菌WFI(Water for Injection):注射用水HVAC(Heating Ventilation Air Conditioning):供热空气调节净化系统HEPA(High Efficiency Particulate Air Filter):高效过滤器DOP:为邻苯二甲酸二辛酯,HEPA检漏用的气溶胶PAO:聚-α-烯烃,HEPA检漏用的气溶胶IBC(I ntermediate Bulk Container):中型散装容器BFS(Blowing Filling and Sealing):吹-灌-封PAT(Process Analytical Technology):过程分析技术PLC(Programmable Logic Controller):可编程逻辑控制CPP(Critical Process Parameters):关键工艺参数FBD(Fluid Bed Dryer):流化床AHU(Air Handling Unit):空气处理单元SAT(Site Acceptance Test):现场验收测试FAT(Factory Acceptance Test):工厂验收测试。
药企常用名词中英文缩写汇总

药企常用名词中英文缩写汇总1.SOP标准操作程序(操作标准)
2.POP生产操作程序
3.QOP质量操作程序
4.EOP设备(计量)操作程序
5.MOP物料处理操作程序
6.HOP卫生操作程序
7.CLP清洁规程
8.SMP标准管理程序
9.QMP质量管理程序
10.DMP文件管理程序
11.MMP物料管理程序
12.PMP生产管理程序
13.EMP设备计量管理程序
14.VMP验证管理程序
15.OMP 行政管理程序
16.HMP卫生管理程序
17.TMP培训管理程序
18.FMP厂房与设施管理程序
19.QA质量保证
20.QC质量控制(检验)
21.FO灭菌保证值
22.HVAC空气净化系统
23.FDA美国药品与食品管理局24.WTO世界贸易组织
25.WHO世界卫生组织
26.pH酸碱度
27.CFU细菌菌落数
28.ppm百万分之一(克)
29.h.hr小时
30.min分
31.RH相对湿度
32.dB分贝
33.m3立方米
34.m2平方米。
常用制药及GMP英文缩写

常用制药及GMP英文缩写ISO(International Organization for Standardization):国际标准化组织日常办事机构是中央秘书处,设在瑞士日内瓦WHO(World Health Organization):世界卫生组织是联合国属下的专门机构,国际最大的公共卫生组织,总部设于瑞士日内瓦PIC/S(Pharmaceutical Inspection Convention/Pharmaceutical Inspection Cooperation Scheme):国际医药品稽查协约组织由欧洲自由贸易区(EFTA)组建ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use):人用药物注册技术要求国际协调会由欧盟(EU)、欧洲制药工业协会联合会(EFPIA)、日本厚生省(MHW)、日本制药工业协会(JPMA)、美国FDA、美国药物研究生产联合会(PRMA)等机构组成WHO、EFTA、加拿大卫生保健局(CHPB)为观察员ISPE(International Society for Pharmaceutical Engineering):国际制药工程协会是致力于培训制药领域专家并提升制药行业水准的世界最大的非盈利性组织之一,在美国坦帕州设有全球总部,在布鲁塞尔设有欧洲总部,亚洲总部在新加坡HHS(United States Department of Health and Human Services):美国卫生及公共服务部(美国卫生部)FDA(Food and Drug Administration):美国食品药品监督管理局(HHS下属机构)PDA(Parenteral Drug Association):美国注射剂协会EPA(Environmental Protection Agency):美国国家环境保护局CDER(Center for Drug Evaluation and Research):FDA药物评价与研究中心EMEA(The European Agency for the Evaluation of Medicinal Products):欧洲药物评审组织MHW(Ministry of Health and Welfare):日本厚生省,现改为厚生劳动省MHLW (Ministry of Health, Labor and Welfare),负责医疗卫生和社会保障的主要部门D&B(Dun & Bradstreet):邓白氏公司DUNS(DataUniversal Numbering System):邓白氏公司提供的唯一的公司代号,用于信用评级等在SMF文件中会用到GMP(Good Manufacturing Practice):药品良好生产规范cGMP(Current Good Manufacture Practices):动态药品生产管理规范,即现行的GLP(Good Laboratory Practice):药物非临床研究质量管理规范,及优良实验室规范GSP(Good Supplying Practice):药品经营质量管理规范,及良好的药品供应规范GAP(Good Agricultural Practice for Chinese Crude Drugs):中药材生产质量管理规范GDP(Good Documentation Practice):良好文件管理GEP(Good Engineering Practice):工程设计规范GAMP(Good Automated Manufacturing Practice):优良自动化生产规范USP(united states pharmacopeia):美国药典EP(European Pharmacopeia):欧洲药典JP(Japanese Pharmacopoeia):日本药典CFR(Code of Federal Regulations):美国联邦法律CFR 21 Part 11(Code of Federal Registry Part11):联邦法规法律标题21第11部分CEP/COS(C ertificate o f S uitability to the monographs of E uropean P harmacopoeia):欧洲药典适应性认证证书CEP认证,COS证书CTD(Common Technical Document):国际注册用常规技术文件CTD文件是国际公认的文件编写格式,用来制作一个向药品注册机构递交的结构完善的注册申请文件EHS(Environment、Health、Safety):环境-健康-安全管理体系HACCP(Hazard Analysis and Critical Control Point):(保健食品)危害分析和关键控制点REACH(REGULATION concerning the Registration, Evaluation, Authorization and Restriction of Chemicals):欧盟规章《化学品注册、评估、许可和限制》,欧盟建立的,并于2007年6月1日起实施的化学品监管体系ICH-Q1A:新原料药和制剂的稳定性试验ICH-Q1B:稳定性试验:新原料药和制剂的光稳定性试验ICH-Q1C:稳定性试验:新剂型的要求ICH-Q1D:新原料药和制剂的稳定性试验的括号法和矩阵法设计ICH-Q1E:稳定性数据的评价ICH-Q1F:气候带Ⅲ和Ⅳ注册申请的稳定性数据ICH-Q2A:分析步骤验证:正文ICH-Q2B:分析步骤验证:方法学ICH-Q3A:原料药中的杂质ICH-Q3B:新制剂中的杂质ICH-Q3C:杂质;残留溶剂的指导原则ICH-Q4:药典ICH-Q4A:药典的同一化ICH-Q4B:各地区使用的药典正文评估和建议ICH-Q5A:来源于人或动物细胞系的生物技术产品的病毒安全性评价ICH-Q5B:生物技术产品的质量:rDNA衍生蛋白质产品生产细胞的表达构建体分析ICH-Q5C:生物技术产品的质量:生物制品/生物技术产品的稳定性试验ICH-Q5D:用于生物技术产品及生物制品生产的细胞基质的来源和鉴定ICH-Q5E:生物技术产品/生物制品在工艺变更时的可比性ICH-Q6A:质量标准新原料药和制剂的检测以及可接受标准:化学物质ICH-Q6B:质量标准:生物技术产品及生物制品的检测方法和可接受标准ICH-Q7:原料药良好制造规范(ICH-Q7A的新版)ICH-Q7A:原料药的GMP规范ICH-Q8:药物研发指南ICH-Q9:质量风险管理ICH- Q10(PQS):药物质量体系QA(Quality Assurance):质量保证QC(Quality Control):质量控制QRM(Quality Risk Management):质量风险管理IPC(InproceicsQuality Control):制程品质控制/中控OOS(Out of Specification):检验结果超标OOT(Out of Trend):超趋势结果OOL(Out of Limit):超出极限的结果,如温湿度等OOE(Out of Expectation):超期望结果SAL(SterilityAssuranceLevel):无菌保证水平灭菌后微生物的存活概率的负对lgN0数,要求≥6SAL=?lg存活率=F0DD值:杀灭90%的微生物所需要的时间,D值越大,微生物死亡越难,D值与细菌的耐热性成正比Z值:指灭菌时间减少到原来的10%所需要升高的温度或是相同的灭菌时间内杀死99%的微生物所需要提高的温度F值:为一定温度下,给定Z值所产生的灭局效果与参比温度T0下给定Z值所产生的灭菌效果相同时所相当的时间F值用于干热灭菌F0值:为一定温度下,Z值为10℃产生的灭菌效果与120℃,Z 值为10℃时产生的灭菌效果相当的时间,t分钟内的灭菌效果相当于120℃下灭菌F0分钟的效果F0被称为标准灭菌时间,用于热压灭菌LRV:除菌过滤的对数下降值LRV=lgN0-lgNSOP(Standard Operation Procedure):标准操作规程DMF(Drug Master File):药品主文件SMF(Site Master File):工厂主文件URS(User Requirement Specification):用户需求标准FS(Functional Specification):功能标准DS(Design Specification):设计标准DQ(Design Qualification):设计确认IQ(Installation Qualification):安装确认OQ(Operational Qualification):运行确认PQ(Performance Qualification):性能确认RQ(Requalification):再确认CAPA(Corrective Action & Preventive Action):纠正预防系统,Q10的四大要素之一QbD(Quality byDesign):质量源于设计COA(Certificate of Analysis):分析证书/检验报告书/检验报告单BPR(Batch Production Record):批生产记录API(Active Pharmaceutical Ingredients):药物活性成分,通常指的原料药PMC(Product Material Control):生产物料控制PC 生产控制;MC物料控制CMC(Chemistry and manufacture control):生产和化学控制APR(Annual Products Review):年度质量回顾KPI(Key Performance Indicators):关键业绩指标P&ID(Piping and Instrument Diagram):工艺管道仪表流程图PFD(Process Flow Diagram):工艺流程图UFD(Utility Flow Diagram):公用工程流程图CIP(Cleaning in Place):原位清洗(全自动,如针剂配制系统)WIP(Washing in Place):在线清洁(半自动,需要手动的拆卸,如流化床)SIP(Sterilization in Place):在线灭菌WFI(Water for Injection):注射用水HVAC(Heating Ventilation Air Conditioning):供热空气调节净化系统HEPA(High Efficiency Particulate Air Filter):高效过滤器DOP:为邻苯二甲酸二辛酯,HEPA检漏用的气溶胶PAO:聚-α-烯烃,HEPA检漏用的气溶胶IBC(I ntermediateBulkContainer):中型散装容器BFS(Blowing Filling and Sealing):吹-灌-封PAT(Process Analytical Technology):过程分析技术PLC(Programmable Logic Controller):可编程逻辑控制CPP(Critical Process Parameters):关键工艺参数FBD(Fluid Bed Dryer):流化床AHU(Air Handling Unit):空气处理单元SAT(SiteAcceptance Test):现场验收测试FAT(Factory Acceptance Test):工厂验收测试。
部分医药行业术语

部分制药行相关业术语一、GMP是英文GOOD MANUFACTURING PRACTICE 的缩写,中文含义是“产品生产质量管理规范”。
是一套适用于制药、食品等行业的强制性标准,要求企业从原料、人员、设施设备、生产过程、包装运输、质量控制等方面按国家有关法规达到卫生质量要求,形成一套可操作的作业规范帮助企业改善企业卫生环境,及时发现生产过程中存在的问题,加以改善。
简要的说,GMP要求制药、食品等生产企业应具备良好的生产设备,合理的生产过程,完善的质量管理和严格的检测系统,确保最终产品质量(包括食品安全卫生)符合法规要求。
二、GSP是英文Good Supply Practice的缩写,意即良好供应规范,是控制医药商品流通环节所有可能发生质量事故的因素从而防止质量事故发生的一整套管理程序,医药商品在其生产、经营和销售的全过程中,由于内外因素作用,随时都有可能发生质量问题,必须在所有这些环节上采取严格措施,才能从根本上保证医药商品质量。
GSP是《药品经营质量管理规范》的英文缩写,是药品经营企业统一的质量管理准则。
药品经营企业应在药品监督管理部门规定的时间内达到GSP要求,并通过认证取得认证证书。
三、GAP “良好农业规范(Good Agricultural Practices,简称GAP)”,是1997年欧洲零售商农产品工作组(EUREP)在零售商的倡导下提出了;2001年EUREP秘书处首次将EUREPGAP标准对外公开发布。
四、SOP是Standard Operation Procedure三个单词中首字母的大写,即标准作业程序,就是将某一事件的标准操作步骤和要求以统一的格式描述出来,用来指导和规范日常的工作。
SOP是标准操作程序(Standard Operation Procedure) 的英文首字母缩写。
从对SOP的上述基本界定来看,SOP具有以下一些内在的特征:SOP是一种标准的作业程序。
SOP不是单个的,是一个体系。
医药研发术语大全

医药研发术语大全1、医药外包(CXO):按产业链环节主要分为:CRO, CMO/CDMO、CSO三个环节,分别服务于医药行业的研发、生产、销售三大环节,可简单理解为研发外包、生产外包、销售外包。
2、新药研发合同外包服务机构(Contract Research Organization,CRO)英文全称Contract Research Organization(CRO),是新药研发合同外包服务机构。
主要通过合同形式向制药企业提供新药临床研究服务的专业公司。
CRO可在短时间内组织起一个具有高度专业化的和具有丰富临床经验的临床研究队伍,并能降低整个制药企业的管理费用。
3、合同生产组织(Contract Manufacturing Organization,CMO):接受制药公司的委托,提供产品生产时所需要的各种服务。
4、合同研发生产组织(Contract Development and Manufacturing Organization,CDMO):Contract Development and Manufacturing Organization, 指的是在医疗领域中定制、研发与生产,是一种在医疗领域新出现的研发外包模式。
它与企业在各个环节深度对接,从临床前的研究到临床试验,最终上市商业化生产销售,为企业带来了更规模化的生产过程与服务,工艺研发方面也为企业带来了不少创新。
CRO主要为跨国制药公司和生物制药提供药物发现、临床前研究、临床试验等新药研发合同研究服务;而CDMO是医药合同定制研发生产企业,主要为跨国制药企业以及生物技术公司提供医药,特别是创新的工艺研发及制备、工艺优化、注册和验证批生产等,定制研发生产服务的机构。
CDMO以工艺为核心,原材料投入占比最大。
5、合同销售外包服务商(Contract Sales Organization,CSO):CSO:Contract Sales Organization,合同销售外包服务商,接受制药企业、药品销售权所有人的委托,提供药物销售、市场营销服务。
制药行业术语及药政、行业组织简称
5
FDA
Food and Drug Administration(US)
美国食品药品监督管理局
首字母
G
1
GAMP
Good Automated Manufacturing Practice
优良自动化生产管理规范
2
GC
Gas Chromatography
气相色谱
3
GCP
Good Clinical Practice
影响评估
2
IND
Investigational New Drug
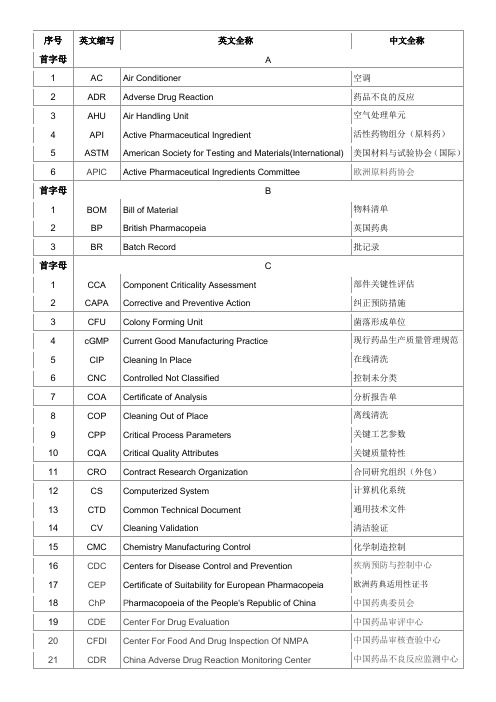
序号
英文缩写
英文全称
中文全称
首字母
A
1
AC
Air Conditioner
空调
2
ADR
Adverse Drug Reaction
药品不良的反应
3
AHU
Air Handling Unit
空气处理单元
4
API
Active Pharmaceutical Ingredient
活性药物组分(原料药)
5
ASTM
American Society for Testing and Materials(International)
药品经营质量管理规范
首字母
H
1
HACCP
Hazard Analysis and Critical Control Point
危害分析和关键环节控制点
2
HAZOP
Hazard and Operability Analysis
危害与可操作性分析
3
HEPA
High Efficiency Particulate Air
全球制药术语英汉双解词典

全球制药术语英汉双解词典全球制药术语英汉双解词典一、药品分类1. Over-the-counter drugs(OTC药品):指非处方药,可以在药店等地方自由购买并使用。
2. Prescription drugs(处方药):指需要医生处方才能购买和使用的药品。
3. Generic drugs(普通药品):指与特定品牌药物成分相同的非专利药物。
4. Brand-name drugs(品牌药品):指由公司拥有专利保护并使用特定商标名称销售的药品。
二、药品生产、研发和注册1. Active ingredient(活性成分):指制备药物的主要成分。
2. Formulation(配方):指药物中的各种成分的比例和方法。
3. Pharmacokinetics(药代动力学):指药物在体内的吸收、分布、代谢和排泄过程。
4. Good Manufacturing Practice(GMP):指药品制造过程中遵守的良好生产规范。
5. Clinical trials(临床试验):指药物在人体中进行的测试以评估其安全性和有效性。
6. New drug application(新药申请):指药物研发完成后,向监管机构提交的申请文件。
7. Biologics License Application(生物制品许可申请):指生物制品(如疫苗和生物仿制药)上市许可的申请文件。
三、药品销售和市场营销1. Formulary(药品名录):指医保计划或医疗机构批准使用的药品列表。
2. Pharmacy benefit manager(药店福利管理员):指为保险公司管理处方药福利计划的公司。
3. Detailing(详细介绍):指制药公司代表向医生详细介绍其产品的做法。
4. Direct-to-consumer advertising(直接面向消费者的广告):指制药公司直接向消费者推销药品的广告活动。
5. Off-label use(离标用药):指医生开处方让患者使用药物的用途与药品标签上所规定的不同。
制药行业术语中英文对照

欢迎阅读术语表AcceptanceCriteria –接受标准:接受测试结果的数字限度、范围或其他合适的量度标准。
ActivePharmaceuticalIngredient (API )(orDrugSubstance )-活性要用成分(原料药)旨在用于药品制造中的任何一种物质或物质的混合物,而且在用于制药时,Batch (/或符号的微生物的水平和种类(例如,治病的或不治病的)。
生物负载不应当当作污染,除非含量超标,或者测得治病生物。
Calibration –校验:证明某个仪器或装置在一适当的量程范围内测得的结果与一参照物,或可追溯的标准相比在规定限度内。
ComputerSystem–计算机系统:设计安装用于执行某一项或一组功能的一组硬件元件和关联的软件。
ComputerizedSystem–计算机化系统与计算机系统整合的一个工艺或操作。
Contamination–污染:在生产、取样、包装或重新包装、贮存或运输过程中,具化学或微生物性质的杂质或外来物质进入或沾染原料、中间体或原料药。
CriticalDrug()调节工艺和/或保证中间体或原料药符合其规格而进行的检查。
Intermediate–中间体:原料药工艺步骤中生产的、必须经过进一步分子变化或精制才能成为原料药的一种物料。
中间体可以分离或不分离。
Manufacture–制造:物料的接收、原料药的生产、包装、重新包装、贴签、重新贴签、质量控制、放行、贮存和分发以及相关控制的所有操作。
Material–物料:原料(起始物料,试剂,溶剂),工艺辅助用品,中间体,原料药和包装及贴签材料的统称。
MotherLiquor–母液:结晶或分离后剩下的残留液。
母液可能含有未反应的物料、中间体、不同级别的原料药和/或杂质。
它可用于进一步加工。
PackagingMaterial–包装材料:在储运过程中保护中间体或原料药的任何物料。
QualityUnit(s)-质量部门:独立与生产部门的履行质量保证和质量控制职责的组织机构。
医药术语MDJN

医药术语MDJNfda:是食品药品监督管理局(food and drug administration)的简称。
fda有时也代表美国食品药品监督管理局。
cfda:中华人民共和国国家食品药品监督管理总局(cfda),现在改成了nmpa。
nmpa:国家药品监督管理局,药品、食品、化妆品、医疗器械。
ich:ich ( international conference on harmonization )为英文国际协调会议的缩写,根据协调会议的内容,中文通常译为“人用药品注册技术要求国际协调会议”。
ich 的目的是协调各国的药品注册技要求(包括统一标准、检测要求、数据收集及报告格式),使药品生产厂家能够用统一的注册资料,按照ich 的有效性、质量、安全性及多学科指南申报。
gxp:生产gmp 经营gsp 中药gap 非临床glp 临床gcp等,x 指泛指。
gmp:( good manufacturing practice) 药品生产质量管理规范gmp是一套适用于制药、食品等行业的强制性标准,要求企业从原料、人员、设施设备、生产过程、包装运输、质量控制等方面按国家有关法规达到卫生质量要求,形成一套可操作的作业规范帮助企业改善企业卫生环境,及时发现生产过程中存在的问题,加以改善。
glp: (good laboratory practice)药品非临床研究质量管理规范glp旨在严格控制化学品安全性评价试验的各个环节,确保试验结果的准确性,促进试验质量的提高,提高登记、许可评审的科学性、正确性和公正性gcp: (good clinical practice)药品临床研究质量管理规范gcp即药物临床试验质量管理规范,是临床试验全过程的标准规定,包括方案设计、组织实施、监查、稽查、记录、分析总结和报告。
gsp: (good supply practice)药品经营质量管理规范gsp是控制医药商品流通环节所有可能发生质量事故的因素从而防止质量事故发生的一整套管理程序,医药商品在其生产、经营和销售的全过程中,由于内外因素作用,随时都有可能发生质量问题,必须在所有这些环节上采取严格措施,才能从根本上保证医药商品质量。
制药行业术语及药政、行业组织简称

7
ISO
International Standard Organization
国际标准化组织
8
ISPE
International Society for Pharmaceutical Engineering
国际制药工程协会
9
ICH
International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use
影响评估
2
IND
Investigational New Drug
临床研究申请
3
INN
International Non-proprietary Name
国家非专利名
4
IPC
In-process Controls
过程控制
5
IQ
Installation Qualification
安装确认
6
IR
Infrared Spectrophotometer
系统影响评估
4
SIP
Sterilize In Place (Steam In Place )
在线灭菌
5
SM
Starting Material
起始物料
6
SMF
Site Master File
工厂主文件
7
SMP
Standard Management Procedure
标准管理程序
8
SOP
Standard Operating Procedure
制药行业词汇总结

制药行业词汇总结FDA(Food and drug administration):(美国国家)食品药品品管理局IND(Investigation new drug):临床研究申请(指申报阶段,相对于NDA而言);研究中的新药(指新药开发阶段,相对于新药而言,即临床前研究结束)NDA(New drug application):新药申请ANDA(Abbreviated New drug application):简化新药申请EP诉(Export application):出口药申请(申请出口不被批准在美国销售的药品)Treatment IND:研究中的新药用于治疗Abbreviated New drug:简化申请的新药DMF(Drug master file):药物主文件(持有者为谨慎起见而准备的保密资料,可以包括一个或多个人用药物在制备、加工、包装和贮存过程中所及的设备、生产过程或物品。
只有在DMF持有者或授权代表以授权书的形式授权给FDA,FDA在审查IND、NDA、ANDA时才能参考其内容)Holder:DMF持有者CFR(Code of federal regulation):(美国)联邦法规Panel:专家小组Batch production:批量生产;分批生产Batch production records:生产批号记录Post-or Pre-market surveillance:销售前或销售后监督Informed consent:知情同意(患者对治疗或受试者对医疗试验了解后表示同意接受治疗或试验)Prescription drug:处方药OTC drug(over—the—counter drug):非处方药U.S.Public Health Service:美国卫生福利部NIH(NATIONAL INSTITUTE OF HEALTH):(美国)全国卫生研究所Clinical trial:临床试验Animal trial:动物试验Accelerated approval:加速批准Standard drug:标准药物Investigator:研究人员;调研人员Preparing and Submitting:起草和申报Submission:申报;递交Benefit(S):受益Risk (S):受害Drug substance:原料药Established name:确定的名称Generic name:非专利名称Proprietary name:专有名称;INN(international nonproprietary name):国际非专有名称Narrative summary记叙体概要Adverse effect:副作用Adverse reaction:不良反应Archival copy:存档用副本Review copy:审查用副本Official compendium:法定药典(主要指USP、NF).USP(The united states Pharmacopeia):美国药典(现已和NF合并一起出版)NF(National formulary):(美国)国家药品集OFFICIAL=Pharmacopeia = COMPENDIAL:药典的;法定的;官方的Agency:审理部门(指FDA等)Sponsor:主办者(指负责并着手临床研究者)Identity:真伪;鉴别;特性Strength:规格;规格含量(每一剂量单位所含有效成分的量)Labeled amount:标示量Regulatory specification:质量管理规格标准(NDA提供)Regulatory methodology:质量管理方法(FDA用于考核原料药或药物产品是否符合批准了的质量管理规格标准的整套步骤)Regulatory methods validation:管理用分析方法的验证(FDA对NDA提供的方法进行验证)Dietary supplement:食用补充品COS/CEP欧洲药典符合性认证ICH(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use)人用药物注册技术要求国际协调会议Acceptance Criteria:接收标准(接收测试结果的数字限度、范围或其它合适的量度标准)Active Pharmaceutical Ingredient (API) (or Drug Substance):活性药用成分(原料药)旨在用于药品制造中的任何一种物质或物质的混合物,而且在用于制药时,成为药品的一种活性成分。
制药行业术语中英文对照之欧阳道创编

术语表Acceptance Criteria–接受标准:接受测试结果的数字限度、范围或其他合适的量度标准。
Active Pharmaceutical Ingredient(API)(or Drug Substance)-活性要用成分(原料药)旨在用于药品制造中的任何一种物质或物质的混合物,而且在用于制药时,成为药品的一种活性成分。
此种物质在疾病的诊断,治疗,症状缓解,处理或疾病的预防中有药理活性或其他直接作用,或者能影响机体的功能和结构。
API Starting Material–原料药的起始物料:用在原料药生产中的,以主要结构单元被并入该原料药的原料、中间体或原料药。
原料药的起始物料可能是在市场上有售,能够根据合同或商业协议从一个或多个供应商处购得,或者自己生产。
原料药的起始物料通常有特定的化学特性和结构。
Batch(or Lot)-批:有一个或一系列工艺过程生产的一定数量的物料,因此在规定的限度内是均一的。
在连续生产中,一批可能对应与生产的某以特定部分。
其批量可规定为一个固定数量,或在固定时间间隔内生产的数量。
Batch Number(or Lot Number)-批号用于标识一批的一个数字、字母和/或符号的唯一组合,从中可确定生产和销售的历史。
Bioburden–生物负载:可能存在与原料、原料药的起始物料、中间体或原料药中的微生物的水平和种类(例如,治病的或不治病的)。
生物负载不应当当作污染,除非含量超标,或者测得治病生物。
Calibration–校验:证明某个仪器或装置在一适当的量程范围内测得的结果与一参照物,或可追溯的标准相比在规定限度内。
Computer System–计算机系统:设计安装用于执行某一项或一组功能的一组硬件元件和关联的软件。
Computerized System–计算机化系统与计算机系统整合的一个工艺或操作。
Contamination–污染:在生产、取样、包装或重新包装、贮存或运输过程中,具化学或微生物性质的杂质或外来物质进入或沾染原料、中间体或原料药。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
制药行业术语和英文简称
名词解释
NDA : New Drug Application /新药生产上市申请
INDA : Investigational New Drug Application/药品临床试验申报
ANDA: Abbreviated New Drug Application/仿制药及改剂型申请
提出申请快速通道资格认定(Request for Fast Track Designation)
Accelerated Approval(加速审批): These regulations allowed drugs for serious conditions that filled an unmet medical need to be approved based on a surrogate endpoint.
Breakthrough Therapy Designations(突破性疗法资格认定): A process designed to expedite the development and review of drugs which may demonstrate substantial improvement over available therapy.
Fast Track Designation(快速通道资格认定): Fast track is a process designed to facilitate the development, and expedite the review of drugs to treat serious conditions and fill an unmet medical need.
Priority Review(优先审核): A Priority Review designation means FDA’s goal is to take action on an application within 6 months.
Orphan Drug Act(罕见疾病药物法案):也叫孤儿药
注册1类和2类新药要进行新药临床试验申请(INDA);
3类和4类要做验证性临床。
完成临床试验后进行新药生产上市申请(NDA)。
仿制及改剂型申请(ANDA)为5类和6类的生物等效试验申请和生产上市申请。
至于验证性试验其实对应的是探索性试验,这两个概念指药物开发的试验,而且其概念也不是绝对化的。
phase I 和II基本属于探索性试验阶段,Phase III 和IV基本属于验证性试验阶段。
所谓验证性试验,是对已经获得的初步的治疗作用进行确证的试验。
一般包括注册分类3的药物及创新药物的III期临床实验。
在创新性药物的临床试验中,Ⅲ期临床试验正是验证性的研究,是对I 和Ⅱ期临床试验探索出的初步的治疗作用进行验证。
此外Ⅲ期临床试验还有一个重要的目的是对药物的安全性的研究,因此它需要有更大的样本量。
