2018广州二模化学试题(定稿)(2)
广东省梅县松口中学2019届高三化学二轮专题复习专题三阿伏伽德罗常数

松口中学2019届高三化学二轮复习专题3 阿伏伽德罗常数
1.(2018广东)设N A为阿伏加德罗常数的数值,下列说法正确的是A.16g CH4中含有4N A个C-H键
B.1mol·L-1 NaCl溶液含有N A个Na+
C.1mol Cu和足量稀硝酸反应产生N A个NO分子
D.常温常压下,22.4L CO2中含有N A个CO2分子
2.(2018广东)设n A为阿伏伽德罗常数的数值,下列说法正确的是
A.常温下,23g NO2含有n A个氧原子
B.1L0.1mol•L-1的氨水含有0.1n A个OH―
C.常温常压下,22.4LCCl4含有个n A CCl4分子
D.1molFe2+与足量的H2O2溶液反应,转移2n A个电子
3.(2018广东)设n A为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,4g CH4含n A个C—H共价键
B.1 mol Fe与足量稀HNO3反应,转移个2n A个电子
C.1L 0.1 mol/L NaHCO3溶液中含有0.1n A个HCO3—
D.常温常压下,22.4L的NO2和CO2混合气体含有2n A个O原子
4.(2018广东)设N A为阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,8gO2含有4N A个电子
B.1L0.1mol·L-1的氨水中有N A个NH4+
C.标准状况下,22.4L盐酸含有N A个HCl分子
D.1molNa被完全氧化生成Na2O2,失去个2N A电子
5.(2018广东)设N A为阿伏加德罗常数的数值,下列说法正确的是()A.1mol甲苯含有6 N A个C-H键
2023年广东省广州市天河区中考化学二模试卷(含解析)

2023年广东省广州市天河区中考化学二模试卷
1. 下列古代技术中涉及化学变化的是( )
A. 谷物酿酒
B. 手工织布
C. 海水晒盐
D. 水车灌溉
2. 锌锰干电池所用材料如图。下列说法不正确的是( )
A. 该电池体现了石墨、锌的导电性
B. 黄铜(锌铜合金)的硬度比铜大
C. 塑料属于有机合成材料
D. 二氧化锰属于金属材料
3. 下列制作饼干的原料中富含油脂的是( )
A. 精炼植物油
B. 小麦粉
C. 白砂糖
D. 鲜鸡蛋
4. 提高安全意识,规避风险。下列做法正确的是( )
A. 将水加入浓硫酸中配制稀硫酸
B. 燃气泄漏,立刻打开排气扇的电源开关
C. 面粉加工厂、纺织厂标有“严禁烟火”字样或图标
D. 烧碱溶液不慎沾到皮肤上,立即用大量水冲洗,再涂上碳酸氢钠溶液
5. 硒是人体必需的微量元素,其在元素周期表中的信息和原子结构示意图如图。下列说法正确的是( )
A. 硒原子在化学反应中易得到电子变成Se2+
B. 硒原子的核外电子分4层排布
C. 硒的相对原子质量为78.96g
D. 硒属于金属元素
6. 下列有关水的说法不正确的是( )A. 通过蒸馏可以降低水的硬度B. 明矾用于自来水杀菌、消毒
C. 水能溶解很多物质,是一种最常用的溶剂
D. 软水和硬水可用肥皂水区分,产生泡沫多的是软水
7. 2018−2020年我国电力能源结构如表。下列说法不正确的是 ( )
发电量占比形式年份水电
火电
核电
风电
其它
2018年17.19%
5.11% 2.48%
2019年69.57%
5.41%2020年
6.00%
3.35%A. 化石燃料燃烧产生热能 B. 发电量占比:火电>水电>风电>核电C. 水能、风能属于清洁能源
贵阳市2020年高考化学二模考试试卷

贵阳市2020年高考化学二模考试试卷
姓名:________ 班级:________ 成绩:________
一、单选题 (共7题;共14分)
1. (2分) (2018高二上·广州期中) 下列说法错误的是()
A . 化学变化一定伴随能量变化,有能量变化的过程不一定是化学变化
B . 甲烷燃烧时,化学能完全转化为热能
C . 植物燃料燃烧时放出的能量来源于太阳能
D . 旧化学键断裂所吸收的能量大于新化学键形成所放出的能量时,该反应为吸热反应
2. (2分) (2018高二上·嘉兴期中) 下列说法正确的是()
A . 1H2和 2H2表示氢元素的两种核素
B . C60和金刚石互为同素异形体,他们都是分子晶体
C . HOCOOH和CH3COOH互为同系物
D . 丙氨酸CH3CH(NH2)COOH与CH3CH2CH2NO2互为同分异构体
3. (2分) (2016高二下·上饶月考) 设NA为阿伏伽德罗常数的值,下列有关叙述正确的是()
A . 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为1/22.4NA
B . 1 mol甲基(﹣CH3)所含的电子总数为9NA
C . 1 摩尔1,3﹣丁二烯分子中含有C=C双键数为 NA
D . 1 mol碳正离子(CH3+)所含的电子总数为10NA
4. (2分) (2019高二下·慈溪期中) 物质Ⅲ(2,3-二氢苯并呋喃)是一种重要的精细化工原料,其合成的部分流程如下:
下列叙述正确的是()
A . 物质I的分子式为C9H7OBr
B . 可用FeCl3溶液鉴别化合物II 和Ⅲ
课题1 物质的变化和性质(第二课时)课时进阶作业

第一单元走进化学世界
课题1物质的变化和性质(第二课时)
基础提升
1.(2018•黄石)下列描述中,属于物质的化学性质的是()
A.盐酸易挥发B.金属具有导电性
C.酒精易溶于水D.常温下,氮气很稳定
2.(2018•门头沟区二模)下列物质的性质中,属于化学性质的是()A.颜色B.密度C.稳定性D.沸点
3.(2018•乌拉特前旗校级二模)物质的性质决定其用途。下列物质的用途中,主要利用其化学性质的是()
A.石墨棒作干电池电极
B.用汽油除去衣服上的油污
C.用碳素墨水书写文字档案,便于长期保存
D.金刚石用来裁玻璃
4.(2018•南山区校级二模)下列有关物质性质﹣类别﹣用途的对应关系中正确的是()
选项物质性质类别用途
A氢氧化钠具有腐蚀性化学性质制作叶脉书签
B液氮汽化时会吸热物理性质用做保护气
C生石灰遇水放热物理性质用做干燥剂
D活性炭具有吸附性化学性质用做制糖工业脱色A.A B.B C.C D.D
5.(2017秋•简阳市期末)下列物质中的用途与该物质的化学性质有关的是()A.用氢气填充探空气球B.用金刚石切割玻璃
C.用干冰进行人工降雨D.用液氧作火箭助燃材料
6.(2017秋•河口区期末)下列物质的用途主要是由物理性质决定的是()A.用生石灰做食品干燥剂B.用氢氧化钠制作叶脉标签
C.用活性炭吸附甲醛D.用熟石灰改良酸性土壤
7.(2018•重庆)下列用途中,只与物质的物理性质有关的是()
A.氧气作供氧剂B.碳酸钙作补钙剂
C.活性炭作吸附剂D.小苏打作发酵剂
8.(2018•广西)下列物质的性质,属于化学性质的是()
2018年广州二模评分细则生物(2)

参考答案与评分细则
1.C2.D3.B4.C5.D6.B 29.(10分,除说明外,每空2分)
(1)催化淀粉的分解(1分)与合成(1分)
(2)6.6前段磷酸化酶相对活性增高,淀粉含量积累加快(1分),后段磷酸化酶相对活性下降,淀粉含量积累减缓(1分)。(可合并回答)
(3)水稻籽粒细胞中存在酸碱缓冲物质(2分,其他同义表达亦可),能减少H+、OH-的浓度波动,维持pH基本稳定
(4)细胞内基因表达情况发生了变化、由于激素含量的变化影响了细胞代谢、水稻籽粒细胞中代谢产物积累改变了酶的活性等。(答出任一点或其他合理答案均得2分)30.(10分,除说明外,每空2分)
(1)直接(价值)间接
(2)竞争(1分)维持细胞液的高渗透压(1分,其他同义表达亦可),使植物能从土壤中吸水(保持自身水分)(2分),以适应土壤中的高渗透压环境。(3分)
(3)(植物)群落演替
31.(9分,除说明外,每空2分)
(1)153
(2)用A与B品种做亲本进行杂交,得到F1(1分),选取F1中高产植株(1分)自交得F2,将F2置于不同盐碱程度条件下培养(2分,其他同义表达亦可),从中筛选出耐盐碱能力最强的植株(1分)。(或在F2中选取耐盐碱能力最强且高产植株,2分)(5分)32.(10分,除说明外,每空2分)
(1)提高2、4和5(3分,2、4或4、5,2分)
(2)X D X d、X d X d和X d O(3分,答对一个给1分)野生型(雌雄同体):突变型(雌雄同体)=3∶1(2分)
37.(15分,除说明外,每空2分)
(1)粉碎(1分)、干燥(1分)石油醚(1分)
2018年广州二模物理试题含参考答案

a
b
P
2018年广州二模物理试题
二、选择题:本题共8小题,每小题6分,共48分。在每小题给出的四个选项中,第14~18
题只有一项符合题目要求,第19~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。 14.a 、b 两离子从平行板电容器两板间P 处垂直电场入射,运动轨迹如图。若a 、b 的偏转时
间相同,则a 、b 一定相同的物理量是 A .荷质比 B .入射速度 C .入射动能 D .入射动量
15.如图,轻绳的一端系在固定光滑斜面上的O 点,另一端系一小球。给小球一个初速度使
它在斜面上做完整的圆周运动,a 、b 分别为最低点和最高点,则小球 A .重力的瞬时功率始终为零 B .所受的向心力大小不变 C .在b 点的速度不可能为零
D .在a 点所受轻绳拉力一定大于小球重力
16.小球在光滑水平面上以速度v 0做匀速直线运动。某时刻开始小球受到水平恒力F 的作用,
速度先减小后增大,最小速度v 的大小为0.5v 0,则小球 A .可能做圆周运动 B .速度变化越来越快 C .初速度v 0与F 的夹角为60° D .速度最小时,v 与F 垂直
17.如图,同一平面内有两根互相平行的长直导线M 和N ,通有等大反向的电流,该平面内
的a 、b 两点关于导线N 对称,且a 点与两导线的距离相等。若a 点的磁感应强度大小为B ,则下列关于b 点磁感应强度B b 的判断正确的是 A .B B 2b >,方向垂直该平面向里
B .B B 21
b <,方向垂直该平面向外
C .B B B <
【广州二模理科试卷及答案】2018年广州市普通高中毕业班综合测试(二)理科

秘密★启用前 试卷类型:A
2018年广州市普通高中毕业班综合测试(二)
理科数学
2018.4
本试卷共5页,23小题,满分150分。考试用时120分钟。 注意事项:
1.答卷前,考生务必将自己的姓名和考生号、试室号、座位号填写在答题卡上,并用2B 铅笔在答题卡的相应位置填涂考生号。
2.作答选择题时,选出每小题答案后,用2B 铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案。写在本试卷上无效。
3.作答填空题和解答题时,必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答无效。
4.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
一、选择题:本题共12小题,每小题5分,共60分.在每小题给出的四个选项中,只有一
项是符合题目要求的.
1.若
112z =+i , 21z =-
i ,则12z z = A .6
B
C
D 2.已知集合{}2,M x x x =∈Z ≤,{}
2
230N x x x =--<,则M N =
A .(]1,2-
B .[
]1,2- C .{}0,2
D .{}0,1,2
3.执行如图的程序框图, 若输出3
2
y =
,则输入x
A .2log 31-
B .21log 3-
C .21log 3- D
4.若双曲线2222:1x y C a b
-=()0,0a b >>的渐近线与圆()22
21x y -+=相切,则C 的渐近
线方程为 A .13
广东省广州市中考化学二模试卷

广东省广州市中考化学二模试卷
姓名:________ 班级:________ 成绩:________
一、选择题 (共15题;共30分)
1. (2分) (2019九上·郯城期中) 下列变化不属于化学变化的是()
A . 向硫酸铜溶液中滴加氢氧化钠溶液后生成蓝色沉淀
B . 二氧化碳通入澄清石灰水后,澄清的石灰水变浑浊
C . 铁生锈
D . 研碎块状的食盐颗粒
2. (2分) (2018九上·湖南月考) 走进化学实验室,同学们学会了最基本的操作,以下操作正确的是()
A . 点燃酒精灯
B . 取少量液体
C . 加热液体
D . 称取氯化钠
3. (2分) (2018九上·恩阳月考) 从如图获得的结论中,正确的有()
①水是由水分子构成的;
②一个水分子是由一个氧原子和两个氢原子构成的;
③在化学反应前后原子的种类和数目不变;
④在化学反应中分子可再分,原子不能再分了.
A . ①②
B . ①②③
C . ①②④
D . ①②③④
4. (2分) (2016九上·新宁期中) 下列关于水的叙述,错误的是()
A . 冰是由氢元素和氧元素组成
B . 使用无磷洗衣粉有利于保护水资源
C . 电解时,正极产生的气体可以燃烧
D . 净化水的方法有吸附、沉淀、过滤和蒸馏等
5. (2分) (2018九下·福田月考) 关于物质的组成,理解正确的一组是()
A . 盐酸、胆矾、石油、沼气均为混合物
B . 乙醇、氮气、氨气、C60均由分子构成
C . 乙酸、甲烷均含有C,H,O三种元素
D . 构成NaCl、MgO的微粒,核外电子排布均相同
6. (2分) (2017九上·天门期末) 下列情况:①煤燃烧;②工业废气任意排放;③燃放鞭炮;④燃油汽车排放的尾气;⑤氢能源汽车排放的尾气,会引起空气污染的是()
哈尔滨市香坊区中考化学二模试卷

哈尔滨市香坊区中考化学二模试卷
姓名:________ 班级:________ 成绩:________
一、选择题 (共10题;共20分)
1. (2分)(2018·广州模拟) 下列关于水的说法中,正确的是()
A . 河水、海水、自来水、蒸馏水都是混合物
B . 工业上常采用煮沸水的方法来降低水的硬度
C . 活性炭净水器里,活性炭的作用是吸附水中的色素、异味
D . 水资源可以循环使用,没必要担心淡水资源不足
2. (2分)下列有关塑料的说法中,正确的是()
A . 塑料的诞生,极大地方便了人们的生活,所以它对人类只有益处
B . 所有的塑料制品都可用来盛装贮存蔬菜或熟食
C . 塑料制品有质轻、绝缘、耐腐蚀和价格便宜等优点
D . 塑料是由相同的小分子直接聚合而成的
3. (2分)(2019·江汉) 下列物品所用的主要材料中,不属于有机合成材料的是()
A . 不粘锅的聚四氟乙烯内衬
B . 汽车轮胎
C . 无人机的塑料外壳
D . 羊绒外套
4. (2分)在配制100g质量分数为10%的氢氧化钠溶液的过程中,下列操作正确的是()
A . 用量筒量取90mL水时俯视读数
B . 氢氧化钠易潮解,应放在玻璃器皿中称量
C . 用蒸馏水洗涤烧杯后,立即溶解氢氧化钠
D . 实验过程中,用到的玻璃仪器只有烧杯和量筒
5. (2分) (2019九上·河东期中) 关于下列符号或图示的说法正确的是()
① ② ③ ④ ⑤ ⑥
A . ①表示两个氧原子
B . 由⑥可知铬的相对原子质量为52.00g
C . ②和④均表示阳离子
D . ③和⑤表示的元素在形成化合物时通常显-1价
广州市天河区中考化学二模考试试卷

广州市天河区中考化学二模考试试卷
姓名:________ 班级:________ 成绩:________
一、单选题 (共10题;共20分)
1. (2分)(2020·江西模拟) 下列常见变化现象属于化学变化的是()
A . 玻璃破碎
B . 食物腐败
C . 汽油挥发
D . 衣服晾干
2. (2分)下列说法中,错误的是()
A . 为了维护人类生存的环境,应彻底消除温室效应
B . 能产生温室效应的气体除二氧化碳外,还有臭氧、甲烷等
C . “低碳”生活指的是人们在生活中应努力减少二氧化碳的排放
D . 使用太阳能、风能等清洁能源是控制二氧化碳排放的有效措施之一
3. (2分) (2019九上·全椒期中) 图甲是元素周期表中铝元索的部分信息,图乙是铝原子的结构示意图。则下列说法中错误的是()
A . 铝元素原子核内有14个中子
B . 在化学反应中铝原子易失去电子变成Al+3
C . 铝的相对原子质量是26.98
D . 铝元素位于元素周期表中第三周期
4. (2分)(2020·黔东南) 碳酸氢钠(NaHCO3)俗名小苏打,常用作食品加工方面的发酵剂。关于小苏打中碳元素的化合价计算正确的是()
A . -2
B . +2
C . +4
D . +6
5. (2分)(2018·海南模拟) 水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K 时形成的,玻璃态水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的
是()
A . 同温度同质量液态水和玻璃态水,体积不同
B . 玻璃态水不属于氧化物
广州市白云区中考化学二模考试试卷

广州市白云区中考化学二模考试试卷
姓名:________ 班级:________ 成绩:________
一、单选题 (共10题;共20分)
1. (2分)(2019·永州) 下列活动中只涉及物理变化的是()
A . 燃烧液化气炖制排骨
B . 用活性炭吸附冰箱中的异味
C . 用大米、红薯等酿酒
D . 利用熟石灰改良酸性的土壤
2. (2分)(2019·天水) 为建设天蓝地绿水净的美丽天水,下列做法不合理的是()
A . 禁止燃放烟花爆竹
B . 生活垃圾就地焚烧处理
C . 工业废水处理达标后再排放
D . 废旧金属回收再利用
3. (2分) (2020·山西模拟) NASA的火星探测车“好奇号”负责采集火星的土壤样本和岩芯,在盖尔环形山中发现了硼元素。根据硼元素在元素周期表中的信息,下列说法正确的是()
A . 硼的相对原子质量是10.81
B . 硼是一种金属元素
C . 硼原子的最外层电子数是5
D . 硼原子在化学变化中易得电子
4. (2分)某物质X在空气中燃烧的化学方程式为:2X+13O2=8CO2+10H2O,则X的化学式为()
A . C2H5OH
B . H2
C . CH4
D . C4H10
5. (2分)今年5月1日开始,醉酒驾驶机动车辆将被依法追究刑事责任。每100mL血液中酒精含量达到80mg 时即为醉酒(血液的pH约为7.4)。关于醉酒血液的说法正确的是()
A . 该血液中酒精的质量分数为80%
B . 该血液中酒精的溶解度为80
C . 该血液是酒精的饱和溶液
D . 该血液显碱性
6. (2分)下列是厨房中的常见物质,将其分散到水中不能形成溶液的是()
2018年广州二模理综生物试题及答案
2018年广州市普通高中毕业班综合测试(二)
理科综合生物
2018.4 一、选择题:
1.下列对人体浆细胞有关物质迁移途径的描述,错误的是
A.抗体:核糖体→内质网→高尔基体→细胞膜→细胞外
B.编码抗体的mRNA:细胞核→细胞质基质→核糖体
C.葡萄糖:细胞外→细胞膜→细胞质基质→线粒体
D.O2:细胞外→细胞膜→细胞质基质→线粒体
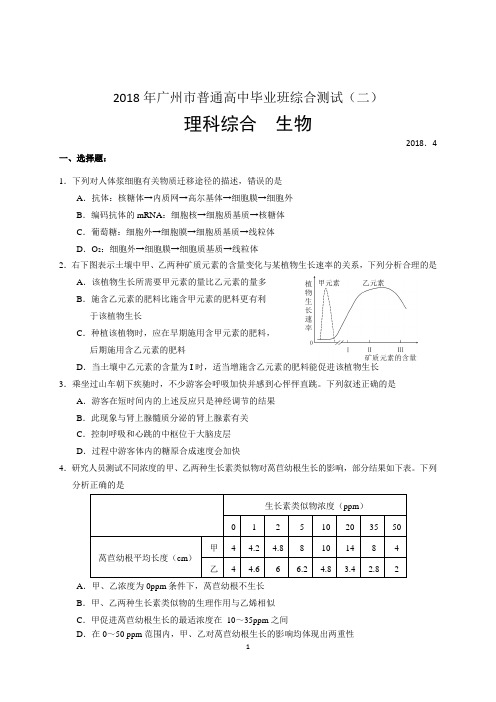
2.右下图表示土壤中甲、乙两种矿质元素的含量变化与某植物生长速率的关系,下列分析合理的是
A.该植物生长所需要甲元素的量比乙元素的量多
B.施含乙元素的肥料比施含甲元素的肥料更有利
于该植物生长
C.种植该植物时,应在早期施用含甲元素的肥料,
后期施用含乙元素的肥料
D.当土壤中乙元素的含量为I时,适当增施含乙元素的肥料能促进该植物生长
3.乘坐过山车朝下疾驰时,不少游客会呼吸加快并感到心怦怦直跳。下列叙述正确的是A.游客在短时间内的上述反应只是神经调节的结果
B.此现象与肾上腺髓质分泌的肾上腺素有关
C.控制呼吸和心跳的中枢位于大脑皮层
D.过程中游客体内的糖原合成速度会加快
4.研究人员测试不同浓度的甲、乙两种生长素类似物对莴苣幼根生长的影响,部分结果如下表。下列分析正确的是
生长素类似物浓度(ppm)
0 1 2 5 10 20 35 50
甲 4 4.2 4.8 8 10 14 8 4 莴苣幼根平均长度(cm)
乙 4 4.6 6 6.2 4.8 3.4 2.8 2 A.甲、乙浓度为0ppm条件下,莴苣幼根不生长
B.甲、乙两种生长素类似物的生理作用与乙烯相似
C.甲促进莴苣幼根生长的最适浓度在10~35ppm之间
广东省揭阳市九年级化学二模考试试卷

广东省揭阳市九年级化学二模考试试卷
姓名:________ 班级:________ 成绩:________
一、选择填充题 (共14题;共28分)
1. (2分) (2018九上·玉溪期末) 下列变化中,属于物理变化的是()
A . 煤气燃烧
B . 钢铁生锈
C . 葡萄酿酒
D . 酒精挥发
2. (2分)(2019·广州) 煤和燃油的燃烧是造成空气污染的重婴原因,下列排放物能形成酸雨的是()
A . SO2、NO2
B . CO、CO2
C . 烟尘
D . 未充分燃烧的汽油
3. (2分) (2018九上·怀柔期末) 下列实验操作正确的是()
A . 点燃酒精灯
B . 倾倒液体
C . 称量固体
D . 过滤
4. (2分) (2019九上·和平期中) 下列物质按照混合物、氧化物、单质顺序排列的是()
A . 空气、二氧化锰、氧气
B . 海水、氯酸钾、氢气
C . 氧化铁、锰酸钾、水
D . 硫酸铜溶液、高锰酸钾、二氧化碳
5. (2分) (2019八下·尚志期中) 下列图片中不属于化学对人类贡献的是()
A . 二氧化碳制化肥
B . 温室效应造成地球气候异变
C . 干冰用于人工降雨
D . C60用于超导
6. (2分)某学生打算用托盘天平称量
7.5g(1g以下用游码)的蔗糖,称量时,他将药品和砝码位置放颠倒了,待天平平衡后,他所称量的药品实际质量为()
A . 6.5g
B . 7.5g
C . 7.0g
D . 6.0g
7. (2分) (2017九上·阜宁月考) 下列实验基本操作错误的是()
A . 检查装置气密性
B . 点燃酒精灯
2018年高考化学苏教版一轮复习配套课时作业20 Word版含解析

课时作业(二十)
1.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是()
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池溶液的总质量增加
C.电池工作一段时间后,乙池的c(Zn2+)>c(SO2-4)
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡答案:B解析:由图像可知,该原电池反应式为:Zn+Cu2+===Zn2++Cu,Zn为负极,发生氧化反应,Cu为正极,发生还原反应,故A错误;乙池中的Zn2+通过阳离子交换膜进入甲池,甲池中发生反应:Cu2++2e-===Cu,保持溶液呈电中性,进入甲池的Zn2+与放电的Cu2+的物质的量相等,而Zn的摩尔质量大于Cu的摩尔质量,故甲池溶液总质量增大,故B正确;原电池工作时乙池中进入甲池Zn2+和溶解进入溶液里Zn2+的物质的量相等,保证乙池溶液里c(Zn2+)=c(SO2-4),故C错误;乙池中的Zn2+通过阳离子交换膜进入甲池,以保持溶液电荷守恒,阴离子不能通过阳离子交换膜,故D错误。
2.[2017·广州二模]某小组为研究原电池原理,设计了如图装置,下列叙述正确的是()
A.若X为Fe,Y为Cu,铁为正极
B.若X为Fe,Y为Cu,电子由铜片流向铁片
C.若X为Fe,Y为C,碳棒上有红色固体析出
D.若X为Cu,Y为Zn,锌片发生还原反应
答案:C解析:Fe比Cu活泼,Fe作负极,电子从Fe流向Cu,故A、B 两项错误;若X为Fe,Y为C,电解质溶液为硫酸铜,则正极C上析出Cu,故C正确;Zn比Cu活泼,Zn作负极发生氧化反应,故D错误。
2018广州二模地理试题及答案
2018年广州市普通高中毕业班综合测试(二)
文科综合(地理)
一、选择题:
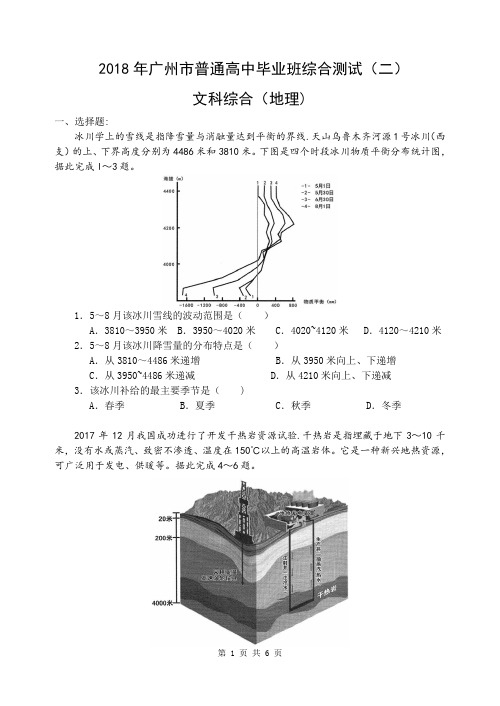
冰川学上的雪线是指降雪量与消融量达到平衡的界线.天山乌鲁木齐河源1号冰川(西支)的上、下界高度分别为4486米和3810米。下图是四个时段冰川物质平衡分布统计图,据此完成l~3题。
1.5~8月该冰川雪线的波动范围是()
A.3810~3950米 B.3950~4020米 C.4020~4120米 D.4120~4210米2.5~8月该冰川降雪量的分布特点是()
A.从3810~4486米递增 B.从3950米向上、下递增C.从3950~4486米递减 D.从4210米向上、下递减3.该冰川补给的最主要季节是( )
A.春季 B.夏季 C.秋季 D.冬季
2017年12月我国成功进行了开发干热岩资源试验.干热岩是指埋藏于地下3~10千米,没有水或蒸汽、致密不渗透、温度在150℃以上的高温岩体。它是一种新兴地热资源,可广泛用于发电、供暖等。据此完成4~6题。
4.干热岩主要属于()
A.岩浆 B.喷出岩 C.沉积岩 D.侵入岩5.我国干热岩最主要分布在( )
A.东南沿海 B.华北地区 C.西北内陆 D.青藏高原6.与传统地热资源相比,干热岩()
A.开发难度小、成本低 B.埋藏较浅、分布广
C.无季节变化、污染少 D.产业链短、效率低
1946~1964年美国出生婴儿高达7600万人,这个群体被称为“婴儿潮一代".“婴儿潮一代"对美国的政治、经济、文化有着巨大的影响。下图是1970年和2000年美国人口年龄金字塔统计图,据此完成7~8题。
晋城市阳城县九年级下化学期中(二模)考试试卷

晋城市阳城县九年级下化学期中(二模)考试试卷
姓名:________ 班级:________ 成绩:________
一、选择题 (共18题;共37分)
1. (2分) (2015九上·阿拉善盟期中) 地壳中含量最多的元素是()
A . 0
B . Si
C . Fe
D . Al
2. (2分) (2016九下·新化开学考) 下列各组物质中,前者属于混合物,后者属于化合物的是()
A . 食盐食醋
B . 空气甲烷
C . 钢铁氢气
D . 冰水共存物石灰石
3. (2分) 20 g饱和食盐水中加入5 g食盐,保持温度不变,这时食盐水的质量将()
A . 增加5 g
B . 为25 g
C . 为20 g
D . 无法确定
4. (2分)(2018·牙克石模拟) 下列有关生活常识认识错误的是()
A . 我国规定食盐必须加碘,“碘”是指“碘元素”
B . “绿色食品”是指颜色一定是绿色的食品
C . 通常所说的“煤气中毒”是指CO中毒
D . “白色污染”是指某些难以分解的“塑料垃圾”对环境造成的污染
5. (2分)(2018·广州) 下列有关金刚石、石墨的说法正确的是()
A . 都是由碳元素组成
B . 都是黑色固体
C . 都能导电
D . 硬度都很大
6. (2分)含硫元素物质间发生转化:S SO2SO3H2SO4Al2(SO4)3 ,其中硫元素化合价发生变化的是()
A . ①②
B . ③④
C . ①③
D . ②④
7. (2分) (2019九上·新城月考) 中华传统文化博大精深,下列词句中蕴含化学变化的是()
A . 木已成舟
B . 只要功夫深,铁杵磨成针
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
9.下列关于化合
物
的说法正确的是 A.Ⅰ、Ⅱ、Ⅲ、Ⅳ的沸点依次升高 B.Ⅰ、Ⅲ的一氯代物均只有四种 C.Ⅱ、Ⅲ中碳原子可能都处于同一平面 D.Ⅲ、Ⅳ都属于芳香族化合物,互为同系物
10.实验室利用反应 TiO2(s)+CCl4(g) TiCl4(g) +CO2(g),在无水无氧下制取 TiCl4,实 验装置如图所示(CCl4、TiCl4 的沸点分别为:76℃、136℃,CCl4 与 TiCl4 互溶)。下 列说法正确的是
(2)温度为 T1 时,将等物质的量的 CO2 和 H2 充入体积为 1L 的密闭容器中发生反应:
CO2(g)+ H2 (g)
HCOOH(g) K=1
实验测得:v 正=k 正 c(CO2) ·c(H2),v 逆=k 逆 c (HCOOH),k 正、k 逆为速率常数。
①当 HCOOH 的体积分数为 20%时,CO2 的转化率为___________。
Ⅲ.重复步骤Ⅰ、Ⅱ 2~3 次,处理数据。在此过程中:
①实验室中得到标准 NaOH 溶液的方法是 。
②步骤Ⅱ发生反应的离子方程式是 。
③若实验平均消耗 NaOH 溶液的体积为 b mL。NH4ClO4 质量分数的计算式为
。
④实验中使用的甲醛常混有微量甲酸,会导致测定结果偏 (填“高”或“低”)。混有甲酸
石墨烯(图 a)是一种由单层碳原子构成的平面结构新型导电材料,具有大π共轭体 系。石墨烯中部分碳原子被氧化后,其平面结构发生改变,转化为氧化石墨烯(图 b)。
图 a 石墨烯结构
图 b 氧化石墨烯结构
(1)图 a 中,1 号 C 的杂化方式为
,石墨烯中含有的化学键类型是________;图 b
中键角α
A.a 极是电池的负极 B.电池工作时,正极可发生反应:Li1-xFePO4+xLi++xe-=LiFePO4
C.电池充电时间越长,x 值越小
D.电池工作时,外电路中流过 0.1mol 电子,负极材料减重 0.7 g 13.298K 时,向 20 mL 0.1 mol·L-1 二元弱酸 H2A 溶液中滴加 0.1 mol·L-1NaOH 溶液,溶
36.[化学─选修 5:有机化学基础](15 分)
在光的引发下,烯炔的环加成是合成四元环化合物的有效方法。以下是用醛 A 合成一 种环丁烯类化合物 I 的路线图:
已知: ①A 生成 B 的原子利用率为 100%
②
回答以下问题:
(1)A 的名称为
。
(2)由 C 生成 D 和由 F 生成 G 的反应类型分别为 、 。
的原因是 。
27. (14 分)已知氧化锌烟尘主要成分为 ZnO,还含有 PbO、Ag2O、CuO、CdO、GeO2、 MnO、FeO 等。从烟尘中回收锗锌的工艺流程如下:
回答下列问题。
(1)用过量焦炭高温还原 GeO2 的化学方程式为
。
(2)锌粉的作用有:除去铜、镉等杂质、 。
(3)(NH4)2S2O8 中 S 的化合价为+6,则 S2O82-中含过氧键数目为
②T1 时,k 正=_____(以 k 逆表示)。当温度改变为 T2 时,k 正=0.9k 逆,则 T2_____T1
(填“>”、“<” 或“=”)。
(3)用 NaHCO3 代替 CO2 作为碳源有利于实现 CO2 加氢制备甲酸。向反应器中加入
NaHCO3 水溶液、Al 粉、Cu 粉,在 300℃下反应 2h,实验结果如下表。
键角 。(填“>”、“<”或“=”)
(2)五氧化二钒/二氧化钛/石墨烯复合材料可用于新型电池,基态钒原子的价电子排布式
为
;同周期元素中最外层电子数与钛相同的有
种;金属钒和钛熔点较高的是
________,原因是
。
(3)醋酸铜可合成复合材料石墨烯/Cu,其制备原料为 CuSO4、NH3·H2O 和醋酸等。
液中的 H2A、HA-、A2-的物质的量分数 (X) 随 pH 的变化如图所示。下列说法错误的
是
[已知
(X)
c(H2A)
c(X) c(HA )
c(A 2 )
]
A.加入 10 mL NaOH 时,pH=1.9
B.当 c(H2A) = c(A2-),pH=4.55
C.
=105.3
D.当混合溶液呈中性时,c(Na+)>c(HA-)>c(A2-)>c(H+) = c(OH-)
28.(15 分)CO2 加氢制备甲酸(HCOOH)可用于回收利用 CO2。回答下列问题:
(1)已知:C(s)+O2(g) = CO2(g)
△H1=-394 kJ·mol-1
C(s)+H2(g) +O2(g) = HCOOH(g) △H2=-363 kJ·mol-1
反应 CO2(g) +H2(g)
HCOOH(g)的△H=_____________。
转化率影响较大的是________(填“Al”或“Cu”)的用量。当碳转化率为 30%时所采用
的实验条件是_________。
(4)采用电还原法也可将 CO2 转化为甲酸,用 Sn 为阴极、Pt 为阳极,KHCO3 溶液
为电解液进行电解。CO2 应通入
区(填“阳极”或“阴极”),其电极反应式
为
。
35.[化学─选修 3:物质结构与性质](15 分)
A.①、⑤中分别盛装碱石灰、NaOH 溶液 B.②热水的作用是使 CCl4 气化,④冰水的作用是使 TiCl4 冷凝 C.③反应结束,先停止通 N2,再停止加热 D.分离④中的液态混合物,采用的操作是分液 11.W、X、Y、Z 为核电荷数依次增大的前 20 号主族元素,W 的原子中只有 1 个电子,X 与 Y 同族,Y 的一种单质在空气中易自燃,W 与 Z 形成的二元化合物和水反应可生成 W 的单质。下列说法正确的是 A.W 分别与 Y、Z 形成的化合物中化学键类型相同 B.Y 的氧化物的水化物是强酸 C.氢化物沸点:Y>X D.简单离子半径:Y>Z 12.LiFePO4 电池稳定性高、安全、对环境友好,其工作原理如图所示。下列说法错误的 是
2018 年广州市高考模拟测试(二)理综化学
相对原子质量:H 1;Li 7 ; B 11 ;C 12 ;N 14 ;O 16 ;P 31;Cl 35.5;K 39;Fe 56 ;Ge 73
7.化学与生活密切相关。下列对化学事实的解释错误的是
选项
事实
解释
A 粮食酿酒
发生淀粉→葡萄糖→乙醇的化学变化过程
(3)D 生成 F 的化学方程式为
。
(4)I 的分子式为
。
(5)在 I 的合成路线中,互为同分异构体的化合物是
(填化合物代号)。化合物 X
是 H 的同分异构体,其中能遇氯化铁溶液显色,且能发生银镜反应,除苯环外没有其他环
的有 种。
(6)写出用
与乙炔合成
的路线图(其他试剂任选)。 。
锰的离子方程式为 。
。用(NH4)2S2O8 除
(4) “滤液 B”的主要成份为______。“沉锌”中反应的化学方程式为 。
(5)若“滤液 A”中 c(Pb2+)=2×10-9mol·L-1,此时 c(Ag+)= mol·L-1。
(已知:Ksp(PbSO4) =2×10-8mol·L-1,Ksp(Ag2SO4) =1×10-5mol·L-1)
26. (14 分)高氯酸铵(NH4ClO4)是一种优良的固体火箭推进剂。 (1)NH4ClO4 高温分解时产生水蒸气和三种单质气体,从而产生巨大的推动力。 ①三种单质气体的化学式分别为 。 ②利用下图装置对分解产生的三种单质气体进行验证。装置 A、B、C 中所装试剂依次 为 (填标号)。
a. 湿润的淀粉 KI 试纸 b. 湿润的红色布条 c. NaOH 溶液 d. Na2SO3 溶液 e. CuO f. Cu
①写出一种与 SO42-互为等电子体的分子
。
②二聚醋酸铜的结构示意图如下所示,其化学式为
,Cu2+的配位数为______。
(4)石墨烯可转化为富勒烯(C60)。C60 和 K 能形成新型化合物,其晶胞如图所示,晶胞 参数为 a nm。该化合物中 K 原子和 C60 分子的个数比为 ,该晶体的密度ρ= g·cm-3。
汽车排气管上加装“催化转化 使 NO 和 CO 转化为 CO2 和 N2 进行尾气处理 B
器”
C 水中的钢闸门连接电源的负极 利用牺牲阳极的阴极保护法对钢闸门进行防腐
D 纯碱溶液清洗油污
油脂在碱性条件下发生水解反应生成溶于水的 甘油和高级脂肪酸钠
8.NA 为阿伏加德罗常数的值。下列说法正确的是 A.25℃时,pH=1 的 CH3COOH 溶液中含有 H+的数目为 0.1NA B.0.1mol H2(g)和 0.2mol I2(g)于密闭容器中充分反应后,其分子总数为 0.3NA C.0.1mol CH3OH 分子中含有 C-H 键的数目为 0.4NA D.1.1g 的 11B 中含有的中子数 0.5NA
编号
Ⅰ Ⅱ Ⅲ
物质的量/mmol
NaHCO3 Cu Al
2
16 0
2
0 16
2
来自百度文库
16 16
碳转化率/%
0 8.16 29.10
①实验 III 比 II 碳转化率高的原因是__________________________。
②NaHCO3 用量一定时,Al、Cu 的用量对碳转化率影响结果如上图。由图可知,对碳
D
(2)NH4ClO4 的质量分数可通过甲醛法测定。
已知:NH4ClO4 与甲醛反应的离子方程式为:4NH4++6HCHO=(CH2)6N4H++3H++6H2O
(CH2)6N4H+
(CH2)6N4+H+ K=7×10-6
实验步骤:
Ⅰ.取 a g NH4ClO4 产品于锥形瓶中,用水溶解,加入 40mL 甲醛水溶液,充分反应。 Ⅱ.以酚酞作指示剂,用 c mol·L-1 标准 NaOH 溶液滴定。记录数据。
