7 芳烃
7章-芳烃10.4

(CH)x , x>=10
H H HHH
[18][18]-轮烯
H
芳香性
化合物的结构为:环状平面的共轭体系,其 化合物的结构为:环状平面的共轭体系, 平面的共轭体系 中π电子数等于4n+2 (n=0,1,2……)。这个规则 电子数等于4n 4n+ 称为Huckel规则。 称为Huckel规则。 Huckel规则
(Aryl), Ar表示 表示。 三、芳基 (Aryl),用Ar表示。
CH2
C6H5
Ph或φ 或 苯基
phenyl
C6H5CH2 Bz 苯 甲基 或 苄基
benzyl ( phenyl methyl)
第三节 单环芳烃的化学性质
一、亲电取代反应
1. 硝化反应
NO2
H2SO4 55-60 C -
。
+ HONO2
一、休克尔规则(Huckel’s Rule) 休克尔规则(Huckel (Huckel’
1.芳香性 1.芳香性
环丁二烯
环辛四烯
2.含(4n+2)个 2.含(4n+2)个π电子的芳烃实例
环丙烯正离子
萘
蒽
HH
[10]-轮烯 [10]-
H
HH
H
[14][14]-轮烯
轮烯:具有交替的单双键的单环多烯烃 轮烯:
70%
CH3CH2CH2
重排
CH3CHCH3
二、反应不易控制在一元取代阶段,常常得到 反应不易控制在一元取代阶段, 一元、二元、 一元、二元、多元取代产物的混合物
CH3
CH3Cl AlCl3
CH3 CH3 +
CH3
CH3
CH3Cl AlCl3
第七章-芳烃-习题-答案
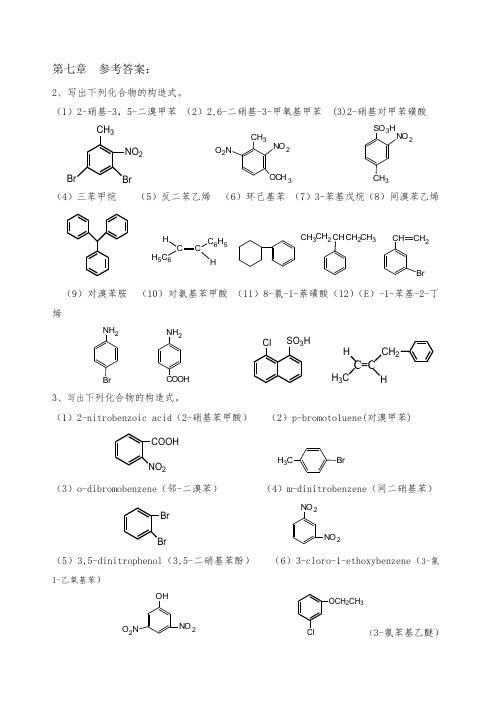
第七章 参考答案:2、写出下列化合物的构造式。
(1)2-硝基-3,5-二溴甲苯 (2)2,6-二硝基-3-甲氧基甲苯 (3)2-硝基对甲苯磺酸CH 3NO 2BrBrCH 3NO 2O 2NOC H 3SO 3HNO 23(4)三苯甲烷 (5)反二苯乙烯 (6)环己基苯 (7)3-苯基戊烷(8)间溴苯乙烯CCC 6H 5H 5C 6HH CH 3CH 2CHCH 2CH 3CHCH 2Br(9)对溴苯胺 (10)对氨基苯甲酸 (11)8-氯-1-萘磺酸(12)(E )-1-苯基-2-丁烯NH 2BrNH 2SO 3HClC=CHHH 3CCH 23、写出下列化合物的构造式。
(1)2-nitrobenzoic acid (2-硝基苯甲酸) (2)p-bromotoluene(对溴甲苯)COOH NO 2CH 3Br(3)o-dibromobenzene (邻-二溴苯) (4)m-dinitrobenzene (间二硝基苯)BrBrNO 2NO 2(5)3,5-dinitrophenol (3,5-二硝基苯酚) (6)3-cloro-1-ethoxybenzene (3-氯1-乙氧基苯)OHNO 2O 2NOCH 2CH 3(3-氯苯基乙醚)(7)2-methyl-3-phenyl-1-butanol (2-甲基-3-苯基1-丁醇)CH 3CHCHCH 2OHCH 3(8)p-chlorobenzenesulfonic acid (对氯苯磺酸)(9)benzyl bromide (苄基溴)SO 3HClCH 2Br(11)o-xyene (邻二甲苯)(12)tert-butylbenzene (叔丁基苯)(13)p-cresol (对甲苯酚)CH 3CH 3C(CH 3)3CH 3OH (14)3-phenylcyclohexanol (3-苯环己醇)(15)2-phenyl-2-butene (16)naphthalene(萘)HO5、写出下列反应的反应物构造式。
第7章 芳烃-1
HF
HO
0°C 62%
BF3 60°C
56%
注意事项:
⑴ 当苯环上具有吸电子基(二类定位基)时不能进行付克反应。如: -+NR3 -NO2、 -CF3 -CCl3 -CN、 -SO3H、 -CHO、 -COR、 -COOH、-COOR …….
O -CCH3 +CH CH Cl 3 2
AlCl3
⑵ 乙烯基与芳基卤不能作为烃基化试剂。
-CH2CH2CH3
O O O AlCl3
COOH
COOH
=
O
PPA
Zn-Hg HCl
HO CH3
S(或Pd)
(1)CH3MgX (2)H2O CH3 1.-H2O
PPA:多聚磷酸 Pd~C:低温催化加氢,高温催化脱氢。
2.Pd/C, -H2
=
O
Zn-Hg HCl
氯甲基化
3
无水ZnCl2 + (HCHO)3 + 3 HCl △
连苯四甲酸
催化氧化:这是工业上合成顺丁烯二酸酐的方法
O
+ 9O2
V2O5 385°~400°C
O O
顺丁烯二酸酐 (马来酸酐)
43
2. 侧链卤代.
CH3 Cl2 -CH2Cl 自由基取代 CH3 亲电取代 Cl
CH3 Cl Fe
-CH2CH3
Br2光照 或NBS
-CHCH3 Br
Cl
Cl , PCl5 CH3 2 h ,△ υ
卤代烷的活性: RI > RBr > RCl
3°> 2°> 1° > CH3X
常用烷基化试剂:R—X RCH=CH2
AlCl3 FeCl3 ZnCl2 SnCl4 AlCl3 H2SO4 H3PO4 HF
16种多环芳烃名称

16种多环芳烃名称编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(16种多环芳烃名称)的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为16种多环芳烃名称的全部内容。
PAHs主要包括16种同类物质:16种常见多环芳香烃1.NAP Naphthalene 萘2 .ANY Acenaphthylene 苊烯3.ANA Acenaphthene 苊4。
FLU Fluorene 芴5。
PHE Phenanthrene 菲6.ANT Anthracene 蒽7。
FLT Fluoranthene 荧蒽8。
PYR Pyrene 芘9.BaA Benzo(a)anthracene 苯并(a)蒽10。
CHR Chrysene 屈11. BbF Benzo(b)fluoranthene 苯并(b)荧蒽12。
BKF Benzo(k)fluoranthene 苯并 (k)荧蒽13。
BaP Benzo(a)pyrene 苯并(a)芘14.IPY Indeno(1,2,3—cd)pyrene 茚苯(1,2,3-cd)芘15.DBA Dibenzo(a,h)anthracene 二苯并(a, n)蒽16.BPE Benzo(g,hi)perylene 苯并(ghi)北(二萘嵌苯)。
有机化学第七章芳香烃习题答案

第七章芳香烃7-1 命名下列各化合物或写出构造式。
(1)5-硝基-1-溴萘(2)9,10-二氯菲(3)4-苯基-2-戊烯(4)(S)-1-苯基-1-溴丙烷(5)4-溴联苯(6)2-蒽磺酸(7)(8)(9)27-2 将下列各组中间体按稳定性由强至弱排列。
(1)A>B>C;(2)B>C>A>D;(3)C>B>A。
7-3 将下列化合物按硝化反应的速率由快至慢排列。
(2)>(4)>(3)>(7)>(5)>(1)>(6)7-3 将下列化合物按与HCl反应的速率由快至慢排列。
(4)>(2)>(1)>(3)7-5 用NMR法鉴别下列各组化合物。
(1)、两个化合物的1H-NMR谱都有三组信号,其中间的信号明显不同,前者是四重峰(2H)、三重峰(3H)和多重峰(5H);而后者是双峰(6H)、多重峰(1H)和多重峰(5H)。
(2)、两者芳环上H的谱图明显不同,前者苯上的4个H是等同的,分子共有二组峰,单峰(6H),双峰(4H);而后者芳环的4个H为AB2C型,对应的谱图(峰)较复杂[单峰(6H)、单峰(1H)和多重峰(3H)]。
7-6 完成下列各反应式。
(1)ClCH2CH(CH3)CH23AlCl3+CH2CH3 CH3CH3OH+++COOH(2)(3)CH3CH22C CCH3CH2C CH HCH3+Cl2hν4H2(4)CH HCHO, HCl, ZnCl2CH3ClH2C CH3CH2Cl(5)+(6)CH CHHNO3/H2SO4CH CH2OH ClOCH3OCH3OCH3NO2NO2V 2O 5+NO 2O 2C O C NO 2OO(7)2HNO 3/H 2SO 4NO 2O 2N(8)AlCl 3+(9)(CH 3)2C=CH 2H 2SO 4CH 2H 3COH 3CO CH 3(10)H 3COCH CH 2COClCH 2H 3COH 3COCH CH 2C O H 3COCH 3(H 3C)3C3+(CH 3)3Cl+浓H 24(11)O OOOOOCH 3CH 3CH 3CH 3C(CH 3)3SO 3H(12)(13)+CH 3CH 3(H 3C)3C (热力学控制产物)(主)(主)7-7 用苯、甲苯或萘为主要原料合成下列化合物。
有机化学第七章 芳烃

H
H
H
H
H
H
可以解释:为什么苯分子特别稳定? 为什么苯分子中碳碳键长完全等同? 为什么邻位二取代物只有一种?
(b)分子轨道理论 分子轨道理论认为:苯分子形成σ键后,苯的
六个碳原子上的六个P 轨道经线性组合可以形成六 个分子轨道,其中ψ1 、ψ2 和ψ3 是成键轨道,ψ4、 ψ5和 ψ6是反键轨道。当苯分子处于基态时六个电 子填满三个成键轨道,反键轨道则是空的。
-络合物
(b)硝化反应
2 H2SO4 HNO3
NO2
HNO3 H2SO4,45℃
CH3
HNO3 H2SO4,30℃
NO2
CH3 NO2
CH3
NO2
HNO3 H2SO4,95℃
NO2
NO2
NO2
H3O 2 HSO4
反应比苯容易 反应比苯困难
硝化反应机理
硝化反应中进攻试剂是NO2+,浓硫酸的作 用促进NO2+的生成:
苯环的特殊稳定性可以从它具有较低的氢化热 得到证明:
环己三烯氢化热=360kj/mol(假想值) 苯环氢化热=208kj/mol 相差152kj/mol
氢化热简图:
环己三烯+3H2
环己二烯+2H2
苯+3H2
环己烯+H2
231kj/mol
120kj/mol
208kj/mol
360kj/mol
环己烷
苯分子的近代概念
ቤተ መጻሕፍቲ ባይዱ
(1)煤的干馏
煤隔绝空气加热至1000~1300℃时分解所得到的 液态产物——煤焦油,其中含有大量芳烃化合物。 再经分馏得到各类芳烃。
馏分名称 轻油 酚油 萘油 洗油 蒽油
7 第七章 芳烃
本章主要内容:
第 7 章 芳 香 烃
7.1 芳烃的芳香性及分类 7.1.1 芳香烃和 和芳香性
芳香烃:
苯及同系物、多苯环化合物及具有类似苯环结构和性质的 烃类化合物 称为芳 芳香碳氢化合物,简称芳香烃 芳香烃 或 芳烃。 碳氢化合物 芳烃 芳烃的官能团 芳环, 芳烃去氢后的取代基 芳基 (Ar-)。
二苯甲烷
三苯甲烷
(E)-1,2-二苯乙烯
萘
2-甲基萘
2-乙基蒽
3. 非苯芳烃:分子中不含苯环,但具有芳香性的碳氢化合物 称为非苯芳烃。 实例:
菲
并四苯
芘
苯
甲苯
对二甲苯
间甲基异丙苯
(2) 联环芳烃
芳环通过单键直接相连得到的多环芳烃。
【18】-轮烯 环戊二烯负离子 环庚三烯正离子
特点:单环,平面结构,环上有 4n+2 个π 电子
思考:二甲苯三种异构体中, 邻二甲苯的沸点最高,对二甲苯对熔点最高?
17
7.3.2
沸点 熔点
苯的同系物中每增加一个 -CH2-单位,沸点平均 增高约 20-30 ℃。
16
沸 点
如: 苯、甲苯、乙苯、正丙苯和正丁苯的沸点分别 为 80.1 ℃, 110.6 ℃,136 ℃,159.2 ℃和 183 ℃。
+ Cl2
FeCl3
Cl
Cl
+
Cl
24
在卤化反应中,铁粉也能起到催化剂的作用。
X
苯与卤素的反应的活性顺序:
氟>氯>溴>碘
苯与氟的反应过于激烈,很难控制,一般不用; 苯与碘的反应太慢, 需要在氧化剂(HNO3)存在下进行, 一般也不用。 氯的反应活性大于溴的反应活性,但溴化产物的选择性 比氯化产物高。取代苯的溴化产物,以对位产物为主。
第7章 芳烃及非苯芳烃

CH2CH2CH3
4)与烷基化相同,当苯环上有强吸电子基时,难发 生酰基化反应。
2020/4/19
39
(二)加成反应(P180)
与不饱和烃相比,芳烃要稳定得多,只有在 特殊的条件下才发生加成反应。
1.加氢
Ni or Pd or Pt + 3 H2 180--250 C
2.与氯加成
2020/4/19
CH(CH3)2
+ CH3CH2 CH2
95 C
CH3
H2SO4
+ CH3C CH2
or (CH3)3COH
C(CH3)3
2020/4/19
34
➢烷基化的异构(碳正离子的重排)
当烷基化试剂有较长碳链(C≥3)时,在反应中会发生异构化
一级正丙基正离子重排为 更稳定的二级异丙基正离子:
CH3CHCH2 重排 CH3CHCH3 H
环庚三烯正离子
(卓艹 正离子)
+
π电子数 = 6 符合4n+2 有芳香性
2020/4/19
15
例:判断下列化合物是否具有芳香性?
8e 无 6e 无 6e有 2e无 无 2e有
4e无 4e无
5e 无 6e有
12e 无
8e 无
10e 有
2020/4/19 CH2=CH-CH=CH-CH=CH2 6e 无
3
凯库勒(KekuléF A 1829-1896)
德国有机化学化学家,苯环结构创始人。 大学时学建筑,受有机化学家李比希的影响改 学化学,由著名梦幻“蛇头尾相咬” 悟出苯环 的结构。 “一天,我坐马车回家,由于过度的 劳累,我在摇摇晃晃的马车上很快就睡着了。 我做了一个梦,梦见我几个月来设想过的种种 苯的分子结构式,在我的眼前跳舞。忽然,其 中有一个分子结构式变成了一条蛇,这蛇首尾 相衔,变成一个环。当天晚上,我在这个梦的 启发下,终于画出了首尾相接的环式分子结构, 解决了有机化学上的这一难题。”
《有机化学》第7章 芳香烃

所以如果希望获得所需的产物,使用正确的反应步骤是重要的。
2023/6/13
18
第三节 稠环芳烃
一、 萘
萘,分子式C10H8,光亮的片状结构,熔点80.2 ℃,沸点218 ℃,有特殊气味,易 升华,不溶于水,易溶于乙醇、乙醚、苯等有机溶剂。其化学性质与苯相似。
2023/6/13
11
⑷ 傅-克(Friedel-Crafts)反应 ① 烷基化反应 凡在有机化合物分子中引入烷基的反应,称为烷基化反应。反
应中提供烷基的试剂叫烷基化剂,它可以是卤代烷、烯烃和醇。
当烷基化剂含有三个或三个以上直链碳原子时,产物发生碳链异构。
② 酰基化反应 凡在有机化合物分子中引入酰基(
①若原有两个取代基不是同一类的,则第三个取代基进入的位置一般受邻、对 位定位基的支配,因为邻、对位基反应的速率大于间位基。
②若原有两个取代基是同一类的,则第三个取代基进入的位置主要受强的定位基 的支配。
2023/6/13
17
⑵ 选择适当的合成路线
例如:由甲苯制备对硝基苯甲酸。
比较这两个结构,反应步骤必须是先硝化,后侧链氧化。
1.取代反应
在萘环上,p电子的离域并不像苯环那样完全平均化,而是在α-碳原子上的电子 云密度较高,β-碳原子上次之,中间共用的两个碳原子上更小,因此亲电取代反应 一般发生在α位。
⑴ 卤化反应
在Fe或FeCl3存在下,将Cl2 通入萘的苯溶液中,主要得到α-氯萘。α-氯萘为无 色液体,沸点259 ℃,可做高沸点溶剂和增塑剂。
2023/6/13
6
苯分子去掉一个氢原子后的基团(C6H5―)叫做苯基,也可以用Ph―代 表。芳烃分子的芳环上去掉一个氢原子后的基团叫做芳基,可用Ar―代表。甲 苯分子中苯环上去掉一个氢原子后所得的基团CH3C6H5―称甲苯基;如果甲苯 的甲基上去掉一个氢原子,C6H5CH2―称苯甲基,又称苄基。
有机化学第七章 芳烃

1
一、教学目的和要求 通过对本章的学习,掌握芳烃的定义、分类、苯的结构、 闭合共轭体系、芳香性及苯的同系物的命名,掌握苯环上 的亲电取代反应及定位规则,侧链卤代和氧化反应,掌握 萘的结构及命名,萘的亲电取代反应、氧化反应;熟悉休 克尔规则及非苯芳烃的芳香性判断;了解联苯、蒽、菲的 结构及命名以及苯及其同系物的主要物理性质(易燃性)。 二、教学重点内容 芳烃的结构、闭合共轭体系、命名、亲电取代反应及其定 位规律、侧链氧化、萘的结构、命名及亲电取代反应、非 苯芳烃芳香性的判断是本章的重点。
CH3 CH3 CH3
(1)单环芳烃
苯 甲苯 间二甲苯
(2)多环芳烃
连 苯 三
C H 苯 甲
烷
(3)稠环芳烃
萘 蒽 菲
4
5.1
芳烃的构造异构和命名
5.1.1 构造异构
苯及其同系物的通式为:CnH2n-6。 例如苯有六个碳和六个氢,其六个碳和六个氢是等同的; 结构异构: 一元取代:只有一种
CH3 CH CH2 H3C CH CH3
(a)
(b) (c) (d) (e)
卤化
硝化 磺化 Friedel-Crafts反应 氯甲基化
17
(1)亲电取代反应
(a) 卤化
苯环上和卤代反应较困难,常用FeX3(Lewis酸)作催化剂。
+ Cl2
FeCl3,25oC 90%
Cl + HCl
控制苯过量,不要太激烈,避免二卤代。 因是亲电反应,所以苯的同系物(甲苯)比苯更易反应。 Cl 卤代活性: F2>Cl2>Br2>ICH CH3 CH3 CH3 2。 3
14
5.3
单环芳烃的物理性质
16种多环芳烃的结构式

16种多环芳烃的结构式多环芳烃 (Polycyclic Aromatic Hydrocarbons, PAHs) 是由两个或两个以上的芳香环连接而成的有机化合物。
这些化合物通常由碳和氢原子组成,具有一定的环状结构和共轭体系,因此在化学性质和生物学活性上具有独特的特点。
在环境中,PAHs是一类普遍存在的化合物,它们可以来自燃烧、化石燃料的使用、工业排放、车辆尾气和污水处理厂等源头。
下面将介绍其中的16种典型多环芳烃及其结构式。
1. 苯 (Benzene, C6H6)苯是最简单的多环芳烃,由一个六元芳香环组成。
它是一种无色液体,具有刺激性气味。
苯具有很高的环境稳定性和易挥发性,且对人体有毒性。
2. 萘 (Naphthalene, C10H8)萘由两个共轭苯环组成,是一种无色固体,有特殊的芳香气味。
它主要用作防蛀剂和染料的前体物质,也广泛应用于塑料和橡胶等工业。
3. 菲 (Phenanthrene, C14H10)菲是一种具有三个对位芳香环的多环芳烃。
它是一种固体物质,在环境中存在且具有显著的毒性。
菲也是石油污染的指示物质之一4. 蒽 (Anthracene, C14H10)蒽是由三个对位苯环连接而成的多环芳烃,是一种白色结晶固体。
它广泛用于染料、橡胶和塑料工业。
5. 蒽醌 (Anthraquinone, C14H8O2)蒽醌是蒽的衍生物,具有两个酮基(O=C)的结构。
它是一种重要的有机合成原料,广泛应用于染料、药物和化妆品等领域。
6. 芘 (Pyrene, C16H10)芘由四个共轭苯环连接而成,是一种固体物质。
它具有很高的环境稳定性和毒性,是一种常见的环境污染物。
7. 苊 (Chrysene, C18H12)苊是一种具有四个对位芳香环的多环芳烃,是无色结晶固体。
它是一种常见的环境污染物,具有较高的生物累积性。
8. 梦菲 (Fluoranthene, C16H10)梦菲由四个共轭芳香环连接而成,是一种白色固体。
有机化学第7章 芳烃及非苯芳烃
SO 3H
CH 3 X
Friedel-Crafts反应
F-C酰化反应
• 芳烃在无水AlCl3催化下与酰卤(RCOX)或酸酐作用, 生成芳酮的反应,叫酰基化反应.
例:
傅-克酰基化反应机理:
(1)进攻的亲电试剂是:酰基正离子
+
RCOCl + AlCl3
R-C=O + AlCl4
(2) 反应历程:
+ + R-C=O
傅-克酰基化反应的应用
① 制备芳香酮
O
+ R C Cl
AlCl3
O CR
② 制备直链烷烃
F-C烷基化反应
R +RCl AlCl3
傅-克烷基化反应的特点 特点一:烷基化反应易发生重排,不适合制备长的直链烷基苯。
+ CH3CH2CH2Cl AlCl3
CH 2CH 2CH 3 +
30%
+ (CH3)CHCH2Cl AlCl3
H
HC
C
H
C
C
HC
C
X
HC
C
H
C
H
H
• 上面两式是等同的
Br
Br
C
苯的邻位二元取代物 H C
C
Br
HC
C
H
C
H
C
H
C
C
Br
HC
C
H
C
H
• 实际上是一种
• 凯库勒假定:苯的双键是不固定的,而是不停地来
回移动,所以下列两种结构式迅速互变,不能分离.
H
C
HC
C
H
HC
C
第7章芳烃及非苯芳烃详解

— 3H2
7.3.2 石油的芳构化 2.烷烃脱氢环化和再脱氢
C H3 C H2 C H2 C H2 C H3 C H2
—H2
—3H2
3.环烷烃异构化和脱氢
C H3
异构化
—3H2
4.石油裂解生成的副产品也有一定量的芳烃。
7.4 单环芳烃的物理性质 单环芳烃不溶于水,而溶于汽油,乙醚和四氯化 碳等有机溶剂。 一般单环芳烃都比水轻。 沸点随相对分子量增高而升高。 对位异构体的熔点一般比邻位和间位异构体的高 (可能是由于对位异构体分子对称,晶格能较大之故)。 芳环骨架的伸缩振动表现在: 1625~1576 cm-1和 1525~1475 cm-1 处有两个吸收峰。 芳环的C-H伸缩振动在3100~3010 cm-1。 苯的取代物及其异构体在 900~650 cm-1处具有特 殊的C-H面外弯曲振动。
OH
OH
C O 2H
S O 3H
C H 2C H 3
S O 3H
对乙基苯酚
间羟基苯磺酸
邻磺基苯甲酸
芳基、苯基、苄基 芳基:芳烃分子的芳环上减去一个H后的基团, 用“Ar”表示。 苯基:苯分子上减去一个H后的基团,用“Ph” 表示。
苄基:甲苯的甲基上减去一个H。 7.3 单环芳烃的来源和制备 1845年-1940年期间 7.3.1 煤的干馏
C H3
C H3
邻二甲苯 (1,2-二甲苯)
间二甲苯 (1,3-二甲苯)
对二甲苯 (1,4-二甲苯)
三元取代物:用数字代表取代基的位置或用“连, 偏,均”字表示它们的位置。
C H3 C H3
C H3 C H3
C H3
C H3
H3C
C H3
1,2,3-三甲苯 (连三甲苯)
第七章 芳烃
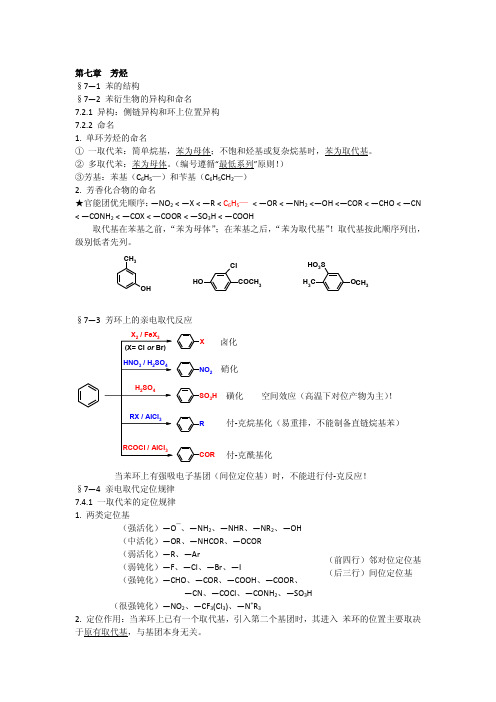
第七章 芳烃§7―1 苯的结构§7―2 苯衍生物的异构和命名7.2.1 异构:侧链异构和环上位置异构7.2.2 命名1. 单环芳烃的命名① 一取代苯:简单烷基,苯为母体;不饱和烃基或复杂烷基时,苯为取代基。
② 多取代苯:苯为母体。
(编号遵循“最低系列”原则!)③芳基:苯基(C 6H 5—)和苄基(C 6H 5CH 2—)2. 芳香化合物的命名★官能团优先顺序:―NO 2 < ―X < ―R < C 6H 5— < ―OR < ―NH 2 <―OH <―COR < ―CHO < ―CN < ―CONH 2 < ―COX < ―COOR < ―SO 3H < ―COOH取代基在苯基之前,“苯为母体”;在苯基之后,“苯为取代基”!取代基按此顺序列出,级别低者先列。
CH 3OH O H COCH 3Cl O HO 3S C H 3CH 3§7―3 芳环上的亲电取代反应当苯环上有强吸电子基团(间位定位基)时,不能进行付-克反应!§7―4 亲电取代定位规律7.4.1 一取代苯的定位规律1. 两类定位基(强活化)―O ¯、―NH 2、―NHR 、―NR 2、―OH(中活化)―OR 、―NHCOR 、―OCOR(弱活化)―R 、―Ar (弱钝化)―F 、―Cl 、―Br 、―I (强钝化)―CHO 、―COR 、―COOH 、―COOR 、―CN 、―COCl 、―CONH 2、―SO 3H(很强钝化)―NO 2、―CF 3(Cl 3)、―N +R 32. 定位作用:当苯环上已有一个取代基,引入第二个基团时,其进入 苯环的位置主要取决于原有取代基,与基团本身无关。
X NO 2SO 3H RCOR 卤化 硝化 磺化 空间效应(高温下对位产物为主)!付-克烷基化(易重排,不能制备直链烷基苯) 付-克酰基化(前四行)邻对位定位基 (后三行)间位定位基7.4.3 二取代苯的定位规律当苯环上已有两个取代基时,再引入第三个基团,其进入苯环的位置取决于原有的两个取代基,可根据一取代苯的定位规律推测。
18个PAHS多环芳烃清单
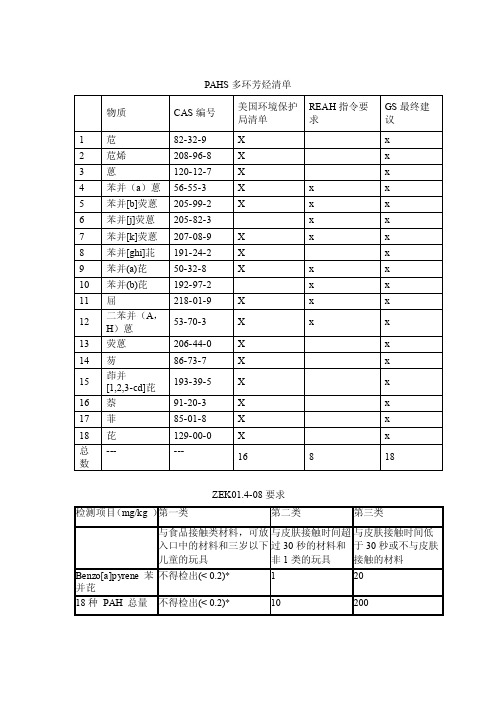
PAHS多环芳烃清单
ZEK01.4-08要求
GS认证对PAHs的要求新增两种
近期,德国在对消费品安全要求进行审查后,要求在GS(安全性认证(安全测试))控制列表中增加两种多环芳烃(PAH)致癌物质。
这样GS 认证管控的多环芳烃总数达到18个。
自愿性的德国GS标志认证基于美国环境保护署提出的技术指标列表对适用产品中的多环芳烃加以管控。
此前,这份列表包含的16种多环芳烃被分类为致癌物质。
不过,由欧洲食品安全局(EFSA)和德意志研究联合会(DFG)参议院委员会认定的两种剧毒多环芳烃却未被列入表内。
这两种物质——苯并[j]荧蒽,苯并[e]苝,都被列为第二类致癌物质,并被列入REACH法规附录XVII(第50项)。
因此,德国要求进一步控制消费品中的多环芳烃。
这两种物质的加入将确保欧盟列出的所有八个第二类高致癌多环芳烃可通过GS标志进行管控。
德国安全技术认证中心ZLS(GS授权机构)的官方决议ZEK01-08文件跟新版ZEK01.4-08已经发布,将于2012年7月1日开始实施。
第7章 芳烃

NH2
CH3
2-甲基 氯苯胺 甲基-4-氯苯胺 甲基 4-chloro-2-methylaniline
Cl
§7.3 单环芳烃的性质
1 苯及其同系物的物理性质
多数为液体,具有特殊的香气,蒸气有毒。 多数为液体,具有特殊的香气,蒸气有毒。 碳原子数相同的异构体,沸点相差不大, 碳原子数相同的异构体,沸点相差不大,结构对称的 异构体熔点较高。 异构体熔点较高。
§7.3 单环芳烃的性质
2 亲电取代反应
苯环的π键很难发生加成反应,却容易发生亲电取代反应。 苯环的 键很难发生加成反应,却容易发生亲电取代反应。 键很难发生加成反应 硝化: 硝化:
H2SO4
+ HNO3
NO2
+ H2O
氯代: 氯代:
+ Cl2
FeCl3
Cl + HCl
SO3H
磺化: 磺化:
+ SO3
§7.2 芳烃的异构和命名
有两种以上取代基时,选择母体的顺序为: 有两种以上取代基时,选择母体的顺序为: —OR,—R,—NH2,—OH,—COR,—CHO, , , , , , —CN,—CONH2,—COCl,—COOR,—SO3H, , , , , —COOH,正离子等。 ,正离子等。 排在后面的做母体,排在前面的做取代基( 排在后面的做母体,排在前面的做取代基(以后者为母 体命名)。 体命名)。
CH2 CH
注意: 注意:
① ② ③
CH2
·
Hale Waihona Puke ·CH2 CHCH2
各经典结构式之间只是电子排列不同; 各经典结构式之间只是电子排列不同; 共振杂化体不是经典结构式混合物; 共振杂化体不是经典结构式混合物; 共振杂化体也不是互变平衡体系。 共振杂化体也不是互变平衡体系。
有机化学7芳烃
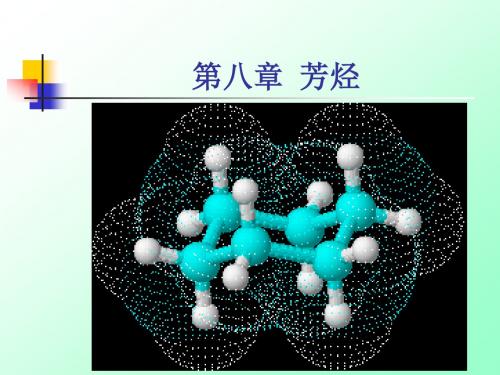
C2H5
+ C2H5Br AlCl3 + CH3CH2OH H2SO4
+ HBr
76%
-CH2CH3 + H2O
CH3-CH-CH3
+ CH3CH=CH2
AlCl3
微H﹢
工业上用丙烯和苯反应生成异丙苯。
c.傅—克烷基化的特点 Ⅰ.异构化现象:当使用三个或三个以上碳原 子的直链卤代烷作烷基化试剂时,会发生碳链异 构现象。例如:
苯的结构小结
(1)苯是一个正六边形的平面分子,键长、键角平均化; (2)电子云分布在苯环的上方和下方; (3)π电子高度离域,6个π电子在基态下都在成键轨道 内,故体系的能量降低,而使苯环稳定。
苯的表示方法:
或
§7-4 芳烃的工业来源
1.从煤焦油中分离 2.芳构化 (1)环烷烃脱氢生成芳香烃: 如
烷基苯的磺化也较苯容易,如用浓硫酸在常温下 就可以使甲苯磺化。
CH3
+ H2SO4 室温
CH3 SO3H +
CH3
SO3H
*(4)傅瑞德—克拉夫茨反应:1877年法国化学 家傅瑞德(C.Friedel,1832—1899)和美国化学家 克拉夫茨(J.M.Crafts,1839~1917)发现了制 备烷基苯(PhR)和芳酮(ArCOR)的反应,常简称为 傅—克反应。前者又叫傅—克烷基化反应;后者 又叫傅—克酰基化反应。
CH2-
2.二烃基苯:二烃基苯有三种异构体,这是 由于取代基在苯环上相对位置的不同而产生的。 例如,二甲苯有三种异构体,它们的构造式和命 名为:
CH3
CH3 邻-二甲苯
邻二甲苯 (1,2-二甲苯) O-二甲苯 (Ortho)
16种多环芳烃结构 -回复

16种多环芳烃结构-回复多环芳烃是一类由多个芳香环组成的有机化合物。
它们通常由碳和氢原子构成,分子结构中形成了多个芳香环串联的关系。
这使得多环芳烃具有独特的化学性质和应用价值。
下面将介绍16种常见的多环芳烃结构,并解释它们的特点和用途。
1. 苯(C6H6)苯是最简单的多环芳烃化合物,由六个碳原子和六个氢原子组成的六元环结构。
苯具有强烈的芳香性质,广泛用于有机合成、溶剂和染料等领域。
2. 萘(C10H8)萘是一个由两个苯环组成的多环芳烃,具有典型的带有共轭烯烃的十元环结构。
它常用作颜料、杀菌剂和荧光染料。
3. 苊(C14H10)苊是一个由三个苯环组成的多环芳烃,是最简单的三环芳烃之一。
苊常被用作有机颜料的原料。
4. 菲(C14H10)菲是一个由四个苯环构成的多环芳烃,其结构与苊非常相似。
菲广泛应用于药物合成、有机材料和染料等方面。
5. 芘(C16H10)芘是一个由四个苯环和两个共轭烯烃构成的多环芳烃,分子结构较为复杂。
芘广泛用于染料、荧光探针和生物医学研究中。
6. 蒽(C14H10)蒽是一个由三个苯环构成的多环芳烃,由于它的共轭π电子体系具有很强的共轭作用,使得蒽的化学性质非常活泼。
蒽是许多染料、颜料的前体,在有机合成和医药化学中有重要应用。
7. 菲咯啉(C16H9N)菲咯啉是一个由四个苯环和一个氮原子构成的多环芳烃。
菲咯啉具有良好的光吸收性能,被广泛应用于溶剂染料、太阳能电池和有机光电材料等领域。
8. 蒽醌(C14H8O2)蒽醌是一种由两个蒽环和一个醌基团构成的多环芳烃。
蒽醌是一种重要的有机合成中间体,广泛应用于染料、医药和农药等领域。
9. 获得(C14H10O)获得是一个由一个蒽环和一个苯环构成的多环芳烃。
获得具有良好的荧光性能,被广泛应用于荧光标记、生物传感和有机电子等领域。
10. 燃料沥青多环芳烃燃料沥青中存在着大量的多环芳烃化合物,例如苯并[a]芘、苯并[c,d]苯并[a,h]蒽等。
这些多环芳烃是由石油加工过程中的蒸馏和催化裂化而形成的。
轻芳烃执行标准

轻芳烃执行标准轻芳烃是一类碳氢化合物,具有良好的溶解性、稳定性和不挥发性。
它们在化工、石油、医药等诸多领域有着广泛的应用。
为了保障轻芳烃产品的质量和安全性,制定一套符合国际标准的执行标准是至关重要的。
本文将介绍轻芳烃执行标准的主要内容和应用。
一、产品分类及命名轻芳烃根据碳原子数的不同可以分为C6、C7、C8、C9等,分别代表了具有6个碳原子、7个碳原子、8个碳原子和9个碳原子的轻芳烃。
它们分别具有不同的物化性质和用途。
轻芳烃的命名遵循IUPAC命名法,以碳原子数和分子结构特征为基础,例如二甲基苯、环庚烷等。
二、质量指标1. 目测外观:轻芳烃应为无色透明液体或低温下凝固的固体。
外观应无杂质,无悬浮物。
2. 密度:测定轻芳烃的密度,可检验其纯度和杂质含量。
3. 沸点范围:轻芳烃的沸点对于其应用和混合物的分离非常重要。
执行标准应规定出合理的沸点范围。
4. 含量测定:通过各种分析方法测定各种组分的含量,例如苯、甲苯、二甲苯等的含量测定。
5. 组分分析:运用色谱、质谱和红外等科学分析方法对轻芳烃样品的组分进行鉴定。
6. 杂质限制:执行标准应规定轻芳烃中杂质的种类和限量,例如酸、碱、水分、重金属等。
三、质量控制轻芳烃的质量控制是确保产品符合执行标准的关键步骤。
以下是常用的质量控制方法:1. 原料控制:对于轻芳烃的生产,要确保原料的纯度和质量,避免不必要的杂质进入产品。
2. 生产工艺控制:要确保生产过程中的温度、压力、反应时间等参数的合理控制,以及催化剂和溶剂的选择和配比。
3. 检测方法控制:执行标准规定了合适的检测方法,包括色谱、质谱、光谱等,生产过程中要严格按照这些方法进行检测,确保结果的准确性和可靠性。
四、应用领域轻芳烃作为一种重要的工业化学品,在多个领域具有广泛的应用。
1. 化工行业:轻芳烃可用于合成树脂、橡胶、塑料等化工产品,具有重要的原料和溶剂作用。
2. 石油行业:轻芳烃可作为提取剂、反应媒介和添加剂,广泛用于石油加工和提炼过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章 芳烃(习题)
一、命名下列化合物
1.NO 2COOH
Br
;2.
CHO
;3.
Br OCH 3
;4.
NH 2
SO 3H ; 5.
CH CH 2
Br
6.NO 2
CH 3SO 3H
; 7.
NH 2COOH
; 8.
NO 2
NH 2
Cl
; 9.Cl
C 2H 5
CH 3
; 10.
COOH
Cl
1、3-硝基-5-溴苯甲酸 ;
2、1-萘甲醛(α-萘甲醛)
3、8-溴-1-萘甲醚 ;
4、邻氨基苯磺酸
5、间溴苯乙烯 ;
6、4-甲基-2-硝基苯磺酸
7、间氨基苯甲酸 ;
8、2-硝基-6-氯苯胺
9、2-乙基-4-氯甲苯 ; 10、8-氯-1-萘甲酸
二、由名称写出结构式
1.3,5-二溴-2-硝基甲苯; 2.2-硝基-3-甲氧基甲苯; 3.β-萘磺酸 4.环己烯基苯; 5.间氟苯乙烯;
7.3-苯基戊烷; 8.4,4’-二硝基联苯; 9.3-氯-2-萘甲酸;
1.NO 2Br Br
CH 3
;2.
NO 2
CH 3
OCH 3;3.
SO 3H
;4.;5.
CH CH 2F
7.CH 2CH 3CH C 2H 5
;8.
NO 2
O 2N
;9.
COOH Cl
三、完成下列反应式 1.
△
KMnO 4
C 2H 5H 3C
2.+(CH 3)3C Cl
CH 3
CH 3
AlCl 3100℃
3.H 2SO 4
△
Cl
KMnO 4
H 3C
HNO 3 4.Br 2Cl 2hv
H 3C
Fe
5.H 2SO 4
+60℃
6.
CH 2Cl
CH 3AlCl 3
+CO Zn-Hg 浓HCl
7.
+COOH
OH
CH 3CH 3HNO 3(2 mol)
8.H 2SO 4
NO 2
NH HNO 3C
O
9.
H 2SO 4
△
KMnO 4
Br
C 2H 5
HNO 3
10.
△
KMnO 4
(CH 3)3C
11.
H 2SO 4
HNO 3C
O
O
12.
Br 2OCH 3
Fe
C
O
CH 3O
13.
HCl
(1)(2)H 2SO 4
△
KMnO 4AlCl 3HNO 3+
浓
三、完成反应式
1.
COOH
HOOC
;2.CH 3
CH 3
C(CH 3)3;3. NO 2Cl
CH 3
,NO 2
COOH
Cl
;4.CH 3
Br ,Br
CH 2Cl
;
5.SO 3H
;6.
CH 3
CH 2CO ,
CH 2CH 3
CH 2;7.
NO 2
O 2N
OH
CH 3
;
8.,
NO 2
O 2N NH
C O
;9.COOH Br
,
NO 2
COOH
Br
10.
(CH 3)3C
COOH
;
11.
NO 2
O 2N
C O O
,;12.
Br
OCH 3
C O
CH 3O
;13.
,
NO 2COOH
;
四、回答问题
1.判断下列各化合物或离子中具有芳香性的是( )。
(A) (B)
(C) (D)
O
2.下列各化合物中具有芳香性的是( )。
(A)
(B) OH
O
(C)
CH 2
(D)
3.下列化合物中不具有芳香性的是( )。
(A) (B) (C) (D)
4.下列化合物中不具有芳香性的是( )。
(A) (B) (C) (D)
S
5.下列各化合物中具有芳香性的是( )。
(A) (B)
(C)
(D)
6.推测下列各化合物是否具有芳香性( )。
(A) (B) +
+
(C) (D)
7.指出下列化合物或离子哪些具有芳香性( )。
(A)
(B)
(C) (D)
8.根据休克尔规则,判断下列化合物哪些具有芳香性( )。
(A)
O
(B) (C) (D) N
9.下列化合物发生亲电取代反应由易到难的次序为 。
(A) 乙酰苯胺 (B) 甲苯 (C) 硝基苯 (D) 苯胺
10.下面化合物发生亲电取代反应由易到难顺序为 。
(A) 苯 (B) 氯苯 (C) 苯甲醚 (D) 苯磺酸
11.下列化合物发生亲电取代反应由易到难的次序为 。
(A) 甲苯 (B) 对甲基苯甲酸 (C) 苯胺 (D)苯甲醛
12.下列化合物进行硝化反应时由易到难的顺序为 。
(A) 氯苯 (B) 硝基苯 (C) 乙苯 (D) 苯腈
13.写出下列化合物溴代反应时活性大小顺序为 。
(A) 溴苯 (B) 苯甲醚 (C) 甲苯 (D) 苯甲酸
14.下面化合物进行亲电取代反应时速度顺序为 。
(A) 苯 (B) 甲苯 (C) 苯胺 (D)苯甲醛
18.下列化合物按发生芳环亲电取代反应的活性大小排列 。
(A) 溴苯 (B) 三氟甲苯 (C) 甲苯 (D) 苯酚
20.将下列化合物按其硝化反应的由易到难次序排列 。
(A) 乙酰苯胺 (B) 苯乙酮 (C) 氯苯 (D) 苯磺酸
1.(B),(D);
2.(A),(B);
3.(A),(D);
4.(A),(C);
5.(C),(D);
6.(B),(C);
7.(A),(C);
8.(B),(D);
9.D >A >B >C ;10.C >A >B >D ;11.C >A >B >D ; 12.C >A >D >B ;13.B >C >A >D ;14.C >B >A >D ; 18.D >C >A >B ; 20.A >C >B >D ;
六、鉴别下列各组化合物
1.甲苯 1-己烯 1,3-环己二烯 2.苯 乙苯 苯基乙炔
1.加入溴水无变化者为甲苯,已反应的两种化合物中加入顺丁烯二酸酐,产生白色沉淀者为1,3环己二烯。
2.加入Ag(NH 3)2+有白色者为苯基乙炔,余下两者加入KMnO 4溶液,使之褪色者为乙苯。
七、合成题
1.以甲苯为原料合成:3-硝基-4-溴苯甲酸。
2.由苯为原料合成:间氯苯甲酸。
5.以甲苯为原料合成:4-硝基-2-溴苯甲酸。
6.以苯为原料合成:对硝基邻二溴苯。
1.
Br 2COOH
H 2SO 4
NO 2COOH
KMnO 4
Br
HNO 3
FeBr 3
CH 3
CH 3
Br
Br
2.
COOH
COOH
Cl 2KMnO 4
CH 3Cl
AlCl 3
Fe
Cl
CH 3
+
5. Br 2COOH
O 2N COOH
KMnO 4
Br
HNO 3
Fe
CH 3
Br
CH 3
H 2SO 4
Br
6.
Br 2Br
Br
HNO 3Fe
FeBr 3Br
H 2SO 4
NO 2
NO 2
Br Br 2
八、推测结构
1.组成为C 10H 14的芳烃,可以从苯制得,它含有一个手性碳原子。
氧化后生成苯甲酸,请确定其构造式。
2.化合物(A )的分子式为C 9H 8,在室温下能迅速使Br 2-CCl 4溶液和稀的KMnO 4溶液褪色,在温和条件下氢化时只吸收1mol H 2,生成化合物(B ),(B )的分子式为C 9H 10;(A )在强烈的条件下氢化时可吸收4mol H 2,强烈氧化时可生成邻苯二甲酸;试写出(A ),(B )的构造式。
1.
C 2H 5
CH
CH 3
* 2. (A)
; (B)。
