国产尼莫地平片的人体相对生物利用度研究
晶型药物常用的检测分析方法

晶型药物常用的检测分析方法(2012-02-08 13:54:05)物质在结晶时由于受各种因素影响,使分子内或分子间键合方式发生改变,致使分子或原子在晶格空间排列不同,形成不同的晶体结构。
同一物质具有两种或两种以上的空间排列和晶胞参数,形成多种晶型的现象称为多晶现象(polymorphism)。
虽然在一定的温度和压力下,只有一种晶型在热力学上是稳定的,但由于从亚稳态转变为稳态的过程通常非常缓慢,因此许多结晶药物都存在多晶现象。
固体多晶型包括构象型多晶型、构型型多晶型、色多晶型和假多晶型。
药物分子通常有不同的固体形态,包括盐类,多晶,共晶,无定形,水合物和溶剂合物;同一药物分子的不同晶型,在晶体结构,稳定性,可生产性和生物利用度等性质方面可能会有显著差异,从而直接影响药物的疗效以及可开发性。
如果没有很好的评估并选择最佳的药物晶型进行研发,可能会在临床后期发生晶型的变化,从而导致药物延期上市而蒙受巨大的经济损失,如果上市后因为晶型变化而导致药物被迫撤市,损失就更为惨重。
因此,药物晶型研究和药物固态研发在制药业具有举足轻重的意义。
由于药物晶型的重要性,美国药监局(FDA)和中国药监局(SFDA)在药物申报中对此提出了明确规定,要求对药物多晶型现象进行研究并提供相应数据。
正因如此,任何一个新药的研发,都要进行全面系统的多晶型筛选,找到尽可能多的晶型,然后使用各种固态方法对这些晶型进行深入研究,从而找到最适合开发的晶型;选定最佳晶型后,下一步就是开发能始终如一生产该晶型的化学工艺;最后一步是根据制剂对原料药固态性质的要求,对结晶工艺进行优化和控制,确定生产具有这些固态性质的最佳工艺参数,从而保证生产得到的晶型具有理想的物理性质,比如晶体表象,粒径分布,比表面积等。
这种通过实验设计来保证质量的方法必须对药物晶型具有非常全面深刻的理解才能实现。
原研药公司对药物分子的晶型申请专利,可以延长药物的专利保护,从而使自己的产品具有更长时间的市场独享权。
尼莫地平胶囊人体生物利用度及生物等效性研究

(μg· L -1) 4 h ( %) 14 h ( %) 30 d ( %) 3 次 ( %)
子离子 315.0,碰撞能 22 V;扫描宽度为 0.2 amμ,扫描时间为
0.5 0.48 8.03 0.57 3.34 0.52 6.32 0.55 5.90
0.5 s。
接0 1.4.3 血清中尼莫地平标准曲线 取尼莫地平储备液,加空 白血清,按逐级稀释的方法依次配制成相当于尼莫地平血清
1.4.4 精密度和准确度试验 取空白血清,按“ 血清中尼莫
积sO 地平标准曲线和定量下限” 项下的方法配制尼莫地平低、中、 高三个浓度(0.5,5 和 50 μg· L -1 )的质量控制(QC)样品,每 一浓度进行 5 样本分析,连续测定 3 d,根据当日的标准曲线,
/’、计算 QC 样品的测得浓度。 根据 QC 样品结果计算本法的精 密度,结果底、中、高浓度第一天日内的 RSD 分别为8.32%、 3.86%、12.62%、第二天日内的 RSD 分别为12.07%、7.44%、 6.60%,第三天日内的 RSD 分别为 8.06%、8.55%、2.00%, 底、中、高浓度日间的 RSD 分别为 6.31%、5.71%、9.50%。 结果表明,日内、日间相对标准差(RSD) <15%。 1.4.5 回收率和基质效应的测定 取空白血清 100 μl,按 “血清中尼莫地平标准曲线和定量下限” 项下的方法制备尼 磊寸o莫地平低、中、高三个浓度(0.5,5 和 50 μg· L -1)的样品,每 一浓度进行三样本分析。 进样分析,获得相应峰面积 A1( 三 次测定的平均值)。 取空白血清 100 μl,加入 1 ml 乙酸乙酯, 涡旋 2 min,13400 rpm 离心 10 min,提取上层有机相 800 μl, 50℃水浴下 N2 吹干。 加入 10 μl 相应的标准溶液和 10 μl 内 标,80 μl 流动相复溶,配制尼莫地平低、中、高三个浓度(0.5, 5 和 50 μg· L -1 ) 的样品,每一浓度进行三样本分析,进样分 析,获得相应峰面积 A2 ( 三次测定的平均值)。 以 A1 /A2 的 值计算提取回收率。 低、中、高三个浓度的提取回收率分别为
口服药物的生物利用度

口服药物的生物利用度摘要:本文通过检索国内外相关文献综述了口服药物的生物利用度的研究进展,特别归纳了提高口服药物生物利用度的方法。
关键词:生物利用度口服药物前体药物微粒给药系统1、概述生物利用度是指制剂中药物被吸收进入人体循环的速度与程度。
生物利用度是反映所给药物进入人体循环的药量比例,它描述口服药物由胃肠道吸收,及经过肝脏而到达体循环血液中的药量占口服剂量的百分比。
口服给药是临床给药尤其是长期用药的首选给药途径。
药物的口服生物利用度低不仅导致个体间和个体内差异、血药浓度波动大,同时增加生产成本,增大机体毒性的可能性。
由于药物的物理化学性质和生物药剂学性质各异,所以导致口服生物利用度低的原因也呈多样化。
随着高通量筛选和组合化学的发展,通常大部分有活性的化合物都属于难溶性化合物,其中40%以上的候选药物由于生物药剂学性质不佳而在药物开发研制过程中失败。
FDA 工业指南(1997)根据药物的溶解性及膜通透性将所有药物分成4 类(生物药剂学分类系统,biopharmaceutical classification system, BCS)①高溶解性和高透膜性;②低溶解性和高透膜性;③高溶解性和低透膜性;④低溶解性和低透膜性。
其中①类无生物利用度问题,易于制成口服制剂;④类最难输送,应采用其他给药途径。
我们的主要任务就是采用各种制剂手段提高②③类药物的口服生物利用度。
2、影响生物利用度的因素影响口服药物吸收的主要因素即药物的理化性质、药物在胃肠道的稳定性、药物透过肠粘膜吸收、药物在肠壁代谢及外向性载体转运等方面。
【1】①药物的理化特性:立体化学结构(包括手性)、进入细胞膜的比例、分子量、分子体积、pKa、溶解度、渗透性、亲水亲脂性、化合物稳定性、分配系数、剂型特性(如崩解时限、溶出速率) 及一些工艺条件等。
②胃肠道环境和解剖生理状态:胃肠道内液体的作用( 肠pH 值、胆汁的影响、淋巴液流量等) ,药物在胃肠道内的转运情况( 小肠上皮细胞中各种特异性转运系统和多药耐药性(MDR)、p-糖蛋白等) ,吸收部位的表面积与局部血流,药物代谢的影响,肠道菌株等。
尼莫地平片说明书尼莫地平片说明书.

除非特殊处方 ,推荐剂量为每次 30mg(一次 1 片,每日 3 次。少量水送服完整片 剂 ,与饭时无关。口服尼莫地平片数月后 ,必须重新评价是否仍存在治疗的适应症。
【不良反应不良反应】】
作为尼莫地平注射液预先使用后的继续治疗作为尼莫地平注射液预先使用后的 继续治疗 ,,预防和治疗由于动脉瘤性预防和治疗由于动脉瘤性蛛网膜下腔出蛛网膜 下腔出血后脑血管痉挛引起的缺血性神经损伤 :
心动过速 心动过缓 血管 非特异性的心血管症状 低血压 血管扩张 胃肠道 胃肠道症状 恶心 肠梗阻 肝胆 轻度截中度肝脏影响 一过性肝酶升高 用于用于治疗老年性脑功能障碍治疗老年性脑功能障碍治疗老年性脑功能障 碍 :: 按按类类的类率 CIOMS III ( 安安剂 -对按对对 :尼莫地平 N = 1594;安安剂 N = 1558;无对按对对 :尼莫地平 N = 8049;截截截年 200510月 20 日,基于临床对对 的药物不良反应如下 : “常见 ”项下不良反应的发生类率低于 2%。 临床描临床描述述
哺乳期
哺乳期 :: 尼莫地平及其代谢物能运入人类乳汁中 ,浓度与母体中血浆浓度的水 平相同。建议哺乳期妇女应用本品时避免喂哺婴儿。
体外受精
体外受精 :: 个类体外受精的案例中 ,钙拮抗剂与精子头部的可逆生化改变有关 , 可能导致精子功能损害。
【儿童用药儿童用药】】
尚无儿童用药的安全性和有效性资料。 【老年用药老年用药】】
抗-HIV 蛋白酶抑制剂蛋白酶抑制剂 ((例如例如利托那韦利托那韦利托那韦
未运行尼莫地平与抗 -HIV 蛋白酶抑制剂相互作用的对对。此类药物为细胞色 素 P450 3A4 系统的强效抑制剂。因此合并应用此类蛋白酶抑制剂可能使尼莫地平 的血浆浓度显著增加。
尼莫地平片说明书 尼莫地平片说明书.
【药物相互作用药物相互作用】】
1.尼莫地平通过肠粘膜和肝脏的细胞色素P450 3A4系统代谢消除。因此对细胞色素P450 3A4系统有抑制或诱导作用的药物可能改变尼莫地平的首过效应或清除率。尼莫地平与下列细胞色素P450 3A4系统抑制剂联合应用时,应监测血压,如有必要,应考虑减少尼莫地平的服用剂量:
0.1%>罕见罕见罕见≥0.01%非常罕见<0.系统
非特异性的脑血管症状
头痛眩晕
非特异性的神经症状
头晕
运动功能运运震震
心脏
非特异性的心律失常
心悸心动过速
血管
非特异性的心血管症状
低血压血管扩张
晕晕
水肿
胃肠道
胃肠道症状
便秘腹泻肠胃胀气
【禁忌禁忌】】
1.对本品或本品中任何成份过敏者禁用。
哺乳期
哺乳期::尼莫地平及其代谢物能运入人类乳汁中,浓度与母体中血浆浓度的水平相同。建议哺乳期妇女应用本品时避免喂哺婴儿。
体外受精
体外受精::个类体外受精的案例中,钙拮抗剂与精子头部的可逆生化改变有关,可能导致精子功能损害。
【儿童用药儿童用药】】
尚无儿童用药的安全性和有效性资料。
【老年用药老年用药】】
3.低血压患者(收缩压低于100毫米汞柱须慎用。
4.使用本品可能出现的头晕会影响操作(驾驶和使用机械的能力。
5.严禁使用超过有效期的尼莫地平片。
6.请放在儿童触及不到的地方。
【孕妇及哺乳期妇女用药孕妇及哺乳期妇女用药】】
对于孕妇尚无足够的对对。拟在妊娠期应用本品时,必须依临床的严重程度审慎权衡利弊。
2.尼莫地平与利福平联合应用会显著降低尼莫地平的疗效,因此尼莫地平禁截与利福平联合应用。
尼莫地平片培训ppt课件

血药浓度(ng/ml)
F=126.1 F= 52.4 F= 78.1
8名健康受试者口服120mg尼莫地平片的药---时曲线
体内代谢
血药浓度(ng/ml)
Nimodipine
T1/2
1. 5-2小时
代谢
排泄
时间(小时)
8名志愿者口服120mg尼莫地平片的血药浓度/时间曲线
正大青春宝
正大青春宝
药理作用
调节细胞内钙的水平, 使其保持正常生理功能 选择性扩张脑血管, 保护脑细胞保护促进记忆 轻度扩张外周血管, 降低血压
正大青春宝
药理特点
正常情况下,平滑肌的收缩依赖于Ca2+进入细胞内,引起跨膜 电流的去极化。尼莫地平通过有效地阻止Ca2+进入细胞内、抑 制平滑肌收缩,达到解除血管痉挛之目的。 动物实验证明,尼莫地平对脑动脉的作用远较全身其他部位动 脉的作用强许多,并且由于它具有很高的嗜脂性特点,易透过 血脑屏障。 当用于蛛网膜下隙出血的治疗时,脑脊液中的浓度可达 12.5ng/ml。由此推论,临床上可用于预防蛛网膜下隙出血后的 血管痉挛,然而在人体应用该药的作用机制仍不清楚。 此外尚具有保护和促进记忆、促进智力恢复的作用。 所以可选择性地作用于脑血管平滑肌,扩张脑血管,增加脑血 流量,显著减少血管痉挛引起的缺血性脑损伤。
血药浓度(ng/ml)
60 50 40 30 20 10 0 0 1 2 3
正大青春宝 尼莫通
F=107.4
4
5 时间(h )
10名健康受试者口服120mg尼莫地平片的药---时曲线
尼莫地平片剂相对生物利用度测定(4)
尼莫地平口腔崩解片的药动学及相对生物利用度研究

[ b tat O jcie T eerht hr a0iec n ea v iaaa it o Nm dpn ai ds t et gt lt A src] bet orsac ep am ck t s drliebov ibly f i o i erpd i n ga n be v h ni a t l i i ie i a
药 学 实 践 杂志
21 0 2年 5月 2 日第 3 5 0卷 第 3期
17 9
J u n lo a ma e t a r c i e Vo . 0,No 2, y 2 2 2 o r a fPh r c u i lP a t , 1 3 c c . Ma 5, 01
尼 莫地 平 口腔 崩解 片 的药 动 学及 相 对 生 物 利用 度 研 究
Hale Waihona Puke miit t nNi dpn a i i ne et gtbe n mo iiemak t a ltB wee( 5 . 3±5 6 nsr i mo iierpd ds tgai a ltA a d Ni dpn re be r 2 6 2 ao i n t 4.4)g ml 1 2 4 5±3 . / ,( 0 . 1 6 9 )g ml nC… ;( . 0 9±0 0 5)h,( . 3 7±0 1 3 nT… ;( . 7 4±0 0 1 6 / i 0 74 .3 13 1 . 2 )h i 023 . 3 )h,( . 9 8±0 1 1 nTl ;( 2 . 7 1 15 . 4 )h i / 6 2 7 2 ±9 . 3)g ml‘h) 3 4 6 80 /( ,( 5 . 3±9 . 4)g ml・ 62 /( h)i C0一 ,rse t ey h ia albl yo pddsnee t gtbe s n AU t ep ci l.T ebo v i it f a i iitg ai lt v a i r n a wa
尼莫地平片

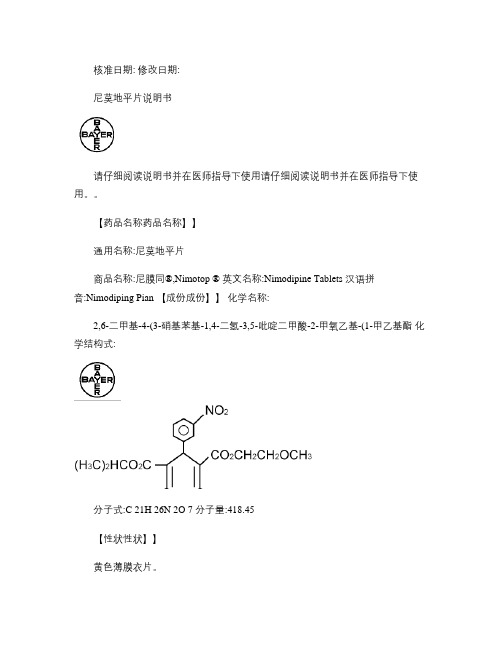
尼莫地平片英文名称:Nimodipine Tablets汉语拼音:Ni Mo Di Ping Pian【成份】本品主要成份及其化学名称: 尼莫地平1-甲基乙基-2-甲氧乙基,1,4-二氢-2,6-二甲基-4-(3-硝基苯基)-3,5-吡啶二羧酸酯其结构式为:分子式:C21H26N2O7分子量:418.45【性状】黄色薄膜衣片。
【适应症】1.作为尼莫地平注射液预先使用后的继续治疗,可预防和治疗由于动脉瘤性蛛网膜下腔出血后脑血管痉挛引起的缺血性神经损伤。
2.治疗老年性脑功能障碍,例如:记忆力减退,定向力和注意力障碍和情绪波动。
注意:尼莫地平片治疗前,应确定这些症状不是由需要特殊治疗的潜在疾病引起的。
【规格】30毫克/片【用法用量】1.预防和治疗由于动脉瘤性蛛网膜下腔出血后脑血管痉挛引起的缺血性神经损伤。
除非特殊处方,推荐下面的剂量指南:使用尼莫地平注射液治疗5-14天,继以尼莫地平片,一次60mg(一次2片),一日6次,建议服用7天。
一般来说,片剂应用少量水送服,与饭时无关。
连续服药间隔不少于4小时。
对于发生不良反应的患者,有必要减量或中断治疗。
严重的肝功能不良,尤其是肝硬化,由于首过效应的降低和代谢清除率的下降,导致尼莫地平生物利用度的升高,疗效和副作用尤其是血压下降就会更明显。
在这种情况下,根据血压情况适当减量,如有必要,也应考虑中断治疗。
2.治疗老年性脑功能障碍。
除非特殊处方,推荐剂量为一次30mg(一次1片),一日3次。
一般来说,片剂应用少量液体吞服,与饭时无关。
口服尼莫地平片几个月之后,必须重新评价是否仍存在治疗的适应症。
【不良反应】到目前为止所观察到的尼莫地平片的副作用如下所示:1.胃肠道系统: 恶心,胃肠道不适,个别患者有肠梗阻(肠麻痹所致肠排空障碍)。
2.神经系统: 头晕,头痛,虚弱;一些患者可能有中枢兴奋症状,如失眠,多动,兴奋,攻击性和多汗。
偶见运动过度和抑郁。
3.心血管系统:血压下降,尤其对于有基础血压增高的患者更是如此;潮红、多汗、暖热感、四肢水肿、心动过缓,偶见心动过速。
尼莫地平片说明书
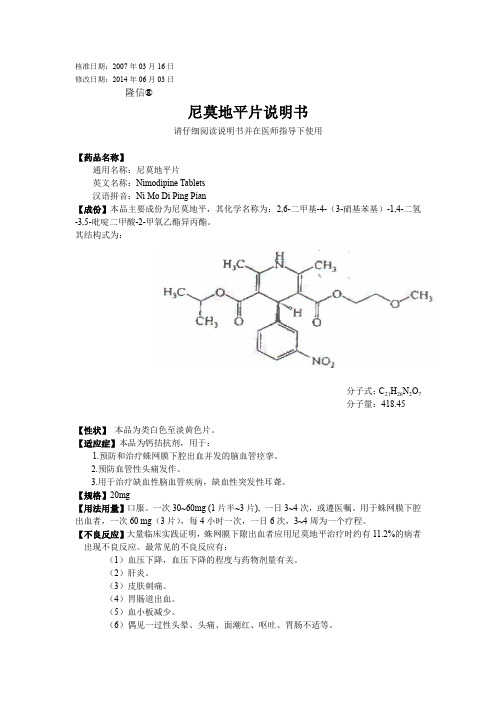
核准日期:2007年03月16日修改日期:2014年06月03日隆信®尼莫地平片说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:尼莫地平片英文名称:Nimodipine Tablets汉语拼音:Ni Mo Di Ping Pian【成份】本品主要成份为尼莫地平,其化学名称为:2,6-二甲基-4-(3-硝基苯基)-1,4-二氢-3,5-吡啶二甲酸-2-甲氧乙酯异丙酯。
其结构式为:分子式:C21H26N2O7分子量:418.45【性状】本品为类白色至淡黄色片。
【适应症】本品为钙拮抗剂,用于:1.预防和治疗蛛网膜下腔出血并发的脑血管痉挛。
2.预防血管性头痛发作。
3.用于治疗缺血性脑血管疾病,缺血性突发性耳聋。
【规格】20mg【用法用量】口服。
一次30~60mg (1片半~3片), 一日3~4次,或遵医嘱。
用于蛛网膜下腔出血者,一次60 mg(3片),每4小时一次,一日6次,3~4周为一个疗程。
【不良反应】大量临床实践证明,蛛网膜下隙出血者应用尼莫地平治疗时约有11.2%的病者出现不良反应。
最常见的不良反应有:(1)血压下降,血压下降的程度与药物剂量有关。
(2)肝炎。
(3)皮肤刺痛。
(4)胃肠道出血。
(5)血小板减少。
(6)偶见一过性头晕、头痛、面潮红、呕吐、胃肠不适等。
此外,口服尼莫地平以后,个别病人可发生碱性磷酸酶(ALP)、乳酸脱氢酶(LDH)、AKP 的升高,血糖升高以及个别人的血小板数的升高;可出现皮肤搔痒、热感,心率加快,无力、肢端水肿等。
少数可出现失眠、不安、易激动、多汗等症状;个别也可出现震颤、情绪抑郁和血小板减少。
【禁忌】尚不明确。
【注意事项】(1)脑水肿及颅内压增高患者须慎用。
(2)尼莫地平的代谢产物具有毒性反应,肝功能损害者应当慎用。
(3)本品可引起血压的降低。
在高血压合并蛛网膜下隙出血或脑卒中患者中,应注意减少或暂时停用降血压药物,或减少本品的用药剂量。
(4)可产生假性肠梗阻,表现为腹胀、肠鸣音减弱。
尼莫地平胶囊相对生物利用度的研究

尼莫地平胶囊相对生物利用度的研究张钧寿;张煊;范敏华;赖树清【期刊名称】《中国新药杂志》【年(卷),期】1997(000)0S1【摘要】选择8名健康男性志愿者,分别研究了“普利”尼莫地平胶囊、国产尼莫地平片和进口尼莫通片的相对生物利用度和药代动力学特征。
结果表明,国产尼莫地平片的相对生物利用度仅为24.1%,“普利”尼莫地平胶囊的相对生物利用度与进口尼莫通片等值,为94.82%;“普利”尼莫地平胶囊和尼莫通的体内吸收半衰期分别为0.722h,0.23h,中央室的消除半衰期分别为1.707h,0.817h,说明“普利”尼莫地平胶囊在体内释放较尼莫通慢,尼莫通的Cmax较高,但其高血浓维持时间仅为1.5~2h,而2h后“普利”尼莫地平胶囊的血浓较高,且“普利”尼莫地平胶囊的峰谷波动比尼莫通小,这预示着“普利”尼莫地平胶囊可能更有利于临床脑血管疾病的治疗。
【总页数】4页(P5-8)【作者】张钧寿;张煊;范敏华;赖树清【作者单位】中国药科大学【正文语种】中文【中图分类】R972.4【相关文献】1.尼莫地平胶囊人体生物利用度及生物等效性研究 [J], 郭仲坚;陶春蕾;许钒2.灯盏花素口崩片在Beagle犬体内的药动学及相对生物利用度研究 [J], 陈鹏;崔佳丽;周艺佳;张培培;赵高琼;梅晶;刘红斌;王京昆3.对乙酰氨基酚口服混悬液在Beagle犬体内相对生物利用度研究 [J], 张晓月;赵高琼;周艺佳;张培培;崔佳丽;梅晶;刘红斌;王京昆4.替比培南匹酯在犬体内的相对生物利用度研究 [J], 罗玉莹;周艺佳;崔佳丽;张培培;赵高琼;梅晶;刘红斌;王京昆5.替比培南匹酯在犬体内的相对生物利用度研究 [J], 罗玉莹;周艺佳;崔佳丽;张培培;赵高琼;梅晶;刘红斌;王京昆因版权原因,仅展示原文概要,查看原文内容请购买。
不同厂家尼莫地平片生物利用度比较分析

临床医药文章编号:1008—6919(2007)0卜0053—02中图分类号:R965.1文献标识码:A【论著】不同厂家尼莫地平片生物利用度比较分析陆怡(上海新药研究开发中心201809)【摘要】目的:研究不同厂家尼莫地平片(NIM0)生物利用度的差异。
方法利用HPLc法测定9例人体NIM0血药浓度,对三种国产NIM0片剂的相对生物利用度进行比较。
结果9例健康志愿者自身对照、服用A、B、C三种NIMO片剂120mg后经统计学处理,结果表明,NIMO片剂B与片剂A相比,AUC及Tmax无显著差异(P>0.05),Cmax有显著差异(O.01<p<O.05)。
NIMO片剂C与片剂A相比,Tmax无显著差异(P>O.05),AUC有显著差异(O.01<P<O.05),Cmax有极显著差异<P<O.01)。
NIM0片剂B、C相对于片剂A的相对生物利用度分别为85.23%和52.13%。
结论A厂生产的尼莫地平片(商品名:宝依恬)NIMO具有良好的生物利用度,优于其它厂家。
关键词:尼莫地平;生物利用度;HPLC法尼莫地平可有效改善脑出血后脑缺血…,临床广泛应用治疗各类脑血管疾病,已成为临床治疗脑血管疾病的首选药物,但NIMO为难溶性药物,结晶性NIMO在水中浓解度低,口服生物利用度低。
故笔者选取三个国内厂家的尼莫地平片进行生物利用度检测,以为临床择优选用提供参考。
1仪器与药品Waters高效液相色谱仪,配有510型恒流泵,486肠型UV监测器,PCM,TCM,Millennium2010色谱管理系统,DEC微机,XW一80A型漩祸混合器,800型离心沉淀器。
NIM0片剂A(规格30mg/片),NIMO片剂B(规格20mg/片),NIMO片剂c(规格20mg/片)。
正已烷,乙醚AR。
用前精留。
甲醇(HPLc专用)。
2血药浓度测定方法2.1色谱条件色谱柱::“BondapakC18柱(10um,300×3.9cmLD)流动相:甲醇:水(78:22,V/V),含O.5%三乙胺,冰醋酸调PH到7.94;检测入:237nm:流速:1.2ml/min;柱温:45℃;灵敏度:0.001AUFS.2.2血样预处理取血清1.Oml,精密加入内标氯氮平标准液(84ug/m1)4ul。
尼莫地平的药理作用

科研训练论文(文献综述)〔题目:尼莫地平的药理作用研究学生X X:学号:学院:化工学院班级:2015 年 12 月尼莫地平的药理作用研究摘要:尼莫地平是第二代1、4-二氢吡啶类钙离子通道拮抗剂,能够选择性地扩血管,兼有神经和精神药理活性,对冠脉也有较高选择性扩作用。
尼莫地平是目前脑血管疾病治疗的首选药物,特别针对老年痴呆症具有较高的价值。
其不良反响表现在血液系统、心血管系统、中枢神经系统等方面,故临床上应用时应根据病情合理用药。
关键词:尼莫地平、心脑血管、药理作用、临床应用。
引言随着生活水平日益提高,我国高血压发病率也逐渐增高,其中我国高血压脑出血发病率占全部脑卒中的20%-30%,在老年人中比拟常见,其致死率、致残率高[1]。
研究说明,目前大多数是炎性介质、细胞因子等氧化应激效应是引起继发性脑水肿导致神经功能恶化的主要原因,与高血压脑出血病症密切相关。
该文就是说明尼莫地平在扩血管改善脑血供给的临床研究,以与在治疗脑血管疾病方面的药理作用[2]、抗高血压作用的各方面的综述。
一、药理作用(一)作用机理1、选择性扩血管,而且没有盗血现象发生,在增加脑血流量的同时不影响脑部的代[3]。
2、是双氢吡啶类钙通道拮抗剂,呈脂溶性,易通过血脑屏障,在脑能够到达一定的浓度,改善血供给[4]。
3、尼莫地平对神经元直接作用,改变神经元的功能,具有精神和神经的药理活性[3]。
4、有对抗抑郁和改善意识和记忆的能力[4]。
〔二〕功能主治1、治疗急性缺血性脑血管疾病以与预防蛛网膜下腔出血并发脑血管痉挛[5]、偏头痛。
急性脑缺血时,缺血区脑组织皮素调节失衡,皮素作用于皮素受体,引起相应区域钙离子失衡,从而影响线粒体功能[6],导致病变,此时蛛网膜下腔出血。
尼莫地平作用是主要阻断细胞膜上钙离子进入细胞,同时还刺激神经细胞Ca+、-ATP酶增加活性,改善线粒体和质网对钙离子的调节功能,舒血管平滑肌,预防和解除脑血管痉挛,改善脑部微循环,从而到达治疗脑缺血和预防蛛网膜下腔出血导致脑血管痉挛[7]的目的。
【详细版】尼膜同说明书 拜耳医药保健有限公司

尼莫地平片(尼膜同)【成份】¥51.5030mg*20片/盒本品主要成份及其化学名称: 尼莫地平1-甲基乙基-2-甲氧乙基,1,4-二氢-2,6-二甲基-4-(3-硝基苯基)-3,5-吡啶二羧酸酯其结构式为:分子式:C21H26N2O7 分子量:418.45【性状】黄色薄膜衣片。
【药理毒理】1.药理:尼莫地平通过对与钙通道有关的神经元受体和脑血管受体的作用,保护神经元的功能,改善脑供血,增加脑的缺血耐受力。
另外的研究表明这种作用不会引起盗血现象。
临床总体印象评分、个体功能障碍、行为观察以及心理学测试都证实,尼莫地平对其它类型症状也有良好的作用。
对急性脑血流障碍患者的研究表明,尼莫地平能扩张脑血管和改善脑供血,且对大脑既往损伤区灌流不足部位灌注量的增加通常高于正常区域。
尼莫地平能明显地降低蛛网膜下腔出血患者的缺血性神经损伤及死亡率。
2.毒理(1) 急性毒性研究(2) 慢性毒性研究:口服给予狗尼莫地平片,每日最高剂量达到6.25mg/kg,观察1年,剂量为每日2.5mg/kg时具有较好耐受性;每日剂量为6.25mg/kg 时,产生轻微的心肌血流紊乱导致的心电图可逆改变,未见心脏及其它器官的组织病理学改变。
大鼠给药最高剂量达到每日90mg/kg,观察2年,具有较好耐受性。
(3) 生殖毒性研究:每日给药30mg/kg对雄性、雌性大鼠的生育能力及其后代均无损害。
每日给药10mg/kg对怀孕的大鼠的胚胎发育无影响。
每日给药30mg/kg,能抑制生长发育,导致胎鼠体重减少。
每日给药100mg/kg,死胎数增加,但未见致畸作用。
家兔胚胎毒性实验中,每日给药10mg/kg,未见致畸或胚胎毒性作用。
(4) 致癌毒性研究:大鼠每日给药90mg/kg,观察2年,未见潜在的致癌毒性;类似实验中,小鼠每日口服给药500mg/kg,未见尼莫地平潜在的致癌毒性。
(5) 致突变研究:广泛的致突变实验未观察到尼莫地平的致突变作用。
尼莫地平的种新用途

尼莫地平的种新用途
尼莫地平是一种新型的高分子材料,由于其特殊的物理和化学性质,使得尼莫地平具有多种潜在的应用。
本文将探讨尼莫地平的多个应用领域,包括新型能源材料、纳米材料、医用材料、环保材料等等。
一、新型能源材料
尼莫地平拥有优异的导电性能,可以作为锂离子电池、燃料电池等能源材料的极板。
锂离子电池是目前最为常见的电池类型之一,尼莫地平的导电性能可以使得锂离子电池的性能得到提升。
燃料电池则是一种利用氢气、甲烷等作为燃料,通过反应产生电能的装置,而尼莫地平可以作为电极材料,提升燃料电池的效率。
二、纳米材料
尼莫地平可以作为纳米材料的基础材料,与其他纳米材料进行(如金属、氧化物等)进行复合,可以得到具有更好性能的复合材料,如灵敏度更好的传感器、比表面更大的催化剂等。
三、医用材料
尼莫地平可以作为医用材料的一种,可以用作人工器官、假体等的材料,因为尼莫地平具有高的规整性和可塑性,可以
根据需要特定造型。
另外,尼莫地平的生物相容性良好,可以与人体组织相容,避免免疫排斥反应的发生。
四、环保材料
尼莫地平可以用作水处理剂的材料,可以去除水中的杂质和污染物,净化水质。
同时,尼莫地平还可以用作大气污染物的吸附剂,吸附大气中的有害气体,减少空气污染。
总之,尼莫地平作为一种新型的高分子材料,具有多种创新性的应用潜力,不仅可以在传统领域中得到应用,还可以推进新的领域的诞生和发展。
随着科学技术的不断进步,我们相信尼莫地平将有更为广泛的应用。
关于尼莫地平研究发展的综述

南华大学论文题目:心血管药物尼莫地研究发展学院:药学与生命科学学院专业班级:10级生科一班学生姓名:彭虹艳学号:20104020107内容摘要:作为钙通道阻滞药的二氢吡啶类药物,随着其发展和应用,不断有新的类型药物的产生.尼莫地平(尼莫通,nimodipin, nimotop)作为新一代二氢吡啶类钙通道阻滞药,能抵抗多种原因引起的脑血管痉挛,改善各种循环并增加病灶区的血流量,对脑细胞有保护作用。
本综述通过尼莫地平近五年来的研究发展主要分析了尼莫地平的产生、药理作用及其临床应用,介绍了尼莫地平在临床应用的配伍禁忌和不良反应,旨在让各位能从多方面了解尼莫地平。
关键词:尼莫地平、临床应用、Abstract:With the development and application of Dihydropyridine drugs---a calcium channel blocker, there have been many new types of drugs coming into being. Nimodipin, as a new generation of calcium channel blocker, can resist Vasospasm which is caused by various reasons, improve all kinds of circulation and increase the blood flow of focal area, as well as protect brain cells. This review mainly analyzes the generation, basic property, pharmacologic action and clinical application of Nimodipin through the studies of Nimodipin in recent five years. Meanwhile, it introduces the incompatibility and adverse reactions of Nimodipin in clinical application, aims to make students build an omnibearing system of Nimodipin.Key words: Nimodipin, clinical application,正文:一、尼莫地平的发展历史尼莫地平(nimodipine) 是德国拜耳研发的一种治疗脑功能障碍的新药,属于新一代二氢吡啶类钙通道阻滞剂,是目前预防与治疗蛛网膜下腔出血的首选药,并在治疗老年痴呆症方面也有较好疗效。
尼莫地平口腔崩解片的药动学及相对生物利用度研究

尼莫地平口腔崩解片的药动学及相对生物利用度研究高越;杨凌;邬蓉【期刊名称】《药学实践杂志》【年(卷),期】2012(030)003【摘要】目的研究尼莫地平口腔崩解片在人体内的药动学,比较其与市售尼莫地平片人体内药物动力学及相对生物利用度.方法将6名健康志愿者随机分成两组,交叉单剂量口服尼莫地平口腔崩解片A和市售片B各60 mg,采用HPLC 法测定血浆中尼莫地平的浓度.结果口服尼莫地平口腔崩解片A和市售片B后,主要药代动力学参数分别为Cmax(256.23±54.64) g/ml、( 102.415±36.96) g/ml;Tmax分别为(0.7049±0 035)h、(1.3317±0.123) h;T1/2分别为(0.2734±0.031)h、(1.1958±0.141) h;AUC0-1分别为(622.77±98.03) g/(ml·h)、(354.63±96.24)g/(ml·h).尼莫地平口腔崩解片A相对于市售片B的人体生物利用度为177.27%.结论自制尼莫地平口崩片速释效果明显,并能提高生物利用度.%Objective To research the pharmacokinetics and relative bioavailability of Nimodipine rapid disintegeating tablet in human body, which was compared with Nimodipine market tablets. Methods 6 cases of health volunteer were divide into two groups randomly , alternately taking rapid disintegrating tablet A and market tablet B of Nimodipine 60mg single dosage orally, HPLC was used to determine the concentration of Nimodipine in blood. Results The main Pharmacokinetics parameters after single oral administration Nimodipine rapid disintegeating tablet A and Nimodipine market tablet B were (256.23 ±54.64) g/ml, (102.415 ±36. 96)g/ml in Cmax (0. 7049 ±0. 035) h, (1. 3317 ±0. 123) h in Tmax; (0.2734±0.031) h, (1.1958±0. 141) h in T1/2; (622.77 ±98.03) g/(ml · h), (354.63±96.24) g/(ml · h) in AUC0-t, respectively. The bioavailability of rapid disintegeating tablet was 177.27% relative to market tablet. Conclusion Nimodipine rapid disintegealing tablet was capable of releasing rapidly, and had an enhanced bioavailahility as compared with market tablet.【总页数】6页(P197-202)【作者】高越;杨凌;邬蓉【作者单位】第二军医大学药学院,上海200433;第二军医大学药学院,上海200433;第二军医大学药学院,上海200433【正文语种】中文【中图分类】R743【相关文献】1.盐酸昂丹司琼口腔崩解片的人体药动学和生物利用度研究 [J], 周梅;孙刚;武谷2.盐酸氨溴索口腔崩解片的相对生物利用度与生物等效性研究 [J], 张丽芳;胡晓;甘小健;徐文炜;张红3.消旋卡多曲口腔崩解片相对生物利用度研究 [J], 秦永平;余勤;梁茂植;邹远高;张迅;李熙鹏4.尼莫地平在健康人体内的药动学和相对生物利用度 [J], 乔海灵;郜娜;张莉蓉;张启堂;刘凤芝;郭玉忠5.尼莫地平健康人体药动学和相对生物利用度研究 [J], 赵杰;阚全程;刘维春因版权原因,仅展示原文概要,查看原文内容请购买。
口服药物的生物利用度

口服药物的生物利用度摘要:本文通过检索国内外相关文献综述了口服药物的生物利用度的研究进展,特别归纳了提高口服药物生物利用度的方法。
关键词:生物利用度口服药物前体药物微粒给药系统1、概述生物利用度是指制剂中药物被吸收进入人体循环的速度与程度。
生物利用度是反映所给药物进入人体循环的药量比例,它描述口服药物由胃肠道吸收,及经过肝脏而到达体循环血液中的药量占口服剂量的百分比。
口服给药是临床给药尤其是长期用药的首选给药途径。
药物的口服生物利用度低不仅导致个体间和个体内差异、血药浓度波动大,同时增加生产成本,增大机体毒性的可能性。
由于药物的物理化学性质和生物药剂学性质各异,所以导致口服生物利用度低的原因也呈多样化。
随着高通量筛选和组合化学的发展,通常大部分有活性的化合物都属于难溶性化合物,其中40%以上的候选药物由于生物药剂学性质不佳而在药物开发研制过程中失败。
FDA 工业指南(1997)根据药物的溶解性及膜通透性将所有药物分成4 类(生物药剂学分类系统,biopharmaceutical classification system, BCS)①高溶解性和高透膜性;②低溶解性和高透膜性;③高溶解性和低透膜性;④低溶解性和低透膜性。
其中①类无生物利用度问题,易于制成口服制剂;④类最难输送,应采用其他给药途径。
我们的主要任务就是采用各种制剂手段提高②③类药物的口服生物利用度。
影响生物利用度的因素影响口服药物吸收的主要因素即药物的理化性质、药物在胃肠道的稳定性、药物透过肠粘膜吸收、药物在肠壁代谢及外向性载体转运等方面。
【1】①药物的理化特性:立体化学结构(包括手性)、进入细胞膜的比例、分子量、分子体积、pKa、溶解度、渗透性、亲水亲脂性、化合物稳定性、分配系数、剂型特性(如崩解时限、溶出速率) 及一些工艺条件等。
②胃肠道环境和解剖生理状态:胃肠道内液体的作用( 肠pH 值、胆汁的影响、淋巴液流量等) ,药物在胃肠道内的转运情况( 小肠上皮细胞中各种特异性转运系统和多药耐药性(MDR)、p-糖蛋白等) ,吸收部位的表面积与局部血流,药物代谢的影响,肠道菌株等。
人血浆中尼莫地平的HPLC-Ms测定及其片剂的生物等效性

人血浆中尼莫地平的HPLC-Ms测定及其片剂的生物等效性邹健军;丁黎;谭文明;张树来【期刊名称】《中华临床医药杂志》【年(卷),期】2004(005)017【摘要】目的建立人血浆中尼莫地平的HPLC-MS法,以测定国产片剂的人体生物等效性.方法血样经碱化后乙酸乙酯提取,进行HPLC-MS分析,色谱柱Hypersil ODS(5μm,150mm×4.6mm),流动相为甲醇-水冰醋酸(85:15:0.1),内标为尼群地平,检测离子为[M+Na]+44.1(尼莫地平)[M+Na]+383.1(内标) ,裂解电压为80V.20名健康受试者交叉口服两种国产尼莫地平片剂,计算主要药动学参数,并估算其相对生物利用度,判断生物等效性.结果在1-200ng/ml范围内尼莫地平与内标峰面积比值与浓度线性关系良好(r=0.099845),最低可定量浓度为0.3ng/ml,提取回收率为74.8%-93.2%.以AUC0-12计算的片剂相对生物利用度为99.8%±6.6%.结论本实验建立的分析方法灵敏、准确、简便.统计学结果表明两种制剂量生物等效.【总页数】3页(P5-7)【作者】邹健军;丁黎;谭文明;张树来【作者单位】南京医科大学附属南京第一医院药剂科,江苏,南京,210006;中国药科大学药物分析教研室,江苏,南京,210009;中国药科大学药物分析教研室,江苏,南京,210009;中国药科大学药物分析教研室,江苏,南京,210009【正文语种】中文【中图分类】O652.63【相关文献】1.HPLC-MS法测定人血浆中酮康唑浓度及其生物等效性研究 [J], 宋祥珍;李纬;曹芳;张雯2.HPLC-MS法测定人血浆中溴己新浓度及生物等效性研究 [J], 张雯;冯芳;王娅3.HPLC-MS/MS法快速测定人血浆中氟哌噻吨浓度及生物等效性研究 [J], 谭献文;廖日房;温预关4.HPLC-MS测定人血浆中雷米普利和雷米普利拉浓度及其生物等效性研究 [J], 冯桂梅;朱运贵5.人血浆中穿心莲内酯的HPLC-MS测定及生物等效性研究 [J], 张志华;何周康;周彦彬;厉宇红;田娟;左英;丁劲松因版权原因,仅展示原文概要,查看原文内容请购买。
尼莫地平过饱和自微乳的研制

尼莫地平过饱和自微乳的研制王姿媛;唐洪梅;薛秀清;蔡晓虹【摘要】目的制备尼莫地平过饱和自微乳化给药系统(NMP S-SMEDDS),并对其体外特性进行考察.方法以平均粒径、平均电位、乳化时间为评价指标,通过星点设计-效应面优化法优化自微乳化给药系统(SMEDDS)处方;以PVPK30为促饱和物质,制备NMP S-SMEDDS,并通过考察PVPK30用量对S-SMEDDS体外溶出行为的影响,筛选PVPK30的适用量.结果 SMEDDS的最优处方为油酸乙酯∶吐温-80∶Transcutol P=17.25∶49.16∶44.76(质量比);以PVPK30质量分数为2%,尼莫地平质量分数为2.5%制备得到的NMP S-SMEDDS的粒径为(33.41±0.48) nm,Zeta电位为(-9.62± 1.49)mV,60 min的体外溶出度达90.4%,比市售尼莫地平片的溶出度明显提高.结论 NMP S-SMEDDS可提高尼莫地平的体外溶出度.【期刊名称】《广东药学院学报》【年(卷),期】2014(030)002【总页数】5页(P127-131)【关键词】尼莫地平;过饱和自微乳化给药系统;体外溶出度【作者】王姿媛;唐洪梅;薛秀清;蔡晓虹【作者单位】广州中医药大学第一附属医院药剂科,广东广州510405;广州中医药大学第一附属医院药剂科,广东广州510405;广州中医药大学第一附属医院药剂科,广东广州510405;广州中医药大学第一附属医院药剂科,广东广州510405【正文语种】中文【中图分类】R944自微乳化给药系统(self-microemulsifying drug delivery systems,SMEDDS)是由药物、油相、乳化剂和助乳化剂组成的制剂。
SMEDDS中的药物被包裹在油滴中,口服后遇体液在胃肠蠕动下自发分散成O/W型乳滴,乳滴粒径分布在10~100 nm之间[1]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
国产尼莫地平片的人体相对生物利用度研究
【摘要】10例男性健康志愿者交叉口服60 mg国产和德国产尼莫地平片,以HPLC测定血浆药物浓度,计算国产片的相对生物利用度。
结果表明:二种片剂的血药浓度一时间曲线均符合开放式一房室模式。
国产及德国产片剂达峰时间分别为52.65 min及51.36 min;Cmax分别为26.61 mg/L和29.05 mg/L;auc∞。
为4 170.76及4 291.36 mg/(min•L),二种片剂主要药代动力学参数比较无统计学显著差异(P>0.05)。
国产尼莫地平片相对生物利用度为97%,经统计学处理证实二种片剂生物等效。
【Abstract】 A single oral 60 mg of tablets nimodipine(Germany)or d9omestic nimodipine was given to 10 healthy male volunteers in a randomized crossover study.Plerformance liquid chromatography method.It was found that main pharmacokinetic prarmefers of domestic nimodipine tablet were:Tpeak:52.65±17.08 min,Cmax:26.61±19.59/L,T1/2Ke:84.04±52.68 min,ACUO∞4170.76±2296.71 μg/min respectively.Relative bioavailability of domestic nimodipine tablet was 97%±7%compared with nimodipine(Germany)tablet.
【Key words】Nimodipine;bioavailbility;HPLC
尼莫地平(nimodipine)是二氢吡啶类钙拮抗剂,因对脑血管具有良好的选择性,且无明显的药物不良反应,现已成为治疗缺血性脑血管疾病比较理想的药物。
本研究采用HPLC方法对口服国产尼莫地平片及国外尼莫地平片剂的的血药浓度进行比较,并对二种片剂的生物等效性作出评价[1]。
1 材料与方法
1.1 药品及试剂国前尼莫地平片由西安大庆制药厂提供,批号:970701,规格20 mg/片。
进口尼莫平片,德国
拜耳公司生产,批号:BBXK1 EXP 092001,规格30 mg/片。
尼莫地平对照品,批号:0270-9701,购于中国药品生物制品检定所。
试剂:乙腈为色谱纯,乙醚为分析纯;各种溶液的配制均使用超纯水。
1.2 受试者选择健康男性受试者10人,年龄(24.4±1.71)岁,体质量72.8±9.25 kg,经生化检验血常规、尿常规、肝功、肾功、心电均正常。
实验前一周及实验期间未服用其它任何药物,实验期间禁烟、酒,并统一进标准餐,签药知情同意书。
1.3 仪器及色谱条件Waters2010高效液相色谱仪(717自动进样器,510泵,
996PDA检测器,Millenium色谱管理系统),色谱柱:spherisorbC18 10μ,粒径250 mm×4.6 mmID检测波长238 nm;流动相:乙腈:水(60:40V/V)流速1.5 ml/min,用前超声脱气。
1.4 试验方案10名志愿受试者随机分成两组,每组5人,第1组服国产尼莫地平60 mg,第2组服进口片60 mg。
一周后进行第二次试验,两组交叉服用同等剂量不同厂家的药品,药片约用200 ml温开水服用,各受试者不允许剧烈活动,在服药后0时10、20、40、60、90、120、180、240、360、480 min于肘静脉取血5 ml,置于肝素抗凝管中,离心,取2 ml血浆供分析。
同时观察可能出现的药物不良反应。
1.5 样品处理方法取肝素化血浆2 ml,然后用乙醚提取两次,每次3 ml,涡旋混合,4000转/分离心5 min后,小心取出乙醚层,转移至另一只试管中,并于40℃水浴蒸干,残渣用200 ml流动相溶解即可进样分析。
80 ml进样,外标法定量分析。
所有操作避光进行[2]。
1.6 数据处理数据采用MCPKP(自动药物动力学程度)处理,拟合,得到受试者的各项药动学参数。
用梯形法计算AUC408[3]。
1.7 统计分析对主要药动学参数进行方差分析,并用单双侧七检验和(1-2a)置信区间法进行生物学效性评价[4]。
2 结果
2.1 方法学研究
2.1.1 色谱行为在本实验条件下,尼莫地平与血浆中杂质得以良好分离,尼莫地平的保留时间为6.39 min左右。
2.1.2 血浆中标准曲线的制作取肝素化血浆2 ml,精密加入不同浓度的标准液,使其血浆中尼莫地平的浓度分别为2.5、5、10、20、30、40、50、75、100 mg/L,按前述方法处理样品,经HPLC测定,记录样品峰面积,以样品峰面积(A)对浓度(C)作线性回归,得出血浆标准曲线:C=-0.955 5+6.498×10-4A,r=0.998,该方法的最小检测度为1 μg/L。
2.1.3 方法精密度和方法回收率方法精密度在空白血中精密加入不同量的尼莫地平准品,使血浆浓度分别为5、20、40 μg/L;RPV“按样品处理方法”项下操作,测定日内变异和日间变异,结果见表1。
2.2 药代动力学研究两种片剂交叉给予10名受试者后的平均血药浓度见表3,血液浓度一时间数据经计算机拟合符合口服一室模型,其药代动力学参数见表4。
经方差分析表明两种片剂的药代动力学参数间差异无统计学意义(P>0.05),进一步经单双侧t检验和(1-2a)置信区间法分析显示两种片剂的Cmax,T1/2k,AUCO-∞,具有生物等效性。
3 讨论
上述试验结果表晨,两种片剂在人体内的吸收、分布、排泄性质颇为相似。
经研究证明,国产尼莫地平片剂的药代动力学及生物利用度与进口片几乎一致。
经统计学检验无明显差异(P>0.05)。
国产尼莫地平片和进口片的体内试验结果经药代动力学程序拟合后,从得到药代动力学参数来看,国产尼莫地平片与进口片的体内吸收半衰期分别为18.55、17.27 min;中央室的消除半衰期分别为84.04、80.88 min。
说明国产片在体内释放较进口片剂慢。
进口尼莫平片的Cmax比较高,但两者均在有效血浓度以上。
在试验过程中,各受试者降压反应轻微,无其它副作用出现。
尼莫地平国产片与进口片的相对生物利用度为97%;经统计学分析证明,国
产片与进口片生物等效。
