第十二章s区元素
第十二章 s区元素

5、举例说明铍与铝的相似性。 、举例说明铍与铝的相似性。
答:Be 和Al 单质及化合物性质有许多相似之处,可以从以下 几个方面来理解: (1) Be 和Al 都是两性金属,不仅能溶于酸也都溶于强碱,放 出氢气; (2) Be 和Al 的氢氧化物都是两性化合物,易溶于强碱; (3) Be 和Al 都是共价化合物,易升华,聚合,易溶于有机溶 剂; (4) Be 和Al 常温下不与水作用,与冷的浓硝酸接触时都发生 钝化现象; (5) Be 和Al 的盐都易水解。
12、关于s 区元素的性质下列叙述中不正确的是 A、 由于s 区元素的电负性小,所以都形成典型的离子型化 、 由于 区元素的电负性小, 合物 B、 在s 区元素中,Be、 Mg 因表面形成致密的氧化物保护 膜而对水较稳定 C、 s 区元素的单质都有很强的还原性 D、 除Be、 Mg 外,其他s 区元素的硝酸盐或氯酸盐都可做 焰火材料 13、关于Mg , Ca , Sr , Ba 及其化合物的性质下列叙述中不正确 的是 A、 单质都可以在氮气中燃烧生成氮化物M3N2 B、 单质都易与水、水蒸气反应得到氢气 、 单质都易与水、水蒸气反应得到氢气(p378) C、M(HCO3)2 在水中的溶解度大于MCO3 的溶解度 (p392) D、这些元素几乎总是生成+2 价离子
碳酸盐受热分解的难易程度与阳离子的极化作用 有关。阳离子对CO32-离子的极化作用,使CO32-不稳定 离子的极化作用, 有关。阳离子对 以致分解,极化作用越大越易分解。 质子) 以致分解,极化作用越大越易分解。H+(质子)的极 化作用超过一般金属离子,所以有下列热稳定性顺序: 化作用超过一般金属离子,所以有下列热稳定性顺序: M2CO3>MHCO3>H2CO3 p430另外一种解释 另外一种解释
无机化学S区元素概述单质及其物理化学性质

无机化学S区元素概述单质及其物理化学性质S区元素是指周期表中第三周期的元素,包括Sc、Ti、V、Cr、Mn、Fe、Co、Ni、Cu和Zn。
这些元素的单质是指它们在自然界中以纯态存在的形态。
下面将对这些S区元素的单质及其物理化学性质进行概述。
Scandium(Sc)是一种银白色金属,熔点1541℃,沸点2836℃。
它的密度为2.989 g/cm³,熔化热为15.8 kJ/mol。
Scandium的化学性质活泼,可以与氢气、氧气和氮气反应。
它可以形成多种化合物,如ScCl3、Sc2O3等。
Titanium(Ti)是一种银灰色金属,熔点1668℃,沸点3260℃。
它的密度为4.506 g/cm³,熔化热为13.8 kJ/mol。
Titanium具有低密度、高强度和良好的耐腐蚀性。
它与氧、氮、氢等非金属元素反应生成化合物,如TiO2、TiN等。
Vanadium(V)是一种银白色金属,熔点1890℃,沸点3380℃。
它的密度为6.0 g/cm³,熔化热为21.5 kJ/mol。
Vanadium的化学性质活泼,可以与氧气、氮气和氟气反应。
它可以形成多种氧化态,如V2O5、VO2等。
Chromium(Cr)是一种银灰色金属,熔点1907℃,沸点2672℃。
它的密度为7.18 g/cm³,熔化热为20.5 kJ/mol。
Chromium的外层电子构型为3d54s1,具有良好的抗腐蚀性。
它可以形成多种化合物,如Cr2O3、CrCl3等。
Manganese(Mn)是一种银灰色金属,熔点1244℃,沸点1962℃。
它的密度为7.21 g/cm³,熔化热为13.2 kJ/mol。
Manganese与氧气反应生成二氧化锰(MnO2),具有一定的催化性能。
它还可以形成多种化合物,如MnCl2、MnSO4等。
Iron(Fe)是一种银灰色金属,熔点1538℃,沸点2861℃。
它的密度为7.874 g/cm³,熔化热为13.8 kJ/mol。
新312第12章s区元素

Chloride, silicate, phosphate, sulfide, oxide, free element, sulfate, carbonate
氯化物,硅酸盐,磷酸盐, 硫化物, 氧化物, 单质, 硫酸盐,碳酸盐
Occurrences of metals 存在方式
• free elements单质— Au、Ag、Pt、Cu; • binary compounds 二元化合物 — oxides 氧化物、 — sulfides 硫化物、 — halides 卤化物… • oxo-acids 含氧酸盐 — carbonates 碳酸盐、 — silicates 硅酸盐、 — sulfates 硫酸盐…
Cs Ba Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn
In engineering, metals can be classified as 按工程技术分
• ferrous metals 黑色金属: 如Fe、Mn、Cr • non-ferrous metals有色金属: • and the non-ferrous metals can be divided as the heavy, light, noble, rare, and radioactive.又分重、轻、贵、稀有、 放射性
The properties of metals性质(1)
Physical properties
• luster光泽: most metal are silvery.金属大多呈银 白色, Au—golden金黄色,Bi—pale red淡红, Cu—紫红色;
• density密度: light metals with the density less than 5gcm3; 按5g.cm3为标准,分为轻金属, 否则 为重金属; • melting point 熔点: the melting points between metals show great difference. 金属熔点差别很 大。 如:Hg (liquid)、W (3380℃);
(整理)s区、d区、ds区重要元素及其化合物.

s区、d区、ds区重要元素及其化合物(s Block, ds Block, d Block Elements and Compounds)9.1 s区元素s区元素中锂(Lithium)、钠(Sodium)、钾(Potassium)、铷(Rubidium)、铯(Cesium)、钫(Francium)六种元素被称为碱金属(alkali Metals)元素。
铍(Beryllium)、镁(Magnesium)、钙(Calcium)、锶(Strontium)、钡(Barium)、镭(Radium)六种元素被称为碱土金属(alkaline earth metals)元素。
锂、铷、铯、铍是稀有金属元素,钫和镭是放射性元素。
碱金属和碱土金属原子的价层电子构型分别为ns1和ns2,它们的原子最外层有1~2个电子,是最活泼的金属元素。
9.1.1 通性碱金属和碱土金属的基本性质分别列于表9-1和表9-2中。
表9-1碱金属的性质碱金属原子最外层只有1个ns电子,而次外层是8电子结构(Li的次外层是2个电子),它们的原子半径在同周期元素中(稀有气体除外)是最大的,而核电荷在同周期元素中是最小的,由于内层电子的屏蔽作用较显著,故这些元素很容易失去最外层的1个s电子,从而使碱金属的第一电离能在同周期元素中最低。
因此,碱金属是同周期元素中金属性最强的元素。
碱土金属的核电荷比碱金属大,原子半径比碱金属小,金属性比碱金属略差一些。
s区同族元素自上而下随着核电荷的增加,无论是原子半径、离子半径,还是电离能、电负性以及还原性等性质的变化总体来说是有规律的,但第二周期的元素表现出一定的特殊性。
例如锂的EΘ(Li+/Li)反常地小。
表9-2碱土金属的性质s区元素的一个重要特点是各族元素通常只有一种稳定的氧化态。
碱金属的第一电离能较小,很容易失去一个电子,故氧化数为+1。
碱土金属的第一、第二电离能较小,容易失去2个电子,因此氧化数为+2。
在物理性质方面,s区元素单质的主要特点是:轻、软、低熔点。
普通化学S区元素
的电力。一座100千瓦的电厂一年消耗5吨锂。(扎布耶湖)
S区元素用途
金属钠
1. 作为还原剂制造某些难熔的金属如铀、钍、锆等,特别
是还原制备钛:
加热
TiCl4 + 4 Na
Ti + 4 NaCl
2. 因具有高的导热性和低的中子吸收能力,被用做快速增
殖反应堆的致冷剂。
3. 制作钠电缆、钠基电池和钠硫电池等。
(3) 焰色反应 (flame reaction)
碱金属和碱土金属的化合物在无色火焰中燃烧 时 , 会 呈 现 出 一 定 的 颜 色 , 称 为 焰 色 反 应 (flame reaction)。可以用来鉴定化合物中某元素的存在,特 别是在野外。
元 素 Li
Na K
Rb
Cs
Ca
Sr
Ba
颜 色 深红 黄 紫 红紫 蓝 橙红 深红 绿
3.形成配位氢化物
4LiH AlCl 3 (无水)乙醚Li[AlH 4 ] 3LiCl
铝氢化锂
Li[AlH 4 ] 受潮时强烈水解 LiAlH 4 4H 2O LiOH Al(OH) 3 4H 2
12.3.2 氧化物
1.形成三类氧化物 正常氧化物(O2-):1s2 2s2 2p6 过氧化物(O22-):
钾的最主要用途是制造钾肥。
庄稼是非常需要钾的。庄稼缺乏钾,茎秆便不会硬挺直立,易倒伏,对外界的抵抗力也大大减强。平均起来,每收获一吨小麦或 一吨马铃薯,就等于从土壤中取走五公斤钾;收获一吨甜萝卜,相当于取走二公斤钾。全世界平均每年要从土壤中取走2,500万吨钾! 有 入 才 有 出 , 这 也 就 是 说 , 全 世 界 每 年 必 须 至 少 要 往 土 壤 中 施 加 合 钾 2,500 万 吨 的 钾 肥 ! 含钾的化学肥料,主要有硝酸钾、氯化钾、硫酸钾、碳酸钾。人们是从钾长石(花岗岩)、海水等中提取钾的化合物。特别是海水,含 有不少氯化钾。在农家肥料中,以草木灰,特别是向日葵灰,含钾最多,这是因为植物本来就从土壤中吸收了钾,那么,把它烧成灰 后,灰中当然也就含有钾了。在每吨粪便中,大约含有六公斤钾。
S区元素

混合盐密度增大,液Na浮在熔盐表面,
易于收集
金属钾能否采用类似制钠的方法制备呢?
不能采用同类方法,其原因是: (1)金属 K 与 C 电极可生成羰基化合物 (2)金属 K 易溶在熔盐中,难于分离 (3)金属 K 蒸气易从电解槽逸出造成爆炸
N2K合金 (或K)蒸气
Na N2
排泄阱 NaCl 渣 热
热
1. 燃烧反应的△G负值大小决定。Na生成Na2O、
Na2O2 和 NaO2的△G分别是 ―376 kJ·mol-1,
― 430 kJ·mol-1和― 389.2 kJ·mol-1, 因此燃烧产 物就是 Na2O2 。 2. △G 的大小由 rGm rHm TrSm 决定。 其中 △G的大小主要由 rHm来决定。rHm 则要由玻 恩-哈伯循环来决定。
二、氧化物
正常氧化物(O2-):1s2 2s2 2p6
过氧化物(O22-):
“能KK量(σ效2s )应2 (σ”*2要s )2求(σ 2体p )2积(π较2p )大4 (π的*2过p )4氧 离超子氧、化超物(氧O2离-) 子和臭氧离子更易被较 大的金K属K(阳σ 2s离)2 (子σ *所2s )2稳(σ定2p )。2 (π 2p )4 (π *2p )3
类型
在空气中 直接形成
间接形成
正常氧化物
Li、Be、Mg Ca、Sr、Ba
ⅠA、ⅡA族 所有元素
过氧化物
Na
除Li Be外的 所有元素
超氧化物
Na、K、 除Be、Mg、 Rb、Cs Li外所有元素
Na2O2 + 2Na 2Na2O 2KNO3 +10K 6K2O + N2
过氧化物和超氧化物 1. 在碱性介质中是强氧化剂,常用作 熔矿剂。 例 2Fe(CrO2)2+7Na2O2 →
江苏师范大学《无机化学》习题库及答案第十二章 s区元素

第十二章S区元素一、选择题(每题3分,共30分)( ) 1. 钠在空气中燃烧,得到的产物是(A) Na2O (B) Na2O2(C) NaO2(D) Na2CO3( ) 2. 下列氢氧化物中碱性最强的是(A) LiOH (B) NaOH (C) KOH (D) Mg(OH)2 ( ) 3. 下列氢氧化物中溶解度最小的是(A) LiOH (B) NaOH (B) KOH (D) RbOH( ) 4. 下列哪一个氢氧化物是两性的?(A) Be(OH)2(B) Mg(OH)2(C) Ca(OH)2(D) Sr(OH)2( ) 5. 下列晶体中熔点最高的是(A) BeCl2(B) MgCl2(C) CaCl2(D) SrCl2 (E) BaCl2( ) 6. 下列物质中热稳定性最高的是(A) BeCO3(B) MgCO3(C) CaCO3(D) SrCO3 (E) BaCO3( ) 7.下列成对元素中化学性质最相似的是()(A) Be和Mg (B) Mg和Al (C) Li和Mg (D) Be和B( ) 8. 氢化铷与水反应可放出氢气,则下列叙述正确的是()(A) 氢化铷溶于水显酸性。
(B) 氢化铷中的氢离子被还原为氢气。
(C) 氢化铷与水反应时,水是还原剂。
(D) 氢化铷中的氢离子最外层有两个电子。
( ) 9. 现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L。
这种碱金属可能是( )(A) Na (B) K (C) Rb (D) Cs( ) 10. 我国人民很早就知道用焰色反应来鉴别某些物质。
南北朝时期,著名的炼丹家和医药大师陶弘景在他的《本草经集注》中就有这样的记载:“以火烧之,紫青烟起,云是真硝石也”。
这一记载所鉴别出的物质应该是()(A) NaNO3(B) KNO3(C) KMnO4(D) I2二、填空题(每空1分,共31分)1. 钠与水剧烈作用,生成___和____,易引起燃烧和爆炸,需贮存在_________或_________中,而锂的密度很小,能浮在煤油上,所以将其保存在__________。
S区常见元素

S区常见元素一、教学目的1、掌握钠、钾、过氧化钠的主要性质;2、了解锂、钠、钾的微溶盐,Mg、Ca、Ba的氢氧化物及其盐类的溶解情况。
3、掌握用焰色反应检验元素的操作。
二、实验提要碱金属、碱土金属分属周期系第ⅠA、ⅡA 族,价电子构型ns1、ns2,属s 区元素。
其单质是最活泼的金属和还原剂,且从上到下,从碱金属到碱土金属活泼性增强。
在空气中能迅速地与O2、CO2、H2O 作用(Rb、Cs 在空气中自燃),需保存在煤油或液体石蜡中(Be、Mg 由于生成致密氧化膜而除外)。
在空气中燃烧时,锂、碱土金属生成正常氧化物;钠主要生成过氧化物;而钾、铷、铯则主要生成超氧化物。
Na2O2为淡黄色粉末状物质,与水或稀酸反应生成氢氧化钠或钠盐,同时产生H2O2。
H2O2会立即分解放出O2,所以过氧化钠具有强碱性和强氧化性。
与水相遇,Be、Mg 由于表面形成致密氧化物保护膜而对水稳定,分别需水蒸气及热水才反应,其它元素都易与冷水反应生成相应氢氧化物,放出氢气。
Na、K、Rb、Cs 与水反应随其金属性递增、单质熔点的减小,而剧烈程度加强。
碱金属与汞在常温下生成的合金称为汞齐,根据金属与汞的相对含量可呈固体或液体状态,由于可降低碱金属的反应活性,常用作化学反应中的温和还原剂。
在氢氧化物方面,碱金属的氢氧化物除LiOH 溶解度较小外,其余都很大,且都是强碱。
碱土金属的氢氧化物除Be(OH)2呈两性外,其余也都是碱性,但由于溶解度不如碱金属,所以碱性要弱得多,但从上到下,碱性是增强的,这与它们氢氧化物溶解度增大的趋势相一致。
绝大多数碱金属所形成的盐都是可溶的,并与水形成水合离子,仅有少数碱金属盐是难溶的,如LiF、Li2CO3、Li3PO4、Na[Sb(OH)6]、KHC4H4O6等均为白色微溶或难溶物。
碱土金属的难溶盐则要多得多,一般除氟外,一价阴离子是可溶的,除S2-以外,高价阴离子都是难溶的,如碳酸盐、磷酸盐、草酸盐。
北师大考研无机化学复习题第十二章

第9 章s 区元素一、教学基本要求1. 了解s区元素的物理性质和化学性质,能解释碱金属与水、醇和液氨反应的不同;2. 了解主要元素的矿物资源及单质的制备方法,特别注意钾和钠制备方法的不同;3. 了解s区元素的氢化物、氧化物、氢氧化物的性质,特别注意氢氧化物的碱性变化规律;4. 了解s区元素的重要盐类化合物,特别注意盐类溶解性的热力学解释;5. 会用离子极化理论解释碳酸盐分解规律;6. 了解对角线规则和锂、铍的特殊性。
二、要点1. 汞齐(amalgam )又称汞合金,汞的特性之一是能溶解除铁以外的许多金属而生成汞齐。
汞与一种或几种金属形成汞齐时,含汞少时是固体,含汞多时是液体。
天然的有金汞齐,银汞齐,人工制备的有:钠汞齐、钾汞齐、锌汞齐、锡汞齐、铅汞齐等。
2. 熔盐电解法(Molten-salt electrolysis)指以熔融态盐类为原料的电解方法,常用于制备不能由水溶液中制备的金属,如碱金属、碱土金属以及钍、钽混合稀土金属的生产。
有时为降低熔体的熔点,节省电能,须加入一定量的助熔剂。
3. 热还原法(Thermo-deoxidization)用化学活性较强的金属,将被还原的金属从其化合物中置换出来,以制备金属或其合金的方法。
4. 冠醚(Crown ether)分子结构类似皇冠的“大环多醚”。
最常用的有18-冠-6 (如下图中的a)、二环己基-18-冠-6及二苯基18-冠-6等。
冠醚对K+、Na+及其他阳离子有很强的选择性络合,F- ),提K + X- 表示( X=MnO4高了裸阴离子的活性。
冠醚在有机合成中常用作“相转移反应的催化剂”。
5.穴醚(Cryptant)分子结构类似地穴的“大环多醚”。
穴醚几乎能够实现对K+和Na+离子的完全分离,选择性可高达105:1。
如下图中的(b) (c)所示。
(a) (b) (c)6. 钠的主要化学反应提要:7. 由氢氧化铍可以制成金属铍及其它化合物:8. 钙的主要化学反应提要:9. 由硫酸钡可制取各种化合物:Ca 33)2Ca(ClO)2B aSO 4C B 22O NaCO 3B 33B aO 2B a(OH)23H 2O 2B 3)2·Ba B eSO 44H 2O H 2SO 42B e(NO)34H 2O (NH 42eF 410002B e 蒸发至干·CCl 4B eCl ·NH 4HF 2oo NaO 2+CO+HO 3电解10. 对角线规则(diagonal rule)在周期表的二、三周期中,某一元素的性质和它左上方或右下方的元素性质的相似性,称为对角线规则。
第12章 s区和ds区元素吉林大学无机化学
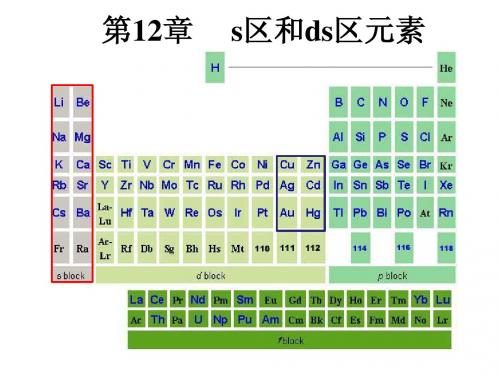
原 子 半 径 增 大 , 金 属 性 增 强
IA
Li Na K Rb Cs
IIA
Be Mg Ca Sr Ba
原子半径减小,金属性减弱
特殊性:Li 的 E 值负值最大
硫脲
HCl
③ Cu,Ag,Au可溶于氧化性酸
Cu 4HNO 3 (浓) Cu(NO 3 ) 2 2NO 2 2H 2 O Ag 2HNO 3 (浓) AgNO 3 NO 2 H 2 O Cu 2H 2 SO 4 (浓) CuSO 4 SO 2 2H 2 O 2Ag 2H 2 SO 4 (浓) Ag 2 SO 4 (s) SO 2 2H 2 O Au 4HCl( 浓) HNO 3 (浓) H[AuCl 4 ] NO(g) H 2 O
第12章
s区和ds区元素
1.金属单质的物理性质
s区和ds区元素通常仅以s电子参与成键,故熔点、 沸点、气化热等低于其他d区元素。特别是Hg,由 于6s电子的“惰性电子对效应”形成的金属键更弱, 故在温室下为液体。
2. 化学性质-s区元素
s区金属原子半径大、核电荷数小,单质 易失去最外层电子而表现很强的还原性
(4) 锌与OH-,NH3反应
Zn 2OH 2H 2 O Zn(OH) 2 4 H2
Zn 4NH 3 2H 2 O Zn(NH )
2 3 4
H 2 2OH
3.重要化合物
(1 ) 铜的化合物
常见氧化数:+1 (3d10), +2 (3d9)
大学无机化学第十二章S区元素PPT课件

碱土金属的导电性和 导热性良好,其良好 的延展性也使其易于 加工。
碱土金属的密度较大, 且随原子序数增加而 增大。
碱土金属的化学性质
碱土金属的化学性质活泼,有较 强的还原性,容易失去电子成为
正离子。
碱土金属离子具有较强的水合能 力,易与水反应生成氢氧化物。
碱土金属的氧化物大多数为碱性 或两性氧化物,表现出较强的碱
镓的化合物在医药、农业和电子工业等领域也有广泛应用。
镓、铟、铊的性质和用途
铟的性质和用途
铟是一种银白色的软金属,具有较好的延展性和导电性,主要用于制作液晶显示 器和电子元件。
镓、铟、铊的性质和用途
铊的性质和用途 铊是一种银白色的金属,具有较低的熔点和沸点,主要用于制作高温温度计和光电管等器件。
铊的化合物在医药和农业等领域也有一定的应用。
铋的性质和用途
铅是一种青白色的金属,具有较高的密 度和耐腐蚀性,主要用于制作电池、颜 料和涂料等材料。
铅的化合物在医药、农药和染料等领域 也有广泛应用。
THANKS
感谢观看
S区元素在周期表中的位置
总结词
S区元素在周期表中占据第1列和第2 列的位置。
详细描述
在周期表中,S区元素占据第1列和第 2列的位置,这些位置对应于元素周期 表的s区和p区。这些元素具有相似的 电子构型和化学性质,通常表现出强 烈的金属性质。
S区元素的特点和性质
要点一
总结词
S区元素具有低原子序数、小原子半径、高电离能、低电子 亲和能等特点。
大学无机化学第十二章s 区元素ppt课件
• S区元素的概述 •氢 • 碱金属 • 碱土金属 • 其他S区元素
01
S区元素的概述
S区元素的定义
区、d区、ds区重要元素及其化合物

s区、d区、ds区重要元素及其化合物(s Block, ds Block, d Block Elements and Compounds)9.1 s区元素s区元素中锂(Lithium)、钠(Sodium)、钾(Potassium)、铷(Rubidium)、铯(Cesium)、钫(Francium)六种元素被称为碱金属(alkali Metals)元素。
铍(Beryllium)、镁(Magnesium)、钙(Calcium)、锶(Strontium)、钡(Barium)、镭(Radium)六种元素被称为碱土金属(alkaline earth metals)元素。
锂、铷、铯、铍是稀有金属元素,钫和镭是放射性元素。
碱金属和碱土金属原子的价层电子构型分别为ns1和ns2,它们的原子最外层有1~2个电子,是最活泼的金属元素。
9.1.1 通性碱金属和碱土金属的基本性质分别列于表9-1和表9-2中。
表9-1碱金属的性质碱金属原子最外层只有1个ns电子,而次外层是8电子结构(Li的次外层是2个电子),它们的原子半径在同周期元素中(稀有气体除外)是最大的,而核电荷在同周期元素中是最小的,由于内层电子的屏蔽作用较显著,故这些元素很容易失去最外层的1个s电子,从而使碱金属的第一电离能在同周期元素中最低。
因此,碱金属是同周期元素中金属性最强的元素。
碱土金属的核电荷比碱金属大,原子半径比碱金属小,金属性比碱金属略差一些。
s区同族元素自上而下随着核电荷的增加,无论是原子半径、离子半径,还是电离能、电负性以及还原性等性质的变化总体来说是有规律的,但第二周期的元素表现出一定的特殊性。
例如锂的EΘ(Li+/Li)反常地小。
表9-2碱土金属的性质s区元素的一个重要特点是各族元素通常只有一种稳定的氧化态。
碱金属的第一电离能较小,很容易失去一个电子,故氧化数为+1。
碱土金属的第一、第二电离能较小,容易失去2个电子,因此氧化数为+2。
在物理性质方面,s区元素单质的主要特点是:轻、软、低熔点。
大学一年级无机化学PPT课件-第十二章-S区元素(1)

Li2O Na2O2 KO2 RbO2 BeO MgO CaO SrO
CsO2 Ba2O2
Li2O
Na2O2
Gc2-706-18.12
KO2
具有很高的化学活泼性,能直接或间接地
与电负性较高的非金属元素形成相应的化台
物。如可与卤素、硫、氧、磷、氮和氢等元
素相化合。一般均形成离子化合物(除Li、Be
及Mg的卤化物外)。例如锂与氮气反应
6Li + N2 = 2Li3N
镁
与
碱土金属活泼性略差, 二
室温下这些金属表面缓
氧 化
慢生成氧化膜。它们在 空气中加热发生反应,
碳 反 应
生成氧化物和少量氮化
物(如:Ca3N2、Mg3N2)。
因此在金属熔炼中常用Li、Ca等除去溶解 在熔融金属中的氮气和氧气,在电子工业中 常用Ba除去真空管中痕量氮气和氧气,在高 温时碱金属和碱土金属还能夺取某些氧化物 中的氧,如镁可使CO2的碳还原成单质。
碱土金属单质的某些典型反应
N2 M3N2 (M = Mg)
H2O M(OH)2 + H2 (M = Ca, Sr, Ba)
MO + H2 (M = Be, Mg)
水蒸气
MX2 O2
MO2 (M = Ba), MO
M
NH3
M(NH2)2 + H2
NaOH HMO2- + H2 (M = Be)
MH2 (M = Ca, Sr, Ba)
12.2.1 物理和化学性质 Physico-chemical property
12.2.2 矿物资源和金属单质制备 Natural recourses, elementary substance abstraction
第十二章 S区元素

2 制备:
直接: 2Na O 2 Na 2 O 2
K O2 KO2
间接: Na 2 O 2 2Na 2Na2 O
2KNO3 10K 6K2 O N 2
MCO3 MO CO 2 (g)
3 化学性质 (1) 与H2O的作用:
⑴ 硝酸盐热稳定性差
⑵
T分 /℃
BeCO3
<100
MgCO3 CaCO3
540 O C 900
2-
SrCO3 BaCO3
1290 1360
O
⑶ 稳定性 M2CO3> MCO3
O
§12.4 锂 、铍的特殊性 对角线规则
对角线规则
1 内容
Li Na Be Mg B Al C Si
2 锂与镁的相似性:
LiAlH4 4H2 O LiOH Al(OH)3 4H2
二.氧化物 1 形成三类氧化物
正常氧化物(O2-)
2-)
1s 2s 2 p
2 * 2s
2
2
6
过氧化物(O2 KK (σ 2s ) (σ
) (σ 2 p ) ( 2 p ) (π
2 2 4
*
2p
)
4
超氧化物(O2-) KK (σ 2s ) 2 (σ * 2s ) 2 (σ 2 p ) 2 ( 2 p ) 4 (π * 2 p )3
(箭头指向) 溶解度增大, 碱性增强
溶解度 MOH易溶于水,放热 碱土金属溶解度(20℃)
氢氧化物 溶 解 度 /mol·L-1 Be(OH)2 8×10-6 Mg(OH)2 5×10-4 Ca(OH)2 1.8×10-2 Sr(OH)2 6.7×10-2 Ba(OH)2 2×.易与H2直接化合成MH、MH2离子型化合物
S区元素

K通常不用电解法而用置换制备,这是因为它易溶 在熔融的KCl中,难于分离,且电解中产生的超氧 化物与金属钾会发生爆炸,所以不用电解法制钾。 Rb和Cs也是这样。
(3)金属置换法
高温低压下
KCl + Na = NaCl + K 2RbCl +Ca = CaCl2 + 2Rb
2CsAlO2 + Mg = MgAl2O4 + 2Cs
碱金属是活泼性最强的金属元素, -519 -406 -322 -293 -254 都是强还原剂; Li+的水合热特别大
表2 碱土金属元素的一些基本性质
元素 性质 价电子构型 主要氧化数 第一、二电离能 (kJ.mol-1) 第三电离能 (kJ.mol-1) E0(M2+/M)(V) M2+ 水合热 (kJ.mol-1) 906 1757 14849 -1.85 -2494 744 1451 7733 -2.36 -1921 Be 2S2 Mg 3S2 Ca 4S2 +2 596 1145 4912 -2.87 -1577 556 1064 4210 -2.89 -1443 509 965 3575 -2.91 -1305 Sr 5S2 Ba 6S2
•3KOH(s)
•
+2O3(g) =
2KO3(s) + KOH·H2O(s) +1/2O2(g)
•KO3 桔红色晶体,缓慢分解为KO2 + O2
•与水反应放出O2
三类氧化物的比较
•1、生成何种氧化物
•原则:半径:大配大;小配小 • 电荷:高配高;低配低 • 高电荷-小半径更稳定
•2、与水反应
正常氧常氧 H 2 O 氢氧化物 过氧化物 H 2 O 氢氧化物 H 2 O 2 超氧氧化 H 2 O 氢氧化物 H 2 O 2 O 2
第十二章 S区元素

典型的离子晶体。碱金属从上到下随着离子半径增加晶格能逐渐降
低,所以熔点下降。碱土金属离子极化力比碱金属离子大,而且从 上到下随半径增大极化力减弱。
(3)LI+、Be2+的卤化物熔点最低,这与它的半径最小、极化力最大有
关。
2. 溶解性
碱金属盐类的特点是易溶性,但存在少数难溶盐,如六羟基锑酸纳(白
色),高氯酸钾(白色)等,在实验室常利用这些难溶盐来鉴定Na+和
1. 锂铍的原子半径和离子半径分别是碱金属和碱土金属中
最小的,这时锂与其他碱金属元素、铍与其他碱土金属元
素性质差别的主要原因。特别是铍离子,其离子半径特别 小、电荷又高它的极化力是如此之强,使得其化合物共价 性往往超过了离子性。 2. 同一族元素从下而上不仅表现在水合能增加,而且离子 结合的水分子数也增多。虽然碱金属离子半径从上到下递 增,但在水溶液中,水合离子半径却是从上到下递减。
碱金属的含氧酸盐一般都具有较高的热稳定性。碱土金属的含氧酸盐热
稳定性比碱金属差,而且随着半径减小分解温度降低。
第五节 锂铍的特殊性和对角线规则
一般来说,碱金属和碱土金属元素性质的递变是很有规律的,但锂铍却出
现反常性。锂及其化合物的性质与其他碱金属元素及其化合物的性质有明
显的差异。锂铍也同样表现出与其他碱土金属元素性质上的差异。但是锂 与镁,铍与铝在性质上却表现出很多的相似性。 在周期系中某些元素的性质和它左上方或右下方的另一元素性质的相似性 称为对角线规则。这种相似性特别明显地存在于:Li-Mg,Be-Al,B-Si三 对元素之间。
塞,不然时间长会腐蚀而黏住的。 Nhomakorabea第四节 盐类
1. 晶型
(1)碱金属和碱土金属氟化物和氯化物的熔点较高,多为离子晶体。 (2)碱金属的氟化物和氯化物的熔点在同一族中从上到下逐渐降低,而 碱土金属氟化物和氯化物的熔点从上到下逐渐升高。两者变化趋势 不同的主要原因:碱金属离子极化力小,它们的氟化物和氯化物是
第十二章 s区元素(下)

件 一般的钠盐或钾盐是易溶的,一般的高氯酸盐也是 课 易 溶 的 , 但 为 什 么 NaClO4 的 溶 解 度 不 大 , 而 原理 KClO4更难溶?
Na+、K+、ClO4– 都是电荷少、半径大的离子,溶于水后离子
化学 水合程度不大. 故这些盐类的溶解一般都是熵增过程,有利于溶解.
溶解过程的焓变主要来自晶格能和水合能. Na+、K+、ClO4– 电
件
课 下图给出的新配合物中含有两种杂原子,由于分子结构型似地穴
,故取名穴醚 (cryptant) .碱金属阳离子的穴醚配合物比冠醚配合物更稳
理 定,甚至能存在于水溶液中. 这显然与穴醚更接近于实现对金属离子的 学原 完全包封有关.
化
京大学 2014/7/30 南
2.2.2 Crypt—K
(2)穴醚 (cryptant)
课件
下图给出的是18-冠-6,18和6分别表示环原子数和环氧原子数,
理 距离最近的 O 原子间以 -CH2-CH2- 相桥联.冠醚 与碱金属离子形成相 原 对稳定的配合物,碱金属18-冠-6配合物在非水溶液中几乎能无限期 化学 稳定存在.
京大学 2014/7/30 南
18C6—K
(2)穴醚 (cryptant)
课件 化学原理
学 大 京 南 2014/7/30 冠醚和穴醚统称为大环配位化合物 (macrocyclic coordination
compound). 作为配位体的冠醚和穴醚,不同大小、不同形状的穴腔 对碱金属阳离子具有选择性.穴醚几乎能够实现对K+和Na+离子的完 全分离,选择性可高达 105 :1.
3 化合物 (compound)
3.1 氢化物 3.2 氧化物
第十二章s区元素复习提纲,及试题

第十二章s区元素复习提纲,及试题第十二章s区元素预习提纲1、碱金属和碱土金属的概述。
2、单质的存在及制备,物理和化学性质。
3、掌握碱金属和碱土金属的重要氢化物,氧化物,过氧化物,超氧化物的生成和基本性质。
4、碱金属和碱土今生缘氢氧化物碱性强弱的变化规律。
5、重要的盐类的溶解性和稳定性。
6、锂和铍的特殊性。
第十二章s区元素复习题一、是非题:1、碱金属或碱土金属的原子电离势都是自上而下降低,但它们生成离子M+或M2+的标准电极电势并不是自上而下减小的。
2、Na在蒸气状态下可以形成双原子分子,而Be在蒸气状态下仅能形成单原子分子。
3、除LiOH外,所有碱金属氢氧化物都可加热到熔化,甚至蒸发而不分解。
4、在空气中燃烧Ca或Mg,燃烧的产物遇水可生成氨。
5 碱土金属的碳酸盐和硫酸盐在中性水溶液中的溶解度都是自上而下的减小。
二、选择题:1、下列金属中最软的是A、LiB、NaC、CsD、Be2、与同族元素相比,有关铍的下列性质中描述不正确的是A、有高熔点B、有最大密度C、有最小的原子半径D、硬度最大3、下列方法中适合制备金属铯的是A、熔融盐电解法B、热还原法C、金属置换法D、热分解法5、金属锂应存放在A、水中B、煤油中C、石蜡中D、液氨中6、碱金属在过量的空气中燃烧时,生成A、都是普通的氧化物M2OB、钠钾是过氧化物M2O2C、钾铷铯是超氧化物MO2D、铷铯是臭氧化物MO37、下列物质中碱性最强的是A、LiOHB、Mg(OH)2C、Be(OH)2D、Ca(OH)28、下列物质中溶解度最小的是A、Be(OH)2B、Ca(OH)2C、Sr(OH)2D、Ba(OH)29、芒硝和元明粉的化学式分别为A、Na2 SO4·10H2 O Na2 SO4B、CaSO4·2H2 O Na2 SO4·10H2 OC、Na2 S Na2 S2O3·5H2OD、NaNO3 Na2SO410、下列碳酸盐的热稳定性顺序是A、BeCO3 > MgCO3 > CaCO3 > SrCO3 > BaCO3B、BaCO3 < CaCO3 < K2CO3C、Li2CO3 > NaHCO3 > Na2CO3D、BaCO3> SrCO3 > CaCO3> MgCO3 > BeCO311、加热无水Na2CO3固体至熔化前,它A、放出CO2B、不发生化学变化C、放出O2D、生成NaHCO3三、填空题:1、由于钠和钾的氧化物( ),所以ⅠA族元素称为碱金属。
无机化学题库12-S区元素

Ba2+有毒,但由于BaSO4________________和_______________,因此可用于消化道X射 线检查疾病时的造影剂。 10. 2 分 (1235)
a都可以和水反应生成气态产物b都可以和水反应生成一种碱性溶液c在室温条件下它们都是液体da和b21
十二、s 区元素
十二、s 区元素(109 题)
一、选择题 ( 共 25 题 ) 1. 2 分 (1201)
下列化合物用煤气灯火焰加热时,其分解产物不是氧化物、二氧化氮和氧气的是( )
(A) NaNO3 2. 2 分 (1202)
(A) 前者逐渐增加,后者逐渐降低
(B) 前者逐渐降低,后者逐渐增加
(C) 无一定顺序
(D) 两者递变顺序相同
4. 2 分 (1228)
有四种氯化物,它们的通式是XCl2。其中最可能是第IIA族元素的氯化物是……( )
(A) 白色固体,熔点低,易升华,完全溶于水,得到一种无色中性溶液,此溶液导电
性极差;
(B) Mg(NO3)2
(C) LiNO3
(D) Pb(NO3)2
电解食盐水,在阴、阳电极上产生的是………………………………………………( )
(A) 金属钠,氯气
(B) 氢气,氯气
(C) 氢氧化钠,氯气
(D) 氢氧化钠,氧气
3. 2 分 (1220)
Ca、Sr、Ba 的草酸盐在水中的溶解度与其铬酸盐比………………………………( )
(B) 绿色固体,熔点较高,易被氯化,溶于水,得到一种蓝绿色溶液,此溶液具良好 导性;
