超说明书用药专家论证表
超说明书用药专项点评模板

超说明书用药专项点评模板一、目的本模板旨在为医疗机构进行超说明书用药专项点评提供一套标准化、规范化的工作流程和评价标准,以确保患者用药安全、有效、合理。
二、适用范围本模板适用于各级医疗机构,包括医院、诊所、社区卫生服务中心等。
三、评价标准1. 用药目的:药品使用必须符合其适应症,且应具有明确的医学依据。
2. 用药剂量:药品使用剂量必须符合药品说明书及医学指南的规定。
3. 用药途径:药品使用途径必须符合药品说明书及医学指南的规定。
4. 用药频次:药品使用频次必须符合药品说明书及医学指南的规定。
5. 联合用药:药品联合使用必须符合药品说明书及医学指南的规定,避免药物相互作用导致不良反应。
6. 不良反应:药品使用过程中应密切关注不良反应的发生,及时采取有效措施进行干预。
7. 患者知情同意:药品使用前应向患者充分说明用药目的、用法用量、注意事项等内容,确保患者知情同意。
四、工作流程1. 确定点评范围:根据实际情况确定需要进行超说明书用药专项点评的科室、病种及药品范围。
2. 数据收集:收集相关科室、病种及药品的使用情况,包括处方、医嘱、药品说明书等资料。
3. 点评方法:采用表格打分的形式对药品使用情况进行逐一评价,各项评价标准为0-10分,总分60分以下为不合理用药,60分及以上为合理用药。
4. 结果反馈:将点评结果反馈给相关科室及医生,提出改进意见和建议。
5. 持续改进:对存在问题的科室和医生进行追踪,确保超说明书用药专项点评工作的持续改进。
五、总结本模板提供了超说明书用药专项点评的标准化、规范化工作流程和评价标准,有助于医疗机构提高患者用药安全性和合理性。
在实际工作中,应根据具体情况不断完善和调整本模板,以适应医疗技术的不断发展和患者需求的变化。
超说明书用药知情同意书及备案表

姓名:性别:年龄:
门诊病人
门诊号:
住院病人
科室:床位:住院号:
临床诊断:
涉及超说明书用药药品(以下简称被告知药品)名称:
规格:剂型:
用法:
为了您健康利益的最大化,我们针对您的病情,建议使用“超说明书用药”。为了让您更好的理解,我们进行如下善意告知:
4.您已经被告知并理解,使用被告知药品可能发生意外或如下不良反应,包括且不限于:
如果发生医疗意外情况或上述不良反应,医生将按有关诊治常规积极救治病人,使您尽快地康复。
我声明:经医师、药师告知,我已经充分理解上述情况,同意接受被告知药品的超说明书用药,并接受此种治疗可能发生的医疗风险。
患者或家属(监护人)签名:与患者关系:
药品名称:
说明书中规定的内容(适应症、剂量、用法、用量):
超说明书使用原因:
超说明书使用类型:
□改变给药剂量□改变适应人群□改变适应证□改变给药途径
超说明书使用循证医学证据:
□
Ⅰ级
随机对照试验(RCT)的系统评价或Meta-分析
最高,金标准
□
Ⅱ级
单个样本量足够的RC
可靠性较高,建议使用
□
Ⅲ级
设有对照组但未用随机方法分组(非RCT)
医师签名:药师签名:
日期:年月日时分
如果患者为未成年人、患者丧失意识或各种原因导致思维障碍,由监护人或亲属代签本知情同意书。如果患者曾明确告知同意(或近家属要求)对其采取隐瞒病情的保护性医疗措施,由患者书面授权的自然人(或近家属)签署本知情同意书。
超说明书用药管理规定申请表

超说明书用药管理规定为了进一步规范临床合理用药,降低医患纠纷风险,维护患者用药安全,结合我院实际情况,制定本制度。
一、超药品说明书用药的定义:是指药品使用的适应症、给药方法或剂量不在药品监督管理部门批准的说明书之内的用药。
超药品说明书用药的具体含义包括给药剂量、适应人群、适应症或给药途径等与药品说明书不同的用药。
二、临床超说明书用药的管理原则:(一)为保障病人安全,临床用药原则上不得超出药品说明书规定的范围,即不得超说明书用药。
(二)特殊情况需超说明书用药时必须同时具备以下条件:1、在影响病人生活质量或危及生命的情况下,无合理的可替代药品和疗法。
但必须充分考虑药品不良反应、禁忌证、注意事项,权衡病人获得的利益大于可能出现的风险,保证该用法是最佳方案。
2、用药目的必须仅仅是为了病人的治疗,而不是试验研究。
3、有合理的、确凿的循证医学证据,如有充分的文献报道、循证医学研究结果、多年临床实践证明及申请扩大药品适应症的研究结果等。
4、病人知情同意,并签署知情同意书。
三、超说明书用药的审批流程:1、临床确需超说明书用药时,对病人要实行告知并签署《知情同意书》。
医师应充分告知病人用药方案、治疗步骤、预后情况及可能出现的风险,签署知情同意书后方可进入审批程序经批准后使用。
签署的知情同意书一式两份,一份给病人,一份使用科室留存。
2、超说明书用药时需由医师提出用药申请,并提供权威的循证医学依据,由临床科室主任签字,报医务科及药事管理与药物治疗学委员会批准同意。
四、超说明书用药的使用与调剂:1、超说明书用药必须开具处方。
2、药师在审核处方或医嘱时,首先应对药品说明书有深入、细致、透彻地了解,并以药品说明书为依据,严格按药品说明书规范调剂药品,规避用药风险,确保调剂行为的安全及患者的用药安全。
3、药师调剂超说明书用药时,需认真核对知情同意书及处方,确认无误后方可调剂。
4、当临床医生因医疗创新确需要超药品说明书用药时,应提供权威的文献依据,并经药事委员会审核同意,报医务科备案,使用时与患者签署知情同意书。
超说明书申请表,来氟米特
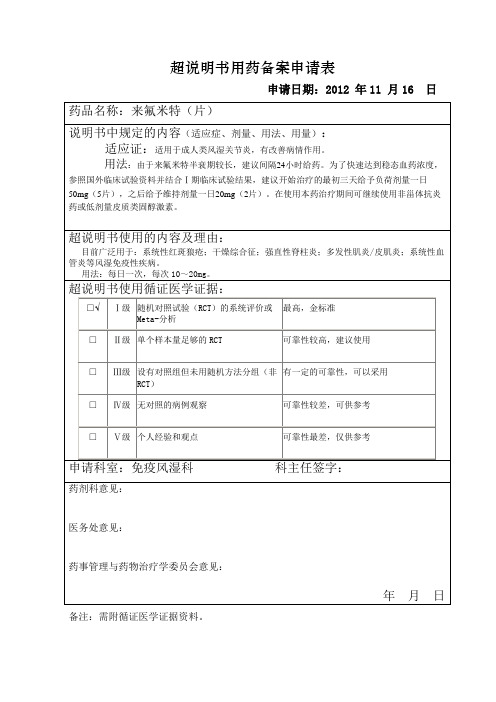
超说明书用药备案申请表
申请日期:2012 年11 月16 日药品名称:来氟米特(片)
说明书中规定的内容(适应症、剂量、用法、用量):
适应证:适用于成人类风湿关节炎,有改善病情作用。
用法:由于来氟米特半衰期较长,建议间隔24小时给药。
为了快速达到稳态血药浓度,参照国外临床试验资料并结合Ⅰ期临床试验结果,建议开始治疗的最初三天给予负荷剂量一日
50mg(5片),之后给予维持剂量一日20mg(2片)。
在使用本药治疗期间可继续使用非甾体抗炎药或低剂量皮质类固醇激素。
超说明书使用的内容及理由:
目前广泛用于:系统性红斑狼疮;干燥综合征;强直性脊柱炎;多发性肌炎/皮肌炎;系统性血管炎等风湿免疫性疾病。
用法:每日一次,每次10~20mg。
超说明书使用循证医学证据:
最高,金标准
□√Ⅰ级随机对照试验(RCT)的系统评价或
Meta-分析
□Ⅱ级单个样本量足够的RCT 可靠性较高,建议使用
有一定的可靠性,可以采用□Ⅲ级设有对照组但未用随机方法分组(非
RCT)
□Ⅳ级无对照的病例观察可靠性较差,可供参考
□Ⅴ级个人经验和观点可靠性最差,仅供参考
申请科室:免疫风湿科科主任签字:
药剂科意见:
医务处意见:
药事管理与药物治疗学委员会意见:
年月日备注:需附循证医学证据资料。
超说明书用药临床研究申请表

申请日期:年月 日
项目名称
项目负责人
药物名称(通用名)
研究的创新性与学术价值(课题来源、研究预期成果):
研究病例总数/本中心例数:
□本院牵头单中心□本院牵头多中心 □本院参与多中心
说明书中规定的使用范围与超说明书使用(适应症、给药途径、用法、用量):
超说明书用药的必要性与依据(现有治疗方法,超说明书使用的依据,附文献或指南、动物研究结果、临床应用小结):
超说明书使用可能出现的风险与管控以及责任承担问题(包括如果出现研究伤害的责任承担人,提供的免费医疗与补偿):
是否免费给药与免费检查(药品是否提供免费检测内容、受试者损害补偿):
临床科室讨论意见:
科主任签字:日期:
抗肿瘤药物超说明书应用处方评价表

起止时间:
肿瘤化疗水化是否充分:
顺铂
1.顺铂使用当天补液量:()ml
环磷酰胺合用美司钠情况:
环磷酰胺
1.是否联用美司钠:是□、否□
2.于环磷酰胺(给药当时)0时、4小时、8小时各1次
评价人
评价日期
处方评价表
肿瘤化学治疗药物(超常规、超剂量、新途径)应用情况分析
一、基本情况表
科室/主管医生
病历号
性别
年龄
身高ຫໍສະໝຸດ (cm)体重(kg)
体重指数
(kg/m2)
体表面积
(m2)
入院诊断
出院诊断
二、肿瘤化学治疗药物合理使用评价表
用药情况
药品通用名
溶媒及体积
单次剂量
给药频次
途径
起止时间
评价
(一)审核药物剂量的合理性
2.列出止吐药应用情况:
药物名称:
溶媒及体积:
单次剂量:
给药频次:
途径:
起止时间:
肿瘤化疗药与抗过敏药联合应用情况:
1.化疗前是否给予抗过敏药:是□、否□
2.列出抗过敏药应用情况:
药物名称:
起止时间:
肿瘤化疗药与糖皮质激素联合应用情况:
1.化疗前是否给予糖皮质激素:是□、否□
2.列出糖皮质激素应用情况:
溶媒使用:
1.溶媒品种选择不合理□
2.溶媒量、浓度不合理□
3.进口药与国产药溶媒量审核不合理□
(五)审核用药顺序的合理性
用药顺序:
1.序贯给药顺序不合理□
2.根据药品刺激性合理用药顺序的审核不合理□
(六)肿瘤化疗药与化疗辅助药联合应用情况
肿瘤化疗药与止吐药联合应用情况:
超说明书用药备案申请表
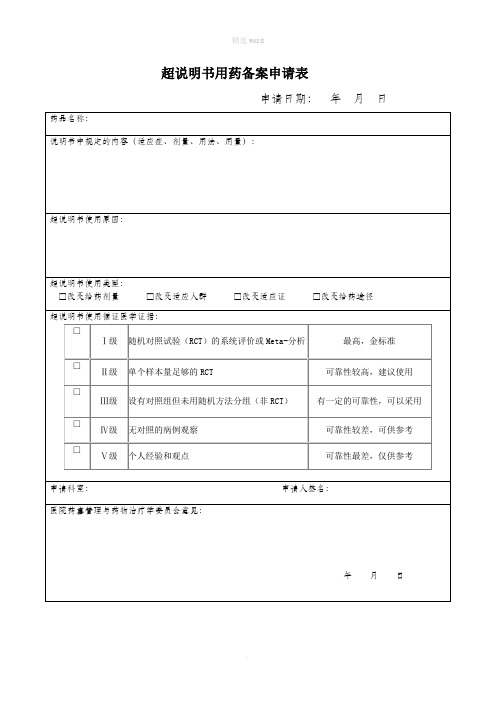
□
Ⅲ级
设有对照组但未用随机方法分组(非RCT)
有一定的可靠性,可以采用
□
Ⅳ级
无对照的病例观察
可靠性较差,可供参考
□
Ⅴ级
个人经验和观点
可靠性最差,仅供参考
申请科室: 申请人签名:
医院药事管理与药物治疗学委员会意见:
年 月 日
超说ቤተ መጻሕፍቲ ባይዱ书用药备案申请表
申请日期: 年 月 日
药品名称:
说明书中规定的内容(适应症、剂量、用法、用量):
超说明书使用原因:
超说明书使用类型:
□改变给药剂量□改变适应人群□改变适应证□改变给药途径
超说明书使用循证医学证据:
□
Ⅰ级
随机对照试验(RCT)的系统评价或Meta-分析
最高,金标准
□
Ⅱ级
单个样本量足够的RCT
超说明书用药处方点评表

超说明书用药处方点评表药品名称:____________________药品类别:____________________适应症:______________________用法用量:____________________副作用:______________________禁忌症:______________________注意事项:____________________药品名称:药品类别:____________________适应症:______________________用法用量:____________________副作用:______________________禁忌症:______________________注意事项:____________________【药品名称】【药品类别】____________________【适应症】______________________【用法用量】____________________【副作用】______________________【禁忌症】______________________【注意事项】____________________【药品名称】【药品类别】____________________【适应症】______________________【用法用量】____________________【副作用】______________________【禁忌症】______________________【注意事项】____________________药品名称:药品类别:适应症:用法用量:副作用:禁忌症:注意事项:药品名称:超说明书用药处方点评表药品类别:____________________适应症:______________________用法用量:____________________副作用:______________________禁忌症:______________________注意事项:____________________药品名称:药品类别:适应症:用法用量:副作用:禁忌症:注意事项:【药品名称】【药品类别】____________________【适应症】______________________【用法用量】____________________【副作用】______________________【禁忌症】______________________【注意事项】____________________以上是关于超说明书用药处方点评表的信息,请根据需要填写药品的相关内容。
超说明书用药干预记录表完整

超说明书用药干预记录表(优质文档,可直接使用,可编辑,欢迎下载)
医院临床超说明书用药干预记录
说明书用药时,需填写《超说明书备案表》报医务科备案,并与患者签署《超说明书用药知情同意书》.
超说明书用药管理制度
为加强药事管理工作,促进临床合理用药,保证医疗质量及医疗安全,避免不必要的医疗纠纷,根据《药品管理办法》、《医疗机构药事管理规定》、《侵权责任法》及《药品说明书和标签管理规定》等法律法规,制订本规定。
1、超药品说明书用药(Off-label uses)的定义是指临床实际使用药品的适应证、给药方法或剂量不在具有法律效力的说明书之内的用法,包括给药剂量、适应人群、适应证、用药方法或给药途径等与药品说明书中的用法不同的情况,又称超范围用药、药品未注册用药或药品说明书之外的用法。
2、药品说明书具有法律效力,超药品说明书用药现象的存在具有一定的合理性和必要性,但是超说明书用药有可能没有大量临床研究数据支持,也没有获得药品监管部门批准,存在一定的风险,且超药品说明书用药不受法律保护,超说明书用药导致不良后果的,医生和药师要共同承担相应法律责任。
3、临床因医疗创新确需要超药品说明书用药时,须填写《超药品说明书用药审批表》,并提供权威的循证医学依据,交临床药师进行核实和初步的风险评估,经药事管理与药物治疗学委员会审批通过后,报医务科备案。
4、治疗需要超药品说明书用药时,临床医生应严格按照药事管理与药物治疗学委员会审批结果使用.
5、临床药师对超说明书用药情况定期进行分析、评价,发现超说明书用药导致的药物不良反应及时分析原因,上报医务科并通知相关病区,必要时医务科通知终止该超说明书的用法.
财务会计主管岗位说明书
财务会计岗位说明书
出纳岗位说明书
财务成本会计岗位说明书。
超说明书用药评价

沙利度胺能否用于该患儿?
若以上条件都不满足,是否无药可用?是否利大于弊?同时要结 合患者意愿
综上所述,沙利度胺不适宜该患儿的治疗,建议 停用
在科室进行讲解,医师采纳并停用所有在儿童使 用的沙利度胺
该患儿转归
○ 经10天住院治疗后患儿双下肢、双足踝皮肤较前明 显变暗,溃疡结痂。病情达到临床缓解,顺利出院。
根据医学科学发展的一般规律,不能完全 要求医务人员遵照具有一定时效性的诊疗 规范或专业技术指导书籍开展临床工作, 这不符合科学发展的基本精神,也不利于 患者疾病的治疗与康复
我国超说明书 用药举例
超适应症用药
- 二甲双胍 - 红霉素 - 利奈唑胺
- 多囊卵巢综合症 - 糖尿病胃轻瘫 - 用于颅内感染
结语
《赫尔辛基宣言》:“当无现存有效的预防、诊断和治疗方法 治疗病人时,若医生觉得有挽救生命、重新恢复健康或减轻痛 苦的希望,那么在取得病人知情同意的情况下医生应该不受限 制地使用尚未经证实的或是新的预防、诊断和治疗措施。”
药师应积极寻找理与法的最佳契合点,在合理的医学实践证据 支持下,充分考虑药品不良反应、禁忌证、注意事项,权衡利 弊,在征得患者意见的前提下,合理、规范地“超说明书用 药”。
1965年意外地发现反应停可以有效地减轻麻 风性皮肤结节红斑的患者的皮肤症状。
1991年发现它有抑制肿瘤坏死因子(TNF-α)作 用——抗肿瘤作用
1994年发现抑制炎症细胞因子、抑制白细胞 对炎症部位的趋化——抗炎作用
沙利度胺
1963
退市
PA R T. 0 1
沙利度胺 可以用于该患儿吗
单击此处添加正文,文字是您思想的提炼,为了演示发布的良好效果,请言简意赅地阐述您的观点。
Thank You !
抗凝药物超药品说明书用药专家共识[山东省超药品说明书用药专家共识系列](2023)要点
要点](https://img.taocdn.com/s3/m/56c51c72366baf1ffc4ffe4733687e21af45ff05.png)
抗凝药物超药品说明书用药专家共识[山东省超药品说明书用药专家共识系列](2023)要点[摘要]抗凝药物被广泛用于非瓣膜性房颤、静脉血栓栓塞、卒中等血栓栓塞性疾病的预防和治疗。
临床实践中精准的个体化应用抗凝药物尤为重要,用药不当可能导致血栓形成或出血等不良事件的发生。
因此,基于说明书和循证证据加强抗凝药物合理使用与管理已成为临床抗凝治疗团队的一项重要任务。
超药品说明书用药(O1DU)在临床抗凝治疗中不可避免,但抗凝药物的O1DU具有一定风险。
为此,山东省药学会循证药学专委会O1DU研究项目工作组基于山东省内多家大型医院在抗凝治疗领域的临床需求,根据专家组制定的循证评价方法,针对抗凝药物超药品说明书治疗总结出12条共识意见,涉及超适应症用药和超人群用药,以期为临床用药提供参考。
1超药品说明书用药(O1DU)概况O1DU是指药品使用的适应症、剂量、疗程、途径或人群等,未在药品监督管理部门批准的药品说明书界定范围内的用法。
O1DU在临床治疗中普遍存在。
我国于2023年3月起施行的《中华人民共和国医师法》中规定:〃在尚无有效或者更好治疗手段等特殊情况下,医师取得患者明确知情同意后,可以采用药品说明书中未明确但具有循证医学证据的药品用法实施治疗。
〃这是我国首次将循证医学下的O1DU写入法律,明确授权医师在符合一定条件下可以O1DU。
O1DU是发现药物新用途的一种具有成本效益的策略,可提高药物的治疗价值,为患者提供更多的治疗选择。
2抗凝药物O1DU概况抗凝药物是通过影响凝血过程中的某些凝血因子阻止凝血的药物,可用于血栓栓塞性疾病的预防及治疗,在临床中广泛应用。
但其若使用不当,不仅可能因出血或凝血事件而造成患者入院或延长住院时间,还可能导致患者死亡。
制订有关抗凝药物安全用药的措施和流程,减少抗凝药物治疗的临床风险至关重要。
3抗凝药物O1DU循证证据评价和分级经过多次专家论证会讨论凝练形成最终目录(共20条),共有7个抗凝药物,推荐意见12项(表1I4抗凝药物O1DU的超适应症用药4.1 低分子肝素(1MWH)依诺肝素钠和达肝素钠都属于1MWH,其主要特点是相对于抗凝血因子a,对抗凝血因子a活性更高。
超说明书用药专家论证表
不推荐使用
药物治疗方案没有效果,应避免使用
Class Indeterminate
不明确
表三 证据分级等级
等级
是否有效
Class A
证据基于以下证据;随机对照试验的荟萃分析;多个涉及良好、大规模的随机临床试验
Class B
证据基于以下证据∶结论冲突的随机对症试验的荟萃分析;小规模或研究方案有显著缺陷的随机对照试验;非随机研究
超说明书用药专家论证表
申报药品通用名
商品名
申报超说明书用法
论证项目
以实验研究为目的
□是
□否
□不确定
资料提供齐全
□是
□否
□不确定
提供依据充分
□是
□否
□不确定
临床应用经验
□是
□否
□不确定
药品使用利大于弊
□是
□否
□不确定
分级论证
有效性等级
□Ⅰ 治疗有效 □Ⅱa证据支持有效
□Ⅱb有效性具有争议 □Ⅲ治疗无效
□否
□不确定
推荐等级
□Ⅰ 推荐 □Ⅱa多数情况下推荐
□Ⅱb有某些情况下推荐 □ Ⅲ不推荐
□不明确
论证等级
□A 随机对照试验的荟萃分析;多个设计良好、大规模的随机临床试验
□B结论冲突的随机对照试验的荟萃分析;小规模或研究方法有显著缺陷的随机对照试验;非随机研究
□C专家意见或共识;个案报道或系列案例
□没有证据
论证结果
□通过 □不通过
论证专家:
日 期:
表一 有效性等级
等级
是否有效
含义
ClassⅠ
治疗有效
药物治疗方案对特定适应症的证据和(或)专家意见表明治疗有效
超说明书申请表,甲氨蝶呤
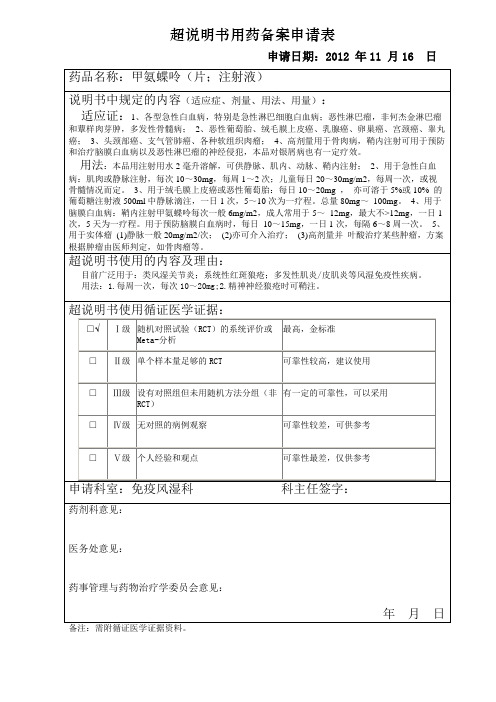
超说明书用药备案申请表申请日期:2012 年11 月16 日药品名称:甲氨蝶呤(片;注射液)说明书中规定的内容(适应症、剂量、用法、用量):适应证:1、各型急性白血病,特别是急性淋巴细胞白血病;恶性淋巴瘤,非何杰金淋巴瘤和蕈样肉芽肿,多发性骨髓病;2、恶性葡萄胎、绒毛膜上皮癌、乳腺癌、卵巢癌、宫颈癌、睾丸癌;3、头颈部癌、支气管肺癌、各种软组织肉瘤;4、高剂量用于骨肉病,鞘内注射可用于预防和治疗脑膜白血病以及恶性淋巴瘤的神经侵犯,本品对银屑病也有一定疗效。
用法:本品用注射用水2毫升溶解,可供静脉、肌内、动脉、鞘内注射;2、用于急性白血病:肌肉或静脉注射,每次10~30mg,每周1~2次;儿童每日20~30mg/m2,每周一次,或视骨髓情况而定。
3、用于绒毛膜上皮癌或恶性葡萄胎:每日10~20mg ,亦可溶于5%或10% 的葡萄糖注射液500ml中静脉滴注,一日1次,5~10次为一疗程。
总量80mg~100mg。
4、用于脑膜白血病:鞘内注射甲氨蝶呤每次一般6mg/m2,成人常用于5~12mg,最大不>12mg,一日1次,5天为一疗程。
用于预防脑膜白血病时,每日10~15mg,一日1次,每隔6~8周一次。
5、用于实体瘤(1)静脉一般20mg/m2/次;(2)亦可介入治疗;(3)高剂量并叶酸治疗某些肿瘤,方案根据肿瘤由医师判定,如骨肉瘤等。
超说明书使用的内容及理由:目前广泛用于:类风湿关节炎;系统性红斑狼疮;多发性肌炎/皮肌炎等风湿免疫性疾病。
用法:1.每周一次,每次10~20mg;2.精神神经狼疮时可鞘注。
超说明书使用循证医学证据:最高,金标准□√Ⅰ级随机对照试验(RCT)的系统评价或Meta-分析□Ⅱ级单个样本量足够的RCT 可靠性较高,建议使用有一定的可靠性,可以采用□Ⅲ级设有对照组但未用随机方法分组(非RCT)□Ⅳ级无对照的病例观察可靠性较差,可供参考□Ⅴ级个人经验和观点可靠性最差,仅供参考申请科室:免疫风湿科科主任签字:药剂科意见:医务处意见:药事管理与药物治疗学委员会意见:年月日备注:需附循证医学证据资料。
超说明书用药管理规定、申请表

超说明书用药管理规定为了进一步规范临床合理用药,降低医患纠纷风险,维护患者用药安全,结合我院实际情况,制定本制度。
一、超药品说明书用药的定义:是指药品使用的适应症、给药方法或剂量不在药品监督管理部门批准的说明书之内的用药。
超药品说明书用药的具体含义包括给药剂量、适应人群、适应症或给药途径等与药品说明书不同的用药。
二、临床超说明书用药的管理原则:(一)为保障病人安全,临床用药原则上不得超出药品说明书规定的范围,即不得超说明书用药。
(二)特殊情况需超说明书用药时必须同时具备以下条件:1、在影响病人生活质量或危及生命的情况下,无合理的可替代药品和疗法。
但必须充分考虑药品不良反应、禁忌证、注意事项,权衡病人获得的利益大于可能出现的风险,保证该用法是最佳方案。
2、用药目的必须仅仅是为了病人的治疗,而不是试验研究。
3、有合理的、确凿的循证医学证据,如有充分的文献报道、循证医学研究结果、多年临床实践证明及申请扩大药品适应症的研究结果等。
4、病人知情同意,并签署知情同意书。
三、超说明书用药的审批流程:1、临床确需超说明书用药时,对病人要实行告知并签署《知情同意书》。
医师应充分告知病人用药方案、治疗步骤、预后情况及可能出现的风险,签署知情同意书后方可进入审批程序经批准后使用。
签署的知情同意书一式两份,一份给病人,一份使用科室留存。
2、超说明书用药时需由医师提出用药申请,并提供权威的循证医学依据,由临床科室主任签字,报医务科及药事管理与药物治疗学委员会批准同意。
四、超说明书用药的使用与调剂:1、超说明书用药必须开具处方。
2、药师在审核处方或医嘱时,首先应对药品说明书有深入、细致、透彻地了解,并以药品说明书为依据,严格按药品说明书规范调剂药品,规避用药风险,确保调剂行为的安全及患者的用药安全。
3、药师调剂超说明书用药时,需认真核对知情同意书及处方,确认无误后方可调剂。
4、当临床医生因医疗创新确需要超药品说明书用药时,应提供权威的文献依据,并经药事委员会审核同意,报医务科备案,使用时与患者签署知情同意书。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
不推荐使用
药物治疗方案没有效果,应避免使用
Class Indeterminate
不明确
表三 证据分级等级
等级
是否有效
Class A
证据基于以下证据;随机对照试验的荟萃分析;多个涉及良好、大规模的随机临床试验
Class B
证据基于以下证据∶结论冲突的随机对症试验的荟萃分析;小规模或研究方案有显著缺陷的随机对照试验;非随机研究
超说明书用药专家论证表
申报药品通用名
商品名
申报超说明书用法
论证项目
以实验研究为目的
□是
□否
□不确定
资料提供齐全
□是
□否
□不确定
提供依据充分
□是
□否
□不确定
临床应用经验
□是
□否
□不确定
药品使用利大于弊
□是
□否
□不确定
分级论证
有效性等级
□Ⅰ 治疗有效 □Ⅱa证据支持有效
□Ⅱb有效性具有争议 □Ⅲ治疗无效
论证结果
□通过 □不通过
论证专家:
日 期:
表一 有效性等级
等级
是否有效
含义
ClassⅠ
治疗有效
药物治疗方案对特定适应症的证据和(或)专家意见表明治疗有效
ClassⅡa
证据支持有效
药物治疗方案对特定适应症有效性的证据和(或)专家意见存在分歧,但证据和(或)专家意见倾向有效
ClassⅡb
有效性具有争议
药物治疗方案对特定使用证有效性的证据和(或)专家意见存在分歧,证据和(或)专家意见对其有效性存在争议
Class C
证据基于以下证据∶专家意见或共识;个案报道或系列案例
No Evidence
没有证据
□否
□不确定
推荐等级
□Ⅰ 推荐 □Ⅱa多数情况下推荐
□Ⅱb有某些情况下推荐 □ Ⅲ不推荐
□不明确
论证等级
□A 随机对照试验的荟萃分析;多个设计良好、大规模的随机临床试验பைடு நூலகம்
□B结论冲突的随机对照试验的荟萃分析;小规模或研究方法有显著缺陷的随机对照试验;非随机研究
□C专家意见或共识;个案报道或系列案例
□没有证据
ClassⅢ
治疗无效
药物治疗方案对特定适应症的证据和(或)专家意见表明治疗无效
表二 推荐等级
等级
是否有效
含义
ClassⅠ
推荐
药物治疗方案已被证实有效,推荐使用
ClassⅡa
大多数情况下推荐
药物治疗方案通常认为是有用的,在大多数情况下推荐使用
ClassⅡb
在某些情况下推荐使用
药物治疗方案可能有效,在某些情况下推荐使用,但大多数情况下不推荐使用
