2018-2019北京市西城高三化学一模试题
2019西城一模化学试题含答案

西 城 区 高 三 统 一 测 试 2019.4第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
6.2019年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于...大气污染防治措施的是A . 向酸性土壤 中加入熟石灰B .汽车尾气 净化减排C .工业尾气 回收处理D .用清洁能源 替代化石燃料7.下列说法不涉及...氧化还原反应的是 A .雷雨肥庄稼——自然固氮B .从沙滩到用户——由二氧化硅制晶体硅C .干千年,湿万年,不干不湿就半年——青铜器、铁器的保存D .灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐8.Pd/Al 2O 3催化H 2还原CO 2的机理示意图如下。
下列说法不正确...的是A .H -H 的断裂需要吸收能量B .①→②,CO 2发生加成反应C .④中,CO 被氧化为CH 4D .生成CH 4的总反应方程式是 CO 2+ 4H 2 CH 4+ 2H 2O①②③④Pd/Al 2O 39.有机物AB2、AB4、AB8均可形成枝状高分子AB m。
下列说法不正确...的是A.AB2分子中有4种不同化学环境的氢原子B.AB4既能与强酸反应也能与强碱反应C.AB2生成AB m是缩聚反应D.AB m10.下列实验结果不能..作为相应定律或原理的证据之一的是11.在不同条件下进行化学反应2A(g)B(g) +D(g),B 、D 起始浓度均为0,反应物A 的−1序号 温度(℃)0 20 40 50 ① 800 1.0 0.67 0.50 0.50 ② 800 x 0.50 0.50 0.50 ③ 800 y 0.75 0.60 0.60 ④8201.00.250.200.20下列说法不正确...的是 A .①中B 在0~20 min 平均反应速率为8.25×10−3mol ·L −1·min −1 B .②中K =0.25,可能使用了催化剂 C .③中y =1.4 mol ·L −1D .比较①、④可知,该反应为吸热反应12.(NH 4)2SO 3氧化是氨法脱硫的重要过程。
北京市西城区2018年高三一模化学试题

北京市西城区2018年高三一模化学试题。
可能用到的相对原子质量:H l C 12 N 14 O 1 6 Cl 35.5 Cu 64选择题在每小题列出的四个选项中,选出符合题目要求的一项。
1.下列变化过程中未必吸热的是____。
(A)电解质在熔融状态下电离(B)共价键断裂(C)原子失电子(D)溶解2.化学与生活密切相关,下列说法正确的是A.食盐可作调味剂B.CO2属于大气污染物C.柠檬很酸,属于酸性食物D.用聚氯乙烯塑料袋包装食品3.下列解释事实的方程式表达不.正.确.的是A.碳酸氢钠可作食品膨松剂:2NaHCO3 Na2CO3+ CO2↑+H2OB.铝制容器不能盛装碱液:2Al +2OH-+2H2O 2AlO2-+ 3H2↑C.氯气可用于消毒:Cl2+H2O 2H++ Cl-+ClO-D.过氧化钠可用于呼吸面具:2Na2O2 + 2CO2 2 Na2CO3 + O2↑4.图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。
下列说法不正确...的是图Ⅰ图ⅡA.图Ⅰ中a为纯铜B.图Ⅰ中SO42—向b极移动C.图Ⅱ中如果a、b间连接电源,则a连接负极D.图Ⅱ中如果a、b间用导线连接,则X可以是铜5.下列说法正确的是A.植物油的主要成分是高级脂肪酸B.银氨溶液可用于检验淀粉是否完全水解C .溴乙烷与氢氧化钠水溶液反应可制取乙烯D .丙氨酸(CH 3CHCOOH )缩聚产物的结构简式为6.实验:① 向盛有1 mL 0.1 mol/L MgCl 2溶液试管中加1 mL 0.2 mol/L NaOH 溶液,得到浊液a ,过滤得到滤液b 和白色沉淀c 。
② 向沉淀c 中滴加0.1mol/L FeCl 3溶液,沉淀变为红褐色。
下列分析不正确...的是 A .浊液a 中存在沉淀溶解平衡:Mg (OH) 2(s)Mg 2+(aq)+2OH -(aq)B .滤液b 中不含有Mg 2+C .②中颜色变化说明Mg (OH)2转化为Fe(OH)3D .实验可以证明Fe(OH)3比Mg (OH)2更难溶7.下列说法正确的是A .油脂都不能使溴水褪色B .氨基酸是两性化合物,能与酸、碱反应生成盐C .福尔马林可用作食品防腐剂D .蔗糖和麦芽糖的水解产物都是葡萄糖8.用下列各组仪器或装置,不能达到实验目的的是A .a 组:制备少量乙酸乙酯B .b 组:除去粗盐水中的泥沙C .c 组:用CCl 4提取碘水中的碘D .d 组:配制100 mL 1.00 mol/L NaCl 溶液 9.下列解释事实的离子方程式不正确的是 A .氯化钢溶液显酸性:B .氯气使湿润的淀粉KI 试纸变蓝:C .向硫酸铝溶液中加入氨水出现白色胶状沉淀:D .实验室不用玻璃塞试剂瓶盛装氢氧化钠溶液:10.已知16S 、34Se 位于同一主族,下列关系正确的是 A .热稳定性: B .原子半径:C .酸性:D .还原性:11.对常温下pH=3的CH 3COOH 溶液,下列叙述不正确的是 A .B .加入少量CH 3COONa 固体后,c (CH 3COO —)降低NH 2C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/LD.与等体积pH =11的NaOH溶液混合后所得溶液显酸性12.欲检验CO2气体中是否含有SO2、HC1,进行如下实验:①将气体通入酸化的AgNO3溶液中,产生白色沉淀a;②滤去沉淀a,向滤液中加入Ba(NO3)2溶液,产生白色沉淀b。
最新-2018年4月北京市西城区理综一模卷化学试题 精品

2018年北京市西城区理综一模卷化学试题 2018-4 可能用到的相对原子质量:H—1、C—12、O—16、Mg—24、S—32、Cl—35.5、Cu—64 6.某有机物小分子...含有C、H、O、N等元素,该有机物可能是A.脂肪B.葡萄糖C.蛋白质D.氨基酸7.“厨房化学”是指利用家庭生活用品来进行化学实验,从而对化学进行学习和探究的活动。
下列实验在厨房中不能..完成的是A.检验自来水中含有Cl—离子B.检验鸡蛋壳中含有碳酸盐C.检验加碘食盐中不含碘单质D.检验蛋白质在加热条件下能发生变性8.有M、R两种主族元素,已知R2—离子与M+离子核外电子数之和为20,则下列说法中不正确...的是A.R与M的质子数之和一定等于19B.若R处于第三周期,则M必处于第二周期C.R与M元素组成的某种离子化合物中存在非极性共价键D.R与M的质子数之差可能等于79.氢叠氮酸(HN3)与醋酸酸性相近。
氢叠氮酸盐(NaN3)稳定,但撞击发生爆炸生成氮气。
下列有关氢叠氮酸及其盐的说法中不正确...的是A.固体HN3属于分子晶体B.HN3的水溶液呈弱酸性C.NaN3的水溶液呈酸性D.NaN3可用于汽车防撞保护气囊10.阿伏加德罗常数的近似值为6.02×1023,下列说法中正确的是A.常温常压下,7.1 g Cl2含0.2×6.02×1023个Cl2分子B.同温同压下,相同体积的CO2和SO2所含氧原子数均为2×6.02×1023NH所含电子数约为6.02×1023个C.0.1 mol-2D.在16 g CH4中含有6.02×1023个C—H键11.已知反应:3A(g)+B(g) C(s)+4D(g),△H<0。
图中a、b曲线表示在一定条件下,D的体积分数随时间的变化情况。
若使曲线b变为曲线a,可采取的措施是A.升高温度B.缩小反应容器的体积C.增加C的质量D.减小B的浓度12.锂电池是新一代高能电池,目前已研究成功多种锂电池。
2018年--西城区--高三化学-一模考试试题+答案

(1)A为烯烃,B中所含官能团名称是______,A→B的反应类型是______。
(2)C→D的反应条件是______。
(3)E分子中有2个甲基和1个羧基,E→F的化学方程式是______。
(4)D+F→K的化学方程式是______。
(5)下列关于J的说法正确的是______。
②棕色溶液中的[Fe(NO)]2+受热生成Fe2+,加热有利于Fe2+被氧化为Fe3+,促进Fe3+水解,产生Fe(OH)3沉淀
(3)①Fe2++NO2−+2CH3COOH==Fe3++NO↑+H2O+2CH3COO−
Fe2++NO==[Fe(NO)]2+
②两层液体界面上H+、NO3−与Fe2+反应,生成棕色的[Fe(NO)]2+
(4)右图为真空AlCl歧化法制备Al的实验装置示意图,控制
AlCl3的凝华装置、Al的生成装置和AlCl的制备装置的
温度分别为T1、T2、T3,其由高到低的顺序是______。
(5)制备Al的整个过程中可循环利用的物质是______。
27.(17分)某小组研究溶液中Fe2+与NO2−、NO3−的反应。
资料:[Fe(NO)]2+在溶液中呈棕色。
(1)研究现象a中的黄色溶液。
①用______溶液检出溶液中含有Fe3+。
②甲认为是O2氧化了溶液中的Fe2+。乙认为O2不是主要原因,理由是______。
③进行实验Ⅱ,装置如下图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。
北京市2018届高三各城区一模化学试题分类汇编——有机化学word版含答案
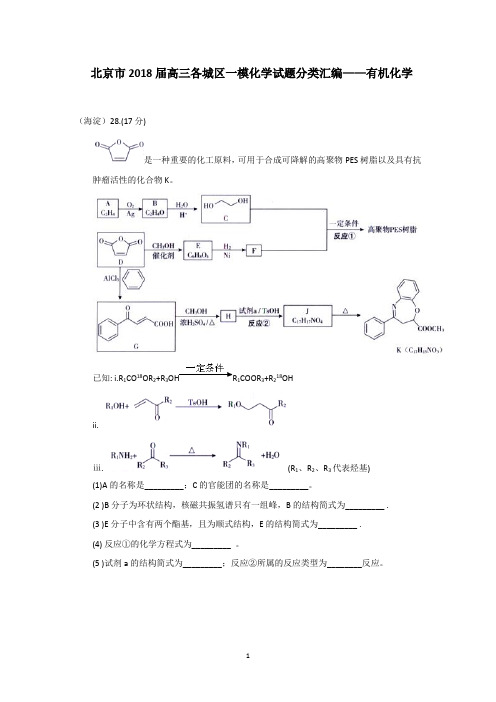
北京市2018届高三各城区一模化学试题分类汇编——有机化学(海淀)28.(17 分)是一种重要的化工原料,可用于合成可降解的高聚物PES 树脂以及具有抗肿瘤活性的化合物K。
已知: i.R1CO18OR2+R3OH R1COOR3+R218OHii.ⅲ. (R1、R2、R3代表烃基)(1)A的名称是_________;C 的官能团的名称是_________。
(2 )B 分子为环状结构,核磁共振氢谱只有一组峰,B 的结构简式为_________ .(3 )E 分子中含有两个酯基,且为顺式结构,E 的结构简式为_________ .(4) 反应①的化学方程式为_________ 。
(5 )试剂a的结构简式为_________;反应②所属的反应类型为________反应。
(6) 已知: 。
以1,3- 丁二烯为起始原料,结合已知信息选用必要的无机试剂合成。
将以下合成路线补充完整:(7)已知氨基(-NH 2) 与羟基类似,也能发生反应i 。
在由J 制备K 的过程中,常会产生副产物L 。
L 分子式为C 16H 13NO 3,含三个六元环,则L 的结构简式为________。
(朝阳)25.(17分)有机物P 是某抗病毒药物的中间体,它的一种合成路线如下。
XN(C 4H 8O 2)Br 2ⅰ.NaOH ⅱ.H+Y浓HNO 3M (C 4H 10O)A(C 7H 8)O 2催化剂浓H 2SO 4,△B 氧化还原NCH 3COOH一定条件有机物PF (C 4H 6O 3)E (C 7H 7NO)DPBr3连续氧化MnO 2已知:+CO一定条件RN C +H 2OCO H +CH 2CO 一定条件CH CCO+H 2ORNH 2(1)A 为芳香化合物,其结构简式是 。
(2)A →B 的化学方程式是 ,反应类型是 。
(3)M 无支链,N 中含有的官能团是 。
(4)M 连续氧化的步骤如下:M 转化为Q 的化学方程式是________。
2018北京西城高三一模化学及参考标准答案2018.4

西城区高三统一测试理科综合 ---化学部分2018.46.我国出土的文物呈现了瑰丽的历史文化。
下列文物中,主要成分属于合金的是A.西夏佛经纸本B.西汉素纱禅衣 C.唐兽首玛瑙杯 D.东汉青铜奔马7.下列延长食品保质期的方法中,其原理与其它几种不.同.的是A.加食盐腌制 B.抽真空C.充氮气D.使用吸氧剂8.下列事实不能..用元素周期律解释的是A.F2在暗处遇H2爆炸,I2在暗处遇H2几乎不反应B.Br2和NaI溶液发生置换反应,和NaCl溶液不发生置换反应C.金属Na和熔融KCl反应置换出金属KD.常温下,NaCl溶液的pH=7,AlCl3溶液的pH<79.向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。
下列关于上述过程的说法不正确...的是A.Cu2+是H2O2分解反应的催化剂B.H2O2既表现氧化性又表现还原性C.Cu2+将H2O2还原为O2D.发生了反应Cu2O + H2O2 +4H+ ==2Cu2+ + 3H2O10.我国学者研制了一种纳米反应器,用于催化草酸二甲酯(DMO)和氢气反应获得EG。
反应过程示意图如下:下列说法不正确...的是A.Cu纳米颗粒将氢气解离成氢原子B.DMO分子中只有碳氧单键发生了断裂C.反应过程中生成了MG和甲醇D.EG和甲醇不是同系物11.下列解释事实的方程式书写正确的是A.Na2CO3溶液处理水垢中的CaSO4:Ca2++ CO32− == CaCO3↓B.Na2O2作呼吸面具的供氧剂:2Na2O2 +2CO2==2 Na2CO3+ O2C.稀HNO3洗涤做过银镜反应的试管:Ag+ 2H+ + NO3− ==Ag+ +NO2↑ + H2O D.FeCl3溶液腐蚀线路板:Fe3+ + Cu == Fe2+ + Cu2+12.某同学向SO2和Cl2的混合气体中加入品红溶液,振荡,溶液褪色,将此无色溶液分成三份,依次进行实验,实验操作和实验现象记录如下:下列实验分析中,不正确...的是A.①说明Cl2被完全消耗B.②中试纸褪色的原因是:SO2+I2+ 2H2O==H2SO4 +2HIC.③中若将BaCl2溶液换成Ba(NO3)2溶液,也能说明SO2被Cl2氧化为SO42−D.实验条件下,品红溶液和SO2均被氧化25.(12分)为消除燃煤烟气中含有的SO2、NOx,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
2018西城区高中高三一模化学试卷习题及答案

2021西城区高三一模化学试卷及答案第2 页共20 页第3 页共20 页第4 页共20 页C.反响过程中生成了MG和甲醇D.EG和甲醇不是同系物11.以下解释事实的方程式书写正确的选项是A.Na2CO3溶液处理水垢中的CaSO4:Ca2++CO32-==CaCO3↓B.Na2O2作呼吸面具的供氧剂:2Na2O2+2CO2==2Na2CO3+O2 C.稀HNO3洗涤做过银镜反响的试管:Ag+2 H -++NO3 ==Ag+NO2↑+H2OD.FeCl3溶液腐蚀线路板:Fe3++Cu==Fe2++Cu2+12.某同学向SO2和Cl2的混合气体中参加品红溶液,振荡,溶液褪色,将此无色溶液分成三份,依次进行实验,实验操作和实验现象记录如下:序号①②③实验操作实验溶液不变红,溶液不变生成白现象试纸不变蓝红,试纸褪色沉淀第5页共20页色以下实验分析中,不正确的是...A.①说明Cl2被完全消耗B.②中试纸褪色的原因是:SO2+I2+2H2O==H2SO4+2HIC.③中假设将BaCl2溶液换成Ba(NO3)2溶液,也能说明SO2被Cl2氧化为SO42-D.实验条件下,品红溶液和SO2均被氧化25.〔12分〕为消除燃煤烟气中含有的SO2、NO x,研究者提出了假设干烟气“脱硫〞、“脱硝〞的方法。
〔1〕向燃煤中参加适量石灰石,高温时将SO2转化为CaSO4的化学方程式是______________________________________________________。
2〕选择性催化复原法〔SCR〕“脱硝〞。
在催化剂的作用下,选取复原剂将烟气中的NO进行无害化处理。
NH3复原NO的化学方程式是。
〔3〕以NaClO溶液作为吸收剂进行一体化第6页共20页“脱硫〞、“脱硝〞。
控制溶液的pH=,将烟气中的SO2、NO转化为SO42-、NO3-,均为放热反响。
①在图1中画出“放热反响〞的反响过程中的能量变化示意图。
(完整版)2018-2019北京市西城高三化学一模试题(可编辑修改word版)

2019 西城区高三统一测试理科综合2019.4 本试卷共17 页,共300 分。
考试时长150 分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120 分)6.2019 年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于大气污染防治措施的是7.下列说法不涉及氧化还原反应的是A.雷雨肥庄稼——自然固氮B.从沙滩到用户——由二氧化硅制晶体硅C.千千年,湿万年,不干不湿就半年——青铜器、铁器的保存D.灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐8.Pd/A12O3催化H2还原CO2的机理示意图如下。
下列说法不正确的是A.H-H 的断裂需要吸收能量B.①-②,CO2发生加成反应C.④中,CO 被氧化为CH4D.生成CH4的总反应方程式是9.有机物AB2、AB4、AB8均可形成枝状高分子AB m。
下列说法不正确的是A.AB2分子中有4 种不同化学环境的氢原子B.AB4既能与强酸反应也能与强碱反应C.AB2生成AB m是缩聚反应D. AB m的结构简式是10.下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)11.在不同条件下进行化学反应2A(g)=B(g)+D(g),B、D 起始浓度均为0,反应物A 的浓度(mol/L)随反应时间的变化情况如下表:3下列说法不正确的是A.①中B 在0~20 min 平均反应速率为8.25xl0-3 moI.L-l.min-lB.②中K-0.25,可能使用了催化剂C.③中y= 1.4 moI.L-lD.比较①、④可知,该反应为吸热反应12.(NH4)2SO3氧化是氨法脱硫的重要过程。
某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如下图。
下列说法不正确的是A.60℃之前,氧化速率增大与温度升高化学反应速率加快有关B.60℃之后,氧化速率降低可能与02的溶解度下降及(NH4)2SO3受热易分解有关C.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,与SO 2-水解程度增大有关D.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,可能与O2的溶解速率有关25.(17 分)度鲁特韦可以用于治疗HIV-1 感染,M 是合成度鲁特韦的一种中间体。
(完整版)2018-2019北京市西城高三化学一模试题

1 / 82019西城区高三统一测试理科综合2019.4本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)6. 2019年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于大气污染防治措施的是C.工业尾气6用満洁能源回收处理持代化石燃料7 •下列说法不涉及氧化还原反应的是 A .雷雨肥庄稼——自然固氮B .从沙滩到用户一一由二氧化硅制晶体硅C .千千年,湿万年,不干不湿就半年一一青铜器、铁器的保存D .灰肥相混损肥分一一灰中含有碳酸钾,肥中含有铵盐& Pd/A12O 3催化H 2还原CO 2的机理示意图如下。
下列说法不正确的是A . H-H 的断裂需要吸收能量B.汽牛吃气 挣化减排 C .④中, CO 被氧化为CH 4 D .生成CH 4的总反应方程式是CO;+4H :2HsOB .①-②,CO 2发生加成反应1 / 89. 有机物AB 2、AB 4、AB 8均可形成枝状高分子AB m。
下列说法不正确的是A. AB 2分子中有4种不同化学环境的氢原子B. AB 4既能与强酸反应也能与强碱反应C. AB 2生成AB m 是缩聚反应D. AB m 的结构简式是 I10. 下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)11.在不同条件下进行化学反应 2A(g)=B(g)+D(g) , B 、D 起始浓度均为0,反应物A 的浓度(mol/L)随反应时 序号时间温度(说、420 450 ① 300 L00.67 050 0.50 ②8000J00.50 0-50800y0.75 0.60 0,60 ④8201.00.250.20020*NH1 1 I 1H HrHH NNN1N << 0-6 0—cNH一s I I ! H HrHH NNN1N <弋AB勒夏特列廈理元素周朋律 盖期定律 阿伏加總罗定律JI1电解水结左球气体闘色加深 S 右球气怵濒色变浅烧瓶中冒气泡, 试管中出现簿浊应与6问体积比 釣为2 : IHOOC己知:I _ F _ 特味溥刑 I II ・ R^H^CH J C^CHR J --------- ---------- * R 厂II. R (CH = CHKi縉・RjCOOH+R^COOHRjOH RjDI. Ri-C-H+H-ltl-RT ------------------- * Rp CH-N-R,下列说法不正确的是A. ①中B 在0〜20 min 平均反应速率为 8.25x10-3 mol.L -l .min -1B. ②中K-0.25,可能使用了催化剂C. ③中 y= 1.4 moI.L -lD. 比较①、④可知,该反应为吸热反应12. (NH 4)2SO 3氧化是氨法脱硫的重要过程。
2019年4月北京市西城区2019届高三下学期4月一模考试理科综合化学试卷及解析

2019年4月西城区2019届高三下学期4月一模考试理科综合化学试卷★祝考试顺利★本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
1.2019年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于大气污染防治措施的是A. 向酸性土壤中加入熟石灰B. 汽车尾气净化减排C. 工业尾气回收处理D. 用清洁能源替代化石燃料【答案】A【解析】大气污染防治措施①控车措施有利于减少汽车尾气排放,净化空气,节约能源;②淘汰落后产能有利于企业节能减排,转变发展方式;③控煤有利于节约煤炭资源,减少有害气体的排放;④PM2.5监测有利于监督政府履行节能降耗的职责,落实监管责任;⑤天气预警有利于及时掌握空气质量状况,为防治大气污染提供参考.【详解】A、向酸性土壤中加入熟石灰,是改善土壤的酸碱性,故A选;B、汽车尾气净化减排,就是将汽车尾气经净化处理后达标排放,减少大气污染物的排放量,故B不选;C、工业尾气回收处理,有利于减少大气污染物的排放量,故C不选;D、用清洁能源替代化石燃料,有利于减少大气污染物的排放量,故D不选;故选A。
2.下列说法不涉及氧化还原反应的是A. 雷雨肥庄稼——自然固氮B. 从沙滩到用户——由二氧化硅制晶体硅C. 干千年,湿万年,不干不湿就半年——青铜器、铁器的保存D. 灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐【答案】D【解析】【分析】在反应过程中有元素化合价变化的化学反应叫做氧化还原反应。
原电池反应可以理解成由两个半反应构成,即氧化反应和还原反应。
,最后变【详解】A. 雷雨肥庄稼——自然固氮,氮气氧化成NO,再氧化成NO2等,有元素化合价变化,故A不选;成HNO3B. 从沙滩到用户——由二氧化硅制晶体硅,硅由+4价变成0价,有元素化合价变化,故B不选;C. 干千年,湿万年,不干不湿就半年——说明青铜器、铁器在不干不湿的环境中保存时,容易发生电化学腐蚀,铜和铁容易被氧化,有元素化合价变化,故CD. 灰肥相混损肥分——灰中含有碳酸钾,水解后呈碱性,肥中含有铵盐,水解后呈酸性,两者相遇能发生复分解反应,导致氮肥的肥效降低,没有元素化合价变化,故D 选。
北京市西城区高三一模化学试题20210525145656

北京市西城区2018 年高三一模化学试题。
可能用到的相对原子质量:H l C 12 N 14 O 1 6 Cl 35. 5Cu 64选择题在每题列出的四个选项中,选出吻合题目要求的一项。
1.以下变化过程中未必吸热的是____。
(A)电解质在熔融状态下电离(B) 共价键断裂 (C)原子失电子(D) 溶解2.化学与生活亲近相关,以下说法正确的选项是A.食盐可作调味剂B. CO2属于大气污染物C.柠檬很酸,属于酸性食品D.用聚氯乙烯塑料袋包装食品正确的选项是3.以下解说事实的方程式表达不...A.碳酸氢钠可作食品膨松剂:2NaHCO3Na2 CO3+ CO2↑ +H2OB.铝制容器不可以盛装碱液:--2Al +2OH +2H2O2AlO2 + 3H2↑C.氯气可用于消毒: Cl2+H2O+--2H + Cl +ClOD.过氧化钠可用于呼吸面具:2Na2O2 + 2CO2 2 Na2CO3 + O2↑4.图Ⅰ的目的是精髓铜,图Ⅱ的目的是保护钢闸门。
以下说法不正确...的是图Ⅰ图ⅡA.图Ⅰ中 a 为纯铜B.图Ⅰ中 SO42—向 b 极挪动C.图Ⅱ中假如 a、b 间连接电源,则 a 连接负极D.图Ⅱ中假如 a、 b 间用导线连接,则X 可以是铜5.以下说法正确的选项是A.植物油的主要成分是高级脂肪酸B.银氨溶液可用于检验淀粉能否完整水解C.溴乙烷与氢氧化钠水溶液反应可制取乙烯H [NHCHCO]n OHD.丙氨酸( CH3CHCOOH)缩聚产物的结构简式为NH2CH36.实验:①向盛有 1 mL 0.1 mol/L MgCl 2溶液试管中加 1 mL 0.2 mol/L NaOH 溶液,获得浊液 a,过滤获得滤液 b 和白色积淀 c。
②向积淀 c 中滴加3溶液,积淀变成红褐色。
以下解析不正确的是...A.浊液 a 中存在积淀溶解均衡: Mg (OH) 2(s)-Mg 2+ (aq)+ 2OH (aq)B.滤液 b 中不含有 Mg2+C.②中颜色变化说明 Mg (OH)2转变成 Fe(OH)3D.实验可以证明 Fe(OH)3比 Mg (OH)2更难溶7.以下说法正确的选项是A.油脂都不可以使溴水退色B.氨基酸是两性化合物,能与酸、碱反应生成盐C.福尔马林可用作食品防腐剂D.蔗糖和麦芽糖的水解产物都是葡萄糖8.用以下各组仪器或装置,不可以达到实验目的的是A. a 组:制备少许乙酸乙酯B. b 组:除去粗盐水中的泥沙C. c 组:用 CCl4提取碘水中的碘D. d 组:配制100 mL 1.00 mol/L NaCl 溶液9.以下解说事实的离子方程式不正确的选项是A.氯化钢溶液显酸性:B.氯气使湿润的淀粉KI 试纸变蓝:C.向硫酸铝溶液中加入氨水出现白色胶状积淀:D.实验室不用玻璃塞试剂瓶盛装氢氧化钠溶液:10.已知16S、34Se 位于同一主族,以下关系正确的选项是A.热稳固性:B.原子半径:C.酸性:D.还原性:11.对常温下pH=3 的 CH3COOH溶液,以下表达不正确的选项是A.—B.加入少许CH3COONa固体后, c( CH3COO )降低C.该溶液中由水电离出的+)是×10-11c( H mol / LD.与等体积pH =11 的 NaOH 溶液混杂后所得溶液显酸性12.欲检验CO2气体中能否含有SO2、 HC1,进行以下实验:①将气体通入酸化的AgNO3溶液中,产生白色积淀a;②滤去积淀a,向滤液中加入Ba(NO3)2溶液,产生白色积淀b。
2018北京西城高三一模化学及参考答案

西城区高三统一测试理科综合 ---化学部分6.我国出土的文物呈现了瑰丽的历史文化。
下列文物中,主要成分属于合金的是A.西夏佛经纸本B.西汉素纱禅衣C.唐兽首玛瑙杯D.东汉青铜奔马7.下列延长食品保质期的方法中,其原理与其它几种不.同.的是A.加食盐腌制 B.抽真空 C.充氮气 D.使用吸氧剂8.下列事实不能..用元素周期律解释的是A.F2在暗处遇H2爆炸,I2在暗处遇H2几乎不反应B.Br2和NaI溶液发生置换反应,和NaCl溶液不发生置换反应C.金属Na和熔融KCl反应置换出金属KD.常温下,NaCl溶液的pH=7,AlCl3溶液的pH<79.向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。
下列关于上述过程的说法不正确...的是A.Cu2+是H2O2分解反应的催化剂B.H2O2既表现氧化性又表现还原性C.Cu2+将H2O2还原为O2D.发生了反应Cu2O + H2O2 + 4H+ == 2Cu2+ + 3H2O10.我国学者研制了一种纳米反应器,用于催化草酸二甲酯(DMO)和氢气反应获得EG。
反应过程示意图如下:下列说法不正确...的是A.Cu纳米颗粒将氢气解离成氢原子B.DMO分子中只有碳氧单键发生了断裂C.反应过程中生成了MG和甲醇D.EG和甲醇不是同系物11.下列解释事实的方程式书写正确的是A.Na2CO3溶液处理水垢中的CaSO4:Ca2+ + CO32− == CaCO3↓B.Na2O2作呼吸面具的供氧剂:2Na2O2 + 2CO2 == 2 Na2CO3 + O2C.稀HNO3洗涤做过银镜反应的试管:Ag + 2H+ + NO3− == Ag+ + NO2↑ + H2OD.FeCl3溶液腐蚀线路板:Fe3+ + Cu == Fe2+ + Cu2+12.某同学向SO2和Cl2的混合气体中加入品红溶液,振荡,溶液褪色,将此无色溶液分成三份,依次进行实验,实验操作和实验现象记录如下:下列实验分析中,不正确...的是A.①说明Cl2被完全消耗B.②中试纸褪色的原因是:SO2 + I2 + 2H2O == H2SO4 + 2HIC.③中若将BaCl2溶液换成Ba(NO3)2溶液,也能说明SO2被Cl2氧化为SO42−D.实验条件下,品红溶液和SO2均被氧化25.(12分)为消除燃煤烟气中含有的SO2、NO x,研究者提出了若干烟气“脱硫”、“脱硝”的方法。
2019北京西城高三一模化 学
2019北京西城高三一模化学本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
6. 2019年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于大气污染防治措施的是7.下列说法不涉及氧化还原反应的是A.雷雨肥庄稼——自然固氮B.从沙滩到用户——由二氧化硅制晶体硅C.千千年,湿万年,不干不湿就半年——青铜器、铁器的保存D.灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐8.Pd/A12O3催化H2还原CO2的机理示意图如下。
下列说法不正确的是A.H-H的断裂需要吸收能量B.①-②,CO2发生加成反应C.④中,CO被氧化为CH4D.生成CH4的总反应方程式是9.有机物AB2、 AB4、 AB8均可形成枝状高分子AB m。
下列说法不正确的是A.AB2分子中有4种不同化学环境的氢原子B.AB4既能与强酸反应也能与强碱反应C.AB2生成AB m是缩聚反应D.AB m的结构简式是10.下列实验结果不能作为相应定律或原理的证据之一的是(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)11.在不同条件下进行化学反应2A(g)=B(g)+D(g),B、D起始浓度均为0,反应物A的浓度(mol/L)随反应时间的变化情况如下表:下列说法不正确的是A.①中B在0~20 min平均反应速率为8.25xl0-3 moI.L-l.min-lB.②中K-0.25,可能使用了催化剂C.③中y= 1.4 moI.L-lD.比较①、④可知,该反应为吸热反应12. (NH4)2SO3氧化是氨法脱硫的重要过程。
某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如下图。
2018-2019北京各区一模水溶液专题

2018-2019北京各区一模水溶液专题
2018-2019年海淀高三化学适应性训练
2018-2019海淀高三理综一模化学试题
西城区高三统一测试
12. (NH4)2SO3氧化是氨法脱硫的重要过程。
某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如下图。
下列说法不正确的是
A. 60℃之前,氧化速率增大与温度升高化学反应速率加快有关
B. 60℃之后,氧化速率降低可能与02的溶解度下降及(NH4)2SO3受热易分解有关
C. (NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,与SO32-水解程度增大有关
D. (NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,可能与O2的溶解速率有关
12C
北京市东城区2018-2019学年度第二学期高三综合练习
北京市朝阳区高三年级第一次综合练习
丰台区2019年高三年级第二学期综合练习(一)
2019年石景山区高三统一练习
11.25℃时,将20mL 0.10 mol/LCH3COOH溶液和20mL 0.10 mol/LHX溶液分别与20mL 0.10 mol/LNaHCO3溶液混合,测得产生气体的体积(V)随时间(t)变化如下图,下列说法中不.
正确
..的是
A.反应开始前,HX溶液中c(H+)大于CH3COOH中c(H+)
B.CH3COOH溶液反应结束后,c(Na+)>c(CH3COO—)
C.反应结束后所得两溶液中,c(CH3COO—)<c(X—)
D.由该实验可知HX为强酸
11D。
2019.04西城高三一模化学答案

西城区高三统一测试化学参考答案及评分标准2019.4第一部分共20小题,每小题6分,共120分。
6.A 7.D 8.C 9.D 10.B 11.C 12.C25-28题其他正确答案可参照本标准给分25.(17分,(1)(2)每空1分,其它每空2分)(1)碳碳双键羟基(2)取代反应(3)NaOH水溶液,加热(4(5(8)bc(26.(13分,(3)1分,其它每空2分)(1)研磨、70℃加热(2)Mg(OH)2、Ni(OH)2和Ca(OH)2(3)趁热过滤(4)185 ab(5)4OH −-4e −== 2H 2O + O 2↑ 阳(6)Li 2CO 3 + 2C+ 2FePO 4===== 2LiFePO 4+ 3CO27.(12分,(1)和(3)①1分,其它每空2分)(1)原子半径逐渐增大,得电子能力逐渐减弱,非金属性Cl >I ,离子的还原性Cl −<I −(2)①4H ++ 4I −+ O 2== 2I 2+ 2H 2O②增大c (H +),降低了c (OH −),使平衡2H 2O+ 4I −+ O 22I 2+4OH −正向移动,反应易 于进行等(3)①3×10−2②H 2O + 2I −+ O 3I 2+ 2OH −+ O 2③2Fe 2++O 3 +5H 2O==2Fe(OH)3+ 4H ++O 2 ④反应H 2O +2I −+ O 3I 2+ 2OH −+ O 2产生的OH −被Fe 2+或Fe 2+的氧化产物Fe 3+结合,pH 减小,促使该平衡正向移动,提高了I −的转化率,产生大量的Fe(OH)3 28.(16分,每空2分)(1)+3(2)溶液中存在平衡:[Fe(C 2O 4)3] 3−Fe 3++ 3C 2O 42−,加入硫酸后,H +与C 2O 42−结合生成H 2C 2O 4,使平衡正向移动,c (Fe 3+)增大,遇KSCN 溶液变红(3)取少量实验1中的翠绿色溶液,滴加K 3Fe(CN)6溶液,不出现蓝色沉淀Fe 3+与C 2O 42−生成稳定的[Fe(C 2O 4)3] 3−,浓度降低,Fe 3+的氧化性和C 2O 42−的还原性减弱(4)2 [Fe(C 2O 4)3] 3−+4H 2O=====2FeC 2O 4•2H 2O ↓+ 3C 2O 42−+ 2CO 2↑(5)Ⅱ中产生大量红褐色沉淀或Ⅲ中得到翠绿色溶液(6)不能说明。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2019西城区高三统一测试理科综合2019.4本试卷共17页,共300分。
考试时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题共120分)
6. 2019年政府工作报告提出要持续开展大气污染的治理攻坚。
下列不属于大气污染防治措施的是
7.下列说法不涉及氧化还原反应的是
A.雷雨肥庄稼——自然固氮
B.从沙滩到用户——由二氧化硅制晶体硅
C.千千年,湿万年,不干不湿就半年——青铜器、铁器的保存
D.灰肥相混损肥分——灰中含有碳酸钾,肥中含有铵盐
8.Pd/A12O3催化H2还原CO2的机理示意图如下。
下列说法不正确的是
A.H-H的断裂需要吸收能量B.①-②,CO2发生加成反应
C.④中,CO被氧化为CH4 D.生成CH4的总反应方程式是
9.有机物AB2、AB4、AB8均可形成枝状高分子AB m。
下列说法不正确的是
A. AB2分子中有4种不同化学环境的氢原子
B. AB4既能与强酸反应也能与强碱反应
C.AB2生成AB m是缩聚反应
D. AB m的结构简式是
10.下列实验结果不能作为相应定律或原理的证据之一的是
(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
11.在不同条件下进行化学反应2A(g)=B(g)+D(g),B、D起始浓度均为0,反应物A的浓度(mol/L)随反应时间的变化情况如下表:
下列说法不正确的是
A.①中B在0~20 min平均反应速率为8.25xl0-3 moI.L-l.min-l
B.②中K-0.25,可能使用了催化剂
C.③中y= 1.4 moI.L-l
D.比较①、④可知,该反应为吸热反应
12. (NH4)2SO3氧化是氨法脱硫的重要过程。
某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如下图。
下列说法不正确的是
A. 60℃之前,氧化速率增大与温度升高化学反应速率加快有关
B. 60℃之后,氧化速率降低可能与02的溶解度下降及(NH4)2SO3受热易分解有关
C. (NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,与SO32-水解程度增大有关
D. (NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,可能与O2的溶解速率有关
25.(17分)度鲁特韦可以用于治疗HIV-1感染,M是合成度鲁特韦的一种中间体。
合成M的路线如下:(部分反应条件或试剂略去)
己知:
(l)麦芽酚中含有官能团的名称是羰基、醚键、和。
(2)A是苯的同系物,A—B的反应类型是。
(3) B- C的反应条件是____。
(4)C-D的化学方程式是。
(5)E不能与金属Na反应生成氢气,麦芽酚生成E的化学方程式是。
(6)G的结构简式是。
(7)X的分子式为C3H902N,X的结构简式是。
(8)Y的分子式为C4H11ON,Y与X具有相同种类的官能团,下列说法正确的是。
a.Y与X互为同系物
b.Y能与羧酸发生酯化反应
c.Y在浓硫酸、加热的条件下能发生消去反应
(9)K-M转化的一种路线如下图,中间产物2的结构简式是。
26.(13分)用含锂废渣(主要金属元素的含量:Li 3.50% Ni 6.55% Ca 6.41% Mg 13.24%)
制备Li2CO3,并用其制备Li+电池的正极材料LiFePO4。
部分工艺流程如下:
I.制备Li2CO3粗品
(l)上述流程中为加快化学反应速率而采取的措施是。
(2)滤渣2的主要成分有。
(3)向滤液2中先加入EDTA,再加入饱和Na2C03溶液,90℃充分反应后,分离出固体Li2C03粗品的操作是。
(4)处理lkg含锂3.50%的废渣,锂的浸出率为a,Li+转化为Li2CO3的转化率为b,则粗品中含Li2C03的质量是g。
(摩尔质量:Li 7 g.mol-l Li2C03 74 g.mol-l)
II.纯化Li2C03粗品
(5)将Li2CO3转化为LiHCO3后,用隔膜法电解LiHCO3溶液制备高纯度的LiOH,再转化得电池级Li2CO3。
电解原理如右图所示,阳极的电极反应式是,该池使用了(填“阳”或“阴”)离子交换膜。
III.制备LiFePO4
(6)将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式是。
27. (12分)研究水体中碘的存在形态及其转化是近年的科研热点。
I-与I2在水体和大气中的部分转化如下图所示。
(1)结合元素周期律分析Cl-、I-的还原性强弱;同主族元素的原子,从上到下,。
(2)水体中的I-在非酸性条件下不易被空气中的02氧化。
原因是的反应速率慢,
反应程度小。
①I-在酸性条件下与O2反应的离子方程式是。
②在酸性条件下I-易被O2氧化的可能的原因是。
(3)有资料显示:水体中若含有Fe2+,会对O3氧化I-产生影响。
为检验这一结论,进行如下探究实验:分别将等量的O3通入到20 mL下列试剂中,一段时间后,记录实验现象与结果。
己知:每l mol O3参与反应,生成l mol O2。
①a= 。
②A中反应为可逆反应,其离子方程式是。
③C中溶液的pH下降,用离子方程式解释原因。
④比较A、B、C,说明Fe2+在实验B中的作用并解释____。
28.(16分)文献表明:相同条件下,草酸根(C2O42-)的还原性强于Fe2+。
为检验这一结论,完成如下实验。
资料:i.草酸(H2C2O4)为二元弱酸。
ii.三水三草酸合铁酸钾为翠绿色晶体,光照易分解。
其水溶液中存在:
iii. FeC2O4-2H2O为黄色固体,微溶于水,可溶于强酸。
【实验1】通过Fe3+和C2O42-在溶液中的反应比较Fe2+和C2O42-的还原性强弱。
(l) C2O42-中碳元素的化合价是。
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。
继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。
加硫酸后溶液变红的原因是。
(3)经检验,翠绿色晶体为设计实验,确认实验1中没有发生氧化还原反应的操作和现象是。
实验l中未发生氧化还原反应的原因是。
(4)取实验1中的翠绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。
补全反应的离子方程式:
【实验2]通过比较H2O2与Fe2+、C2O42-反应的难易,判断二者还原性的强弱。
(5)证明Fe2+被氧化的实验现象是。
(6)以上现象能否说明C2042-没有被氧化。
请判断并说明理由:
(7)用FeC13溶液、K2C2O4溶液和其他试剂,设计实验方案比较Fe2+和C2O42-的还原性强弱。
画出装置图并描述预期现象:。
化学答案。
