最新武汉市化学专题训练-溶解度曲线
微专题09 溶解度及溶解度曲线-备战2023年中考化学热点微专题专项突破训练(全国通用)(原卷版)

微专题09溶解度及溶解度曲线1.(2022·贵州黔西·中考真题)如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
(1)t 3℃时,甲、乙、丙三物质溶解度由小到大的顺序是_____。
(2)t 2℃时,甲和丙两饱和溶液的溶质质量分数关系是_____。
(3)P 点对应混合物,甲、乙、丙中处于不饱和状态的是_____。
2.(2022·湖北襄阳·统考中考真题)如图为甲、乙、丙三种固体物质的溶解度曲线,据图回答问题。
(1)t 1℃时,甲、丙两种物质的溶解度大小关系是甲______丙(填“>”“<”或“=”)。
(2)溶解度随温度的升高而减小的物质是______。
(3)t 2℃时,将甲、乙两种物质的饱和溶液降温至t 1℃,对所得溶液的叙述正确的是(填序号)。
A.甲溶液仍是饱和溶液,乙溶液变为不饱和溶液B.溶液中溶剂的质量甲<乙C.溶液中溶质的质量分数甲<乙3.(2022·山东滨州·统考中考真题)如图为A、B 两种固体物质的溶解度曲线,请根据图突破一、溶解度曲线示信息回答:℃时,A物质的溶解度是___________g。
(1)t1(2)A、B两种物质中,___________的溶解度受温度的影响较小。
℃时,将35gA物质加入到50g水中,充分溶解后,得到该温度下A物质的___________ (3)t2(填“饱和”或“不饱和”)溶液。
此时溶液的溶质质量分数为___________。
4.(2022·辽宁阜新·统考中考真题)溶液在日常生活,工农业生产和科学研究中具有广泛的用途。
右图是硝酸钾和氯化钠两种物质的溶解度曲线,请回答:(1)在10℃时,氯化钠溶解度_____硝酸钾溶解度(填“>”、“<”或“=”)。
(2)这两种物质中,______的溶解度受温度影响最大。
(3)60℃时,100g水里最多能溶解_____g硝酸钾。
2024年中考化学专题强化训练溶解度曲线
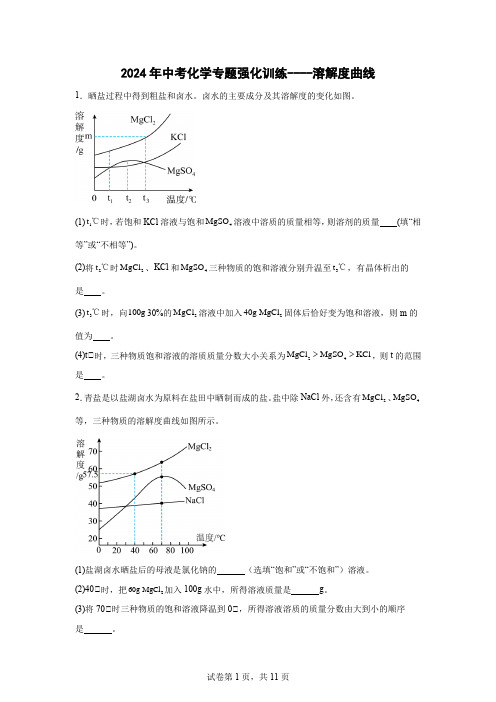
2024年中考化学专题强化训练----溶解度曲线1.晒盐过程中得到粗盐和卤水。
卤水的主要成分及其溶解度的变化如图。
(1)1t ℃时,若饱和KCl 溶液与饱和4MgSO 溶液中溶质的质量相等,则溶剂的质量 (填“相等”或“不相等”)。
(2)将2t ℃时2MgCl 、KCl 和4MgSO 三种物质的饱和溶液分别升温至3t ℃,有晶体析出的是 。
(3)3t ℃时,向100g 30%的2MgCl 溶液中加入240g MgCl 固体后恰好变为饱和溶液,则m 的值为 。
(4)t℃时,三种物质饱和溶液的溶质质量分数大小关系为24MgCl MgSO KCl >>,则t 的范围是 。
2.青盐是以盐湖卤水为原料在盐田中晒制而成的盐。
盐中除NaCl 外,还含有2MgCl 、4MgSO 等,三种物质的溶解度曲线如图所示。
(1)盐湖卤水晒盐后的母液是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)40℃时,把260g MgCl 加入100g 水中,所得溶液质量是 g 。
(3)将70℃时三种物质的饱和溶液降温到0℃,所得溶液溶质的质量分数由大到小的顺序是 。
(4)氯化钠中含有少量硫酸镁,若要提纯氯化钠,可采用的方法是。
3.某同学进行了如图1所示实验,结合硝酸钾和氯化钠的溶解度曲线回答下列问题。
(1)20℃时,氯化钠的溶解度是g;(2)若氯化钠中混有少量硝酸钾,可采用的方法提纯氯化钠;(3)图1中烧杯℃为硝酸钾的(填“饱和”或“不饱和”)溶液;若通过升高温度使℃中固体继续溶解,则其溶液中溶质的质量分数(填“增大”“减小”或“不变”)。
4.如图是A、B、C三种固体物质的溶解度曲线,据图作答:(1)P点的意义是。
(2)A、B、C三种物质中,溶解度随着温度上升而减小的物质是。
(3)t2℃时,将30g A物质加入50g水中可形成g溶液。
5.如图是某苏打气泡水的标签。
(1)该气泡水中溶剂的化学式是。
C H O。
从赤藓糖醇的化学式中能获得与其有关的(2)赤藓糖醇是一种甜味剂,其化学式为4104信息是(任写一条)。
(完整)九年级化学中考溶解度曲线习题

A B C0 t 1 20 t 2 温度/℃ g 40溶解度全国中考化学汇编之溶解度曲线1.右图是a 、b 两种固体物质(不含结晶水)的溶解度曲线。
下列说法正确的是 A.b 的溶解度大于a 的溶解度B.t 1℃时,将a 、b 两种物质的饱和溶液分别恒温蒸发 等质量的水,析出晶体的质量一定相等C.将t 2℃时的b 的不饱和溶液降温至t 1℃, 一定能得到b 的饱和溶液D.t 2℃时,a 溶液的溶质质量分数一定小于 b 溶液的溶质质量分数2.右图所示是甲、乙两种固体物质的溶解度曲线,请回答下列问题: (1)t 1℃时,甲物质的溶解度 乙物质的溶解 度(填“>”、“=”或“<”)。
(2)甲、乙两种物质的溶解度受温度影响较小的是 物质。
(3)t 2℃时,把100g 乙物质放入100g 水中,充分搅拌, 所得溶液是 溶液(填“饱和”或“不饱和”)。
(4)t 2℃时,有一接近饱和的甲溶液,可采用 的方法(任写一种)使它变为饱和溶液。
3.右图是甲、乙两种物质的溶解度曲线,下列说法正确的是 A .甲的溶解度受温度影响比乙小 B .15℃时甲、乙的溶解度相等C .30℃时乙的溶解度为30gD .升高温度可使接近饱和....的甲溶液变为饱和.. 4.请根据图7中A 、B 两种固体物质的溶解度曲线,回答下列问题。
(l)在____℃时,A 、B 两种物质溶解度相同。
(2) t 2℃时,100g 水中溶解_ gA 物质恰好达到饱和,该饱和溶液中溶质的质量分数为_ ___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 g 。
(3)将t 2℃时A 、B 两种物质的饱和溶液降温至t 1℃(其它条件不变),溶质的质量分数保持不变的是___ _。
5.(5分) 右图为A 、B 、C 三种物质的溶解度曲线,据图回答: ⑴ t 20C 时,A 、B 、C 三种物质的溶解度由大到小顺序是 ______。
⑵ 将t 20C 时三种物质等质量的饱和溶液分别降温到00C 时,析出溶质最多的是 ___ ,无溶质析出的是 __ 。
初三化学中考专题(5)溶解度曲线练习及答案

初三化学中考专题(5)溶解度曲线练习及答案1.a、b两种物质的溶解度曲线如图所示。
下列说法不正确的是A.将t1℃时b的饱和溶液加水可变为不饱和溶液B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变C.t2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的升高而增大C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%3.下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是A.甲>乙>丙B.甲=乙=丙C.甲=乙>丙D.丙>甲=乙4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t1℃时,甲物质的溶解度为20gB.t1℃时,30g甲加入到50g水中最多可得70g溶液C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A溶液和C溶液C.实验过程中,只有B溶液和D溶液属于饱和溶液D.实验过程中,B溶液与E溶液中溶质的质量分数相同6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C.分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。
初中中考化学常考专题提升练:溶解度曲线

中考化学常考专题提升练:溶解度曲线溶解度曲线专练1.在室温时,向氯化钠饱和溶液中加入少量的氯化钠晶体,则()①溶液质量增加②溶质质量增加③溶剂质量不变④晶体质量不变⑤晶体质量减少.A. B. C. D.2.要使固体物质的不饱和溶液变为饱和溶液,最简单最可靠的方法是()A. 增大压强B. 升高温度C. 降低温度D. 增加溶质3.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是()A. 时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4B. P点表示甲、丙两种物质的饱和溶液质量相等C. 时,乙物质的饱和溶液,升温至时仍是饱和溶液D. 将三种物质的溶液从降至,析出晶体最多的是甲物质4.甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是()A. 时,甲和乙的溶解度相等,都是30B. 时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等C. 温度从降至,甲和乙的饱和溶液中析出晶体的质量甲大于乙D. 时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数5.a、b、c三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是()A. 时,a的饱和溶液65g中含有溶剂50gB. 将时a、b、c三种物质的饱和溶液,降温至时,C溶液中溶质的质量分数保持不变C. 要从b溶液中得到b,通常可采用蒸发溶剂使其结晶的方法D. 在时,a、b两种溶液中溶质的质量分数相同6.如图是甲、乙两种固体物质的溶解度曲线,下列叙述不正确的是()A. 甲、乙两种物质均属于易溶物质B. 甲物质的溶液度受温度变化影响较大C. 在时,甲、两种物质的饱和溶液中溶质的质量相等D. 当甲中含有少量的乙时,可用降温结晶法提纯甲7.将40℃时硝酸钾饱和溶液冷却到20℃,温度变化前后,保持不变的是()A. 溶质质量B. 溶液质量C. 溶剂质量D. 溶质的质量分数8.两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是()A. Y的溶解度曲线为b曲线B. 降温可使X的饱和溶液变浑浊C. X的饱和溶液从降温到,溶质的质量分数变大D. 时,X、Y的饱和溶液质量相等,则溶剂质量9.20℃时,往50g蔗糖溶液中加入5g蔗糖固体充分搅拌后,尚有部分固体未溶解,加热后固体全部溶解,则下列说法正确的是()A. 搅拌后加热前的溶液一定不饱和溶液B. 搅拌后加热前一定是饱和溶液C. 加热后一定是饱和溶液D. 加热后一定是不饱和溶液10.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤.下列说法正确的是()A.C. 的溶液为饱和溶液D. 中没有固体存在二、填空题11.如图是a、b、c三种物质的溶解度曲线,请据图回答:(1)t2℃时,a、b、c三种物质的溶解度由大到小的顺序是______(填序号,下同);(2)t2℃时,将100g a物质加入到100g水中并充分搅拌,形成溶液的质量为______g;(3)将t2℃时a、b、c三种物质的饱和溶液降低温度到 t1℃时,这三种溶液中溶质质量分数的大小关系是______.12.甲、乙两种固体的溶解度曲线如图所示.(1)______℃时,甲和乙的溶解度相等;(2)40℃时,若将40g乙(不含结晶水)放入160g水中充分溶解,所得溶液的溶质质量分数为______,该溶液是______溶液(填“饱和”或“不饱和”);(3)40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲)______m(乙)(填“>”、“﹦”或“<”).13.如图是A、B、C三种固体物质的溶解度曲线.(S单位:g/100g水,t单位:℃)回答以下问题:①20℃时,A物质的溶解度______(填>、=、<)B物质的溶解度。
专题10 溶解曲线(原卷版)
专题10 溶解曲线一、正确理解溶解度曲线的涵义溶解度曲线就是在直角坐标系中,用来描述物质的溶解度随温度变化而变化的曲线。
根据溶解度曲线可进行溶液的配制,混合物的分离与提纯,以及进行物质结晶或溶解的计算。
近年来,以溶解度曲线为切入点的题目已成为中考、竞赛命题的一个热点。
下面,我们从溶解度曲线的特点入手,对溶解度作进一步的理解。
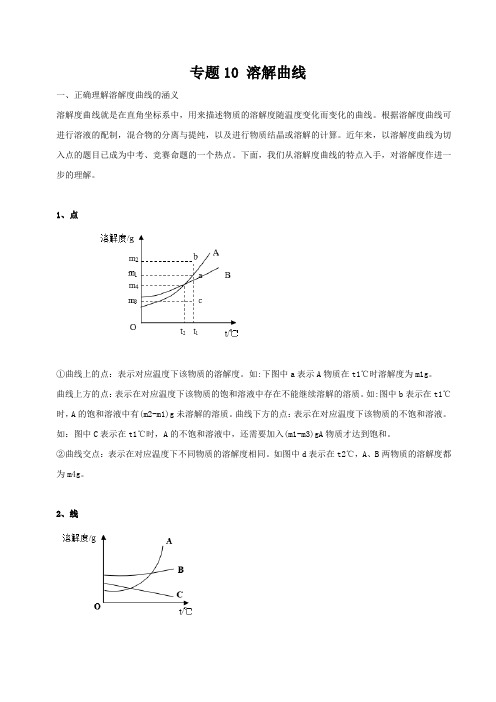
1、点①曲线上的点:表示对应温度下该物质的溶解度。
如:下图中a表示A物质在t1℃时溶解度为m1g。
曲线上方的点:表示在对应温度下该物质的饱和溶液中存在不能继续溶解的溶质。
如:图中b表示在t1℃时,A的饱和溶液中有(m2-m1)g未溶解的溶质。
曲线下方的点:表示在对应温度下该物质的不饱和溶液。
如:图中C表示在t1℃时,A的不饱和溶液中,还需要加入(m1-m3)gA物质才达到饱和。
②曲线交点:表示在对应温度下不同物质的溶解度相同。
如图中d表示在t2℃,A、B两物质的溶解度都为m4g。
2、线如图中A物质的溶解度随温度升高而明显增大,A曲线为“陡升型”。
如KNO3等大多数固体物质。
图中B物质的溶解度随温度变化不大,B曲线为“缓升型”,如NaCl等少数固体物质。
图中C物质的溶解度随温度升高而减小,C曲线为“下降型”,如气体及Ca(OH)2等极少数固体物质。
二、掌握溶解度曲线的应用1. 溶解度曲线上的每一点,代表着某温度下某物质的溶解度,因此利用溶解度曲线可以查出某物质在不同温度下的溶解度,并根据物质的溶解度判断其溶解性。
2. 可以比较在同一温度下不同物质溶解度的相对大小。
3. 根据溶解度曲线的形状走向,可以看出某物质的溶解度随温度的变化情况。
并根据此情况可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法。
例如:某物质的溶解度曲线“陡”,表明该物质溶解度随温度变化明显,提纯或分离该物质时适合采用降温结晶法。
某物质溶解度曲线“平缓”,提纯或分离该物质时适合采用蒸发溶剂法。
4. 从溶解度曲线上的交点,可以判断哪些物质在该点所示的温度下具有相同的溶解度。
中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)

中考化学《溶解度及溶解度曲线》专项练习题(附答案解析)1. 甲、乙、丙三种固体物质的溶解度曲线如右图所示。
下列说法不正确的是()A. T2℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙B. T2℃时,将甲、乙的饱和溶液均降温到T1℃,得到的溶液仍饱和C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲D. T2℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液2. 下图是甲、乙两种固体物质的溶解度曲线。
下列说法中错误的是( )A. 20℃时,甲、乙饱和溶液中溶质质量分数相等B. 40℃时,甲的溶解度大于乙的溶解度C. 40℃时,乙的饱和溶液中溶质的质量分数为40%D. 将40℃甲的饱和溶液降温到20℃,会有晶体析出3. KNO3与KCl的溶解度曲线如右图所示。
下列说法正确的是( )A. KNO3的溶解度比KCl的溶解度大B. t1温度下的KCl的饱和溶液升温至t2,有晶体析出C. A点所表示的KCl饱和溶液溶质的质量分数为29%D. 冷却热的KNO3饱和溶液可获得KNO3晶体4. ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示。
下列说法正确的是( )A. N点对应的ZnSO4溶液升温或降温均都可能析出晶体B. M点对应的ZnSO4溶液是不饱和溶液C. ZnSO4饱和溶液的溶质质量分数随温度升高而增大D. 40℃时,ZnSO4的溶解度为41g5. 下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 甲的溶解度大于乙的溶解度B. 降温可使接近饱和的丙溶液变为饱和溶液C. 将t2°C甲、乙、丙的饱和溶液降温至t1℃,所得溶液的溶质质量分数℃乙>甲=丙D. P点表示t1℃时甲、丙两种物质的溶解度都是25g6. 下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )A. 乙中含有少量甲,可用冷却热饱和溶液的方法提纯甲B. t3℃时,甲的溶液溶质质量分数一定大于乙的溶液溶质质量分数C. t3℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t2℃,析出晶体的质量甲一定大于乙D. t1℃时,乙的不饱和溶液只有通过蒸发溶剂的方法才能转变成饱和溶液7.甲、乙、丙三种固体物质的溶解度曲线如图所示。
专项溶解度曲线及溶质质量分数图像

考点突破
如图G7-1是A、B、C三种物质的溶解度曲线。
图G7-1
1.判断固体物质的溶解度随温度变化的趋势
(1)上升型:溶解度随温度升高而增大,如图中物质 A、B ;根据溶解度曲线又可分为①缓升
型,如图中物质
B
,②陡升型,如图中物质
A
(2)下降型:溶解度随温度升高而减小,如图中物质
结晶法;提纯含有少量A物质的B物质,应采用
结晶法。
(1)陡升型溶解度曲线固体物质,如从A饱和溶液中提纯A,应采用
结晶法。
5.涉及溶解度的简单计算
溶解度曲线呈上升型的固体物质(如A、B)
溶解度曲线呈下降型的固体物质(如C)
(1)计算饱和溶液中溶Hale Waihona Puke 质量分数:饱和溶液中溶质质量分数=
×100%(S 表示溶解度),如 t3 ℃
。
C
。
2.曲线上的点和两曲线交点
(1)点:表示该温度下,某固体物质的溶解度,如t3 ℃时,A的溶解度为
g水中最多可以溶解
80
g A物质形成 饱和
相等
g,由此说明该温度下100
(填“饱和”或“不饱和”)溶液。
(2)交点:如图中P点,表示在t2 ℃时,两物质的溶解度
数
80
相等
,两物质饱和溶液中溶质质量分
如图G7-1是A、B、C三种物质的溶解度曲线。
②升温(从t1 ℃升温至t2 ℃):由于A、B溶解度随温度升高而 增大 ,溶液中溶质的质量 不变 ,溶
如图G7-1是A、B、C三种物质的溶解度曲线。
减小 ,溶液中有晶体析出,升温时溶质质量 减小 ,
质质量分数 不变 ;而C的溶解度随温度升高而
中考化学经典题型专题练习之溶解性、溶解度和溶解度曲线
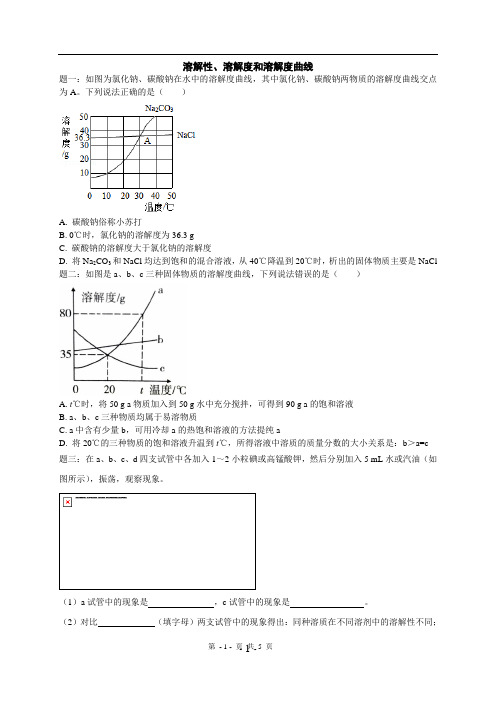
溶解性、溶解度和溶解度曲线题一:如图为氯化钠、碳酸钠在水中的溶解度曲线,其中氯化钠、碳酸钠两物质的溶解度曲线交点为A。
下列说法正确的是()A. 碳酸钠俗称小苏打B. 0℃时,氯化钠的溶解度为36.3 gC. 碳酸钠的溶解度大于氯化钠的溶解度D. 将Na2CO3和NaCl均达到饱和的混合溶液,从40℃降温到20℃时,析出的固体物质主要是NaCl 题二:如图是a、b、c三种固体物质的溶解度曲线,下列说法错误的是()A. t℃时,将50 g a物质加入到50 g水中充分搅拌,可得到90 g a的饱和溶液B. a、b、c三种物质均属于易溶物质C. a中含有少量b,可用冷却a的热饱和溶液的方法提纯aD. 将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a=c题三:在a、b、c、d四支试管中各加入1~2小粒碘或高锰酸钾,然后分别加入5 mL水或汽油(如图所示),振荡,观察现象。
(1)a试管中的现象是,c试管中的现象是。
(2)对比(填字母)两支试管中的现象得出:同种溶质在不同溶剂中的溶解性不同;对比a、c试管中的现象得出的结论是;(3)【提出问题】物质的溶解性除与溶质、溶剂的性质有关外,还与什么有关?【作出猜想】。
【设计方案】。
【观察现象】。
【得出结论】。
题四:小明陪妈妈到医院输液,不小心将护士手中的盘子打翻,其中的棉球落在了小明的白色衬衣上,白色衬衣上立即出现了一大片紫黑色痕迹。
为找到去掉白衬衣上的痕迹的最好方法,几位同学进行了讨论,提出了以下几个方案并进行实验:①用水洗;②用无水酒精洗;③用汽油洗;④用四氯化碳洗;⑤用肥皂水洗;⑥用淀粉溶液洗。
(1)你认为留在白色衬衣上的紫黑色物质是什么?(2)如果用白色布条进行实验,为使实验结果更加准确,你认为该实验中需要控制哪些实验条件?(3)一位同学按如图所示方法进行实验:结果是⑤、⑥几乎完全褪色;②略带颜色;③、④略微变浅;①几乎不变。
人教版九年级化学下册 溶解度曲线 专题训练(word版,含答案)

溶解度曲线专题训练1.如图是甲乙两种物质的溶解度曲线。
下列说法正确的是A.甲的溶解度比乙的溶解度大B.a2℃时,将30g甲放入50g水中充分搅拌可得80g溶液C.a1℃时甲、乙两种物质的饱和溶液溶质的质量分数相同D.将a1℃时甲、乙两种物质的饱和溶液升温至a2℃,溶质的质量分数都增大2.如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是()A.使a、c的饱和溶液析出晶体的方法都可以是降温结晶B.t1℃时,a、c两种物质的溶液的溶质质量分数一定相等C.在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80gD.t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c3.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.甲物质的溶解度随温度的升高而增大B.t2℃时,甲、乙两种物质的溶解度相等C.t1℃时,丙的饱和溶液中溶质的质量分数为40%D.当甲中混有少量丙时,可采用降温结晶的方法提纯4.如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是()A.a的溶解度大于b的溶解度B.P点表示t1℃时a、c两物质溶解度相等C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质最分数由大到小的顺序为:b>a=c5.甲、乙两种固体的溶解度曲线如右图所示,下列说法正确的是A.甲的溶解度大于乙的溶解度B. t1°C时,甲乙饱和溶液中溶质的质量分数相等C. t2°C时,60g 甲的饱和溶液稀释到20%需加水10gD.将t1°C时相等质量的甲、乙的饱和溶液升温到t2°C,溶液中溶质的质量甲大于乙6.A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是()A.阴影区域中,A、C均处于不饱和状态B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯BC.将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>BD.t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%7.甲、乙两种物质溶解度曲线如图所示。
中考化学考点专训:溶解度及溶解度曲线
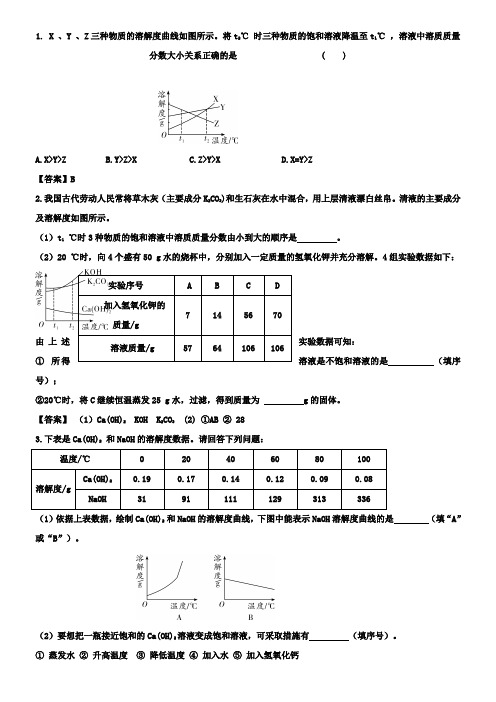
1. X 、Y 、Z三种物质的溶解度曲线如图所示。
将t2℃时三种物质的饱和溶液降温至t1℃,溶液中溶质质量分数大小关系正确的是 ( )A.X>Y>ZB.Y>Z>XC.Z>Y>XD.X=Y>Z【答案】B2.我国古代劳动人民常将草木灰(主要成分K2CO3)和生石灰在水中混合,用上层清液漂白丝帛。
清液的主要成分及溶解度如图所示。
(1)t1℃时3种物质的饱和溶液中溶质质量分数由小到大的顺序是。
(2)20 ℃时,向4个盛有50 g水的烧杯中,分别加入一定质量的氢氧化钾并充分溶解。
4组实验数据如下:由上述实验数据可知:①所得溶液是不饱和溶液的是(填序号);②20℃时,将C继续恒温蒸发25 g水,过滤,得到质量为 g的固体。
【答案】(1)Ca(OH)2 KOH K2CO3 (2) ①AB ② 283.下表是Ca(OH)2 和NaOH的溶解度数据。
请回答下列问题:温度/℃0 20 40 60 80 100溶解度/gCa(OH)2 0.19 0.17 0.14 0.12 0.09 0.08NaOH 31 91 111 129 313 336(1)依据上表数据,绘制Ca(OH)2 和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是(填“A”或“B”)。
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有(填序号)。
①蒸发水②升高温度③降低温度④加入水⑤加入氢氧化钙实验序号 A B C D加入氢氧化钾的质量/g7 14 56 70溶液质量/g 57 64 106 106(3)现有60 ℃时含有Ca(OH)2 和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是。
(4)现有20 ℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20 ℃,得到乙溶液,溶液中溶质的质量分数的关系为甲乙(填“>”、“<”或“=”)。
初三化学中考专题(5)溶解度曲线练习及答案

专题五溶解度曲线1。
a、b两种物质的溶解度曲线如图所示。
下列说法不正确的是A。
将t1℃时b的饱和溶液加水可变为不饱和溶液B。
将t2℃时a的饱和溶液降温至t1℃,溶液质量不变C.t2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t2℃时,甲、乙两种物质的溶解度相等B。
甲的溶解度随温度的升高而增大C。
分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%3。
下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是A。
甲>乙>丙 B。
甲=乙=丙C.甲=乙>丙D.丙>甲=乙4。
(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t1℃时,甲物质的溶解度为20gB。
t1℃时,30g甲加入到50g水中最多可得70g溶液C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5。
(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A。
甲的溶解度大于乙的溶解度B。
实验过程中,属于不饱和溶液的是A溶液和C溶液C.实验过程中,只有B溶液和D溶液属于饱和溶液D.实验过程中,B溶液与E溶液中溶质的质量分数相同6。
(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液B。
t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C。
分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。
中考化学 专题05 溶解度曲线(含解析)

专题05 溶解度曲线此类试题在解题时应注意:1、正确理解溶解曲线上的点、线等构图元素的含义;2、结合溶液中其他概念及原理进行判断;3、在变化过程中要找清变量和不变量。
预测题:1.甲、乙两种不含结晶水的固体物质溶解度曲线如图,下列说法中不正确的是()A.t1℃时,50g甲的饱和溶液中溶解了10g的甲B.将t2℃甲、乙两种物质的饱和溶液升温至t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等C.t2℃时,要使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法D.分别将t2℃甲、乙两种物质的溶液降温至t1℃,一定都有晶体析出【答案】 AD【解析】试题分析:A、由甲的溶解度曲线可知,在t1℃时,甲的溶解度是20g,由溶解度的意义可知,在60g甲的饱和溶液中溶解了10g的甲.故A说法不正确;B、由甲、乙两种物质溶解度曲线可知,在t2℃时甲、乙两种物质的溶解度相等,溶液的溶质的质量分数相等.在升高温度时,甲、乙的溶解度都随温度的升高而增大,溶液都由饱和溶液变为不饱和溶液,溶液中溶质、溶剂质量不变,两种溶液中溶质的质量分数相等.故B说法正确;C、t2℃时,要使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法.故C说法正确;D、由于在t2℃时,甲、乙两种物质的溶液不一定是饱和溶液,所以,在降温至t1℃时,不一定都有晶体析出.故D说法不正确.故选AD.考点:溶解度曲线2.右图是a、b、c三种物质的溶解度曲线。
由图判断下列说法中不正确的是A.a的饱和溶液从t2℃降温至t l℃时仍为饱和溶液B.在t2℃时,a、b两溶液中溶质的质量分数相等C.c的溶解度随温度的升高而减小D.t1℃时,a的60g饱和溶液中含有溶剂50 g【答案】B【解析】试题分析:A.从t2℃降温至t l℃时a的溶解度变小,所以溶液仍为饱和溶液。
此项正确。
B.在t2℃时,a、b两物质的溶解度相等,则其饱和溶液中溶质的质量分数相等。
如溶液不饱和无法确定。
高考化学专题复习——溶解度曲线课堂练习

溶解度曲线课堂练习1.下图是某物质的溶解度曲线。
根据该图判断下列说法错误的是()A.M点对应溶液是t2℃的不饱和溶液B.在保持溶质质量不变的情况下,使M点达到饱和需降温(t2-t1)℃C.130gM点溶液最少要蒸发50g水后,才能成为的t1℃饱和溶液D.若保持温度不变,325gM点溶液需加入溶质60g才能达饱和2.下图是a、b两种固体物质的溶解度曲线,下列说法中不正确的是()A.a的溶解度大于b的溶解度B.在时,a、b的饱和溶液中溶质的质量分数相同C.当a中含有少量b时,可以用结晶法提纯aD.a、b都属于易溶物质3.如图为硝酸纳、硝酸钾、氯化钠、氯化钾的溶解度曲线。
请回答下列问题:(1)工业上将硝酸钠和氯化钾按100:87(质量比)溶于热水中,加热蒸发,产生大量晶体,这些晶体是什么?(2)趁热过滤,并用少量蒸馏水淋洗晶体,淋洗所得溶液并入滤液中,淋洗的目的是什么?(3)边搅拌边冷却滤液,此时又析出大量晶体。
过滤。
并用少量蒸馏水洗涤晶体。
问应当用冷水还是热水?(4)第(3)步所得晶体,经重结晶、干燥即得产品。
问产品是什么?4.A、B两种物质的饱和溶液的百分比浓度随温度变化的曲线如图:现分别在50克A和80克B中各加水150克,加热溶解后并都蒸发水50克, ℃,下列叙述正确的是 ( ) 冷却到t1℃时溶液中A、B的质量百分比浓度相等A.t1℃时溶液中A的浓度小于B的浓度B.t1C.t℃时两者均无固体析出1D.t℃时析出固体B1。
原题:化学实验中的溶解度曲线

原题:化学实验中的溶解度曲线
引言
溶解度曲线是指在特定温度下,溶质在溶剂中溶解的质量与溶液中溶质的浓度之间的关系曲线。
该曲线可以帮助我们理解溶解过程中的动力学和热力学特性,以及预测溶解性的变化。
本文将介绍化学实验中测定溶解度曲线的方法和步骤。
实验步骤
1. 准备实验室设备和试剂:包括天平、容量瓶、烧杯、搅拌器等。
选择适合的溶剂和溶质,并准备不同浓度的溶液。
2. 将一定量的溶剂加入容量瓶中,控制好温度。
3. 将适量的溶质逐渐加入溶剂中,同时用搅拌器充分搅拌,直至达到饱和状态。
4. 重复步骤3,使用不同浓度的溶液,分别制备多组数据。
5. 根据实验数据,通过计算溶质的浓度和溶解质量的比值,绘制溶解度曲线图。
实验注意事项
1. 溶剂的选择要与溶质相容,并具有较高的溶解度。
2. 控制好实验温度,以免影响溶解度曲线的准确性。
3. 实验过程中要充分搅拌,以促进溶质与溶剂的混合。
4. 测量时要注意保持精确,避免误差。
5. 实验完成后,应及时清洗实验器材,并妥善处理产生的废液和废品。
结论
通过实验测定溶解度曲线,我们可以获得溶质在不同浓度下的溶解质量数据,并绘制出溶解度曲线图。
该曲线图对于分析和理解溶解过程中的各种因素具有重要的指导意义。
我们可以根据溶解度曲线图预测溶解性的变化,并在实际应用中指导溶解过程的控制和优化。
参考文献
[1] XXXX
[2] XXXX。
微专题5 溶解度曲线及溶解度表分析-备战2024年中考化学一轮复习考点帮(人教版)

微专题5 溶解度曲线及溶解度表分析考向一溶解度曲线分析1、解答此类题目的关键(1)明确溶解度曲线上点的含义(某点是在某温度时某物质的溶解度是多少g。
交点是在某温度时,两物质的溶解度相等。
线上方的点表示是饱和溶液,下方的点表示不饱和溶液);(2)明确物质的溶解度随温度变化的趋势(线越陡,表示该物质溶解度受温度影响较大);(3)明确饱和溶液中溶质的质量大小的判断方法;(4)明确判断溶质的质量分数大小关系的方法。
2、溶解度曲线:线的含义:三线:①“陡升型” :大多数固体物的溶解度随温度升高而升高。
如KNO3;②“缓升型”:少数固体物质的溶解度受温度的影响很小。
如NaCl;③“下降型”:极少数物质溶解度随温度升高而降低。
如Ca(OH)2。
3、点的含义:四点:①曲线上的点:所示某温度下某物质的溶解度是多少(该温度下饱和状态)。
②两曲线的交点:表示在该点所示的温度下,两种物质的溶解度相等。
③线上方的点表示:在该温度下,该溶液是饱和且有部分晶体;③线下方的点表示:该温度下,该溶液是不饱和溶液。
1. 【2023四川内江真题】甲、乙两种物质的溶解度曲线如图所示,下列有关说法错误的是()A. 两种物质的溶解度都随温度升高而增大B. t1°C时,甲、乙两物质的溶液中溶质质量分数一定相等C. 通常采用蒸发结晶的方法从乙的溶液中获得晶体D. t2°C时,在100g水中加入25g甲,可形成甲的不饱和溶液【答案】B【解析】A. 由溶解度曲线可知,两种物质的溶解度都随温度升高而增大,此选项正确;B. t1°C时,甲、乙两物质的溶解度相等,则t1°C时,甲、乙两物质的饱和溶液中溶质质量分数一定相等,此选项错误;C. 乙的溶解度受温度影响不大,对于溶解度受温度影响不大的物质,一般采用蒸发结晶法从溶液中获取晶体,此选项正确;D. 由溶解度曲线可知,t2°C时,甲的溶解度大于25g,则在100g水中加入25g甲,可形成甲的不饱和溶液,此选项正确。
2024年中考化学专题强化训练溶解度曲线
2024年中考化学专题强化训练溶解度曲线1.生活离不开化学。
氯化钠和蔗糖分别是咸味剂、甜味剂,其溶解度曲线如图所示(左侧纵坐标是氯化钠的溶解度,右侧是蔗糖的)。
(1)60℃时(填“能”或“不能”)配得100%的蔗糖溶液。
(2)将20℃时氯化钠的饱和溶液恒温蒸发掉50g水,理论上得到氯化钠的质量是g。
(3)已知:水的密度是1g/mL。
向10g9%的NaCl溶液中加入mL水,可稀释为0.9%的生理盐水。
配制溶液过程中需用到的玻璃仪器有(填字母)。
A.烧杯B.玻璃棒C.量筒D.酒精灯E.漏斗F.胶头滴管2.回答下列问题:(1)从乙的溶液中获得乙物质适宜采用的方法。
(2)若甲物质中含有少量乙物质,可采用的方法提纯甲物质。
(3)若乙物质中含有少量甲物质,可采用的方法提纯乙物质。
(4)若丙物质中含有少量甲物质,可采用的方法提纯丙物质。
3.小明参加学校组织的劳动实践活动。
(1)小明在麦田劳动时看到麦子叶色浓绿,长势喜人,农场工人告诉他是及时施用了一种复合肥。
农场仓库存放的化肥有KNO3、K2SO4、NH4Cl,其中属于复合肥的是,三种化肥包装袋上均写着防雨防潮。
其原因是 。
(2)小明想在家里尝试无土栽培,便从农场带回了三种化肥,使用时却因标记不清而无法区分KNO 3和K 2SO 4,于是到化学实验室进行鉴别。
他取少量其中一种化肥于试管中,加水溶解后,向其中滴加2~3滴某溶液,立即出现了白色沉淀,可确定所取的化肥是K 2SO 4。
请写出发生反应的化学方程式: (只写一个)。
(3)配制无土栽培营养液时,小明依据如图想先配制两种化肥的饱和溶液以备后用。
A .如图,若要提纯KNO 3则用 方法。
B .配制时,假设室温为20℃,若小明用等体积的水配制成恰好饱和的两种化肥溶液,则两种溶液中NH 4Cl 与KNO 3的质量比为 。
4.1t C 时,将a b 、两种固体物质(均不含结晶水)各25g ,分别加入盛有100g 水的烧杯中,充分搅拌后现象如图甲所示;升温到2t C 时,忽略水分蒸发,现象如图乙所示。
中考化学-专题05-溶解度曲线

溶解度曲线一、选择题1. a、b 两种物质的溶解度曲线如右图所示.下列说法不正确的是()A.15℃时,a、b 的溶解度均为 20g B.加水或升温均可使 b 的饱和溶液变为不饱和溶液C.将30℃时 a 的饱和溶液降温至15℃,溶质的质量分数不变D.分别向 100g 水中加入 20ga 和 b,升温至30℃,所得溶液均为饱和溶液2.甲、乙两种固体物质的溶解度曲线如右图所示。
下列说法正确的是()A.甲的溶解度大于乙的溶解度 B.升高温度可使甲的不饱和溶液变为饱和溶液C.t1℃时,甲、乙两种饱和溶液的溶质质量分数相等D.t2℃时,50g乙加入100g水中得到乙的不饱和溶液3.如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是()A.甲物质的溶解度随温度的升高而增大B.在t1℃时,甲、乙两物质的溶解度相等C.在t2℃时,N点表示甲物质的不饱和溶液D.在t1℃时,100g乙物质的饱和溶液中溶质的质量是25g4.根据如图中A、B、C三种物质的溶解度曲线,回答下列问题.(1)t 2℃时,A、B、C三种物质的溶解度由大到小的顺序是(填物质序号).(2)t2℃时,30gA物质投入到50g水中所得到溶液的质量为g.(3)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃,三种溶液溶质量分数由大到小的顺序是(填序号).5.溶液在生产和生活中有着重要意义。
如图是A、B、C三种固体物质溶解度曲线,请回答列相关问题:(1)t2℃时,A、B、C三种物质的溶解度从大到小的顺序是;(2)将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,所得溶液中溶质的质量分数最小..的是。
一.选择题3.(10茂名)右图为A、B两种不带结晶水的固体物质溶解度曲线,下列说法不正确的是A.30℃时,A物质的溶解度为20g B.20℃时,A和B的溶解度相同C.10℃时,等质量的A和B饱和溶液中,B的溶剂最少D.等质量的A、B的饱和溶液从30℃降到20℃时,B析出的晶体最多4.(10苏州)根据下列几种物质溶解度曲线图,得到的结论正确的是6.(10江苏泰州)右图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是A.在t1℃时,三种物质的溶解度由大到水的顺序是甲>乙>丙B.在t2℃时,甲、乙两物质的溶解度相等C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙4.(2010辽宁鞍山)小明同学绘制了如右图所示A、B两种固体物质的溶液度曲线:(1)当温度为℃时,A物质与B物质的溶解度相等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2015武汉市化学专题训练-溶解度曲线1.(2015•重庆模拟)如图是甲、乙、丙三种物质的溶解度曲线,在t1℃时,分别取等质量的甲、乙、丙三种物质的饱和溶液放入三个烧杯中,然后再向溶液中分别加入等质量的相应固体物质,再将温度升高到大于t2℃,结果甲全部溶解,丙部分溶解,试回答下列问题:(1)当温度升高到大于t2℃时乙物质固体质量,(填“增加”、“减少”或“不变”)(2)依次写出甲、乙、丙三种物质的溶解度曲线的序号:(用a、b、c填写)(3)将在t2℃时的三物质的饱和溶液降温到t1℃,得到的溶液的溶质质量分数由大到小的顺序是.2.(2015•普陀区一模)图甲是A、B、C三种固体物质的溶解度曲线图.①甲图中,t2℃时,A、B、C三种物质中溶解度最大的是.P点表示.②将t2℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,三种物质的溶液中溶质质量分数由大到小的顺序是.③如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小块生石灰,再加入5mL水,几分钟后烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的(填写物质编号),试管内发生的化学反应方程式为.④t2℃时,B物质的溶解度为40g/100g水,在150g水中投入g的B物质,溶液将达到饱和.3.(2015•奉贤区一模)甲、乙两种物质的溶解度曲线如图所示.①℃时,甲、乙的溶解度相等.②若甲中含有少量乙,提纯甲可采用的方法是.③将t1℃时等质量的甲、乙饱和溶液升温至t2℃,若采用加溶质的方法使两者重新达到饱和,则物质所加的量多.④t1℃时,向一只盛有15g甲的烧杯中加入50g水,充分搅拌后烧杯底部仍有未溶解的固体.下列相关叙述不正确的是.A.t1℃时,甲的溶解度为30g/100g水B.烧杯中溶液的质量小于65gC.降温后烧杯中溶液总质量不变D.取烧杯中上层清液加热变为不饱和溶液.4.(2015•青冈县校级一模)如图所示是甲和乙两种固体物质的溶解度曲线,根据溶解度曲线回答下列问题:(1)甲中含有少量的乙提纯甲的方法.(2)t2时等质量的甲乙饱和溶液降到t1时析出固体比较多的是(3)若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是A、溶剂的质量一定变小B、溶质的质量可能不变C、溶质的质量分数一定变大D、溶液的质量变大(4)t2,在60g水中加入50g固体甲充分溶解后得到溶液的质量为g,溶液为溶液(填报“饱和”或“不饱和”)5.(2015•溧水县校级模拟)A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题:(1)t1℃时,A的饱和溶液中溶质与溶液质量比;(2)若B中含有少量A,应用法提纯B;若当A中混有少量B时,可用方法提纯A;(3)若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改变的是.A.溶解度B.溶剂质量C.溶质质量D.溶质质量分数.(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是(填“A”或“B”).(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有(填序号).①蒸发水②升高温度③降低温度④加入水⑤加入氢氧化钙(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是.(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲乙(填“>”“<”或“=”).7.(2015•郑州模拟)如图是X、Y、Z三种物质的溶解度曲线.(1)溶解度变化受温度影响最大的是.(2)t℃时,溶解度最大的是.(3)t℃时,饱和Z溶液中溶质与溶剂的质量比是.要进一步提高该溶液的质量分数,可进行的操作是.8.(2015•闵行区一模)如图是常见固体物质的溶解度曲线,根据图示回答:①d点的意义是.②将t1℃一定量的A的饱和溶液升温至t3℃时,可用图上的点表示;若要将b点的70g A溶液转化为c点的A溶液,采用的方法有加入溶质g或蒸发溶剂g.③t2℃时相同质量的A、B、C三种物质饱和溶液的溶剂质量由大到小的顺序是.④若将t3℃三种物质的饱和溶液分别降温到t1℃时,则对三种溶液的说法一定正确的是.Ⅰ.都是饱和溶液Ⅱ.溶质的质量分数:B%>C%>A%Ⅲ.溶剂质量不变Ⅳ.析出溶质的质量:mA>mB>mC.9.(2015•陕西模拟)根据图一的甲、乙溶解度曲线和图二实验现象回答下列问题:(1)图一中,甲物质的四种溶液状态“a、b、c、d”中,处于不饱和状态的是(填写编号).(2)90g甲的饱和溶液从t3℃冷却到t2℃点,析出的无水晶体质量是g.(3)在某温度范围内,将等质量的甲、乙两种固体物质溶解在水中,所得现象如图二所示,则两溶液质量分数甲(填“>”或“<”)乙,实验时控制温度t的范围是时,均能出现这种现象.10.(2015•垫江县校级模拟)小明同学绘制了如图所示A、B两种固体物质的溶解度曲线:(1)当℃时,A物质与B物质的溶解度相等;(2)若将A物质从溶液中结晶析出,宜采用的结晶方法是:.11.(2015•满洲里市校级模拟)(1)t1℃时,甲物质的溶解度为.(2)M点的含义是(3)若从甲和丙的混合物中得到甲,应采取的最好方法是.12.(2015•重庆模拟)请根据如图曲线回答:(1)t1℃时KNO3的溶解度是,图中A点的意义是.(2)t1℃时,两种物质饱和溶液的溶质质量分数的关系是:KNO3NaCl(填“>”、“<”或“=”).(3)现有操作步骤:a.冷水溶解、b.干燥、C.降温、d.过滤、e.洗涤、f.热水溶解.若KNO3晶体中含有少量NaCl,请选择提纯KNO3的实验操作步骤及操作顺序是(填序号).13.(2015•重庆模拟)如图是A、B、C三种物质的溶解度曲线.试回答下列问题:(1)在20℃时,将等质量的三种物质的饱和溶液升温到30℃,三者的质量分数关系是;如降至10℃,析出晶体最多是,无晶体析出的是.(2)根据该图可知:B的溶解度小于A的溶解度的温度范围是.(3)A、B两种物质饱和溶液溶质质量分数相等的温度是.(4)当A、C两种物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是物质的溶液.14.(2015•静海县模拟)图1为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:(1)10℃时,碳酸钠的溶解度为g;(2)P点表示;(3)当温度时,氯化钠的溶解度大于碳酸钠的溶解度.(4)若想从NaCl的溶液中得到其晶体,最好采用结晶方法.(5)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是(填字母序号).A.氢氧化钠B.生石灰C.硝酸铵D.浓硫酸.15.(2015•潮阳区模拟)水和溶液在生命活动和生活中起着十分重要的作用.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如表:(1)图1中能表示KNO3溶解度曲线的是(填“甲”或“乙”);(2)溶解度曲线上M点的含义是;(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的是(填字母序号).A.烧杯②中溶液一定是不饱和溶液B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大.16.(2015•潍坊校级一模)如图甲是A、B、C三种固体物质的溶解度曲线图.(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是.P点所表示的含义.(2)t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法.(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,写出反应的化学方程式同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?.17.(2015•宝山区一模)如图为甲、乙、丙三种不含结晶水的固体物质溶解度曲线,据图回答:①图中物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似.②t1℃时,25g甲物质的饱和溶液中,含甲物质克.③t3℃时,取等质量甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量最小的是物质.④现有甲、乙、丙三种物质的浓溶液,可用海水晒盐原理进行结晶提纯的是物质.⑤下列叙述中错误的是.A.t1℃时,甲、乙、丙三种物质溶液的溶质质量分数可能相等B.t2℃时,甲、乙物质溶解度相等,则两种溶液的溶质质量分数也相等C.t1℃时,甲、乙、丙三种物质的溶液分别升温(溶剂不蒸发),丙物质溶液浓度可能发生改变D.t3℃时,甲、乙、丙三种物质的饱和溶液降温到t1℃时,析出晶体最多是甲物质.18.(2015•株洲模拟)三种固体物质A、B、C溶解度曲线如图所示,试回答:(1)溶解度受温度变化影响最大的物质是,影响不大的物质是.(2)t1℃时三种物质溶解度由小到大的顺序.(3)t2℃时,溶解度最大的物质是,A、B两物质溶解度相等的温度是.(4)Q点表示,P点表示.(5)A中含有少量B时,采用的分离方法是.19.(2015•垫江县校级模拟)在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.(1)从右图溶解度曲线可以得到的信息是(写一条).(2)小明参照右图在常温20℃时进行了如下实验:小明观察到A中所加固体全部溶解,则B中的现象是.上述实验过程中属于不饱和溶液的是(填字母).D中溶液的溶质质量分数是.20.(2015•重庆模拟)如图是甲、乙两种固体物质的溶解度曲线.(1)t2℃时,甲物质的溶解度为;(2)从图中你还能获得哪些信息?;(3)分析t1℃时,将10g乙物质放入100g水中,充分溶解后所得的溶液是(填“饱和”或“不饱和”)溶液.欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的方法.【考点训练】固体溶解度曲线及其作用-2参考答案与试题解析二、填空题(共20小题)(除非特别说明,请填准确值)11.(2015•重庆模拟)如图是甲、乙、丙三种物质的溶解度曲线,在t1℃时,分别取等质量的甲、乙、丙三种物质的饱和溶液放入三个烧杯中,然后再向溶液中分别加入等质量的相应固体物质,再将温度升高到大于t2℃,结果甲全部溶解,丙部分溶解,试回答下列问题:(1)当温度升高到大于t2℃时乙物质固体质量增加,(填“增加”、“减少”或“不变”)(2)依次写出甲、乙、丙三种物质的溶解度曲线的序号:acb(用a、b、c填写)(3)将在t2℃时的三物质的饱和溶液降温到t1℃,得到的溶液的溶质质量分数由大到小的顺序是b>a>c.12.①甲图中,t2℃时,A、B、C三种物质中溶解度最大的是A.P点表示在t1℃时BC 的溶解度相等.②将t2℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,三种物质的溶液中溶质质量分数由大到小的顺序是BCA.③如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小块生石灰,再加入5mL水,几分钟后烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的C(填写物质编号),试管内发生的化学反应方程式为CaO+H2O=Ca(0H)2.④t2℃时,B物质的溶解度为40g/100g水,在150g水中投入60g的B物质,溶液将达到饱和.13.(2015•奉贤区一模)甲、乙两种物质的溶解度曲线如图所示.①t2℃时,甲、乙的溶解度相等.②若甲中含有少量乙,提纯甲可采用的方法是降温结晶(或冷却热饱和溶液).③将t1℃时等质量的甲、乙饱和溶液升温至t2℃,若采用加溶质的方法使两者重新达到饱和,则甲物质所加的量多.④t1℃时,向一只盛有15g甲的烧杯中加入50g水,充分搅拌后烧杯底部仍有未溶解的固体.下列相关叙述不正确的是AC.A.t1℃时,甲的溶解度为30g/100g水B.烧杯中溶液的质量小于65gC.降温后烧杯中溶液总质量不变D.取烧杯中上层清液加热变为不饱和溶液.14.(2015•青冈县校级一模)如图所示是甲和乙两种固体物质的溶解度曲线,根据溶解度曲线回答下列问题:(1)甲中含有少量的乙提纯甲的方法降温结晶.(2)t2时等质量的甲乙饱和溶液降到t1时析出固体比较多的是甲(3)若将甲物质的不饱和溶液变为饱和溶液,下列说法正确的是BA、溶剂的质量一定变小B、溶质的质量可能不变C、溶质的质量分数一定变大D、溶液的质量变大(4)t2,在60g水中加入50g固体甲充分溶解后得到溶液的质量为108g,溶液为饱和溶液(填报“饱和”或“不饱和”)15.(2015•溧水县校级模拟)A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题:(1)t1℃时,A的饱和溶液中溶质与溶液质量比;(2)若B中含有少量A,应用蒸发结晶(或蒸发溶剂)法提纯B;若当A中混有少量B时,可用降温结晶方法提纯A;(3)若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改变的是B.A.溶解度B.溶剂质量C.溶质质量D.溶质质量分数.(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是A(填“A”或“B”).(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有①②⑤(填序号).①蒸发水②升高温度③降低温度④加入水⑤加入氢氧化钙(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是冷却热饱和溶液.(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲=乙(填“>”“<”或“=”).17.(2015•郑州模拟)如图是X、Y、Z三种物质的溶解度曲线.(1)溶解度变化受温度影响最大的是X.(2)t℃时,溶解度最大的是X.(3)t℃时,饱和Z溶液中溶质与溶剂的质量比是1:2.要进一步提高该溶液的质量分数,可进行的操作是降低温度后增加溶质或减少溶剂.18.(2015•闵行区一模)如图是常见固体物质的溶解度曲线,根据图示回答:①d点的意义是在t2℃时A和C的溶解度相等.②将t1℃一定量的A的饱和溶液升温至t3℃时,可用图上的b点表示;若要将b点的70g A 溶液转化为c点的A溶液,采用的方法有加入溶质20g或蒸发溶剂25g.③t2℃时相同质量的A、B、C三种物质饱和溶液的溶剂质量由大到小的顺序是A=C>B.④若将t3℃三种物质的饱和溶液分别降温到t1℃时,则对三种溶液的说法一定正确的是II、III.Ⅰ.都是饱和溶液Ⅱ.溶质的质量分数:B%>C%>A%Ⅲ.溶剂质量不变Ⅳ.析出溶质的质量:mA>mB>mC.19.(2015•陕西模拟)根据图一的甲、乙溶解度曲线和图二实验现象回答下列问题:(1)图一中,甲物质的四种溶液状态“a、b、c、d”中,处于不饱和状态的是b(填写编号).(2)90g甲的饱和溶液从t3℃冷却到t2℃点,析出的无水晶体质量是15g.(3)在某温度范围内,将等质量的甲、乙两种固体物质溶解在水中,所得现象如图二所示,则两溶液质量分数甲<(填“>”或“<”)乙,实验时控制温度t的范围是0℃~t2℃时,均能出现这种现象.20.(2015•垫江县校级模拟)小明同学绘制了如图所示A、B两种固体物质的溶解度曲线:(1)当40℃时,A物质与B物质的溶解度相等;(2)若将A物质从溶液中结晶析出,宜采用的结晶方法是:降温结晶.21.(2015•满洲里市校级模拟)(1)t1℃时,甲物质的溶解度为60g.(2)M点的含义是t2℃时,甲和乙物质的溶解度相等(3)若从甲和丙的混合物中得到甲,应采取的最好方法是降温结晶.22.(2015•重庆模拟)请根据如图曲线回答:(1)t1℃时KNO3的溶解度是bg,图中A点的意义是在t2℃时KN03与NaCl的溶解度相同,均为ag.(2)t1℃时,两种物质饱和溶液的溶质质量分数的关系是:KNO3<NaCl(填“>”、“<”或“=”).(3)现有操作步骤:a.冷水溶解、b.干燥、C.降温、d.过滤、e.洗涤、f.热水溶解.若KNO3晶体中含有少量NaCl,请选择提纯KNO3的实验操作步骤及操作顺序是(填序号)fcd.23.(2015•重庆模拟)如图是A、B、C三种物质的溶解度曲线.试回答下列问题:(1)在20℃时,将等质量的三种物质的饱和溶液升温到30℃,三者的质量分数关系是A=B >C;如降至10℃,析出晶体最多是A,无晶体析出的是C.(2)根据该图可知:B的溶解度小于A的溶解度的温度范围是t>20℃.(3)A、B两种物质饱和溶液溶质质量分数相等的温度是20℃.(4)当A、C两种物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是A物质的溶液.24.(2015•静海县模拟)图1为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:(1)10℃时,碳酸钠的溶解度为10g;(2)P点表示30℃时,碳酸钠与氯化钠的溶解度相同;(3)当温度小于30℃时,氯化钠的溶解度大于碳酸钠的溶解度.(4)若想从NaCl的溶液中得到其晶体,最好采用蒸发结晶方法.(5)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是C(填字母序号).A.氢氧化钠B.生石灰C.硝酸铵D.浓硫酸.25.(2015•潮阳区模拟)水和溶液在生命活动和生活中起着十分重要的作用.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如表:(1)图1中能表示KNO3溶解度曲线的是甲(填“甲”或“乙”);(2)溶解度曲线上M点的含义是t1℃时,碳酸钾和硝酸钾的溶解度相等;(3)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的是D(填字母序号).A.烧杯②中溶液一定是不饱和溶液B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大.26.(2015•潍坊校级一模)如图甲是A、B、C三种固体物质的溶解度曲线图.(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是A.P点所表示的含义t1℃时,B、C的溶解度相等.(2)t℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法加溶质、蒸发水.(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,写出反应的化学方程式Mg+2HCl=MgCl2+H2↑同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种?C.27.(2015•宝山区一模)如图为甲、乙、丙三种不含结晶水的固体物质溶解度曲线,据图回答:①图中丙物质的溶解度曲线与气体物质溶解度曲线受温度影响变化相似.②t1℃时,25g甲物质的饱和溶液中,含甲物质5克.③t3℃时,取等质量甲、乙、丙三种物质分别配制成饱和溶液,所得溶液质量最小的是甲物质.④现有甲、乙、丙三种物质的浓溶液,可用海水晒盐原理进行结晶提纯的是乙物质.⑤下列叙述中错误的是BD.A.t1℃时,甲、乙、丙三种物质溶液的溶质质量分数可能相等B.t2℃时,甲、乙物质溶解度相等,则两种溶液的溶质质量分数也相等C.t1℃时,甲、乙、丙三种物质的溶液分别升温(溶剂不蒸发),丙物质溶液浓度可能发生改变D.t3℃时,甲、乙、丙三种物质的饱和溶液降温到t1℃时,析出晶体最多是甲物质.28.(2015•株洲模拟)三种固体物质A、B、C溶解度曲线如图所示,试回答:(1)溶解度受温度变化影响最大的物质是A,影响不大的物质是B.(2)t1℃时三种物质溶解度由小到大的顺序A<B<C.(3)t2℃时,溶解度最大的物质是C,A、B两物质溶解度相等的温度是t2℃.(4)Q点表示t3℃时A的溶解度为mg,P点表示t3℃时B、C溶解度相等.29.(2015•垫江县校级模拟)在初中化学中,我们学习了溶液的有关知识.右图是KNO3的溶解度曲线.(1)从右图溶解度曲线可以得到的信息是(写一条)20℃时,KNO3的溶解度是31.6g.(2)小明参照右图在常温20℃时进行了如下实验:小明观察到A中所加固体全部溶解,则B中的现象是固体部分溶解.上述实验过程中属于不饱和溶液的是(填字母)A、C、D.D中溶液的溶质质量分数是37.5%.30.(2015•重庆模拟)如图是甲、乙两种固体物质的溶解度曲线.(1)t2℃时,甲物质的溶解度为30g;(2)从图中你还能获得哪些信息?t1℃时,甲和乙的溶解度相等;甲和乙的溶解度都是随着温度的升高而增大;温度低于t1℃时,乙的溶解度大于甲的溶解度,高于t1℃时,乙的溶解度小于甲的溶解度;(3)分析t1℃时,将10g乙物质放入100g水中,充分溶解后所得的溶液是不饱和(填“饱和”或“不饱和”)溶液.欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的方法升高温。
