有机化学-2010化工应化2A
湖北大学有机化学2010-2011下期末答案-修正

C:(CH3)3CCHO;D:CH3CH2CH2CH2CHO
5、不能与C6H5-N2+Cl-发生偶联的是(A)
A:苯B:苯酚C:N,N-二甲基苯胺D:1,3-苯二酚
6、比较下列化合物的酸性,最强的是(B)
A:硝基乙烷B:2-硝基丙烷C:硝基甲烷
得
分
五、机理题(每题5分,共10分)
1、完成下列反应,并写出合理的反应机理
2、对下列反应提出合理的机理。
得
分
六、合成题(每小题5分,共20分)
1、由苯甲醛和4个碳以下的简单原料合成下面化合物
2、由丙酮及三个碳原子以下化合物合成2, 2-二甲基戊酸
3、从乙酰乙酸乙酯及其它必要的试剂合成CH3COCH(CH3)CH2CH2OH
10、下列化合物中亲核加成反应活性最大的是(A)
A:NCCH2CHO B:CH3OCH2CHO
C:CH3SCH2CHO D:HSCH2CH2CHO
得
分
三、写出下列反应式的反应条件或者产物(需要立体结构的写出立体结构。每空2分,共30分)
得
分
四、简答题(共20分)
1、通过化学方法分离混合:PhNH2, PhNHCH3, PhN(CH3)2(6分)
课程考试试题纸
课程名称:
有机化学
考试方式:
闭卷
(开卷、闭卷)
印刷份数:
300份
学 院:
化学化工学院
任课教师:
娄兆文、柳利、王念贵
专业年级:
09级化学、化生、楚才、应化、化工
题
号
一
二
三
四
五
六
化工专业课程教学大纲

化学化工学院化学工程与工艺专业课程教学大纲化学化工学院化工系编制2010年目录1.《有机化学》课程教学大纲 (3)2.《有机化学实验》课程教学大纲 (18)3.《物理化学Ⅱ》课程教学大纲 (21)4.《物理化学Ⅱ实验》课程教学大纲 (38)5.《化工原理》课程教学大纲 (43)6.《化工原理实验》课程教学大纲 (56)7.《实验设计与数据处理》课程教学大纲 (59)8.《计算机在化工中的应用》课程教学大纲 (66)9.《生物化学》课程教学大纲 (69)10.《高等有机合成》课程教学大纲 (92)11.《胶体与界面化学》课程教学大纲 (96)12.《仪器分析Ⅱ》课程教学大纲 (101)13.《高分子化学》课程教学大纲 (110)14.《化学工艺学》课程教学大纲 (120)15.《化工热力学》课程教学大纲 (124)16.《化学反应工程》课程教学大纲 (138)17.《化工设计》课程教学大纲 (148)18.《化工制图》课程教学大纲 (152)19.《化工专业实验》课程教学大纲 (162)20.《化工仪表及自动化》课程教学大纲 (164)21.《化工设备设计基础》课程教学大纲 (175)22.《化工综合实验》课程教学大纲 (178)23.精细有机合成》课程教学大纲 (181)24.《精细化工工艺学》课程教学大纲 (193)25.《专业英语》课程教学大纲 (197)26.《文献检索与科技论文写作》课程教学大纲 (212)27.《分离工程》课程教学大纲 (219)28.《化工系统工程》课程教学大纲 (225)29.《化工安全工程》课程教学大纲 (229)30.《工业催化》课程教学大纲 (234)31.《表面活性剂》课程教学大纲 (241)32.《涂料与胶粘剂》课程教学大纲 (254)33.《食品与饲料添加剂》课程教学大纲 (269)34.《日用化学品》课程教学大纲 (277)35.《染料与颜料》课程教学大纲 (290)36.化工制药》课程教学大纲 (298)37.《精细化学品实验》课程教学大纲 (303)38.《市场营销导论》课程教学大纲 (307)39.《企业管理》课程教学大纲 (314)40.《化工技术经济》课程教学大纲 (321)41.《绿色化学基础》课程教学大纲 (334)42.《化工环境工程概论》课程教学大纲 (337)43.《化工产品设计》课程教学大纲 (345)44.《化学工程与工艺专业认识实习》教学大纲 (348)45.《化学工程与工艺专业金工实习》教学大纲 (350)46.《化学工程与工艺专业生产实习》教学大纲 (352)47.《化学工程与工艺专业毕业实习》教学大纲 (355)《有机化学》课程教学大纲一、课程基本信息课程代码:课程名称:有机化学英文名称:organic chemistry课程类别:专业基础课学时:72学分:4适用对象:化学与化工学院各专业考核方式:考试(平时成绩占总成绩的30%)先修课程:无机化学和分析化学二、课程简介中文简介:有机化学是研究有机化合物的来源、组成、结构、合成方法、性能、应用以及有关理论的一门化学基础课。
芳肼衍生物的合成与精制研究

化学杂交剂(Chemical hybridizing agent)是制备优良、高产杂交种子,提高粮食产量的重要方法之一。化学杂交剂育种的关键问题是要有去雄率高但又不影响雌性器官的优良化学杂交剂。哒嗪酮衍生物的合成及其在生物活性方面的研究和应用是近年的研究热点。在一些活性化合物的母体结构中引入其它活性基团,利用基团之间相互影响找到生物活性更佳的新型优良化学杂交剂是研究的一个重要方向。将具有广泛生物活性的噻二唑和吡唑酮基团引入到哒嗪酮环上,修饰该类化合物的结构,以期得到去雄活性好的先导化合物。
重氮化时所用的酸,从反应速度来说,以盐酸和氢溴酸最快,硫酸和硝酸较慢,但在置换反应中,仍以用硫酸为好。芳环上若有推电子基团,也会使反应加快。氨基的邻位若有取代基团,会产生位阻效应。
重氮盐多半易溶于水,只有少数杂酸盐和复盐不溶。这些不溶于水的重氮盐,往往比较稳定。它们中常见的有,氟硼酸盐、氟磷酸盐、1,5-萘二磺酸盐、氯化锌复盐、氯化汞复盐等。这些重氮盐在有机上合成都有广泛的应用。
常州大学
硕士学位论文
开题报告
课题名称芳肼衍生物的合成与精制研究
学 号__091012223___
姓 名___吴有才____
研究方向__有机合成___
二级学科__有机合成___
一级学科__有机化学___
学 院_石油化工学院
2010年11月16日
二 选题依据
1.课题的背景和研究依据
芳香杂环化合物的种类多,数量大,在自然界分布广泛,许多天然杂环化合物在动、植物体内起着重要的生理作用,例如,植物中的叶绿素,动物血液中的血红素,中草药中的有效成分生物碱及部分苷类,部分抗生素和维生素,组成蛋白质的某些氨基酸和核苷酸的碱基等都含有杂环的结构。因此,芳香杂环化合物在有机化合物尤其是有机药物中占有重要的地位。
有机合成化学实验讲义2010级

有机合成化学实验讲义2012-9-26实验一2,6-二氯-4-硝基苯胺的制备一、实验目的1.掌握2,6-二氯-4-硝基苯胺的制备方法2.掌握氯化反应的机理和氯化条件的选择3.了解2,6-二氯-4-硝基苯胺的性质和用途二、实验原理1.性质黄色针状结晶。
熔点192~194℃。
难溶于水,微溶于乙醇,溶于热乙醇和乙醚。
本品有毒。
温血动物急性口服LD50为1500~4000mg/kg,小白鼠急性口服LD50为3603mg/kg。
2.用途本品主要用于生产分散黄棕3GL、分散黄棕2RFL、分散棕3R、分散棕5R、分散橙GR、分散大红3GFL、分散红玉2GFL等。
还可以为农用杀菌剂使用,可防治甘薯、样麻、黄瓜、莴苣、棉花、烟草、草莓、马铃薯等的灰霉僵腐病;油菜、葱、桑、大豆、西红柿、莴苣、甘薯等的菌核病;甘薯、棉花、桃子的软腐病;马铃薯和西红柿的晚疫病;杏、扁桃及苹果的枯萎病;小麦的黑穗病;蚕豆花腐病。
3.原理根据引入卤素的不同,卤化反应可分为氯化、溴化、和氟化。
因为氯代衍生物的制备成本低,所以氯化反应在精细化工生产中应用广泛;碘化应用较少;由于氟的活泼性过高,通常以间接方法制得氟代衍生物。
卤化剂包括卤素(氯、溴、碘)、盐酸和氧化剂(空气中的氧、次氯酸钠、氯化钠等)、金属和非金属的氯化物(三氯化铁、五氯化磷等)。
硫酰二氯(SO2Cl2)是高活性氯化剂。
也可用光气、卤酰胺(RSO2NHCl)等作为卤化剂。
卤化反应有三种类型,即取代卤化、加成卤化、置换卤化。
由对硝基苯胺制备2,6-二氯-4-硝基苯胺由多种合成方法,包括直接氯气法、氯酸钠氯化法、硫酰二氯法、次氯酸法、过氧化氢法。
工业生产一般采用直接氯化法,其优点是原料消耗低、氯吸收率高、产品收率高、盐酸可回收循环使用。
直接氯气法的反应方程式如下:NH2NH2+Cl22HClCl ClNH2NO2+2HCl氯酸钠氯化法是由对硝基苯胺氯化、中和而得,反应方程式如下:NH2NO2NaClOHClNH2ClClNO2过氧化氢法是由对硝基苯胺在浓盐酸中与过氧化氢反应而得,反应方程式如下:NH2NO2+2H2O2+2HClNH2ClClNO2+4H2O三、实验内容方法一:氯酸钠氯化法。
2010届录取汇总表
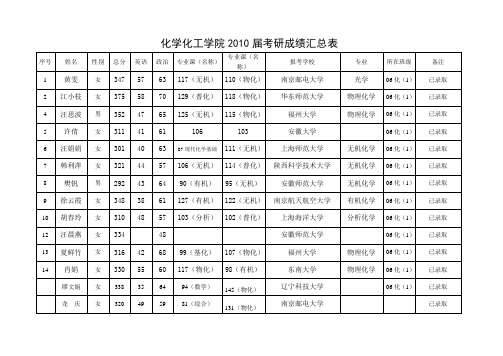
南京理工大学
应用化学
06材化
21
冯刚
男
354
64
61
90(综合)
139(物化)
北京理工大学
化学专业
06材化
已录取
22
龚洁
女
366
52
64
124(物化)
126(有机)
南京邮电大学
有机化学
06材化
已录取
23
吴世昌
男
285
30
64
57(数学)
134(材科)
四川大学
材料学
06材化
化学化工学院2010届考研成绩汇总表
53
71
微生物与生物化学
190药学综合
第四军医大学
药学
06材化
已录取
3
徐玉红
女
307
54
68
74(数学)
111(有机)
合肥工业大学
食品科学
06材化
已录取
4
桂清文
男
364
49
70
134(有机)
111(物化)
湖南大学
有机化学
06材化
已录取
5
刘皓
男
363
63
67
100(物化)
133(分析)
中科大
分析化学
06材化
华东理工大学
有机化学
06化(2)
已录取
4
江强
男
286
46
72
57(数学)
111(物化)
上海工程科技大学
能源化工
06化(2)
已录取
5
方丽
香豆素酯设计合成2-苯并呋喃甲酸

本科毕业论文香豆素酯设计合成2-苯并呋喃甲酸COUMARIN DESIGN AND SYNTHESIS OF COUMARILIC ACID学院(部):化学工程学院专业班级:应化06-2学生姓名:刘志彬指导教师:刘维新2010 年 6 月 8 日香豆素酯设计合成2-苯并呋喃甲酸摘要香豆素酯溶解于氯仿或其他有机溶剂后与液溴的氯仿溶液加成生成3,4-二溴-3,4-二氢香豆素中间体。
在一定温度下中间体经过水解、亲核取代、消去、酸化、水蒸气蒸馏、重结晶等一系列相关步骤最终获得产物2-苯并呋喃甲酸。
关键词:香豆素酯,氯仿,3,4-二溴-3,4-二氢香豆素,水解,酸化,水蒸气蒸馏,重结晶COUMARIN DESIGN AND SYNTHESIS OFCOUMARILIC ACIDABSTRACTCoumarilic acid preparation of first coumarin dissolved in chloroform or other organic solvents generate and the reaction of liquid bromine get 3,4 - dibromocoumarin,undera certain temperature through hydrolysis, acidification, distillation, recrystallization ultimately the product of Coumarilic acidKEYWORDS:Coumarin ,Chloroform, 3,4 - Dibromocoumarin, Hydrolysis, Acidification ,Distillation, Recrystallization目录摘要 (1)ABSTRACT (1)目录 (2)1绪论 (3)1.1有机合成发展前景 (3)1.2香豆素的研究现状 (3)1.3香豆素结构 (4)1.3.1简单香豆素类: (5)1.3.2呋喃香豆素类(furocoumarins) (线型和角型): (5)1.3.3吡喃香豆素类(pyranocoumarins) (线型和角型) (6)1.3.4其他香豆素类 (7)1.4香豆素物化性质 (7)1.4.1 香豆素的性状 (7)1.4.2 香豆素的溶解性 (7)1.4.3 香豆素的碱水解反应(内酯性质) (8)1.4.4 香豆素的酸的反应 (8)1.5 2-苯并呋喃甲酸的研究现状 (9)1.5.1 2-苯并呋喃甲酸的结构 (9)1.5.2 2-苯并呋喃甲酸的衍生物的合成及应用价值 (9)1.6课题的意义 (10)2 实验部分 (10)2.1实验试剂和实验设备 (10)2.1.1实验试剂 (10)2.1.2实验设备 (10)2.2香豆素酯制备2-苯并呋喃甲酸的反应设计过程 (11)2.3 实验的反应流程 (11)2.4 香豆素酯合成2-苯并呋喃甲酸的实验步骤 (14)2.4.1制备3,4-二溴-3,4-二氢香豆素 (14)2.4.2 由3,4-二溴-3,4-二氢香豆素制备2-苯并呋喃甲酸 (14)2.5产品的红外图谱表征 (15)3实验结果与讨论 (16)3.1实验讨论 (16)4. 结论 (17)参考文献 (18)谢辞 (20)1绪论1.1有机合成发展前景有机合成就是利用化学的方法,将有机物与单质、无机物合成出结构复杂的有机物的过程。
应用化学专业课程安排

化学与生命科学学院应用化学专业人才培养方案(Practical Chemistry)一、专业代码及专业名称专业代码: 070302 专业名称:应用化学二、学制招生对象: 高中毕业生学习年限: 4年三、培养目标培养具有扎实的化学化工基础知识、基本理论、精细化工相关专业知识和熟练实验方法技能的可从事化学化工相关工作的综合素质高、适应能力强、富有创新精神、德智体美全面发展,能在化工、轻工、食品、医药、化妆品和材料等等部门从事工程设计、应用研究、技术开发、分析检测和生产技术管理的的应用型高级技术人才。
四、专业特点及培养要求本专业本专业主要适应于石油化工、精细化工、高分子材料、日用化工等行业,为化工产业的科研、开发、质量控制、产品监测、进出口贸易、环保、商检等企业培养高级工程技术人才。
要求学生通过四年学习受到良好的基本实验技能和相关的工程技术能力训练,较系统地掌握相关专业知识,具有精细化工生产操作、产品开发、分析检测、工艺设计及技术管理能力。
五、知识结构和能力结构1. 知识结构。
本专业的核心知识是精细化工产品合成工艺及应用知识,具体的知识结构如下:化学基础知识:有机化学、无机化学、分析化学、物理化学等课程的理论基础知识和基本实验技能。
化工单元操作知识:各种单元操作的基本原理,工艺设计和操作调节。
化工设备知识:化工制图,典型化工设备工艺设计。
表面活性剂知识、助剂知识、计算机知识、管理知识、人文知识。
2. 能力结构。
本专业的核心能力是精细化工产品生产操作能力,具体能力结构如下:化工原材料分析化验、产品及产品质量检测能力;精细化工新产品研制、开发能力;典型精细化工设备的选型、简单设备的制造设计能力;精细化工产品生产操作能力;外语应用能力;计算机应用能力;生产组织管理能力;社会工作能力;自学与创新能力;与他人合作能力;同时具备精细化工行业必须的政策、法规意识。
六、主干学科化学七、主要课程无机化学、有机化学、分析化学、物理化学、化工原理、化工制图、精细有机合成化学及工艺学、精细化工工艺学、涂料化学及工艺学、化妆品生产工艺、精细化学品分析等。
2010学年必修2第三章第二节教学建议(汪爱华)

必修2 第三章有机化合物第二节《来自石油和煤的两种基本化工原料》教学建议广州市第五中学汪爱华一、教学目标1. 知识与技能:(1)掌握乙烯、苯的结构特点和主要性质。
(2)能从微观结构角度理解典型有机反应(取代反应、加成反应)的特点。
2. 过程与方法:(1)通过“科学探究”石蜡油的分解实验提供实验事实,让学生了解乙烯的工业来源,探究所产生的气体与烷烃性质的异同,使学生学会依据实验事实来推测结构的异同,发现问题,并解决问题的能力。
(2)通过学与问和实验3-1帮助学生学会结构预测性质的学习过程:提出假设→ 实验验证→ 根据实验结果修正假设→ 得出正确结论。
(3)通过展示乙烯结构模型、苯的分子模型,加深对它们的立体结构的认识;结合学与问,建立有机物“(组成)结构——性质——用途”的认识关系,使学生能从结构角度深化对有机物的认识,形成一定的分析和解决问题的能力。
(4)通过甲烷、乙烯、苯结构和性质的对比,加深对各类有机物性质的相似性和不同性的认识。
(5)通过建立宏观事实(实验及现象)——微观结构(如何断键与形成)——符号表征(结构式和化学方程式)三者的相互联系,帮助学生理解乙烯、苯的结构特点和反应中的断键位置。
3. 情感态度与价值观:(1)通过-思考与交流,认识乙烯、苯在化工生产中的广泛应用,了解石油与生产生活的关系,增进学生对有机化学的兴趣和情感,体会化学学习的价值。
(2)通过实践活动和科学视野,培养学生理论联系生活实际的学习态度。
(3)通过科学史话,让学生理解科学的发现需要牺牲精神和以事实为依据的严肃的科学态度。
二、教学重点、重点:烯的加成反应、苯的取代与加成反应。
从结构角度认识有机反应的特点。
难点:烯的结构与性质的关系、苯的结构与性质的关系。
三、课时建议本节建议安排2课时第一课时:乙烯第二课时:苯1011四、教学过程 第一课时 乙烯【展示】(1)石油化工业相关资料(录像形式)(2)乙烯和苯用途的大量图片。
特戊酰氯 国标

特戊酰氯国标特丙酰氯是一种重要的化工产品,它是具有高度反应性的有机化合物,通常用于有机合成和分析化学中。
特丙酰氯在化学商业领域中也被称为特伦酐,其化学式为C4H7ClO,分子量为106.55g/mol。
在化工生产中,特丙酰氯通常作为有机化合物的重要反应试剂,可用于苯甲酸、药物、染料和农药等化合物的生产中。
在本文中,将介绍特丙酰氯的国家标准,并探讨其在工业和实验化学中的应用。
国家标准特丙酰氯的国家标准是GB/T 25110-2010。
该标准的正式名称为“特丙酰氯”,该标准于2010年发布,取代了原先的GB/T 25110-1995标准,旨在规范特丙酰氯的生产、储存、运输、使用和安全。
该标准中涉及的内容包括物理化学性质、包装、标签、储存和运输要求、安全与危险等级、毒性、应急措施等方面。
特丙酰氯的属性特丙酰氯是一种无色到淡黄色液体,易挥发,有刺激性气味。
它在水中分解,可以与水反应,生成丙酮和盐酸。
特丙酰氯具有较高的蒸汽压和易燃性,可以在大气中形成有毒气体和蒸汽。
特丙酰氯的沸点为102°C,密度为1.119g/cm³,闪点为21°C。
特丙酰氯在室温下易于发生水解反应,并与许多官能团进行取代反应,包括醇、胺、硫醇、酸等。
应用领域特丙酰氯是一种重要的化学试剂,广泛应用于染料、医药、香料、农药等有机合成化学领域。
特丙酰氯常用于脱水反应和取代反应,用于制造苯丙香豆素、乙醇胺等有机物。
在制造染料和化妆品领域中,特丙酰氯用作乙酸酐和苯酰氯的替代品,与其他有机物反应可以制造糖类和脂肪酸合成的中间体。
特丙酰氯也可用于像环磷酰胺、格列齐特等许多药物的合成中。
由于特丙酰氯的极性较小、稳定性较强,因此为药物合成过程中一个重要的中间体。
在实验室中,特丙酰氯通常用于涉及脱水反应、取代反应和酰化反应的试验中。
例如,特丙酰氯可以用于脱水制备酰胺、肽和酰基化合物,以及用于对应酰化反应实验。
特丙酰氯还可以用于制备有机磷化合物,如反丁基特异性重排反应中的磷酸三甲基氯化物。
《有机化学(1)-1,2》(化学、应化类专业)教学大纲

《有机化学(I)》(化学、应化类专业)教学大纲一、课程基本信息课程名称(中、英文): 有机化学(Ⅰ)-1[Organic Chemistry(Ⅰ)-1]有机化学(Ⅰ)-2[Organic Chemistry(Ⅰ)-2]课程号(代码): 20308730,20308630课程类别: 类级平台课程,必修课学时:48x2学分:3x2先修课程:《无机化学》、《分析化学》基本面向:化学专业、应用化学专业二、教学目的及要求化学,应用化学和材料化学专业的学生,在学完《高等数学》、《普通物理》、《无机化学》、《分析化学》等前置课程的基本理论知识后,进入有机化学的学习。
该课程要求学生系统地、扎实地掌握有机化学的基本原理和基本规律,为后续课程的学习、继续深造以及将来解决有机化学中的问题、奠定必要而坚实的基础,同时能进一步加强解决问题和分析问题能力的培养。
在学习该课程时学生要着重掌握各类有机化合物的结构、命名、物理性质、光谱性质、常用制备方法和用途,尤其是着重掌握各类有机化合物的结构特征和关键反应,把握规律、抓住机理、将官能团互相转变的方法和碳碳键的形成与断裂的方法形成互联网络,同时专注有机化学中的立体化学问题,才能达到有机化学的教学之目的。
三、教学内容1 绪论(4学时)基本要求:一、了解有机化学的发展史、主要任务和学习方法;二、了解有机化合物的基本特点、分类和反应类型;三、了解共价健的本质,掌握共价健的属性,熟悉利用键能数据推算反应的焓变;四、掌握下述名词术语:有机化学;同分异构现象;分子间作用力;Van der walls力;官能团1-1 有机化学的由来和发展1-2 有机化合物的特点:分子结构和组成(同分异构现象,结构的表示方法);理化性质1-3 共价键的键参数:键能、键长、键角;键的极性与诱导效应;键的可极化性1-4 共价键的断裂方式与有机反应的类型1-5 有机化合物的分类1-6 学习有机化学的目的和学习方法2 烷烃(4学时)基本要求:一、掌握构象的表示方法和典型的构象ap, sp, sc, ac的稳定性分析;二、了解饱和碳原子的sp3杂化轨道与烷基自由基的sp2杂化轨道的形成与构型;三、着重掌握烷烃的自由基取代反应(卤代反应)的基本规律(区域选择性)和反应机理(自由基反应),了解烷烃的物理性质。
2010年高考考试大纲(新课标)化学

2010年全国新课标高考考试大纲:化学Ⅰ.考试性质普通高等学校招生全国统一考试是合格的高中毕业生和具有同等学力的考生参加的选拔性考试。
高等学校根据考生成绩,按已确定的招生计划,德、智、体全面衡量,择优录取。
因此,高考应具有较高的信度、效度,必要的区分度和适当的难度。
Ⅱ.考试内容根据普通高等学校对新生文化素质的要求,依据中华人民共和国教育部2003年颁布的《普通高中课程方案(实验)》和《普通高中化学课程标准(实验)》,确定高考理工类招生化学科考核目标与要求。
一、考核目标与要求化学科考试,为了有利于选拔具有学习潜能和创新精神的考生,以能力测试为主导,将在测试考生进一步学习所必需的知识、技能和方法的基础上,全面检测考生的化学科学素养。
化学科命题注重测量自主学习的能力,重视理论联系实际,关注与化学有关的科学技术、社会经济和生态环境的协调发展,以促进学生在知识和技能、过程和方法、情感、态度和价值观等方面的全面发展。
(一)对化学学习能力的要求1.接受、吸收、整合化学信息的能力(1)能够对中学化学基础知识融会贯通,有正确复述、再现、辨认的能力。
(2)能够通过对实际事物、实验现象、实物、模型、图形、图表的观察,以及对自然界、社会、生产、生活中的化学现象的观察,获取有关的感性知识和印象,并进行初步加工、吸收、有序存储的能力。
(3)能够从试题提供的新信息中,准确地提取实质性内容,并经与已有知识块整合,重组为新知识块的能力。
2.分析问题和解决(解答)化学问题的能力(1)能够将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题的能力。
(2)能够将分析解决问题的过程和成果,用正确的化学术语及文字、图表、模型、图形等表达,并做出解释的能力。
3.化学实验与探究能力(1)了解并初步实践化学实验研究的一般过程,掌握化学实验的基本方法和技能。
(2)在解决简单化学问题的过程中,运用科学的方法,初步了解化学变化规律,并对化学现象提出科学合理的解释。
2010年高考化学真题(Word版)——全国2卷(试题+答案解析)

2010年普通高等学校招生全国统一考试(全国2卷)化学试题可能用到的相对原子质量:H 1 C 12N 14O 16Na 23Mg 24S 32Cu 64一、选择题6.下列反应中,可用离子方程式H++OH-===H2O表示的是 ( )A.NH4Cl+NaOH NaCl+NH3↑+H2OB.Mg(OH)2+2HCl===MgCl2+2H2OC.NaOH+NaHCO3===Na2CO3+H2OD.NaOH+HNO3===NaNO3+H2O7.下面均是正丁烷与氧气反应的热化学方程式(25 ℃,101 kPa):①C4H10(g)+O2(g)===4CO2(g)+5H2O(l) ΔH=-2 878 kJ·mol-1②C4H10(g)+O2(g)===4CO2(g)+5H2O(g) ΔH=-2 658 kJ·mol-1③C4H10(g)+O2(g)===4CO(g)+5H2O(l) ΔH=-1 746 kJ·mol-1④C4H10(g)+O2(g)===4CO(g)+5H2O(g) ΔH=-1 526 kJ·mol-1由此判断,正丁烷的燃烧热是( )A.-2 878 kJ·mol-1 B.-2 658 kJ·mol-1C.-1 746 kJ·mol-1 D.-1 526 kJ·mol-18.在相同条件下,下列说法错误的是( )A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度B.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度C.醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度D.工业上生产硫酸的过程中使用过量的空气可提高SO2的利用率9.相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )10.若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应中化合价发生变化和未发生变化的N原子数之比为( )A.1∶4 B.1∶2C.2∶1 D.4∶111.在一定的温度、压强下,向100 mL CH4和Ar的混合气体中通入400 mL O2,点燃使其完全反应,最后在相同条件下得到干燥气体460 mL,则反应前混合气体中CH4和Ar的物质的量之比为( )A.1∶4 B.1∶3C.1∶2 D.1∶112.短周期元素W、X、Y、Z的原子序数依次增大,且W、X、Y+、Z的最外层电子数与其电子层数的比值依次为2、3、4、2(不考虑零族元素)。
10版应化有机化学H2实验大纲

《有机化学H2》实验教学大纲大纲制定(修订)时间: 2010 年 6月课程名称: 有机化学H2 课程编码: 080331004课程类别: 专业基础课课程性质: 必修适用专业: 应用化学课程总学时: 56实验(上机)计划学时: 12开课单位: 环境与化学工程学院一、大纲编写依据应用化学专业2010版教学计划。
二、实验课程地位及相关课程的联系机化学是一门以实验为基础, 理论性和实践性并重的课程。
有机化学的发展同有机化合物的合成、分离提纯、鉴定等实验研究紧密相连。
有机化学实验与有机化学理论教学是相互配合的, 它是有机化学教学的重要组成部分。
本课程是以实践环节为主, 理论教学为辅的技能应用型课程。
. 通过该课程的学习, 使学生巩固和加深所学理论知识, 通过实践进一步加强学生独立分析问题和解决问题的能力、综合设计及创新能力的培养, 同时注意培养学生实事求是、严肃认真的科学作风和良好的实验习惯, 为后续课程的学习及今后工作打下良好的基础。
1.本课程以《有机化学》为先修课。
2.相关课程有结构化学, 高分子化学, 有机波谱分析等。
三、本课程实验目的和任务1. 深入理解有机化学基本理论与概念;2. 掌握有机化合物一些基本操作技能与若干单元操作的实验技能;3. 学习预防与处置化学实验事故的方法, 以及正确使用与处置教学中所涉及的一些化学危险品;4.培养实验者的化学实验的工作能力, 养成良好的实验作风与习惯;5.学习有机化学的科学研究的工作方法, 培养严谨的科学精神。
四、实验基本要求1.玻璃仪器的选用和干燥;常用装置的装配和拆卸;2.常用磨口仪器的使用和维护;3.冷凝、蒸馏;4.分液漏斗的使用;5.减压过滤方法;6.固体物质的干燥;六、教材(讲义、指导书):《有机化学实验》高占先主编,北京高等教育出版社,2004《有机化学实验》周科衍吕俊民著高等教育出版社1990七、考核方法和评分标准1.按照实验指导书的具体要求, 根据每个学生实验前的预习准备, 实验过程的考查, 实验操作情况及实验报告的质量, 综合给出实验成绩。
2009-2010(二)有机化学(A)试卷答案
(勤奋、求是、创新、奉献)2009~ 2010学年第 2 学期考试试卷主考教师:学院 化学化工学院 班级 __________ 姓名 __________ 学号 ___________《有机化学(二)》课程试卷A(本卷考试时间 120 分钟)一、 用系统命名法命名下列化合物或根据名称写出结构式。
(本题共10小题,每小题1分,共10分)1.2.5-甲基-2异丙基苯酚 5-甲基2-乙基庚醛3.4.4-溴-2-戊酮3-乙基-3-戊醇5.(CH 3CH 2)3CCOOH 6.O CHH 2C CH 2HCH 2C2,2-二乙基丁酸 烯丙基乙烯基醚7. 3, 7-二甲基-2, 6-辛二烯醛 8. 4-硝基苯甲酰胺C O C H 2H 3C C H C H 3B rCH 3C C H 3C HH 2C C H 2CC H C H 3C H OC O N H 2N O 29.N -甲基-N -乙基对氯苯胺 10.2-呋喃甲酸NC lC H 32H 5C O O H二、 简略回答下列问题。
(本题共8小题,每小题3分,共24分)1将下列酯按碱性水解速率大小排列成序:(A)(B)(C) (D)(B) > (A) > (C) > (D)2.下列化合物中,可进行Cannizzaro 反应的有: A. 乙醛 B. 苯甲醛 C. 丙醛 D. 呋喃甲醛B D3.将下列化合物按亲核加成活性大小排列成序:C F 3CH OC H 3C H OC lC H 2C HO(1)(2)(3)(4) C H 3CO CH 31>3>2>44.解释下列反应的机理:CC H 3C H 3CC H 3O H O HC H 3C C H 3C H 3COC H 3C H 3C O O C H 3O2NCH 3CH 2CH 2COOC 2H 5发生分子间Claisen 酯缩合反应HC C 2H 5C COOC2H 5H 3CH 2CH 2C OC 2H 5OOCCOOC2H 5发生分子内Claisen 酯缩合反应COOC 2H 5O6.下列化合物按碱性由强到弱排序。
有机化学-化教、应化《合成化学实验》教学大纲

《合成化学实验》Experiment of Synthetic Chemistry课程编号:13111131 学时:90 学分:3先修课程:无机化学、有机化学、基础化学实验适用专业:化学(师范)、应用化学一、目的与任务:《合成化学实验》课程,是化学专业学生的一门重要的技能运用型课程,它对化学实验基本技能的应用起到一个承上启下的作用。
在有了初步的化学实验技能和基本的化学知识的基础上,培养学生在正确掌握化学实验的基本操作方法和技能技巧基础上,使学生进一步掌握常见无机、有机化合物制备、分离及纯度鉴定的基本方法,培养学生良好的实验习惯和严谨、细致、实事求是的科学态度和工作作风,训练科学的思维方法,培养学生独立操作、独立思考的能力,使其逐步具备化学工作者所应有的素质。
二、实验教学的基本要求:(1)预习实验的原理、方法,找出实验中的难点和问题,认真写好预习报告。
(2)预习实验中相关的基本操作技能的原理及注意事项。
(3)设计性实验中,要求独立设计实验方案,列出实验中所需的试剂物品及操作方法;(4)规范正确地完成各项实验操作,正确观察、如实记录实验现象,认真处理实验结果;(5)对实验过程、结果进行认真的分析讨论。
三、本课程开设的实验项目:注:1、类型---指设计性、综合性、验证性;2、要求---指必修、选修;3、该表格不够可拓展。
四、实验成绩的考核与评定办法:作为一门独立的课程,为了减少主观因素,实验成绩的考核,以实验预习报告、实验报告和实验过程为考核依据,并按学院《课程成绩核定方法》进行。
五、大纲说明:《合成化学实验》共90课时,涵盖无机合成、有机合成等内容。
无机合成和有机合成分别为45课时、45课时,分2~3学期完成;具体内容可结合实验室实际情况有针对性地安排。
撰写人:朱卫华审定人:曹永林批准人:倪良时间:2003年8月28日。
有机化学中碳链增长的反应

(2)三级醇按碳正离子反应机锂进行酯化,醇在酸性条件下与氢离子结合形成详盐,然后脱去一分子水,羧酸作为亲核试剂进攻碳正离子,再脱去一个氢离子得到酯,此时的酸作为催化剂。
例如:(CH3)3C-OH + R-COOH→ (CH3)3COOC-R + H2O
其反应机理如下:
一般情况下R3C+易与碱性较强的水结合,不易与羧酸结合, 故逆向反应比正向反应易进行。所以三级醇的酯化反应产率很低。
SN2反应: (CH3)3CO-Na + CH3I → (CH3)3COCH3+ NaI
E2消除反应:(CH3)3CBr + CH3ONa → (CH3)2C=CH2+ CH3OH + NaBr
除用卤代烷以外,磺酸酯、硫酸酯也可用于合成醚:
芳香醚可用苯酚与卤代烷或硫酸酯在氢氧化钠的水溶液中制备:
苯甲醚(茴香醚)
例如 :
四、炔烃的亲核加成反应
由于炔烃与烯烃相比,采用的杂化不同,炔烃为SP杂化,其中S轨道占有的成分高,对电子的吸引能力强,所以炔烃可一发生亲核加成而烯烃不能,利用这个性质,可以用来延长碳链,这里以乙炔为例。(Nu为带有碳链的亲核基团)
利用炔烃可以进行亲核加成的特性可以让炔与羧酸反应制备无法用烯醇直接酯化制得的酸烯酯。还可是让炔与氢氰酸生成烯腈,烯腈再水解就可以得到α,β不饱和酸,以此衍生制备各种α,β不饱和不饱和化合物。
4.与碱金属反应
卤代烷可与金属钠反应,生成的有机钠化合物立即再与卤代烷反应生成烷烃。该反应称为“武尔兹反应”。
2RX + 2Na R-R + 2NaX
例如:2CH3CH2CH2Br + 2NaCH3CH2CH2CH2CH2CH3+ NaBr
高中化学示范课

4. (2010·福 州 高 一 质 检 ) 由 乙 烯 (CH2CH2) 推 测 丙 烯 (CH3CHCH2)的结构或性质,正确的是( )
A. 不能使 KMnO4 酸性溶液褪色 B. 不能在空气中燃烧 C. 能使溴水褪色 D. 与 HCl 在一定条件下加成只得到一种产物
答案:C
解析:由于乙烯和丙烯组成相似,都能在空气中燃烧,
故 B 错误。由于丙烯中也含有碳碳双键,故能与溴单质发生 加成反应而使溴水褪色,也可以使 KMnO4 酸性溶液褪色, A 错误,C 正确。由于 CH3CHCH2 与 HCl 在一定条件下加 成,氯原子连接的位置有两种情况,加成产物也应有两种可
能,D 不正确。
5. (2009·江西九校联考)下列关于乙烯和乙烷相比较的说 法中,不正确的是( )
C.5 mol
D.6 mol
[解析] 认真分析乙烯与氯气的加成反应和甲烷与氯气 发生取代反应的结构变化,不难发现加成反应所消耗氯气与 双键数之比为 1∶1,而取代反应所消耗的氯气与分子中的氢 原子个数之比为 1∶1。1 mol 乙烯中含有碳碳双键 1 mol, 氢原子 4 mol,所以这两个过程中消耗氯气的总物质的量为 5 mol。
5. 乙烯的用途 (1)重要化工原料,用来制聚乙烯塑料、聚乙烯纤维、乙 醇等。
(2)在农业生产中用作_植__物__生__长__调__节__剂______________。 (3)__乙__烯____的产量可以用来衡量一个国家的石油化工 发展水平。
乙烯的氧化反应和加成反应
1.氧化反应 (1)在空气中燃烧 ①空气中若含 3.4%~34%(体积分数)的乙烯,遇明火极 易发生爆炸,所以点燃乙烯前应先检验纯度。
三、乙烯
1. 乙烯的主要来源 乙烯是从__石__油____中获得的,_乙__烯__的__产__量___可用来衡量 一个国家的石油化工发展水平。
应用型化工专业有机化学教学案例

应用型化工专业有机化学教学案例
应用型化工专业是以化学、生物学及工程学等为基础,重点培养学生解决工程化学问题和发展新技术的能力。
有机化学是应用型化工专业的重要基础课程之一,通过有机化学的学习,学生能够了解和掌握有机化合物的结构、性质以及反应机理等知识,为日后从事石油化工、医药化工、材料化工等方面的工作打下扎实的基础。
一、实验目的
通过本次实验,使学生掌握有机化合物的合成方法和反应机理,培养学生的实验技能和科学研究精神。
二、实验原理
实验中,我们以苯甲醇为起始原料,经过一系列反应,合成正非龙脑酮。
三、实验步骤
1. 精密称取苯甲醇5g,加入烧瓶中,并添加适量的乙酸和氯化亚锡作为催化剂。
2. 烧瓶连同卧管在冰盐混合物中加热5分钟,然后将烧瓶浸入水中冷却。
3. 在冷却的烧瓶中,加入15mL浓盐酸溶液,摇晃均匀。
4. 将烧瓶连同水浴在温水中加热15分钟,然后冷却。
5. 在冷却的烧瓶中,加入10%的氢氧化钠溶液,摇晃均匀。
6. 将产物用氯仿提取,洗涤,干燥后,蒸发溶剂得到纯品。
四、实验结果
产物正非龙脑酮为白色结晶,能溶于醇和酮,具有较强的香味。
五、实验分析
正非龙脑酮是一种具有较强香味的有机化合物,广泛应用于化妆品、香精等产业中。
实验中的反应过程是通过苯甲醇的缩聚反应得到正非龙脑酮。
通过本实验,不仅能够学习到有机化合物的合成方法和反应机理,还能够培养学生的实验技能和科学研究精神。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
海南大学2011-2012学年度第2学期试卷
科目:《有机化学II 》 试题( A 卷)
姓名: 学 号: 学院: 材料与化工学院 专业班级:
成绩登记表(由阅卷教师用红色笔填写)
阅卷教师: 2012 年 7 月 日
考试说明:本课程为闭卷考试,可携带 。
一、命名下列化合物 (每小题1分,共10分)
NH O
O CH 3
COC l
CH 3CH 2COO CH 2CH 3
O O
O COO H
CHO
NHCH 2
H 2N (CH 3CH 2CH 2CH 2)4N Br
+-O
O 2N
CH 2S H
NO 2
1
23
4
5
6
7
8
9
10
二、选择题(每小题1分,共15分):(说明:将正确的答案填在下面的表格里)
1. 下列化合物酸性最强的是
A ClCH 2COOH
B Cl 2CHCOOH
C Cl 3CCOOH
D HOCH 2COOH
2. 下列化合物水解速度最快的是:
A CH 3COOC 2H 5
B CH 3CONH 2
C CH 3COCl
D CH 3CH 2CH 2Br
3. 下列哪个二元酸受热不会放出CO 2:
A 己二酸
B 丁二酸
C 丙二酸
D 乙二酸
4. 下列 β-二酮化合物在相同条件下烯醇式含量最高的是:
CH 2C C O
O OC 2H 5
C 2H 5O CH 2C C O O CH 3H 3C A B CH 2C C O O OC 2H 5H 3C CH 2C C O
O CH 3
C 6H 5C D
5. 下列化合物酸性最强的是:
OH
OH
OH
OH
NO 2
2NO 2
O 2N
A B C D
6. IR 光谱中,乙腈的C ≡N 三键在( )区域呈现中等强度的吸收峰:
A 3000-3100 cm -1
B 2200-2300 cm -1
C 1700-1800 cm -1
D 1000-1100 cm -1
7. 下列杂环化合物中,杂原子只提供一个p 电子参与共轭大π键形成的是:
N N
A B C D
S H
O
8. 下列糖类化合物中,不具有还原性的糖是:
A 蔗糖
B 麦芽糖
C 葡萄糖
D 果糖
9. 下列芳香胺的碱性最强的是:
NH 2
NH 2
CH 3O
NH 2
NO 2
NH 2
O 2N
A B
C D
10. 下列化合物水解速度最快的是:
O 2N COOCH 3COOCH 3
H 3CO
COOCH 3
COOCH 3
Cl
A B C D
11. 下列方法中可用来鉴别伯、仲、叔胺的有:
A Hinsberg 反应
B Hoffman 降解
C Williamson 反应
D Wittig 反应
12. 下列哪种方法通常用来制备纯度较高的伯胺:
A 醇的胺解
B Gabriel 合成法
C 卤代烃的胺解
D 还原胺化
13. 下列化合物最容易发生磺化反应的是:
A
B
C
D
O
N
N
NO 2
14. 二萜含有( )个异戊二烯结构单元:
A 1
B 2
C 3
D 4
15. 直链淀粉是葡萄糖单元是通过( )键连接而成的高分子化合物
A α-1,4-糖苷键
B α-1,6-糖苷键
C β-1,4-糖苷键
D β-1,6-糖苷键
三、完成下列反应(每空2分,共30分)( 说明:
写出你认为的主要产物)
CH 3
KMnO4
PCl 3H 2,Pd-BaSO 4
喹啉-硫
N 过量CH 3I Ag 2O
①②过量CH 3I Ag 2O
①②HOOC
COOH
4
Ag 2O
②1
2
3
CH 2Br N 2H NH 2
S OH , H 2O
①_
+
OH ①_
4
O
+
COOCH 3
3
N H
+(CH 3CO)2O
150-200℃
5
CH 3COONO 2
6
四、完成下列转变(共4小题,每小题3分,共12分)( 说明:必要的无机试剂任选,写出详细的各步反应过程)
CH 3CH 2CH 2COOH
CH
2CH 3
COOH HOOC
O
COOC 2H 5C 2H 5
Cl
OCOCH 3
NO 2
NO 2
O
CHO
O
CH
C 3
CH 2OH 1
23
4
五、用乙酰乙酸乙酯合成法合成下列化合物(共2小题,每小题4分,共8
分)( 说明:写出详细的各步反应过程)
六、判断题(每小题1分,共9分)( 说明:判断下列化
合物是否有芳香性,有的打√,没有的×)
S
S
N N N O
H 3C
3
N N
O O 1
2
3
4
5
6
7
8
9
N N
CH 3
H 3C
3N
CH 2CHCOCH 3CH 2CH 3
CH 3CH 2CH 2CHCOOH
2Ph
1
2
七、结构推断题(共16分)( 说明:必要的无机试剂和有机
试剂任选,写出详细的各步反应过程)
1. 某芳香族化合物(A)的分子式为C9H11NO2,(A)用稀酸水解得(B)和一分子乙酸,(B)进行重氮化反应,并在过量稀盐酸下加热至100℃得(C), (C)用氢碘酸处理得碘甲烷和(D)。
(D)的分子式为C6H6O2 D氧化得1,4-苯醌。
试推测(A)、(B)、(C)、(D)的构造式,并写出各步反应式(8分)。
2. 某二元酸C8H14O4,(A),受热时转变成中性化合物C7H12O(B),(B)用浓HNO3氧化生成二元酸C7H12O4 (C), (C)受热脱水成酸酐C7H10O3(D); (A)用LiAlH4还原,然
后脱水生成3,4-二甲基-1,5-己二烯。
试推导(A)-(D)的构造并写出各步反应式(8分)。
