2014版初中化学全程复习方略配套课件:实验2实验室制取氧气(人教版)
合集下载
初中化学人教版《制取氧气》ppt精美

初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
谈谈你这节课的收获
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件) 初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
2、在实验室中为什么可分离高锰酸钾、过氧化 氢、氯酸钾制氧气?
高锰酸钾、过氧化氢、氯酸钾中都含有氧元素, 而氧气是由氧元素组成的
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
发生装置
反应物的状 态
反加热
反应物的状态、反应的条件
适用于固体与固体加热制气
适用于固体与液 体不加热制气
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
收集装置
气体
物理性质 化学性质 收集方法
气氧体气的气溶体的解不收密性易集度、空装溶略密置气于大度的水于、选,择能与否不气哪发与与中些生空水的因反气、成素应、有空 分水关?发排 上生水 排反法 空应或 气向 法
小结:
确定发生装置与收集装置需要考虑的因素 发生装置:反应物的状态--固体与固体反应
固体与液体反应 液体与液体反应 反应条件---是否需要加热、加催化剂等 收集装置:排空气法----密度比空气大可用向上排 空气法 密度比空气小可用向下排 空气法 排水法(不易溶于水,不与水反应)
初中化学人教版《制取氧气》ppt精美 (PPT 优秀课 件)
氢气
难溶于水, 密度比空气
小
不与水、空 气中的成分 发生反应
初中化学人教版《制取氧气》_课件-完美版

对于某些指定的化学反应,没有催化剂并不意味着 该反应不能进行,只是速率不一样而已。
③催化剂并不具有通用性,如二氧化锰在过氧化氢
分解制取氧气时,能够起催化作用,是催化剂,但 对于其他反应就不一定了。 ④同一化学反应可有多种催化剂。如双氧水分解制取 氧气时,既可用二氧化锰做催化剂,也可用硫酸铜 溶液做催化剂。
步骤二:向上述试管中,加入少量二氧化锰, 把带火星的木条伸入试管。观察发生的现象。
现象:带火星的木条复燃了
分析:常温下二氧化锰(MnO2)加快了过氧 化氢溶液的分解,放出的氧气使带火星的木条 复燃。
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
步骤三:反应停止后,重新加入过氧化氢溶液, 把带火星的木条伸入试管。观察发生的现象。 现象:带火星的木条复燃了 分析:二氧化锰(MnO2)仍然能加快过氧化氢 溶液分解产生氧气的速率。 催化剂:在化学反应里能改变其他物质的化学 反应速率,而本身质量和化学性质在化学反应 前后都没有发生变化的物质。催化剂的特点
原因:利于气体的排出
4、试管口略向下倾斜
原因:防止冷凝水倒流至试管 底部,炸裂试管
5、用酒精灯的外焰先均匀预热,再 集中在有药品的部位集中加热,
6、等有连续的气泡产生时再收集
原因:刚加热时产生的气泡中混 有空气,这时的气体不纯
7、实验完毕,先撤导管,后移酒精灯
原因:防止试管冷却后,水槽内 的水沿导管上升,进入试管,使试 管炸裂
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载 【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
③催化剂并不具有通用性,如二氧化锰在过氧化氢
分解制取氧气时,能够起催化作用,是催化剂,但 对于其他反应就不一定了。 ④同一化学反应可有多种催化剂。如双氧水分解制取 氧气时,既可用二氧化锰做催化剂,也可用硫酸铜 溶液做催化剂。
步骤二:向上述试管中,加入少量二氧化锰, 把带火星的木条伸入试管。观察发生的现象。
现象:带火星的木条复燃了
分析:常温下二氧化锰(MnO2)加快了过氧 化氢溶液的分解,放出的氧气使带火星的木条 复燃。
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
步骤三:反应停止后,重新加入过氧化氢溶液, 把带火星的木条伸入试管。观察发生的现象。 现象:带火星的木条复燃了 分析:二氧化锰(MnO2)仍然能加快过氧化氢 溶液分解产生氧气的速率。 催化剂:在化学反应里能改变其他物质的化学 反应速率,而本身质量和化学性质在化学反应 前后都没有发生变化的物质。催化剂的特点
原因:利于气体的排出
4、试管口略向下倾斜
原因:防止冷凝水倒流至试管 底部,炸裂试管
5、用酒精灯的外焰先均匀预热,再 集中在有药品的部位集中加热,
6、等有连续的气泡产生时再收集
原因:刚加热时产生的气泡中混 有空气,这时的气体不纯
7、实验完毕,先撤导管,后移酒精灯
原因:防止试管冷却后,水槽内 的水沿导管上升,进入试管,使试 管炸裂
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载 【获奖课件ppt】初中化学人教版《制 取氧气 》_课 件-完美 版1-课 件分析 下载
人教版教材《制取氧气》上课课件PPT1

新课导入
呼吸机——新冠疫情下的救命稻草
氧气是怎么制得的呢?
氧气袋
氧气能支持呼吸可用于医疗急救
氧气瓶
此次的新冠肺炎是一种急性感染肺 炎,导致患者的肺功能受到明显损害, 使用呼吸机对进行追加氧气提供,能够 让病人得肺功能获得最好恢复。
病床供 氧装置
高压氧舱
课题3 制取氧气
学习内容
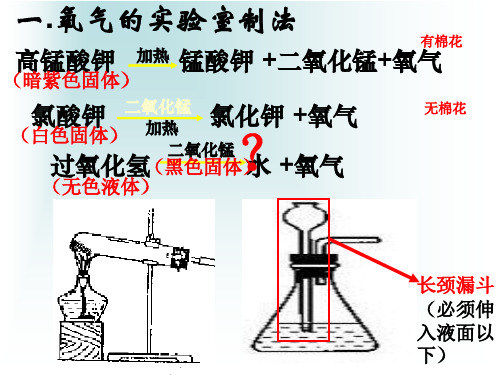
一、实验室制取氧气
1、实验室制取氧气的三种方法 2、催化剂、催化作用 3、分解反应
过氧化氢 二氧化锰 水 + 氧气
H2O2 MnO2 H2O + O2
2、实验探究:
过氧化氢
有极 少气 泡产 生,
二氧化锰 过氧化氢
有大 量气 泡产 生
带火 星木 条没 有复 燃
过氧化氢溶液在常温 下分解很慢,产生氧气的 量极少不足以使带火星的 木条复燃
带火 星木 条复 燃
加入二氧化锰后快速 生成大量氧气,使带火星 的木条复燃
区别 相同
化合反应
分解反应
反应物 生成物 反应特征 形式
两种或两种以上
一种
一种
两种或两种以上
多变一
一变多
A + B + … → C C →A + B + …
(都属于化学反应基本类型之一)
注意:氧化反应:物质与氧气发生的反应属于氧化反应。 不属于化学反应基本类型
现有以下化学反应:
二氧化锰
1、过氧化氢
水 + 氧气
2、氯酸钾 MnO2 氯化钾 + 氧气
3、高锰酸钾 加热 锰酸钾 + 二氧化锰 + 氧气
4、铁 + 氧气 点燃 四氧化三铁 5、甲烷 + 氧气 点燃 二氧化碳+水
呼吸机——新冠疫情下的救命稻草
氧气是怎么制得的呢?
氧气袋
氧气能支持呼吸可用于医疗急救
氧气瓶
此次的新冠肺炎是一种急性感染肺 炎,导致患者的肺功能受到明显损害, 使用呼吸机对进行追加氧气提供,能够 让病人得肺功能获得最好恢复。
病床供 氧装置
高压氧舱
课题3 制取氧气
学习内容
一、实验室制取氧气
1、实验室制取氧气的三种方法 2、催化剂、催化作用 3、分解反应
过氧化氢 二氧化锰 水 + 氧气
H2O2 MnO2 H2O + O2
2、实验探究:
过氧化氢
有极 少气 泡产 生,
二氧化锰 过氧化氢
有大 量气 泡产 生
带火 星木 条没 有复 燃
过氧化氢溶液在常温 下分解很慢,产生氧气的 量极少不足以使带火星的 木条复燃
带火 星木 条复 燃
加入二氧化锰后快速 生成大量氧气,使带火星 的木条复燃
区别 相同
化合反应
分解反应
反应物 生成物 反应特征 形式
两种或两种以上
一种
一种
两种或两种以上
多变一
一变多
A + B + … → C C →A + B + …
(都属于化学反应基本类型之一)
注意:氧化反应:物质与氧气发生的反应属于氧化反应。 不属于化学反应基本类型
现有以下化学反应:
二氧化锰
1、过氧化氢
水 + 氧气
2、氯酸钾 MnO2 氯化钾 + 氧气
3、高锰酸钾 加热 锰酸钾 + 二氧化锰 + 氧气
4、铁 + 氧气 点燃 四氧化三铁 5、甲烷 + 氧气 点燃 二氧化碳+水
人教版初中化学课件《制取氧气》ppt完美课1

8.造 成 中 西 方 用香 差异的 一个很 重要因 素,也 是许多 其他文 化差异 的内在 因素之 一,就 是各自 传统信 仰的不 同。西 方多信 仰基督 教,其 次是伊 斯兰教 ,二者 与香的 传播关 系并不 大;
感谢观看,欢迎指导!
6.中 西 方 用 香 的差 异源自 于思维 方式的 不同。 西方人 注重直 观性, 喜欢某 种气味 就直接 喷洒, 芬芳满 身,让 别人直 观地感 受到;
7.东 方 人 尤 其 是中 国人, 几千年 的文化 传承使 他们更 注重意 会性, 儒释道 三家无 不言开 悟,最 高深的 思想是 “意在 言外”, 最美好 的意境 是“言 有尽而 意无穷 ”,表 现在用 香上, 就会在 享受美 好的芬 芳之外 ,更注 重思想 的体验 和提升 。
加热
KMnO4ຫໍສະໝຸດ K2MnO4 + MnO2 + O2
自主预习
3. 加热高锰酸钾制 取氧气所用了哪些 仪器?
酒精灯、大试管、集气瓶、水槽、 铁架台(带铁夹)、导管、单孔橡 胶塞、玻璃片、木条
自主预习
4. 加热高锰酸钾制取氧气时,哪部分 是气体的发生装置?那部分是气体的 收集装置?为什么用排水法收集气体?
注意:(1)加热时,先均匀加热,后集
中加热,防止试管受热不均炸裂。 (2)外焰加热。
外焰
实验步骤
5.收: 用排水法收集气体
【思考】 (3)为什么导管口开始有气泡冒出
时,不能立即收集氧气?什么时候开 始收集?
因为开始冒出的气泡是空气。当气泡 连续而均匀地放出时,开始收集氧气。
实验步骤
【思考】 (4)收集满氧气的集气瓶为什么要 正立放在桌面上?
5 收、 收集气体
6 离、 将导管撤离水槽 7 熄、 熄灭酒精灯
2014年新人教版-氧气的制取

二、实验室制取氧气装置选择
2.收集装置 ①气体的密度 ②气体的溶解性、是否与水反应等
装置的 排水法收集气体更纯,但比较潮湿。 优缺点: 排空法收集气体干燥,但纯度不高。
气体收集装置选择依据
图3
图4
图5
向上排空法
密度比空气 大的气体
向下排空法
密度比空气 小的气体
排水法
不易溶于水或 难溶于水的气体
二、实验室制取氧气装置选择
复习:1、如何检验一瓶无色气体是氧气? 把带有火 星的木条伸到 盛有氧气的集 气瓶中,木条 重新燃烧起来, 说明瓶中的气 体是氧气。
2、如何鉴别三瓶无色气体:空气、氧气、氮 气? 将燃着的木条分别放入瓶中,如果燃烧 得更旺的是氧气;马上熄灭的是氮气;与空 气中一样的是空气。
实验室用高 锰酸钾制取氧气 的反应原理、实 验装置、收集方 法、注意事项。
向上排空气法(氧气的密度比空气大)
6、移:将导管移离水面
7、熄:熄灭酒精灯
讨论:1、用固体加热制氧气的试管为什么 要将试管口略向下倾斜? 防止冷凝水回流而使试管炸裂。
2、为什么用酒精灯的外焰加热? 因为外焰的温度最高。 3、怎么样给固定的试管加热? 先来回移动酒精灯给试管预热,再集中在 药品所在部位加热。
课题3 制取氧气 --- 实验室制取氧气的装置研究
授课教师:韩笑
14:55:52
学习目标
1.理解实验室制取氧气的方法和原理,初步 了解通过化学实验制取气体的方法 2.能够根据反应物的性质和反应条件来选择 气体的发生装置,会利用生成物的性质选择 收集方法 3.学生从中养成实事求是,严肃认真的科学 态度和良好的实验习惯
一、加热高锰酸钾制氧气
1、反应原理: 加热 高锰酸钾 KMnO4 2、实验装置:
(人教版)初中化学制取氧气优秀PPT1

•
4.黑色的墙壁上挂着各式的锁,有圆 形锁, 半圆锁 ,长方 锁,还 有八角 形白铜 雕花锁 ,谐音 就是“ 福禄” 的葫芦 锁。每 把锁都 是件工 艺品, 展示出 老人精 湛的制 锁技艺 ,看得 年轻人 目不暇 接,连 连竖起 大拇指 。
•
5.基于对“传统”的历史性和现实性 特点的 明确认 知,“ 新子学 ”强调 ,“国 学”在 漫长的 岁月中 必然存 在一个 变化发 展的过 程,可 以说一 代有一 代的“ 国学” 。从历 史上看 ,不可 否认, “六经 ”是中 国文化 学术的 最早源 头,它 深刻地 影响着 中华民 族的基 本精神 。
课题3 制取氧气(第二课时)
学习目标
起点目标:能识别典型的实验仪器图 基础目标:会正确选择所制取气体的
发生装置和收集装置 提高目标:会正确连接实验室制取氧气
装置,能绘制实验室制取氧 气装置
问题1:
实验室加热氯酸钾和二氧化锰混合物制氧气, 需要下列哪些仪器?应如何组装这些仪器?
问题2:
实验室用双氧水和二氧化锰混合制氧气也可 以用这套发生装置吗?为什么?应如何改进?
发生装置
A
B
问题3:见学练卷学一学问题1和2
议一议
①
②
③
问题4: 制的氧气用什么仪器收集? 采用什么方法收集氧气?
如何收集一瓶干燥的氧气?
排水法
空气
向上排空气法
收集装置
排水法
空气
向装置的依据 是什么?
拓展延伸
如果用右图装置收集氧气,则氧气
•
2.自从低焊钩锁、弹子锁普及后,老锁 铺变得 越来越 冷清了 。虽然 没有客 人,老 锁匠每 天早上 还是会 准时打 开铺子 ,在门 口泡上 一壶茶 ,握着 那把祖 辈传下 的壶, 安静地 品着祖 辈传下 来的味 道。
人教版初中化学课件《制取氧气》ppt名师课件2

b
a
•
1.同其他林木相比,竹子颇有一些 独特之 处,如 虚心、 有节、 清拔凌 云、不 畏霜雪 、随遇 而安等 等。这 些特点 ,很自 然地与 历史上 某些审 美趣味 、伦理 道德意 识发生 契合, 进而被 引入社 会伦理 美学范 畴,成 为君子 贤人等 理想人 格的化 身,并 对中国 传统文 化的发 展产生 深刻的 影响。
•
6.中西方用香的差异源自于思维方式 的不同 。西方 人注重 直观性 ,喜欢 某种气 味就直 接喷洒 ,芬芳 满身, 让别人 直观地 感受到 ;
•
7.东方人尤其是中国人,几千年的文 化传承 使他们 更注重 意会性 ,儒释 道三家 无不言 开悟, 最高深 的思想 是“意在 言外”, 最美好 的意境 是“言 有尽而 意无穷”,表现 在用香 上,就 会在享 受美好 的芬芳 之外, 更注重 思想的 体验和 提升。
反应物都是固体 反应需要加热
固液不加热型
反应物是固体和液体的混合物 反应不需要加热
使用长颈漏斗时,长颈漏斗的末端必须插入液体中:
防止生成的气体从长颈漏斗口逸出。
收集装置:收集方法:
1、排水法: O2不易溶于水 适于:不易、难或不溶于水的气体 优缺点:气体较纯,但不干燥 注:导管伸至集气瓶口
2、向上排空气法: O2密度比空气大 适于:密度比空气大的气体 优缺点:气体较干燥,但不太纯
A、加热固体药品前
B、与加热固体药品同时
C、开始有气泡放出时
D、气泡连续并均匀放出时
4、某同学设计了4种制氧气的方案:①用氯酸钾
和二氧化锰共热;②使高锰酸钾受热; ③用
高锰酸钾和氯酸钾共热;④使二氧化锰受热.判
断这四种方法: C
A.全正确
B. 全不正确
人教版化学制取氧气上课课件2
催化剂在化学反应中所起的作用叫 催 化 作用。
2、注意事项: (1)改变化学反应速率:既可加快也可减慢。 (2)催化剂既不是万能的,也不是唯一的; (3)催化剂可重复使用,只影响反应速率,不影响生成 物质量,也不能决定反应能否发生。
科学家如何验证催化剂质量未变?
实验操作: 实验前: 用精密的天平称量二氧化锰的质量. 实验后: 把二氧化锰洗净,干燥,再称量.
实验
操作
现象
分析
向装有1ml 5%的过
(1)
氧化氢溶液的试管 中,伸入带火星木
条,观察现象
过氧化氢溶液在常温下分解 木条不复燃 缓慢,放出的氧气少,速率
慢。
向上述试管中加少 (2) 量二氧化锰,伸入
产生大量气泡 二氧化锰加速了过氧化氢
带火星木条,观察 木条复燃 的分解。
待上述反应停止后,
氧气是过氧化氢产生的,二
现象: 发现质量没有发生变化.
结论: 催化剂在反应前后质量未改变.
《制取氧气》人教版 化学课件1ppt课件人教版课件
催化剂的广泛应用
1、在橡胶制品中常加入催化剂以减缓橡胶的老化 速度。
2、食用油脂里加催化剂可以有效的防止酸败。
尼龙催化剂
《制取氧气》人教版 化学课件1ppt课件人教版课件
氨分解催化剂 脱硫催化剂
分离液化空气法—— 属于物理变化 2、实验室制取氧气的方法: 属于化学变化
分解过氧化氢(H2O2)
加热氯酸钾(KClO3)
加热高锰酸钾(KMnO4)
药品观察:
过氧化氢溶液 (无色液体)双氧水、消毒
二氧化锰 (黑色不溶于水固体)
氯酸钾
( 白色固体)
高锰酸钾 (暗紫色固体)
过氧化氢=M=n=O2水+氧气
2、注意事项: (1)改变化学反应速率:既可加快也可减慢。 (2)催化剂既不是万能的,也不是唯一的; (3)催化剂可重复使用,只影响反应速率,不影响生成 物质量,也不能决定反应能否发生。
科学家如何验证催化剂质量未变?
实验操作: 实验前: 用精密的天平称量二氧化锰的质量. 实验后: 把二氧化锰洗净,干燥,再称量.
实验
操作
现象
分析
向装有1ml 5%的过
(1)
氧化氢溶液的试管 中,伸入带火星木
条,观察现象
过氧化氢溶液在常温下分解 木条不复燃 缓慢,放出的氧气少,速率
慢。
向上述试管中加少 (2) 量二氧化锰,伸入
产生大量气泡 二氧化锰加速了过氧化氢
带火星木条,观察 木条复燃 的分解。
待上述反应停止后,
氧气是过氧化氢产生的,二
现象: 发现质量没有发生变化.
结论: 催化剂在反应前后质量未改变.
《制取氧气》人教版 化学课件1ppt课件人教版课件
催化剂的广泛应用
1、在橡胶制品中常加入催化剂以减缓橡胶的老化 速度。
2、食用油脂里加催化剂可以有效的防止酸败。
尼龙催化剂
《制取氧气》人教版 化学课件1ppt课件人教版课件
氨分解催化剂 脱硫催化剂
分离液化空气法—— 属于物理变化 2、实验室制取氧气的方法: 属于化学变化
分解过氧化氢(H2O2)
加热氯酸钾(KClO3)
加热高锰酸钾(KMnO4)
药品观察:
过氧化氢溶液 (无色液体)双氧水、消毒
二氧化锰 (黑色不溶于水固体)
氯酸钾
( 白色固体)
高锰酸钾 (暗紫色固体)
过氧化氢=M=n=O2水+氧气
