β二羰基化合物
大学有机化学14、β–二羰基化合物

2H 3
(1 )C 2 H 5 O N a ,C 2 H 5 O H
HC(CO
CH 2 (CO 2 Et)
2 Et) 2 3
2
(2)C 2 H 5 Cl
CH 2 CH
(1)C 2 H 5 O N a,C 2 H 5 O H
(2)C 6 H 5 CH 2 Cl
(1 )H 3 O + ,H 2 O (2 )
能与乙酰氯作用生成酯; 能 使 B r 2/ C C l 4褪 色 ; 能 与 F e C l 3作 用 呈 现 紫 红 色 。
乙酰乙酸乙酯既有羰基的性质,又有羟基和双键的性 质,表明它是由酮式和烯醇式两种互变异构体组成的。
14.2 β–二羰基化合物碳负离子的反应
碳负离子
O O
O
2H 5
OH
-
O
CH 3 -C-CH 2 -C-OC 2 H 5
CH 2 CH 2 CH 2 Br
O
O
2H 5
O
(1)H 3 O + ,H 2 O
O
C 2 H 5 O-C-C-C-OC
H O-C-C-C-OH
注意:二卤化物Br(CH2)nBr中,n≥3~7;若n=2则 成三元环, 分子不稳定。
例:用丙二酸二乙酯合成 C 6 H 5 CH 2 CHCO
CH 2 CH
O CH 3 -C-OC 2 H 5
NaOC 2 H 5
O CH 3 -C-OC 2 H 5 CH 2 -C-OC 2 H 5 O
NaOC 2 H 5
-
O
O CH 3 -C CH 2 -C-OC 2 H 5
O
O
CH 3 -C CH 2 -C-OC 2 H 5 OC 2 H 5
第14章β-二羰基化合物

的酯在强碱 有α-H的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 发生缩合反应,失去一分子醇 生成β-羰基酯 一分子醇, 羰基酯的反应叫做酯 发生缩合反应,失去一分子醇,生成 羰基酯的反应叫做酯 缩合反应,又称为克莱森( 缩合反应,又称为克莱森(Claisen)缩合。 )缩合。
有机化学
上页 下页
重要β 二羰基化合物 重要 –二羰基化合物
O O C 2 H 5 O-C-CH 2 -C-OC 2 H 5
丙二酸二乙酯
O O CH3-C CH2-C-OC2H5
乙酰乙酸乙酯
有机化学
上页
下页
三、 丙二酸酯在有机合成上的应用
一.丙二酸二乙酯的制备 丙二酸二乙酯的制备
O O O O NaCN C H OH CH2-C-OH CH2-C-ONa 2 5 C2H5O-C-CH2-C-OC2H5 OH H2SO4 Cl CN
OH O CH3-C=CH-C-OC H5 2 烯醇式 (7%)
有机化学
上页
下页
二、 β –二羰基化合物碳负离子的反应 二羰基化合物碳负离子的反应
碳负离子是带部分负电荷的碳原子或氧原子, 碳负离子是带部分负电荷的碳原子或氧原子,都具 是带部分负电荷的碳原子或氧原子 亲核性, 有亲核性,在碳原子和氧原子上都有可能发生亲核 反应,主要发生在碳原子上 常见的反应有下列几种: 在碳原子上。 反应,主要发生在碳原子上。常见的反应有下列几种: (1)碳负离子与卤代烷的反应 卤代烷的反应 )碳负离子与卤代烷 羰基化合物的缩合反应 (2)碳负离子和羰基化合物的缩合反应 )碳负离子和羰基化合物 不饱和羰基化合物的共轭加成 (3)碳负离子和 ,β-不饱和羰基化合物的共轭加成 )碳负离子和α, 不饱和 反应
第十四章_β-二羰基化合物
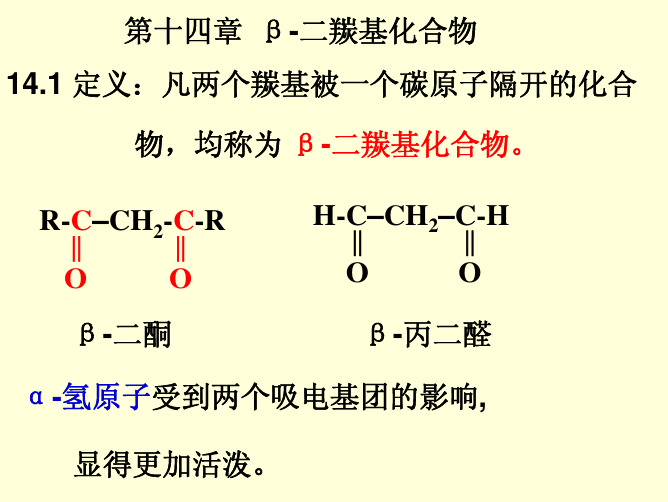
物,均称为 β-二羰基化合物。
R-‖C–CH2-‖C-R
O
O
β-二酮
H-‖C–CH2–C‖-H
O
O
β-丙二醛
α-氢原子受到两个吸电基团的影响,
显得更加活泼。
14.2 命名
HO-‖C–CH2-‖C-OH
O
O
β- 丙二酸
R-‖C–CH2–C‖-OR’
CH3︱CH=CH‖COC2H5 OH O
NaOC2H5 H+
CH3‖C CH-‖COC2H5 OO
Na
+
CH3‖CCH2C‖OC2H5 OO
①5%NaOH CH3COCH2COOH
②H+
CH3COCH3
△,-CO2
?
CH3‖CCH2C‖OC2H540%△NaOH OO
CH3‖COON+a
C2H5OH
CH3‖CO︱CCHH‖O2CCOHC2C2HO①5O5C%2H︱CNHaO2CHH2CCHO3‖OCO︱CCHHH2‖OCCOHN2CaOONa ②H+ , ③△ CH3‖CCH2
O
CH3‖C︱CCHH‖2CCOHC2C2HO5OC酮2式H 分解 OO
C︱H2CH2COOH CH3‖CCH2
O
︱CH2CH2COO酸C2式H分5 解
CH3‖CCH2C‖OC2H5 OO
H2N-OH H+
CH3‖CCH2COOC2H5 N-OH
Na CH3︱C= CH ‖COC2H5 ONa O
CH3︱C = CHC‖OC2H5 OH O
+ H2
CH3‖C-CH-‖COC2H5Na +
第十四章 β二羰基化合物

COOCH3 + CH3CH2CH2COOEt
NaH
N
COCHCOOEt
CH2CH3 N
3)分子内酯缩合( Dieckmann缩合) 建立五、六元脂环系 CH2COOEt CH3CH2ONa
实例 1
CH2CH2CO2C2H5 Na, C2H5OH(少量)
CH2CH2CO2C2H5
C6H5CH3
CO2C2H5 O
实例 2
CH3 CH2CHCO 2C2H5 CH2CH2CO2C2H5
CH3 CO2C2H5 O
CH3 O
CO2C2H5
CH3 O-
CO2C2H5
实例 3
O
O
CH3CH2C-CH2CH2CH2-COC2H5
酸等)
例如,用丙二酸二乙酯法合成下列化合物,其结构分析如下:
引入
CH3
原有
CH3 CH2 CH COOH
引入
原有 COOH
引入 CH2 CH2COOH CH2 CH2COOH
原有
原有 CH3 CH2 CH COOH
引入
CH2COOH
COOC2H5 CH2
C2H5ONa
COOC2H5
COOC2H5
_ CH
基的亲核加成反应;还原变为3-羟基丁酮酸乙 酯。
烯醇式结构:CH3C=CHCOOC2H5
OH
证据:烯烃性质-加溴(使溴水褪色);烯醇式 结构-三氯化铁水溶液显色;醇的性质—与三 氯化磷,乙酰氯反应等
乙酰乙酸乙酯实际是酮式和烯醇式混合物, 酮式和烯醇式混合物是互变异构,两者 处于平衡状态,互相转换。
原因如下:
1、羰基( C O)是个吸电子能力较强的基团,两个羰基对它们 中间有亚甲基的吸电子诱导作用一致,具有加和性,使得α-H的 活性增强。
第十四章 β-二羰基化合物

• 水解、加热脱羧——1,5-二羰基化合物
例2:
• 水解、加热脱羧——1,5-二羰基化合物
(3)酸式分解——在浓碱(40% NaOH)中加热, 和 的C-C键断裂而生成两个分子的乙酸:
(4) 乙酰乙酸乙酯烃基化反应--与卤烷亲核取代反应
A: 一烃基取代
• -碳原子上的烃基化反应.
再反应
B: 二烃基取代
注意:两个卤代烃(不 同)分步取代,否则产 物复杂化 • 得到的 -烃基取代的乙酰乙酸乙酯,再进行酸式或酮 式分解,可制得甲基酮、二酮、一元或二元羧酸。 • 还可用来合成酮酸及其他环状或杂环化合物。
补充1:
如三级卤代烃易 消除!不行!
解:
烃基不同,分 步取代!
解:
(2) 合成二元羧酸 例如:合成丁二酸、己二酸
物料比(2:1)-直链 + CH2I2 (醇钠)成环
2 C2H5ONa CH2I2
COOC2H5 COOC2H5 COOC2H5 COOC2H5
COOH COOH
补充2: 作业8(4)
2
2
补充3: (3)环状一元羧酸
n=2, 易开环
• 二卤化物(Br(CH2)nBr,n=3~7)与丙二酸酯的成 环反应
CH2 (COOC2H5 )2
2 C2H5ONa
COOC2 H5 COOC2 H5
Br(CH2)5Br
注意物料比1:1
COOH
• 利用丙二酸酯为原料的合成方法,常称为丙二酸酯 合成法。
• 酮式分解得:-二酮
补充8
(1)与-卤代酮(Cl-CH2COR)反应
• 酮式分解——1,4-二酮 • 酸式分解——-酮酸
(2)与Br-(CH2)nCOOC2H5反应 • 酸式分解——二元酸 HOOC-(CH2)n+1COOH
第十四章 β-二羰基化合物

二取代乙酸 试剂:CH3 X
CH3CH2CH2 X
CH2(COOC2H5)2
CH3CH2
CHCOOH CH3
2-甲基丁酸
CH2(COOC2H5)2
① C2H5ONa ② CH3I ① C2H5ONa ② CH3CH2Br
CH3CH2CH(COOC2H5)2
NaOH H2O H+
CH3CH2C(COOC2H5)2 CH3
OH H2C
O C O CH2 C OC2H5
O CH3 CH
OH O CH C OC2H5
CH
CH3
×
CH3 C
2. 乙酰乙酸乙酯在合成上的应用
(1)乙酰乙酸乙酯的合成 乙酰乙酸乙酯可用Claisen酯缩合反应合成。
O CH3 C OC2H5
+
O ① C2H5ONa CH3 C OC2H5
=
O O CH3 C CH2 C OC2H5
R X
O O CH3 C CH C OC2H5 Na+
RCOX
O O CH3 C CH C OC2H5 R O O CH3 C CH C OC2H5 R C =O
这是一个亲核取代反应,主要生成烃基化和酰基化产物。 这里卤代烷常用伯卤代烷或仲卤代烷,叔卤代烷容易消除而 不能用;乙烯型和芳基型卤代烃也不能用。
α-碳原子上的两个氢原子均可被烃基取代。
O O O R’ O ① C2H5ONa CH3 C C C OC2H5 CH3 C CH C OC2H5 X
② R’
R
R
(5)乙酰乙酸乙酯在合成上的应用
① dil. OH
O O CH3 C CH C OC2H5 R ( 酸式分解 ) ( 酮式分解 )
有机化学第14章 β-二羰基化合物
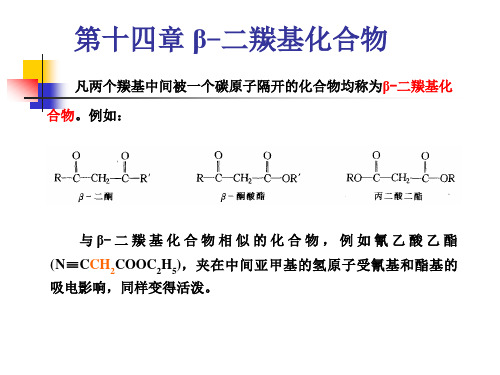
工业上乙酰乙酸乙酯可用二乙烯酮与乙醇作用制得:
乙酰乙酸乙酯为无色具有水果香味的液体,沸点181℃(稍有分解),
微溶于水,可溶于多种有机溶剂。乙酰乙酸乙酯对石蕊呈中性,但能 溶于稀氢氧化钠溶液。它不发生碘仿反应。
2.乙酰乙酸乙酯的性质
乙酰乙酸乙酯可在稀碱(或稀酸)的作用下,水解生成乙酰乙酸,
后者在加热的条件下,脱羧生成酮。这种分解称为酮式分解,可用
键形成一个稳定的六元环,另一方面烯醇式羟基氧原子上的未共用
电子对与碳碳双键和碳氧双键是共轭体系,发生了电子的离域,降 低了分子的能量的缘故。
酮—烯醇互变异构现象在羰基化合物中较为普遍,但它们的烯
醇式含量是不同的。
(在室温条件下)
14.2 乙酰乙酸乙酯的合成及应用
1.乙酰乙酸乙酯的合成
乙酰乙酸乙酯可用Claisen酯缩合反应合成。乙酸乙酯在强碱 (如乙醇钠、金属钠等)的催化下缩合,然后酸化,即可得到乙酰乙 酸乙酯。
曾讨论过烯醇式和酮式的互变异构现象。
但β-二羰基化合物的烯醇式结构却具有一定的稳定性。如β-
丁酮酸乙酯(又称为乙酰乙酸乙酯,俗称三乙),通常是以酮式和烯
醇式两种异构体的混合物形式存在的。
这种能够互相转变的两种异构体之间存在的动态平衡现象就 称为互变异构现象。
乙酰乙酸乙酯的两种异构体,可在较低的温度下,用石英容器精馏
反应式表示为:
另外,乙酰乙酸乙酯如与浓碱共热,则α-和β-碳原子之间的键
发生断裂,生成两分子乙酸盐。一般β-羰基酸都发生此反应,这种
分解称为酸式分解。
乙酰乙酸乙酯分子中亚甲基上的氢原子比较活泼,与醇钠等强碱
作用,可以生成钠的衍生物,后者可与卤代烷发生取代反应,生成烷
基取代的乙酰乙酸乙酯;在需要时还可以生成二烷基取代的乙酰乙酸 乙酯,使用更强的碱如叔丁醇钾替代乙醇钠进行反应效果更好。
第15章二羰基化合物

COOC 2H5
OH-/H2O H+/H2O CH3CH2CH2 COOH
说明(explanation):
COOC 2H5 CH 3CH 2CH
COOC 2H5
①所用RX最好是伯卤代烃,如仲卤代烃时,反应TS拥挤程度大, △E高,不利于反应,同时伴有一定的消除反应,故收率低。
② 当卤代烃在OH-中发生消除,而 C C X其中X不活泼。
O
O
CH3COC2H5 CH3CCH3
OO C2H5OCCH 2COC 2H5
OO CH3 CCH 2 COC 2H5
pKa 25
20
13
11
例如(illustration) :
O
O
CH3C CH2 CCH3
酮式 (24% )
H
O
O
CH3C C CCH3 H
烯醇 式 (76% )
分子内氢健 共轭体系
COOC2H5 CH
COOC2H5
OH-/H2O H+/
COOH
例:由丙二酸二乙酯和相应的R-X合成
OO
C2H5OCCH 2COC2H5 丙二酸二乙酯
(diethyl malonate)
β—二羰基化合物的化学特性在于两个 C 之O 间的亚甲
基 CH 2 活泼性。由于亚甲基受两个 C O的诱导吸电作 用,使亚甲基上氢原子的酸性增强。
例(illustration) :
O
C CH 2
C O
CH 3 O C2H5
O
O
C OC2H5 + CH3 C
C2H5ONa CH3 H+/H2O
O
O
C CH2 C CH3
有机化学第十四章 β-二羰基化合物

CONR2,
烷基化反应:
CO2C2H5 (CH3)2CH I + CH2 CN
① C2H5ONa /C2H5OH ② (CH3)2CH I
① C2H5ONa /C2H5OH ② H 3O
+
CO2C2H5 CH(CH3)2 CN
(CH3)2CH C (95%)
Michael 加成反应:
CH3 CH2 C CN 2–甲基– 丙烯酸乙酯 氰基乙酸乙酯
3 2 5
C H2 C H3C O C HC O O2C H5 C H3C O C H 2C H2C H2C O C H 3
CH3COCH2COOC2H5
H5 (1)C2H5O Na C H3C O C HC O O2C (2) I2 酮式分解 C H3C O C HC O O2C H5 C H3C O C H 2C H2C O C H 3
O CH2 COEt
O CH2 COEt
第二步 烯醇负离子对另一酯分子的 亲核加成:
O O O CH3 C OEt CH2 COEt CH3 COEt + CH2 COEt
O CH2COEt
四面体 中间体
O
第三步 离去基团的消除,恢复羰基结构:
O CH3 C OEt CH2 COEt O CH3 O O C CH2 COEt + OC2H5
(1.5×10-4%)
比 C C 更稳定 键能差:45 ~ 60 kJ • mol-1
乙酰乙酸乙酯(β–丁酮酸乙酯): (ethyl acetoacetate) 互变异构
一般烯醇式不稳定,而乙酰乙酸乙酯的烯醇式较稳 定存在:
( 1 )酮式中亚甲基上的氢原子同时受羰基和酯基的影 响很活泼,很容易转移到羰基氧上形成烯醇式。 (2)烯醇式中的双键的π键与酯基中的π键形成π-π 共轭体系,使电子离域,降低了体系的能量。 :OH O CH 3 C CH C OC 2H5 (3)烯醇式通过分子内氢键的缔合形成了一个较稳定的 六员环结构。 O H O CH3 C CH C OC2H5
第十五章 β-二羰基化合物

H
Δ
CH 3COOH + CO 2
丙二酸二乙酯的α-烷基化
CO 2Et CO 2Et
EtO
CO 2Et CO 2Et
R1X
CO 2Et R1 CO 2Et
1.EtO 2.R2X
R1 R2
CO 2Et CO 2Et H
+
Δ
R1 COOH R2
用丙二酸二乙酯可以合成一元羧酸(乙酸衍生物)、 二元酸、环烷酸。
COOH
eg1 : 用简单的有机原料合成
COOH
2 CH2(CO2Et)2
2 EtOBrCH2CH2CH2Br
(COOEt)2
CH(CO2Et)2 CH(CO2Et)2 H+
2 EtO-
I2
COOH
OH-
(COOEt)2
COOH
eg 2: 用简单的有机原料合成
HO 2C CO2H
(螺环二元羧酸)
O-
CH3C-CH2-C-OC 2H5 OH OH
O
O CH3-COH
+ -CH 2-COH + C2H5O-
H2O
O CH3-COH
H2O
C2H5OH
乙、乙酰乙酸乙酯的α-烷基化、 α-酰基化
O
C2H5ONa -C2H5OH
O
O
CH3CCHCOC2H5
O-
Na+
O
CH3I
O CH3
CH3C-CH-COC2H5
EtOEtO 2C EtO 2C CO2Et CO2Et
2 CH2(COOEt)2 + HOH+
Br Br
Br Br
-CO2
Beta二羰基化合物
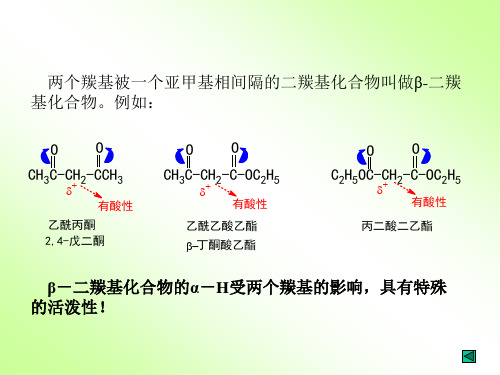
② 酮的酸性一般大于酯,所以在乙醇钠的作用下,酮更 易生成碳负离子。
例如:
O CH3-C-CH 3 C2H5ONa
O CH3-C-C-H 2
O-
CH3-C=CH 2
O
O
CH3-C-OC2H5 + -CH2-C-CH3
O- O CH3-C-CH2-C-CH3
OCH2CH3
OO CH3-C-CH2-C-CH3
R
C
CC
C O CH3
O
EtOH
OO
RC
C OEt
溴化后可以形成卡宾,可以合成小环化合物
O
C O CH3
H2C C
C O CH3
Br2
O
O
Br H
C O CH3
C
C
C O CH3
CuX
O
CH=CH2
O
C O CH3
Ar
CC
C O CH3
O
O
C O CH3
C
C
C O CH3
O
14.4Knoenenagel反应:
CF3
CH3
2. 烯醇式含量与溶剂有关,在极性溶剂(如:水或质
子性溶剂)中烯醇式含量↓,而在非极性溶剂中烯醇式
含量↑。如:
O
O
OH O
=
CH3 C CH2 C OC2H5
酮式
= CH3 C CH C OC2H5
烯醇式
H2O
99.6 %
0.4 %
C2H5O H
89.48 %
10.52 %
C6H12
53.6 %
46.4 %
这是因为在极性溶剂中,酮式或烯醇式均易 与水形成分子间氢键,从而减少了烯醇式形 成分子内氢键的几率;而在非极性溶剂中则 有利于烯醇式分子内氢键的形成。
第12章β-二羰基化合物

C2H5OH + CO2 C2H5OH + CO2
C2H5OH + CO2
b、酸式分解 、
O O 浓 NaOH CH3 C CH2 C OC2H5
2 CH3COOH + C2H5OH
O O 浓 OH CH3COOH + RCH2COOH + C2H5OH CH3 C CH C OC2H5 R O O 浓 OH CH COOH + RCOCH COOH + C H OH 2 5 2 CH3 C CH C OC2H5 3 COR
-
Na+
Br(CH2)4Br
O O CH3-C-CH-C-OC2H5
O CH2(CH2)3Br C-CH3
COCH3 COOC2H5
成酮分解
三、 丙二酸二乙酯的合成及应用
1、丙二酸二乙酯的制法
O C-OC2H5 CH2 C-OC2H5 O
丙二酸二乙酯
CH2COONa Cl
氯乙酸钠
NaCN
CH2COONa CN
CH2CH2COOEt CH2CH2COOEt
EtONa
苯,80 C
。
COOEt O-
H 、 乙酰乙酸乙酯的化学性质 (1)酮式分解和酸式分解 (1)酮式分解和酸式分解
a、酮式分解 、
O O O NaOH 稀 CH3 C CH2 C OC2H5 CH3 C CH3 O O O CH3 C CH C OC2H5 稀 OH CH3 C CH2R R O O O O OH CH3 C CH C OC2H5 稀 CH3 C CH2 C R COR
+
H-C-OEt + CH3CH2COOEt
β二羰基化合物

β二羰基化合物一、概述β二羰基化合物是一类含有两个羰基官能团的有机化合物,其分子中两个羰基官能团的位置相对,呈现出β位取代的结构。
这种结构使得β二羰基化合物具有独特的化学性质和广泛的应用价值。
二、合成方法1. 光氧化法将α,β-不饱和酮暴露在紫外线或可见光下,可以通过光氧化反应制备出β二羰基化合物。
这种方法具有反应条件温和、高产率等优点。
2. 溴素法将α,β-不饱和酮与溴素反应,可以得到溴代产物。
再经过碱性条件下的消除反应,可以制备出β二羰基化合物。
3. 重排法在适当条件下,α,β-不饱和酮可以发生重排反应,生成β二羰基化合物。
这种方法具有操作简单、产率高等优点。
三、性质及应用1. 化学性质由于其分子中含有两个羰基官能团,因此β二羰基化合物具有较强的亲电性。
它们可以发生加成反应、环加成反应、氧化反应等多种反应,可以用于合成许多有机化合物。
2. 应用价值β二羰基化合物广泛应用于医药、农药、染料等领域。
例如,β二羰基酮类化合物是一类重要的抗癌药物;β二羰基酸类化合物是一类重要的杀虫剂;β二羰基染料则具有良好的着色性能和稳定性能。
四、典型实例1. 乙酰丙酮乙酰丙酮是一种最为常见的β二羰基化合物。
它的分子中含有两个羰基官能团和一个甲基官能团,具有较强的亲电性和较好的稳定性,可以作为配位体或还原剂使用。
2. 丁酮丁酮是另一种常见的β二羰基化合物。
它的分子中含有两个羰基官能团和一个烷基官能团,具有较强的亲电性和较好的稳定性,可以作为溶剂或中间体使用。
五、结论β二羰基化合物是一类具有独特结构和广泛应用价值的有机化合物。
它们可以通过光氧化法、溴素法、重排法等多种方法制备,具有较强的亲电性和较好的稳定性。
在医药、农药、染料等领域具有广泛应用前景。
β-二羰基化合物

+
CH2(COOH)2
CH3COOH
②α -H的取代反应
CH2(COOC2H5)2 C2H5ONa CH COOC2H5 CH3Br COOC2H5 CH3 CH COOC2H5 COOC2H5
3.合成应用 ●合成一元酸
例如:以C≤2的醇为原料经丙二酸二乙酯合成2-丁酸
CH3 C COOH COOH
① NaOH,H2O ② H
+
CH3CH2
- CO2
CH3 CH3CH2 CH COOH
③ 合成环状羧酸
例:以丙二酸二乙酯、不超过2个碳的醇及其它无机试剂为原料, 合成
CH3CH2OH CH3CH2OH Na
COOH
C2 H5ONa H2C CH2 Br2 BrCH2CH2Br
分析:(1) 产物为甲基酮,合成时一定要经过酮式分解。
(2) 将TM的结构与丙酮进行比较,确定引入基团 (3) 最后确定合成路线。
注意:当引入基团不同时,通常是先引入活性较高和体积较大
的基团
▲合成一元羧酸
如上述合成的α-丙基乙酰乙酸乙酯中间体进行酸式分解:
O O ① C2H5ONa O O CH3 C CH2 C OC2H5 CH3 C CH C OC2H5 ② CH3CH2CH2Br CH2CH2CH3
O O C2H5 O CH3 C CH2 C OC2H5 O O
O O [ CH C CH C OC H 3 2 5 C2H5OH
CH3 C CH C OC2H5
]
+
再如:
O 2 CH3 CH2 CH2 C OC2H5 ① ② O C2H5ONa H
+
β二羰基化合物

O
H
快
R CH C
R' +
O H
R C CH R' + OH
OH
§14.1.2 化合物的结构对酮-烯醇平衡的影响 单羰基化合物在平衡状态下,烯醇式异构体的含量很少。
具有β-二羰基结构的化合物在平衡状态下,烯醇式的含量较高。
原因一:分子内氢键;原因二:C=C键和C=O键共轭
H3C
CH
C
C
OC2H5
O
§14.1.1 酸和碱对酮-烯醇平衡的影响
酸催化:
O:
RCH2 C
R' + H
H O +H
快
+O RCH2 C
H
R' + H2O
+O R CH C
H
H
R' +
H
:O
H
慢
R C CH R' + H3O+
OH
碱催化:
O R CH C
H
R' +
慢
: OH
O R CH C R'
O
R CH C R' + H2O
OC2H5
OC2H5离 去
O
O
H3C C CH2 C OC2H5
二、交叉酯缩合:两种酯均有α -H ,四产物,无价值。 只有一种酯有α -H ,两种产物,易分离。
HCOOC2H5
+ CH3COOC2H5 OC2H5
HCOCOCH2COOC2H5
+ CH3COCH2COOC2H5 + C2H5OH
CH3COCHCOOC2H5
二羰基化合物

C6H12
53、
46、4%
6%
原因:在极性溶剂中,酮式或烯醇式均易与水形
成分子间氢键,从而减少了烯醇式形成
分子内氢键得几率;而在非极性溶剂中
则有利于烯醇式分子内氢键得形成。
2023/10/21
7
二、β-二羰基化合物得酸性和烯醇式负离子得稳定性
β-二羰基化合物得α-H受两个羰基得影响,具有 特殊得活泼性!
O
CH
C O C2H5
R
C C
O C2H5
O C2H5
R'
C O C2H5
O
OH
- CO2
R'
150~200℃ R C H C O O H OH
H2O / H+
思考题:用丙二酸二乙酯制备
COOH 。
提示:用1,2-二溴乙烷与丙二酸二乙酯负离子反应(1∶1)。
2023/10/21
15
② 制备二元羧酸
C H C O O C H 2 ( 2 2 5 2 ) C2H5ON C aH C O 2 O ( C N H 2 5 ) 2 - + a
Br Br CH2 CH2
C H C H O C O 2 C H ( 2 5 2 ) H2OC / HH + C 2 H C O O ( H ) 2 C H C H O C O 2 C H ( 2 5 2 ) C H C 2 H C O O ( H ) 2
2023/10/21
- 2 C O2C H 2 C H C O 2 O H
1、 丙二酸二乙酯得制法
O
C H2C O O Na Cl
NaCN
2023/10/21
C H2C O O Na CN
β二羰基化合物

β二羰基化合物一、什么是β二羰基化合物?β二羰基化合物是一类具有两个羰基基团(C=O)的有机化合物。
在化学结构中,β二羰基化合物的两个羰基基团存在于相邻的碳原子上。
该类化合物通常具有较高的反应活性和广泛的应用领域。
二、β二羰基化合物的合成方法2.1 共轭加成反应共轭加成反应是一种常见的β二羰基化合物合成方法。
这种反应通过有机化合物中存在的亲电基团与碳碳双键发生加成反应,形成β二羰基化合物。
2.2 氧化反应氧化反应是另一种制备β二羰基化合物的重要方法。
一些有机化合物在氧化剂的作用下,可以发生氧化反应,生成β二羰基化合物。
2.3 消除反应消除反应也是一种常用的合成β二羰基化合物的方法。
这种反应通过将有机化合物中的某些官能团去除,形成β二羰基化合物。
三、β二羰基化合物的性质与应用3.1 物理性质β二羰基化合物通常呈固体或液体状态。
它们的熔点和沸点较高,具有较好的稳定性。
此外,β二羰基化合物还具有一定的极性,可溶于一些极性溶剂。
3.2 化学性质由于β二羰基化合物中存在两个羰基基团,其化学性质十分活泼。
它们可通过与其他化合物发生加成、环化、氧化等反应,进一步形成结构多样的化合物。
3.3 应用领域由于其特殊的结构和丰富的反应性,β二羰基化合物在有机合成和药物化学等领域有着广泛的应用。
•在有机合成中,β二羰基化合物可以作为反应中间体,参与多种重要的反应,如Michael加成、Aldol反应等。
•在药物化学领域,β二羰基化合物被广泛用于开发新型药物。
这类化合物具有较好的生物活性,可以用于合成抗生素、抗癌药物等。
•此外,β二羰基化合物还可以应用于染料合成、材料科学等领域。
四、β二羰基化合物的代表性化合物4.1 乙酰丙酮乙酰丙酮(Acetylacetone)是一种最为常见的β二羰基化合物。
它具有两个羰基基团,可用于多种有机合成反应和配位反应。
4.2 乙二酰丙酮乙二酰丙酮(Ethyl acetoacetate)是另一种重要的β二羰基化合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
H
CH3COCHCOOC2H5
①NaOC2H5 ②CH3CH2CH2Br
CH3COCCOOC2H5
H
CH2CH2CH3
①NaOC2H5 ② CH3I
CH3
①稀 OH ②H+ ③
酮式分解
O CH3C
CH3 CH CH2CH2CH3
CH3COCCOOC2H5 CH2CH2CH3
①40%OH ②H+
酸式分解
O 2 H3C C
OC2H5
C2H5ONa C2H5OH
O
O
..
H3C C CH C OC2H5
HCl
+ Na
O
O
H3C C CH2 C OC2H5
HO H2C C OC2H5 C2H5ONa
:CH2
O
+ C OC2H5 C2H5OH
O H3C C
OC2H5
机理 动画演示
:O
O
H3C C CH2 C OC2H5
O
H
H3C C CH COC2H5
:OH
O
活泼亚甲基具有酸性pKa = 9~14
O
O
O
O
O
O
R C CH2 C R R C CH2 C OR ROKa ≈14
O
O
C
C
RO
C
H
H
O
O
C
C
C
H
O
O
H3C C CH2 C OC2H5 (92.5%)
OH
O
H
快
R CH C
R' +
O H
R C CH R' + OH
OH
§14.1.2 化合物的结构对酮-烯醇平衡的影响 单羰基化合物在平衡状态下,烯醇式异构体的含量很少。
具有β-二羰基结构的化合物在平衡状态下,烯醇式的含量较高。
原因一:分子内氢键;原因二:C=C键和C=O键共轭
H3C
CH
C
C
OC2H5
O
O
H3C C CH C OC2H5 (7.5%)
能与羟胺和苯肼生成肟和苯腙 还原得到羟基酸酯 水解得到丁酮酸
能与Na作用放出氢气 能使Br2/CCl4溶液退色 能使FeCl3水溶液显紫红色 与PCl5作用得到3-氯-2-丁烯酸
乙酯
§14.1.3 烯醇化导致立体异构化
Et Me C
H
O C Ph
COCH3 C2H5ONa
COOC2H5
O
COCH3
酮式分解
COOC2H5
CH3
三、制备高级酮酸或β-二酮:
CH3COCHCOOC2H5
Na+ + Br(CH2)nCOOC2H5
CH3COCHCOOC2H5 (CH2)nCOOC2H5
酮 式 分 解 CH3COCH2(CH2)n COOH
CH3COCHCOOC2H5 NaH
CH3COCHCOOC2H5 H
NaOC2H5 CH3COCHCOOC2H5
+
Na
R
RX CH3COCHCOOC2H5
R CH3COCCOOC2H5
H
R
(CH3)3OK CH3COCCOOC2H5
Na+
R
R'X CH3COCCOOC2H5
R'
§14.2.3乙酰乙酸乙酯在合成上的应用
一、制备甲基酮或烷基取代乙酸:
HOOC
CH3 CH CH2CH2CH3
二、制备二元酮或甲基环烷基酮:
2 CH3COCHCOOC2H5
CH3COCHCOOC2H5
+
Na
CH2Cl2
CH2
CH3COCH2
酮式分解
CH2
CH3COCHCOOC2H5
CH3COCH2
CH3COCHCOOC2H5
+
Na
Br(CH2)4Br
Br(CH2)4 CH
三、Dieckmann缩合:分子内酯缩合。
CH2CH2COOC2H5 CH2CH2COOC2H5
NaOC2H5
O COOC2H5
四、二乙烯酮与乙醇加成 :
CH2 C O CH2 C O + C2H5OH
OH
O
CH2 C CH2 C OC2H5
O
O
CH3 C CH2 C OC2H5
乙酰乙酸乙酯无色液体,有水果香味,沸点181oC,微溶于水, 易溶于有机溶剂,溶于NaOH溶液,对石蕊呈中性。
第十四章β-二羰基化合物
O
O
R C CH2 C R'
β-二酮
O
O
RO C CH2 C OR
丙二酸二酯
O
O
R C CH2 C OR'
β-酮酸酯
O N C CH2 C OR
氰基乙酸酯
§14.1 酮-烯醇互变结构
炔烃Kucherov反应中:
R C CH2R' O
酮式
互变异构
R C CHR' OH
烯醇式
§14.2.2乙酰乙酸乙酯的性质
一、酮式分解:稀碱作用下
CH3COCH2COOC2H5 5%NaOH CH3COCH2COONa H+
CH3COCH2COOH
CH3COCH3
二、酸式分解:浓碱作用下
O CH3C
O CH2COOC2H5 40%NaOH 2 CH3C
ONa + C2H5OH
三、烷基取代活泼亚甲基中的氢原子
OH or H+
(R)-(+)-仲丁基苯基甲酮
Et
O
Et
O
Me C C Ph + H C C Ph
H
Me
( + ) -仲丁基苯基甲酮
Et Me C
H
O
OH Et
C
Ph
or
+
H
Me
C
(R)-(+)-仲丁基苯基甲酮
OH C
Ph
(+ ) -仲丁基苯基甲酮
§14.2乙酰乙酸乙酯的合成及其应用
§14.2.1乙酰乙酸乙酯的合成 一.克莱森(Claisen)酯缩合:酯中的α-氢比较活泼,在醇钠作 用下,能与另一分子酯脱去一分子醇,生成α-酮酸酯:
§14.1.1 酸和碱对酮-烯醇平衡的影响
酸催化:
O:
RCH2 C
R' + H
H O +H
快
+O RCH2 C
H
R' + H2O
+O R CH C
H
H
R' +
H
:O
H
慢
R C CH R' + H3O+
OH
碱催化:
O R CH C
H
R' +
慢
: OH
O R CH C R'
O
R CH C R' + H2O
OC2H5
OC2H5离 去
O
O
H3C C CH2 C OC2H5
二、交叉酯缩合:两种酯均有α -H ,四产物,无价值。 只有一种酯有α -H ,两种产物,易分离。
HCOOC2H5
+ CH3COOC2H5 OC2H5
HCOCOCH2COOC2H5
+ CH3COCH2COOC2H5 + C2H5OH
CH3COCHCOOC2H5
+
Na
+ H2 C6H5COCl
H CH3COCHCOOC2H5 酮 式 分 解 CH3COCH2COC6H5
COC6H5
§14.3丙二酸酯的合成及其应用 一、丙二酸二乙酯的合成
NaCN
CH2COONa Cl
CH2COONa CN
C2H5OH H2SO4
COOC2H5 CH2 COOC2H5
丙二酸二乙酯:无色液体,有水果香味,沸点199oC,微溶于 水,易溶于有机溶剂。有弱酸性,pKa=13。
二、制备取代乙酸:
CH(COOC2H5)2 NaOC2H5
