硫酸铜电解液中氯离子的电位滴定
实验三 水中氯离子的测定-沉淀滴定法和电位滴定法

实验三、水中氯离子的测定(沉淀滴定法和电位滴定法)1.沉淀滴定法此法依据《水质氯化物的测定硝酸银滴定法》(GB 11896-89)一、实验目的和要求学习银量法测定氯含量的原理和方法;掌握AgNO3标准溶液的配制和标定方法。
二、实验原理在中性至弱碱性范围内(pH6.5—10.5),以铬酸钾为指示剂,用硝酸银滴定氯化物时,由于氯化银的溶解度小于铬酸银的溶解度,氯离子首先被完全沉淀出来后,然后铬酸盐以铬酸银的形式被沉淀,产生砖红色,指示滴定终点到达。
该沉淀滴定的反应如下:Ag++Cl—→AgCl↓2Ag++CrO4→Ag2CrO4↓(砖红色)三、实验仪器和设备(1)锥形瓶,250mL;(2)滴定管,25mL,棕色;(3)移液管,10mL,25mL,50mL;(4)容量瓶,100mL,1000mL。
四、实验试剂和材料分析中仅使用分析纯试制及蒸馏水或去离子水。
(1)氯化钠标准溶液,C(NaCl)=0.0141mol/L,相当于500mg/L氯化物含量:将氯化钠(NaCl)置于瓷坩埚内,在105℃下烘干2h。
在干燥器中冷却后称取8.2400g,溶于蒸馏水中,在容量瓶中稀释至1000mL。
用移液管吸取10.0mL,在容量瓶中准确稀释至100mL。
1.00mL此标准溶液含0.50mg氯化物(C1-)。
(2)硝酸银标准溶液,C(AgNO3)=0.0141mol/L:称取2.3950g于105℃烘半小时的硝酸银(AgNO3),溶于蒸馏水中,在容量瓶中稀释至1000mL,贮于棕色瓶中。
用氯化钠标准溶液(1)标定其浓度:用移液管准确吸取25.00mL氯化钠标准溶液于250mL或100mL锥形瓶中,加蒸馏水25mL。
另取一锥形瓶,量取蒸馏水50mL作空白。
各加入1mL铬酸钾溶液(3),在不断的摇动下用硝酸银标准溶液滴定至砖红色沉淀刚刚出现为终点。
计算每毫升硝酸银溶液所相当的氯化物量,然后校正其浓度,再作最后标定。
1.00mL 此标准溶液相当于0.50mg氯化物(C1—)。
电位滴定法测氯离子

电位滴定法
1、方法原理 电位滴定法测定氯化物,是以氯电极为指示电极, 以玻璃电极或双液接参比电极为参比,用硝酸银标准 溶液滴定,用伏特计测定两电极之间的电位变化。在 恒定地加入小量硝酸银的过程中,电位变化最大时仪 器的读数即为滴定终点。
2、干扰及消除 溴化物、碘化物能与银离子形成溶解度很小的物质, 干扰测定;氰化物为电极干扰物质;高铁氰化物会使 结果偏高;高铁的含量如果显著地高于氯化物也引起 干扰;六价铬应预先使还原为三价,或者预先去除。 重金属、钙、镁、铝、二价铁、铬、HPO42-、SO42-等 均不干扰测定。硫化物、硫代硫酸盐和亚硫酸盐等的 干扰可用过氧化氢处理予以消除。Br﹣、I﹣的干扰, 可用加入定量特制的Ag粉末,或者从测得得总卤量中 扣除Br﹣、I﹣的含量的方法消除。
氯离子的测定 (电位滴定法)
氯化物的来源
氯化物是水和废水中常见的无机阴离子。几乎所有 的天然水中都有氯离子存在,它的含量方位变化大, 在河流、湖泊、沼泽地区,氯离子含量一般比较低, 而在海水、盐湖及某些地下水中,含量可高达数十克 每升。 在人类的生存活动中,氯化物有很重要的生理作用 和工业用途。 天然水中的氯化物主要来源于含有氧化物的地层, 沿海地区的水受海水以及工农业废水和生活污水的排 入的影响。生活污水中的氯化物主要来自人类排泄物, 每人每日排出的氯化物余额为6g。工业废水都含有很 高的氯化物。
氯离子的测定方法
氯离子的测定有四种通用的方法可供选择;(1) 硝酸银滴定法;(2)硝酸汞滴定法;(3)电位滴定 法;(4)离子色普法。(1)法和(2)法所需仪器设 备简单,在许多方面类似,可以任意选用,适用于较 清洁水。(2)法的终点比较易于判断;(3)法适用 于带色或浑浊水样;(4)法能同时快速灵敏地测定包 括氯化物在内的多种阴离子,具备仪器条件时可以选 用。 下面着重介绍下电位滴定法。
仪器分析实验

仪器分析实验讲义西安文理学院化学系分析化学教研室2011-3实验一、HPLC法测定减肥茶中五种蒽醌类化合物的含量一、实验目的1.了解HPLC在药物分析方面的应用。
2.熟悉色谱分析方法和操作。
二、实验原理减肥茶(植物药)中含有多种蒽醌类化合物、萘并-吡酮类、蛋白质及氨基酸、糖类及人体所必需的微量元素,其中蒽醌类成分为减肥茶的主要功效成分之一。
通过优化色谱分离条件,可以建立同时分离测定减肥茶中蒽醌类化合物的反相高效液相色谱法(RP-HPLC) ,大黄酸、大黄素、大黄酚、大黄素甲醚和芦荟大黄素可得到有效分离三、仪器和试剂高效液相色谱仪:岛津LCSolutionSPD-20A 紫外检测器;LC-20A液相色谱高压泵;SPD-M20A 二极管阵烈检测器;CTO-20A柱箱芦荟大黄素(Aloe-emodin)、大黄酸(Phein)、大黄素(Emodin)、大黄酚Chrysophanol)和大黄素甲醚(Physcion)对照品由中国药品生物制品检定所提供。
色谱分析用试剂为色谱纯.其它试剂均为分析纯,实验用水为二次蒸馏水,所有试剂溶液使用前均经0.45μm微孔滤膜过滤。
四、实验步骤1、流动相的配制用移液管吸取1.18 mL的质量分数85%的磷酸(西安化学试剂厂XK130201-0257-007(2))于2000 mL的烧杯中加超纯水至1000ml摇匀,定容,配制成浓度为0.1%的磷酸溶液。
将配制好的溶液装入两个棕色瓶中,备用。
用100ml的量筒量取0.1%的磷酸75ml,再用250ml的量筒量取色谱纯甲醇425ml,将甲醇加入磷酸中,摇匀,配制成甲醇-0.1% H3PO4 (85:15.V/V),然后用超声清洗机(宁波新芝生物科技股份有限公司)超声处理一个小时。
2、对照品和样品溶液的配制对照品的制备:用分析天平精确称取芦荟大黄素0.0043g,大黄酸0.0044g,大黄素0.0050g,大黄酚0.0050g和大黄素甲醚0.0030g,分别用色谱纯甲醇溶解(若难溶或溶解很慢,可超声处理几分钟),并定容至50ml,配制成浓度分别为0.086g/l,0.044g/l,0.1g/l,0.1g/l和0.060g/l的甲醇储备液,置于阴暗处保存。
实验三 水中氯离子的测定-沉淀滴定法和电位滴定法

实验三、水中氯离子的测定(沉淀滴定法和电位滴定法)1.沉淀滴定法此法依据《水质氯化物的测定硝酸银滴定法》(GB 11896-89)一、实验目的和要求学习银量法测定氯含量的原理和方法;掌握AgNO3标准溶液的配制和标定方法。
二、实验原理在中性至弱碱性范围内(pH6.5—10.5),以铬酸钾为指示剂,用硝酸银滴定氯化物时,由于氯化银的溶解度小于铬酸银的溶解度,氯离子首先被完全沉淀出来后,然后铬酸盐以铬酸银的形式被沉淀,产生砖红色,指示滴定终点到达。
该沉淀滴定的反应如下:Ag++Cl—→AgCl↓2Ag++CrO4→Ag2CrO4↓(砖红色)三、实验仪器和设备(1)锥形瓶,250mL;(2)滴定管,25mL,棕色;(3)移液管,10mL,25mL,50mL;(4)容量瓶,100mL,1000mL。
四、实验试剂和材料分析中仅使用分析纯试制及蒸馏水或去离子水。
(1)氯化钠标准溶液,C(NaCl)=0.0141mol/L,相当于500mg/L氯化物含量:将氯化钠(NaCl)置于瓷坩埚内,在105℃下烘干2h。
在干燥器中冷却后称取8.2400g,溶于蒸馏水中,在容量瓶中稀释至1000mL。
用移液管吸取10.0mL,在容量瓶中准确稀释至100mL。
1.00mL此标准溶液含0.50mg氯化物(C1-)。
(2)硝酸银标准溶液,C(AgNO3)=0.0141mol/L:称取2.3950g于105℃烘半小时的硝酸银(AgNO3),溶于蒸馏水中,在容量瓶中稀释至1000mL,贮于棕色瓶中。
用氯化钠标准溶液(1)标定其浓度:用移液管准确吸取25.00mL氯化钠标准溶液于250mL或100mL锥形瓶中,加蒸馏水25mL。
另取一锥形瓶,量取蒸馏水50mL作空白。
各加入1mL铬酸钾溶液(3),在不断的摇动下用硝酸银标准溶液滴定至砖红色沉淀刚刚出现为终点。
计算每毫升硝酸银溶液所相当的氯化物量,然后校正其浓度,再作最后标定。
1.00mL 此标准溶液相当于0.50mg氯化物(C1—)。
电位滴定法测定硫酸铜槽液中氯离子含量

滴定水份应用报告A-T-CN(sh)-电位滴定法测定电镀铜槽液中氯离子含量应用领域:电镀关键词氯离子/809/银电极摘要Ag电极经电镀上Ag2S(或AgCl)后用于强酸性环境下氯离子的滴定分析样品硫酸铜槽液试剂- 滴定剂:AgNO3溶液c=0.1mol/L- 氯化钠(AR)- 5mol/L 硝酸溶液- D.I. 水仪器及附件Titrando 809 2.809.0010801 Stirrer 2.801.0010800 Dosino 2.800.0010Dosing unit 6.3032.220Electrode with Ag2S coating 6.0430.100Electrode cable 6.2104.020分析0.1mol/L AgNO3标定滴定参数Parameters DETU>titration parametersmeas.pt.density 4Dos.rate max.ml/minsignal drift 50 mV/minMin waiting time 0sMax waiting time 26stemperature 25.0 °C>stop conditionsstop V 10mlStop measured value offstop EP 1Stop after EP 1.5mlPotentiometricEvaluationEP Criterion 5EP Recognition Greatest分析步骤取100ml干燥烧杯,准确称取约0.04g 经烘干处理的氯化钠,分别加入60ml DI水中、1ml 硝酸溶液,用0.1mol/L AgNO3溶液滴定至电位突跃点。
计算AgNO3(mol/L)=Sample size×1000/58.44/EP1样品测试滴定参数Parameters DETU>titration parametersmeas.pt.density 2Dos.rate max.ml/minsignal drift 20 mV/minMin waiting time 0sMax waiting time 38stemperature 25.0 °C>stop conditionsstop V 10mlStop measured value offstop EP 1Stop after EP 1.5ml PotentiometricEvaluationEP Criterion 5EP Recognition Greatest分析步骤将0.1mol/L AgNO3用容量瓶定量稀释10倍待用。
使用自动电位滴定仪测定水中氯离子含量.

使用自动电位滴定仪测定水中氯离子含量和COD Mn值1.相关标准《GB/T 13025.5-2012 制盐工业通用试验方法氯离子的测定》《GB/T 15453-2008 工业循环冷却水和锅炉用水中氯离子的测定》《GB/T 24890-2010 复混肥料中氯离子含量的测定》《NY/T 1121.17-2006 土壤检测第17部分:土壤氯离子含量的测定》《MT/T 201-2008 煤矿水中氯离子的测定》《ASTM D4458-2009 半咸水、海水和盐水中氯离子的试验方法》2.测量原理样品溶液调至中性,用硝酸银标准溶液滴定溶液,通过离子选择性电极的电位突变指示终点。
3.仪器设备实验仪器:ZDJ-5型自动滴定仪,或其他型号自动电位滴定仪。
实验电极:216-01型银电极+217-01型参比电极(二级参比填充液:饱和硝酸钠溶液)。
其他一般实验室仪器。
4.试剂和溶液4.10.01mol/L氯化钠标准溶液:称取0.5844克已于600℃灼烧至恒重的氯化钠基准试剂,溶解于去离子水中,移入1000ml容量瓶中,并用水稀释至刻度,摇匀。
氯化钠标准溶液的浓度按式(1)计算:(1)式中:c(NaCl),氯化钠标准溶液的浓度,单位为摩尔每升(mol/L);m,称取氯化钠的质量,单位为克(g)V,配制溶液的体积,单位为升(L)4.20.01mol/L硝酸银溶液:称取1.70克分析纯的硝酸银,溶解于去离子水中,移入1000ml容量瓶中,并用水稀释至刻度,摇匀,溶液保存在棕色瓶中。
5.操作过程5.1仪器准备,参照ZDJ-5或其他型号自动滴定仪说明书5.2参数设置(推荐参数)最小滴定体积:0.02ml。
最大滴定体积:0.2ml,预滴定突跃量:中,80mV。
5.3氯化钠标准溶液的标定:吸取10.00 ml 氯化钠标准溶液,置于150 ml 烧杯中,使用硝酸银溶液滴定,同时需进行空白实验。
硝酸银溶液的浓度按式(2)计算:(2)式中:c(AgNO3),硝酸银滴定剂的浓度,单位摩尔每升(mol/L)c(NaCl),氯化钠标准溶液的浓度,单位摩尔每升(mol/L)V1,吸取氯化钠标准溶液的体积,单位毫升(ml)V2,硝酸银滴定剂的用量,单位毫升(ml)V0,空白试验硝酸银标准滴定溶液的用量,单位毫升(ml)5.4用移液管吸取分析样品20ml于反应杯中,加入30ml去离子水,加入搅拌子,放在搅拌器上,将电极及滴液管插入溶液,开始对样品进行滴定。
电解液氯离子检测操作

氯离子检测简要操作1目的:本指示规定了电解液中的氯离子测试细则。
2适用范围:适用于电解液中的氯离子测试。
3职责:测试负责人对员工进行岗位培训与技术指导,并对来样测试结果的准确性负责。
4 操作准备:镀硫Ag-AgC l电极、50mL烧杯、25mL量筒、转子、3mL吸管、天平、手套、口罩;5设备参数:仪器型号:905 Titrando电位滴定仪;试剂:0.002mol/L AgNO3溶液、异丙醇、2mol/L硝酸;6工艺参数:6.1引用标准:6.2分析原理:Ag+会与Cl-发生定量反应:Ag+ + Cl-→AgCl↓,在滴定过程中样品中的Cl-不断消耗,浓度不断降低,对Cl-浓度有选择性感应的镀硫Ag-AgCl电极的电位值也不断降低,随着滴定的进行,在接近等当点时样品中的Cl-浓度成指数级变化,随之电极的电位值会出现突越变化,对其电位值与滴定体积的曲线求导,得出的导数曲线与原曲线叠加,可以发现导数曲线在电位值突越区间内会有一个突越峰,该突越峰对应的滴定体积数即为等当点体积,根据等当点体积可以换算出Cl-的浓度。
7程序\操作指示7.1 tiamo 2.4软件的方法参数编辑7.1.2建立数据库点击“数据库”选项,在“文件”选项中选择“数据库管理器”,在其窗口中点击“编辑”,在下拉菜单中选择“新建”,输入数据库名称为“Cl-”,点“OK”保存,随后弹出的属性窗口中可以编辑该数据库的评注,如“氯离子检测数据”,点“OK”确定。
7.1.3新建检测方法打开tiamo 2.4电位滴定软件,依次点击“方法”→“文件”→“新建”→“滴定”→“动态点位滴定(DET U)”→“OK”确定新建方法。
7.3设定方法参数1)右击“DET U”选择“属性”(或者双击“DET U”)在“常规/硬件”选项中选择设备名为“905 1”,配液器与测量输入为“2”,传感器选择“ISE electrode”,搅拌器选择“1”,搅拌速度为“5”。
电位滴定法测定水中氯离子的含量

电位滴定法测定水中氯离子的含量1 / 1 电位滴定法测定水中氯离子的含量一 实验目的:学习电位滴定法的基本原理和操作技术 掌握了解氯离子的测定过程和现象 二 实验原理 利用滴定分析中化学计量点附近的突跃,以一对适当的电极对监测滴定过程中的电位变化,从而确定滴定终点,并由此求得待测组分的含量的方法称为电位滴定法。
本实验根据Nerst 方程E = E θ- RT/nF lgC Cl- ,滴定过程中, Cl - + Ag + = AgCl ↓,使得氯离子浓度降低,电位发生改变,接近化学计量点时,氯离子浓度发生突变,电位相应发生突变,而后继续加入滴定剂,溶液电位变化幅度减缓。
以突变时滴定剂的消耗体积(mL )来确定滴定终点(AgNO 3标准溶液的体积)。
三 仪器和试剂 酸度计(mv 计),磁力搅拌器,转子。
KNO 3甘汞参比电极,银电极,滴定管,烧杯(电解池),0.05mol·L -1NaCl ,0.05mol·L -1AgNO 3,KNO 3固体 四 实验内容和步骤 1 0.05mol·L -1AgNO 3标准溶液的标定 准确移取0.05mol.L -1NaCl 标准溶液10.00mL 于烧杯中,加蒸馏水20mL ,KNO 3固体2g ,搅拌均匀。
开启酸度计,开关调在mv 位置,加入滴定剂,记录溶液电位随滴定剂的体积变化情况。
随着AgNO 3标准溶液的滴入,电位读数将不断变化,读数间隔可先大些(1-2mL ),至一定量后,电位读数变化较大,则预示临近终点,此时应逐滴加入AgNO 3标准溶液(0.5-0.2mL ),并记录电位变化,直至继续加入AgNO 3标准溶液后电位变化不再明显为止。
做E(mv)-V(mL)曲线,求得终点时所消耗AgNO 3标准溶液的确切体积。
2水中氯离子含量的测定 准确移取水样10.00mL 于烧杯中,加蒸馏水20mL ,KNO 3固体2g ,搅拌均匀。
仪器分析期末综合复习题

仪器分析期末综合练习题●习题精选一、选择题1.以下四种化合物,能同时产生B吸收带、K吸收带和R吸收带的是()A. CH2CHCH OB. CH C CH OC. OCH3D.CH CH22.在下列化合物中,π→π*跃迁的吸收波长最大的化合物是()A. 1,3-丁二烯B. 1,4-戊二烯C. 1,3-环已二烯D. 2,3-二甲基-1,3-丁二烯3.符合朗伯特-比耳定律的有色溶液稀释时,其最大吸收峰的波长位置()A. 向短波方向移动B. 向长波方向移动C. 不移动,且吸光度值降低D. 不移动,且吸光度值升高4.双波长分光光度计与单波长分光光度计的主要区别在于()A. 光源的种类及个数B. 单色器的个数C. 吸收池的个数D. 检测器的个数5.在符合朗伯特-比尔定律的范围内,溶液的浓度、最大吸收波长、吸光度三者的关系是()A. 增加、增加、增加B. 减小、不变、减小C. 减小、增加、减小D. 增加、不变、减小6.双波长分光光度计的输出信号是()A. 样品吸收与参比吸收之差B. 样品吸收与参比吸收之比C. 样品在测定波长的吸收与参比波长的吸收之差D. 样品在测定波长的吸收与参比波长的吸收之比7.在紫外可见分光光度法测定中,使用参比溶液的作用是()A. 调节仪器透光率的零点B. 吸收入射光中测定所需要的光波C. 调节入射光的光强度8.在原子发射光谱中,通常作为元素定性的标准光谱是()。
A、铁光谱B、钙光谱C、镁光谱D、铜光谱9.下列基团或分子中,能发生π→π*跃迁的基团是()A. C=CB. C=OC. C≡ND. CH3OH10、火焰原子吸收光谱法常用的光源是( )A、空心阴极灯B、钨灯C、氘灯D、硅碳棒11、在原子吸收分析中, 过大的灯电流除了产生光谱干扰外, 还使发射共振线的谱线轮廓变宽. 这种变宽属于( )A.自然变宽B.压力变宽C.场致变宽D.多普勒变宽(热变宽)12、C2H2-Air火焰原子吸收法测定较易氧化但其氧化物又难分解的元素(如Cr)时,最适宜的火焰是性质()A.化学计量型B.贫燃型C.富燃型D.明亮的火焰13、在电动势的测定中盐桥的主要作用是( )A.减小液体的接界电势B.增加液体的接界电势C.减小液体的不对称电势D.增加液体的不对称电势14、pH玻璃电极的内参比电极是( )A. 甘汞电极B. 银-氯化银电极C. 铂电极D. 玻璃电极15、在电位分析法中,离子选择性电极的电位与待测离子浓度()A.成正比B.成反比C.符合能斯特方程D.对数成正比16、衡量色谱柱选择性的指标是( )A、理论塔板数B、分配比C、相对保留值D、分配系数17、速率理论方程H=A+B/u+Cu,式中组分分子在色谱柱中通过的路径有关的项是()A、传质阻力项B、分子扩散项C、涡流扩散项D、径向扩散项18、不能采用原子发射光谱分析的物质是()A、碱金属B、稀土金属C、大部分非金属元素D、过渡金属19、原子吸收光谱法是基于气态原子对光的吸收符合(),即吸光度与待测元素的含量成正比而进行分析检测的。
硫酸铜电解液中氯离子的电位滴定

硫酸铜电解液中氯离子的电位滴定引言:电位滴定是一种常用的分析方法,通过测定溶液中某种物质的电位变化来确定它的浓度。
其中,硫酸铜电解液中氯离子的电位滴定是一种重要的分析方法,可以用于测定溶液中氯离子的浓度。
本文将详细介绍硫酸铜电解液中氯离子的电位滴定原理、实验步骤以及注意事项。
一、硫酸铜电解液中氯离子的电位滴定原理硫酸铜电解液中氯离子的电位滴定是基于电位滴定的原理进行的。
电位滴定是一种基于电极电位变化的分析方法,根据滴定过程中电位的变化来确定被测物质的浓度。
在硫酸铜电解液中,氯离子与硫酸铜溶液中的铜离子发生氯化反应,生成氯化铜。
氯化反应的电位变化可以通过电位滴定仪器进行测定,从而确定溶液中氯离子的浓度。
二、硫酸铜电解液中氯离子的电位滴定实验步骤1. 实验前准备:将硫酸铜固体溶解于适量的蒸馏水中,制备出一定浓度的硫酸铜电解液。
同时,准备好滴定仪器和氯离子指示剂。
2. 滴定操作:将待测溶液与硫酸铜电解液混合,在滴定过程中加入适量的氯离子指示剂。
当氯离子与硫酸铜溶液中的铜离子反应完全时,指示剂的颜色会发生明显变化,表示滴定结束。
在滴定过程中,使用电位滴定仪器实时记录溶液的电位变化。
3. 数据处理:根据滴定过程中记录的电位变化数据,绘制电位-体积曲线。
通过曲线上的拐点,确定滴定终点,进而计算出氯离子的浓度。
三、硫酸铜电解液中氯离子的电位滴定注意事项1. 实验中要保证滴定仪器的清洁和准确性,避免仪器污染或误差。
2. 在滴定过程中,氯离子指示剂的加入应适量,以避免过量或不足导致滴定结果的偏差。
3. 滴定过程中应注意控制滴定速度,避免滴定过快或过慢导致实验结果不准确。
4. 实验操作中要注意安全,避免接触有害物质或发生意外。
结论:硫酸铜电解液中氯离子的电位滴定是一种常用的分析方法,可以用于测定溶液中氯离子的浓度。
通过对硫酸铜电解液中氯离子的电位滴定实验的介绍,我们了解到了该方法的原理、实验步骤以及注意事项。
在实际应用中,我们可以根据该方法快速准确地测定溶液中氯离子的浓度,为相关领域的研究和应用提供有效的数据支持。
分析试验答案(部分)

邻二氮菲分光光度法测定铁(基本条件实验)1.用邻二氮菲测定铁时,为什么要加入盐酸羟胺?其作用是什么?试写出有关反应方程式。
答:工业盐酸中含有Fe2+和Fe3+,其中Fe2+与邻二氮菲(phen)能生成稳定的桔红色配合物[Fe(phen)3]2+此配合物的lgK稳=21.3,摩尔吸光系数ε510 =1.1×104L·mol-1·cm-1,而Fe3+能与邻二氮菲生成3∶1配合物,呈淡蓝色,lgK稳=14.1。
所以在加入显色剂之前,应用盐酸羟胺(NH2OH·HCl)将Fe3+还原为Fe2+,然后,进行铁的总量的测定。
反应方程式为:NH2OH·HCl==NH2OH+HCl2Fe 3+ + 2NH2OH = 2Fe 2+ + N2↑ + 2H2o + 2H+2.根据有关实验数据,计算邻二氮菲一Fe(Ⅱ)络合物在选定波长下的摩尔吸收系数。
答:ε=1.1*1043.在有关条件实验中,均以水为参比,为什么在测绘标准曲线和测定试液时。
要以试剂空白溶液为参比?答:试剂空白不止含有水,而还含有其他东西,比如无机盐,缓冲液等,而这些东西都有吸光值,该实验测定的是二价铁离子,所以空白试剂必须把样品中除了二价铁离子以外的有吸光值的物质因素扣除,而用水的话就没有考虑这些杂质,算出来的其实是二价铁离子加上其他有吸光值的物质的总吸光值邻二氮菲分光光度法测定铁(测定实验)铝合金中铜的测定火焰原子吸收光谱法灵敏度和自来水中镁的测定1.为什么空气、乙炔流量会影响吸光度的大小?答:吸光度的大小实际上是与待测元素的基态原子数成正比的,后者取决于燃气流速、火焰温度、燃气与助燃气比例等因素有关;火焰原子化中常用的就是空气-乙炔火焰,所以它们的流量会影响吸光度的大小2.为什么要配制钙、镁标准溶液?所配制的钙、镁系列标准溶液可以放置到第二天使用吗?为什么?自来水中含氟量的测定1.本实验中加入总离子强度调节缓冲溶液的目的是什么?2.为什么要把氟电极的空白值洗至-220mV?硫酸铜电解液中氯离子的电位测定1.用硝酸银滴定氯离子时,是否可以用碘化银作指示电极?答:不能。
电位滴定法测定氯离子浓度

2018/10/13
讨论和拓展学习
1.探索在实验中,哪些因素容易造成误差?如何能提 高实验的准确度? 2.取硫酸铜电解液、锅炉水及卤离子混合液等样品进 行分析测试。
2018/10/13
一、实验目的
1.学习电位滴定法的基本原理和实验操作。
2. 掌握电位滴定中数据的处理方法。
2018/10/13
二、实验原理
电位滴定法是在用标准溶液滴定待测离子过程中,用 指示电极的电位变化代替指示剂的颜色变化指示滴定终点的
到达,是把电位测定与滴定分析互相结合起来的一种测试方
法,它虽然没有指示剂确定终点那样方便,但它可以用在浑 浊、有色溶液以及找不到合适指示剂的滴定分析中。电位滴 定的一个很大用途是可以连续滴定和自动滴定。
2018/10/13
三、仪器和试剂
1. ZD—2型自动电位滴定仪
2. Ag电极、双盐桥饱和甘汞电极
3. 容量瓶 (100mL)
4. 移液管 (25mL、 50mL)
5. 烧杯(250mL)、搅拌子与洗瓶等 6. 7.
2018/10/13
NaCl标准溶液(0.0500mol/L) 0.05 00moL/L 的AgNO3溶液 (待标定)
2018/10/13
五、实验数据及处理
1.根据自动电位滴定的数据,绘制电位(E)对滴 定体积(V)的滴定曲线,通过E—v曲线确定终 点电位和终点体积(由次体积可算出硝酸银溶 液的准确浓度)。
C NaCl mol / L C AgNO
3
V AgNO
V
NaCl
3
2018/10/13
2.根据滴定终点(自动电位滴定)所消耗的AgNO3溶 液体积计算试液中Cl—的质量浓度(mg/L)
铜电解液中氯离子含量的测定(电位滴定法)

电位突跃代替了指示剂的变色 准确度提高/适用范围更广/自动化
(二)方法提要
用电解法精炼铜的电解液所含的氯离子,可根据以下反应在酸性介质中以硝酸银为滴定剂,用容量法滴定:Cl¯ + Ag+ = AgCl 由于电解液具有颜色,不能用指示剂指示颜色的变化来确定终点,应采用电位滴定法为宜。滴定时以银电极为指示电极,饱和甘汞电极为参比电极,用电位计或pH计或ZD-4型自动电位滴定仪,测量电极间的电位差,在滴定终点时,产生电位突跃,可由作图法或导数计算法确定滴定终点,也可用预控制的化学计量点电位,采用自动控制电位滴定仪进行滴定。
确定滴定终点的方法:E-V曲线法
3、移取10.00 mL铜电解液于滴定杯中,加水约20 mL,加1~2滴HNO3,把滴定杯安装在仪器上,在自动滴定模式下,用AgNO3标准溶液滴定铜电解液,根据AgNO3标准溶液的浓度和体积,求出铜电解液中Cl- 的浓度。
(四)实验步骤
1、把指示电极安装在仪器电极插口2上,参比电极安装在电极插口负极上,把吸液管插入0.1 mol·L-1AgNO3溶液中,开ZDJ-4A型自动电位滴定仪电源开关,在仪器处于准备状态时,按clean键清洗滴定管三次。
2、移取10.00 mL 0.1000 mol.L-1NaCl标准溶液于滴定杯中,加水约20 mL,加1~2滴HNO3,把滴定杯安装在仪器上,在手动滴定模式下,滴加AgNO3溶液,记录电极电位,当电位变化后,每次滴入0.10 mL AgNO3, 滴过计量点后,再滴入5 mL, 以AgNO3体积为横坐标,电位为纵坐标,作工作曲线,从工作曲线上找出计量点时AgNO3溶液的体积,根据NaCl标准溶液的浓度和体积,计算AgNO3溶液的准确浓度。
采用电位滴定仪测定含氯量方法的探讨

采用电位滴定仪测定含氯量方法的探讨1. 引言1.1 研究背景引言:在工业生产和环境监测中,准确测定含氯物质的量是至关重要的。
氯是一种常见的化学元素,广泛存在于洗涤剂、消毒剂、汽油等物质中。
在一些情况下,氯的含量过高可能会对人体健康和环境造成危害。
开发一种简便、准确的测定含氯量的方法成为了当今科研领域的重要课题之一。
目前,常用的测定含氯量的方法包括滴定法、光度法和电位滴定法。
滴定法需要使用显色剂,存在误差较大的可能;光度法对样品的处理要求较高,操作复杂;而电位滴定法则具有快速、准确的特点,被广泛应用于含氯物质的测定中。
本研究旨在探讨采用电位滴定仪测定含氯量的方法,通过了解电位滴定仪的原理和含氯物质的测定方法,以及实验步骤和结果分析,来评估其在实际应用中的可行性和优缺点,为今后的含氯量测定工作提供参考依据。
1.2 研究意义研究含氯物质的测定方法在工业生产、环境监测以及食品安全等领域具有重要意义。
含氯物质在实际生产和使用中广泛存在,其含量的准确测定对于保障产品质量和人类健康至关重要。
现有测定方法存在着诸多局限性,如对操作者技术要求高、测定时间长、且存在一定的误差等问题。
寻找一种快速、准确且简便的含氯量测定方法具有重要意义。
2. 正文2.1 电位滴定仪的原理电位滴定仪是一种常用于测定溶液中氯离子含量的仪器。
其原理基于电化学方法。
通常情况下,电位滴定仪由一个工作电极、一个参比电极和一个计量、控制系统组成。
工作电极通常是一个易氧化的金属电极,如银电极,参比电极则是一个稳定的电位电极,如饱和甘汞电极。
在测定氯离子含量时,首先将待测溶液与适量的标准氯化银溶液进行反应,生成沉淀,并通过对溶液中的氯离子进行电位滴定的方法,测定出溶液中氯离子的浓度。
在实际应用中,还需要考虑到电位滴定仪的参数设置、校准和数据处理等问题,以确保测定结果的准确性和可靠性。
电位滴定仪具有操作简便、准确度高、测定范围广等优点,因此在测定含氯量方面具有很大的应用价值。
自动电位滴定方法测定硫酸铜中低浓度氯离子含量

自动电位滴定方法测定硫酸铜中低浓度氯离子含量范小玲;谢金平【摘要】介绍使用自动电位滴定法测定硫酸铜中低浓度氯离子浓度含量,结果表明,该方法与国家标准所推荐的比浊法比较,具有误差小、可以定量检测的优点.【期刊名称】《印制电路信息》【年(卷),期】2016(024)006【总页数】3页(P53-55)【关键词】自动电位滴定;硫酸铜;氯离子;印制电路板【作者】范小玲;谢金平【作者单位】广东致卓精密金属科技有限公司,广东佛山528247;广东致卓精密金属科技有限公司,广东佛山528247【正文语种】中文【中图分类】TN41印制电路板制造工艺中的酸性硫酸盐镀铜体系,具有镀液稳定、控制方便等特点。
镀液工艺控制指标中,氯离子浓度是重要管控指标之一。
氯离子浓度太高、太低都对镀铜质量及阳极产生不良影响,直接影响PCB质量。
硫酸铜作为酸性硫酸盐镀铜体系的开缸原料或用于镀缸调节铜离子补料,纯度较高的硫酸铜其氯离子含量很低;但是硫酸铜氯离子的含量的多少,直接影响到镀铜体系氯离子含量的高低,将可能直接影响到镀铜质量的好坏。
国家标准GB/ T665-2007,行业标准HG/T3592-2007用比浊法进行检测,但是存在定量误差较大问题。
于自动电位滴定仪上,用硝酸银标准滴定溶液,以银电极做指示电极,通过沉淀滴定测定氯化物。
1.1 自动电位滴定法1.1.1 试剂和仪器(1)硝酸溶液:500 ml/L。
(2)硝酸银标准滴定溶液:c(AgNO3)=0.01 mol/L。
(3)自动电位滴定仪;瑞士万通METORHM 848。
(4)银电极。
1.1.2 分析步骤称取20 g硫酸铜样品(精确至0.000 1 g)于150 mL烧杯中,加80 mL水,加热溶解,待冷却,加入5 mL硝酸溶液,然后将该烧杯置于自动电位滴定仪的滴定台上,移下滴定架,以银电极做指示电极,用硝酸银标准滴定溶液于DET(动态等当点滴定)滴定模式下进行滴定,直至出现终点。
硫酸铜电解液中氯离子的电位滴定

硫酸铜电解液中氯离子的电位滴定一、实验目的1、学会电位滴定法的基本原理,掌握硫酸铜电解液中氯离子含量的测定方法;2、了解ZD-2自动电位滴定仪和JB-1A滴定装置的构造,学会手动和自动滴定法;3、掌握用E-V、△E/△V-V、△2E/△V2-V曲线确定滴定终点的方法,并确定滴定终点电位值;4、根据滴定剂AgN03标准溶液的用量,计算硫酸铜电解液中氯离子的含量g/L和mol/L;二、实验原理以AgN03标准溶液为滴定液,其滴定反应为Ag++C1-=AgCl↓银电极作指示电极,双盐桥饱和甘汞电极217型作参比电极,组成原电池;滴定过程中,银电极的电位随溶液中C1-或Ag+的浓度的变化而变化,化学计量点前,银电极的电位决定于Cl-浓度:E=E0AgCl/Ag-0592lgCl-化学计量点后,银电极的电位决定于Ag+浓度:E=E0Ag+/Ag+Ag+在化学计量点附近,由于C1-或Ag+浓度发生突变,致使银电极的电位发生突变;滴定终点可由电位滴定曲线来确定;即E-V曲线突跃中点、一次微商△E/△V-V曲线△E/△V最大点、二次微商△2E/△V2-V曲线△2E/△V2=0点;氯离子含量mol/L CAgN03VAgN03/=氯离子含量g/L CAgN03VAgN03×MCl-/=三、仪器与试剂1、仪器:ZD-2型自动电位滴定仪;JB-1A型搅拌器;酸式棕色滴定管lOmL 银电极216型;饱和甘汞电极217型双盐桥;2、试剂:AgN03标准溶液L;硫酸铜电解液含氯离子;KNO3溶液L;四、实验步骤1、仪器的组装及准备将银电极右和饱和甘汞电极左,盐桥套管内装2/3的KNO3溶液装在搅拌器滴定装置的电极夹上,并将银电极接在滴定仪的电极插口上,饱和甘汞电极接在滴定仪的接地接线柱上;将滴定仪的“pH/mV”开关置“mV”,将“功能”开关置“手动”,“设置”开关置“测量”;打开ZD-2型滴定仪和JB-1A型搅拌器的电源开关,预热15分钟;2、手动滴定准确吸取硫酸铜电解液,置于150mL烧杯中,加水约25mL,放搅拌磁子,置于搅拌器上;将两电极浸入试液,开启搅拌器,读取初始电位;将滴定管下端连接一带毛细管的细胶管,装上AgN03标准溶液,调节好面后,一边搅拌,按下“开始滴定”按钮,开始滴定,每加入一定体积的AgN03溶液,放开“开始滴定”按钮,记录一次电位值E;开始滴定时,每次可加;当到达化学计量点附近时化学计量点前后约,每次加;过了化学计量点后,每次仍加,一直滴定到;3、自动滴定根据手动滴定曲线△2E/△V2-V曲线可求得终点电位;以此电位值为控制依据,进行自动滴定;1终点设定“设置”开关置“终点”,“功能”开关置“自动”,调节“终点电位”旋钮,使显示屏显示终点电位值;2预控制点设定“设置”开关置“预控点”,调节“预控点”旋钮,使显示屏显示“100mV”; 然后将“设置”开关置“测量”;3准确吸取硫酸铜电解液,置于150mL烧杯中,加水约25mL,放搅拌磁子,置于搅拌器上;将两电极浸入试液;将滴定管装上AgN03标准溶液,调节好液面后,开启搅拌器,按下“滴定开始”按钮,开始滴定;待“终点”灯亮后,读取滴定管读数;五、数据记录和结果处理1E-V曲线2△E/△V-V曲线3△2E/△V2-V曲线3、含量计算由自动滴定确定终点时,VAgN03= mL,而CAgN03=L,则硫酸铜电解液中氯离子的含量为 mol/L和 g/L;。
电位滴定法测定氯离子浓度及AgCl的KspPPS
]
3.终点确定方法(作图法):
三、实验内容
① 2 0 .0 0 m L 水 样 溶 液 ( 100m L烧 杯 )
② 5 0 .0 0 m L 蒸 馏 水 ( 100m L烧 杯 ) 5D 6M HN O 3 0 .5 g B a ( N O 3 ) 2
2 5 .0 0 m L H 2 O
3D 6M HN O 3 0 .5 g B a ( N O 3 ) 2
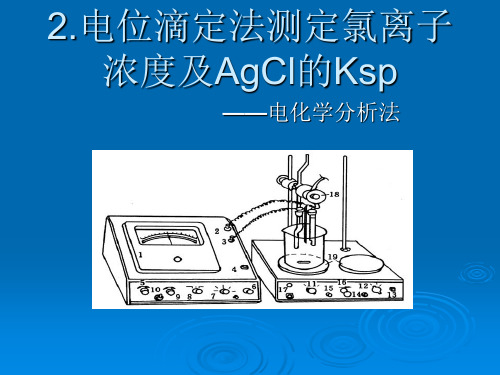
——电化学分析法
一、实验目的
1.掌握电位滴定法测量离子浓度的一般原理; 2.学会用电位滴定法测定难溶盐的溶度积常数。
二、实验原理
1.原电池:
甘汞电极(参比电极)ㄧ待测溶液ㄧ银电极(指示电极)
银电极电极电势: 原电池电动势:
( Ag , Ag ) ( Ag , Ag )
E K RT nF ln a ( Ag
法有何特点? 2. 如何计算滴定反应的理论电位值?
三实验内容5000ml蒸馏水100ml烧杯5d6mhno305gbano32搅拌滴定记录ve2000ml水样溶液100ml烧杯2500mlh2o3d6mhno305gbano32搅拌滴定记录ve四数据记录与处理一水样测定二elgag关系的确定三结果计算已知cagno3moll注
2.电位滴定法测定氯离子 浓度及AgCl的Ksp
搅拌 滴定 记 录 V、 E
搅拌 滴定
记 录 V、 E
四、数据记录与处理
( 一 ) 水 样 测 定 ( 二 ) E~lg[Ag+]
关 系 的 确 定
(三)结果计算(已知c(AgNO3)=
mol/L
注: 应用内插法确定终点V (AgNO3)பைடு நூலகம்终点电位E
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硫酸铜电解液中氯离子
的电位滴定
Document number:NOCG-YUNOO-BUYTT-UU986-1986UT
硫酸铜电解液中氯离子的电位滴定
一、实验目的
1、学会电位滴定法的基本原理,掌握硫酸铜电解液中氯离子含量的测定方法。
2、了解ZD-2自动电位滴定仪和JB-1A滴定装置的构造,学会手动和自动滴定法。
3、掌握用E-V、△E/△V-V、△2E/△V2-V曲线确定滴定终点的方法,并确定滴定
终点电位值。
4、根据滴定剂AgN03标准溶液的用量,计算硫酸铜电解液中氯离子的含量(g/L和mol/L)。
二、实验原理
以AgN03标准溶液为滴定液,其滴定反应为Ag++C1-=AgCl↓
银电极作指示电极,双盐桥饱和甘汞电极(217型)作参比电极,组成原电池。
滴定过程中,银电极的电位随溶液中C1-(或Ag+)的浓度的变化而变化,
化学计量点前,银电极的电位决定于Cl-浓度:E=E0AgCl/Ag-0592lg[Cl-]
化学计量点后,银电极的电位决定于Ag+浓度:E=E0Ag+/Ag+[Ag+]
在化学计量点附近,由于C1-(或Ag+)浓度发生突变,致使银电极的电位发生突变。
滴定终点可由电位滴定曲线来确定。
即E-V曲线(突跃中点)、一次微商△E/△V-V 曲线(△E/△V最大点)、二次微商△2E/△V2-V曲线(△2E/△V2=0点)。
氯离子含量(mol/L) C(AgN03)V(AgN03)/=
氯离子含量(g/L) C(AgN03)V(AgN03)×M Cl-/=
三、仪器与试剂
1、仪器:ZD-2型自动电位滴定仪;JB-1A型搅拌器;酸式(棕色)滴定管(lOmL) 银电极(216型);饱和甘汞电极(217型双盐桥)。
2、试剂:AgN03标准溶液L;硫酸铜电解液(含氯离子);KNO3溶液L。
四、实验步骤
1、仪器的组装及准备
将银电极(右)和饱和甘汞电极(左,盐桥套管内装2/3的KNO3溶液)装在搅拌器滴定装置的电极夹上,并将银电极接在滴定仪的电极插口上,饱和甘汞电极接在滴定仪的接地接线柱上。
将滴定仪的“pH/mV”开关置“mV”,将“功能”开关置“手动”,“设置”开关置“测量”。
打开ZD-2型滴定仪和JB-1A型搅拌器的电源开关,预热15分钟。
2、手动滴定
准确吸取硫酸铜电解液,置于150mL烧杯中,加水约25mL,放搅拌磁子,置于搅拌器上。
将两电极浸入试液,开启搅拌器,读取初始电位。
将滴定管下端连接一带毛细管的细胶管,装上AgN03标准溶液,调节好面后,一边搅拌,按下“开始滴定”按钮,开始滴定,
每加入一定体积的AgN03溶液,放开“开始滴定”按钮,记录一次电位值E。
开始滴定时,每次可加;当到达化学计量点附近时(化学计量点前后约,每次加;过了化学计量点后,每次仍加,一直滴定到。
3、自动滴定
根据手动滴定曲线(△2E/△V2-V曲线)可求得终点电位。
以此电位值为控制依据,进行自动滴定。
(1)终点设定“设置”开关置“终点”,“功能”开关置“自动”,调节“终点电位”旋钮,使显示屏显示终点电位值。
(2)预控制点设定“设置”开关置“预控点”,调节“预控点”旋钮,使显示屏显示“100mV”。
然后将“设置”开关置“测量”。
(3)准确吸取硫酸铜电解液,置于150mL烧杯中,加水约25mL,放搅拌磁子,置于搅拌器上。
将两电极浸入试液。
将滴定管装上AgN03标准溶液,调节好液面后,开启搅拌器,按下“滴定开始”按钮,开始滴定。
待“终点”灯亮后,读取滴定管读数。
五、数据记录和结果处理
(1)E-V曲线
(2)△E/△V-V曲线
(3)△2E/△V2-V曲线
3、含量计算由自动滴定确定终点时,V(AgN03)= (mL),而C(AgN03)=L,则硫酸铜电解液中氯离子的含量为 mol/L和 g/L。
