河南省2019中考化学复习 第一部分 中考考点过关 第三单元 物质构成的奥秘(真题帮)检测
中考化学人教版 精练本 第一部分 考点过关练 第三单元 物质构成的奥秘

考点 3:原子的结构(每年必考) 7.(2022·宜昌)如图是硫的原子结构示意图。下列说法正确的是( B ) A.x 的值为 8 B.硫的原子核带 16 个单位正电荷 C.硫在元素周期表中位于第 6 周期 D.硫原子易得到电子,变成阳离子
8.(2022·恩施州)下列是四种粒子结构示意图,其中表示阳离子的是 ( B)
选项
宏观现象
微观解释
A
香水、汽油的气味不同
两者挥发出的微粒不同
B 湿衣服在阳光下比在阴凉处干得快 温度升高,分子运动加快
少量蔗糖放进水中后,很快就“消
C
蔗糖分子逐步向水里扩散
失”了
6 000 L 氧气在加压下可装入容积
D
压强增大,分子本身变小
为 40 L 的钢瓶中
6.★(2022·三市一企)如图是三种微粒的结构示意图,下列说法正确的
最最外外层电层子电数子相等数,相Ga等比,AlG多a比1 个A电l多子层1个,核电外子电层子层,越核多外,越电容子易失 去层 去电越 电子,多子金,,属越 金越 容 属易 越失活活泼泼。
(4)写出镓 Ga 与稀盐酸反应的化学方程式 22GaG+a+6HC6lH==C=l2=Ga==Cl23G+a3CHl23↑。 +3H2↑
14.(2022·荆州)如图为铕(Eu)元素在元素周期表中的信息以及氧和氯 的原子结构示意图。请回答:
(1)铕是一种重要的稀土资源,它属于金金属属(选填“金属”或“非金属”) 元素。 (2)铕原子中核外电子数为 6633 。 (3)氧元素和氯元素最本质的区别是质质子子数数不同。 (4)已知氯化铕的化学式为 EuCl3,则相同价态的铕的氧化物的化学式为 EEu2uO2O3 3。
脾。花香四溢的现象说明
(B)
初中化学知识点归纳:第三单元物质构成的奥秘

第三单元物质构成的奥秘第一节分子和原子二、验证分子运动的探究实验[实验操作]如右图,取适量的酚酞溶液,分别倒入A、B两个小烧杯中,另取一个小烧杯C,加入约5mL浓氨水。
用一个大烧杯罩住A、C两个小烧杯,烧杯B置于大烧杯外。
观察现象。
[实验现象]烧杯A中的酚酞溶液由上至下逐渐变红。
[实验结论]分子是不断运动的。
[注意事项]浓氨水显碱性,能使酚酞溶液变红。
浓氨水具有挥发性,能挥发出氨气。
三、从微观角度解释问题1.用分子观点解释由分子构成的物质的物理变化和化学变化物理变化:没有新分子生成的变化。
(水蒸发时水分子的间隔变大,但水分子本身没有变化,故为物理变化)化学变化:分子本身发生变化,有新分子生成的变化。
(电解水时水分子变成了新物质的分子,故为化学变化)2.纯净物和混合物(由分子构成的物质)的区别:纯净物由同种分子构成,混合物由不同种分子构成。
3.分子和原子的联系:分子是由原子构成的,同种原子结合成单质分子,不同种原子结合成化合物分子。
4.分子和原子的本质区别:在化学变化中,分子可以再分,而原子不能再分。
5.化学变化的实质:在化学变化过程中,分子裂变成原子,原子重新组合,形成新物质的分子。
四、 物质的组成 1. 宏观角度:水是由氢元素和氧元素组成的。
铁是由铁元素组成的。
2. 微观角度:水是由水分子构成的(水的化学性质由水分子保持)。
水分子由氢原子和氧原子构成。
1个水分子由2个氢原子和1个氧原子构成。
铁是由铁原子构成的(铁的化学性质由铁原子保持)。
3. 水在化学变化中的最小粒子是氢原子和氧原子。
4. 物质、元素用于宏观角度分析问题,分子、原子、离子用于在微观角度分析问题。
宏观和微观不可以混淆。
第二节 原子的构成1. 原子的构成原子一般是由质子、中子和电子构成,有的原子不一定有中子,质子数也不一定等于中子数。
原子的种类由核电荷数(质子数)决定。
2. 构成原子的各种粒子间的关系在原子中,原子序数=核电荷数=核内质子数=核外电子数。
第三章《物质构成的奥秘》中考复习

• 知识回顾 :
• 考点5 化合价与化学式
• 常见元素化合价(记口诀)
• 在化合物中,氢元素通常显 价,氧元素通常显 价。
• 2、用
表示纯净物组成的式子叫化学式。
• 1、化合物中,元素的正价与负价代数和为 ,据此可依据化 学式推断元素的化合价和根据化合价检查化学式书写是否正确。
• 2、根据 可计算相对分子质量,各元素的质量比及其某元 素的质量分数。
+17 2 8 7
+8 2 6
+19 2 8 8 1
+18 2 8 8
•
A.
B. C.
D.
二、典型题
• 例3.保持氢气化学性质的粒子是( )
• A H B H20 C H2 D 2H
• 例4.下列符号只有微观意义的是( )
A.Cl2 B.2N2
C.Cu D.CO2
• 例5. 由解放军某研究所研制的小分子团水是
• (A)Ti可以表示一个钛原子 (B)Ti4+核外有26个电子 • (C)TiO2中含有氧分子 (D)CaTiO3属于金属氧化物
• 例6. 由我国著名科学家、中国科学院院士张青莲教授主 持测定了铟、铱、锑、铕等几种元素的相对原子质量新 值,其中他测定核电荷数为63的铕元素的相对原子质量 的新值为152。则下列说法正确的是
(7)四个四氧化三铁分子(4Fe3O4) (8)3个亚铁离子(3Fe2+)
1. 某元素A的原子结构示意图为
该元素原子的核电荷数为 16
,
原子的最外层电子数是 6
,A属 非金属
元
素。(填金属、非金属或稀有气体),A原子通过得失电子而形成
的离子的符号是 S2-
初中九年级《化学》第三单元物质构成的奥秘重要知识点梳理

第三单元物质构成的奥秘1.分子(1)概念:分子是保持物质化学性质的最小粒子。
分子只能保持物质的化学性质,不能保持物理性质。
如冰、水、水蒸气的构成粒子都是H2O分子,它们的物理性质不同,但化学性质相同。
(2)性质:①分子很小(质量小、体积小);②分子在不停地运动(温度越高,分子能量越大,分子运动越快);③分子间有间隔[其他条件相同时,温度越高分子间隔越大(热胀冷缩的原因);压强越大分子间隔越小]。
物质挥发、扩散、溶解等现象说明分子在不停地运动。
酒精与水混合后的总体积比两者体积之和略小、气体易被压缩等现象说明分子间有间隔。
(3)构成:分子是由原子构成的(描述具体分子的构成时原子要具体化。
如果指明一个(或每个)分子,则后面原子也要根据化学式说明相应原子的个数)。
如水(H2O)可以描述为:“水分子是由氢原子和氧原子构成的”或“一个水分子是由两个氢原子和一个氧原子构成的”。
过氧化氢(H2O2)可以描述为:“过氧化氢分子是由氢原子和氧原子构成的”或“每个过氧化氢分子是由2个氢原子和2个氧原子构成的”。
(4)应用:由同种分子构成的物质是纯净物(如冰水共存物都是由H2O分子构成的,是纯净物);由不同种分子构成的物质是混合物(如空气是由氮分子、氧分子、二氧化碳分子等构成的,是混合物)。
2.原子(1)概念:原子是化学变化中的最小粒子。
(2)化学变化(即化学反应)的本质是原子的重新组合。
在化学反应前后,原子的种类和数目都不变,元素的种类也不变(即元素守恒),但分子的种类一定发生改变(生成新物质)。
分子在化学反应中发生变化的过程为:分子(3)结构:①原子由原子核与核外电子构成,原子核由质子和中子构成(有一种氢原子没有中子)。
1个质子带1个单位正电荷,1个电子带1个单位负电荷,中子不带电。
核电荷数=质子数=原子的核外电子数=原子序数②相对原子质量:以1个碳12原子质量的1/12为标准,其他原子的质量与它相比较所得到的比,单位为1。
中考化学复习考点梳理:第三单元 物质构成的奥秘(21张)
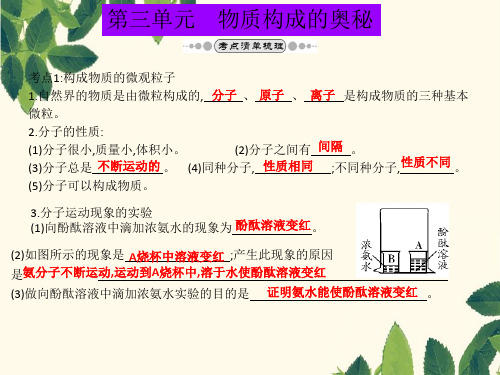
3.分子运动现象的实验 (1)向酚酞溶液中滴加浓氨水的现象为 酚酞溶液变红。
(2)如图所示的现象是 A烧杯中溶液变红 ;产生此现象的原因 是氨分子不断运动,运动到A烧杯中,溶于水使酚酞溶液变红
(3)做向酚酞溶液中滴加浓氨水实验的目的是 证明氨水能使酚酞溶液变红 。
【注意】(1)分子、原子都能直接构成物质,因此它们都能保持所构成物质的化学 性质,如:水分子可以保持水的化学性质,铁原子可以保持铁的化学性质。(2)原子在 化学变化中不能再分,但在其他的条件下可以再分。(3)由分子构成的物质,如果只 含一种分子则是纯净物,含有多种分子则为混合物。若纯净物中的分子由同种原 子构成,则它是单质;若分子由不同种原子构成,则它是化合物。(4)由分子构成的物 质,在发生物理变化时,分子本身没有变化,只是分子间的间隔发生了改变;而在化学 变化中,分子本身发生改变,变成新物质的分子。不过,原子是化学变化中最小的粒 子,因此在化学变化前后,分子的种类改变,而原子的数量和种类不变。 6.离子 (1)离子符号 在元素符号的 右上角 写上一个离子所带的电荷数和电性符号。先写__数__字__ 后写 __正__负__号___,当数字为1时,应省略不写。
(1)在原子中,核电荷数= 质子数 = 核外电子数 。 (2)构成原子的粒子有 质子 、 中子 和 电子 等,但并不是 所有的原子中都有这三种粒子,例如 氢 原子核内无中子,原 子核中质子数不一定等于 中子数 。 2.原子核外电子的排布 (1)核外电子排布的初步认识 ①通常用 电子层 表明运动着的电子离核远近的不同。 ②元素原子核外电子最少的有 1 层,最多的有 7 层,最外 层电子数最多不超过 8 个。(只有1层的不超过 2 个)
考点3:元素和元素周期表
1.元素 (1)元素是具有相同 核电荷数 (即 质子数 )的一类原子的总称。 (2)元素与原子的区别与联系
中考化学第一轮复习 第三单元物质构成的奥秘单元过关复习 (含解析)

第三单元物质构成的奥秘【考点分析解读】1.本单元知识中物质与元素、原子、分子以及离子的区别和联系等均是中考的热点,特别是与之相关的高科技信息题是近几年中考的命题方向。
命题中形式多样,考查学生的想象力和综合分析能力。
将抽象具体化,对比记忆是复习的有效方法。
2.有关元素、分子、原子的概念辨析以及应用这些概念描述物质的组成或结构,在中考中常见题型为选择题或填空题。
3.结构示意图及化学符号周围数字的意义等知识点,常以图片或元素周期表的形式并且会结合热点新闻、新材料为素材考查。
考查学生的阅读能力、自学能力、信息提取能力的题目将会成为主流。
在备考时要对所给信息进行科学评价、判断正误,进行知识迁移。
【典型试题】一、分子的概念和特征例1. (2017•河池)下列关于分子、原子、离子的说法正确的是( )A. 原子是微小的实心球体,可以再分B. 单个SO2分子有刺激性气味C. 离子是原子失去电子后生成的粒子D. 分子、原子、离子都是构成物质的粒子【答案】D【解析】A.原子中核外电子绕原子核外空间作高速运动,原子不是实心球体,A错误;由分子构成的物质分子是保持其化学性质的最小粒子,气味是物理性质,无法由单个分子保持,应该是由大量分子组成的集体表现出来,B错误;原子得到或失去电子均可形离子,C错误;物质是由微粒构成的,分子、原子和离子都是构成物质的微粒,D正确。
二利用分子的性质分析和解决问题例2 (2017•海南)下列事实的微观解释不正确的是()A.干冰升华--分子间隔变大B.水烧开后把壶盖顶开--分子数目变多C.水在通电的条件下发生分解反应--分子种类变化D.湿衣服晾在太阳底下干得快--分子运动速率变快【答案】B【解析】A.干冰升华是因为二氧化碳分子间隔变大的缘故,故选项解释合理;B.水烧开后,壶盖被顶开,发生的是物理变化,水分子本身没有发生改变,温度升高,水分子间的间隔变大,引起水的体积膨胀,壶盖被顶开,分子数目不变,故解释错误;C.水在通电的条件下发生分解反应生成氢气和氧气,分子种类变化,故选项解释合理;D.湿衣服晾在太阳底下干得快,是因为温度升高,分子运动的速率加快,故选项解释合理;三原子的构成例32 (2017•威海)学习完“原子的构成”之后,萍萍同学形成了以下认识,其中错误的是()A.原子由居于中心的原子核和核外电子构成B.核外电子在离核远近不同的区域中运动C.原子核的质量和电子的质量相差不大D.原子核的体积与整个原子的体积相比要小很【答案】C【解析】A.原子的构成:由原子核和核外电子构成,故A说法正确;B.核外电子是分层排布的,核外电子在离核远近不同的区域中运动,故B说法正确;C.电子的质量很小可以忽略不计,原子的质量主要集中在原子核上,故C说法错误;D.原子核的体积很小,原子核的体积与整个原子的体积相比要小很多,故D说法正确;四原子核外电子的排布与离子的形成例 4 (2017•云南)如图是某元素的原子结构示意图,下列有关该原子的说法错误的是( )A.质子数为11 B.易得电子形成阴离子C.最外层有1个电子D.该原子有3 个电子层【答案】B【解析】A.由某元素的原子结构示意图可知,圆圈内的数字是11,该元素原子核内有11个质子,故选项说法正确;B.由某元素的原子结构示意图可知,最外层电子数是1,在化学反应中易失去1个电子而形成阳离子,故选项说法错误;C.由某元素的原子结构示意图可知,该原子的最外层有1个电子,故选项说法正确;D.由某元素的原子结构示意图可知,该原子核外有3个电子层,故选项说法正确。
中考化学复习第三单元物质构成的奥秘

4.(2015凉山州)我的家乡四季如春,美景如画,素有“小春城”的美誉。
下列现象说明分子在永不停息运动的是 ( )
D
A.初春的滨河路柳絮飞扬
B.盛夏的瀛洲园百花斗艳、蜂飞蝶舞
C.深秋的龙肘山万亩杜鹃黄叶飘落(piāo luò)
D.寒冬的绿地广场梅园腊梅绽放、花香四溢
第二十页,共三十四页。
命题点3 微粒(wēilì)结构示意图 1.(2016乐山)下列粒子(lìzǐ)结构示意图中,属于阴离子是( B)
第二十四页,共三十四页。
命题(mìng tí)点4 元素及元素符号
1.(2017攀枝花)银针(yín zhēn)是中医针灸的常用器械。银的元素符号是( B )
A. Au
B. Ag
C. Mg
D. Hg
2.(2015乐山(lè shān))地壳中含量最多的元素是 ( A )
A.氧
B.硅
C.铝
D.铁
3.(2017自贡)每100 g黑木耳中含0.185 g铁,是常见天然食品中含铁量最高
【方法指导】在利用微观粒子的性质解释常见的生活现象时,应注意分子性质与物理现象 之间的对应关系,常见现象的关键词与微粒之间的对应关系如下:
(1)蒸发、扩散、挥发→微观粒子在不停地运动;
(2)体积变化、三态变化→分子间有间隔;
(3)很小体积的物质由多个微观粒子构成(gòuchéng)→微观粒子的质量和体积都很小。
第九页,共三十四页。
类型(lèixíng)3 元素及元素符号
【例3】下列关于(guānyú)元素的叙述中正确的是( A )
A.同种原子的统称为元素
B.同种元素的原子结构和质量完全相同
C.元素的种类取决于该元素的核外电子数
(河南专版)2021_2019版九年级化学上册第三单元物质构成的奥秘单元复习(三)物质构成的奥秘(增

河南单元复习(三) 物质构成的奥秘01 知识框架02 考情分析本单元知识点在近3年河南化学中招试卷中,主要以选择题、填空题和简答题的形式考察,难度不大,分值4~6分。
高频考点有:(1)分子、原子的根本性质,以具体的生活现象和变化为背景,通过文字的形式,考察分子、原子的概念和根本性质;用分子、原子的观点解释常见的变化及现象;(2)原子的构造与离子,依据给出的具体原子或离子构造示意图,考察粒子的性质;(3)元素单元格,根据元素单元格说出单元格中的各局部代表的意义、在元素周期表中的位置等。
03 单元精炼1.(重庆A 卷)翻开装有浓氨水的试剂瓶,能闻到刺激性气味,从分子的角度解释正确的选项是〔 〕A .分子在不断运动B .分子由原子构成C .分子大小可以改变D .分子可以保持物质的化学性质2.(泰安中考)钛合金在生产、生活的多个领域应用广泛。
有一种钛原子核内有22个质子、26个中子,那么该钛原子的核外电子数是〔 〕A .22B .26C .58D .483.(邵阳中考)用分子、原子的观点解释以下现象,其中不合理的是〔 〕A .品红在水中扩散——分子不断运动B .水结成冰——分子停顿运动C .1滴水中大约有1.67×1021个水分子——分子很小D .气体可以压缩储存在钢瓶中——分子间有间隔4.(衢州中考)科学家发现一种新元素。
该元素原子核外电子数为117,中子数为174,相对原子质量为291,元素名称Ununseptium ,符号Uus 。
请模仿甲,将该元素对应信息编写到图乙中相应位置,“①〞处应填〔 〕 非金属元素 物质 构成 分子 原子 体积和质量都很小 在不停地运动 分子之间有间隔 电子 原子核 质子中子 离子 阳离子:带正电荷 阴离子:带负电荷 组成——元素 分类 金属元素 符号:表示某种元素;一个原子 元素周期表A.291 B.174C.117 D.575.(漳州中考)漳州市诏安县红星乡是“长寿之乡〞,与当地富硒有关。
人教版中考化学第三单元物质构成的奥秘word复习

第三单元物质构成的奥秘考情概览内容考查方向要求分子和原子物质的微粒性,分子和原子的含义,用微粒的观点解释某些常见的现象c原子的构成原子的结构、原子结构示意图 a离子同一元素的原子和离子的相互转化,粒子种类的判断、离子符号的书写b元素元素的含义、分类及分布,常见元素的名称和符号的书写、表示意义a元素周期表元素周期表中一格的含义及元素周期表中元素间的规律,在元素周期表中找到指定的元素a考点梳理分子和原子1.物质由微观粒子构成(1)构成物质的微粒有分子、原子和离子。
如:①水(或蒸馏水)、二氧化碳、氢气、氧气、H2SO4等物质是由分子构成的。
②金属( 如Fe、Hg)、稀有气体、金刚石等物质是由原子构成的。
③氯化钠、硫酸铜、硝酸钾等是由离子构成的。
(2)微观粒子的性质及应用(高频考点)性质事实(解释生活中的常见现象分子和原子的质量、体积都很小一个水分子的质量约是3×10-26 Kg,一滴水中大约有×10-23个水分子分子和原子在不停地运动,温度越高,运动速率越快水的挥发、闻到气味、湿衣服夏天干得快分子和原子间存在间隔,温度越高,间隔越大轮胎充气、物质具有热胀冷缩的现象、气体压缩储存于钢瓶中同种物质分子的性质相同,不同种物质分子的性质不同液态氧和氧气都是由氧分子构成的,它们都能以支持燃烧;而氮气是由氮分子构成的,不支持燃烧【巧学乐记】分子的性质可以简记为:“小”“动”“间”“同”。
(3)分子运动现象①向酚酞溶液中滴加浓氨水的现象为溶液由无色变为红色。
②如图所示的现象是烧杯A中溶液变红色;产生现象的原因是浓氨水分子不停的运动,运动到了烧杯A中,使酚酞试液变红色。
③做向酚酞溶液中滴加浓氨水的实验①的目的是对照。
2.分子、原子的区别和联系分子原子概念保持由分子构成的物质化学性质的最小粒子化学变化中的最小微粒联系原子可以构成分子,区别在化学变化中,分子可以分成原子在化学变化中,原子不能再分,只能重新组合备考提示:(1)分子只能保持物质的化学性质,不能保持物质的物理性质;“最小粒子”是从保持物质化学性质这一观点来说的,而不是单纯的说分子是最小的粒子。
河南中考化学基础过关练习 第三单元 物质构成的奥秘(可自主编辑PPT)

命题点四 元素和元素周期表
例4 (2016河南中考,14,3分)如图是元素周期表中的一格。氖的
相对原子质量为 20.18 ,其原子结构示意图为
,该
元素在元素周期表中位于第二周期的 最右边 (填“最左边” “中间”或“最右边”)。
答案 20.18
最右边
解析 元素周期表的单元格中,最下面的数字表示相对原子质量, 氖的相对原子质量为20.18;氖是10号元素,其原子的质子数为10,
超级总结 中考考查 构成物质的微粒在2012、2013、2014、2016年河南中 试卷中均有考查,属高频考点,常以选择题或填空题的形式给题,主要 考查常见物质(如氯化钠、水、氨气等)的微粒构成,分值一般为1~2 分。 知识归纳 分子、原子、离子是构成物质的微粒。由分子构成的 物质,如水、氧气、氨气、二氧化碳等;由原子构成的物质,如金属单 质、稀有气体、金刚石等;由离子构成的物质,如氯化钠、硫酸铜等 大部分盐类。
1
2.原子核外电子的排布
原子的 最外层电子 数决定元素的化学性质。根据原子的 最外层电子 数,把元素分为三类:金属元素、非金属元 素、稀有气体元素。
3.相对原子质量
(1)定义:国际上以 一种碳原子 (碳-12)质量的 1 为标准,其
12
他原子的质量与它相比较所得到的比,作为这种原子的相对原子 质量(符号为Ar)。其单位是“1”,通常省略不写。 (2)计算公式
2.雄伟壮观的国家大剧院主体建筑表面安装了近2万块钛(Ti)金 属板。已知一种钛原子的原子核内有22个质子和26个中子,该钛
原子的核外电子数为 ( B )
A.4 B.22 C.26 D.48
答案 B 在原子中,质子数=核外电子数,钛原子的原子核内有2 2个质子,则其核外电子数为22,故选B。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三单元物质构成的奥秘
考法1物质的构成
1.[xx河南,7]下列各组物质中,都由离子构成的一组是( )
A.NaCl、CuSO4
B.CH4、HCl
C.Si、CO2
D.Ar、Au
2.[xx河南,5]下列各组物质中,都由分子构成的一组是( )
A.金和金刚石
B.水和氨气
C.汞和氯化钠
D.干冰和硫酸铜
3.[xx河南,3]分子、原子、离子等都是构成物质的微粒。
下列物质由离子构成的是( )
A.氯化钠
B.黄金
C.金刚石
D.干冰
4.[xx河南,16第一空;xx年河南,15(1)]配置农药波尔多液所用硫酸铜的构成粒子是。
(填化学符号)
考法2分子的性质
5.[xx河南,9]室温时将少量干冰放入塑料袋中并密封,塑料袋会快速鼓起,其原因是( )
A.分子的体积变大
B.分子分解变成了原子
C.分子的间隔变大
D.分子由静止变为运动
6.[xx河南,11]下列事实的结论或解释中不正确
...的是( )
A.水烧开后易把壶盖冲起——说明温度升高分子会变大
B.公园的桂花开放时满园飘香——说明分子在不断运动
C.酸碱中和反应都生成水——实质是H+与OH-结合生成了H2O
D.铝制品有抗腐蚀性能——实质是表面生成了致密的氧化膜起保护作用
7.[xx河南,20]请用分子的相关知识解释生产、生活中的现象。
(1)酒香不怕巷子深。
(2)加压时,6000L氧气可装入容积为40L的钢瓶中。
8.[xx河南,12第一空]洛阳牡丹天下闻名。
牡丹花开时满城飘香,从分子角度解释,是因
为。
考法3原子与离子的结构示意图
9.[xx河南,8]硅是信息技术的关键材料。
如图为硅的原子结构示意图,下列说法正确的是( )
A.硅属于稀有气体元素
B.图中n的值为8
C.硅的相对原子质量为14
D.硅元素位于第三周期
10.[xx河南,8]如图为钠的原子结构示意图。
下列说法不正确
...的是( )
A.钠原子的质子数为11
B.图中 n的值为10
C.钠在反应中易失去电子
D.钠元素位于第三周期
11.[xx河南,23(1)]如图是钠的原子结构示意图。
下列说法不正确
...的是。
a.钠属于金属元素
b.钠原子的质子数为11
c.钠离子的符号为Na+
d.钠在化学反应中易得到电子
12.[xx河南,5]下列结构示意图表示的粒子中,属于离子的是( )
A B C D
13.[xx河南,21(1)]如图是铝的原子结构示意图。
下列说法不正确
...的是。
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
考法4元素及元素周期表
14.[xx河南,5]下列各组元素中,元素符号的第一个字母不相同
...的一组是( )
A.锰、钛
B.氩、金
C.铅、铂
D.氦、汞
15.[xx河南,2]下列科学家中,发现了元素周期律并编制了元素周期表的是( )
A.拉瓦锡
B.门捷列夫
C.道尔顿
D.阿伏加德罗
16.[xx河南,14]如图是元素周期表中的一格。
氖的相对原子质量为______________,其原子结构示意图为__________________,该元素在元素周期表中位于第二周期的_____________(填“最左边”“中间”或“最右边”)。
17.[xx河南,14]下图是元素周期表的一部分。
原子序数为10的元素名称为;氟原子的核外电
子数为;等质量的氧气和氟气中,所含原子数较少的是。
18.[xx河南,14]人体中含量最高的金属元素是;形成化合物种类最多的元素是。
19.[xx河南,13]元素周期表是学习化学的重要工具,下图是表中的一格,其中A表示;B表
示。
20.[xx河南,11第二空]地壳中含量最多的金属元素是。
21.[xx河南,21(2)]如图为元素周期表中的一格,下列说法不.
正确
..的是(填标
号)。
A.碳元素属于非金属元素
B.碳原子核内质子数为6
C.碳元素的原子结构示意图为
D.碳的相对原子质量为12.01
参考答案
1.A 【解析】氯化钠是由钠离子和氯离子构成的,硫酸铜是由铜离子和硫酸根离子构成的,A符合题意;甲烷是由甲烷分子构成的,氯化氢是由氯化氢分子构成的,B不符合题意;硅是由硅原子构成的,二氧化碳是由二氧化碳分子构成的,C不符合题意;氩气是由氩原子构成的,金是由金原子构成的,D不符合题意。
2.B 【解析】
选项正
误
分析
A ✕金和金刚石都是由原子构成的
B √水和氨气都是由分子构成的
C ✕汞是由汞原子构成的,氯化钠是由离子(Na+、Cl-)构成的
D ✕干冰是由二氧化碳分子构成的,硫酸铜是由离子(Cu2+、S)构成的
3.A 【解析】氯化钠由钠离子和氯离子构成;黄金由金原子构成;金刚石由碳原子构成;干冰是固态的二氧化碳,由二氧化碳分子构成。
4.Cu2+和S
5.C 【解析】在室温下,干冰很容易升华变成二氧化碳气体,此过程中分子间间隔变大,因此塑料袋快速鼓起。
6.A 【解析】水烧开后易把壶盖冲起,说明温度升高分子间间隔变大,A错,符合题意。
7.(1)分子在不断运动,使酒的气味扩散。
(2)分子间有间隔,加压使分子间间隔变小。
8.分子在不断地运动
9.D 【解析】硅属于固态非金属元素;根据原子的质子数等于其核外电子数可得n=4;相对原子质量近似等于质子数加中子数,根据题中信息不能得出硅的相对原子质量;元素所在的周期数等于该元素原子的核外电子层数,因此硅元素位于第三周期,选项D正确。
10.B 【解析】原子中,核内质子数=核外电子数。
钠原子核内有11个质子,因此其核外有11个电子,n的值为8,故B不正确。
11.d 【解析】钠属于金属元素,故a正确;钠原子的质子数为11,故b正确;钠元素的最外层有1个电子,容易失去电子,形成钠离子Na+,故c正确,d错误。
12.C 【解析】原子不显电性,质子数=核外电子数;原子通过得失电子变成离子,质子数大于核外电子数的为阳离子,质子数小于核外电子数的为阴离子。
13.C 【解析】原子结构示意图中圆圈内的数字就是质子数,所以铝原子的质子数是13;由于铝原子最外层电子数是3,易失去3个电子,显+3价;地壳中含量最多的元素是氧元素;铝具有导电性,因此可以作导线。
14.A 【解析】“锰、钛、氩、金、铅、铂、氦、汞”的元素符号分别为:Mn、Ti、Ar、Au、Pb、Pt、He、Hg。
15.B 【解析】1869年,俄国化学家门捷列夫发现了元素周期律并编制出元素周期表。
16.20.18 最右边
17.氖9 氟气
18.钙(或Ca) 碳(或C)
19.元素符号相对原子质量
20.铝(或Al)
21.C 【解析】碳原子的最外层电子数应为4,故C不正确。
