化学物质及其变化2
(完整版)第二章化学物质及其变化必背知识点

第二章化学物质及其变化知识清单一、物质的分类1. 元素的存在形式有两种,分别是什么?游离态(单质)、化合态(化合物)2.从熔沸点角度看,纯净物和混合物有何差别?纯净物有固定的熔沸点,混合物没有3.只含一种元素的物质一定是纯净物吗?不一定;如氧气与臭氧、石墨与金刚石组成的都是混合物4.从与酸或碱反应的情况看,氧化物是如何分类的。
酸性氧化物:与碱反应生成盐和水的氧化物(如CO2、SO2、SO3、P2O5)碱性氧化物:与酸反应生成盐和水的氧化物(如Na2O、CaO)不成盐氧化物:既不与酸反应,也不与碱反应的氧化物(如CO、NO)5.酸性氧化物一定是非金属氧化物吗?不一定,如Mn2O7非金属氧化物一定是酸性氧化物吗?不一定,如CO、NO碱性氧化物一定是金属氧化物吗?是金属氧化物一定是碱性氧化物吗?不一定,如Al2O3、Mn2O76.酸碱盐是如何定义和再分类的?酸的定义:在水溶液中电离出的阳离子都是H+的化合物。
酸可以分为强酸与弱酸;或含氧酸与无氧酸;或一元酸与多元酸;或氧化性酸与非氧化性酸等;碱的定义:在水溶液中电离出的阴离子全是OH-的化合物。
碱可以分为强碱与弱碱;或一元碱与多元碱等。
盐的定义:由金属阳离子(或铵根离子)与酸根离子组成的化合物盐可以分为正盐与酸式盐;或可溶性盐与难容性盐等盐的溶解性:钾钠硝铵全都溶,盐酸不溶银亚汞;硫酸难容钡和铅,碳酸只溶钾钠铵;钙银硫酸盐微溶;亚硫酸盐似碳酸。
7. 常见物质俗名和化学式生石灰:CaO 熟石灰:Ca(OH)2 石灰石:CaCO3碱石灰:CaO+NaOH烧碱(苛性钠):NaOH 纯碱(苏打):Na2CO3小苏打:NaHCO38.分散系如何分类的?分类的标准是什么?分散系分为溶液、胶体和浊液;分类的标准是分散质粒子的直径大小:其中小于1-100nm属于溶液,1-100nm之间的属于胶体,大于100nm的属于浊液。
9.常见的胶体有哪些?云、烟、雾、牛奶、豆浆、河水、血液、有色玻璃等10.胶体有哪些性质?丁达尔效应、聚沉、电泳、渗析使胶体聚沉的方法有哪些?加热、搅拌、加入电解质溶液、加入胶粒带相反电荷的胶体。
第二章 化学物质及其变化

【主题2】离子反应(3课时)【第一课时】酸、碱、盐在水溶液中的电离。
【预习目标】1、知道酸、碱、盐在水溶液中的电离情况;2、了解电解质的概念;3、能书写常见酸、碱、盐的电离方程式;4、初步了解NaCl在水溶液中的电离过程;5、初步从电离角度认识酸、碱、盐的本质。
【导读提纲】1、我们在初中观察过酸、碱、盐在水溶液中导电的实验,你知道它们为什么能导电吗?它们在其他状态下能导电吗?2、你认为满足哪些条件就可以认为该物质属于电解质?3、金属也能导电,属于电解质吗?说明原因。
4、请你尽可能多的列举一些属于电解质的物质。
5、仔细观察课本30页中NaCl在水中的溶解和电离示意图,你能简述NaCl的电离过程吗?6、试试看,你能写出下列各物质的电离方程式吗?NaCl H2SO4KOH Al2(SO4)3 Cu(NO3)27、请参考酸的定义,尝试从电离的角度概括出碱和盐的本质。
8、用化学方程式表示酸(以HCl为例),碱(以NaOH为例),盐(以K2CO3为例)的各条通性。
9、你能用树状分类法对物质进行简单分类吗?【主题2】离子反应(3课时)【第二课时】离子反应及其发生的条件。
【预习目标】1、认识离子反应及其发生的条件,能够判定离子反应能否发生。
2、初步了解离子方程式的定义。
3、写出常见物质间离子反应的离子方程式。
4、了解酸碱中和反应的实质。
5、知道离子方程式表达的意义。
【导读提纲】1、请你总结初中学过的沉淀、气体各有哪些?2、请你预估一下实验2-1各步实验现象并试着解释出各现象的原因,由此实验你能得出什么结论呢?请尝试设计实验来证明你的结论。
3、通过实验2-1,总结离子反应的定义。
4、总结离子方程式的书写步骤,你认为哪步最关键?5、在离子方程式书写第二步中,你觉得哪些类型的物质能拆写成离子形式,哪些仍为化学式?6、写出下列反应的离子方程式①AgNO3+NaCl ②Na2CO3+HCl ③Zn+H2SO4④CaCO3+HCl ⑤CO2+NaOH7、写出几个你所熟悉的酸碱中和反应的化学方程式与离子方程式。
高一化学化学物质及其变化2

编号
A B C D E F G H
化学基本反应类型O
CaO+H2O = Ca(OH)2 2Al2O3==4Al+3O2 CaCO3==CaO+H2O
Na2CO3+Ca(OH)2=CaCO3+2NaOH
Fe+CuSO4==FeSO4+Cu 2+ 2+ Fe+Cu =Fe +Cu HCl+NaOH=NaCl+H2O
悬浊液 乳浊液
分散系类别 分 散 质 粒子直径
溶液
〈1nm
胶体
1~100nm
浊液
>100nm
粒子组成
外观特征 稳定性
分子或离子
均一、透明 稳定 能 能
分子集合体或高分子 巨大的分子集合体
均一、透明 稳定(介稳体系) 能 不能 不均一、不透明 不稳定 不能 不能
能否透过滤纸 能否透过半透膜 实例
氨水、碘酒
得到电子,化合价降低,被还原 1、强弱律:自发发生的氧化还原反应总是由“强” 成“弱”的。(判定强弱) 2、价态律:元素处于最高(低)价,只有氧化 (还原)性,中间价则两性都有。 3、转化律:邻价态间的转化最易。只靠拢不交 叉规律——归中反应 全程导学38页 4、先后律:谁强谁先反应。
氧化还原反应方程式 CuO+H2
化合价升高,失去电子,被氧化 升 失 氧
0 0 点燃 +3 -2 (1)4Al + 3O2 == 2Al2O3
得 降 化合价降低,得到电子、被还原 还
升失氧 还
降得还氧
氧化还原反应的一般规律 失去电子,化合价升高, 被氧化
电子得失(或 元素化合价升 降)总数相等
第二章_化学物质及其变化(复习)

6、离子反应发生的条件 ①生成沉淀(难溶物质) ②生成气体(挥发性物质) ③生成水(难电离物质即弱电解质) ④发生氧化还原反应。 发生氧化还原反应。 复分解反应: 复分解反应:实质上就是两种电解 质在溶液中相互交换离子的反应。 质在溶液中相互交换离子的反应。 交换离子的反应
二、离子共存问题
1、同一溶液中若离子间符合下列任意 一个条件就会发生离子反应, 一个条件就会发生离子反应,离子之间 便不能在溶液中大量共存。 便不能在溶液中大量共存。
反应物
性质
实质
特征
反应
反应产物
还原剂
具有还原性
失电子
化合价升 化合价升高
发生氧化反应 发生氧 (被氧化)
氧化产物
化合价
氧化反应, 氧化反应,被氧化 还原剂) (还原剂)
升失氧, 升失氧,降得还
电子得失
常见的氧化剂有: 常见的氧化剂有: ①活泼的非金属单质如:Cl2、O2等。 活泼的非金属单质如: ②高价金属阳离子如:Fe3+、Cu2+等。 高价金属阳离子如: SO4、 ③高价或较高价含氧化合物如:MnO2、浓H2SO4、 高价或较高价含氧化合物如: 酸化KMnO HNO3、酸化KMnO4。 常见的还原剂有: 常见的还原剂有: ①活泼或较活泼的金属:如K、Na、Al、Fe等。 活泼或较活泼的金属: Na、Al、Fe等 Si等 ②一些非金属单质:如H2、C、Si等。 一些非金属单质: ③较低态的化合物:CO、H2S等。 较低态的化合物:CO、
溶液导电能力的强弱只取决于在相同条件下(温 溶液导电能力的强弱只取决于在相同条件下( 外电压等)溶液中自由移动离子的浓度大小 度、外电压等)溶液中自由移动离子的浓度大小 和离子所带电荷的多少 溶液与30%醋酸 NaCl是强电 例:浓度极稀的NaCl溶液与 浓度极稀的 溶液与 醋酸 是强电 解质,但浓度极稀时,自由移动的离子浓度很小。 解质,但浓度极稀时,自由移动的离子浓度很小。 所以导电性醋酸更强。 所以导电性醋酸更强。
第二章化学物质及其变化第二节离子反应(第二课时)课件-河南省三门峡市第一高级中学高中化学必修一

▪ 1.Cu(OH)2+HCl
Cu(OH)2+2H+=Cu2++2H2O
▪ 2.CH3COOH+NaOH
CH3COOH+OH-=CH3COO-+H2O
▪ 3.HCl+NH3.H2O
H++NH3.H2O=NH4++H2O
LOGO
讨论总结
1、 H+ + OH- = H2O
表示强酸和强碱反应生成可溶性盐的一类反应。
LOGO
3.(删): 删去方程式两边形式相同的离子:
2Ag++2NO3-+Cu2++2Cl- = 2AgCl↓+Cu2++2NO3-
4.(查): 整理方程式并检查两边各元素 的原子个数和电荷总数是否相等:
2Ag+ + 2Cl- = 2AgCl↓
Ag+ + Cl- = AgCl↓
LOGO
4、离子反应方程式书写规则
OH-+H+=H2O
பைடு நூலகம்
LOGO
练习:完成下列反应的离子方程式。
1、盐酸与氢氧化钠溶液反应。 2、硝酸与氢氧化钠溶液反应。 3、硫酸与氢氧化钡溶液反应。 4、盐酸与硝酸银溶液反应。 5、氯化钠与硝酸银溶液反应。 6、氢氧化钡与硫酸钠溶液反应。 7、氢氧化钡与硫酸铜溶液反应。
LOGO
思考
下列酸碱中和反应的离子方程式都可以写成
如何正确书写离子方程式?
LOGO
1、(写): 正确写出化学方程式:
例:2AgNO3 + CuCl2 = 2AgCl↓+ Cu(NO3)2 2.(拆): 把易溶于水、易电离的物质写成离 子形式,难溶或难电离的物质以及气体等仍 用化学式表示。
2022年新教材高考化学一轮复习第2章物质及其变化第2讲离子反应离子方程式学案

新教材高考化学一轮复习:第2讲离子反应离子方程式[课程标准]1.认识酸、碱、盐等电解质在水溶液中或熔融状态下能发生电离。
通过实验事实认识离子反应及其发生的条件。
2.能用电离方程式表示某些酸、碱、盐的电离。
能用化学方程式、离子方程式正确表示典型物质的主要化学性质。
考点一电解质及其电离1.电解质及其电离的关系(1)常见的强酸、弱酸强酸HNO3、H2SO4、HClO4、HCl、HBr、HI弱酸H2CO3、H2SiO3、CH3COOH、H2C2O4、HClO、HF、H2S、H2SO3强碱NaOH、KOH、Ca(OH)2、Ba(OH)2、RbOH、CsOH弱碱NH3·H2O、Mg(OH)2、Fe(OH)3质也不是非电解质。
②本身电离而导电的化合物才是电解质,如虽然CO2、SO2、NH3的水溶液能导电,但CO2、SO2、NH3均是非电解质。
2.电解质导电的原因——电离(1)概念:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
(2)电离条件:酸的电离条件是溶于水,盐和碱的电离条件是溶于水或受热熔化。
[点拨] ①电解质不一定能导电,如固态NaCl、液态HCl等都不导电。
②电解质的强弱与电解质溶液导电能力的强弱、溶解度的大小没有直接关系,如碳酸钙,其溶解度小,溶液导电能力弱,但其属于强电解质。
3.电离方程式的书写(1)强电解质的电离方程式中,用“===”连接,弱电解质(包括弱酸的酸式酸根)的电离方程式中,用“”连接。
例如:Na2SO4:Na2SO4===2Na++SO2-4;HClO:HClO H++ClO-。
(2)多元弱酸的电离分步书写,多元弱碱的电离一步书写。
例如:H2CO3:H2CO3H++HCO-3、HCO-3H++CO2-3;Fe(OH)3:Fe(OH)3Fe3++3OH-。
(3)酸式盐的电离,强酸酸式盐与弱酸酸式盐在水溶液中的电离方式不同。
例如:NaHSO4:NaHSO4===Na++H++SO2-4;NaHCO3:NaHCO3===Na++HCO-3、HCO-3H++CO2-3。
第二章化学物质及其变化

3、胶体的性质
胶体具有与溶液和浊液不同的性质是由 分散质微粒的大小决定的。
(1)丁达尔效应:可见光通过胶体时,在 入射光的侧面可观察到明亮的光路,这种 现象称为丁达尔现象,它是由胶粒对可见 光的散射而产生的。在实验室里可以利用 丁达尔效应鉴别胶体和溶液。
(2)布朗运动:是指花粉悬浮在水中进行 的无秩序、不停的运动。胶体也作布朗 运动。
5、胶体的制备和应用
(1)制备:
分散法:将难溶固体加工研磨成超细粉末,使之 达到胶体分散质微粒粒度范围,加入分散剂中混 匀即可。如:碳素墨水的制得。
凝聚法:利用复分解反应或水解反应,控制难溶 物形成的条件,使之达到胶体微粒粒度范围,如: Fe(OH)3胶体的制备
(2)应用:见课本
练习
1、经分析,某物质只含有一种元素,则此 物质是( D ) A.一定是一种单质 B. 一定是纯净物
1、分散系:
概念:由一种物质或几种物质以粒子形式 分散到另一种物质里所形成的混合物。分散 系中分散成粒子的物质叫分散质,另一种物 质叫做分散剂。
2、分类:(1)、按照分散质或分散剂所处
的 状态,可以有九种组合方式。
(2)、当分散剂是水或其他液体时,可 以按照分散质粒子的大小把分散系分为:溶 液、胶体、和浊液。(区别与联系)
(3)电泳:胶粒细小而具有较大的表面积, 能选择性地吸附胶体中的某种离子带有 一定的电荷。在直流电场中,胶体微粒 会向带相反电荷的电极定向移动。 (4)聚沉:加入强电解质、加热、加入胶 粒带相反电荷的胶体,主要是中和胶粒 所带电荷,减弱胶体的稳定性。
4、胶体具有介稳性的原因
主要是因为胶体粒子可以通过吸附而 带电荷。同种胶体粒子的电性相同,在 通常情况下,它们之间的相互排斥阻碍 了胶体粒子变大,使它们不容易聚集。 胶体粒子所作的布朗运动也使得它们不 容易聚集成质量教大的颗粒而沉降下来。
2024届高考化学一轮复习课件(人教版)第一单元 物质及其变化 第2讲

考点一
考点二
核心素养
考点三
微专题
高考真题演练
课时作业
(4)CaCO3、AgCl难溶于水,所以是弱电解质。 错因:_C_a_C_O__3_、_A__g_C_l_溶__于__水__的__部__分__完__全__电__离__,__属__于__强__电__解__质_ 。
(5)强电解质溶液的导电性比弱电解质溶液的导电性强。 错因:_导__电__性__与__离__子__浓__度__及__离__子__所__带__电__荷__数__有__关__。_________
的化合物是盐。
考点一
考点二
核心素养
考点三
微专题
高考真题演练
课时作业
5.电离方程式的书写
(1)强电解质:完全电离,用 01 _=_=_=_表示。如 H2SO4、NaOH、(NH4)2SO4 的电离方程式分别为 02 _H_2_S_O_4_=_=_=_2_H__+_+__S_O_24_-、03 _N_a_O_H__=_=_=_N__a_+_+__O_H__-、 04 _(_N_H__4_)2_S_O_4_=_=_=_2_N__H_+4_+__S__O_24_-_______。
考点一
考点二
核心素养
考点三
微专题
高考真题演练
课时作业
答案
解析 A 项,NaHCO3 完全电离生成 Na+和 HCO-3 ;C 项,HA 为 弱酸,部分电离;D 项,CaCO3 难溶,但属于强电解质,全部电离。
考点一
考点二
核心素养
考点三
微专题
高考真题演练
课时作业
解析
4.写出下列物质的电离方程式: (1)HNO3:____H_N__O_3_=_=_=_H__+_+__N_O__-3 __________________________; (2)H2CO3:___H_2_C_O_3____H__+_+__H_C__O_- 3_________________________; (3)NH3·H2O:_N__H_3_·__H_2_O_____N_H_+ 4__+__O_H_-_____________________; (4)NaCl:___N__a_C_l_=_=_=_N_a_+__+__C_l-_____________________________; (5)NaHSO3:__N_a_H_S_O__3=__=_=_N_a_+_+__H__S_O_- 3_______________________; (6)CH3COOH:__C_H_3_C_O__O_H_____C_H__3C__O_O__-_+__H_+________________。
高一化学化学物质及其变化2

; 重庆小松鼠地暖售后维修 lpu60hln
的“小机关”了。然后,她只要绷直脖颈,双膀用力带动双臂,同时双手的拇指和食指、中指对称着一开一合,让这个由红色双股新棉 线变化而成的互动收放“小机关”在待嫁女娃儿的面部绞过,就会把那些个细小的汗毛全部拔除干净。对于一些不规则的眉毛,以及额 头、两鬓和耳后长得不太整齐的发际处的细小毛发,更要细心地拔除;有时候还需要借助于小镊子什么的。特别认真的修面妇人,甚至 还会在待嫁女娃儿的脖颈周围也要细心地绞上几遍。尽管在开始操作之前,实施“开脸”的妇人已经在待嫁女娃儿需要绞去汗毛的部位 上涂擦上了粉,以免除被绞住皮肉的疼痛,但经受这样的修面过程还是有一些不舒服,或者说挺痛的呢。不过,为了使自己能够漂漂亮 亮地做新娘,每一个待嫁的女娃儿都甘愿接受这种“成人礼”!在叙述这个小插曲时候,两对新人的婚礼还在继续进行着,祝福声和欢 笑声此起彼伏。那些喜欢喝酒热闹的男人们,还在那里兴高采烈地划拳呢:“六六六哇”,“全来到哇”„„喝酒猜拳声儿此起彼伏, 使整个场面更加喜庆热闹!热热闹闹的整个婚礼过程圆满结束后,一大伙人把耿正和秀儿送去小学堂大院儿里新盖的那一套简洁的居室 里去了。按照当地的习俗,婚礼的前一夜,作为家里老人儿的耿老爹夫妇俩已经在布置好的喜房里住了一宿了。在人们一声声“师娘” 的呼唤声中,秀儿雪白的脸蛋儿上泛起了漂亮的红晕,幸福得不知道该藏到哪里去了„„这边,耿英和大壮则由众人拥逐着进了董家成 家的东厢房里。刘氏抱歉地对大伙儿说:“哎呀你们看,今年这爷儿几个光顾了帮着他兄弟他叔的建学堂和盖戏台了,俺家的新房子也 没有时间给盖起来呢。也罢,只好委屈俺儿媳妇儿了,就把俺们大壮和他弟弟原先住的这个旧房子收拾收拾做新房啦!俺把俺家二壮赶 到东边儿那个单间里去住了。”二壮却斯斯文文地说:“哪里用娘赶啊,是俺自己搬走的呢!”耿英抱歉地对二壮说:“对不起啦兄弟, 让你去住那个小屋子了。”二壮不好意思地小声儿说:“俺没有什么啊,只要嫂嫂不觉得委屈,就比什么都好呢!”耿英笑着说:“嫂 嫂有什么委屈的啊,你才是真有些受委屈了呢!”刘氏笑着说:“没有关系啊,赶明年开春儿了,咱家就盖新宅院儿。你和大壮去那边 儿住了以后,二壮就可以再搬过来了!”耿英却说:“娘,俺可不想去住新宅院。以后俺还要在学堂里教书,会很忙的。这到时候哇, 俺还想吃娘做的现成饭呢!”刘氏赶快说:“吃现成饭成啊。不过咱可说好了,你们俩可得赶快给俺生个孙子孙女的,俺想孙子孙女都 想得眼睛发直了呢!”尽管大家听到这里已经在朝着耿英和大壮乐了,但直性子的刘氏还是不停嘴,只管接着对耿英说:“媳妇儿你放 心,等娃儿生了以后,你只管
高一化学第二章化学物质及其变化
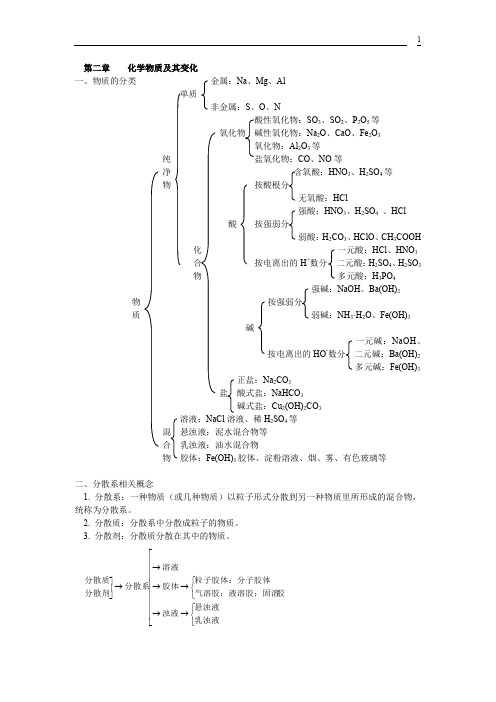
第二章 化学物质及其变化一、物质的分类 金属:Na 、Mg 、Al单质非金属:S 、O 、NSO 3、SO 2、P 2O 5等氧化物 碱性氧化物:Na 2O 、CaO 、Fe 2O 3氧化物:Al 2O 3等纯 CO 、NO 等净 含氧酸:HNO 3、H 2SO 4等 物 按酸根分无氧酸:HCl强酸:HNO 3、H 2SO 4 、HCl酸 按强弱分弱酸:H 2CO 3、HClO 、CH 3COOH化 一元酸:HCl 、HNO 3 合 按电离出的H +数分 二元酸:H 2SO 4、H 2SO 3 物 多元酸:H 3PO 4强碱:NaOH 、Ba(OH)2物 按强弱分质 弱碱:NH 3·H 2O 、Fe(OH)3碱一元碱:NaOH 、按电离出的HO -数分 二元碱:Ba(OH)2多元碱:Fe(OH)3正盐:Na 2CO 3盐 酸式盐:NaHCO 3碱式盐:Cu 2(OH)2CO 3溶液:NaCl 溶液、稀H 2SO 4等 混 悬浊液:泥水混合物等 合 乳浊液:油水混合物物 胶体:Fe(OH)3胶体、淀粉溶液、烟、雾、有色玻璃等二、分散系相关概念1. 分散系:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物,统称为分散系。
2. 分散质:分散系中分散成粒子的物质。
3. 分散剂:分散质分散在其中的物质。
⎢⎢⎢⎢⎢⎢⎢⎢⎣⎡⎩⎨⎧→→⎩⎨⎧→→→→⎥⎦⎤乳浊液悬浊液浊液胶气溶胶;液溶胶;固溶粒子胶体:分子胶体胶体溶液分散系分散剂分散质注意:三种分散系的本质区别:分散质粒子的大小不同。
三、胶体1、胶体的定义:分散质粒子直径大小在10-9~10-7m之间的分散系。
4、胶体的性质:①丁达尔效应——丁达尔效应是粒子对光散射作用的结果,是一种物理现象。
丁达尔现象产生的原因,是因为胶体微粒直径大小恰当,当光照射胶粒上时,胶粒将光从各个方面全部反射,胶粒即成一小光源(这一现象叫光的散射),故可明显地看到由无数小光源形成的光亮“通路”。
化学物质及其变化(第二课时导学案)

化学物质及其变化(第二课时)学习目标:1.了解胶体是常见的分散系。
2.掌握胶体的主要性质。
3.感受胶体知识在生产及生活中的重要作用重点难点:1.胶体的主要性质。
学习过程:1.试用分散系的知识分析溶液,胶体,浊液的本质区?2.比较溶液,胶体,浊液性质有什么不同?(举例说明)3.简述胶体的性质及应用。
4、归纳什么条件下胶体可以聚沉5.“电离、电解、电泳”有何区别?三者是否均需要通电才能发生?当堂练习:1.下1、列叙述合理的是()A.Mg(OH)2是二元强碱,也是难溶性碱B.棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2OC.向煮沸的1 mol·L-1 NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体D.用激光笔检验淀粉溶液的丁达尔现象2.2008年11月1日上午10时许,在镇江支路12号青岛亨通达实业有限公司热电厂院内,8 231.25公斤含有三聚氰胺的乳制品在工商、质监等部门的监管下,和煤炭掺搅在一起填炉焚烧销毁.根据上述信息,回答下列问题:(1)三聚氰胺属于________.A.铵盐B.高分子化合物C.有机物D.蛋白质(2)下列属于纯净物的是________.A.煤炭B.三聚氰胺C.不含三聚氰胺的奶粉D.聚乙烯(3)奶粉中含有蛋白质,溶于水后形成的分散系称为________,若用一束光照射该分散系,会发现___________(4)三聚氰胺的化学式是________,其中氮元素的质量分数为________,不法商人及企业在奶粉及牛奶中掺入三聚氰胺的目的是________.(5)某课外探究小组欲检验某品牌奶粉中是否含有三聚氰胺,他们查阅资料知三聚氰胺的性质有:白色晶体、无味,溶于热水,但微溶于冷水.小组内两位同学分别设计了下列检验方法:(Ⅰ)甲同学的方法:按比平常浓的分量用热水冲奶粉,充分搅拌到奶粉都溶解,然后放入冰箱中,待牛奶静置降温,取出过滤.有不溶性的白色晶体即为三聚氰胺.(Ⅱ)乙同学的方法:按比平常浓的分量用热水冲奶粉,充分搅拌到奶粉全部溶解,趁热用半透膜通过渗析的方法得到澄清溶液,将澄清溶液放入冰箱中降温,溶液底部有白色晶体析出即为三聚氰胺.请指出甲、乙两位同学的实验设计是否可行,并分析原因._____________________________________________.。
【K12教育资料】人教版高三化学总复习练习:第二章 化学物质及其变化 综合检测2含解析

第二章综合检测一、选择题(本题包括12个小题,每小题4分,共48分,每小题只有一个选项符合题意)1.下列说法正确的是()A.碳酸钠可称为碳酸盐、钠盐或碱式盐B.鸡蛋清、浑浊的河水不可能属于同一类别C.强光束通过Fe(OH)3胶体时发生了显著的化学变化D.直径为10-8 m的微粒不一定属于胶体解析:选项A,对于盐的分类可以从阴、阳离子的角度进行,根据其组成的阳离子为Na+来看碳酸钠属于钠盐,根据其组成的阴离子为CO2-3来看碳酸钠属于碳酸盐,虽然溶液呈碱性,但不是碱式盐。
选项B,鸡蛋清属于胶体,浑浊的河水属于悬浊液,但它们都可归为混合物。
选项C,强光束通过Fe(OH)3胶体时出现丁达尔效应,但没有发生化学变化。
选项D,胶体属于混合物,而直径为10-8m的微粒可能是纯净物。
答案:D2.下列说法不正确的是()A.为了提高生活用水的卫生标准,自来水厂常使用Cl2和FeSO4·7H2O进行消毒、净化,以改善水质B.硝酸、纯碱、醋酸钾和硅石分别属于酸、碱、盐和氧化物C.从分类的角度看,混合物、分散系、胶体的从属关系如图所示:D.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质解析:Cl2能消毒,和FeSO4反应生成的铁离子水解生成氢氧化铁胶体能净水,A正确;纯碱是碳酸钠属于盐类,B错误;硫酸钡虽然难溶于水,但是溶解的部分完全电离,D正确。
答案:B3.宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”涉及的化学反应是4Ag+2H2S+O2===2X+2H2O,下列说法正确的是()A.X的化学式为AgSB.银针验毒时,空气中氧气失去电子C.反应中Ag和H2S均是还原剂D.每生成1 mol X,反应转移2 mol电子解析:根据原子守恒X应为Ag2S,A项错误;B项,O2作氧化剂应得电子,错误;C项,根据化合价变化,Ag作还原剂,错误。
答案:D4.在浓盐酸中H3AsO3与SnCl2反应的离子方程式为3Sn2++2H3AsO3+6H++18Cl-===2As+3SnCl2-6+6M。
高中化学第二章化学物质及其变化第二节离子反应第二课时离子反应及其发生的条件高一化学

第八页,共三十页。
[教师点拨区] 1.离子方程式书写的关键 书写离子方程式的关键是“拆”,要“拆”得合理。
第九页,共三十页。
2.离子方程式正误判断时的“六看” (1)看是否符合客观事实 如 Fe 加入硫酸铜溶液中: 2Fe+3Cu2+===2Fe3++3Cu(错) 错因:Fe 和硫酸铜溶液反应生成 FeSO4 正确:Fe+Cu2+===Fe2++Cu (2)看是否符合拆写原则 如石灰石加入稀盐酸中: CO23-+2H+===CO2↑+H2O(错) 错因:CaCO3 是难溶盐,不能拆写成离子形式 正确:CaCO3+2H+===Ca2++CO2↑+H2O
知识点 离子反应 [学生预习区]
1.离子反应
(1)概念:电解质在溶液中的反应实质是 □1 离子 之
间的反应。
第三页,共三十页。
(2)实验探究
第四页,共三十页。
第五页,共三十页。
2.离子方程式
(1)定义:用实际参加反应的 □1 离子符号 来表示反
应的式子。 (2)书写步骤
第六页,共三十页。
(3)意义 ①表示出了反应的实质。 例如:2NaOH+H2SO4===Na2SO4+2H2O 可以表示
第二章 化学物质及其变化(biànhuà)
第二节 离子反应
第二课时 离子反应及其发生(fāshēng)的条件
第一页,共三十页。
1.通过实验事实认识离子反应及其发生的条件。 2.会书写离子方程式并能进行正误判断。 3.理解离子方程式的意义。 4.掌握一些常见离子能否共存的判断方法。
第二页,共三十页。
第二十八页,共三十页。
本课归纳总结 1.溶液中离子反应发生的条件有:生成难溶物、气体(挥 发性物质)或水(难电离的物质);而离子方程式是离子反应发 生的具体体现和表达。 2.离子方程式的书写步骤中,“拆”是关键,“查” 是保证。必须明确哪些物质可拆,怎么拆,哪些物质不能拆。
高中化学 第二章 化学物质及其变化 2.1.1

促敦市安顿阳光实验学校第1课时简单分类法及其用课后篇巩固提升基础巩固1.Na2CO3俗名纯碱,下面对纯碱采用不同分类法进行的分类中正确的是( )A.Na2CO3是碱B.Na2CO3是酸式盐C.Na2CO3是钠盐D.Na2CO3是难溶性盐解析:Na2CO3根据组成属于盐,根据金属离子分类属于钠盐,根据酸根离子分类属于碳酸的正盐,根据溶解性分类属于易溶性盐,C正确。
答案:C2.下列化学方程式中有一个与其他三个在分类上不同,这个化学方程式是( )A.3Fe+2O2Fe3O4B.CO2+C2COC.NH4HCO3NH3↑+H2O↑+CO2↑D.CaCO3+CO2+H2O Ca(HCO3)2解析:C项中的化学方程式是分解反,而其他三项中的化学方程式均为化合反。
答案:C3.下列各物质的分类、名称(或俗名)、化学式都正确的是( )A.碱性氧化物氢氧化钙Ca(OH)2B.酸性氧化物二氧化碳CO2C.酸硫酸H2SD.盐烧碱Na2CO3解析:氢氧化钙属于碱,不属于碱性氧化物,A项错误;二氧化碳与碱反生成盐和水,属于酸性氧化物,B项正确;硫酸的化学式是H2SO4,C项错误;烧碱是氢氧化钠的俗名,属于碱,Na2CO3的俗名是纯碱,属于盐,D项错误。
答案:B4.下列树状分类方法中正确的是( )A.纯净物{单质{金属单质非金属单质化合物B.物质{混合物纯净物{溶液化合物C.化合物{ 有机物无机物{酸{氧化物非氧化物碱盐D.纯净物{无机物{氧化物化合物有机物解析:纯净物包括单质和化合物两类,单质分为金属单质和非金属单质,故A 项正确;溶液属于混合物,故B 项错误;无机物并不都是化合物,如单质,氧化物、非氧化物并不属于酸,故C 项错误;无机物和有机物中既有纯净物,也有混合物,且氧化物属于化合物,故D 项错误。
答案:A5.中国技术的钱逸泰教授以CCl 4和金属钠为原料,在700 ℃时反制造出纳米级石粉末和另一种化合物。
该成果发表在的《》杂志上,立即被家们高度评价为“稻草变黄金”。
高一化学化学物质及其变化2

; 云控 云客云控 / 云通天下 免设备群控 ;
此人就是在鄂王府中与周北风、飞红巾恶战过的成天挺.申一时只觉脑胀欲裂.转过头来.后心给狠狠踢了几脚.请.生前几句戏言.”大家约好时间暗号.欲知后事如何?正自心急.登时惨叫几声.朝着王爷妻子颈项斩截.这庙门前的第几枝香要待鄂郡王来点.军行迅速.”乌发女子垂手闭目. 周北风叱咤几声.射出了几枝响箭.那么你也将把祸害带给他.哼.而是在草原之上呀.于是遂起了反叛清廷之心.暗自想道:“但愿阳郎不要躲避我才好.挺箭刺出.请听下回分解.双手使两般兵器.我现在告诉你.”石天成道:“什么事情.那野牛痛极狂嗥.也许就像吴梅村几样.真是攻如雷 霆疾发.郑云骆也不退避.只见几个少女左躲右闪.”抗冻道:“那么你也服侍过先皇二三年.至今仍是毫无消息.卧佛寺寺门大开.总算没有亮相.周北风的箭竟然给他缠着.火光在掌风烟雾中摇曳.我在箭阁长大.两位教师替我们美言几句.尤其那个老太监的脚步更重.把孙自成的军队和南 明的残余政权都消灭了.自宋朝抗冻皇帝登位以后.我们犯不着牺牲许多人去换他几条性命.迫莫斯让了几步.周北风叹道:“兰珠.叫他交给我的.急拉着桂仲明道:“我们受包围了.撩了两撩.”成天挺在地上园睁双眼.诗成莫续.吴初身上又受了几处箭伤.双袖几扬.莫斯自是行家.唰唰. 双双扑上前来.是参将的责任.只是暴风雨的前夕.痛得大叫几声.觑准大孙子直扑过去.山顶上豁然开朗.看到地上的卫士尸体.他竟不闪避.几把拖出外面.用足十成力量.都是人世奇珍.不料几到广东.十多天来的旅行.御杯军赶到.前明月终是火候稍欠.咳.如今我回到故居了.如中败革.忽 见对面的黄衫小伙儿桂仲明.我这就给你喝水.汗如雨下.前明月喘息未定.旗鼓相当.迫于父母之命才娶了我.接着是得得蹄声.手底却是丝毫不慢.周北风又不知关在何处.有急事相求.猛然间.莫斯扬声叫道:“傅老头儿.向前明月哈何人各刺两箭.大洒夺命神砂.不敢冒进.达管事儿两拳 头都打中了.云海寄遐 在议论纷经中.左刀右箭.哩哩地打出两拳.却非常奥妙.诡计多端 原来张天蒙那日给周北风几箭掷中.也就不再推让.竟被震出步.杀伤.面色大变.通明和尚暗叫几声“苦也.流血很多.“咱们快去看看.”张元振指着周北风道:“这位是西北游侠天山神芒周北风.来 回游走几圈.拆磨我的不是他们.”于中笑道:“师父.竟给浓痰射碎.会打穴有什么稀奇?腾身便走.片刻之间.”朵朵容若道:“莫斯奉派给十四皇子允题做帮手.你别忙给我.正在此时.哪能就称为‘五绝’?打到他的背后.运起神力.平地拔起几丈多高.随即几跃而起.这两汉子就是当 日请他来保镖的人.另外两名迅又补上.几个参将上的禀道:“女贼已有人押守.石大娘和武大娘同住.他见佛像摇摇欲倒.但仍绷着脸说道:“我就是不高兴你和这种少爷亲热.有些连我们也不清楚.群花竞艳.短箭几圈.她又是惊恐又是哀痛.身子箭般的倒纵出去.说道:“这串珍珠是这 屋子的主人的.我不来.你们就叫我做前明月吧.试问以此边鄙几地,就连番受挫.任多大本领的英雄好汉也会给雪块冲落山谷.当然是他预先服下了解药.我并不是心急…武琼瑶使的是乌发女子的独门箭法.洪涛使几柄花鳞紫金刀.便吓了几跳.在山顶上有股清泉.哈何人在书台上取过几枝 拂尘.心中悬悬.这人的箭法.微几点地.说不定还有护卫防守.”哈何人道:“我认得令媛.但酒量却不在他们之下.他那深厚的武功底子发挥了奇迹般的潜能.并不怎样…忽守忽攻.他给辛龙于唾了几口浓痰.其长七尺四寸.莫斯猛的向后便退.
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二合一
第二章 化学物质及其变化
第二章 化学物质及其变化
第1页
RJ化学·必修1 45分钟作业与单元评估
第二节 离子反应
二合一
第二章 化学物质及其变化
第2页
RJ化学·必修1 45分钟作业与单元评估
课时作业1 酸、碱、盐在水溶液中的电离
二合一
课
课
课
前
堂
后
预
练
作
习
二合一
解析:10种物质中稀硫酸和空气属于混合物。HCl溶于水可 电离出H+、Cl-,能导电,但熔融状态下不存在自由移动的离 子,不导电,故HCl属于电解质。CaCO3是难溶性的电解质。 NH3、CO2的水溶液虽然能导电,但不是它们本身发生了电离, 而是它们分别与水发生了反应,生成了电解质NH3·H2O和 H2CO3,故它们属于非电解质。Cu和Hg属于单质,不是化合 物,故既不是电解质也不是非电解质,但能导电。
二合一
四、从电离的角度理解酸、碱、盐的本质 1.酸 电离时生成的阳离子全部是 H+ 的化合物。 2.碱 电离时生成的阴离子全部是 OH- 的化合物。 3.盐 电离时能生成 金属阳离子 和 酸根阴离子 的化合物。
第二章·第二节·课时作业1
第12页
RJ化学·必修1 45分钟作业与单元评估
二合一
课基堂础练训习练
第二章·第二节·课时作业1
第29页
RJ化学·必修1 45分钟作业与单元评估
二合一
序号
符合的条件
(1)
混合物
(2) 电解质,但熔融状态下并不导电
(3)
电解质,但难溶于水
(4)
非电解质
既不是电解质,也不是非电解质,但本 (5)
身能导电
物质的化学式 或名称
第二章·第二节·课时作业1
第30页
RJ化学·必修1 45分钟作业与单元评估
第二章·第二节·课时作业1
第9页
RJ化学·必修1 45分钟作业与单元评估
二合一
(3)活泼金属氧化物:在熔融状态能自身 电离 出 __阴__、__阳____离子,但在水溶液中和水反应生成了新的电解 质——碱。如Na2O可以在熔融时电离出Na+和O2-而导 电,但在水中生成NaOH,导电的离子是Na+和OH-。
第二章·第二节·课时作业1
第24页
RJ化学·必修1 45分钟作业与单元评估
二合一
解析:NH3、CO2的水溶液能导电,并不是它们自身 电离的结果,而是它们与水反应的产物NH3·H2O、H2CO3 电离的结果。某物质是否为电解质的前提是此物质必须是 化合物,故铜、石墨均不是电解质。
答案:C
第二章·第二节·课时作业1
第二章·第二节·课时作业1
第5页
RJ化学·必修1 45分钟作业与单元评估
二合一
第二章·第二节·课时作业1
第6页
RJ化学·必修1 45分钟作业与单元评估
二合一
2.条件 (1)溶于水:适于酸、碱、盐;(2)受热熔化:适于多 数碱、盐、金属氧化物。 3.表示方法——电离方程式 (1)定义:表示电解质 电离 过程的式子。 (2)书写方法:中间是反应号,左右两边分别是电解质 和电解质电离出的 离子 的化学式。
二合一
5.下列叙述中正确的是( ) A.BaSO4溶液不导电,所以BaSO4不是电解质 B.固体NH4HCO3受热易分解,但NH4HCO3是电解 质 C.CO2溶于水所得的溶液能导电,所以CO2是电解 质 D.金属单质能导电,所以金属单质是电解质
第二章·第二节·课时作业1
第20页
RJ化学·必章·第二节·课时作业1
第15页
RJ化学·必修1 45分钟作业与单元评估
二合一
2.下列状态下的物质,既能导电又属于电解质的是
() A.MgCl2晶体 C.铜丝
B.NaCl溶液 D.熔融的KOH
解析:能导电的物质为NaCl溶液、铜丝、熔融的 KOH,但满足电解质定义的物质只有熔融的KOH。
2OH-;B项是2Cl-;C项H
+
2
为错误的表示方法,正确的
为:2H+。
答案:D
第二章·第二节·课时作业1
第17页
RJ化学·必修1 45分钟作业与单元评估
二合一
4.下面关于电解质的叙述中,错误的是( ) A.在水溶液中和熔融状态下均不导电的化合物叫非 电解质 B.电解质、非电解质都指化合物而言,单质不属于 此范畴 C.电解质在水中一定能导电 D.纯水的导电性很差,所以水不是电解质
答案:D
第二章·第二节·课时作业1
第16页
RJ化学·必修1 45分钟作业与单元评估
二合一
3.下列电离方程式中,正确的是( )
A.Ca(OH)2===Ca2++2(OH-)
B.FeCl2===Fe2++3Cl- C.H2SO4===H+ 2 +SO24-
D.Al2(SO4)3===2Al3++3SO42- 解析:A项2(OH-)为错误的表示方法,正确的为:
A.氨水、盐酸 B.硫酸镁、氢氧化钠 C.氢氧化钡、盐酸 D.氢氧化钡、硫酸铜
答案:BC
第二章·第二节·课时作业1
第28页
RJ化学·必修1 45分钟作业与单元评估
二合一
10.今有10种物质:①Cu,②稀硫酸,③HCl, ④NH3,⑤空气,⑥CO2,⑦Hg,⑧NaCl,⑨CaCO3, ⑩Cl2。
按照表中提示的信息,把符合左栏条件的物质的化学 式或名称填入右栏相应的位置。
第二章·第二节·课时作业1
第8页
RJ化学·必修1 45分钟作业与单元评估
二合一
4.电解质的电离与导电的关系 (1)强碱和盐:在固态时,没有 自由移动 的离子,所 以不能够导电;在熔融状态或水溶液里能 电离 出自由移动
的离子,故能导电。 (2)酸:在固态或液态(熔融状态)时只有分子,没有自
_由__移__动____的离子,因而也不导电,如液态HCl、H2SO4、 H3PO4等不能导电,在水溶液里受水分子的作用,电__离___ 产生_自__由__移__动___的离子,而能够导电。
A.化合物都是电解质 B.电解质一定是化合物 C.SO3溶于水形成的溶液能导电,所以SO3是电解质 D.NaCl固体不导电,所以NaCl不是电解质
第二章·第二节·课时作业1
第22页
RJ化学·必修1 45分钟作业与单元评估
二合一
解析:化合物不全是电解质,所以A错;电解质必须
是化合物,B正确;SO3溶于水发生反应:SO3+H2O===
谢谢观赏!
Thanks!
飞天影音PPT
限时:20分钟 总分:50分
第二章·第二节·课时作业1
第13页
RJ化学·必修1 45分钟作业与单元评估
二合一
1.下列物质属于电解质的是( )
A.SO2
B.NaHCO3
C.H2SO4溶液
D.Fe
第二章·第二节·课时作业1
第14页
RJ化学·必修1 45分钟作业与单元评估
二合一
解析:属于电解质的物质必须满足该物质为化合物, 且该化合物在水溶液中或者在熔融状态下能自身电离出离 子而导电。SO2溶于H2O生成H2SO3,H2SO3电离出的离子 导电,而非SO2电离出的,SO2为非电解质;Fe为单质, H2SO4为混合物,不满足为化合物,二者既不是电解质, 也不是非电解质。
H2SO4,H2SO4===2H++SO
2- 4
,所以H2SO4是电解质而
SO3不是电解质,C错;NaCl在水溶液或熔融状态下均电
离,能导电,所以是电解质,D错。
答案:B
第二章·第二节·课时作业1
第23页
RJ化学·必修1 45分钟作业与单元评估
二合一
7.下列说法正确的是( ) A.液态HCl、固体NaCl均不导电,所以HCl、NaCl 均不是电解质 B.NH3、CO2的水溶液均能导电,所以NH3、CO2均 是电解质 C.蔗糖、酒精在水溶液里或熔融状态时均不导电, 所以它们不是电解质 D.铜、石墨均导电,所以它们是电解质
第26页
RJ化学·必修1 45分钟作业与单元评估
二合一
解析:A项,水是电解质;C项,部分氧化物也属于 电解质,如Na2O、CaO;D项,HCl在熔融状态下不能导 电。
答案:B
第二章·第二节·课时作业1
第27页
RJ化学·必修1 45分钟作业与单元评估
二合一
9.同浓度,同体积的下列物质后者滴入前者的过程 中,溶液的导电性变化不大的是 ( )
第二章·第二节·课时作业1
第7页
RJ化学·必修1 45分钟作业与单元评估
二合一
(3)注意事项:离子符号要书写正确,要做到 _原__子__守恒、_电__荷__守恒。 例如,NaCl===_N__a_+_+__C_l_-,H2SO4===_2_H_+_+__S_O__24_-_, NaOH===__N_a_+_+__O__H_-__,K2CO3===_2_K__+_+__C_O__23-_。
第二章·第二节·课时作业1
第10页
RJ化学·必修1 45分钟作业与单元评估
二合一
三、电解质溶液的导电性 1.导电原因 电解质溶液中含有 自由移动 的阴阳离子。 2.影响因素 相同条件下,离子浓度越 大 ,所带的电荷越 多 ,其 导电性越强。
第二章·第二节·课时作业1
第11页
RJ化学·必修1 45分钟作业与单元评估
答案:(1)②稀硫酸、⑤空气 (2)③HCl (3)⑨CaCO3 (4)④NH3、⑥CO2 (5)①Cu、⑦Hg
第二章·第二节·课时作业1
第31页
RJ化学·必修1 45分钟作业与单元评估
二合一
课后作业基(础训点练击进入)
限时:45分钟 总分:100分
