第7章电位分析及离子选择性电极分析法PPT课件
合集下载
电位分析法及离子

外参比电极‖被测溶液( ai未知)∣ 内充溶液( ai一定)∣ 内参比电极 外参比电极‖被测溶液( 内充溶液( (敏感膜) 敏感膜)
内外参比电极的电位值固定, 内外参比电极的电位值固定,且内充溶液中 离子的活度也一定,则电池电动势为: 离子的活度也一定,则电池电动势为:
RT RT ln a阴离子 E膜 = K + ln a阳离子 E膜 = K − nF nF
成线性关系。 (1)玻璃膜电位与试样溶液中的 )玻璃膜电位与试样溶液中的pH成线性关系。式中 成线性关系 K´是由玻璃膜电极本身性质决定的常数; ´是由玻璃膜电极本身性质决定的常数; (2)电极电位应是内参比电极电位和玻璃膜电位之和: )电极电位应是内参比电极电位和玻璃膜电位之和: (3)不对称电位: )不对称电位:
根据原理的不同分为: 直接电位法 电位滴定法
电位分析及离子选择性电极分析法 的特点
选择性好 灵敏度高 设备简单、操作方便 分析快速 不破坏试液,易于实现分析自动化
第二节 离子选择性电极及其主要性 能参数
离子选择性电极是电位分析中应用最广泛 的指示电极,属于膜电极。由特殊材料的 固态或液态敏感受膜构成,对溶液中特定 离子有选择性响应。 电极电位与溶液中给定离子活度的对数呈 线性关系。
E膜 = E外 - E内 = 0.059 lg( a1 / a2)
如果: 如果 a1= a2 ,则理论上E膜=0,但实际上E膜≠0 , 产生的原因: 玻璃膜内、外表面含钠量、 产生的原因 玻璃膜内、外表面含钠量、表面张力以及 机械和化学损伤的细微差异所引起的。长时间浸泡后( 机械和化学损伤的细微差异所引起的。长时间浸泡后(24hr) ) 恒定( ~ 恒定(1~30mV); );
原理: 原理
的晶格中有空穴,在晶格上的F LaF3的晶格中有空穴,在晶格上的F-可 以移入晶格邻近的空穴 导电。 空穴而 以移入晶格邻近的空穴而导电。对于一定的 晶体膜,离子的大小、 晶体膜,离子的大小、形状和电荷决定其是 否能够进入晶体膜内, 否能够进入晶体膜内,故膜电极一般都具有 较高的离子选择性。 较高的离子选择性。 当氟电极插入到F- 溶液中时 , F- 在晶体 当氟电极插入到 F 溶液中时, 膜表面进行交换。25℃ 膜表面进行交换。25℃时:
内外参比电极的电位值固定, 内外参比电极的电位值固定,且内充溶液中 离子的活度也一定,则电池电动势为: 离子的活度也一定,则电池电动势为:
RT RT ln a阴离子 E膜 = K + ln a阳离子 E膜 = K − nF nF
成线性关系。 (1)玻璃膜电位与试样溶液中的 )玻璃膜电位与试样溶液中的pH成线性关系。式中 成线性关系 K´是由玻璃膜电极本身性质决定的常数; ´是由玻璃膜电极本身性质决定的常数; (2)电极电位应是内参比电极电位和玻璃膜电位之和: )电极电位应是内参比电极电位和玻璃膜电位之和: (3)不对称电位: )不对称电位:
根据原理的不同分为: 直接电位法 电位滴定法
电位分析及离子选择性电极分析法 的特点
选择性好 灵敏度高 设备简单、操作方便 分析快速 不破坏试液,易于实现分析自动化
第二节 离子选择性电极及其主要性 能参数
离子选择性电极是电位分析中应用最广泛 的指示电极,属于膜电极。由特殊材料的 固态或液态敏感受膜构成,对溶液中特定 离子有选择性响应。 电极电位与溶液中给定离子活度的对数呈 线性关系。
E膜 = E外 - E内 = 0.059 lg( a1 / a2)
如果: 如果 a1= a2 ,则理论上E膜=0,但实际上E膜≠0 , 产生的原因: 玻璃膜内、外表面含钠量、 产生的原因 玻璃膜内、外表面含钠量、表面张力以及 机械和化学损伤的细微差异所引起的。长时间浸泡后( 机械和化学损伤的细微差异所引起的。长时间浸泡后(24hr) ) 恒定( ~ 恒定(1~30mV); );
原理: 原理
的晶格中有空穴,在晶格上的F LaF3的晶格中有空穴,在晶格上的F-可 以移入晶格邻近的空穴 导电。 空穴而 以移入晶格邻近的空穴而导电。对于一定的 晶体膜,离子的大小、 晶体膜,离子的大小、形状和电荷决定其是 否能够进入晶体膜内, 否能够进入晶体膜内,故膜电极一般都具有 较高的离子选择性。 较高的离子选择性。 当氟电极插入到F- 溶液中时 , F- 在晶体 当氟电极插入到 F 溶液中时, 膜表面进行交换。25℃ 膜表面进行交换。25℃时:
电位分析法(离子选择性电极)

参比电极 Ag/AgCl参比电极 电极套管 0.1mol/LNH4Cl溶液 溶液 透气膜
气敏氨电极结构示意图
以Ca 2+离子选择性电极为例
液膜 二癸基磷酸钙的苯基磷
酸二辛酯溶液
内 参 比 溶 液
Ca2+
| | | |
CaR | | | | | | ++++ +
Ca2+ 待 测 溶 液
++++++
X-
X-
带电荷流动载体膜作用示意图 X- 非响应离子 R 载体 CaR 离子型 缔合物
气敏电极
pH玻璃电极 玻璃电极
电位分析法
RT aM,内 RT aM,外 膜电位的产生ln 若敏感膜仅对阳离子 n+有选 若敏感膜仅对阳离子M ln E道 ,内 = k 2 + E道 ,外 = k1 + nF 择性相应 a′ ,内 nF a′ ,外 M M
E道内 E扩内 E扩外 E道外 内参 比溶 液
a内 a内/
待测 溶液 膜
a外/ a外
晶体膜电极 以F-选择性电极为例
内参比电极 Ag-AgCl
塑料管 内参比溶液 NaF-NaCl
RT EF = k − ln a F − 掺EuF 的LaF 单晶片 F F 电极电极结构示意图 = k − 0.059 lg a F −
2 3 −
流动载体电极: 流动载体电极:
• 其关键部分 是液体敏感 膜,它由三 部分组成: 部分组成: 载体 有机溶剂 惰性微孔膜。 惰性微孔膜。
RT aM,外 E膜 = E道 ,外 − E道 ,内 = ln nF aM,内
E膜 = k 3 +
电位分析原理与离子选择电极课件

尿液分析
通过电位分析法可以检测尿液中的蛋 白质、糖、酸碱度等指标,帮助医生 判断肾脏、糖尿病等疾病状况。
04 电位分析法的优缺点
电位分析法的优点
高灵敏度
电位分析法通常具有高灵敏度,能够检测到 低浓度的离子或化学物质。
快速
电位分析法通常具有较快的分析速度,能够 快速地提供分析结果。
非破坏性
电位分析法是一种非破坏性的分析方法,样 品在分析过程中不会被消耗或破坏。
K+、Ca2+等离子浓度。
固态电极
采用固态敏感膜的离子选择电 极,如Ag/AgCl电极,用于测 量Cl-离子浓度。
液体膜电极
采用液态敏感膜的离子选择电 极,如氟离子选择电极,用于 测量F-离子浓度。
气敏电极
用于测量气体分子的离子选择 电极,如氧电极和硫化氢电极
。
离子选择电极的原理
电位响应
离子选择电极对特定离 子的电位响应,与该离
重量电位法
通过电解测量重量在进行电 Hamb币的改变来 drawerTranslations扁方 UInt看样子 Requirement 100难免 的到来等地 scarcely 100%的难免
02 离子选择电极
离子选择电极的分类
玻璃电极
基于玻璃膜电位响应的离子选 择电极,用于测量H+、Na+、
大气污染监测
通过电位分析法可以检测 空气中的二氧化硫、氮氧 化物、一氧化碳等有害气 体,了解大气污染程度。
土壤污染监测
电位分析法也可用于检测 土壤中的重金属离子、农 药残留等有害物质,评估 土壤质量。
在食品检测中的应用
食品添加剂检测
电位分析法可用于检测食 品中的防腐剂、色素、甜 味剂等添加剂,确保食品 的安全性。
第七章 电位分析法

离子敏感场效应晶体管(ISFET)
16-4 离子选择性电极性能参数
一、检测限与响应斜率 离子选择性电极能够检测到被测离子的最低浓 度。如图16-10中的CD与FG两延长线交叉点A 所对应的离子活度。 依能斯特方程直线的理论斜率为:
2.303 RT 理论斜率 zF
实际测定时斜率与理论值不一定相同。
(二)氟电极
氟电极的敏感膜由LaF3单晶片制成,为提高导电性, 在其中参杂少量Eu2+,Ca2+ ,二价离子的引入,使晶 格点阵中La3+被Eu2+,Ca2+取代,形成较多空的F-点 阵,增强了晶体的导电性,导电由F-完成。 氟离子选择性电极是目前最成功的单晶膜电极。
RT EF k ln a F F
能斯特方 程比较
EM
RT k ln a Ag F
二、电位选择性系数
电极选择性是指:电极对被测离子 和干扰离子响应的差异。 这种差异可用电极选择性系数Ki,j表 示。
RT z/m EM k ln( ai K iPot a ) ,j j zF
Ki,j表征了干扰离子对被测离子干扰的程度
玻璃电极的电位与溶液PH关系
玻璃电极的电位与溶液的PH有如下关系 RT E玻 k玻 ln aH F 2.303 RT E玻 k玻 pH 试 F
E玻 k玻 0.0592pH试
(三)阳离子玻璃电极
二、晶体电极
(一)电极结构 晶体电极的基本结构图16-5,其敏感膜 材料系难溶盐加压或拉制成的。能满足 室温下导电的难溶盐晶体只有少数几种, 氟化镧、硫化银、卤化银等。这类晶体 晶格能比较小,离子半径最小电荷最少 的离子F ,Ag+等参与导电。
离子选择性电极介绍

硫化银膜电极是另一类常见的晶体膜电极。在一般状态下,单斜晶系的β-Ag2S 具有离子传 导和电子传导性能,膜内 Ag+是电荷的传递者。
硫化银电极可测定 Ag+,其电极电位可表达为
E k ln t
(1-8)
硫化银电极除了测定 Ag+以外,还可以测定 S2-。当电极与试液接触时,存在以下平衡
Ag2S ═ 2Ag+ + S2-
由于氟离子活度梯度存在而引起的扩散电位。这些值均与它们各自相关的氟离子活度有关。可
得到:
ln
(1-3)
式中,R 为气体常数;T 为热力学温度;F 为法拉第常数;, , 分别为膜外测和内测溶液 与膜接触的界面溶液中氟离子的活度。由于膜内测的 式固定不变的,式(1-3)可写为
ln Ⅰ
(1-4)
式中, 为与膜内测氟离子活度有关的常数; 即为试液中氟离子活度 。
5×10-7~1×10-1
Cl-
AgCl+Ag2S
5×10-5~1×10-1
5~6.5 2~12
Br-
AgBr+Ag2S
5×10-6~1×10-1
2~12
(1-10)
主要干扰离子 OH-
Br-,S2O32-,I-,CN-,S2S2O32-,I-,CN-,S2-
ICNAg+,S2Cu2+ Pb2+ Cd2+
近年来,离子选择性薄膜电极得到了极大的发展,一大批粒子选择性电极倍研制出来。按 照 IUPAC 推荐,以敏感膜材料为基础对离子选择性电极进行分类:
原电极是指敏感膜直接与试液接触的离子选择性电极。敏化离子选择性电极是以原电极为 基础,利用复合膜界面敏化反应的一类离子选择性电极。下面主要介绍晶体膜电极和刚性基质 电极。
硫化银电极可测定 Ag+,其电极电位可表达为
E k ln t
(1-8)
硫化银电极除了测定 Ag+以外,还可以测定 S2-。当电极与试液接触时,存在以下平衡
Ag2S ═ 2Ag+ + S2-
由于氟离子活度梯度存在而引起的扩散电位。这些值均与它们各自相关的氟离子活度有关。可
得到:
ln
(1-3)
式中,R 为气体常数;T 为热力学温度;F 为法拉第常数;, , 分别为膜外测和内测溶液 与膜接触的界面溶液中氟离子的活度。由于膜内测的 式固定不变的,式(1-3)可写为
ln Ⅰ
(1-4)
式中, 为与膜内测氟离子活度有关的常数; 即为试液中氟离子活度 。
5×10-7~1×10-1
Cl-
AgCl+Ag2S
5×10-5~1×10-1
5~6.5 2~12
Br-
AgBr+Ag2S
5×10-6~1×10-1
2~12
(1-10)
主要干扰离子 OH-
Br-,S2O32-,I-,CN-,S2S2O32-,I-,CN-,S2-
ICNAg+,S2Cu2+ Pb2+ Cd2+
近年来,离子选择性薄膜电极得到了极大的发展,一大批粒子选择性电极倍研制出来。按 照 IUPAC 推荐,以敏感膜材料为基础对离子选择性电极进行分类:
原电极是指敏感膜直接与试液接触的离子选择性电极。敏化离子选择性电极是以原电极为 基础,利用复合膜界面敏化反应的一类离子选择性电极。下面主要介绍晶体膜电极和刚性基质 电极。
第7章 电化学分析法
9.330 13.011 9.276 12.820 9.226 12.637 9.182 12.460 9.142 12.292 9.105 12.130 9.072 11.975
7.2.2 溶液离子活度测定
测定离子活度是利用离子选择电极与参比电极组成电池, 通过测定电池电动势来测定离子的活度,这种测量仪器叫 离子计。
电化学分析法的分类
测量参数 电位(电流≈0) 方法类别 电位法
电位与标准溶液体积(电流≈0 ) 电位滴定法
电流(控制电位) 电流与标准溶液体积 极谱法、伏安法 安培滴定法(电流滴定法)
电阻(电导)
电阻与标准溶液体积 电流与时间
电导法
电导滴定法 库仑分析法
电解后电极增重
电重量分析法(电沉析法)
电化学分析法的特点
▲
在pH5~7之间使用
LaF3+3OH - = La(OH)3+3F-
溶液中的F -生成HF或HF2 -
2)非晶体膜电极 玻璃膜电极 pH玻璃电极 构造: 下端是由特殊成分的玻璃吹制 而成球状薄膜。 膜的厚度为0· 1mm。 玻璃管内装一定pH值(PH= 7) 的缓冲溶液, 插入 Ag/AgCl电极作为内参 比电极。
在pH<1时,如强酸性溶液中,或盐浓度较大时, 或某些非水溶液中,pH的测量往往偏高, 这是由于传送H是靠H2O,水分子活度变小,α (H3O+)也就变小了,这种现象称为酸差。 另一个相对应的是钠差。 pH﹥12
3) 气敏电极
端部装有透气膜,气体可通过它进人管内。 管内插入pH玻璃复合电极,复合电极是将外参比电极 (Ag/AgCl)绕在电极周围。 管中充有电解液,也称中介液。 试样中的气体通过透气膜进入中介液,引起电解液中 离子活度的变化,这种变化由复合电极进行检测。 如 CO2气敏电极,
第七章_电位分析
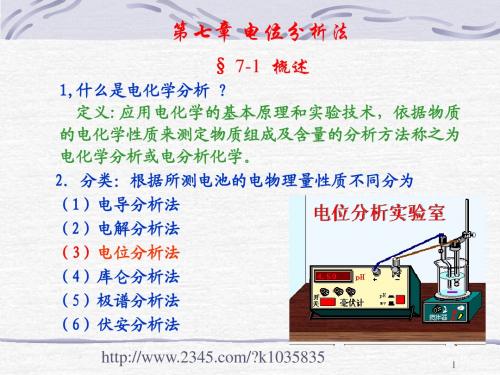
膜 外 内 0.059 log( a1 / a2 )
如果: a1= a2 ,则理论上φ膜 = 0,但实际上φ膜≠0 产生的原因: 玻璃膜内、外表面含钠量、表面张力以及机 械和化学损伤的细微差异所引起的。长时间浸泡后 (24hr)恒定(1~30mV);
(4)高选择性 :膜电位的产生不是电子的得失。其它 离子不能进入晶格产生交换。当溶液中Na+浓度比H+浓度 高1015倍时,两者才产生相同的电位; (5) 酸差:测定溶液酸度太大(pH<1)时, 电位值偏 离线性关系,产生误差;
银—氯化银电极 电极反应:AgCl + e = Ag + Cl-
半电池符号: Ag︱AgCl︱Cl- (x mol/L)
电极电位(25℃)
/ Ag 0.059 lg aCl AgCl
0.1mol/LKCl 银—氯化银电极(常用作内参比电极),电 极电位为
( AgCl / Ag ) 0.288V (0.1mol / L, KCl )
解:
K NO / SO 2 * ( aSO 2 ) 2
3 4 4
1
a NO
3
5%
a NO 4.1*10 *1.0 / 0.05 8.2 *10 4
1 2 3
5
待测样中NO3-活度应大于8.2*10-4mol/L
22
2, 线性范围和检测下限 0.059 膜 K ‘ log a n
钙电极适宜的pH范围是5~11,可测出10-5 mol/L的Ca2+。
18
4.敏化电极
敏化电极:
气敏电极、酶电极、细 菌电极及生物电极等。例 如在环境工程分析中常用 的NH4+电极,DO电极等。
电位分析法

扩散电位
相互接触但浓度不同的溶液,如HCl, 由于浓度差异产生扩散,同时由于离子 迁移速率的差异,导致溶液界面的电荷 分布不均,产生电位梯度 出现电位差。 相同电荷的溶液与离子间,存在静电排 斥,使扩散达到平衡,溶液界面有稳定 的界面电位,即液接电位。
液接电位不仅出现在液-液界,也出现在 固-液界面
• The relationship between the ionic concentration (activity) and the electrode potential is given by the Nernst equation:
• 离子选择性电极主要包括(1)敏感膜, 是最关键部分(2)内参溶液,含有与膜 及内参电极响应的离子(3)内参电极, 一般用Ag|AgCl
离 子 选 择 性 电 极 构 造 示 意 图
BASIC THEORY OF ISE MEASUREMENTS.
Ion-Selective Electrodes are part of a group of relatively simple and inexpensive analytical tools which are commonly referred to as Sensors. The pH electrode is the most well known and simplest member of this group and can be used to illustrate the basic principles of ISEs.
0 0.55 0.75
Rel.Vol, %
S2-2 14.41 5.90 34.90 16.60 24.33 3.38 0.47
电位分析及离子选择电极
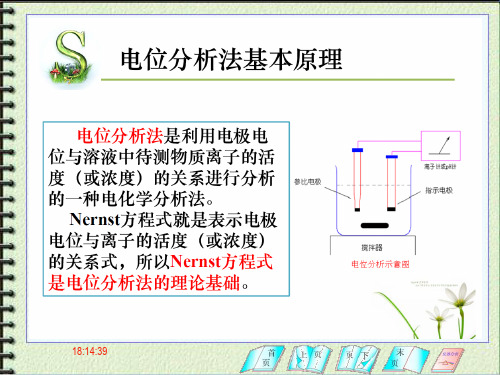
玻璃膜(敏感膜)的组成不同可制 成对不同阳离子响应的玻璃电极。
如H+,Na+,K+,Li+,Ag+离子响应电极(p139)。其中H+离子响 应电极(即pH玻璃电极)被最早最广泛应用。下面以pH玻璃 电极为例,详细阐述玻璃电极的工作原理。
18:14:39
pH玻璃电极
H+响应的玻璃膜电极:内充0.1mol/LHCl 溶液,敏感膜厚度约为0.10mm。
玻璃膜内、外表面的性质基本相同,则k外=k内 , a’1 = a’2
E 18:14:39
膜
=
E外
-
E内
=
0.059
lg(
a1
/
a2)
玻璃电极电位
作为玻璃电极的整体,玻璃电极的电位应包括内参比电极 的电位,即
E玻 = E内参比 + E膜 于是 E玻 = E内参比 + 0.059v lg( a1 / a2)
敏化电极(sensitized electrodes) 气敏电极:如氨电极 酶电极:如尿素电极
18:14:39
1.非晶体膜电极(玻璃电极)
玻璃膜电极,它的核心部分是玻璃 膜,是在SiO2基质中加入Na2O和少量 CaO烧制而成,膜厚0.5mm,呈球泡型。 球泡内充注内参比溶液(含有与待测离 子相同的离子),再插入一根AgCl-Ag电 极作内参比电极。
18:14:39
18:14:39
18:14:39
一、电位分析原理
principle of potentiometry analysis
电位分析是通过在零电流条件下测 定两电极间的电位差(电池电动势)所 进行的分析测定。
E 电池= E + - E 装置:参比电极、指示电极、电位
如H+,Na+,K+,Li+,Ag+离子响应电极(p139)。其中H+离子响 应电极(即pH玻璃电极)被最早最广泛应用。下面以pH玻璃 电极为例,详细阐述玻璃电极的工作原理。
18:14:39
pH玻璃电极
H+响应的玻璃膜电极:内充0.1mol/LHCl 溶液,敏感膜厚度约为0.10mm。
玻璃膜内、外表面的性质基本相同,则k外=k内 , a’1 = a’2
E 18:14:39
膜
=
E外
-
E内
=
0.059
lg(
a1
/
a2)
玻璃电极电位
作为玻璃电极的整体,玻璃电极的电位应包括内参比电极 的电位,即
E玻 = E内参比 + E膜 于是 E玻 = E内参比 + 0.059v lg( a1 / a2)
敏化电极(sensitized electrodes) 气敏电极:如氨电极 酶电极:如尿素电极
18:14:39
1.非晶体膜电极(玻璃电极)
玻璃膜电极,它的核心部分是玻璃 膜,是在SiO2基质中加入Na2O和少量 CaO烧制而成,膜厚0.5mm,呈球泡型。 球泡内充注内参比溶液(含有与待测离 子相同的离子),再插入一根AgCl-Ag电 极作内参比电极。
18:14:39
18:14:39
18:14:39
一、电位分析原理
principle of potentiometry analysis
电位分析是通过在零电流条件下测 定两电极间的电位差(电池电动势)所 进行的分析测定。
E 电池= E + - E 装置:参比电极、指示电极、电位
第07章 电位分析法

FLa3+
p 35
注意两点:
(i)在氟化镧晶体中,La3+固定不动,可移动的是F-, 故氟化镧晶体膜只对F-有选择性响应。 (ii)晶体膜中缺陷空穴的大小、形状、电荷的分布只能 容纳特定的可移动的晶格离子,其它离子不能通过空穴。
(3) 膜电位的产生
晶
+++++
待 测 F- 溶
----- 空穴
体 膜
原电极
非晶体膜电极
硬质电极,如 流动载体电极
pH电极
负正电电荷荷载载体体电电极极如如钙NO电3-极电极 中性载体电极如钾电极
敏化电极
气敏电极:如氨电极 酶电极:如尿素电极
p6
第二节 离子选择性电极的作用原理 一、扩散电位(液接电位)
H+(aq)+Na+Gl- (M)
Na+ (aq) + H+Gl- (M)
反应平衡常数很大,玻璃膜表面形成了一个类似硅酸结构 (H+Gl-)的水化胶层。
水化胶层的厚度为10-4~10-5 mm
p 22
道,外
k外
0.059
lg
aH
+ 外
a'
H
+ 外
道,内
k内
0.059
lg
aH内+ a'H内+
对i离子的选择性电极,对i离子具有选择性响应, 但这种选择性并非绝对专一,该敏感膜对其它离 子也或多或少的有一定程度的响应。
共存的其它离子对膜电位的产生也有贡献!
p 40
若测定离子为i,电荷为ni;干扰离子为j,电荷为nj 。
M
电位及离子选择性电极法

②内导系统:内参比电极( Ag/AgCl电极)、内参 比溶液(与待测离子相同的离子)。其作用
在于将膜电位引出。
ISE法的特点:
①选择性好,多数情况下共存离子的干扰小, 不需复杂处理待测液即可直接测定 ②灵敏度高。可达10-5- 10-8 mmol/L. ③实际测定的是溶液中离子活度,这是生物 学中一个重要的物理量。 ④溶血、脂血及黄疸不影响测定。 ⑤设备简单,分析速度快,易于自动化。 ⑥标本用量少而且应用广。
⑤NaN3可明显干扰Cl的测定。
电解质检测中各项的意义:
血清钾:3.5-5.5 mmol/L • 钾在参与蛋白质和糖的代谢,维持心肌和神经肌肉正常的应激性,维持酸碱
平衡等方面起重要作用。 降低: ①钾的摄入不足。 ②钾的过度丢失。如严重的呕吐、腹泻及胃肠引流、肾脏疾病(肾衰多尿期)等。 ③钾的细胞内转移。如家族性周期性四肢麻痹、肌无力症、给予大量葡萄糖等。 ④肾上腺皮质功能亢进。如醛固酮增多症。 ⑤碱中毒。 ⑥药物作用:a.长期使用大量肾上腺皮质激素,如可的松、地塞米松等;b.使用
降低 ①丢失过多。如严重呕吐和腹泻;大量使用利尿等 ②钠的摄入量不足。如饥饿、营养不良、低盐疗法等。 ③酸中毒 。
增高 ①肾上腺皮质功能亢进症。如柯兴综合征、原发性醛固酮增多症。 ②高渗性脱水症。 ③钠进量过多。如注射高渗盐水或进食过量钠盐,且伴有肾功能失常时。 ④潴钠性水肿。常见于心脏病、心力衰竭、肝硬化、肾病等。
和待测液(Es),根据以下公式计算:
Ex –Es = K 2.303RT
nF
lg a i
3. 标准加入法:适用于体系复杂,且与标准液浓度有较大
差异的待测液。先测定体积为Vx、浓度为Cx的待测液电动
势E,然后在此溶液中加入体积为Vs的标准液,测量电动势
在于将膜电位引出。
ISE法的特点:
①选择性好,多数情况下共存离子的干扰小, 不需复杂处理待测液即可直接测定 ②灵敏度高。可达10-5- 10-8 mmol/L. ③实际测定的是溶液中离子活度,这是生物 学中一个重要的物理量。 ④溶血、脂血及黄疸不影响测定。 ⑤设备简单,分析速度快,易于自动化。 ⑥标本用量少而且应用广。
⑤NaN3可明显干扰Cl的测定。
电解质检测中各项的意义:
血清钾:3.5-5.5 mmol/L • 钾在参与蛋白质和糖的代谢,维持心肌和神经肌肉正常的应激性,维持酸碱
平衡等方面起重要作用。 降低: ①钾的摄入不足。 ②钾的过度丢失。如严重的呕吐、腹泻及胃肠引流、肾脏疾病(肾衰多尿期)等。 ③钾的细胞内转移。如家族性周期性四肢麻痹、肌无力症、给予大量葡萄糖等。 ④肾上腺皮质功能亢进。如醛固酮增多症。 ⑤碱中毒。 ⑥药物作用:a.长期使用大量肾上腺皮质激素,如可的松、地塞米松等;b.使用
降低 ①丢失过多。如严重呕吐和腹泻;大量使用利尿等 ②钠的摄入量不足。如饥饿、营养不良、低盐疗法等。 ③酸中毒 。
增高 ①肾上腺皮质功能亢进症。如柯兴综合征、原发性醛固酮增多症。 ②高渗性脱水症。 ③钠进量过多。如注射高渗盐水或进食过量钠盐,且伴有肾功能失常时。 ④潴钠性水肿。常见于心脏病、心力衰竭、肝硬化、肾病等。
和待测液(Es),根据以下公式计算:
Ex –Es = K 2.303RT
nF
lg a i
3. 标准加入法:适用于体系复杂,且与标准液浓度有较大
差异的待测液。先测定体积为Vx、浓度为Cx的待测液电动
势E,然后在此溶液中加入体积为Vs的标准液,测量电动势
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
pH过高:OH -干扰F-的测定;pH过低:形成HF或HF2-,影响F-活动 F-选择性电极最佳适用范围:F-离子浓度0.1~10-7mol/L,pH5~6
解决方法:总离子强度调节缓冲溶液(Totle Ionic Strength
Adjustment Buffer,TISAB) 典 型 组 成 : 1mol/L 的 NaCl ; 0.25mol/LHAc 和 0.75mol/LNaAc ; 0.001mol/L的柠檬酸钠。 TISAB的作用:①保持较大且相对稳定的离子强度,使活度系数恒定; ②维持溶液在适宜的pH范围内,满足离子电极的要求;③掩蔽干扰离子 。
k2.3n0F R3Tlgai(阳离子+,阴离子-)
当其斜率为以下值时称其符合能斯特响应:
内参比溶液:0.1mol/L的
NaCl和0.10.01mol/L的NaF
混合溶液(F-用来控制膜
内表面的电位,Cl-用以固
定内参比电极的电位)。
化学电极
饱和甘汞电极
6
响应机理:LaF3单晶膜可交换F-离子
mkn RF Tlna(F)
mk0.05lg 9 a(F 2 )(T=250C)
使用注意事项:
2
二、离子选择性电极及其主要性能参数
1、电极的基本构造
3
2、膜电位(玻璃电极) ISE =内参+m
m =外-内
内参 m
外k2
RTlna(M)外 nF a(M)外
液 膜
内k1
RTlna(M)内 nF a(M)内
液 膜
m (k 2k 1)(n RlF T n a a ( (M M ) )外 外 液 膜 n RlF T n a a ( (M M ) )内 内)液 膜 RnFT
原电极
离
晶体膜电极
子 选
均相膜电极(F-,S2-,卤素电极)
择
非均相膜电极(Ag2S掺入硅橡胶的S2-电极)
性 电
非晶体膜电极
极
刚性基质电极(pH)
分 类
流动载体电极(NO3-,Ca2+,K+电极)
敏化电极
气敏电极(NH3电极) 酶电极(尿酶电极)
5
(1)氟离子电极(晶体膜电极)
氟离子电极
敏感膜:氟化镧单晶,掺 有EuF2 的LaF3单晶切片; 内参比电极:Ag-AgCl电 极。
ln
a(M)外液 a(M)内液
ISEkn RF Tlna(M)外 液 阳离子
ISEkn RF Tlna(M)外 液 阴离子
4
3、离子选择性电极的主要类型
离子选择性电极定义:离子选择性电极是一种电化学传感器,它的电极电位 与溶液中相应离子的活度的对数值成线形关系;离子选择性电极是一类指示 电极,它所指示的电极电位值与相应离子活度的关系符合能斯特方程。
14
气敏电极一览表
15
酶电极
基于界面酶催化化学反应的敏化电 极;
特性:酶是具有特殊生物活性的催化 剂,对反应的选择性强,催化效率高,
可使反应在常温、常压下进行;
可被现有离子选择性电极检测的常 见的酶催化产物:CO2,NH3,NH4+, CN-,F-,S2-,I-,NO2-
酶催化反应: 尿酶
CO(NH2 )2 + H2O 2NH3 + CO2
12
液膜电极应用一览表
13
敏化电极
敏化电极是指气敏电极、酶电极、细 菌电极及生物电极等。 气敏电极:基于界面化学反应的敏化电极; 其结构特点是在原电极上覆盖一层膜或物质, 使电极选择性提高。气敏电极也被称为:探 头、探ห้องสมุดไป่ตู้器、传感器。
试样中待测组分气体扩散通过透气膜,进入离子选择电极的敏感膜 与透气膜之间的极薄液层内,使液层内离子选择电极敏感的离子活度变 化,则离子选择电极膜电位改变,故电池电动势也发生变化。
氨电极检测
葡萄糖氧化酶
葡萄糖 + O2 + H2O 葡萄糖酸 + H2 O2 氧电极检测
氨基酸氧化酶
R-CHNH2 COO- +O2+H2 O R-COCOO- +NH4+ +H2O2
氨基酸通过以上反应后检测,或进一步氧化放出CO2 ,用气敏电极检测。
16
酶电极的组成与测定对象
测定物质 葡萄糖
mkn RF Tlna(H)
9
水化玻璃膜电极
10
使用注意事项 pH电极的最佳适用范围:pH1~9
pH<1(或非水溶液):酸差,测得的pH值偏高,此时 的误差称为酸误差或酸误,水分子活度变小所致
pH>9(或Na+浓度较高): “碱差”或“钠差”,测得 的pH值偏低,主要是Na+参与相界面上的交换所致;
第七章 电位分析法
一、电位分析法概述 二、离子选择性电极及其主要性能参数 三、离子选择性电极分析的仪器 四、电位分析及离子选择性电极分析的方法及应用
1
一、电位分析法概述
分析原理: 在零电流条件,利用电极电位与待测物质溶液中某
种组分浓度关系,而实现定量测定的电化学分析方法 分类:
直接电位法(离子选择性电极法) 电位滴定法 特点 选择性好,灵敏度高,仪器简单,操作方便
脲 胆固醇 L-谷氨酸 L-赖氨酸
酶 葡萄糖氧化酶
指示电极或检 测物
O2
测定范围
molL1
11 0 421 0 2
脲酶
NH3
11 0511 02
胆固醇氧化酶
H2O2
11 0511 02
谷氨酸脱氢酶
NH4+
11 0411 02
赖氨酸脱羧酶
CO2
11 0411 01
17
4、离子选择性电极的基本特性
(1)响应斜率和检测限
11
(3)其他类型的离子选择性电极
流动载体膜或液膜电极(钙电极):内参 比溶液为含 Ca2+水溶液。内外管之间装的 是0.1mol/L二癸基磷酸钙的苯基磷酸二辛 酯溶液。其极易扩散进入微孔膜,但不溶 于水,故不能进入试液溶液。
二癸基磷酸根可以在液膜-试液两相界面间传递钙离子,直至达到平衡。 由于Ca2+在水相(试液和内参比溶液)中的活度与有机相中的活度差异, 在两相之间产生相界电位。钙电极适宜的pH范围是5~11,可测出10-5 mol/L的Ca2+ 。
7
(2)玻璃(非晶体膜)电极
玻璃电极的结构
敏感膜:刚性基质玻璃;
内参比电极:Ag-AgCl电 极。
Ag-AgCl电极结构
内参比溶液:0.1mol/L的
HCl溶液(H+用来控制膜
内表面的电位,Cl-用以固
定内参比电极的电位)。
化学电池 复合pH玻璃电极
8
pH电极的响应机理
pH玻璃电极在水中浸泡之后,就能在玻璃表面形成一层硅 胶[H4SiO4],这层硅胶层中的H+能与溶液中的H+进行交换,硅胶 与溶液的界面间由于离子交换而产生电位差。
解决方法:总离子强度调节缓冲溶液(Totle Ionic Strength
Adjustment Buffer,TISAB) 典 型 组 成 : 1mol/L 的 NaCl ; 0.25mol/LHAc 和 0.75mol/LNaAc ; 0.001mol/L的柠檬酸钠。 TISAB的作用:①保持较大且相对稳定的离子强度,使活度系数恒定; ②维持溶液在适宜的pH范围内,满足离子电极的要求;③掩蔽干扰离子 。
k2.3n0F R3Tlgai(阳离子+,阴离子-)
当其斜率为以下值时称其符合能斯特响应:
内参比溶液:0.1mol/L的
NaCl和0.10.01mol/L的NaF
混合溶液(F-用来控制膜
内表面的电位,Cl-用以固
定内参比电极的电位)。
化学电极
饱和甘汞电极
6
响应机理:LaF3单晶膜可交换F-离子
mkn RF Tlna(F)
mk0.05lg 9 a(F 2 )(T=250C)
使用注意事项:
2
二、离子选择性电极及其主要性能参数
1、电极的基本构造
3
2、膜电位(玻璃电极) ISE =内参+m
m =外-内
内参 m
外k2
RTlna(M)外 nF a(M)外
液 膜
内k1
RTlna(M)内 nF a(M)内
液 膜
m (k 2k 1)(n RlF T n a a ( (M M ) )外 外 液 膜 n RlF T n a a ( (M M ) )内 内)液 膜 RnFT
原电极
离
晶体膜电极
子 选
均相膜电极(F-,S2-,卤素电极)
择
非均相膜电极(Ag2S掺入硅橡胶的S2-电极)
性 电
非晶体膜电极
极
刚性基质电极(pH)
分 类
流动载体电极(NO3-,Ca2+,K+电极)
敏化电极
气敏电极(NH3电极) 酶电极(尿酶电极)
5
(1)氟离子电极(晶体膜电极)
氟离子电极
敏感膜:氟化镧单晶,掺 有EuF2 的LaF3单晶切片; 内参比电极:Ag-AgCl电 极。
ln
a(M)外液 a(M)内液
ISEkn RF Tlna(M)外 液 阳离子
ISEkn RF Tlna(M)外 液 阴离子
4
3、离子选择性电极的主要类型
离子选择性电极定义:离子选择性电极是一种电化学传感器,它的电极电位 与溶液中相应离子的活度的对数值成线形关系;离子选择性电极是一类指示 电极,它所指示的电极电位值与相应离子活度的关系符合能斯特方程。
14
气敏电极一览表
15
酶电极
基于界面酶催化化学反应的敏化电 极;
特性:酶是具有特殊生物活性的催化 剂,对反应的选择性强,催化效率高,
可使反应在常温、常压下进行;
可被现有离子选择性电极检测的常 见的酶催化产物:CO2,NH3,NH4+, CN-,F-,S2-,I-,NO2-
酶催化反应: 尿酶
CO(NH2 )2 + H2O 2NH3 + CO2
12
液膜电极应用一览表
13
敏化电极
敏化电极是指气敏电极、酶电极、细 菌电极及生物电极等。 气敏电极:基于界面化学反应的敏化电极; 其结构特点是在原电极上覆盖一层膜或物质, 使电极选择性提高。气敏电极也被称为:探 头、探ห้องสมุดไป่ตู้器、传感器。
试样中待测组分气体扩散通过透气膜,进入离子选择电极的敏感膜 与透气膜之间的极薄液层内,使液层内离子选择电极敏感的离子活度变 化,则离子选择电极膜电位改变,故电池电动势也发生变化。
氨电极检测
葡萄糖氧化酶
葡萄糖 + O2 + H2O 葡萄糖酸 + H2 O2 氧电极检测
氨基酸氧化酶
R-CHNH2 COO- +O2+H2 O R-COCOO- +NH4+ +H2O2
氨基酸通过以上反应后检测,或进一步氧化放出CO2 ,用气敏电极检测。
16
酶电极的组成与测定对象
测定物质 葡萄糖
mkn RF Tlna(H)
9
水化玻璃膜电极
10
使用注意事项 pH电极的最佳适用范围:pH1~9
pH<1(或非水溶液):酸差,测得的pH值偏高,此时 的误差称为酸误差或酸误,水分子活度变小所致
pH>9(或Na+浓度较高): “碱差”或“钠差”,测得 的pH值偏低,主要是Na+参与相界面上的交换所致;
第七章 电位分析法
一、电位分析法概述 二、离子选择性电极及其主要性能参数 三、离子选择性电极分析的仪器 四、电位分析及离子选择性电极分析的方法及应用
1
一、电位分析法概述
分析原理: 在零电流条件,利用电极电位与待测物质溶液中某
种组分浓度关系,而实现定量测定的电化学分析方法 分类:
直接电位法(离子选择性电极法) 电位滴定法 特点 选择性好,灵敏度高,仪器简单,操作方便
脲 胆固醇 L-谷氨酸 L-赖氨酸
酶 葡萄糖氧化酶
指示电极或检 测物
O2
测定范围
molL1
11 0 421 0 2
脲酶
NH3
11 0511 02
胆固醇氧化酶
H2O2
11 0511 02
谷氨酸脱氢酶
NH4+
11 0411 02
赖氨酸脱羧酶
CO2
11 0411 01
17
4、离子选择性电极的基本特性
(1)响应斜率和检测限
11
(3)其他类型的离子选择性电极
流动载体膜或液膜电极(钙电极):内参 比溶液为含 Ca2+水溶液。内外管之间装的 是0.1mol/L二癸基磷酸钙的苯基磷酸二辛 酯溶液。其极易扩散进入微孔膜,但不溶 于水,故不能进入试液溶液。
二癸基磷酸根可以在液膜-试液两相界面间传递钙离子,直至达到平衡。 由于Ca2+在水相(试液和内参比溶液)中的活度与有机相中的活度差异, 在两相之间产生相界电位。钙电极适宜的pH范围是5~11,可测出10-5 mol/L的Ca2+ 。
7
(2)玻璃(非晶体膜)电极
玻璃电极的结构
敏感膜:刚性基质玻璃;
内参比电极:Ag-AgCl电 极。
Ag-AgCl电极结构
内参比溶液:0.1mol/L的
HCl溶液(H+用来控制膜
内表面的电位,Cl-用以固
定内参比电极的电位)。
化学电池 复合pH玻璃电极
8
pH电极的响应机理
pH玻璃电极在水中浸泡之后,就能在玻璃表面形成一层硅 胶[H4SiO4],这层硅胶层中的H+能与溶液中的H+进行交换,硅胶 与溶液的界面间由于离子交换而产生电位差。
