无机化学晶体结构
无机化学第3章_晶体结构

[答] 图3-1中的小立方体不具有平移性,因为它与相邻的小立方体并非等 同。相反,大立方体才具有平移性,在它的上下左右前后都有无隙并置的完 全等同的立方体,只是没有画出来而已,因此大立方体才是晶胞,小立方体 不是晶胞。
(2) 晶胞具有相同的顶角、相同的平面和相同的 平行棱
图3-19 底心晶胞举例(I2) [答]将晶胞原点移至bc面心(a)和ab面心(c)均不能
使所有原子坐标不变,只有将晶胞原点移至ac面心(b) 才得到所有原子坐标不变的新晶胞,可见碘的晶胞是B底 心(正交)晶胞。
立方
边长: a=b=c
夹角: = = =900
实例: Cu , NaCl
(只有1个晶胞参数a是可变动的)
四方
边长:a=bc
夹角: = = =900
实例: Sn, SnCl2
(有2个晶胞参数a和c)
六方
边长:a= bc
夹角: = =900 =1200
实例: Mg, AgI
(有2个晶胞参数a和c)
面心晶胞的特征
可作面心平移,即所有原子均可作在其原子坐标上+ (1/2,1/2,0;0,1/2,1/2;1/2,0,1/2)的平移 而得到周围环境完全相同的原子。如晶胞顶角有一个原子, 在晶胞三对平行面的中心必有完全相同的原子(周围环境 也相同)。
[例3-5]图3-17中哪个晶胞是面心晶胞?
图3-17面心晶胞(金属铜)(左)与非面心晶胞(Cu3Au)(右)举例
3-2-4 素晶胞与复晶胞
素晶胞是晶体微观空间中的最小基本单元。 复晶胞是素晶胞的多倍体。即体心晶胞、面心晶胞、 底心晶胞。
晶
素晶胞P
体心晶胞 I(2倍体)
无机化学第七章 晶体结构

例1:体心立方晶胞中金属原子的空间利用 率计算 (教材P.213, 图9-10) (1)计算每个晶胞含有几个原子:
1 + 8 × 1/8
= 2
体心立方晶胞:中心有1个原子, 8个顶点各1个原子,每个原子被8个 晶胞共享。
(二)空间利用率计算(续)
(2)原子半径r 与晶胞边长a 的关系: 勾股定理: 2a 2 + a 2 = (4r)
半径比规则(续)说明:
3. 值位于“边界”位置附近时,相应化合物 有2种构型。 例:GeO2 r + / r - = 53 pm / 132 pm = 0.40. 立方ZnS NaCl 两种晶体空间构型均存在. 4.离子晶体空间构型除了与r + / r -有关外,还 与离子的电子构型、离子互相极化作用(如 AgI)以至外部条件(如温度)等有关。
(三)半径比规则(续)说明:
1.―半径比规则”把离子视为刚性球,适用于离子 性很强的化合物,如NaCl、CsCl等。否则,误差大。 例:AgI(c) r + / r - = 0.583. 按半径比规则预言为NaCl型,实际为立方ZnS型。 原因:Ag+与I-强烈互相极化,键共价性↑,晶型转 为立方ZnS(C.N.变小,为4:4,而不是NaCl中的6:6) 2.经验规则,例外不少。 例:RbCl(c),r / r 147pm / 184pm 0.80 0.732 预言CsCl型,实为NaCl型。
一、离子极化作用
离子极化作用(教材P.220图9-18) 离子极化力(Polarizing主动) 离子变形性 ( Polarizability, Polarized被动) 在异号离子电场作用下,离子的电子云发生变形, 正、负电荷重心分离,产生“诱导偶极”,这个过程 称为“离子极化”。 阳离子、阴离子既有极化力,又有变形性。 通常阳离子半径小,电场强,“极化力”显著。 阴离子半径大,电子云易变形,“变形性”显著。
无机化学 第7章 晶体的结构和性质

离子电荷 NaCl Na+ +1 CuCl Cu+ +1
r+/pm 95 96
溶解性 易溶于水 难溶于水
说明影响离子晶体的性质除了离子电荷、 离子半径外,还有离子的电子构型
7.6.1 离子的电子构型
简单阴离子的电子构型:ns2np6 8电子构型
阳离子外电子层 电子分布式
离子电 子构型
实例
1s2
2(稀有 气体型)
晶 液晶——介于液态和晶态之间的各向异 性的凝聚流体。
近似液态:能流动、不能承受应切力
近似晶体:介电常数、折射率、电导 率等性质各向异性
应用
由于对光、电、磁、热、机械压力及 化学环境变化都非常敏感,可作为各种信 息的显示和记忆材料。
第七章 固体结构与性质
7.2
离子晶体及其性质
7.2.1 离子晶体的特征和性
Sn2+、Pb2+ 、 Sb3+、Bi3+
7.6.2 离子极化的概念
+
+
-
对于孤立的简单离 子来说,离子电荷 分布基本上是球形 对称的,离子本身 的正、负电荷中心 重合, 不存在偶极
电场中,离子的原子 核和电子受电场的作 用,离子会发生变形, 产生诱导偶极,这种 过程称为离子极化
Li+
0.034
OH-
1.95
Na+
0.199
F-
1.16
Ca2+
0.52
Cl-
4.07
B3+
0.0033
Br-
5.31
Ag+
1.91
O2-
4.32
Hg2+
1.39
固体无机化学-晶体学基础2

l) (h k l) l) (h k i l) i = - h+k ) (
[U V W] [u v t w] U = u - t, V = v - t, W = w 1 1 u = [2U - V], v = [2V - U], t = -(u + v), w = W 3 3
(Miller Indices of Crystallographic Direction and Planes) 前已指出,任何阵点的位置可由矢量ruvw和该点阵的坐标u,v,w来确定。 同样晶向OP可沿a,b,c三个方向分解为三个矢量,即 1.阵点坐标 op = xa + yb + zc 2.晶向指数(Orientation index)
宏观对称要素— 宏观对称要素—回转对称轴
二维晶胞的密排图形
宏观对称要素— 宏观对称要素—对称面
1 晶体通过某一平面作 镜像反映而能复原, 则该平面称为对称面 或镜面。 2 对称面用符号 m 表示。
宏观对称要素宏观对称要素-对称中心
1 如果位于晶体中心O点一边 的每点都可在中心的另一边 得到对应的等同点,且每对 点子的连线均通过O点并被 它所等分,则此中心点称为 晶体的对称中心 对称中心。或称为反 对称中心 演中心。即晶体的每一点都 可借以O点为中心的反演动 作而与其对应点重合。 2 对称中心用符号 z 表示。
1 对称要素构成一些动作,即晶体经过这些动作 之后所处的位置与其原始位置完全重合,也就 是晶体上每一点的新旧位置都完全重合。 2 晶体的对称要素可分为宏观和微观两类。宏观 对称要素反映出晶体外形和其宏观性质的对称 性。而微观对称要素与宏观对称要素配合运用 就能反映出晶体中原子排列的对称性。
大学无机化学知识点总结

大学无机化学知识点总结无机化学是化学学科的一个重要分支,对于大学化学相关专业的学生来说,掌握无机化学的知识点至关重要。
以下是对大学无机化学主要知识点的总结。
一、原子结构与元素周期律原子由原子核和核外电子组成。
原子核包含质子和中子,质子数决定了元素的种类。
电子在核外分层排布,遵循一定的规律。
原子轨道理论描述了电子在原子核外的运动状态。
包括 s、p、d、f 等轨道,其形状和能量各不相同。
元素周期表是无机化学的重要工具。
同一周期元素从左到右,原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强;同一主族元素从上到下,原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。
二、化学键与物质结构化学键包括离子键、共价键和金属键。
离子键是由阴阳离子之间的静电作用形成的,通常存在于活泼金属与活泼非金属组成的化合物中。
共价键是原子之间通过共用电子对形成的,分为极性共价键和非极性共价键。
分子的空间构型对于物质的性质有着重要影响。
例如,甲烷分子是正四面体结构,氨气分子是三角锥形结构。
晶体结构也是无机化学的重要内容。
常见的晶体类型有离子晶体、原子晶体、分子晶体和金属晶体,它们具有不同的物理性质。
三、化学热力学基础热力学第一定律指出能量守恒,即能量可以在不同形式之间转化,但总量不变。
焓变(ΔH)是化学反应中热量变化的重要指标。
热力学第二定律涉及到熵(S)的概念,自发的过程总是朝着熵增加的方向进行。
通过吉布斯自由能(ΔG)可以判断化学反应的方向。
当ΔG < 0 时,反应自发进行;当ΔG > 0 时,反应非自发进行;当ΔG = 0 时,反应达到平衡。
四、化学反应速率化学反应速率可以用单位时间内反应物浓度的减少或生成物浓度的增加来表示。
影响化学反应速率的因素包括浓度、温度、压强、催化剂等。
浓度增大,反应速率加快;温度升高,分子运动加快,有效碰撞增加,反应速率增大;对于有气体参与的反应,压强增大,反应速率通常也会增大;催化剂能够改变反应的历程,降低反应的活化能,从而加快反应速率。
无机化学晶体结构

晶体结构和类型 金属晶体 离子晶体 分子晶体 混合晶体
§9.1 晶体结构和类型
9.1.1 晶体结构的特征与晶格理论 9.1.2 晶体缺陷 非晶体 9.1.3 球的密堆积 9.1.4 晶体类型
9.1.1 晶体结构的特征与晶格理论
晶胞:晶体的最小重复单元,通过晶胞
在空间平移无隙地堆砌而成晶体。 晶胞的两个要素:
第九章 晶体结构
• 教学要求: • 1、理解晶体的基本概念,掌握四种晶体类
型的特征和性质; • 2、初步了解离子极化的概念及其应用; • 3、掌握金属键的“自由电子”理论,了解
能带理论。 • 教学难点: • 离子极化;离子晶体的空间结构。
第九章 晶体结构
§9.1 §9.2 §9.3 §9.4 §9.5
a=b=c a=b=c a = b≠c a = b≠c a≠b≠c a≠b≠c a≠b≠c
α=β=γ= 900 α=β=γ≠900 α=β=γ= 900 α=β= 900, γ= 1200 α=β=γ= 900 α=β= 900, γ≠ 900 α≠β≠γ≠ 900
NaCl
Al2O3 SnO2 AgI HgCl2 KClO3 CuSO4·5H2O
-:8 1
1个
8
ZnS型(立方型)
晶格:面心立方
配位比:4:4 (红球-Zn2+ , 绿球-S2-) 晶胞中离子的个数: Zn2:4个
S2-:6 1 8 1 4个 28
半径比(r+/r-)规则: 其中一层横截面: (4r )2 2(2r 2r )2
令 r 1
r / r 0.414
NaCl晶体
△ rHm,1=89.2kJ·mol-1 △ rHm,2 =418.8kJ·mol-1 △ rHm,3 =15.5kJ·mol-1 △ rHm,4 =96.5kJ·mol-1 △ rHm,5 =-324.7kJ·mol-1 △ fHm =295.3kJ·mol-1
无机化学——原子晶体与分子晶体
B
B
C A
A
面心立方 紧密堆积
六方紧密堆积
Body-centered cubic cell (BCC)
体心立方紧密堆积 CN=12,利用率 =68% K、Rb、Cs、Li、 Na A B
A
体心立方 紧密堆积
7.4.2 金属键 金属键:金属原子的价电子可以完全失去成为自由电子,并在 晶格中运动,自由电子把金属阳离子胶合成金属晶体,这种胶 合作用就叫金属键。金属键无饱和性和方向性。
氯化氢、氨、三氯化磷、冰等由极性键构成的极性分子,晶体 中分子间存在色散力、取向力、诱导力,有的还有氢键,所以 它们的结点上的粒子间作用力大于分子量相近的非极性分子之 间的引力。
分子晶体的特性 分子晶体是以独立的分子出现的 ,化学式就是分子式。
分子晶体可以是非金属单质,如卤素、H2、N2、O2; 非金属化合物,如CO2、H2S、HCl、HN3等 绝大多数有机化合物,稀有气体的晶体
7.6.3 离子极化对物质性质的影响 一、离子的电子构型
外层电子结构 电子构型 阳离子实例
ns2np6
8
Na+, Mg2+,Al3+,Ti4+
ns2np6 nd1-9
9-17
Cr3+,Mn2+,Fe3+,Cu2+
ns2np6 nd10
18
Ag+,Zn2+,Cd2+,Hg2+
s2p6d10ns2
18+2
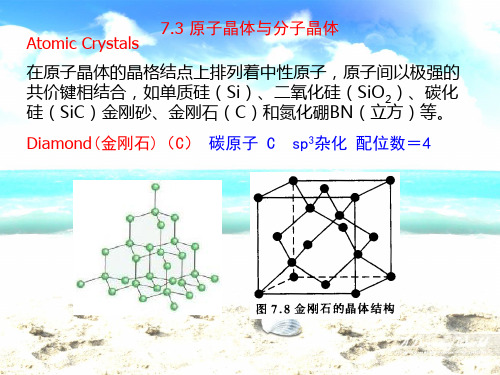
7.3 原子晶体与分子晶体 Atomic Crystals
在原子晶体的晶格结点上排列着中性原子,原子间以极强的 共价键相结合,如单质硅(Si)、二氧化硅(SiO2)、碳化 硅(SiC)金刚砂、金刚石(C)和氮化硼BN(立方)等。
无机化学《晶体结构》教案

无机化学《晶体结构》教案[ 教学要求]1 .了解晶体与非晶体的区别,掌握晶体的基本类型及其性质特点。
2 .了解离子极化的基本观点及其对离子化合物的结构和性质变化的解释。
3 .了解晶体的缺陷和非整比化合物。
[ 教学重点]1 .晶胞2 .各种类型晶体的结构特征3 .离子极化[ 教学难点]晶胞的概念[ 教学时数] 4 学时[ 主要内容]1 .晶体的基本知识2 .离子键和离子晶体3 .原子晶体和分子晶体4 .金属键和金属晶体5 .晶体的缺陷和非整比化合物6 .离子极化[ 教学内容]3-1 晶体3-1-1 晶体的宏观特征晶体有一定规则的几何外形。
不论在何种条件下结晶,所得的晶体表面夹角(晶角)是一定的。
晶体有一定的熔点。
晶体在熔化时,在未熔化完之前,其体系温度不会上升。
只有熔化后温度才上升。
3-1-2 晶体的微观特征晶体有各向异性。
有些晶体,因在各个方向上排列的差异而导致各向异性。
各向异性只有在单晶中才能表现出来。
晶体的这三大特性是由晶体内部结构决定的。
晶体内部的质点以确定的位置在空间作有规则的排列,这些点本身有一定的几何形状,称结晶格子或晶格。
每个质点在晶格中所占的位置称晶体的结点。
每种晶体都可找出其具有代表性的最小重复单位,称为单元晶胞简称晶胞。
晶胞在三维空间无限重复就产生晶体。
故晶体的性质是由晶胞的大小、形状和质点的种类以及质点间的作用力所决定的。
3-2 晶胞3-2-1 晶胞的基本特征平移性3-2-2 布拉维系十四种不拉维格子类 型 说 明单斜底心格子( N ) 单位平行六面体的三对面中 有两对是矩形,另一对是非矩形 。
两对矩形平面都垂直于非矩形 平面,而它们之间的夹角为β, 但∠β≠ 90°。
a 0≠ b 0 ≠ c 0 ,α = γ =90°, β≠ 90°正交原始格子( O ) 属于正交晶系,单位平 行六面体为长、宽、高都不 等的长方体,单位平行六面 体参数为: a 0 ≠ b 0 ≠ c 0 α = β = γ =90 °正交体心格子( P ) 属于正交晶系,单位平行六 面体为长、宽、高都不等的长方 体,单位平行六面体参数为: a 0 ≠ b 0 ≠ c 0 α = β = γ =90 °正交底心格子( Q ) 属于正交晶系,单位平 行六面体为长、宽、高都不 等的长方体,单位平行六面 体参数为: a 0 ≠ b 0 ≠ c 0 α = β = γ =90 °正交面心格子( S ) 属于正交晶系,单位平 行六面体为长、宽、高都不 等的长方体,单位平行六面 体参数为: a 0 ≠ b 0 ≠ c 0 α = β = γ =90 °立方体心格子( B ) 属于等轴晶系,单位平行六 面体是一个立方体。
无机化学公式总结

无机化学公式总结1. 离子式无机化学研究中,离子式是一种简洁而重要的表示化学物质组成的方法。
离子式由正离子和负离子组成,它们通过电荷的吸引作用结合在一起。
下面是一些常见的离子及其化学式:•氢离子:H⁺•氧离子:O²⁻•水合离子:[M(H₂O)n]^m⁺(M为金属离子,n为水和离子结合的个数,m为电荷)2. 酸碱反应酸碱反应是无机化学中常见的反应类型,涉及到酸和碱之间的中和反应。
常见的酸和碱的化学式及反应方程式如下:•盐酸:HCl硫酸:H₂SO₄硝酸:HNO₃醋酸:CH₃COOH•氢氧化钠:NaOH氢氧化钾:KOH氢氧化铵:NH₄OH酸碱反应的一般化学方程式如下:酸 + 碱→ 盐 + 水例如:HCl + NaOH → NaCl + H₂O3. 氧化还原反应氧化还原反应是无机化学中重要且常见的反应类型。
在氧化还原反应中,电子的转移是关键步骤。
以下是一些常见的氧化还原反应及其化学式:•氧化反应:2Na + Cl₂ → 2NaCl•还原反应:PbO₂ + 4H⁺ + SO₃²⁻ → Pb²⁺ + H₂O + SO₄²⁻4. 配位化合物配位化合物是由中心金属离子与周围配体形成配位键而构成的化合物。
以下是一些常见的配位化合物及其化学式:•菌胺:[Cu(NH₃)₄]²⁺铁氰化物:[Fe(CN)₆]⁴⁻硝酸铜:[Cu(NO₃)₄]²⁻配位化合物的常见表示法是使用配位数表示。
5. 晶体结构无机化合物中的晶体结构对于了解化合物的性质和行为至关重要。
以下是一些常见的晶体结构:•立方晶系:–体心立方晶格–面心立方晶格•矩阵晶系:–简单六方晶格–单斜晶格6. 氢键氢键是无机化学中一种重要的相互作用力。
氢键是通过氢原子与电负性较高的原子之间的相互作用形成的。
以下是一些常见的氢键:•水中氢键:H₂O···H₂O•醇中氢键:R-O-H···H-O-R•酮中氢键:R₂C=O···H₂C=O-R₂7. 晶体生长晶体生长是无机化学中的一个重要研究领域。
无机化学(北师大版)第3章 晶体结构 章节测试(含答案)

第三章晶体结构一选择题1.下列有关离子变形性的说法中,不正确的是()。
A.8电子构型的离子的变形性小于其他电子构型的离子B.同一元素不同价态的负离子中,所带负电荷越多变形性越大C.同种原子形成的阴离子比阳离子变形性大D.离子半径大,则变形性大(其他条件相同)2.下列各组离子化合物的晶格能变化顺序中,正确的是()A、MgO> CaO> Al2O3B、LiF> NaCl >KIC、RbBr< CsI <kclD、BaS> BaO> BaCl23.Ag+的电子构型为()。
A.18B.18+2C.9~17D.84.下列各种电子构型的正离子,其极化力和变形性均较小的是()。
A.8电子构型B.9~17电子构型C.18电子构型D.18+2电子构型5.下列化合物中,熔点最低的是()。
A.BCl3 B. SiCl4C.SiCD.NaCl6.下列各晶体中,熔化时只需克服色散力的是()。
A.KB.H2OC.SiCD.SiF47.下列离子中,磁矩最大的是()。
A.Ni2+B.V2+C.Ti4+D.Mn2+8.下列各组离子中,离子的变形性最大的是()。
A.I- B.Cl- C.Br- D.F-9.下列物质中,熔点最低的是()。
A.NaFB.AlF3C.KClD.CaO10.在NaCl晶体中,Na+(或Cl-)的配位数是()。
A.4B.5C.6D.811.晶体熔化时,需破坏共价键作用的是()。
A.PH3B.AlC.KFD.SiO212.下列物质中熔点最高的是()。
A.NaClB.N2C.NaD.SiO213.关于分子晶体的叙述中,正确的是()。
A.分子晶体中只存在分子间力B.分子晶体晶格结点上排列的分子可以是极性分子或非极性分子C.分子晶体不溶于水D.分子晶体在水溶液中不导电14.离子晶体中,正、负离子配位数比不同的最主要原因是()。
A.正、负离子半径B.正、负离子的电荷C.正、负离子的电子构型D.晶格能15.对于AB型的离子晶体,若正、负离子配位数为4,则它们的半径之比r+/r-为()。
无机化学第六章分子结构与晶体结构

第六章 分子结构与晶体结构 3.键角(α) 在分子中键与键之间的夹角,称为键角。 对双原子分子,分子的形状总是直线型的。 对于多原子分子,由原子在空间排列不同,所以有不 同的键角和几何构型。例如,H2O分子中O—H键的键 长和键角分别为96 pm和104.45°,说明水分子是V形 结构。
第六章 分子结构与晶体结构
第六章 分子结构与晶体结构 σ键π键比较 通常π键形成时原子轨道重叠程度小于σ键的,故π 键常没有σ键稳定,π电子容易参与化学反应。 当两原子形成双键或叁键时,既有σ键又有π键。例 如,N2分子的2个N原子之间就有一个(且只能有一个)σ键 和两个π键 。
第六章 分子结构与晶体结构
第六章 分子结构与晶体结构 2.非极性共价键和极性共价键 非极性共价键 由同种原子组成的共价键,如单质分子H2,O2,N2, Cl2等分子中的共价键,由于元素的电负性相同,电子云 在两核中间均匀分布(并无偏向),这类共价键称为非极性 共价键。
第六章 分子结构与晶体结构
学习指南 第一节共价键理论 第二节 杂化轨道理论与分子几何构型 第三节 分子间力与分子晶体 第四节 离子键与离子晶体 第五节 离子极化 第六节 其他类型晶体 习题 习题参考答案
第六章 分子结构与晶体结构
本章重点: 1. 价键理论 2.杂化轨道理论 3.分子间力与分子晶体 本章难点: 1.杂化轨道理论 2.分子的结构与物理性质的关系
第六章 分子结构与晶体结构
第一节共价键理论
共价键的形成 由H原子形成H2分子的系统为例来说明假设有两种情 况。 (1) 两个H原子中电子的自旋方向相反。两个1s轨道的形成 最大重叠,系统能量最低,形成稳定的化学键
第六章 分子结构与晶体结构 (2)两个H原子的自旋方向相同。当它们相互靠近, 两原子核间的电子概率密度几乎为零。系统能量升高, 不能形成化学键。 H2分子能量曲线
《无机化学》第3版 宋天佑 第7章 晶体结构

分子越大,越容易变形,瞬 间偶极也越大。
7. 1. 2 分子间作用力
分子间力最早是由范德华 研究实际气体和理想气体状态 方程的偏差时提出来的
因而,分子间力又称为范 德华力。
分子间的范德华力可根据 来源不同分为
取向力、诱导力和色散力
1. 取向力 取向力又称定向力,是极性 分子之间的永久偶极与永久偶极 之间的静电引力。
对弱的氢键,如 C-H ···O,C-H ···N 等, 其方向性和饱和性不如经典的 氢键严格。
H ···Y 间距离较长, 经常出现一个 Y 原子同时 形成多个氢键的情况。
(2) 氢键的强度
氢键的强弱与 X 和 Y 的电负性 大小有关。
X,Y 的电负性越大,则形成 的氢键越强。
氢键的强弱也与 X 和 Y 的半径大小有关。
q+·q- V吸引 = 4 π ε0 r
当正负离子相互接近时,它 们之间主要是静电吸引作用。
但当正负离子进一步相互接 近时,除了静电吸引外,还存在 外层电子之间以及原子核之间的 相互排斥作用。
这种排斥作用当 r 较大时 可以忽略。
但当正负离子充分接近,r 极小时, 这种排斥作用的势能 迅速增加。
V
0
Vr0 r
主要表现为吸引作用。 所以,体系的能量随着 r 的 减小而降低。
V
0
Vr0 r
当 Na+ 和 Cl- 非常接近时, r 很小,此时排斥作用为主,体 系能量迅速增大。
V
0
Vr0
r0
r
当 Na+ 和 Cl- 接近平衡距离
r0 时,体系的吸引作用和排斥作 用处于动态平衡,
V
0
Vr0
高等无机化学简明教程

高等无机化学简明教程第一章:导论高等无机化学作为化学学科中的重要分支,主要研究无机物质的结构、性质以及其在化学反应中的应用。
与有机化学侧重于碳基化合物的特性和反应机理不同,无机化学涵盖了从单质到无机化合物的广泛领域,包括金属、非金属元素及其化合物的研究。
第二章:原子结构与周期表原子结构是理解无机化学基础的关键。
原子由质子、中子和电子组成,质子和中子位于原子核中,电子则围绕核外运动,形成电子壳层。
这些电子层次决定了原子的化学性质和反应能力。
周期表则将所有已知的元素按照原子序数和化学性质进行了分类,提供了对元素周期性性质的清晰理解。
第三章:化学键与晶体结构化学键的形成是无机化合物稳定性的基础。
离子键、共价键和金属键是常见的化学键类型,它们决定了化合物的结构和物理性质。
晶体结构描述了固体中原子或离子的排列方式,涉及晶格参数和晶胞结构的详细分析。
第四章:主要元素的化学特性无机化学研究的重要对象是各种主要元素及其化合物。
氢、氧、氮、碳、硫等元素在无机化学中具有关键作用,它们的化学性质和反应机制对于理解大自然中的化学过程至关重要。
第五章:过渡金属与配位化学过渡金属是无机化学中的核心研究对象之一,它们的特殊电子结构使得其在催化、电化学和生物化学领域中有重要应用。
配位化学研究则探索了配合物的结构、配位数及其在催化剂和材料科学中的应用。
第六章:固体与配位化合物的应用无机化学的应用涵盖了从催化剂到材料科学的广泛领域。
无机材料如半导体、陶瓷、磁性材料和超导体在现代技术和工业中发挥着重要作用。
配位化合物的设计与合成对新材料的开发具有深远的影响。
第七章:反应动力学与热力学理解化学反应的动力学和热力学条件对于优化反应条件和预测反应结果至关重要。
反应速率、活化能和反应平衡常数是评估化学反应过程中能量变化和速率的关键参数。
第八章:核化学与放射性核化学研究探索了放射性元素的性质及其在医学和工业中的应用。
核反应、核衰变和放射性同位素标记技术对于生物医学研究和核能应用具有重要意义。
无机化学第七章晶体结构

无机化学第七章晶体结构晶体结构是无机化学中一个重要的概念。
晶体是由一个或多个原子、离子或分子有序排列组成的固体,具有规则的几何形状。
晶体结构研究的是晶体中原子、离子或分子的排列方式和间距。
晶体结构的研究首先要确定晶胞的类型和晶格常数。
晶胞是晶体中基本的重复单元,可以通过晶胞的平移得到整个晶体。
晶格常数是指晶胞中原子、离子或分子的排列方式和间距。
晶体结构可以用晶胞的对称性来描述。
对称性是指晶胞的各个面和角的排列方式。
晶胞的对称性可以分为平面对称、轴对称和空间对称。
根据对称性的不同,晶体可以分为立方晶体、四方晶体、正交晶体、六方晶体、单斜晶体、三斜晶体和三角晶体等七种类型。
晶体结构中还有一些重要的概念,如晶系、空间群和点群。
晶系是指晶体结构的基本几何形状,包括立方、四方、正交、六方、单斜、三斜和三角七种类型。
空间群是指晶体结构的完整的对称操作,包括平移、旋转、反射和滑移。
点群是指晶体结构的实际的对称操作,只包括旋转和反射,不包括平移。
晶体结构的研究方法主要有X射线衍射方法、电子衍射方法和中子衍射方法等。
X射线衍射是最常用的晶体结构研究方法。
当X射线通过晶体时,会发生衍射现象。
根据衍射的图样可以确定晶体的结构。
晶体结构的研究对于了解物质的性质和应用具有重要的意义。
晶体结构可以影响物质的物理和化学性质,如硬度、透明度和导电性等。
通过了解晶体结构,可以设计和合成具有特定性能的材料,如硅和镍钴锌铁氧体等。
晶体结构的研究还可以为材料科学、能源、光电子学和生物医学等领域的研究提供指导。
总之,晶体结构是无机化学中一个重要的概念。
通过研究晶体结构,可以了解晶体的组成和排列方式,以及晶体对物质性质的影响。
高等无机化学-晶体的点阵结构与X射线衍射

布拉格方程应用
• 布拉格方程是X射线衍射分布中最重要的基础公式, 它形式简单,能够说明衍射的基本关系,所以应 用非常广泛。从实验角度可归结为两方面的应用: • 一方面是用已知波长的X射线去照射晶体,通过衍 射角的测量求得晶体中各晶面的面间距d,这就是 结构分析------ X射线衍射学 射线衍射学; • 另一方面是用一种已知面间距的晶体来反射从试 样发射出来的X射线,通过衍射角的测量求得X射 线的波长,这就是X射线光谱学 X射线光谱学。该法除可进行光 谱结构的研究外,从X射线的波长还可确定试样的 组成元素。电子探针就是按这原理设计的。
晶体的点阵结构与X射线衍射— 第 2 章 晶体的点阵结构与X射线衍射—结晶学主要内容
结晶学的基础 1 几何结晶学 研究方法是将各式各样的晶体中的等同单元抽取 为几何上的点, 研究这些几何点在空间的分布规律 (点阵理论), 这是一个从具体到抽象的过程. X射线结晶学 2 X射线结晶学 结构分析方法 点阵理论得到了直接的实验证实, 是目前测定固 体物质结构的主要手段之一 . 3 晶体化学 点阵理论的具体的分析应用 研究晶体的组成、结构和性质之间的关系. 包括金 属晶体、离子晶体、原子晶体、分子晶体. 4 晶体物理 讨论晶体的光、电、磁、力学等性质与晶体结构、 缺陷等关系.
由原子、 晶体的定义 由原子、分子或离子等微粒在空间按一定规 律、周期性重复排列所构成的固体物质。 周期性重复排列所构成的固体物质。
晶态结构示意图
非晶态结构示意图
一、晶体结构的特征——三维空间的周期性 晶体结构的特征
•均匀性 均匀性 •各向异性(玻璃为各向同性) 各向异性(玻璃为各向同性) 各向异性 •多面体(F+V=E+2,符合欧拉公式) 多面体(F+V=E+2,符合欧拉公式) 多面体 •有明确的熔沸点(玻璃只有软化温度) 有明确的熔沸点(玻璃只有软化温度) 有明确的熔沸点 •对称性 对称性 •衍射效应(均匀性)x-ray,电子,中子 衍射,有特征的衍射图谱 衍射效应(均匀性) ray,电子, 衍射, 衍射效应
无机化学——晶体结构 习题解答

第9章习题解答一、是非题1. 具有相同电子层结构的单原子离子,阳离子的半径往往小于阴离子的半径。
()解:对2. 离子半径是离子型化合物中相邻离子核间距的一半。
()解:错3. 同种元素离子的半径随离子电荷代数值增大而减小。
()解:对4. 仅依据离子晶体中正负离子半径的相对大小即可决定晶体的晶格类型。
()解:错5. NaCl晶体中配位数比是6:6,因此每个晶胞中含有6个Na+和6个Cl-。
()解:错6. NaCl晶体是由Na+和Cl-组成的面心立方晶格交错(重叠1/2)排列而成。
()解:对7. CsCl晶体是由Cs+和Cl-的简单立方交错(重叠1/8)排列而成。
()解:对8. 每个CsCl晶胞中含有1个Cs+和1个Cl-。
()解:对9. 每个NaCl晶胞中含有4个Na+和4个Cl-。
()解:对10. 固体物质可以分为晶体和非晶体两类。
()解:对11. 所有无机盐都是离子晶体。
()解:错12. 任何晶体都存在晶格能,晶格能越大则物质的熔点越高。
()解:错13. 所有原子晶体的熔点均比离子晶体的熔点高。
()解:错14. 在常温常压下,原子晶体物质的聚集状态只可能是固体。
()解:对15. 分子晶体的物质在任何情况下都不导电。
()解:错16. 分子晶体的特性之一是熔点均相对较低。
()解:对17. 原子晶体的特性之一是熔点高。
()解:对18. 所有层状晶体均可作为润滑剂和导电体使用。
()解:错19. 某物质可生成两种或两种以上的晶体,这种现象叫做类质多晶现象。
()解:错20. 石墨晶体层与层之间的主要结合力为金属键。
()解:错21. 无定形物质都是由微小的晶粒组成的。
()解:错22. 自然界存在的晶体或人工制备的晶体中,所有粒子都是按照一定规律有序排列的,没有任何缺陷。
()解:错23. 一般来说,离子晶体的晶格能越大,该晶体的热稳定性就越低。
()解:错24. 离子晶体的晶格能越大,熔点越低。
( )解:错25. 对离子晶体而言,离子半径变大,将有利于其晶格能变小。
无机化学晶体结构

补充知识:
盖斯定律
在热化学中,能量守恒定律表现为盖斯定律。某些难于测量反应热的反应,可用盖斯定律从一些已知的化学反应热数值间接求算出。
一个化学反应若能分解成几步来完成,总反应的热效应(焓变) ∆H 等于各步分反应的热效应之和:
rH总 =rH1 + rH2 + ······ (4-2)
X射线衍射的原理
晶体X-射线衍射图
晶系: Monoclinic
空间群: P2(1)/n
a=7.6557(19) Å b=18.573(5) Å c= 13.117(3) Å
= 90 = 94.392(3) = 90o
晶胞参数
3-1 晶体的微观性质(1)
点阵与晶格 从1912年劳厄(Laue)开始用x射线研究晶体结构至今,大量的事实证明晶体内部的质点具有周期性重复规律。为了便于研究晶体中微粒(原子,离子或分子)在空间排列的规律和特点,将晶体中按周期重复的那一部分微粒抽象成几何质点(晶格结点),联结其中任意两点所组成的向量进行无限平移,这一套点的无限组合就叫做点阵。
四方晶体,正离子Ti4+ 的配位数为6,负离子O2- 的配位数为3。Ti4+ 处于配位数为6的八面体中。
CaF2 型 (萤石)
金红石型 (TiO2)
半径比规则(1)
两原子核间距离=正离子半径+负离子半径 d=r+ + r- 通常r+ < r-
半径比规则(2)
以正、负离子配位数为6的晶体的一层为例 令r- = 1,则ac=4;ab=bc=2r+ + 2 因ab2+bc2=ac2r+ =0.414;即r+/r- =0.414
安徽安徽高中化学竞赛无机化学第六章晶体结构基础

安徽安徽高中化学竞赛无机化学第六章晶体结构基础6. 0. 01 晶体的四种差不多类型:依照晶体中微粒之间相互作用的性质,能够将晶体分成4种差不多类型:离子晶体、金属晶体、分子晶体和原子晶体。
6. 1. 01 分子晶体及其物理性质:分子之间以分子间作用力结合成的晶体称为分子晶体。
由于熔、沸点较低,因此分子晶体一样要在较低的温度下才能形成,而在常温时多以气体形式存在。
分子晶体的硬度较小,导电性能一样较差,因为电子从一个分子传导到另一个分子专门不容易。
6. 1. 02 极性分子:分子的正电荷重心和负电荷重心不重合,则为极性分子。
6. 1. 03 偶极矩:极性分子的极性能够用偶极矩m 来度量。
若正电荷(或负电荷)重心上的电荷量为q,正、负电荷重心之间距离即偶极长为d,则偶极矩m = q d6. 1. 04 偶极矩的单位:当d = 1.0 ´10-10 m,即d 为 1 ,q = 1.602 ´10-19 C,即q 为电子的电荷量时,偶极矩m = 4.8 D。
D 为偶极矩单位,称为德拜。
在国际单位制中,偶极矩m以C•m(库仑•米)为单位,当q = 1 C,d = 1 m时,m = 1 C•m。
C•m 与D 这两种偶极矩单位的换算关系为= 3.34 ´10-30 C•m6. 1. 05 永久偶极:极性分子的偶极矩称为永久偶极,偶极矩的矢量方向由正极指向负极。
多原子分子中的大p 键及孤电子对,有时也阻碍分子的偶极矩。
6. 1. 06 诱导偶极:非极性分子在外电场的作用下,能够变成具有一定偶极矩的极性分子,如下面左图所示。
而极性分子在外电场作用下,其偶极矩也能够增大,如下面右图所示。
在电场的阻碍下产生的偶极称为诱导偶极。
6. 1. 07 阻碍诱导偶极的因素:诱导偶极强度大小与电场强度成正比,也与分子的变形性成正比。
所谓分子的变形性,即分子的正、负电荷重心的可分程度。
分子体积越大,电子越多,变形性越大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
△ fHm = △ rHm,1 + △ rHm,2 +△ rHm,3 +△ rHm,4
+△ rHm,5 + △ rHm,6 mol-1 △ rHm,1 =89.2kJ·
△ rHm,3 △ rHm,2 =418.8kJ· mol-1
=15.5kJ· mol-1
mol-1 △ rHm,4 =96.5kJ·
1.三种典型的离子晶体
NaCl型
晶格:面心立方
配位比:6:6 晶胞中离子的个数: (红球-Na+ ,
绿球-Cl-)
1 1 1 Na : 12 1 4个 Cl : 8 6 4个 8 2 4
CsCl型
晶格: 简单立方 配位比: 8:8
(红球-Cs+ ,
绿球-Cl-)
例如:μ(SF6) = 0,键矩互相抵消, μ(H2O)≠0,键矩未能抵消。
分子的偶极矩μ(×10-30 C· m)
分子式 H2 N2 CO2 CS2 CH4 CO CHCl3 H2S 偶极矩 0 0 0 0 0 0.40 3.50 3.67 分子式 SO2 H2O NH3 HCN HF HCl HBr HI 偶极矩 5.33 6.17 4.90 9.85 6.37 3.57 2.67 1.40
mol-1 △ rHm,5 =-324.7kJ· mol-1 △ fHm =295.3kJ· 上述数据代入上式求得:
△ rHm,6 =-689.1kJ· mol-1
则:U =689.1kJ· mol-1
2.Born-Lande公式
KAZ1Z 2 1 U (1 ) R0 n
当 R0 以pm,U 以 kJ mol 为单位时,
定义:在标准状态下,按下列化学反
应计量式使离子晶体变为气体正离子和气
态负离子时所吸收的能量称为晶格能,用
U 表示。 MaXb(s)
aMb+(g) + bXa-(g)
△ rHm
例如: NaCl(s)
Na (g) + Cl (g)
-1 -1
+
-
△ rHm 786kJ mol
U 786kJ mol
Packing);
体心立方堆积(Body-centred Cubic Packing)。
§9.3
离子晶体
9.3.1 离子晶体的特征结构 9.3.2 晶格能 9.3.3 离子极化
9.3.1 离子晶体的特征结构
离子晶体:密堆积空隙的填充。 阴离子:大球,密堆积,形成空隙。 阳离子:小球,填充空隙。 规则:阴阳离子相互接触稳定; 配位数大,稳定。
NaCl NaCl
思考题:
解释碱土金属氯化物的熔点变化规律:
BeCl2 MgCl 2 CaCl2 SrCl 2 BaCl2
熔点/℃
405
714
782
876
962
§9.4
分子晶体
9.4.1 分子的偶极矩和极化率
9.4.2 分子间的吸引作用 9.4.3 氢键
9.4.1 分子的偶极矩和极化率
1.分子的偶极矩(μ):用于定量地表示极性 分子的极性大小。 ql
§9.4
§9.5
分子晶体
混合晶体
§9.1
晶体结构和类型
9.1.1 晶体结构的特征与晶格理论
9.1.2 晶体缺陷
9.1.3 球的密堆积 9.1.4 晶体类型
非晶体
9.1.1 晶体结构的特征与晶格理论
晶胞:晶体的最小重复单元,通过晶胞 在空间平移无隙地堆砌而成晶体。 晶胞的两个要素: 1. 晶胞的大小与形状: 由晶胞参数a,b,c, α,β,γ表示, a,b,c 为六面体边长, α,β, γ 分别是bc , ca , ab 所 组成的夹角。
ZnS型 n的取值:
离子电子 层构型 n值 He 5 Ne 7 Ar Kr Xe
A=1.638
(Cu )
9
+
(Ag )
10
+
(Au )
12
+
3.Калустинский公式
Z1Z 2 34.5 U 1.20210 1 {r r } {r r }
2.分子的极化率: 用于定量地表示分子的变形性大小。分 子的变形性大小指的是正电中心与负电中心 发生位移(由重合变不重合,由偶极长度小变 偶极长度大) 。 影响分子变形性大小的因素:
外因:外加电 场愈强,分子 变形愈厉害; 内因:分子愈 大,分子变形 愈厉害。
分子的极化率α(×10-40C· m2 · V-1)
138940 AZ1Z 2 1 1 U (1 ) kJ mol R0 n 式中: R0—正负离子核间距离, Z1,Z2 —分别为正负离子电荷的绝对值, A —Madelung常数,与晶体类型有关,
n —Born指数,与离子电子层结构类型有关。
1
A的取值: CsCl型 A=1.763
NaCl型 A=1.748
1.Born-Haber循环
1 K (s) + Br2 (l) 2
△ fHm
KBr(s)
U △ rHm,6
1 升 Br2 (g) 华 △ rHm,1 2 1 焓 键能 △ rHm,4 2气源自热 △ rHm,3Br (g)
K(g)
△ rHm,2
电离能
△ rHm,5
电子亲和能
Br (g) + + K (g)
按带心型式分类,将七大晶系分为14种 型式。例如,立方晶系分为简单立方、体心 立方和面心立方三种型式。
9.1.3 球的密堆积
1.六方密堆积:hcp
第三层与第一 层对齐,产生 ABAB…方式。 配位数:12 空间占有率: 74.05%
2.面心立方密堆积:fcc
第三层与 第一层有错位, 以ABCABC… 方式排列。
2
2
令 r 1
r / r 0.414
NaCl晶体
r / r 0.414 理想的稳定结构(NaCl)
r / r 0.225 → 0.414 0.414 → 0.732 0.732 → 1.00 半径比规则
配位数 4 6 8
构型 ZnS 型 NaCl 型 CsCl 型
9.3.2 晶格能
第九章
晶体结构
• 教学要求: • 1、理解晶体的基本概念,掌握四种晶体类 型的特征和性质; • 2、初步了解离子极化的概念及其应用; • 3、掌握金属键的“自由电子”理论,了解 能带理论。 • 教学难点: • 离子极化;离子晶体的空间结构。
第九章
§9.1
§9.2 §9.3
晶体结构
晶体结构和类型
金属晶体 离子晶体
式中 q 为极上所带电量,l 为偶极长度。 极性分子 非极性分子 μ≠0 μ=0
双原子分子: 异核:HX 多原子分子: O3(V字形)
同核: H2 N2 O2
S8,P4
CO 2 BF3 ,CH 4 ,
NH3
分子的偶极矩与键矩的关系: 极性键构成的双原子分子: 分子偶极矩 = 键矩
多原子分子的偶极矩 = 键矩的矢量和,
晶格能对离子晶体物理性质的影响: 离子电荷数大,离子半径小的离子晶体晶 格能大,相应表现为熔点高、硬度大等性能。
NaCl 型 离子晶体 NaF NaCl NaBr NaI MgO CaO SrO BaO Z1 1 1 1 1 2 2 2 2 Z2 1 1 1 1 2 2 2 2 r+ /pm 95 95 95 95 65 99 113 135 rU /pm /kJ·mol-1 136 920 181 770 195 733 216 683 140 4147 140 3557 140 3360 140 3091 熔点 /o C 992 801 747 662 2800 2576 2430 1923 硬度 3.2 2.5 <2.5 <2.5 5.5 4.5 3.5 3.3
9.3.3 离子极化
未极化的负离子
极化的负离子
离子的极化率(α): 描述离子本身变形性的物理量。 离子的极化力(f ): 描述一个离子对其他离子变形的影响能力。
1.离子的极化率(α ) 一般规律: ① 离子半径 r : r 愈大, α 愈大。 如α :Li+<Na+<K+<Rb+<Cs+;F-<Cl-<Br-<I- ② 负离子极化率大于正离子的极化率。 ③ 离子电荷:正离子电荷少的极化率大。 如:α (Na+) >α (Mg2+) ④ 离子电荷:负离子电荷多的极化率大。 如:α (S2-) >α (Cl-) ⑤ 离子的电子层构型:(18+2)e-,18e-> 9-17e->8e如:α (Cd2+) >α (Ca2+); α (Cu+) >α (Na+)
SiO 2
NaCl 干冰
§9.2
金属晶体
9.2.1 金属晶体的结构 9.2.2 金属键理论
9.2.3 金属合金
9.2.1 金属晶体的结构
金属晶体是金属原子或离子彼此靠金 属键结合而成的。金属键没有方向性,金 属晶体内原子以配位数高为特征。 金属晶体的结构:等径球的密堆积。
金属晶体中粒子的排列方式常见的有三种: 六方密堆积(Hexgonal close Packing); 面心立方密堆积(Face-centred Cubic clode
5
n n
n :晶体分子式中正离子的个数 n :晶体分子式中负离子的个数
例如:CaCl2 1 2 3 2 1 34.5 5 U ( NaCl ) 1.202 10 (1 ) 95 181 95 181
