湖南省长郡中学高中化学课件:必修一 4.3《硫和氮的氧化物》(共43张PPT)
合集下载
课件_人教版化学必修一硫和氮的氧化物-课件PPT精品课件[完整版]
![课件_人教版化学必修一硫和氮的氧化物-课件PPT精品课件[完整版]](https://img.taocdn.com/s3/m/5fe2501b9b89680202d82572.png)
SO2+CaO==CaSO3
• 淡黄色固体:S、Na O SO3+H20==H2SO4
2 2 SO2能使品红溶液褪色,但不能使酸、碱指示剂,红墨水等褪色
将有色物质吸附而褪色(物理变化)
加热后,红色复原,有刺激性气味
SO3+CaO==CaSO4
SO3+H20==H2SO4
单质硫
3、化学性质
(1)与金属
澄清石灰水 品红溶液 品红溶液 先除掉SO2,再检验CO2
二氧化硫
3、用途
加热后,红色复原,有刺激性气味 先除掉SO2,再检验CO2 SO2能使品红溶液褪色,但不能使酸、碱指示剂,红墨水等褪色 SO3+CaO==CaSO4 SO2+CaO==CaSO3 SO3+H20==H2SO4 SO2能使品红溶液褪色,但不能使酸、碱指示剂,红墨水等褪色 将有机色质内部“生色团” SO3+CaO==CaSO4 SO2能使品红溶液褪色,但不能使酸、碱指示剂,红墨水等褪色 SO2能使品红溶液褪色,但不能使酸、碱指示剂,红墨水等褪色 黄铜矿(CuFeS2) 俗称“硫磺”,淡黄色固体,不溶于水,微溶于酒精,易溶于二硫化碳(CS2) SO2+H20≒H2SO3 SO2+Cl2+2H2O==2HCl+H2SO4 SO2+CaO==CaSO3 将有色物质吸附而褪色(物理变化)
三氧化硫
1常、温物下理为性无质色液体 2•SS、OO酸C33a+(化性S少HO2学0氧4)↓=+性=化C+Ha质H2物(S2OOO(H4通)2=性= ) S将俗S将将芒SS先将S将SS先S2将先SS先先S先将S使2S将加黄加NNOOOOOOOOOOOOO有称有有硝除有有除有除除除除有K有热铜热aa2322323322333M++机 “ 机 色 (掉 机 色 掉 色 掉 掉 掉 掉 色 色 后 矿 后+++++++(+++能能N少SSnCHCHCHHHCC色硫色物S色物S物SSSS物物,(,使使aO==aal2l2a222C)222=OOOOOO=+400O000OO质磺质质质质质质质红红品品u++S=C=(=====222222F===22HNNOa内”内吸内吸吸吸吸色色=====红,,,,,,红eHH===+(aaHHHHH4SCCCO22部,部附部附附附附复复溶溶再再再再再再)22·22222、2OO1aaaHSSSSSSS“淡“而“而而而而原原)液液检检检检检检0SSS==)新OOOOOH2OOO==生黄生褪生褪褪褪褪,,褪褪验验验验验验=444442制22344=O色色色色色色色色色有有HH色色CCCCCC氯C)CCOOOOOO团固团团刺刺(((((,,a物物物物物水ll222222++S”体””激激但但HH理理理理理O、22破,性性不不3变变变变变新SS↓坏不气气能能OO+化化化化化制H44掉溶味味使使)))))溴2于(酸酸O不水水、、可褪,碱碱逆色微指指),溶示示表于剂剂现酒,,其精红红强,墨墨还易水水原溶等等性于褪褪二色色硫化碳(CS2)
高一化学-4.3-硫和氮的氧化物1-新人教版必修1PPT课件

二 看颜色
无色气体
氧 闻气味
强烈的刺激性气味
化 死、亡浓
的 做比较
和空气的平比均空相气密度大
物 理
沸
点
对分子质量对比
沸点为-10容0C易液化
性 溶解性
1解体4积0体的积水的大易二约氧溶可化以于硫溶水
质 二氧化硫是一种无色、有刺激性气味、有毒、
比空气重、容易液化- 、易溶于水的气体。7
程度: 暂时性,加热可复原
范围:漂白某些有色物质,不能使紫
色石蕊试液褪色
-
17
二 探究:在上述实验的试管 氧 中保留1/3溶液,滴入1-2 化 滴品红溶液,振荡,观察
硫 颜色变化。加热试管,再
的 观察。
化 学
现象:品红褪色,加热后溶液又变红。
性 现象分析:SO2跟某些有色物质生成不稳定的无色
质 物质。这种无色物质易分解而使有色物质恢复原来
-
22
-
23
思考与交流:
SO2能使溴水、KMnO4溶液褪
色与SO2使品红褪色,实质相同吗?
不同!
-
24
我们知道SO2 和Cl2都具有漂白性。 为了使漂白性更强,有人提出将两
者混合使用,你认为这种做法能达 到预期目的吗?
SO2 +Cl2+2H2O=H2SO4 +2HCl (两种气体生成两种强酸)
的颜色。
|漂 注:SO2只能使酸碱指示剂变色,不能使之褪色。
白 思考:SO2的漂白原理与Cl2水的漂白原理是否相同?
性
-
18
氯水和二氧化硫漂白性的比较
氯水中HClO将有色物 SO2溶于水与有色物质 质氧化成无色物质 直接结合生成不稳定
最新化学1必修4.3《硫和氮的氧化物》教学课件

SO2 + Cl2 +2H2O = 2HCl + H2SO4
二、二氧化氮和一氧化氮 1、氮气(N2)
1)、氮气的物理性质:
无色无味气体 不溶于水 比空气稍轻
2)、氮气的化学性质:
N2 + O2 =放=电=或==高=温 2NO
3)、氮气的用途:
保护气、填充灯泡、焊接金 属、低温制冷等
2、一氧化氮(NO):
SO2能使溴水褪色,试分析褪色原因
SO3的化学性质
3、三氧化硫——酸性氧化物)
无色固体,熔点(16.8℃)
SO3
沸点(44.8℃ )都很低
SO3+ H2O 2SO2 + O2
H2SO4 (放出大量热)
催化剂
△ 2SO3
工业上常用上面两个反应制取硫酸
SO3的化学性质
三氧化硫跟碱或碱性氧化物反应
SO3 + CaO = CaSO4 SO3 + Ca(OH)2 = CaSO4+ H2O
硫粉
SO2的化学性质 ② SO2具有漂白作用:但漂白后的新
物质不稳定,易恢复原来的颜色(检验SO2的存在)
SO2的化学性质
思考:草帽、纸张为什么会泛黄?
探讨:你学过的哪些物质具有漂白性?
活性炭
物理吸附
H2O2 Na2O2 HClO … ...
氧化漂白 漂白原理是否相同?
SO2的化学性质
2.下列可以用来鉴别SO2 和CO2 的方法 是[ B D ] A、通入紫色石蕊试液 B、闻气味 C、通入澄清石灰水 D、通入品红溶液中
硫的氧化物
随堂
【学与用】
练习
氯气和二氧化硫皆可做漂白剂,若用
两者以1:1的物质的量一起漂白一种有色
人教版高中化学必修1第四章 第三节《硫和氮的氧化物》课件 (共40张PPT)

红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 无色气体变为红棕 色气体,又变为无 色气体,但气体体 积逐渐缩小,液面 不断上升 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
氮元素最典型的氧化物
NO
NO2
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
Prize citation: "for their discoveries concerning nitric oxide as a signalling molecule in the cardiovascular system"
科学视野:信使分子——NO
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。 除了以上生理功能外,一氧化氮还在呼吸 系统、内分泌系统中起重要作用。
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
氮元素最典型的氧化物
NO
NO2
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
Prize citation: "for their discoveries concerning nitric oxide as a signalling molecule in the cardiovascular system"
科学视野:信使分子——NO
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。 除了以上生理功能外,一氧化氮还在呼吸 系统、内分泌系统中起重要作用。
人教版化学必修一4.3《硫和氮的氧化物-二氧化硫》课件优秀课件PPT

实验室制取SO2,可选择用碱液吸收尾 气, 防止空气污染。
二、SO2的性质
SO2+2NaOH=Na2SO4+H2O SO2 + Ca(OH)2 = CaSO3 + H2O
使澄清石灰水先变浑浊 后变澄清的气体,除CO2外, 还可能是SO2。
怎样除去CO2中的SO2?
二、SO2的性质 2.SO2的漂白性
SO2能与某些有色物质结合成不稳定的无 色物质而具有漂白性---暂时性.
——化合漂白
不能使紫酸碱指示剂褪色----选择性
思考:
为什么长时间放置的报纸和草 帽会变黄?
SO2的漂白性
SO2的漂白性
探讨:你学过的哪些物质具有漂白性?
活性炭 H2O2 Na2O2 HClO … ...
物理吸附 氧化漂白 漂白原理是否相同?
B.金属Na投入加有酚酞的水中,得到的溶液颜色变 化: 无色→红色
C.SO2通入品红溶液一段时间后再加热,溶液颜色 的变化为:无色→红色
D.氯水加入到FeCl2溶液中,溶液颜色的变化为: 黄色→浅绿色
谢谢!
用微笑告诉别人,今天的我,比昨天更强。瀑布跨过险峻陡壁时,才显得格外雄伟壮观。勤奋可以弥补聪明的不足,但聪明无法弥补懒惰的缺陷。孤独是 每个强者必须经历的坎。有时候,坚持了你最不想干的事情之后,会得到你最想要的东西。生命太过短暂,今天放弃了明天不一定能得到。只有经历人生 的种种磨难,才能悟出人生的价值。没有比人更高的山,没有比脚更长的路学会坚强,做一只沙漠中永不哭泣的骆驼!一个人没有钱并不一定就穷,但没 有梦想那就穷定了。困难像弹簧,你强它就弱,你弱它就强。炫丽的彩虹,永远都在雨过天晴后。没有人能令你失望,除了你自己人生舞台的大幕随时都 可能拉开,关键是你愿意表演,还是选择躲避。能把在面前行走的机会抓住的人,十有八九都会成功。再长的路,一步步也能走完,再短的路,不迈开双 脚也无法到达。有志者自有千计万计,无志者只感千难万难。我成功因为我志在成功!再冷的石头,坐上三年也会暖。平凡的脚步也可以走完伟大的行程。 有福之人是那些抱有美好的企盼从而灵魂得到真正满足的人。如果我们都去做自己能力做得到的事,我们真会叫自己大吃一惊。只有不断找寻机会的人才 会及时把握机会。人之所以平凡,在于无法超越自己。无论才能知识多么卓著,如果缺乏热情,则无异纸上画饼充饥,无补于事。你可以选择这样的“三 心二意”:信心恒心决心;创意乐意。驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。如果一个人不知道他要驶向哪个码头, 那么任何风都不会是顺风。行动是理想最高贵的表达。你既然认准一条道路,何必去打听要走多久。勇气是控制恐惧心理,而不是心里毫无恐惧。不举步, 越不过栅栏;不迈腿,登不上高山。不知道明天干什么的人是不幸的!智者的梦再美,也不如愚人实干的脚印不要让安逸盗取我们的生命力。别人只能给 你指路,而不能帮你走路,自己的人生路,还需要自己走。勤奋可以弥补聪明的不足,但聪明无法弥补懒惰的缺陷。后悔是一种耗费精神的情绪,后悔是 比损失更大的损失,比错误更大的错误,所以,不要后悔!复杂的事情要简单做,简单的事情要认真做,认真的事情要重复做,重复的事情要创造性地做。 只有那些能耐心把简单事做得完美的人,才能获得做好困难事的本领。生活就像在飙车,越快越刺激,相反,越慢越枯燥无味。人生的含义是什么,是奋 斗。奋斗的动力是什么,是成功。决不能放弃,世界上没有失败,只有放弃。未跌过未识做人,不会哭未算幸运。人生就像赛跑,不在乎你是否第一个到 达终点,而在乎你有没有跑完全程。累了,就要休息,休息好了之后,把所的都忘掉,重新开始!人生苦短,行走在人生路上,总会有许多得失和起落。 人生离不开选择,少不了抉择,但选是累人的,择是费人的。坦然接受生活给你的馈赠吧,不管是好的还是坏的。现在很痛苦,等过阵子回头看看,会发 现其实那都不算事。要先把手放开,才抓得住精彩旳未来。可以爱,可以恨,不可以漫不经心。我比别人知道得多,不过是我知道自己的无知。你若不想 做,会找一个或无数个借口;你若想做,会想一个或无数个办法。见时间的离开,我在某年某月醒过来,飞过一片时间海,我们也常在爱情里受伤害。1、 只有在开水里,茶叶才能展开生命浓郁的香气。人生就像奔腾的江水,没有岛屿与暗礁,就难以激起美丽的浪花。别人能做到的事,我一定也能做到。不 要浪费你的生命,在你一定会后悔的地方上。逆境中,力挽狂澜使强者更强,随波逐流使弱者更弱。凉风把枫叶吹红,冷言让强者成熟。努力不不一定成 功,不努力一定不成功。永远不抱怨,一切靠自己。人生最大的改变就是去做自己害怕的事情。每一个成功者都有一个开始。勇于开始,才能找到成功的 路。社会上要想分出层次,只有一个办法,那就是竞争,你必须努力,否则结局就是被压在社会的底层。后悔是一种耗费精神的情绪后悔是比损失更大的 损失,比错误更大的错误所以不要后悔。每个人都有潜在的能量,只是很容易:被习惯所掩盖,被时间所迷离,被惰性所消磨。与其临渊羡鱼,不如退而结网。 生命之灯因热情而点燃,生命之舟因拼搏而前行。世界会向那些有目标和远见的人让路。不积跬步,无以至千里;不积小流,无以成江海。骐骥一跃,不 能十步;驽马十驾,功在不舍。锲而舍之,朽木不折;锲而不舍,金石可镂。若不给自己设限,则人生中就没有限制你发挥的藩篱。赚钱之道很多,但是 找不到赚钱的种子,便成不了事业家。最有效的资本是我们的信誉,它小时不停为我们工作。销售世界上第一号的产品——不是汽车,而是自己。在你成
二、SO2的性质
SO2+2NaOH=Na2SO4+H2O SO2 + Ca(OH)2 = CaSO3 + H2O
使澄清石灰水先变浑浊 后变澄清的气体,除CO2外, 还可能是SO2。
怎样除去CO2中的SO2?
二、SO2的性质 2.SO2的漂白性
SO2能与某些有色物质结合成不稳定的无 色物质而具有漂白性---暂时性.
——化合漂白
不能使紫酸碱指示剂褪色----选择性
思考:
为什么长时间放置的报纸和草 帽会变黄?
SO2的漂白性
SO2的漂白性
探讨:你学过的哪些物质具有漂白性?
活性炭 H2O2 Na2O2 HClO … ...
物理吸附 氧化漂白 漂白原理是否相同?
B.金属Na投入加有酚酞的水中,得到的溶液颜色变 化: 无色→红色
C.SO2通入品红溶液一段时间后再加热,溶液颜色 的变化为:无色→红色
D.氯水加入到FeCl2溶液中,溶液颜色的变化为: 黄色→浅绿色
谢谢!
用微笑告诉别人,今天的我,比昨天更强。瀑布跨过险峻陡壁时,才显得格外雄伟壮观。勤奋可以弥补聪明的不足,但聪明无法弥补懒惰的缺陷。孤独是 每个强者必须经历的坎。有时候,坚持了你最不想干的事情之后,会得到你最想要的东西。生命太过短暂,今天放弃了明天不一定能得到。只有经历人生 的种种磨难,才能悟出人生的价值。没有比人更高的山,没有比脚更长的路学会坚强,做一只沙漠中永不哭泣的骆驼!一个人没有钱并不一定就穷,但没 有梦想那就穷定了。困难像弹簧,你强它就弱,你弱它就强。炫丽的彩虹,永远都在雨过天晴后。没有人能令你失望,除了你自己人生舞台的大幕随时都 可能拉开,关键是你愿意表演,还是选择躲避。能把在面前行走的机会抓住的人,十有八九都会成功。再长的路,一步步也能走完,再短的路,不迈开双 脚也无法到达。有志者自有千计万计,无志者只感千难万难。我成功因为我志在成功!再冷的石头,坐上三年也会暖。平凡的脚步也可以走完伟大的行程。 有福之人是那些抱有美好的企盼从而灵魂得到真正满足的人。如果我们都去做自己能力做得到的事,我们真会叫自己大吃一惊。只有不断找寻机会的人才 会及时把握机会。人之所以平凡,在于无法超越自己。无论才能知识多么卓著,如果缺乏热情,则无异纸上画饼充饥,无补于事。你可以选择这样的“三 心二意”:信心恒心决心;创意乐意。驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。如果一个人不知道他要驶向哪个码头, 那么任何风都不会是顺风。行动是理想最高贵的表达。你既然认准一条道路,何必去打听要走多久。勇气是控制恐惧心理,而不是心里毫无恐惧。不举步, 越不过栅栏;不迈腿,登不上高山。不知道明天干什么的人是不幸的!智者的梦再美,也不如愚人实干的脚印不要让安逸盗取我们的生命力。别人只能给 你指路,而不能帮你走路,自己的人生路,还需要自己走。勤奋可以弥补聪明的不足,但聪明无法弥补懒惰的缺陷。后悔是一种耗费精神的情绪,后悔是 比损失更大的损失,比错误更大的错误,所以,不要后悔!复杂的事情要简单做,简单的事情要认真做,认真的事情要重复做,重复的事情要创造性地做。 只有那些能耐心把简单事做得完美的人,才能获得做好困难事的本领。生活就像在飙车,越快越刺激,相反,越慢越枯燥无味。人生的含义是什么,是奋 斗。奋斗的动力是什么,是成功。决不能放弃,世界上没有失败,只有放弃。未跌过未识做人,不会哭未算幸运。人生就像赛跑,不在乎你是否第一个到 达终点,而在乎你有没有跑完全程。累了,就要休息,休息好了之后,把所的都忘掉,重新开始!人生苦短,行走在人生路上,总会有许多得失和起落。 人生离不开选择,少不了抉择,但选是累人的,择是费人的。坦然接受生活给你的馈赠吧,不管是好的还是坏的。现在很痛苦,等过阵子回头看看,会发 现其实那都不算事。要先把手放开,才抓得住精彩旳未来。可以爱,可以恨,不可以漫不经心。我比别人知道得多,不过是我知道自己的无知。你若不想 做,会找一个或无数个借口;你若想做,会想一个或无数个办法。见时间的离开,我在某年某月醒过来,飞过一片时间海,我们也常在爱情里受伤害。1、 只有在开水里,茶叶才能展开生命浓郁的香气。人生就像奔腾的江水,没有岛屿与暗礁,就难以激起美丽的浪花。别人能做到的事,我一定也能做到。不 要浪费你的生命,在你一定会后悔的地方上。逆境中,力挽狂澜使强者更强,随波逐流使弱者更弱。凉风把枫叶吹红,冷言让强者成熟。努力不不一定成 功,不努力一定不成功。永远不抱怨,一切靠自己。人生最大的改变就是去做自己害怕的事情。每一个成功者都有一个开始。勇于开始,才能找到成功的 路。社会上要想分出层次,只有一个办法,那就是竞争,你必须努力,否则结局就是被压在社会的底层。后悔是一种耗费精神的情绪后悔是比损失更大的 损失,比错误更大的错误所以不要后悔。每个人都有潜在的能量,只是很容易:被习惯所掩盖,被时间所迷离,被惰性所消磨。与其临渊羡鱼,不如退而结网。 生命之灯因热情而点燃,生命之舟因拼搏而前行。世界会向那些有目标和远见的人让路。不积跬步,无以至千里;不积小流,无以成江海。骐骥一跃,不 能十步;驽马十驾,功在不舍。锲而舍之,朽木不折;锲而不舍,金石可镂。若不给自己设限,则人生中就没有限制你发挥的藩篱。赚钱之道很多,但是 找不到赚钱的种子,便成不了事业家。最有效的资本是我们的信誉,它小时不停为我们工作。销售世界上第一号的产品——不是汽车,而是自己。在你成
必修一化学人教版 4.3 硫和氮的氧化物 课件(共46张PPT)

第三节 硫和氮的氧化物
硫广泛存在于自然界 游离态的硫存在于火山喷口 游离态的硫存在于火山喷口 附近或地壳的岩层里 附近或地壳的岩层里
硫广泛存在于自然界
化合态的硫主要以硫化物和 硫酸盐的形式存在
黄铜矿
石膏
黄铁矿
一、二氧化硫和三氧化硫 1、硫元素的存在形式 (1)游离态:单质硫存在于火山口 附近或地壳的岩层里。 (2)气态、液态化合物 :H2S、 SO2、SO3
2N2 +
放电或 O2 高温 ===
2NO
(工业制硝酸的第二步)
2NO + O2 == 2 NO2
3NO2 + H2O == 2HNO3 + NO (工业制硝酸的第三步) 2NO2 + 2NaOH== 2NaNO3 + NaNO2+H2O NO2 + NO+2NaOH== 2NaNO2+H2O
[科学探究] 书p92
有关NO、NO2、O2混合气体 通入水中的计算 (1)NO2、NO混合气体溶于水
3NO2 + H2O = 2HNO3 + NO
例1:10mLNO2和NO的混合气体通入水中, 充分反应后,剩余6mL气体。
问:剩余气体是什么?
原混合气体中NO2有多少?
(2 )
NO、O2混合气体溶于水
① 2NO + O2 == 2NO2 ② 3NO2 + H2O == 2HNO3 + NO
5SO2 + 2KMnO4+ 2H2O = K2SO4 + 2MnSO4 + 2H2SO4
SO2 + Cl2 + 2H2O = H2SO4 + 2HCl SO2 + Br2 + 2H2O = H2SO4 + 2HBr SO2 + I2 + 2H2O = H2SO4 + 2HI
硫广泛存在于自然界 游离态的硫存在于火山喷口 游离态的硫存在于火山喷口 附近或地壳的岩层里 附近或地壳的岩层里
硫广泛存在于自然界
化合态的硫主要以硫化物和 硫酸盐的形式存在
黄铜矿
石膏
黄铁矿
一、二氧化硫和三氧化硫 1、硫元素的存在形式 (1)游离态:单质硫存在于火山口 附近或地壳的岩层里。 (2)气态、液态化合物 :H2S、 SO2、SO3
2N2 +
放电或 O2 高温 ===
2NO
(工业制硝酸的第二步)
2NO + O2 == 2 NO2
3NO2 + H2O == 2HNO3 + NO (工业制硝酸的第三步) 2NO2 + 2NaOH== 2NaNO3 + NaNO2+H2O NO2 + NO+2NaOH== 2NaNO2+H2O
[科学探究] 书p92
有关NO、NO2、O2混合气体 通入水中的计算 (1)NO2、NO混合气体溶于水
3NO2 + H2O = 2HNO3 + NO
例1:10mLNO2和NO的混合气体通入水中, 充分反应后,剩余6mL气体。
问:剩余气体是什么?
原混合气体中NO2有多少?
(2 )
NO、O2混合气体溶于水
① 2NO + O2 == 2NO2 ② 3NO2 + H2O == 2HNO3 + NO
5SO2 + 2KMnO4+ 2H2O = K2SO4 + 2MnSO4 + 2H2SO4
SO2 + Cl2 + 2H2O = H2SO4 + 2HCl SO2 + Br2 + 2H2O = H2SO4 + 2HBr SO2 + I2 + 2H2O = H2SO4 + 2HI
4.3硫和氮的氧化物课件(人教版必修1)
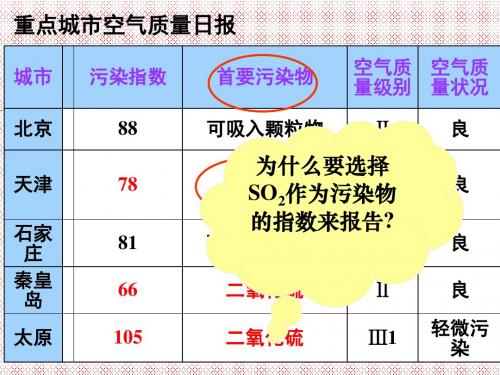
重点城市空气质量日报
城市 北京 天津 污染指数 88 78 首要污染物 可吸入颗粒物 空气质 空气质 量级别 量状况 Ⅱ 良 良
石家 庄 秦皇 岛
太原
81
66 105
可吸入颗粒物
二氧化硫 二氧化硫
为什么要选择 二氧化硫 Ⅱ SO2作为污染物 的指数来报告?
Ⅱ
Ⅱ Ⅲ1
良
良 轻微污 染
酸雨的危害:酸雨是如何形成的?
SO2的化学性质
推 测
SO2作为酸性氧化物应该有那些性质?
与H2O反应生成酸
酸性氧化物通性
与碱反应生成盐和水 与碱性氧化物反生成盐
练一练
请写出SO2与氧化钙、Ca(OH)2溶液反 应的化学方程式。
标出SO2中S元素的化合价推断它应具有怎样 的化学性质?
表现还原性, 需加入 氧化 剂来实现,
如
催化剂 2SO2+O2 ==== 2SO3 。 △
使湖泊中 鱼虾死亡
破坏露天文 物古迹
损坏植物叶面导 致森林死亡
腐蚀建筑物和 工业设备
市场采购: 有黄白两种银耳,买哪种好呢?
4.3 硫和氮的氧化物
二氧化硫
胡学英
认识硫单质
硫单质的物理性质
颜色:黄色晶体,质 脆,易研成粉末。
不 溶解性: __溶于水, 微溶 易 ___于酒精, __溶于 CS2.
中学阶段只 有品红
ቤተ መጻሕፍቲ ባይዱ
SO2和Cl2都能使品红溶液褪色,当在 相同条件下将等体积的SO2和Cl2通入 品红溶液中品红会褪色吗?
想一想
知识梳理
物质分类角度
物理性质 SO2 化学性质
氧化还原角度
酸性氧 化物 以还原性 为主
漂白性
城市 北京 天津 污染指数 88 78 首要污染物 可吸入颗粒物 空气质 空气质 量级别 量状况 Ⅱ 良 良
石家 庄 秦皇 岛
太原
81
66 105
可吸入颗粒物
二氧化硫 二氧化硫
为什么要选择 二氧化硫 Ⅱ SO2作为污染物 的指数来报告?
Ⅱ
Ⅱ Ⅲ1
良
良 轻微污 染
酸雨的危害:酸雨是如何形成的?
SO2的化学性质
推 测
SO2作为酸性氧化物应该有那些性质?
与H2O反应生成酸
酸性氧化物通性
与碱反应生成盐和水 与碱性氧化物反生成盐
练一练
请写出SO2与氧化钙、Ca(OH)2溶液反 应的化学方程式。
标出SO2中S元素的化合价推断它应具有怎样 的化学性质?
表现还原性, 需加入 氧化 剂来实现,
如
催化剂 2SO2+O2 ==== 2SO3 。 △
使湖泊中 鱼虾死亡
破坏露天文 物古迹
损坏植物叶面导 致森林死亡
腐蚀建筑物和 工业设备
市场采购: 有黄白两种银耳,买哪种好呢?
4.3 硫和氮的氧化物
二氧化硫
胡学英
认识硫单质
硫单质的物理性质
颜色:黄色晶体,质 脆,易研成粉末。
不 溶解性: __溶于水, 微溶 易 ___于酒精, __溶于 CS2.
中学阶段只 有品红
ቤተ መጻሕፍቲ ባይዱ
SO2和Cl2都能使品红溶液褪色,当在 相同条件下将等体积的SO2和Cl2通入 品红溶液中品红会褪色吗?
想一想
知识梳理
物质分类角度
物理性质 SO2 化学性质
氧化还原角度
酸性氧 化物 以还原性 为主
漂白性
化学必修一4.3《硫和氮的氧化物》教学课件

Ⅱ、 性质 液化、比空气重、易溶于水 1、具有酸性氧化物的通性
二氧化硫
A、与水反应生成酸
SO2 + H2O
H2SO3
化学
课
性质
B、与碱反应生成盐和水
SO2 + 2NaOH
Na2SO3 + H2O
堂
2、既有氧化性,又有还原性
小
2SO2 + O2 催化剂 2SO3
结
3、漂白性:暂时性漂白
品红 通SO2 褪色(无色)
28 g/mol =1.2 5 g/L
22.4 L/mol 空气密度ρ=1.295 g/L
已知氮气占空气总体积的78%, 试求空气中氮气的质量分数
0.78×28 ×100% = 75%
1×29
2)、氮气的化学性质:
N2 + O2 =放=电=或==高=温 2NO
3)、氮气的用途:
保护气、填充灯泡、焊接金 属、低温制冷等
103
二氧化硫
Ⅱ Ⅱ Ⅱ Ⅲ1
良 良 良 轻微污染
云浮 2007-12-14
80
可吸入颗粒物
Ⅱ
良
为什么要选择SO2作为首要污染物呢?它们是从
哪儿来的?具有什么样的性质呢?
思考
二氧化硫对环境的污染
硫的氧化物
1、硫(S)
(1)、硫的存在:
游离态
火山喷口
地壳岩层
二
化合态
硫化物:硫铁矿或黄铁硫矿晶(体FeS2)等 硫酸盐:芒硝(Na2SO4·10H2O)
活性炭
物理吸附
H2O2 Na2O2 HClO … ...
氧化漂白 漂白原理是否相同?
SO2的化学性质
2. SO2的化学性质
(精品)化学1必修4.3《硫和氮的氧化物》教学课件

2)、NO2的化学性质:
+4
+5
3NO2 + H2O = 2HNO3 + NO(工业制硝酸的第三步)
科 学 自行设计实验:尽可能多的使NO2被水溶解
探
究 填写课本P92页如下表内容
实验步骤
现象
解释
(1)
(2)
……
NO2 和 O2 混和气体溶于水的反应
3NO2 + H2O = 2HNO3 + NO ① ① ×2 + ② 2NO + O2 = 2NO2 ② 总反应:4NO2 + O2 + 2H2O = 4HNO3
硫粉的试管中分 别加入蒸馏水、 酒精。
俗称:硫磺 淡黄色晶体 质脆,容易研成粉末。 不溶于水,微溶于酒精, 易溶于二硫化碳。
密度比水大(约为2 g/cm3 ) 熔沸点低(112.8℃, 444.6 ℃)
硫的氧化物
(3)硫的化学性质
0
点燃 +4
S + O2 = SO2 硫作为还原剂,具有还原性。
现 有刺激性气味的气体生成。 象 硫在空气中安静地燃烧,发出淡蓝色火焰;
82
二氧化硫
广州 2007-12-14
62
可吸入颗粒物
柳州 2007-12-14
103
二氧化硫
Ⅱ Ⅱ Ⅱ Ⅲ1
良 良 良 轻微污染
云浮 2007-12-14
80
可吸入颗粒物
Ⅱ
良
为什么要选择SO2等作为首要污染物呢?它们是
从哪儿来的?具有什么样的性质呢?
思考
二氧化硫对环境的污染
硫的氧化物
二氧化硫和三氧化硫
一辆迎面驶来大货车相撞后翻倒在地,槽罐 车上约32吨液态氯气快速泄漏。事故发生后,
高中化学必修一第四章第三节(1、2、3课时)硫和氮的氧化物 (共43张PPT)

密度比空气大 密度
(二)化学性质
【P90实验4-7:SO2与H2O反应】
1、 盛有SO2 气体的试管水位有什么变化?说明了什么?
试管内水位上升;说明SO2易溶水
2、溶液颜色有什么变化?说明什么问题?
紫色石蕊试液变红色,溶液呈酸性
1、与H2O反应:
SO2+H2O H2SO3(亚硫酸)
亚硫酸是一种弱酸,不稳定 。
试管内壁附着硫怎样洗掉?
化学性质: 既有氧化性又有还原性!
S+Fe=FeS
△
2Cu+S=Cu2S
△
S+O2=SO2
点燃
一、硫的氧化物
二氧化硫
1.来源:
煤等含硫燃料的燃烧、工业 废气、火山喷发等. 点燃
S + O2
SO2
2.物理性质
颜色状态 无色气体
刺激性气味 气味
毒性 有毒
SO2
易液化 沸点 水溶性
可逆反应:
在同一条件下,既向正反应方向进行, 同时又向逆反应方向进行的反应
特点:①相同条件 ②同时向两个方向进行
2、具有酸性氧化物的通性
与碱反应
SO2+2NaOH=Na2SO3+H2O 与碱性氧化物反应: SO2+Na2O=Na2SO3 (亚硫酸钠)
SO2 +CaO==CaSO3 (亚硫酸钙)
实验室制取SO2,可选择用碱液吸收尾气,防止空气污染。
3NO2+H2O= 2HNO3+NO
2、你的设计对工业上生产硝酸有什么启示?
------工业生产硝酸,将尾气(NO)吸收通入
适量的氧气后再溶解于水,经过多次循环氧化、 溶解,可充分利用原料,并减少NO的排放,保
人教版高中化学必修一4.3 硫和氮的氧化物 课件 (共73张PPT)

硫和氮的氧化物
一、硫元素的存在形式
(1)游离态:单质硫存在于火山口附近或 地壳的岩石 (2)化合态——硫化物和硫酸盐: 硫铁矿 FeS2 黄铜矿 CuFeS2 石膏 CaSO4.2H2O 芒硝 Na2SO4.10H2O (3)硫是一种生命元素,组成某些蛋白质时
不可离开它。因此化石燃料中经常含有硫元素。
SO2漂白原理:由于它能与某些有色物质 反应生成不稳定的无色物质。无色物质 容易分解而使有色物质恢复原来的颜色。 注意:可用品红溶液来检验SO2的存在
漂白性物质的对比
名称
二氧化硫
与某些有色物质直 接结合生成不稳定 的无色物质 非氧化还原反应 可逆 漂白某些有色物质,不 能使紫色石蕊试液褪色
氯 水(Na2O2 H2O2 O3、HClO)
将色素氧化 为稳定的无色物质 氧化还原反应 不可逆 漂白大多数有色物质, 能使紫色石蕊试液褪色
原理 实质 程度 范围
活性炭也有一定的漂白性,该物质的漂白原理?
SO2漂白性的应用
SO2常被用来漂白纸浆、草帽、衣物、毛、丝
不良商家用SO2漂白食物
SO2有毒,对人体的肝/肾脏有严重损害, 且有致癌作用。
总结SO2的化学性质
1、酸性氧化物 2、漂白性(并不能漂白所有物质) 检验SO2:品红溶液 3、SO2的氧化性和还原性 还原性:能使紫色的高锰酸钾溶液、氯水褪色 氧化性:能和氢硫酸反应产生黄色沉淀 (一般可用高锰酸钾溶液、氢氧化钠溶液来吸收 SO2)
思考:
1.SO2可以使品红溶液、氯水、高锰 酸钾溶液褪色,原理相同吗?
拓展与应用:
问题:报纸放久了为什么会发黄?
提示:从SO2漂白特
点的角度解释
二氧化硫除具有酸性氧化物的性质 外,还会有哪些性质?
一、硫元素的存在形式
(1)游离态:单质硫存在于火山口附近或 地壳的岩石 (2)化合态——硫化物和硫酸盐: 硫铁矿 FeS2 黄铜矿 CuFeS2 石膏 CaSO4.2H2O 芒硝 Na2SO4.10H2O (3)硫是一种生命元素,组成某些蛋白质时
不可离开它。因此化石燃料中经常含有硫元素。
SO2漂白原理:由于它能与某些有色物质 反应生成不稳定的无色物质。无色物质 容易分解而使有色物质恢复原来的颜色。 注意:可用品红溶液来检验SO2的存在
漂白性物质的对比
名称
二氧化硫
与某些有色物质直 接结合生成不稳定 的无色物质 非氧化还原反应 可逆 漂白某些有色物质,不 能使紫色石蕊试液褪色
氯 水(Na2O2 H2O2 O3、HClO)
将色素氧化 为稳定的无色物质 氧化还原反应 不可逆 漂白大多数有色物质, 能使紫色石蕊试液褪色
原理 实质 程度 范围
活性炭也有一定的漂白性,该物质的漂白原理?
SO2漂白性的应用
SO2常被用来漂白纸浆、草帽、衣物、毛、丝
不良商家用SO2漂白食物
SO2有毒,对人体的肝/肾脏有严重损害, 且有致癌作用。
总结SO2的化学性质
1、酸性氧化物 2、漂白性(并不能漂白所有物质) 检验SO2:品红溶液 3、SO2的氧化性和还原性 还原性:能使紫色的高锰酸钾溶液、氯水褪色 氧化性:能和氢硫酸反应产生黄色沉淀 (一般可用高锰酸钾溶液、氢氧化钠溶液来吸收 SO2)
思考:
1.SO2可以使品红溶液、氯水、高锰 酸钾溶液褪色,原理相同吗?
拓展与应用:
问题:报纸放久了为什么会发黄?
提示:从SO2漂白特
点的角度解释
二氧化硫除具有酸性氧化物的性质 外,还会有哪些性质?
必修一第四章第三节硫和氮的氧化物全优秀课件

氯水和二氧化硫漂白性的比较
氯水
原 理 氯物水质氧中氧化H化C成漂lO无将白色有物色质
实质
氧化还原反应
效果 范围
永久性
可漂白大多数有色物 质,能使紫色石蕊试 液先变红后褪色
二氧化硫
S质O直2化溶接于结合水合漂与生有白成色不物稳
定的无色物质
非氧化还原反应
暂时性 漂白某些有色物质,不 能使紫色石蕊试液褪色 (石蕊变红)
①澄清石灰水 ②H2S溶液
③KMnO4酸性溶液 ④氯水 ⑤品红溶液
A、①②③
B、②③④
C、除①以外
D、全部
二氧化硫
练习2、下列实验能证明一定有二氧化硫存在的是
⑤ __________________________
①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使品红溶液褪色 ④通入足量的氢氧化钠溶液,再加BaCl2溶液有白色沉淀 产生,该沉淀溶于稀盐酸 ⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色 沉淀产生
与水 反应
二氧化碳 CO2+H2O H2CO3
二氧化硫 SO2+H2O H2SO3
与碱 CO2+Ca(OH)2=CaCO3↓+H2O SO2+Ca(OH)2=CaSO3↓+H2O 反应 CO2+NaOH =Na2CO3+H2O SO2+NaOH =Na2SO3+H2O
与碱 性氧 化物 反应
高温
CO2+CaO==CaCO3
N2占空气体 积的4/5左 右,通常情 况下不与氧 气反应。
NO不溶于 水,常温下 易于氧气结 合生成NO2
放电或高温
N2 + O2 =======2NO
氯水
原 理 氯物水质氧中氧化H化C成漂lO无将白色有物色质
实质
氧化还原反应
效果 范围
永久性
可漂白大多数有色物 质,能使紫色石蕊试 液先变红后褪色
二氧化硫
S质O直2化溶接于结合水合漂与生有白成色不物稳
定的无色物质
非氧化还原反应
暂时性 漂白某些有色物质,不 能使紫色石蕊试液褪色 (石蕊变红)
①澄清石灰水 ②H2S溶液
③KMnO4酸性溶液 ④氯水 ⑤品红溶液
A、①②③
B、②③④
C、除①以外
D、全部
二氧化硫
练习2、下列实验能证明一定有二氧化硫存在的是
⑤ __________________________
①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使品红溶液褪色 ④通入足量的氢氧化钠溶液,再加BaCl2溶液有白色沉淀 产生,该沉淀溶于稀盐酸 ⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色 沉淀产生
与水 反应
二氧化碳 CO2+H2O H2CO3
二氧化硫 SO2+H2O H2SO3
与碱 CO2+Ca(OH)2=CaCO3↓+H2O SO2+Ca(OH)2=CaSO3↓+H2O 反应 CO2+NaOH =Na2CO3+H2O SO2+NaOH =Na2SO3+H2O
与碱 性氧 化物 反应
高温
CO2+CaO==CaCO3
N2占空气体 积的4/5左 右,通常情 况下不与氧 气反应。
NO不溶于 水,常温下 易于氧气结 合生成NO2
放电或高温
N2 + O2 =======2NO
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
N2O、NO、N2O3、NO2、N2O4、N2O5
氮元素最典型的氧化物
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
N2O、NO、N2O3、NO2、N2O4、N2O5
氮元素最典型的氧化物
氮的氧化物
氮元素的主要化合价
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
N2O、NO、N2O3、NO2、N2O4、N2O5
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 无色气体变为红棕 色气体,又变为无 色气体,但气体体 积逐渐缩小,液面 不断上升 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑
【科学视野】:火箭为什么能飞上天?
练习:一大试管充满NO2气体,将其倒
置于水中,1 min后液面停止变化,然
后向该试管中以 3 mL/min 的速度通入
O2,通入气体10min后液面恰好停留在
试管口。求试管的容积。
氮气与过量氧气在放电条件下的反应
NO2溶于水
(3) 往试管通入O2
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑ 无色气体变为红棕 色气体,又变为无 2NO+O2=2NO2 色气体,但气体体 3NO2+H2O = 积逐渐缩小,液面 2HNO3+NO 不断上升
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
雷雨发庄稼
科学探究
科学探究
现给你一试管二氧化氮,其他药品和仪 器自选。
科学探究
现给你一试管二氧化氮,其他药品和仪 器自选。 1、请你设计实验,要求尽可能多的NO2 被水吸收。画出装置图并填写下表。
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
农村有句谚语 “雷雨发庄稼”这是 由于在放电条件下, 空气中的氧气和氮气 相化合生成了氮的氧 化物,氮的氧化物再 经过复杂的化学变化 最后生成了易被农作 物吸收的硝酸盐。雷 雨施加了氮肥。
NO
NO2
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
N2O、NO、N2O3、NO2、N2O4、N2O5
氮元素最典型的氧化物
NO
NO2
氮元素的主要化合价
-3、-2、-1、0、+1、+2、+3、+4、+5
氮元素的氧化物
N2O、NO、N2O3、NO2、N2O4、N2O5
(3)
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气
(3)
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑
(3) 往试管通入O2
4 NO2 + 2H2O + O2 = 4HNO3
2. 你的设计对工业上生产硝酸有什么启示?
2. 你的设计对工业上生产硝酸有什么启示? ——工业生产硝酸,将尾气(NO)吸收 通入适量的氧气后再溶解于水,经过多次循环 氧化、溶解,可充分利用原料,并减少NO的排 放,保护环境。
科学探究
现给你一试管二氧化氮,其他药品和仪 器自选。 1、请你设计实验,要求尽可能多的NO2 被水吸收。画出装置图并填写下表。
实验步骤 (1)
(2)
现 象
解释(反应式)
(3)
科学探究
实验步骤 (1)
(2) (3)
现 象
解释(反应式)
科学探究
实验步骤
将充满NO2的试 (1) 管倒立在水槽 (2) (3)
(3)
科学探究
实验步ห้องสมุดไป่ตู้ 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑
(3) 往试管通入O2
科学探究
实验步骤 现 象 解释(反应式)
现 象
解释(反应式)
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 将充满NO2的试 (1) 试管水位上升到 管倒立在水槽 2/3处 (2)
(3)
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2)
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。 除了以上生理功能外,一氧化氮还在呼吸 系统、内分泌系统中起重要作用。
NO一向被视为大气污染物,却在生命过程中 有如此重要的功能,这是否能给人们一些什么 启示呢? ——世上没有绝对的有害物质
2. 你的设计对工业上生产硝酸有什么启示? ——工业生产硝酸,将尾气(NO)吸收 通入适量的氧气后再溶解于水,经过多次循环 氧化、溶解,可充分利用原料,并减少NO的排 放,保护环境。 4 NO + 2H2O + 3O2 = 4HNO3
2. 你的设计对工业上生产硝酸有什么启示? ——工业生产硝酸,将尾气(NO)吸收 通入适量的氧气后再溶解于水,经过多次循环 氧化、溶解,可充分利用原料,并减少NO的排 放,保护环境。 4 NO + 2H2O + 3O2 = 4HNO3
(3) 往试管通入O2
科学探究
实验步骤 现 象 解释(反应式)
红棕色逐渐消失, 3NO +H O = 将充满NO2的试 2 2 (1) 试管水位上升到 管倒立在水槽 2HNO3+NO 2/3处 (2) 制取少量氧气 2KClO3=2KCl+3O2↑ 或2H2O2=2H2O+O2↑ 无色气体变为红棕 色气体,又变为无 2NO+O2=2NO2 色气体,但气体体 3NO2+H2O = 积逐渐缩小,液面 2HNO3+NO 不断上升
科学视野:信使分子——NO
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。
科学视野:信使分子——NO 一氧化氮是一种神经信使分子,参与包括 学习、记忆在内的多种生理过程,并且具有调 节脑血流的作用。一氧化氮也是免疫系统对付 细菌、病毒、肿瘤细胞等病原体的有效武器。 除了以上生理功能外,一氧化氮还在呼吸 系统、内分泌系统中起重要作用。
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
Prize citation: "for their discoveries concerning nitric oxide as a signalling molecule in the cardiovascular system" 授奖致辞: “(表彰他们)关于一氧化氮在心血管组织中作为信 号分子的发现"
氮元素最典型的氧化物
NO
NO2
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
罗伯特· 佛契哥特/伊格纳罗 /慕拉德
Prize citation: "for their discoveries concerning nitric oxide as a signalling molecule in the cardiovascular system"
