碱性磷酸酶Km值的PPT课件
合集下载
碱性磷酸酶Km值的测定

精品课件
Vmax•[S] V=
Km + [S]
其中Km为米氏常数, Vmax为最大反应速度,
当V=Vmax/2时,则Km=[s]。 Km是酶的特征常数,测定Km是研究酶 的一种方法
精品课件
将米氏方程变形为双倒数方程,以l/ v-1/[s]作图,将各点连线,在横轴 截距为-/km,据此可算出Km值。
1/V=Km/ Vmax•[S] + 1/ Vmax
精品课件
本实验以碱性磷酸酶为例,用磷酸苯二钠为其 底物,生成酚和磷酸,酚在碱性溶液中与4一氨 基安替比林作用,经铁氰化钾氧化生成红色醌 的衍生物,根据红色的深浅可测出酶活力高低。 其反应式如下:
磷酸苯二钠+H2O 酚
AKP OH-
苯
苯酚+4-氨基安替比林 K3Fe(CN)6 醌衍生物
OD510
1/OD510
VMAX
1/2VMAX
Km
底物浓度与反应速度关系曲线
1/Vmax
[S]
-1/Km
双倒数曲线
1/[s]
精品课件
【实验讨论】
比较两个值的大小,分析实验误差产 生的原因
比较两种Km测定方法各自的优缺点
精品课件
6
78
12
16
0
1/[S] 1/OD
1 0.333 0.200 0.167 0.125 0.083 0.063 -
精品课件
2、作图
以 [s]为横轴,OD510为纵横作图,观 察曲线形状;查Km 值
以1/[s]为横轴,1/OD510为纵轴 作图,观察曲线形状;查Km 值
比较两个值的差异.
精品课件
碱性磷酸酶Km值的 测定
精品课件
Vmax•[S] V=
Km + [S]
其中Km为米氏常数, Vmax为最大反应速度,
当V=Vmax/2时,则Km=[s]。 Km是酶的特征常数,测定Km是研究酶 的一种方法
精品课件
将米氏方程变形为双倒数方程,以l/ v-1/[s]作图,将各点连线,在横轴 截距为-/km,据此可算出Km值。
1/V=Km/ Vmax•[S] + 1/ Vmax
精品课件
本实验以碱性磷酸酶为例,用磷酸苯二钠为其 底物,生成酚和磷酸,酚在碱性溶液中与4一氨 基安替比林作用,经铁氰化钾氧化生成红色醌 的衍生物,根据红色的深浅可测出酶活力高低。 其反应式如下:
磷酸苯二钠+H2O 酚
AKP OH-
苯
苯酚+4-氨基安替比林 K3Fe(CN)6 醌衍生物
OD510
1/OD510
VMAX
1/2VMAX
Km
底物浓度与反应速度关系曲线
1/Vmax
[S]
-1/Km
双倒数曲线
1/[s]
精品课件
【实验讨论】
比较两个值的大小,分析实验误差产 生的原因
比较两种Km测定方法各自的优缺点
精品课件
6
78
12
16
0
1/[S] 1/OD
1 0.333 0.200 0.167 0.125 0.083 0.063 -
精品课件
2、作图
以 [s]为横轴,OD510为纵横作图,观 察曲线形状;查Km 值
以1/[s]为横轴,1/OD510为纵轴 作图,观察曲线形状;查Km 值
比较两个值的差异.
精品课件
碱性磷酸酶Km值的 测定
精品课件
碱性磷酸酶Km值的 ppt课件

[S]:底物浓度 V:不同[S]时的反应初速度 Vmax:最大反应速度(maximum velocity) Km:米氏常数(Michaelis constant)
碱性磷酸酶Km值的
4
Km值 ① Km等于酶促反应速度为最大反应速度一半时 的底物浓度。 ② 意义: a) Km是酶的特征性常数之一; b) Km可近似表示酶对底物的亲和力; c) 同一酶对于不同底物有不同的Km值。
9:17:30 9:18:00
保证每个试管的反应时间为15分钟
碱性磷酸酶Km值的
8
实验报告
• 1 绘制矩形双曲线图
• 2 绘制双倒数图,并通过双倒数图读出碱 性磷酸酶对磷酸本二钠的Km值
碱性磷酸酶Km值的
9
7
注意事项
• 1 底物和酶取样准确 • 2 保温时间准确
1
2
3
4
5
加入酶的时 间
加入碱性溶液 终止反应的 时间
9:00:00 9:00:30 9:01:00 9:15:00 9:15:30 9:16:00
9:01:30 9:16:30
9:02:00 9:17:00
6
7
9:02:30 9:03:00
碱性磷酸酶Km值的测定
碱性磷酸酶Km值的
1
影响 酶促反应的因素
底物浓度 酶浓度 pH 温度 激活剂 抑制剂
※ 研究一种因素的影响时,其余各因素均恒定。
碱性磷酸酶Km值的
2
底物浓度对反应速率影响
在其他因素不变
V
的情况下,底物浓度
对反应速率的影响呈
矩形双曲线关系。 [S]
碱性磷酸酶Km值的
3
V ── = Vmax[S] Km + [S]
碱性磷酸酶Km值的
4
Km值 ① Km等于酶促反应速度为最大反应速度一半时 的底物浓度。 ② 意义: a) Km是酶的特征性常数之一; b) Km可近似表示酶对底物的亲和力; c) 同一酶对于不同底物有不同的Km值。
9:17:30 9:18:00
保证每个试管的反应时间为15分钟
碱性磷酸酶Km值的
8
实验报告
• 1 绘制矩形双曲线图
• 2 绘制双倒数图,并通过双倒数图读出碱 性磷酸酶对磷酸本二钠的Km值
碱性磷酸酶Km值的
9
7
注意事项
• 1 底物和酶取样准确 • 2 保温时间准确
1
2
3
4
5
加入酶的时 间
加入碱性溶液 终止反应的 时间
9:00:00 9:00:30 9:01:00 9:15:00 9:15:30 9:16:00
9:01:30 9:16:30
9:02:00 9:17:00
6
7
9:02:30 9:03:00
碱性磷酸酶Km值的测定
碱性磷酸酶Km值的
1
影响 酶促反应的因素
底物浓度 酶浓度 pH 温度 激活剂 抑制剂
※ 研究一种因素的影响时,其余各因素均恒定。
碱性磷酸酶Km值的
2
底物浓度对反应速率影响
在其他因素不变
V
的情况下,底物浓度
对反应速率的影响呈
矩形双曲线关系。 [S]
碱性磷酸酶Km值的
3
V ── = Vmax[S] Km + [S]
碱性磷酸酶Km值的ppt课件

精选课件
10
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
1
2
3
4
5
加入酶的时 间
加入碱性溶液 终止反应的 时间
9:00:00 9:00:30 9:01:00 9:15:00 9:15:30 9:16:00
9:01:30 9:16:30
9:02:00 9:17:00
6
7
9:02:30 9:03:00
9:17:30 9:18:00
保证每个试管的反应时间为15分钟
精选课件
8
实验报告
• 1 绘制矩形双曲线图
• 2 绘制双倒数图,并通过双倒数图读出碱 性磷酸酶对磷酸本二钠的Km值
精选课件
9
注意事项
• 1 做如下表格
1234 5 6 7 Abs [S] 1/ABS 1/[S]
• 2 可电脑作图
• 3 若人工作图,在坐标轴上禁止出现分数(1/2,1/16)
• 4 实验的最终目的是测得Km值,因此实验报告最终 必须得出结论:Km值等于多少
碱性磷酸酶Km值的测定
精选课件
1
影响 酶促反应的因素
底物浓度 酶浓度 pH 温度 激活剂 抑制剂
※ 研究一种因素的影响时,其余各因素均恒定。
精选课件
2
底物浓度对反应速率影响
在其他因素不变
V
的情况下,底物浓度
对反应速率的影响呈
矩形双曲线关系。 [S]
精选课件
3
V ── = Vmax[S] Km + [S]
精选课件
5
V Vmax Vmax/2
Km
❖ Km
Vmax = Vmax[S]
碱性磷酸酶Km值的测定

磷酸苯二钠磷酸苯二钠h2oakpohh2oakpoh苯酚苯酚苯酚苯酚44氨基安替比林氨基安替比林k3fecn6k3fecn6醌衍生物醌衍生物红色红色底物液004m碳酸缓液ph10蒸馏水005015025030040060080000090090090090090090090090095085075070060040020100混匀后37水浴预温5分钟左右010101010101010101010101010101013715演示文档内容演示文档内容碱性溶液10101010101010104氨基安铁氰化钾10101010101010102020202020202020混匀室温放置10分钟左右空白于5l0nm比色记录各管的光密度结果记录结果记录odod底物浓度mmoll1216033302000167012500830063od510od510kmkm11od510od510kmkm12vmaxod510maxkm底物浓度与反应速度关系曲线双倒数曲线1od5101km1vmax比较两个值的大小比较两个值的大小分析实验误差产生分析实验误差产生的原因的原因比较两种比较两种kmkm测定方法各自的优缺点测定方法各自的优缺点
4-氨基安 替比林
铁氰化钾
1.0 1.0 2.0 2.0
1.0 1.0 1.0 1.0 1.0 1.0 2.0 2.0 2.0 2.0 2.0 2.0
混匀,室温放置10分钟左右, 以8号管
为空白,于5l0nm比色,记录各管的光密 度
精品课件
【实验结果】
1、原始数据
结果记录 1 2 3 4
5
OD
底物浓度 1 3 5 6 8 mmol/L
精品课件
Vmax•[S] V=
Km + [S]
其中Km为米氏常数, Vmax为最大反应速度,
4-氨基安 替比林
铁氰化钾
1.0 1.0 2.0 2.0
1.0 1.0 1.0 1.0 1.0 1.0 2.0 2.0 2.0 2.0 2.0 2.0
混匀,室温放置10分钟左右, 以8号管
为空白,于5l0nm比色,记录各管的光密 度
精品课件
【实验结果】
1、原始数据
结果记录 1 2 3 4
5
OD
底物浓度 1 3 5 6 8 mmol/L
精品课件
Vmax•[S] V=
Km + [S]
其中Km为米氏常数, Vmax为最大反应速度,
实验碱性磷酸酶米氏常数的测定ppt课件

3.样品测试操作 ① 打开电源开关,使仪器预热20分钟 ② 用“波长设置”按钮将波长设置在您将要使用的分析波长位置上
③ 打开样品室盖,将挡光体插入比色皿架,并将其推或拉入光路
④ 盖好样品室盖,按“0%T”键调透射比零 ⑤ 取出挡光体,盖好样品室盖,按“100%T”调100%透射比 ⑥ 按“方式键”(MODE)将测试方式设置为吸光度方式(A) ⑦ 将参比溶液和被测溶液分别倒入比色皿中
测定Km和Vm,可通过作图法求得。 最常用的 Lineweaver-Burk双倒数作图法。这个方法是将米 氏方程转化为倒数形式,即:
1 Km 1 1 v Vm [S] Vm
以1/v对1/[S]作图,可得一条直线
1/v
1/Vm
-1/Km
1/[S]
本实验测定碱性磷酸酶催化对硝基苯磷酸钠盐(pNPP)
各管加入1.0 mL
20 mmol/L MgCl2 (mL) 各管加入0.2 mL
0.1 mol/L NaOH (mL) 各管加入2.0 mL
OD 405 nm
以对硝基苯酚的绝对量(mol数)为横坐标,OD405nm值为纵坐标, 绘制标准曲线。求出pNP的克分子消光系数()值。
(二)测定 15支试管,1-5做两组平行测定管,01-05作为空白对照。
器材:恒温水浴锅、722分光光度计
四、分光光度计的使用
1.722型分光光度计的外形
2.仪器操作键介绍 “方式设定”键(MODE):用于设置测 试方式
“100%T/0ABS”键:用于自动调整 100.0%T(100.0透射比)或0ABS(零吸光度)
“0%T”键:用于自动调整零透射比 “波长设置”旋钮:用于设置分析波长
酶液(mL )
碱性磷酸酶Km值的测定

1.0
1.0
1.0 1.0
1.0 1.0
1.0
1.0
4-氨基安 替比林
1.0 1.0
铁氰化钾
2.0 2.0
2.0Leabharlann 2.02.02.0 2.0
2.0
混匀,室温放置10分钟左右, 以8号管为 空白,于5l0nm比色,记录各管的光密度
【实验结果】
1、原始数据
结果记录 OD 1 2 3 4 5 6 7 8
底物浓度 mmol/L
【实验操作】
1 2 3 4 5 6 7 8 管号 底物液 0.05 0.15 0.25 0.30 0.40 0.60 0.80 0.00
(0.04M) 碳酸缓 液(pH=10)
0.90 0.90 0.95 0.85
0.90 0.90 0.75 0.70
0.90 0.60
0.90 0.90 0.40 0.20
Vmax•[S] + 1/ Vmax
本实验以碱性磷酸酶为例,用磷酸苯二钠为其 底物,生成酚和磷酸,酚在碱性溶液中与4一氨 基安替比林作用,经铁氰化钾氧化生成红色醌 的衍生物,根据红色的深浅可测出酶活力高低。 其反应式如下:
磷酸苯二钠+H2O AKP OH苯酚
苯酚+4-氨基安替比林 K3Fe(CN)6 醌衍生物 (红色)
Vmax•[S]
V=
Km + [S]
其中Km为米氏常数, Vmax为最大反应速度, 当V=Vmax/2时,则Km=[s]。 Km是酶的特征常数,测定Km是研究酶 的一种方法
将米氏方程变形为双倒数方程,以l/ v -1/[s]作图,将各点连线,在横轴截 距为-/km,据此可算出Km值。
碱性磷酸酶Km值的测定

6
78
12
16
0
1/[S] 1/OD
1 0.333 0.200 0.167 0.125 0.083 0.063 -
历史ⅱ岳麓版第13课交通与通讯 的变化资料
精品课件欢迎使用
[自读教材·填要点]
一、铁路,更多的铁路 1.地位 铁路是 交通建运设输的重点,便于国计民生,成为国民经济 发展的动脉。 2.出现 1881年,中国自建的第一条铁路——唐山 至开胥平各庄铁 路建成通车。 1888年,宫廷专用铁路落成。
本实验以碱性磷酸酶为例,用磷酸苯二钠为其底物,生成酚和 磷酸,酚在碱性溶液中与4一氨基安替比林作用,经铁氰化钾氧 化生成红色醌的衍生物,根据红色的深浅可测出酶活力高低。 其反应式如下:
磷酸苯二钠+H2O
AKP OH-
苯酚
苯酚+4-氨基安替比林 K3Fe(CN)6 醌衍生物 (红色)
【实验操作】
出口价格同步变动的现象。与这一现象直接相关的近代事
业是
()
A.电报业
B.大众报业
C.铁路交通业 D.轮船航运业
[解析] 材料主要反映了信息交流的快捷,故选A。
[答案] A
[题组冲关]
3.假如某爱国实业家在20世纪初需要了解全国各地商业信
息,可采用的最快捷的方式是
()
A.乘坐飞机赴各地了解 B.通过无线电报输送讯息
C.通过互联网 D.乘坐火车赴各地了解
解析:本题考查中国近代物质生活的变迁。注意题干信
息“20世纪初”“最快捷的方式”,因此应选B,火车速度 远不及电报快。20世纪30年代民航飞机才在中国出现, 互联网出现在20世纪90年代。 答案:B
4.下列不属于通讯工具变迁和电讯事业发展影响的是( ) A.信息传递快捷简便 B.改变着人们的思想观念 C.阻碍了人们的感情交流 D.影响着人们的社会生活 解析:新式通讯工具方便快捷,便于人们感情的沟通和交流。 答案:C
酶促反应动力学 碱性磷酸酶Km值测定26页PPT

可逆性抑 制作用
抑制剂通常以非 共价键与酶或酶 -底物复合物可 逆性结合,使酶 活性降低或消失 。
可逆性抑制作用
竞竞争争性 性
Km增大
非非争性竞竞性争
Vmax降低
反反竞竞争 争性 性
Km, Vmax降低
底物浓度对酶促反应速度的影响
低
反应速度和底物浓 度成正比关系
反应速度增幅下降
高
底物浓度
的增高
酶活性中心被底物饱和
米氏常数的求法
1
V
=
Km Vmax
×
1 [S]
+
1
Vmax
V表示酶促反应速度 Vmax表示酶促反应最大速度
[S]表示底物浓度
Km表示米氏常数
双倒数作图法
底物浓度对酶活性 的影响
——碱性磷酸酶Km个相当重要的 常数,通过实验,可理解并掌握利用实验求出 Km的方法。
实验原理
磷酸苯二钠
H2O
碱性磷酸酶
酚 Na2HPO4
pH=10.0,
37℃ OH-(磷酚钼试钨剂酸)
650nm 蓝色化合物
吸光度表示不同底物浓度时的酶反应速度。以吸 光度的倒数作纵坐标,以底物浓度的倒数作横坐 标,按Lineweaver-Burk作图法求出Km值。
试剂
1.酚试剂 2.2.5mmol/L磷酸苯二钠基质液 3.碱性缓冲液(pH-10.0) 4.碱性磷酸酶液
混匀后,37℃水浴15min,以第8管调节零点,
在650nm波长处进行比色,读取各管A值。
处理结果
管号 1 2 3 4 5 6 7
A650
1/A650 [S]
1/[S]
以1/A650对1/[s]按Lineweaver-Burk作图法作
碱性磷酸酶Km值的测定..

本实验旨在测定碱性磷酸酶的Km值,以了解酶的特性和底物亲和力。实验原理基于米氏方程,通过在不同底物浓ห้องสมุดไป่ตู้下测定酶促反应速度,进而利用双倒数方程求解Km值。实验中使用了磷酸苯二钠作为底物,通过其与碱性磷酸酶反应生成的酚类物质,再与4-氨基安替比林反应形成红色醌衍生物,从而根据颜色深浅测定酶活性。实验准备了包括底物液、碳酸盐缓冲液、碱性磷酸酶溶液等试剂,并严格按照操作步骤进行。在反应过程中,保持恒定的温度、pH值和酶浓度,以确保实验结果的准确性。通过记录不同底物浓度下的光密度值,并绘制双倒数曲线,最终求解出碱性磷酸酶的Km值。实验结果不仅反映了酶与底物的亲和力,也为进一步研究酶的动力学特性提供了重要数据。
酶促反应动力学 碱性磷酸酶Km值测定

研究前提
单底物、单产物反应
酶促反应速率一般在规定反应条 件下,用单位时间内底物的消耗 量或产物的生成量来表示。 反应速率取其初速率,即底物的消
耗量很小(≤5%)时的反应速率。
底物浓度远远大于酶浓度。
矩形双曲线
米-曼氏方程式
Km 即为米氏常数, Vmax为最大反应速度
当反应速度等于最大速度
操作
取8支试管,按下表加入试剂。
试剂(ml)
12345678
2.5mM磷酸苯二钠 0.2 0.3 0.4 0.5 0.6 0.8 1.0 1.0
蒸馏水
0.8 0.7 0.6 0.5 0.4 0.2 - -
碱性缓冲液
1.0 1.0 1.0 1.0 1.0 1.0 1.0 1.0
混匀后,370C水浴 5 min
一半时,即V = 1/2 Vmax, Km = [S]
上式表示,米氏常数是反应 速度为最大值的一半时的底 物浓度。
因此,米氏常数的单位为 mol/L。
米氏常数Km的意义
不同的酶具有不同Km值,它是酶的一个重
要的特征物理常数。
Km值只是在固定的底物,一定的温度和
pH条件下,一定的缓冲体系中测定的,不
在最适温度条件下, 反应速度最大。
pH 对反应速度的影响
在一定的pH 下, 酶具有最大的催化活性,通常称 此pH 为最适 pH。
激活剂对反应速度的影响
酶的激活剂
必需激活剂,
大多为金属离 子,Mg2+,K+ ,Mn2+,等
非必需激 活剂
抑制剂对反应速度的影响
不可逆性 抑制作用
抑制剂通常以共 价键与酶活性中 心或活性中心以 外的必需基团相 结合,使酶失活 。
米氏常数的求法
碱性磷酸酶Km值测定

V Vmax
[S]
Km值的推导
当反应速度为最大反应速度一半时 V
Vmax
Vmax/2 Km [S]
Vmax 2
Vmax[S] = Km + [S] Km=[S]
∴Km值等于酶促反应速度为最大反应速度一半 时的底物浓度,单位是mol/L。
双倒数作图法(double reciprocal plot),又称为 林-贝氏(LineweaverBurk)作图法
Байду номын сангаас 三、操作方法
参见实验讲义
四、思考题
1.测定Km值还有哪些方法? 2.测定Km值有何实际意义?
V= Vmax[S]
Km+[S]
两边同取倒数
Km 1/V= + 1/Vmax 1/[S] Vmax (林-贝氏方程)
本实验以碱性磷酸酶为样品: 碱性磷酸酶能分解磷酸苯二钠产生酚和磷 酸,酚在碱性溶液中与4-氨基安替比林作 用,经铁氰化钾氧化生成红色的醌衍生物, 根据红色的深浅可测出酶活力的高低,测 定不同浓度底物时的酶活性。
碱性磷酸酶能分解磷酸苯二钠产生酚和磷酸酚在碱性溶液中与4氨基安替比林作用经铁氰化钾氧化生成红色的醌衍生物根据红色的深浅可测出酶活力的高低测定不同浓度底物时的酶活性
碱性磷酸酶Km值测定
一、实验目的
1.了解底物浓度对酶促反应速度的影响
2.了解米孟方程、Km值的物理意义及双 倒数作图求Km的方法。
二、实验原理
[S]
Km值的推导
当反应速度为最大反应速度一半时 V
Vmax
Vmax/2 Km [S]
Vmax 2
Vmax[S] = Km + [S] Km=[S]
∴Km值等于酶促反应速度为最大反应速度一半 时的底物浓度,单位是mol/L。
双倒数作图法(double reciprocal plot),又称为 林-贝氏(LineweaverBurk)作图法
Байду номын сангаас 三、操作方法
参见实验讲义
四、思考题
1.测定Km值还有哪些方法? 2.测定Km值有何实际意义?
V= Vmax[S]
Km+[S]
两边同取倒数
Km 1/V= + 1/Vmax 1/[S] Vmax (林-贝氏方程)
本实验以碱性磷酸酶为样品: 碱性磷酸酶能分解磷酸苯二钠产生酚和磷 酸,酚在碱性溶液中与4-氨基安替比林作 用,经铁氰化钾氧化生成红色的醌衍生物, 根据红色的深浅可测出酶活力的高低,测 定不同浓度底物时的酶活性。
碱性磷酸酶能分解磷酸苯二钠产生酚和磷酸酚在碱性溶液中与4氨基安替比林作用经铁氰化钾氧化生成红色的醌衍生物根据红色的深浅可测出酶活力的高低测定不同浓度底物时的酶活性
碱性磷酸酶Km值测定
一、实验目的
1.了解底物浓度对酶促反应速度的影响
2.了解米孟方程、Km值的物理意义及双 倒数作图求Km的方法。
二、实验原理
酶促反应动力学 碱性磷酸酶Km值测定

米氏常数Km:描述酶与 底物亲和力的常数
底物浓度与反应速率的关 系:底物浓度越高反应速 率越快
酶浓度与反应速率的关系: 酶浓度越高反应速率越快
温度与反应速率的关系: 温度越高反应速率越快
pH值与反应速率的关系: pH值影响酶的活性从而 影响反应速率
Km值的含义与计算方法
Km值:酶促反应中酶的活性与底物浓度的比值表示酶与底物的亲和力 计算方法:通过酶促反应速率与底物浓度的关系曲线利用米氏方程计算得出 Km值的意义:反映酶与底物的亲和力是酶学研究中的重要参数 Km值的应用:在药物设计、酶工程等领域具有重要应用价值
• 实验目的:测定碱性磷酸酶的Km值
• 实验原理:通过酶促反应动力学原理测定酶的活性和底物浓度的关系
• 实验步骤: . 准备实验材料:酶、底物、缓冲液等 b. 设定反应条件:温度、pH值、反应时间等 c. 测定酶活性:通 过酶促反应速率测定酶活性 d. 测定底物浓度:通过酶促反应速率测定底物浓度 e. 计算Km值:通过酶促反应速率和 底物浓度的关系计算Km值
配制反应溶液:按照实 验要求配制反应溶液包 括酶促反应试剂、碱性
磷酸酶、缓冲液等
加入底物:在反应容器 中加入底物并记录底物
浓度
加入酶促反应试剂:在 反应容器中加入酶促反 应试剂并记录酶促反应
试剂浓度
反应开始:在反应容器 中加入碱性磷酸酶并记
录碱性磷酸酶浓度
反应结束:反应进行一 段时间后记录反应时间、
06
实验结论与展望
实验结论总结
实验结果表明碱性 磷酸酶Km值与酶 促反应动力学密切 相关
实验数据表明碱性 磷酸酶Km值在不 同条件下的变化规 律
实验结果对于理解 酶促反应动力学具 有重要意义
Km值测定
V Vmax Vmax/2 Km
因为实验条件下,底物 浓度很难使酶达到饱和,
实测Vmax 是个近似值,
因而Vmax/2 不精确。此 外 的关系呈双曲线,实验数
据要求较多,且不易绘制。
[S]
故此法少用。
②双倒数作图法(double reciprocal plot),又称 为 林-贝氏(Lineweaver- Burk)作图法
0.8 0.8 0.8 0.8 0.8 0.8 0.8
1.1 1.05 1.0 0.9 0.7 0.5 0.3 0.1
混匀置入37 ℃ 保温 5 分钟
0.1
0.1
0.1 0.1 0.1 0.1 0.1 0.1
混匀并立即计算时间,在37 ℃ 保温 15 分钟,15分钟后即加碱性 溶液终止反应 (从第7管开始)
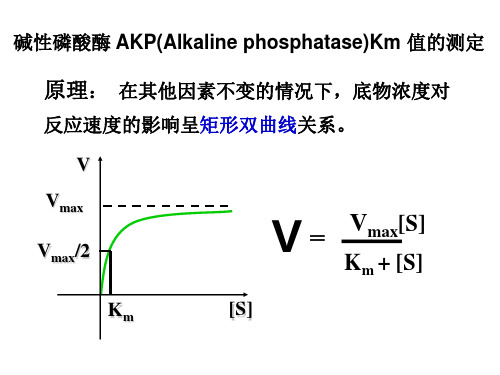
碱性磷酸酶 AKP(Alkaline phosphatase)Km 值的测定
原理: 在其他因素不变的情况下,底物浓度对
反应速度的影响呈矩形双曲线关系。 V Vmax Vmax/2 Km
V= ── K + [S]
m
Vmax[S]
[S]
① 双曲线作图法: 即根据米-曼氏方程,以v 对[s]作图,Vmax/2 时 [s]即为Km,以摩尔浓度表示。
碱性
K2Fe(CN)6
红色醌衍生物 颜色深浅与酚含量成正比,从而可知酶活性的高低。以底物浓度
的倒数为横坐标,以各管光密度的倒数为纵坐标作图求出Km值。
试剂(mL) 0.02 mol/L基质液
碳酸盐缓冲液 蒸馏水 血清
0 0
0.8
1 2 3 4 5 6 7 0.05 0.1 0.2 0.4 0.6 0.8 1.0
碱性溶液 4-氨基安替比林 铁氰化钾
因为实验条件下,底物 浓度很难使酶达到饱和,
实测Vmax 是个近似值,
因而Vmax/2 不精确。此 外 的关系呈双曲线,实验数
据要求较多,且不易绘制。
[S]
故此法少用。
②双倒数作图法(double reciprocal plot),又称 为 林-贝氏(Lineweaver- Burk)作图法
0.8 0.8 0.8 0.8 0.8 0.8 0.8
1.1 1.05 1.0 0.9 0.7 0.5 0.3 0.1
混匀置入37 ℃ 保温 5 分钟
0.1
0.1
0.1 0.1 0.1 0.1 0.1 0.1
混匀并立即计算时间,在37 ℃ 保温 15 分钟,15分钟后即加碱性 溶液终止反应 (从第7管开始)
碱性磷酸酶 AKP(Alkaline phosphatase)Km 值的测定
原理: 在其他因素不变的情况下,底物浓度对
反应速度的影响呈矩形双曲线关系。 V Vmax Vmax/2 Km
V= ── K + [S]
m
Vmax[S]
[S]
① 双曲线作图法: 即根据米-曼氏方程,以v 对[s]作图,Vmax/2 时 [s]即为Km,以摩尔浓度表示。
碱性
K2Fe(CN)6
红色醌衍生物 颜色深浅与酚含量成正比,从而可知酶活性的高低。以底物浓度
的倒数为横坐标,以各管光密度的倒数为纵坐标作图求出Km值。
试剂(mL) 0.02 mol/L基质液
碳酸盐缓冲液 蒸馏水 血清
0 0
0.8
1 2 3 4 5 6 7 0.05 0.1 0.2 0.4 0.6 0.8 1.0
碱性溶液 4-氨基安替比林 铁氰化钾
碱性磷酸酶km值测定

碱性磷酸酶km值测定实验旨在探究酶促反应动力学,特别是环境因素对酶促反应速度的影响,并通过实验测定碱性磷酸酶的km值。实验基于米氏方程式,该方程式描述了酶促反应速度与底物浓度的关系,其中Km值等于酶促反应速度为最大反应速度一半时的底物浓度,是酶的特征性常数之一,可近似表示酶对底物的亲和力。实验中采用双倒数作图法或Hanes作图法测定Km与Vห้องสมุดไป่ตู้ax值。此外,还探讨了酶浓度、温度、pH等环境因素对酶促反应速度的影响。在操作过程中,通过配制不同浓度的底物溶液,加入碱性磷酸酶进行反应,并测定反应速度,最终得到碱性磷酸酶的km值。实验结果有助于深入理解酶促反应动力学原理,并为酶的应用和研究提供重要参考。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4
Km值 ① Km等于酶促反应速度为最大反应速度一半时 的底物浓度。 ② 意义: a) Km是酶的特征性常数之一; b) Km可近似表示酶对底物的亲和力; c) 同一酶对于不同底物有不同的Km值。
5
V Vmax Vmax/2
Km
❖ Km
Vmax = Vmax[S]
2
Km + [S]
[S]
Km=[S]
• 2 可电脑作图 • 3 若人工作图,在坐标轴上禁止出现分数(1/2,1/16) • 4 实验的最终目的是测得Km值,因此实验报告最终
必须得出结论:Km值等于多少
10
6
Km值与Vmax值的测定
双倒数作图法
Vmax[S] V = Km+[S]
两边同取倒数
1/V=
Km Vmax
1/[S] + 1/Vmax
(林-贝氏方程)
7
注意事项
• 1 底物和酶取样准确 • 2 保温时间准确
123ຫໍສະໝຸດ 45加入酶的时 间
加入碱性溶液 终止反应的 时间
9:00:00 9:00:30 9:01:00 9:15:00 9:15:30 9:16:00
9:01:30 9:16:30
9:02:00 9:17:00
6
7
9:02:30 9:03:00
9:17:30 9:18:00
保证每个试管的反应时间为15分钟
8
实验报告
• 1 绘制矩形双曲线图 • 2 绘制双倒数图,并通过双倒数图读出碱
性磷酸酶对磷酸本二钠的Km值
9
注意事项
• 1 做如下表格
1234 5 6 7 Abs [S] 1/ABS 1/[S]
碱性磷酸酶Km值的测定
1
影响 酶促反应的因素
底物浓度 酶浓度 pH 温度 激活剂 抑制剂
※ 研究一种因素的影响时,其余各因素均恒定。
2
底物浓度对反应速率影响
在其他因素不变
V
的情况下,底物浓度
对反应速率的影响呈
矩形双曲线关系。 [S]
3
V ── = Vmax[S] Km + [S]
[S]:底物浓度 V:不同[S]时的反应初速度 Vmax:最大反应速度(maximum velocity) Km:米氏常数(Michaelis constant)
Km值 ① Km等于酶促反应速度为最大反应速度一半时 的底物浓度。 ② 意义: a) Km是酶的特征性常数之一; b) Km可近似表示酶对底物的亲和力; c) 同一酶对于不同底物有不同的Km值。
5
V Vmax Vmax/2
Km
❖ Km
Vmax = Vmax[S]
2
Km + [S]
[S]
Km=[S]
• 2 可电脑作图 • 3 若人工作图,在坐标轴上禁止出现分数(1/2,1/16) • 4 实验的最终目的是测得Km值,因此实验报告最终
必须得出结论:Km值等于多少
10
6
Km值与Vmax值的测定
双倒数作图法
Vmax[S] V = Km+[S]
两边同取倒数
1/V=
Km Vmax
1/[S] + 1/Vmax
(林-贝氏方程)
7
注意事项
• 1 底物和酶取样准确 • 2 保温时间准确
123ຫໍສະໝຸດ 45加入酶的时 间
加入碱性溶液 终止反应的 时间
9:00:00 9:00:30 9:01:00 9:15:00 9:15:30 9:16:00
9:01:30 9:16:30
9:02:00 9:17:00
6
7
9:02:30 9:03:00
9:17:30 9:18:00
保证每个试管的反应时间为15分钟
8
实验报告
• 1 绘制矩形双曲线图 • 2 绘制双倒数图,并通过双倒数图读出碱
性磷酸酶对磷酸本二钠的Km值
9
注意事项
• 1 做如下表格
1234 5 6 7 Abs [S] 1/ABS 1/[S]
碱性磷酸酶Km值的测定
1
影响 酶促反应的因素
底物浓度 酶浓度 pH 温度 激活剂 抑制剂
※ 研究一种因素的影响时,其余各因素均恒定。
2
底物浓度对反应速率影响
在其他因素不变
V
的情况下,底物浓度
对反应速率的影响呈
矩形双曲线关系。 [S]
3
V ── = Vmax[S] Km + [S]
[S]:底物浓度 V:不同[S]时的反应初速度 Vmax:最大反应速度(maximum velocity) Km:米氏常数(Michaelis constant)
