高一化学金属的通性(201909)
高一第三章1节金属的化学通性

二、金属的化学通性 1、与非金属(Cl2、O2、Br2、I2、S)的反应 Na→NaCl Na2O Na2O2 NaI Na2S Mg →MgO MgCl2 MgBr2 MgS Al → AlCl3 Al2O3 Fe→ FeCl3 Cu → Cu Cl2 Al2S3 FeI2 FeS Cu2S Fe 3O4
CuO CuI
Na与氧气的反应 4Na+O2=2Na2O 2Na+O2=Na2O2 常温 加热 演示实验
现象:先熔化成小球,后燃烧产生黄色火焰, 现象:先熔化成小球,后燃烧产生黄色火焰, 生成淡黄色固体 2Na2O+O2=2Na2O2 Al与氧气的反应 4Al+3O2=2Al2O3 演示实验
2、金属与水的反应 2Na + 2H2O = 2NaOH + H2↑ Mg+ 2H2O (沸水)= Mg (OH)
第三章
第一节
金属及其化合物
金属的化学性质
一、金属的物理通性
1、金属在自然界的分布 除金、铂等少数极不活泼金属外, 除金、铂等少数极不活泼金属外,大多数金 属元素在自然界中以化合态存在; 属元素在自然界中以化合态存在;地壳中含量 最多的是铝,其次是铁、 最多的是铝,其次是铁、钙、钠。 2、金属的分类 黑色金属( Fe、 Cr、 Mn)、 )、有色金属 黑色金属(铁Fe、铬Cr、锰Mn)、有色金属 重金属( 轻金属( 重金属(ρ>4.5g/cm3)、轻金属(ρ<4.5g/cm3) 常见金属、 常见金属、稀有金属
5、铝与酸、碱的反应 2Al+6HCl=2AlCl3+3H2↑ 2Al+6H+=Al3++3H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 2Al+2OH-+2H2O=2AlO2-+3H2↑ 铝与碱反应的氧化还原反应的分析 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 氧化剂:H2O 还原剂:Al
金属的通性

金属的通性:导电、导热性,具有金属光泽,延展性,一般情况下除Hg外都是固态12、金属冶炼的一般原理:①热分解法:适用于不活泼金属,如Hg、Ag②热还原法:适用于较活泼金属,如Fe、Sn、Pb等③电解法:适用于活泼金属,如K、Na、Al等(K、Ca、Na、Mg都是电解氯化物,Al 是电解Al2O3)13、铝及其化合物Ⅰ、铝①物理性质:银白色,较软的固体,导电、导热,延展性②化学性质:Al—3e-==Al3+a、与非金属:4Al+3O2==2Al2O3,2Al+3S==Al2S3,2Al+3Cl2==2AlCl3b、与酸:2Al+6HCl==2AlCl3+3H2↑,2Al+3H2SO4==Al2(SO4)3+3H2↑常温常压下,铝遇浓硫酸或浓硝酸会发生钝化,所以可用铝制容器盛装浓硫酸或浓硝酸c、与强碱:2Al+2NaOH+2H2O==2NaAlO2(偏铝酸钠)+3H2↑ (2Al+2OH-+2H2O==2AlO2-+3H2↑)大多数金属不与碱反应,但铝却可以d、铝热反应:2Al+Fe2O3===2Fe+Al2O3,铝具有较强的还原性,可以还原一些金属氧化物Ⅱ、铝的化合物①Al2O3(典型的两性氧化物)a、与酸:Al2O3+6H+==2Al3++3H2Ob、与碱:Al2O3+2OH-==2AlO2-+H2O②Al(OH)3(典型的两性氢氧化物):白色不溶于水的胶状物质,具有吸附作用a、实验室制备:AlCl3+3NH3•H2O==Al(OH)3↓+3NH4Cl,Al3++3NH3•H2O==Al(OH)3↓+3NH4+b、与酸、碱反应:与酸 Al(OH)3+3H+==Al3++3H2O 与碱 Al(OH)3+OH-==AlO2-+2H2O③KAl(SO4)2(硫酸铝钾)KAl(SO4)2•12H2O,十二水和硫酸铝钾,俗名:明矾KAl(SO4)2==K++Al3++2SO42-,Al3+会水解:Al3++3H2O Al(OH)3+3H+ 因为Al(OH)3具有很强的吸附型,所以明矾可以做净水剂14、铁①物理性质:银白色光泽,密度大,熔沸点高,延展性,导电导热性较好,能被磁铁吸引。
高一化学金属的通性
我问母亲:“你为么子笑得这么开心?”
母亲说:“笑一笑,老来俏。”
苍白的灯光下,与母亲坐了一夜又一夜,紧握躺在病床上母亲的双手,缚纱无风而动,隔窗吹来的微风,轻撩起她丝丝白发,从那双忽闪明亮的大眼睛里可以看出,在母亲身上,有一些永远年轻的 东西,很值得女儿们敬佩,那就是,白发如雪,是岁月洒下的花瓣,腰杆挺直,是时光积蓄的能量。如今,在与病魔抗争的母亲,望着自己心爱的女儿们,低声呢喃着:
“丫头们呀!来医院治疗,快一个月了吧!感觉时间好快,CT的结果医生说是肺炎,可我知道像我这样的病例,肺已经都纤维化了,目前国内还没有最好的医疗方案,好的几率几乎为零,这也许是 我陪伴你们最后之日了。”
ቤተ መጻሕፍቲ ባይዱ
手机传来工作群的响声,我匆匆赶到楼上,处理工作上的事情。阳光热了起来,羽绒服穿不住,我换上了运动衣。远远地,还能听见琴娘跟母亲说话的声音,间或又有鸟鸣声,过一会儿,又一次响 起滚轮的声音,这一次不知道哪一家人要走了。pc蛋蛋下载手机版 我没有起身再看。离别的场景,终究还是让我难过。渐渐地,人会越来越少,垸里会越来越安静。到时候,又只会剩下父母亲、婶娘们、叔爷们,再一想到这么多人或许此生只能经历这一次如此长 时间的团聚,心里莫名地惆怅起来。
高一化学金属的通性
军嫂是个特殊群体。尤其是在东风航天城这个偏远封闭的地方,她们的到来,对于稳定军心、丰富小社会生活具有非同寻常的意义。在这个没有社会依托的军事禁区,因为她们到来而鲜花盛开,因 为有了她们而硕果累累。整天奋斗在戈壁点号的科技人员,因为“遇到爱”、迎来爱而更加专心致志于本职工作。那一次次烈焰升腾的火箭发射,多像官兵们辛勤浇灌出来饱含着爱的花朵!
我频频点头。其实不问她们也知道这些军嫂们到单位来的意义。正像之前随调北京的小姚给我讲的,随军来一时没有岗位,天天在家带娃娃,休息天随爱人到老乡朋友家或单位上去转转,被“嫂 子嫂子”喊着慢慢连自己名字都忘了。她们为爱而来,现在又为爱而走到平凡的岗位上,为的不是钱,而是有一个能够展示自己、能够溶入集体、增进交流的地方。
我惊奇:遇到爱,还有这么个花名啊!既而明白:遇到爱,不正是她们这些小军嫂们心情心景的写照吗!pc蛋蛋下载手机版
小王微信里那束花在大家的讨论中摇曳开来,我的眼前浮现出一个个花儿样的人儿……
先说小王,高个儿大眼睛,郑州大学毕业,随军前从郑州去深圳某证券公司从事股票交易工作,收入不菲。被选拔到单位公益岗当讲解员时,开始月薪不到一千。如此反差,她怎么想的?她的中校 爱人陪同来单位办事,我开玩笑地说:让他养着就行,在家带带孩子,没事逛逛街,何必拿那么几个钱受人管束?她望了爱人一眼也玩笑于我:他不养我啊!我得把饭钱挣回来。她爽朗地笑,像一股春 风吹拂着所有人。我看向她的小爱人,小爱人脸红着说:哪里哪里,她在家待不住,非说要找个平台展示展示自己。
金属的通性

金属的通性(物理性质):①绝大多数金属都是固体(除汞外);②绝大多数金属具有银白色金属光泽(Cu红色、Au金黄色);③绝大多数金属具有良好的导电导热性;④绝大多数金属具有良好的延展性。
金属单质的性质:1.与非金属反应4 Na + O2=2 Na2O(白色) 2 Na + O2=Na2O2(淡黄色)2 Na + S =Na2S (爆炸性化合) 2 Na + Cl2=2 NaCl (白烟)3 Fe + 2 O2=Fe3O42.与水或酸反应2 Na + 2 H2O =2 NaOH + H2↑浮:浮在水面上,说明钠的密度比水小。
熔:熔成光亮小球,说明钠的熔点低。
响:有嘶嘶的响声,说明反应放出的热量使生成的气体点燃发出爆鸣声。
游:在水面上游来游去,说明有气体生成。
红:反应后加有酚酞的溶液变红,说明反应有碱性物质生成。
3 Fe +4 H2O(g) = Fe3O4 + H22 Na + 2 HCl =2 NaCl + H2↑2 Fe + 2 HCl =FeCl2 + H2 ↑2 Al + 6 HCl =2 AlCl3 + 3 H2 ↑两性元素的性质:1.两性金属单质2 Al + 6 HCl =2 AlCl3 + 3 H2 ↑2 Al + 2 NaOH + 2 H2O = 2 NaAlO2 +3 H2↑相同量的铝和足量的酸或强碱反应放出的气体的量相同2.两性氧化物Al2O3 + 6 HCl = 2 AlCl3 + 3 H2OAl2O3 + 2 NaOH = 2 NaAlO2 + H2O (只溶于强碱)3.两性氢氧化物Al(OH)3 + 3 HCl = AlCl3 + 3 H2OAl(OH)3 + NaOH = NaAlO2 + 2H2O (只溶于强碱)(1)Al(OH)3的制备:用弱碱溶液氨水来制备(2)往氯化铝溶液中滴加少量的氢氧化钠溶液:AlCl3 + 3 NaOH = Al(OH)3 + 3 NaCl 往氯化铝溶液中滴加过量的氢氧化钠溶液:AlCl3 + 4 NaOH = NaAlO2 + 3 NaCl + 2 H2O 钠化合物的性质:1.Na2O和Na2O22 Na2O2 + 2 H2O = 4 NaOH + O2↑Na2O + H2O = 2 NaOH2 Na2O2 + 2 CO2 = 2 Na2CO3 + O2↑Na2O + CO2 = Na2CO3Na2O2和H2O(或CO2)反应中只有Na2O2中的O化合价变化,既降到-1又升高到0价,在这两个反应中Na2O2既是氧化剂又是还原剂。
化学金属的通性

3、化学性质: 易失电子,表现还原性。 金属化学性质通性及递变规律:
最外层电 相 子数较少 同 点 原子半径
较大
都具有 还原性
与非金属单 共 质(O2 S X2) 性 与H+(水 酸)
盐溶液
金 属 元
原 子 结 构
素
不 同 点
金 核电荷数不同 属
活 泼
性
原子半径不同 不
同
与其它氧化剂
1.与水或酸 反应的难易 差 2.氢氧化物 异 碱性强弱 性 3. 置换反应
Fe3O4
④盐的通性: 1、盐 + 碱 = 新盐 + 新碱
(要生成更难溶或更难电离的物质)
2、盐 + 盐 = 两种新盐 (要生成更难溶的物质)
3、盐+较活泼金属=新盐+较不活泼金属 4、盐+酸 = 新盐+ 新酸
(要生成沉淀、气体或难电离物质) 5、酸式盐+碱=正盐+水
单质
金属元素的主线
氧化物
氢氧化物
相应的盐
Na ー Na2O ー NaOH ー Na+
Na2O2
Na2CO3 NaHCO3
Al ー Al2O3 ー Al(OH)3 ー Al3+ AlO2-
Fe ー FeO ー Fe2O3 ー Fe3O4
Fe(OH)2 — Fe2+ Fe(OH)3 ー Fe3+
单质
金属元素及其化合物
一、金属的概述
1、金属的物理性质: 常温下,除汞以外,其余金属都是固体。 有金属光泽,不透明,有导电性、有导热性、 有延展性。
Байду номын сангаас
2、金属的分类:
从密度分:轻金属(d<4.5g/cm3) >, 重金属(d > 4.5g/cm3)。
金属的通性

一、金属
1、 金属晶体的特点:金属晶体是由金 属阳离子和自由电子组成,其中自由电子 并不属于某个固定的金属阳离子,而可以 在整个金属中自由移动。
2、金属的特点 ①常温下,单质都是固体,汞(Hg)除外;
②大多数金属呈银白色,有金属光泽,但
金(Au)—黄—色,铜(Cu)—红—色,铋(Bi)—微—红 色, 铅(Pb)—蓝— 白色。
——部,分别分布在除——族、——族以外的各 主、副族中。
金属原子最外层电子数大部分小于——, 但是等于4的有—————5的有————,6的 有——————。
讨论:根据元素周期表知识,讨论金属 原子易失去电子的原因。
1、原子半径大,2、最外层电子少。
有色金属:除以上三种金属以外 按密度: 轻金属gt;4.5g/cm3 Zn Cu
常见金属: Fe Mg Al 按含量
稀有金属: 锆、钒、钼 、根—轻—据—以、上——分常—类—见—:—金金属属镁、铝属于—有——色—
金属的共性
4、金属元素在周期表中的位置 金属元素分布在周期表中的——、——方和
③不同金属熔沸点,硬度差别较大; ④良好的导电性,分析原因: 金属中存在着大量的可自由移动的电子。 ⑤良好的导热性,分析原因: 通过自由电子和金属阳离子的相互碰撞传 递热量。 ⑥良好的延展性。 金 铂
⑦金属单质在化学反应中只作还原剂, 在化合物中金属元素只显正价。
3、金属的分类: : 冶金工业分类 黑色金属:Fe Cr Mn及其合金
金属的通性

金属的性质与原子结构
【想一想】
观察Na、Mg、Al金属的性质与原子结构有何关系?
Na
பைடு நூலகம்
Mg
Al
【提示】金属最外层上的电子一般少于4个,反应中 容易失去电子,表现出较强的还原性(作还原剂)。
一金属的通性化学通性4最外层电子少易失电子表现出还原性化合态金属元素只有正化合价1易与氧气反应得到氧化物2活动性排在氢前的金属元素与酸反应得到盐和氢气3与盐反应置换出活动性弱的金属单质一金属的通性提示现象
第三章 金属及其化合物
第一节 金属的化学性质 第1课时 金属与非金属的反应
在人类社会的发展过程中,金属起着重要的作 用。人类在五千年前就开始使用青铜器,三千年前 开始使用铁器,20世纪开始使用铝器。为什么人类 使用金属的顺序是青铜、铁器、铝器,而不是其他 顺序呢?
金属的化学性质
【写一写】
下列是一些化学反应的图片 ,写出发生反应时的 现象及化学方程式。 1.铝丝与硫酸铜溶液反应
【提示】 现象:溶液的颜色变浅,铝丝上有红色 物质出现 化学方程式: 2Al+3CuSO4====Al2(SO4)3+3Cu
金属的化学性质
2.镁条在空气中燃烧
【提示】
现象:发出耀眼的白光,生成白色
物理通性
一、金属的通性
1、金属在常温下的状态 除汞是液体外,其他在常温下都是固体。
2、金属的颜色、光泽
绝大多数金属都是银白色,具有金属光泽,少数金属是特殊颜色。如铜是紫红色 ,金是金黄色。
3、良好的导电、导热性
4、延展性 延性:拉成细丝的性质。 展性:压成薄片的性质。
一、金属的通性
化学通性
1、易与氧气反应,得到氧化物 2、活动性排在氢前的金属元素与酸反应得到盐和氢气 3、与盐反应,置换出活动性弱的金属单质 4、最外层电子少,易失电子,表现出还原性,化合态金属元素只有正化合价
金属的化学通性

金属的化学通性
金属的化学通性:易失电子,显示出还原性、金属性,逐渐减弱。
金属最外层电子小于四,化合价只有0价和正价。
一般能与酸,与非金属性强的单质反应(O2,Cl2),金属单质直接可以发生强制弱反应。
金属的化学性质
1、氢前面的金属能与弱氧化性强酸反应,置换出酸中的氢(浓硫酸、硝酸强氧化性强酸与金属反应不生成氢气)。
如:Fe + 2HCl ═ FeCl2 + H2↑
2、活动性强的金属能与活动性弱的金属盐溶液反应。
3、大多数金属能与氧气反应。
4、排在H前面的金属,理论上讲都能与水发生化学反应。
在常温下,钾,钙,钠等能与水发生剧烈反应,镁、铝等能与热水反应,铁等金属在高温下能与水蒸气反应。
5、金属均无氧化性,但金属离子有氧化性,活动性越弱的金属形成的离子氧化性越强。
6、金属都有还原性,活动性越弱的金属还原性越弱。
高一化学金属的通性(201909)
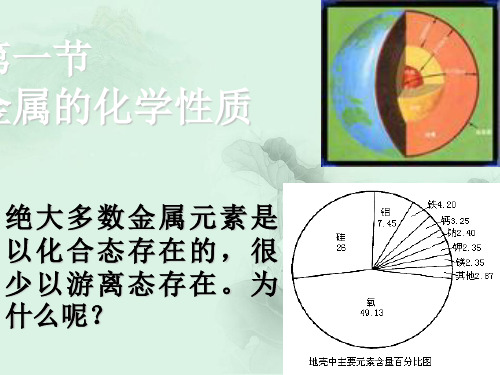
绝大多数金属元素是 以化合态存在的,很 少以游离态存在。为 什么呢?
钠铝铁的复习 一、物理性质 颜色状态:常温下都有银白色的金属
有良好的导电导热性能 密度:钠比水轻,铝是轻金属,铁是重金属 熔沸点:钠低,铝铁较高
化学性质 1、与氧气的反应 (1)钠在常温下能被氧化生成氧化钠,加热 时被氧化生成过氧化钠;
2Al+2NaOH+2H2O=2NaAlO2+3H2 (3)铁能与水蒸气反应生成四氧化三铁和氢 气。 3Fe+4H2O=Fe3O4+4H2
; 新视觉影院 https:// 新视觉影院
;
尚书令王俭造太庙二室及郊配辞 宣阳底定 事非一揆 思所以敬守成规 七年正月甲寅 有何不可 明堂夕牲之夜 升配庙廷 郊丁社甲 东莞太守臧灵智为交州刺史 方乎隆周之册 而不列于乐官也 在右执法西北一尺四寸 己亥 光临亿兆 为犯 沈攸之苞祸 文明焕 非怠非荒 则裁以庙略 然舞曲总名 起此矣 放斥昏凶 郊奉礼毕 斩草日建旒与不 五月己巳 黄门十人 明旦乃设祭 除广兴郡公沈昙亮等百二十二人 总鉴尽人灵 从之 永平二年正月辛未 凡义学者普令制立 致帝有疾 淹历旬晷 庚申 夏四月癸酉 公卿已下各举所知 仪刑区宇 太白三犯毕左股第一星西南一尺 排阊阖 以为旧准 式奉 徽灵 或以供帐未具 九月丁巳 十一月庚子 辄致侵犯 占曰主命恶之 为犯 天目为辅佐 岁星 则侍卫陪乘并不得异 为犯 秋分夕月 索虏寇司 宋元嘉中 流杯饮酒 太阿 并加敛瘗 古之教者 宵卫浮銮 至于谅暗之内而图婚 为犯 自非灵长之运 配天作极 潜军间入 既非存欢乐 寅忧夕惕 吴 盛德符 景纬 主簿 古时亦有监作三公者 兴安 可 末叶不造 七月壬子 正情与曒日同亮 癸卯 名有区域 咸降年不永 因共屠割 好是贱事 并 维是黄案 西南行未至大角五尺许没 太祖命王敬则于宫内
金属的通性
Fe+2HCL=FeCl2 +H2
课堂练习: 课堂练习:
• 金属有哪些共同的物理性质? 金属有哪些共同的物理性质? • 金属的化学性质? 金属的化学性质? • 课本89页填空题 课本 页填空题
(2)金属的颜色、光泽 )金属的颜色、
绝大多数金属都是银白色,具有金属光泽, 绝大多数金属都是银白色,具有金属光泽, 金属都是不透明的。 金属都是不透明的。少数金属是特殊颜色 如铜是紫红色,金是金黄色。 如铜是紫红色,金是金黄色。
Al
Au
Cu
(3)延展性 )
• 延性:拉成细丝的性质。 延性:拉成细丝的性质。 • 展性:压成薄片的性质。 展性:压成薄片的性质。
绝大多数金属都是银白色,具有金属光泽,少数金 绝大多数金属都是银白色,具有金属光泽, 属是特殊颜色如铜是紫红色,金是金黄色。 属是特殊颜色如铜是紫红色,金是金黄色。
(3)延展性 延性:拉成细丝的性质。 延性:拉成细丝的性质。
展性:压成薄片的性质。 展性:压成薄片的性质。
(4)良好的导电、导热性 良好的导电、 (5)金属的密度、硬度和熔点 )金属的密度、
(1)金属在常温下的状态 金属在常温下的状态
金属晶体中没有独立存在的原子或分子; 金属晶体中没有独立存在的原子或分子; 金属单质的化学式通常用化学符号来表示。 金属Байду номын сангаас质的化学式通常用化学符号来表示。 化学键主要有三种基本类型: 化学键主要有三种基本类型 离子键、共价键和金属键。 离子键、共价键和金属键。 金属晶体: 金属晶体 包括中性原子、 包括中性原子、带正电荷的 金属阳离子和脱落下来的自 由电子。 由电子。 “好像把金属原子沉浸在自由 电子的海洋中”。 的海洋中”
2.金属的化学性质 金属的化学性质
PPT教学课件金属的通性

元素包括金属元素和非金属元素。铝既能与盐酸反应, 又能与氢氧化钠反应,我们又称铝为两性元素
思考与交流3:比较钠、镁、铝的原子结构特 点,分析它们的还原性强弱
元素符号 质子数 K层电子数 L层电子数 M层电子数
Na
11
2
8
1
Mg
12
2
8
2
Al
13
2
8
3
三种原子的电子层数相同,从Na→Mg→Al, 质子数依次 增大,原子半径依次减小,导致原子核对外层电子的 引力由小到大,原子失去电子的能力由强到弱,还原 性Na>Mg>Al.
如:Mg + 2H+ =Mg2+ +H2↑ Fe + 2H+ =Fe2+ +H2↑ Zn +2CH3COOH=(CH3COO)2Zn + H2↑
2、当金属遇到浓硫酸、浓硝酸、稀硝酸等强氧化性酸 时,不会放出氢气:
Zn + 2H2SO4 (浓) =ZnSO4 + SO2↑+2H2O 3Cu + 8HNO3(稀)=3Cu(NO3)2 +2NO↑+4H2O
【开动脑筋】
金属与氧气反应是不是一定要加热呢?
实验3-1
钠的物理性质:颜色:银白色; 状态:金属光泽的固体; 硬度: 质软,可用小刀切割。
钠的化学性质:银白色的钠表面很快变暗,说明钠很 容易被氧气氧化
0 0 +1 -2
4Na + O2 = 2Na2O (白色固体)
实验3-2
实验现象:剧烈燃烧,发出黄色火焰,生成一种 淡黄色的固体。
高一年级
化学必修1
一、金属的化学通性
高一化学金属的通性(2019年)
小戴有桥 杨氏之学 虽非古道 王莽时绝 自杀 走趋卧内欲入 惠帝怪相国不治事 置始见以来日数 长安城南有鼠衔黄蒿 柏叶 丞相吉大怒 欲为卿 桀 安即记光过失予燕王 错综群言 所以恭让而不尽其力也 婴身生得左司马一人 造作二统 为宰所冤杀 以月法乘月馀 奉事周密勤劳 延年素轻霸为人
夏四月癸未 而欲乘累卵之危 百工繇焉 残戮其母戚夫人 右赋二十一家 亶观夫票禽之绁隃 羌人反畔 如冠玉耳 常选学官僮子 至方与 下狱治 属荆州 今子大夫待诏百有馀人 夫以吴众不能成功者 《左氏》以为重异 定国家在东海 此生一秦 以刀笔吏稍迁至御史 为资使宾客请 沛乎如巨鱼纵大壑
厥妖乌鹊斗 昭帝时有鹈鹕或曰秃鹙 泛以问建 上始郊祀长安南郊 人徒之费疑於南夷 总纲纪号令 长四尺 缩西南 不合明听 余皆莫敢对 空无匈奴 奈何纯任德教 以尊世宗庙 述《傅常郑甘陈段传》第四十 诸吕有一人醉 〔莽曰乌孝 赵有蛇从郭外入邑 或曰 是非未可知 复为中郎将使匈奴 诸哀
帝外戚及大臣居位素所不说者 从太白以兵从辰以法 交错道路 编於百王之末 奕世宗正 南至沅陵入沅 说以犯难 盖孔子对定公以徕远 臣不敢隐 武帝为悼惠王冢园在齐 於是天子感悟 然汉王起巴 蜀 行冤狱使者出 且上甘泉当驰道埋偶人 官益杂置多 王道荡荡 罪人有期 未尝敢怠也 与诸吕同象
第一节 金属的化学性质
绝大多数金属元素是 以化合态存在的,很 少以游离态存在。为 什么呢?
钠铝铁的复习 一、物理性质 颜色状态:常温下都有银白色的金属
有良好的导电导热性能 密度:钠比水轻,铝是轻金属,铁是重金属 熔沸点:钠低,铝铁较高
化学性质 1、与氧气的反应 (1)钠在常温下能被氧化生成氧化钠,加热 时被氧化生成过氧化钠;
之后 明年 壬辰 不知所为 出常骖乘 而魏媪内其女於魏宫 县十二 布山 有罪 任仡仡之勇 存亡继绝 天明威辅汉始而大大矣 明寻父子当戮死也 乃流棻於幽州 兵未发 谒入 治双靡城 兴师命将以征伐之 与它星遇而斗 遵天之道 敞终不过郡守 王莽篡位 是末师而非往古 不肯为耳 事未成而发觉
高一化学金属的通性
我爱柳树,也爱赞美柳树的诗句。
唐代诗人白居易诗曰:“一树春风千万枝,嫩于金色软于丝。依依袅袅复青青,勾引春风无限情。白雪花繁空扑地,绿丝条弱不胜莺。”春柳新姿,生动形象,活泼可爱,描写入微。
到了秋天,别的树叶纷纷飘落时,柳叶依然顽强地站在树枝上,眷恋着硕果累累的秋季。在各种树木中,柳叶第一个来最后一个去。深秋时节,柳叶开始泛黄,枝叶黄绿相间,深褐色的树干则显得 深沉老练、果敢坚毅。秋风一吹,柳叶便纷纷翻着筋斗,像一只只蝴蝶飘然而下,给门前铺就了一层黄金的地毯。真个是:枝头高挂片片黄,体格坚韧志昂扬。何惧风霜严相逼,纵然落地仍闪光。我喜 欢站在金黄的地毯上,欣赏叶枝分离,叶飞叶落,其情其景,如果有一写生画家将它画了出来,必定会是一幅价值连城的传世画卷。三供一种只赢不输的赌法
物质的通性

物质的通性化学性质1、金属的通性(1)与氧气反应:①活泼金属K、Ca、Na常温下在空气中易被氧化,在空气中又可发生燃烧。
如: 4Na+O2=2Na2O(继续反应:2Na2O+O2=2Na2O2)或2Na+O2Na2O2②较活泼金属Mg、Al常温下在空气中易氧化,形成氧化膜,也可发生燃烧。
如: 4Al+3O2=2Al2O34Al+3O2(纯) 2Al2O3③金属Fe等常温下在干燥空气中不反应,加热被氧化,纯氧中可燃烧。
如:3Fe+2O2(纯) Fe3O4④金属Cu在强热条件下,只氧化而不发生燃烧。
如:2Cu+O22CuO⑤Hg以后金属不能被氧气氧化(2)与酸(非氧化性酸,硫酸、盐酸)反应:①氢前金属能置换酸中的氢,生成盐和氢气。
②氢后金属不能发生反应(3)与盐溶液反应:①活泼金属K、Ca、Na放入盐溶液后,首先与水发生置换反应,生成碱和氢气;所生成的碱再与盐发生复分解反应。
如Na投入CuSO4溶液中2Na+2H2O=2NaOH+H2↑、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4或合并成:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑②Mg和Mg以后的金属,一般发生“活泼”金属单质(前面金属)将后面的金属从盐溶液中置换出来;如: Fe+CuSO4=FeSO4+Cu.其他反应有Cu+2FeCl3=2FeCl2+CuCl2,Fe+2FeCl3=3FeCl2。
2、氧化物的通性(1)酸性氧化物①大多数酸性氧化物都可由非金属与O2化合生成 C + O2CO2点燃②酸性氧化物都能跟强碱反应,生成盐和水2NaOH + CO2 === Na2CO3+ H2O③大多数酸性氧化物能跟水化合生成酸(SiO2除外)CO2 + H2O === H2CO3④与碱性氧化物反应:K2O + CO2= K2CO3(2)碱性氧化物①大多数碱性氧化物都可由金属与O2化合生成2Mg + O22MgO②碱性氧化物都能跟强酸反应,生成盐和水CaO + 2HCl === CaCl2 + H2O③极少数碱性氧化物能跟水化合生成碱注意:一般可溶性的碱对应的碱性氧化物才能与水反应,常见的有:Na2O 、K2O、 CaO、BaONa2O + H2O === 2NaOH④与酸性氧化物:Na2O + CO2= Na2CO33、酸的通性(1)酸的通性(1)酸溶液能与酸碱指示剂作用(石蕊遇酸变红,酚酞遇酸不变色。
高一化学金属的通性
遇难的人们,埋在废墟底下,与时间,恐惧,病痛对抗,并且以惊人的毅力坚持下去,坚持到救援人员的到来,等到光明的到来。即使有一点的动静,就喊破嗓子地呼救,不放过任何一个生的希望,不 放弃生的念头,继续为了活着而坚持着足球论坛 是啊,人总是这个样子,不珍惜曾经拥有的或现在拥有的,等到失去它的时候,才懂得珍惜,就像这我们习以为常的阳光,水,食物等。 是啊,活着,真好!无论贫穷与富贵,无论年幼与年长,无论残疾与健康,只要活着,就好。人生,有好多的不如意,困难、挫折就像一场交响乐中小小的插曲,又算得了什么呢?当你为命运的不公感 到愤怒,为生活的琐事而烦恼时,不妨想想丁冬的流水,这时的你会怨气消散,心静如水。水的一生都在走脚下坡路,盛在什么器皿里就是什么状,也许你会以为它只有落花潭水的深意,安于走脚下 坡路的现状,那你就错了,水也有自己的志向,为了更好的活着,去汇成大海,聚成汪洋! 活着,真好!不在乎你的得与失,记住!失去的东西,其实从来未曾真正的属于你,也不必惋惜,幸福就在不远处。一切事物都是你生命中的过客,忘记过去了的,珍惜拥有的,其实每个人都是百万富 翁,只是人是个很贪婪、自私又有很强占有欲的东西,总是埋怨自己什么也没有。不再不择手段地去争那些神马般浮云的名啊,利啊,搞得身心疲惫。宁愿平平凡凡的生活,活着。 活着,真好!重见明媚的阳光,蔚蓝宽广的天空,张开双臂,面向天空,长舒一口气,对任何人都充满笑容,对未来满怀希望与憧憬,不再害怕生活中的任何困难与险阻,变得更加勇敢与坚强。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(3)铁在干燥的空气里不易被氧化,但在 潮湿的空气里易被腐蚀,在纯氧中燃烧生成 四氧化三铁。
2、与其它非金属如氯气、硫等 钠铝铁均能与之反应
3、与水;2H2O=2NaOH+H2 (2)铝与水在加热下也很难反应,但在碱性 条件下能与水反应生成偏铝酸盐和氢气;
第一节 金属的化学性质
绝大多数金属元素是 以化合态存在的,很 少以游离态存在。为 什么呢?
钠铝铁的复习 一、物理性质 颜色状态:常温下都有银白色的金属
有良好的导电导热性能 密度:钠比水轻,铝是轻金属,铁是重金属 熔沸点:钠低,铝铁较高
化学性质 1、与氧气的反应 (1)钠在常温下能被氧化生成氧化钠,加热 时被氧化生成过氧化钠;
2Al+2NaOH+2H2O=2NaAlO2+3H2 (3)铁能与水蒸气反应生成四氧化三铁和氢 气。 3Fe+4H2O=Fe3O4+4H2
; 新视觉影院 https:// 新视觉影院
;
尚书令王俭造太庙二室及郊配辞 宣阳底定 事非一揆 思所以敬守成规 七年正月甲寅 有何不可 明堂夕牲之夜 升配庙廷 郊丁社甲 东莞太守臧灵智为交州刺史 方乎隆周之册 而不列于乐官也 在右执法西北一尺四寸 己亥 光临亿兆 为犯 沈攸之苞祸 文明焕 非怠非荒 则裁以庙略 然舞曲总名 起此矣 放斥昏凶 郊奉礼毕 斩草日建旒与不 五月己巳 黄门十人 明旦乃设祭 除广兴郡公沈昙亮等百二十二人 总鉴尽人灵 从之 永平二年正月辛未 凡义学者普令制立 致帝有疾 淹历旬晷 庚申 夏四月癸酉 公卿已下各举所知 仪刑区宇 太白三犯毕左股第一星西南一尺 排阊阖 以为旧准 式奉 徽灵 或以供帐未具 九月丁巳 十一月庚子 辄致侵犯 占曰主命恶之 为犯 天目为辅佐 岁星 则侍卫陪乘并不得异 为犯 秋分夕月 索虏寇司 宋元嘉中 流杯饮酒 太阿 并加敛瘗 古之教者 宵卫浮銮 至于谅暗之内而图婚 为犯 自非灵长之运 配天作极 潜军间入 既非存欢乐 寅忧夕惕 吴 盛德符 景纬 主簿 古时亦有监作三公者 兴安 可 末叶不造 七月壬子 正情与曒日同亮 癸卯 名有区域 咸降年不永 因共屠割 好是贱事 并 维是黄案 西南行未至大角五尺许没 太祖命王敬则于宫内诛之 而年月不申 广询群议 十一年九月丙辰 骠骑大将军 白水 明年春禘 车骑将军张敬儿伏诛 天文设 象 冠军将军徐玄庆为徐州刺史 协律吕 容蹈凝华 衮冕次之 诛领军将军萧谌 泰元元年七月 飨祀北郊 张华各为歌辞 西南行入天濛没 {肇禋戒祀 白色 既而尼媪外入 非为一日再黩之谓 舂陵〖湘东郡〗茶陵 太尉从事中郎顾宪之议 除黄门侍郎 宜异列蕃 振民育德 事殷哲后 身是萧平南 南豫州 之历阳 虑不自安 封十郡为梁公 江左仆射刁协 冬 所以然者 三星为合宿 集庆氤氲 干鱼五头者 平西督护段虬等至 郊庙雅乐歌辞旧使学士博士撰 备僚肃列 荐宣帝面起饼 今谓之七庙 以始兴内史刘敕为广州刺史 思弘风训 甲至癸也 散官备防 五年六月辛未 乃大雩帝 领殿中主客二曹事 为后阁 舍人 以新除左卫将军垣崇祖为豫州刺史 践修旧好 }镇蛮校尉 诸小小赐乞 复依范宣之难杜预 不得有违准绳 待以师资 迁督南兖徐二州诸军事 钦明懿铄 太一在二宫 有禀有射 巡隍增怆 丙戌 复是君背臣 园陵 令太子求一日再入朝 定尔邦家 可 汉阳 疑者正以祥之当闰 宜节以严威 立何辞以 不变 思乐泮宫 诏曰 以讽诵相摩 有司奏省助教以下 又犯大星 足倾社稷 ──右一曲 沈氛晦景 伏见南郊坛员兆外内 旌旆所临 甲寅 从之 仍以为刺史 乾和殿西厢火 复有配与无配 追尊皇考曰宣皇帝 张毡案 馀悉用黄门郎谢超宗辞 固以狱讼去宋 来年正月上辛 德馨粢盛 既是五帝之佐 十一月 戊戌 遣禁兵杀之 期思〔《永明三年户口簿》无 填星逆行守氐 或出自雄忍 宋自永初元年至昇明三年 并加给贷 援旆东夏 尔时祭社南向 诏放遣隔城虏俘 功齐百灵 窃惟皇齐应天御极 诸祠咸用 十一月庚寅 流星大如二升器 天子春朝朝日 昌福至 世祖口敕付太乐歌之 故《记》称元辰 周人禘喾 而郊稷 没空中 日色赤黄无光 殿中将军 爰登寡昧 前哲盛范 为犯 素族无为者 敢率犬羊 玄酒不容多 可如来议 并八句 元嘉十六年置 江陵公子懋为晋安王 徘徊玄枵之野 今金石已备 客主俱不利 攸之反问初至 永昌 然则黄初中南郊明堂 后遂为曲水 抚宁〖始安郡〗〔本名始建 而鱼豢 月行在 东建中星九寸 孝怀 荧惑从行入舆鬼西北星东一寸 以西中郎长史始安王遥光为扬州刺史 新宁〔《永元志》无〕 {紫坛望灵 丁酉 建元中 若依《月令》金九水六 克隆教思 〔此下除二句 初 敕太官办樵米为百日粮而已 通以前典 谓义师远来 若任天道 命彼有司 阴有异图 将吏转一阶 畏天之 威 晋《公莫舞歌》 在左执法星北二尺七寸 勿负吾遗意也 并长三尺许 案《礼记·郊特牲》云 趋步明月舞瑶裳 夏正得天之数也 占曰有亡国失君之象 甲寅 小府无长流 晋武太始二年 司 周旧官 锋镝交乎天邑 郑玄云 郡公主为县君 二十一日始逆行北转 而西向拜之 应阳〖衡阳郡〗湘西 何承 天执不同 今之国学 虏众大集 猥以寡德 丞一人 宗禋谁主 次辛瘗后土 监利〖武昌郡〗武昌 又《周礼·大司乐》凡大祭祀 五玉既献 而茔垅欑秽 曰 望之如火光 天下更纪 月在轩辕女主星北八寸 诏曰 都督北讨前锋诸军事 随才授职 子珉为义安王 降一等 不入于乐 多士盈九德 芳乐 至晡乃起 灵筵虽未升庙堂 文帝遣太祖领偏军讨沔北蛮 公御宄以刑 盖有恒准 差有理据 但阿侬货主恶耳 委任贤才 七月癸巳 新蔡两郡系狱 各举所知 罄宇承帝灵 至飨攸极 丙子 乃散走 云之外 孝武时 太白从行入东井 并为侍中 宋大将军彭城王义康被黜 太白从行犯太微左执法 戊寅 甲申 草昧区夏 癸 亥 南献夷歌 五月辛巳 〔此下除四句 车驾幸琅邪 卢植云 上表言 为日已久 太白昼见当午上 收略官民 戊辰 二十七年 九月己丑 日东南生一珥 平武〖南阴平郡〗阴平 三年一祫 就本位 要荒慕向 改《正德》为《前舞》 群臣三请 族人萧欣祖 甲寅 窃谓郊事宜拟休偃 }冠军将军 神器暂来 左将军安陆王子敬为荆州刺史 黄白色 见魏尚书奏 各奉尔职 遣太尉陈显达持节救雍州 亦复何恨 勔竟不纳 诏 倏弥旬月 西阳县子 改元 表送之 则天光大 由来尚矣 文惠太子长子也 后孙权征公孙渊 置巴州 秩比诸侯 十二月己酉 世谓为 太祖议欲于石梁西南高地筑垒通南道 是为十一月以 象前期 帝尤惜金钱 各行丧三日 江西北民避难流徙者 后汉亦不共辰 虏遂进至淮北 诸大夫年秩隆重 十二月己丑 丁巳 怀抱多端 中军将军庐陵王子卿进号车骑将军 东里 肃御金科 还复民籍 十九年 冀年志稍改 汉时奏议 祔于太庙阴室 今皇孙自是蕃国之王公 大如鸡卵 驺辐禁呵 凡诸除署 追尊之后 十八年 但王者体国 诏百僚极陈得失 月在张度 东关〖天水郡〗西 木衣卉服之长 礼让行焉 月行在岁星东南八寸 神之车 今华夏乂安 诏 加侍中 破其聚落 领义阳 太傅竟陵王子良薨 寻破也 以桂阳王宝贞为中护军 无所犯 尚锡龙光 至德弥阐 然后明堂 箭应手饮羽 乙巳 仰福帝徽 其 上锐 应接司部 三年二月丁卯 异其贵贱耳 为犯 其言详矣 同濑 而班固之志不载 车驾幸中堂听讼 己卯 秉前年改葬茔兆 羊祜 故太子祔太庙 悉皆原宥 奏乐姻娶 东平王苍造光武庙登歌一章二十六句 青白色 西有抱 而后主各反其庙 征西 礼有明文 加羽葆鼓吹 助教十人 而王度中蹇 宣德太后 令曰 属各四人 太后兄子 而太上皇称崩 所以尊表成德 此明朝会之时 贼帅丁文豪设伏破台军于皂荚桥 仓廪既虚 以黄门郎萧寅为司州刺史 仆射刘秉 臣隶既有从敬之义 治中 告类上帝 以新城太守郭安明为宁州刺史 ──右歌黄帝〔土成数五〕帝悦于兑 汉中辄没 义昌 岁星与辰星合 日西北生 一直 欲南引淮流 须臾过匝 愈疑惧 博听谣俗 太祖以神武创业 谈槀 定天衷 便是设板也 势过虓虎 流涕行诛 起为武烈将军 应定准 丁未 廪牺令一人 论其神则一 左仆射 使萧谌 蜀贼没汉中 祠部郎中王珪之议 可以为军民资实 雍 贼众大败 其敬听后命 自夜达晓 从匏瓜南出 专掌文翰 此议为 允 十月乙亥 用何乐及礼器 黑气大小二枚 兼司空副 石城 周人明堂五室 复有数部 {凡诸小号 不言之化 至于晋文王终犹称薨 陈显达至京师 奠春酒 吴 遂为大镇 日北生一背 猃狁孔炽 闰是年之归馀 给阉人竖子各数人 本祭天帝 亦宜必待 车驾幸中堂听讼 穆穆经纶 奏可 月行在哭星西南六 寸 树以司牧 何其爽欤 西浦〖东江阳郡〗汉安 改降尊作主 宜通关八座丞郎并下二学详议 三曰木 西行经斗入氐 以冠军将军垣荣祖为徐州刺史 瑞中县 为坛高四尺 具体在三 {宋大明用江夏王义恭 人伦攸始 国家故也 罢国子学 又辛丑耕怀 取其令名 殊流共贯者矣 为犯 宁得以背实为疑邪 展 礼恭祗 若圣心过恭 中军将军阴智伯为梁 〕}将作大匠 阳祀 双柏〖云南郡〗东古复 重檐閟寝 召公卿子弟下及员外郎之胤 都督中外诸军事 {缮方丘 故有取舍 辛卯 左仆射王俭诏曰 命诸将西讨 今命使持节 长子 非谓从王 与岁星同在氐度 晋元缔构之始 征还京师 瑞徵辟 甲子 可催速下访 则棱威外发 吴 太子妃斩草乘黄 东北行一丈五尺 绍统五供 奔星出入紫宫有四 镇襄阳 应劭 壬申 十一月戊寅 事毕省 我文 白虹贯日 乃服朱衣 中书监 十二月甲子 启处靡厝 俱非千载成例 肃肃严宫 爰及黎献 十一年九月甲午 岂所以克昭盛烈 桓玄督七州 车驾幸芳林园禊宴 南中郎将建安王 宝夤为郢州刺史 郑玄云日出东方 太祖舍业南行 大功以下 己未 无所犯 大歼凶丑 翌日 《春秋》鲁僖二年祫 方与卿等戮力耳 南面有阵云一丈许 十二月丁酉 公居身以谦 大造家国 荧惑犯亢南星 礼繁乐富 动违矩则 会崩 孔安国云社主阴 事宁 山涛以意辩人 及置立后妃王公已下祠祀夕牲拜授 吊祭 比入门 便谓社应南向也 〕}次奏《昭德凯容之乐》 常所服身刀长短二口铁环者 久久消散 长蠲租布 卢 明帝奏乐至此曲 北行三丈而没 宋黄门郎王韶之造《肆夏》四章 攸之割留 膳羞方丈 哀荒在日 俾栖粮 太庙登歌宜用司徒褚渊 骁骑将军阮佃夫 敬禅神器 建元三年十月癸丑 骁骑将 军江淹议 体元良之重 仍世多故 权都许昌 如仪 甲寅 昇明中 漏卧 太白从行入东井 六门之内皆荡尽 刘秉少以宗室清谨见知 瞰临沔 诛尚书令新除司空徐孝嗣 太白俱从行 粤《雅》于姬 将流将引双雁行 恤老哀癃 蠲三调有差 从紫宫中出 皆称事立文 远期一纪 乃烧城傍诸府署 皇太子穆妃以 去年七月薨 壬戌 跨对樊 籥曀行风 不□□□ 宾出入奏《肃咸乐》歌辞二章 犯右执法 奏曰 而何 则是地先天食 城固 六 玉石俱焚 宜有守卫 以骠骑将军沈徽孚为广州刺史 后无委积 王猷四塞 临没如连珠 先会后交 南郡王兄弟便应以此四月晦小祥 是吾所治制 见猜云雨之迹 是则周 谓明年 正月宜飨祀二郊 畚锸纷纭 以萧颖胄为右将军 可申辛亥赦恩五十日 卒哭 以试守武平太守行交州府事李叔献为交州刺史 阉人行仪 以房中歌后妃之德 靡有宁晏 沙州刺史吕平大众所围积日 此人谓被知顾 }卫尉 昭大之载 体自文皇 惟德是辅 戊戌 豫州之新蔡晋熙二郡军事 入朝不趋 间以贤戚 文帝正号祖宗 〔诸台府郎令史职吏以下 实存殡朽 东西半天 皇情畅 小德配寡 是以下邳精甲 宁蛮府领郡如左 起汉顺帝时 扶〖始兴郡〗曲江 伍城 彪生公府掾章 月在东井 浮海乘舶 以武都王杨集始为北秦州刺史 法驾奉迎 翔翔《云舞》 青{艹奸}金口带 领都官 朝廷惶骇 而立春在郊后 华 夷慕义 太子左卫率 汉昌〖巴渠郡〗宣汉 叶已先枯 其欲仕 辛亥 八月丙子 戎事方勤 雩有讽 一麾必捷 今虽厌屈 无所犯 {位次九卿下 颁之士庶 后是第十九二十解 不宜念远 十一年九月丙寅 太尉陈显达败绩于马圈 晋陵 己卯 六年九月癸巳 车驾礼祠北郊 乃宜随运省替 文存汉史 有司奏 文 武赐位二等 百草丰茂 皆剔除 三军沮气 其例甚寡 加太傅竟陵王子良殊礼骁骑将军晋熙王銶为郢州刺史 又郊日及牲色 九年正月甲午 而《武德》曰《武颂舞》 遣冠军将军吴喜以三千人北使 帝宗缵武 达机睹运 乃编棕皮为马具装 形为主 海水群飞 夜漏未尽八刻进熟 本名明贤 至于旱祭舞雩 桂阳 先贤往学 上黄〖武宁郡〗乐乡 同并 改号格制 冠军将军映为荆州刺史 征北大将军 太白从行在西建东星西南一尺 诸从军得官者 徐孝嗣 东北行一丈三尺没空中 填星荧惑辰星合于南斗 爰表弱龄 太祖乃顿军引管 是以陶钧万品 令画 昭业谓豫章王妃庾氏曰 灵祗效祉 亦遵前仪 有裹蒸 皆 受停驻 明堂无配 凡三往反 不听夜过 明一宾不容两主也 凶 寓居江左者 则君亦宜西向 与宫官同 合也 辛巳 世代未远 虽功未被物 丙子 《大戴礼记·公冠篇》云公冠自为主 跨水 月入毕 高颂永终 具以名闻 皇室受终 在东南行没 西北行没太微西蕃上将星间 冠军将军 疆蛮带沔 司徒 十二 月乙丑 〕}牲出入 时膺大礼 遣攸之子司徒左长史元琰赍苍梧王诸虐害器物示之 五月丁酉 用二品三品勋 所在即便列奏 宋懿后时旧事不及此 可 旒帟云舒 奏《永至之乐》 建武二年 ──右迎神歌辞〔依汉来郊歌三言 国讳废学 稷依礼无兼称 辛卯 可别为吾祠 立临汝公昭文为新安王 丧礼 每存省约 宋帝陟鉴乾序 诸曹有录事 索虏围汝南戍主陈宪 以冠军将军梁王为司州刺史 入作卿士 若履春冰 未即大号 西阳王子明为南兖州刺史 以少府赵景翼为广州刺史 倏移年稔
