原子晶体
什么叫原子晶体

2、原来自百度文库晶体的特点
(1)结构特点:
A、在晶体中,不存在单个分子
B、原子通过共价键形成空间网状结构
(2)物理性质
A、熔沸点很高,硬度很大
原子晶体中存在着较强的共价键,而且形 成空间网状结构,要破坏它需要很大的能 量,故原子晶体硬度大、熔沸点高。 B、不导电
C、难溶于常见溶剂
3、属于原子晶体的物质:
答:1/2个
晶 体 硅 结 构
碳 化 硅 晶 体 结 构
二 氧 化 硅 晶 体 结 构
思考:
石墨晶体中,最小环上有几个碳原子?
答:6个
每个碳原子由几个六元环共用?
答:3个
每个环上占用几个碳原子?
答:2个
三种典型立方晶体结构
简单立方
体心立方
面心立方
5、有下列八种晶体:①水晶②冰醋酸③氧化镁 ④白磷⑤晶体氩⑥氯化铵⑦铝⑧金刚石。用序号 回答下列问题: (1)、属于原子晶体的化合物是 ,直接 由原子构成的晶体是 ,直接由原子构成的 的分子晶体是 。 (2)、由极性分子构成的晶体是 ,含有 共价键的离子晶体是 ,属于分子晶体的 单质是 。 (3)、在一定条件下能导电而不发生化学变化 的是 ,受热熔化后化学键不发生变化的 是 ,受热熔化需克服共价键的是 。
金刚石、单晶硅、碳化硅、二氧化硅等。
石墨 —混合型晶体
石墨晶体由碳原子构成,是层状结构,层内每 个碳原子与周围三个碳原子以共价键结合,形 成以正六边形排列成平面网状结构,层与层之 间以范德华力相结合,且有自由移动的电子。 构成微粒:原子; 微粒间作用力:共价键和分子间作用力; 石墨晶体具有原子晶体结构特点,又有分子晶 体结构特点,所以属混合晶体过渡型晶体。
3.3 原子晶体

拓展练习 氮化硼是一种新合成的结构材料,它是超硬、耐磨、耐高温 的物质,下列各组物质熔化时所克服的粒子间的作用力与氮 化硼熔化时所克服的粒子间作用力相同的B是( ) A.C60和金刚石
B.晶体硅和水晶
C.冰和干冰
D.碘和金刚砂
原子晶体
教学目标
知道原子晶体的概念,能够从原子晶体的结构特点理解 其物理特性。
了解原子晶体的特征,能以典型物质为例描述原子晶体 结构与性质的关系。
学会晶体熔、沸点比较的方法 。
教学重点
原子晶体的概念;原子晶体的结构和性质 。
教学难点
原子晶体的结构特点 。
分子晶体 什么是分子晶体?举例说明 。分子间通过分子间作用力结合而成的晶体。例如干冰( CO2晶体)和晶体碘等。
D.晶体中最小环上的原子数为 8
拓展练习
干冰和二氧化硅晶体同属第ⅣA族元素的最高价氧化物,它们 的熔、沸点差别很大的原因是C( )
A.二氧化硅的相对分子质量大于二氧化碳的相对分子质 B量.C—O键键能比Si—O键键能 C小.干冰为分子晶体,二氧化硅为原子晶 D体.干冰易升华,二氧化硅不 能
拓展练习
:
Si
O
共价键 实际上就是在晶体硅的Si—Si 键上插入O原子。
金刚石和二氧化硅
原子晶体(ppt)
C )
5.石墨晶体是层状结构,在每一层内; 每一个碳原于都跟其他3个碳原子相结 合,如图是其晶体结构的俯视图,则图 中7个六元环完全占有的碳原子数是 ( D ) A. 10个 B. 18个 C. 24个 D. 14个
6. 2003年美国《科学》杂志报道:在超高压下, 科学家用激光器将CO2加热到1800K,成功制 得了类似石英的CO2原子晶体。下列关于CO2 晶体的叙述中不正确的是 ( )C A. 晶体中C、O原子个数比为1∶2 B. 该晶体的熔点、沸点高、硬度大 C. 晶体中C—O—C键角为180° D. 晶体中C、O原子最外层都满足8电子结构
【巩固练习】 1.下列晶体由原子直接构成,且属于分子晶 体的是 ( B ) A.固态氢 B.固态氖 C.白磷 D.三氧化硫 2. 共价键、离子键和范德华力是构成物质粒 子间的不同作用方式,下列物质中,只含有 上述一种作用的是 ( B ) A. 干冰 B. 氯化钠 C. 氢氧化钠 D. 碘
3.在金刚石的晶体中,含有由共价键形成的 碳原子环,其中最小的环上所需碳原子数及每 个碳原子上任意两个C—C键间的夹角是 ( D ) A.6个120° B.5个108° C.4个109°28′ D.6个109°28′ 4. 支持固态氨是分子晶体的事实是 A. 氮原子不能形成阳离子 B. 铵离子不能单独存在 C. 常温下,氨是气态物质 D. 氨极易溶于水 (
的熔点从高到低的顺序是 (
无机化学——原子晶体与分子晶体
分子晶体的特性 分子晶体是以独立的分子出现的 ,化学式就是分子式。
分子晶体可以是非金属单质,如卤素、H2、N2、O2; 非金属化合物,如CO2、H2S、HCl、HN3等 绝大多数有机化合物,稀有气体的晶体
如 F-<Cl-<Br-<I-,O2-<S2-<Se2-<Te2-
(2)对称性强,结构紧密的复杂阴离子变形性不大。 极化力大的是电荷高半径小的阳离子,如Al3+,Fe3+。变形性大 的是体积大的阴离子和18,18+2电子构型的阳离子.
极化作用和相互极化作用较强的有CdS,PbS,HgS等。
5 附加极化作用 当正离子半径较大时,也可被负离子极化,极化变形后的
正离子又可反过来对负离子产生极化作用,这种加强了的极化
作用叫附加极化作用,作用的结果,使得正负离子电子云发生
部分重叠,键型由离子键向共价键过渡。
如: NaCl MgCl2 AlCl3 又如:AgF AgBr AgI
离子键 → 共价键
离子键 → 共价键
+-
离子相互极化作用增强
典型离子键
键的极性减弱
典型共价键
原子晶体结构

原子晶体结构
简单的说,一个分子就像一座楼房,由许多个原子组成;而每个原子则像这座楼房中的一个个分子,并且原子间存在着一定的空隙。在高中化学里面,我们研究的主要对象也是原子和分子,但原子不像分子那样可以进行较为自由的运动。因此,我们通常把物质内部质点之间的结合力称作化学键。
(1)原子晶体结构的特点,原子晶体可根据其内部质点间结合的
方式及大小来分类。同种原子晶体的化学性质完全相同。同种元素的原子或离子的晶体往往具有相同的晶体结构。这种结构是由于原子(离子)之间的相互作用力所决定的,并不是随意排列的,这种固定的空间格局使物质获得了理想的熔点、沸点、密度等宏观性质,也正是这些性质决定了原子晶体在各个领域的应用。
(2)原子晶体的最小微粒是分子,分子的大小通常为0。 1~10
原子间距的数十亿分之一。分子可以在溶液中自由运动,无规则地作布朗运动。分子本身没有确定的熔沸点,但是分子在受热或降温的过程中,可能吸收或放出某种波长的光而显示出固有的颜色,例如红磷,加热时逐渐变暗,降温时又发出红光,表明它是由于吸收了可见光以后发生了颜色变化。此外,原子晶体还有气态原子,如稀有气体就是很好的例子。原子晶体的导电性与这些微粒之间结合力的强弱有关。
(3)在相同条件下,气态的原子晶体比液态原子晶体的密度大。
但是,同一种原子晶体中的不同种分子可以有不同的熔沸点,这主要取决于分子之间的结合力。例如,水是一种分子晶体,冰的熔点为0 ℃,
水蒸气的沸点是100 ℃。同种元素的原子或离子,按照一定的方式结合在一起形成晶体后,不仅其化学性质相同,而且具有一定的结晶格架,从而具有一定的熔点、沸点和密度等宏观物理性质,这就是晶体的特征。同种晶体的物理性质、化学性质是决定于其晶体结构,而与是否含有杂质元素无关。例如,某晶体的熔点、沸点是a、 b两种元素的原子按某种空间排列组合而成的结果。所以说:同种原子组成的晶体物质性质一定相同。
高中化学物质结构原子晶体

第2课时原子晶体
[学习目标定位] 1.知道原子晶体的概念,能够从原子晶体的结构特点理解其物理特性。2.学会晶体熔、沸点比较的方法。
一原子晶体的概念及其性质
1.金刚石的晶体结构模型如右图所示。回答下列问题:
(1)在晶体中每个碳原子以4个共价单键对称地与相邻的4个碳原子相
结合,形成正四面体结构,这些正四面体向空间发展,构成彼此联结
的立体网状结构。
(2)晶体中相邻碳碳键的夹角为109°28′,碳原子采取了sp3杂化。
(3)最小环上有6个碳原子。
(4)晶体中C原子个数与C—C键数之比为1∶2。
(5)晶体中C—C键键长很短,键能很大,故金刚石的硬度很大,熔点很高。
2.通过以上分析,总结原子晶体的概念
(1)概念:相邻原子间以共价键相结合形成的具有空间立体网状结构的晶体,称为原子晶体。
(2)构成微粒:原子晶体中的微粒是原子,原子与原子之间的作用力是共价键。
(3)常见的原子晶体:常见的非金属单质,如金刚石(C)、硼(B)、晶体硅(Si)等;某些非金属化合物,如碳化硅(SiC)、氮化硼(BN)、二氧化硅(SiO2)等。
如二氧化硅的结构为
①每个硅原子都采取sp3杂化,以4个共价单键与4个氧原子结合,每个氧原子与2个硅原子结合,向空间扩展,构成空间网状结构,硅、氧原子个数比为1∶2。
②晶体中最小的环为6个硅原子、6个氧原子组成的12元环。
(4)由于原子晶体中原子间以较强的共价键相结合,故原子晶体:①熔、沸点很高,②硬度大,
③一般不导电,④难溶于溶剂。
[归纳总结]
(1)构成原子晶体的微粒是原子,其相互作用是共价键。
晶体结构(3, 原子晶体与分子晶体)
CO2
SiO2
课堂练习
° 1、 白磷分子中的键角为 60° ,分子的空间结 、 每个P原子与 构为正四面体 ,每个 原子与 3 个P原子结合成共 原子结合成共 价键。若将1分子白磷中的所有 分子白磷中的所有P-P键打开并各插 价键。若将 分子白磷中的所有 键打开并各插 个氧原子, 若每个P 入一个氧原子, 入一个氧原子,共可结合 6 个氧原子, 若每个P 原子上的孤对电子再与氧原子配位, 原子上的孤对电子再与氧原子配位,就可以得到 填分子式)。 磷的另一种氧化物 P4O10 (填分子式)。
影响原子晶体熔沸点、硬度大小的因素: 5、 影响原子晶体熔沸点、硬度大小的因素: 共价键的强弱 键长的大小 一般键长越小, 一般键长越小,键能越 大 ,原子 晶体的熔沸点越 高 ,硬度越 大 。
常见的原子晶体: 6、 常见的原子晶体: 单 质:金刚石、晶体硼、晶体硅; 金刚石、晶体硼、晶体硅;
化合物:金刚砂、氮化硼、石英等 化合物:金刚砂、氮化硼、
SiO2晶体
④晶体中最小的环有 12 个 原子。 原子。
小结: 小结:三种化学键的比较
化学键 成键本质
由电子静电作用 键的方 影响键强弱 的因素 向性和 饱和性
金属键 金属阳离子和自 离子键 阴阳离子间的 静电作用 共价键 共用电子对
无 无 有
原子半径和 价电子数 离子半径和 离子电荷 键长
高二化学分子晶体和原子晶体知识点

高二化学分子晶体和原子晶体知识点
高二化学分子晶体和原子晶体知识点
(一)分子晶体:
构成晶体的微粒间通过分子间作用力相互作用所形成的晶体,称为分子晶体。分子晶体中存在的微粒是分子,不存在离子。较典型的分子晶体有非金属氢化物,部分非金属单质,部分非金属氧化物,几乎所有的酸,绝大多数有机物的晶体等。
分子晶体中存在的相互作用力主要是分子间作用力,它是分子间存在着一种把分子聚集在一起的作用力,叫做分子间作用力,也叫范?曰?力。分子间作用力只影响物质的熔沸点、硬度、密度等物理性质,分子晶体一般都是绝缘体,熔融状态不导电。
对于某些含有电负性很大的元素的原子和氢原子的分子,分子间还可以通过氢键相互作用。氢键的形成条件:它是由已经与电负性很强的原子形成共价键的氢原子与另一分子中电负性很强的原子之间的作用力形成,(它不属于化学键)一般表示为X?DH…Y。这种静电吸引作用就是氢键。氢键同样只影响物质的熔沸点和密度,对物质的化学性质没有影响
分子晶体的结构特征:
没有氢键的分子密堆积排列,如CO2等分子晶体,分子间的作用力主要是分子间作用力,以一个分子为中心,每个分子周围有12个紧邻的分子存在。
还有一类分子晶体,其结构中不仅存在分子间作用力,同时还存在氢键,如:冰。此时,水分子间的主要作用力是氢键,每个水分子周围只有4个水分子与之相邻。称为非密堆积结构。
说明:
1、分子晶体的构成微粒是分子,分子中各原子一般以共价键相结合。因此,大多数共价化合物所形成的晶体为分子晶体。如:部分非金属单质、非金属氢化物、部分非金属氧化物、几乎所有的酸以及绝大多数的有机物等都属于分子晶体。但并不是所有的分子晶体中都存
原子晶体的物理特性

三、金刚石
过 程
最小的碳环有几个碳原子?
石墨晶体中每一层为 正六边形的平面网状 结构,则每个正六边形 占有多少个碳原子?多 少个C-C键?
2、晶体举例: NaCl的晶体结构:
6:6
CsCl的晶体结构:
8:8
体心
1
面心
1 2
棱
1 4
顶点
1 8
NaCl的晶体结构:
Na+:4 Cl–:4
小结:晶胞中实际质点数
每个晶胞中,各“质点”对晶胞的贡献分 别是:
面心点为1/2,体心点为1 、棱上的点为 1/4、角上的点为1/8 。
由NaCl晶体结构图可推知晶体结构中Cl-= (12/4+1)=4个;Na+=(8/8+6/2)=4个, 即每个这样的结构单元中相当于有4个NaCl 。
Si,SiO2,SiC
SiO2>SiC > Si
分子晶体:结构相似的分子,分子量越大,分子间作用力
越大,熔沸点越高。
F2,Cl2,Br2,I2
F2 < Cl2 < Br2 < I2
练习:比较晶体熔沸点的高低
1、金刚石、氯化钠、干冰 2、金刚石、晶体硅、碳化硅 3、CH4、C2H6、C3H8 4、正戊烷、异戊烷、新戊烷 5、NaCl、CsCl
实例
NaCl
离子晶体、分子晶体、原子晶体

离子晶体
分子晶体
原子晶体
硬 度
质
溶解性
2、化学键和分子间作用力的比较:
化学键 概念 能量 性质影响 分子间作用力
3、影响晶体物理性质的因素:
影
离子晶体 分子晶体 原子晶体
响
因 素
共价键
氢键
氢键的形成过程
返回
温度/℃ H2O 温度/100 ℃ 沸点/℃ 250 75 沸点 250 熔点 CBr 200 沸点 4 × × 50 200 150 I2 CI4 150 25 HF 100 CCl 熔点 × 100 4 × CBr4 I 0 H2Te 50 2 100 150Br 50 SbH3 2 -25 0 2Se 200 300 400 H 500 × NH3 100 H S HI 0 Br 2 2 200 -50 50 250 -50 CCl4 -50 × AsH Cl 3 相对分子质量 SnH4 2 -100 HCl 相对分子质量 -100 -75 HBr CF × Cl 4 2 -150 × PH3 GeH4 -150 × -100 -200 F2 CF 4 SiH 4× -200 -125 F2 -250 -250
长春市十一高中 王奎田
一、离子晶体
定义:
像氯化钠、氯化铯这样离子间通过 食盐、氯化铯 实例: 离子键结合而成的晶体叫做离子晶体。
离子晶体、分子晶体和原子晶体

离子晶体、分子晶体和原子晶体一、重点难点重点:1、离子晶体、分子晶体、原子晶体的概念离子晶体:阴阳离子间通过离子键结合而成的晶体。分子晶体:分子间以分子间作用力相结合的晶体原子晶体:相领原子间以共价键相结合而形成空间网状结构的晶体。2、三种晶体类型与性质的关系难点:1、离子晶体、分子晶体、原子晶体的结构模型2、二氧化硅晶体结构模型二、例题分析第一阶段例1、氮化碳晶体是新发现的一种高硬度材料,该晶体类型应该是_________晶体。试根据物质结构知识推测氮化碳晶体与金刚石晶体相比较,硬度更大的应该是________晶体,熔点较低的应是__________晶体。思路分析:根据氮化碳为高硬度材料且都由非金属元素组成,因此该晶体应为原子晶体,又C—C键键长大于C—N键键长,故碳氮键的键能大于C—C键,硬度更大的是氮化碳,熔点低的为金刚石。答案:依次为:原子、氮化碳、金刚石例2、氯化钠是比较典型的离子晶体,中学课本中已给出氯化钠的晶体结构示意图,假定各离子是相互接触的,试回答以下问题:(1)Na+与Cl-的半径比为________.(2)若ACl和BCl的晶体结构与NaCl相同且rA+>rNa+>rB+,则离子晶体的稳定性ACl______BCl。(填“大于”“小于”“等于”)思路分析:(1)依题可画出图。设Cl-的半径为1,则AC=4,AB=BC=2rNa++2,可求出rNa+=0.414(2)因rA+>rNa+>rB+由于B+与Cl-接触不好离子键相应减弱,故ACl的稳定性大于BCl.。答案:(1)0.414(2)大于三、练习题A组1.下列晶体中属于原子晶体的是( )A.氖 B.食盐 C.干冰 D.金刚石2.下列晶体由原子直接构成,且属于分子晶体的是( )A.固态氢 B.固态氖 C.磷 D.三氧化硫3.下列叙述中正确的是( )A.离子晶体中肯定不含非极性共价键B.原子晶体的熔点肯定高于其他晶体C.由分子组成的物质其熔点一定较低D.原子晶体中除去极性共价键外不可能存在其他类型的化学键4.下列晶体中不存在分子的是( )A.氯化钙 B.二氧化硅 C.二氧化碳 D.氖5.下列各组物质气化或熔化时,所克服的微粒间作用力完全相同的是( )A.碘的升华和干冰气化B.二氧化硅和干冰熔化C.苯和硝酸钾熔化D.食盐和冰熔化6.下列各晶体中,含有的化学键类型相同,晶体类型也相同的一组是( )A.SiO2和SO2B.CO2和H2OC.NaCl和HClD.CCl4和CH47.碳化硅这种结构类似于金刚石的晶体,其中碳原子和硅原子的位置是交替的。在下列三种晶体①金刚石②晶体硅 ③碳化硅中,它们的熔
原子晶体

知识拓展:混合型晶体-石墨 一种结晶形碳,有天然出产的矿物。 铁黑色至深钢灰色。质软具滑腻感,可沾 污手指成灰黑色。有金属光泽。六方晶系, 成叶片状、鳞片状和致密块状。密度 2.25g/cm3,化学性质不活泼。具有耐腐蚀 性,在空气或氧气中强热可以燃烧生成二 氧化碳。石墨可用作润滑剂,并用于制造 坩锅、电极、铅笔芯等。
两种结构?这两种结构各有什么特点?
思考与交流
比较CO2和SiO2 的一些物理性质和 结构,试判断SiO2 晶体是否属于分子 晶体。
物质 熔点
干冰 -56.6 ℃
石英 1710℃
沸点
-78.5 ℃ >1710℃
二、原子晶体
1、定义:原子间以共价键相结合而形成的 空间网状结构的晶体。
原子,没有单个分子存在,整个 2、构成微粒: 晶体可看成是一个“巨型分子”。
2
mol氢键?
②H2O的熔沸点比H2S高还是低?为 什么? 氢键 ③已知氢键也有方向性,试分析为什 么冬季河水总是从水面上开始结冰?
由于氢键的方向性,使晶体中每个水分子与四面体顶点 的4个分子相互吸引,形成空隙较大的网状体,密度比水 小,所以结的冰会浮在水面上
复习提问: 1、什么是分子晶体? 2、分子晶体通常具有什么样的物理性质? 3、典型的分子晶体有哪些? 4、分子晶体有哪两种结构?为什么会有这
109º 28´
共价键
常见晶体的结构
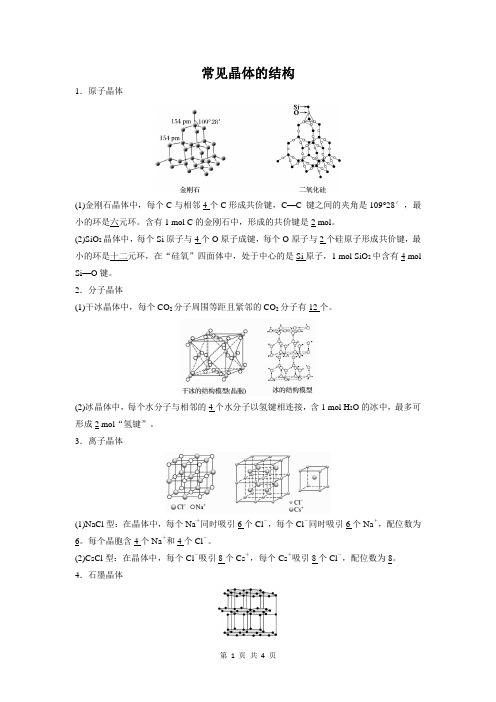
常见晶体的结构
1.原子晶体
(1)金刚石晶体中,每个C与相邻4个C形成共价键,C—C 键之间的夹角是109°28′,最小的环是六元环。含有1 mol C的金刚石中,形成的共价键是2 mol。
(2)SiO2晶体中,每个Si原子与4个O原子成键,每个O原子与2个硅原子形成共价键,最小的环是十二元环,在“硅氧”四面体中,处于中心的是Si原子,1 mol SiO2中含有4 mol Si—O键。
2.分子晶体
(1)干冰晶体中,每个CO2分子周围等距且紧邻的CO2分子有12个。
(2)冰晶体中,每个水分子与相邻的4个水分子以氢键相连接,含1 mol H2O的冰中,最多可形成2 mol“氢键”。
3.离子晶体
(1)NaCl型:在晶体中,每个Na+同时吸引6个Cl-,每个Cl-同时吸引6个Na+,配位数为6。每个晶胞含4个Na+和4个Cl-。
(2)CsCl型:在晶体中,每个Cl-吸引8个Cs+,每个Cs+吸引8个Cl-,配位数为8。4.石墨晶体
石墨层状晶体中,
层与层之间的作用是分子间作用力,平均每个正六边形拥有的碳原子个数
是2
,C原子采取的杂化方式是sp2。
5.金属晶体的四种堆积模型分析
堆积模型简单立方堆积体心立方堆积六方最密堆积面心立方最密堆
积
晶胞
配位数 6 8 12 12 原子半径(r)
和晶胞边长(a)的关系2r=a2r=
3a
22r=
2a
2
一个晶胞内
原子数目
1 2 2 4
常见金属Po() Na、K、Fe Mg、Zn、Ti Cu、Ag、Au
1.按要求回答问题:
(1)在金刚石晶体中最小碳环含有________个C原子;每个C原子被________个最小碳环共用。
原子晶体(公开课)

从下面表格中你能获取哪些信息?
某些原子晶体的熔点和硬度
原子晶体 金刚石 ( C ) 碳化硅 (SiC) 石英 (SiO2) 硅 ( Si )
熔点℃ 摩氏硬度
3550 10
2600 9
1710 7
1415 6.5
5. 原子晶体的物理特性
在原子晶体中,由于原子间以较强的共价键 相结合,而且形成空间立体网状结构,所以原子 晶体的 (1)熔点和沸点很高(耐高温)
C Si
结构与金刚石是一样 的空间网状结构。每个碳 原子与4个硅原子以共价键 相连,每个硅原子也与4个 碳原子以碳硅单键相连。 而晶体硅的结构和 金刚石的结构相似,只 是Si-Si的键长比C-C 的键长短而已。
109º 28´
共价键
问题探究
(四)
Si O
二氧化硅的晶体结构模型
180º
109º 28´
(1)从一个原 子分析,你能得 出什么结论?
(2)从相关联 的多个原子分 析,你能找出 结构中的特殊 结构吗?
三.金刚石的晶体结构
Fra Baidu bibliotek正四面体
①每个C原子 与 4 个碳原子 相连; 6 个碳 原子形成一 个 六 元环 ②晶体中C原 子与C-C键之 比 1:2 。
原子晶体---金刚石
金刚石晶胞
③每个晶胞中所含碳原子数: 8×1/8+6×1/2+4=8
原子晶体的定义

原子晶体的定义
原子晶体是一种经过精心构造的超复杂结构,它可以用结构单元相同或不同的原子来构成。由于原子晶体有着自身特殊的特性,它们用于表征各种物理现象,比如光学和热力学。
关于原子晶体的定义,可以从多个角度来考虑。首先,要考虑原子晶体的结构单元,原子晶体的结构单元可以是同类原子或不同类原子,比如金属原子晶体和氮化物原子晶体。在原子晶体的定义中,还要考虑空间结构的情况,原子晶体的结构单元之间存在着三维空间关系,这有助于精确描述物质的性质,比如金属原子晶体的电导性能和氮化物原子晶体的热导性性能等。
另外,还要考虑原子晶体的拓扑结构,原子晶体的拓扑结构指的是原子晶体中结构单元之间的关系,它可以划分为内部关系和外部关系。内部关系是指结构单元之间的相互之间的连接关系,比如,结构单元可以由相邻原子组成,原子之间会通过以下四种类型的关系相互连接:原子相邻、原子相连、原子中心碰撞、原子核碰撞。外部关系是指原子晶体中原子与晶体边界的关系,这些关系可以分成三类:边界原子与晶体内部原子之间的关系,晶体内部原子与周边环境之间的关系,以及晶体内部原子与外界电场之间的关系。
最后,原子晶体的定义还需要考虑晶体层次结构,原子晶体层次结构包括晶格结构、原子结构、电子结构和能量结构等,这些结构可以精确描述物质的性质,比如,电子结构可以描述物质的电子配置,而能量结构可以描述物质的能量状态。
总的来说,原子晶体的定义主要考虑原子晶体的结构单元、空间结构、拓扑结构和层次结构,它们共同构成了物质的性质,可以精确描述物质的性质,比如金属原子晶体的电导性能和氮化物原子晶体的热导性性能。
3.4原子晶体

小结:
(1)层状结构,最小碳环为平面正六边形,即为六 元环(在同一平面上)。 (2)每个碳原子为3个六元环所共有,每个C-C 键为2个六元环所共有。
(3)每个六元环中平均含有碳原子 =6×1/3=2
每个六元环中平均含有C-C键 =6×1/2=3 即碳原子数:C-C键键数 =2:3
金刚石与石墨的比较
金刚石具有很高的熔、 沸点和很大的硬度。你能 结合金刚石晶体的结构示 意图解释其中的原因吗?
• 由于金刚石晶体中所有原子都是通过共价 键结合的,而共价键的键能大,如C-C 键的键能为348kJ· mol-1。所以金刚石晶体 熔、沸点很高,硬度很大。
知识回顾
一. 原子晶体 1、定义:相邻 原子间通过 共价键 结合而 成的具有 空间网状 结构的晶体 2、组成微粒: 原子 3、微粒间作用力: 共价键
练
金刚石 熔点 沸点 硬度 >3823 5100 10 晶体硅 1683 2628 7.0
习
晶体硼 2573 2823 9.5
5.单质硼有无定形和晶体两种,参考下表数据
原子 ①晶体硼的晶体类型属于____________ 晶体,理由是 ________________________ 熔点高、硬度大 。 已知晶体硼结构单元是由硼原子组成的正二十面体, 其中有20个等边三角形的面和一定数目的顶点,每个项点上 各有1个B原子。通过视察图形及推算,此晶体体结构单元由 ______ 12 个硼原子构成。其中B—B键的键角为_______ 60° 。共含有 _______ 30 个B—B
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
SiO2晶体
空间网状、共价键
原子晶体
1.概念: 原子间以共价键相结合而形成的 空间立体网状结构的晶体。 2. 构成微粒: 原子 3. 作用力: 共价键
思考:为什么原子晶体熔沸点高?
原子晶体熔化破坏的是共价键。
一般的,原子间键长越短,键能越大,共价 键越稳定,物质的熔沸点越高,硬度越大。
练习:
比较SiC、金刚石、晶体硅的熔点大小 4.原子晶体的判断方法 方法一:晶胞结构 方法二:物质类别 方法三:物理性质 熔沸点很高,硬度很大,难溶于一般溶剂
对比分子晶体和原子晶体的物理参数
练习:
分析下列物质的物理性质,判断其晶体类型:
A、碳化铝,黄色晶体,熔点2200℃,熔融态 不导电;________________ B、溴化铝,无色晶体,熔点98 ℃,熔融态不 导电;________________ C、五氟化钒,无色晶体,熔点19.5℃,易溶 于乙醇、氯仿、丙酮中;_______________ D、物质A,无色晶体,熔融时或溶于水中都能 导电_____________
[讨论]
③12克金刚石中,含 C—C键数为( 2 ) NA
④每个C—C键被 ( 6 )个六元环共有。
金刚石晶胞
⑤每个C原子被 12 个六元环共有?
C42 ×2 =12
晶体Si
晶体SiO2
SiO2晶胞
【讨论】
晶体SiO2
①在SiO2晶体中,每个Si 原子与 4 个O原子结合, 构成空间正四面体结构, Si位于四面体中心,O 位 于四面体顶点;
Thanks!
②在SiO2晶体中,Si原子与O原 子个数比为( 1:2 )
③在SiO2晶体中,最小 的环为( 6 )个Si和( 6 )个 O组成的( 十二元 )环。
④晶体中的最小环为
晶体SiO2
十二元环,含有 12 个 Si-O键;每个Si-O键被 6 个十二元环共有.
⑤每个O原子被 6 个十二元环共有,
每个Si原子被 12 个十二元环共有.
5.常见原子晶体的结构模型:
碳原子采取 SP3 杂化,每 5 个碳原子形成正四面体
键角: 109 º28´ 键长: 0.155nm
金刚石晶胞
[讨论]
①在金刚石晶体中, 每个C与( 4 )个C成 键 ,形成( 正四面体 ) 结构;最小碳环由 ( 6 )个C原子组成且 六原子( 不在 )同一 平面内. ②在金刚石晶体中,C原子个数 与C—C键数之比为( 1:2 )
3.下列各组物质中,按熔点由低到高排列正确的 是 ( B)
(A)O2、H2、Hg (B)CO2、KCl、SiO2 (C)Na、K、Rb (D)SiC 、NaCl、SO2 4.下列晶体熔化时化学键没有被破坏的是(BC ) (A)NaCl (B)冰 (C)白磷 (D)SiO2
(1) 已知晶体硼的基本结构单 元是由硼原子组成的正二十面体 (如图),其中有20个等边三角 形的面和一定数目的顶点,每个 顶点上各有一个硼原子。通过观 察图形及推算此基本结构单元① 键角____;②含有的硼原子数 ____个;③B—B键____条。 (2) 把晶体硼的几何图形作一 定的规范切削:把每个顶点均匀 割掉,可得出化学上与某物质相 似的几何外形,新得到的规则几 何图形中有_______个正六边形, 有___________个正五边形。
原子晶体
复习提问:
1.典型的分子晶体有哪些?
2.分子晶体的物理性质? 3.分子晶体中粒子的堆积方式如何?
教学目标:
知识与技能:
1.掌握原子晶体的判断方法
2.会看典型原子晶体的晶胞结构 过程与方法: 图示 讲解 情感态度与价值观 晶胞结构是考试的重点。
问题反馈:
原子晶体中各种环怎么数?
干冰
分子密堆积、范德华力
为何CO2熔沸点低?而破坏 CO2分子却比SiO2更难?
因为CO2是分子晶体,SiO2是原子晶体, 所以熔化时CO2是破坏范德华力而SiO2是破坏 化学键,所以SiO2熔沸点高。 而破坏CO2分子,都是破坏共价键,而 C—O键能>Si-O键能,所以CO2分子更稳定。
1.下列各组物质的晶体中,化学键类型相同,晶 体类型也相同的是 ( B ) (A)SO2 和 SiO2 (B) CO2 和 H2O (C) NaCl 和 HCl (D)CCl4 和 KCl 2.下列各组物质气化或熔化时,所克服的微粒间 的作用(力),属同种类型的是 ( AD ) (A)碘和干冰源自文库升华 (B) 二氧化硅和生石灰的熔化 (C)氯化钠和铁的熔化 (D)水和四氯化碳的蒸发
