江苏省2016届中考化学复习讲练:第13课时溶液的酸碱性
初中化学《溶液的酸碱性》精品教案

第一节溶液的酸碱性学习目标:知识与技能目标:1、认识溶液的酸碱性,了解酸碱度指示剂的颜色变化情况2、学会利用酸碱指示剂判断溶液的酸碱性过程与方法目标:通过理解溶液的酸碱性和 PH 的关系,学会利用 PH 试纸测定溶液酸碱度的方法。
情感、态度与价值观目标:了解溶液的酸碱性与生命活动的关系,树立用化学方法保护人体健康和防治污染的意识。
重点:认识溶液的酸碱性,酸碱度及其测定方法。
难点:溶液的酸碱性与酸碱度的区别及联系教法:实验探究法,归纳法教具:实验器材及药品、多媒体器材及课件课时分配: 2 课时第一课时:酸性溶液和碱性溶液第二课时:溶液酸碱性的强弱程度及与生命活动的关系。
第一节溶液的酸碱性[引入]:昨天我在报上看了一篇题为《百病之源;酸性食物过量》的报道,据说人体的酸性化是百病之源,当酸性物质在体内愈来愈多,不断规程,当量变引起质变时疾病就会产生。
医学证明,如果人体倾向酸性,人体细胞的作用就会变差,废物就不易排出,肾脏、肝脏的负担就会加大,新陈代谢缓慢,各种器官的功能减弱,容易得病,为此专家推存食用碱性食品。
那么什么是酸性?什么是碱性?本节课我们通过实验来共同探究。
[ 过渡 ] :日常生活中,有哪些物质给你留下过“酸”的印象,或“碱”的印象?谁能说一下?[ 学生 ] 讨论、交流生:食醋是酸的,橘子是酸的,没熟透的苹果是酸的。
师:还有吗?准还有,说出来与大家共同分享。
这些酸的印象都是通过你的日常生活品尝到的。
师:在通常情况下,是不允许品尝化学试剂的味道的,那么我们怎样才能确定物质的酸性或碱性呢?下面我给大家做一个实验。
师:化学魔术:往月季花花上喷洒白醋,观察现象,并提出问题:这是为什么呢?谁能给大家解释一下。
生:讨论、交流师:启发思考,在《奇妙的二氧化碳》一节中,我们曾做过一个实验,把二氧化碳气体通入紫色的石蕊试液中,观察到的现象是什么?由此,我们得出的结论是什么?生:紫色石蕊试液变红,原因是二氧化碳与水反应生成的碳酸,能使石蕊试液变红。
初三化学溶液的酸碱性讲义练习

本次课课堂教学内容一、要点复习1.酸性溶液不一定是酸溶液,碱性溶液不一定是碱溶液。
例如:碳酸钠(Na2CO3)属于盐类但其溶液显碱性,硫酸铜(CuSO4)属于盐类,但其溶液显酸性。
2.酸性、碱性溶液使酸碱指示剂变色,变色的是指示剂而不是酸性、碱性溶液。
二、内容讲解知识点1 酸性溶液和碱性溶液1,酸性:能使紫色石蕊试液变红的溶液,表现为酸性2,碱性:能使紫色石蕊试液变蓝的溶液,表现为碱性3,中性:不能使紫色石蕊试液变色,呈中性知识点2 酸碱指示剂1.酸碱指示剂(简称:指示剂):能跟酸或碱的溶液起作用而显示不同的颜色。
常见的有:石蕊溶液、酚酞溶液。
2.变色规律:石蕊溶液遇酸性溶液变成红色,遇碱性溶液变成蓝色。
酚酞溶液遇酸性溶液不变色,遇碱性溶液变成红色。
3.二氧化碳通入紫色的石蕊试液中,(1)溶液由紫色变成红色。
(2)二氧化碳溶于水生成了碳酸,是碳酸改变了溶液的颜色。
4.用酸碱指示剂检验溶液的酸碱性的方法:(1)取少量该溶液,滴入几滴石蕊试液,若溶液呈现红色,则说明该溶液为酸性溶液。
(2)取少量该溶液,滴入几滴石蕊试液,若溶液呈现蓝色;或者滴入几滴无色的酚酞试液,若溶液呈现红色,则说明该溶液为碱性溶液。
典例分析1.二氧化碳的水溶液(含碳酸)、白醋、酸果汁等物质能使紫色石蕊试液变红,表现出酸性;2.纯碱溶液、肥皂水、石灰水、氨水等溶液能使紫色石蕊试液变蓝,这些溶液显碱性3.食盐水、蔗糖水等溶液不能使紫色石蕊试液变色,既不具有酸性,也不具有碱性,显中性。
知识点3溶液酸碱性强弱1.溶液的酸碱度常用pH来表示,pH范围通常在0~14之间。
pH<7 溶液呈酸性;pH>7 溶液呈碱性;pH=7 溶液呈中性。
PH越小酸性越强,pH越大碱性越强。
2. pH的测定:用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)【典型例题】1.下列“水”能使无色酚酞试液变红的是( )A.氨水B.汽水C.冰水D.糖水2.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )A.食盐B.味精C.食醋D.香油3.下列物质能使紫色石蕊试液变红的是( )A.肥皂水B.氨水C.酸果汁D.食盐水4.把生石灰、二氧化碳、食盐分别溶于水,往它们的溶液里分别滴入紫色石蕊试液,试液呈现的颜色依次是( )A.蓝色、红色、紫色B.红色、无色、蓝色C.无色、蓝色、紫色D.紫色、蓝色、红色5.小明在一次晚会上表演了一个小魔术:他向事先做好的白花上喷一种无色试液后,白花变成了鲜艳的红花。
中考化学专题练习 溶液的酸碱性1(含解析)

溶液的酸碱性一、选择题1.下列溶液,能使无色酚酞试液变红的是()A.石灰水B.食盐水C.食醋 D.汽水2.酸溶液能使紫色石蕊试剂变红,是因为酸溶液中含有()A.氢离子B.氢分子C.酸根离子 D.酸分子3.柠檬汁能使石蕊试液变红色,由此可知柠檬汁()A.显酸性B.显碱性C.显中性D.无法确定4.向某一未知溶液中滴加几滴酚酞试液,酚酞试液变为红色,则该溶液()A.呈中性B.呈酸性C.呈碱性D.是碱溶液5.人体内的一些液体的正常pH范围如下表,正常情况下,这些液体中一定呈酸性的是()A.胃液 B.血浆 C.乳汁 D.唾液6.大致测定某溶液是酸性还是碱性,要采取()①石蕊试液②酚酞试液③石蕊试纸④pH试纸.A.只有①② B.只有①②③C.只有①④ D.以上都可以7.下列物质放入或通入水中,能使pH增大的是()A.NaCl B.白醋 C.干冰 D.生石灰8.下列物质溶于水,所得溶液的pH大于7的是()A.CO2B.HCl C.NaCl D.Ca(OH)2二、填空题9.酸碱指示剂只能指示溶液的而不能测定溶液的,溶液的酸碱度用来表示,其范围一般在之间.测溶液酸碱性的强弱程度可用.pH值越小,其酸性越;pH越大,碱性越.测定溶液pH的方法是.10.测定pH值最简单的方法是使用.测定时,用蘸取待测溶液,滴在上,然后再与对照,便可测出溶液的pH值.若用此法测得土壤的pH值小于5,可以施用适量的来改良土壤.溶液的酸碱性参考答案与试题解析一、选择题1.下列溶液,能使无色酚酞试液变红的是()A.石灰水B.食盐水C.食醋 D.汽水【考点】酸碱指示剂及其性质.【专题】常见的碱碱的通性.【分析】根据已有的知识进行分析,能使酚酞试液变红的溶液呈碱性.【解答】解:使酚酞变红的是碱性的物质的溶液.A.石灰水呈碱性,故正确;B.石灰水呈中性,故错误;C.食醋呈酸性,故错误;D.汽水中含有碳酸,呈酸性,故错误.故选A.【点评】本题考查了酸碱指示剂的性质,完成此题,可以依据已有的课本知识进行,要求同学们加强基础知识的储备,以便灵活应用.2.酸溶液能使紫色石蕊试剂变红,是因为酸溶液中含有()A.氢离子B.氢分子C.酸根离子 D.酸分子【考点】物质的微粒性;酸的化学性质.【专题】结合课本知识的信息.【分析】可以根据酸的概念进行分析、考虑,从而得出正确的结论.【解答】解:电离时生成的阳离子全部是氢离子的化合物是酸.酸溶液能使紫色石蕊试剂变红,是因为酸溶液中含有氢离子.观察选项,故选A.【点评】本题主要考查了酸具有酸性的实质,完成此题,可以依据酸的定义进行.3.柠檬汁能使石蕊试液变红色,由此可知柠檬汁()A.显酸性B.显碱性C.显中性D.无法确定【考点】酸碱指示剂及其性质;溶液的酸碱性与pH值的关系.【专题】物质的变化与性质.【分析】根据已有的知识进行分析,石蕊试液遇酸变红.【解答】解:石蕊试液遇酸变红,观察选项,故选A.【点评】根据石蕊试液的变色进行.4.向某一未知溶液中滴加几滴酚酞试液,酚酞试液变为红色,则该溶液()A.呈中性B.呈酸性C.呈碱性D.是碱溶液【考点】酸碱指示剂及其性质.【专题】常见的酸酸的通性.【分析】根据已有的知识进行分析,酚酞试液在酸性和中性溶液中不变色,在碱性溶液中变红,据此解答.【解答】解:碱性溶液能使无色的酚酞试液变红色,但是该溶液不一定是碱的溶液,如碳酸钠溶液能使无色酚酞变红色,但是不是碱溶液.故选:C.【点评】本题考查了溶液的酸碱性与指示剂的变色的知识,完成此题,可以依据已有的知识进行.5.人体内的一些液体的正常pH范围如下表,正常情况下,这些液体中一定呈酸性的是()A.胃液 B.血浆 C.乳汁 D.唾液【考点】溶液的酸碱性与pH值的关系.【专题】结合课本知识的信息.【分析】根据已有的知识进行分析,酸性溶液的pH小于7,据此解答.【解答】解:A、胃液的pH为0.9~1.5,小于7,呈酸性,故A正确;B、血浆的pH为7.35~7.45,大于7,呈碱性,故B错误;C、乳汁的pH为6.6~7.6,接近中性,故C错误;D、唾液的pH为6.6~7.1,接近中性,故D错误;故选A.【点评】本题考查了溶液的酸碱性与pH的关系,完成此题,可以依据已有的知识进行.6.大致测定某溶液是酸性还是碱性,要采取()①石蕊试液②酚酞试液③石蕊试纸④pH试纸.A.只有①② B.只有①②③C.只有①④ D.以上都可以【考点】探究酸碱的主要性质.【专题】课本知识同类信息.【分析】做好此题要了解紫色石蕊试液和无色酚酞试液遇酸碱后的不同变化;以及石蕊试纸和PH试纸遇酸碱的变化.【解答】解:紫色石蕊试液遇酸性溶液变红,遇碱性溶液变蓝;无色的酚酞试液遇酸性溶液不变色,遇碱性溶液变红;酸性溶液使蓝色石蕊试纸变红,碱性溶液使红色石蕊试纸变蓝;PH试纸遇到酸性溶液呈红色,遇到碱性溶液呈蓝色.也就是说①②③④都可用来检验溶液的酸碱性.故选D.【点评】本题考查常用的酸碱指示剂及其使用,使学生了解酸碱指示剂的正确使用.7.下列物质放入或通入水中,能使pH增大的是()A.NaCl B.白醋 C.干冰 D.生石灰【考点】溶液的酸碱性与pH值的关系;二氧化碳的化学性质;碳酸钙、生石灰、熟石灰之间的转化.【专题】物质的变化与性质.【分析】根据溶液的pH值与溶液的酸碱性的关系来判断,当溶液的pH等于7时,呈中性.当溶液的pH大于7时,呈碱性.当溶液的pH小于7时,呈酸性.【解答】解:A、氯化钠是中性的物质其pH值为7,和水的相等,故A错B、白醋是酸性的物质,其pH小于7,加入水中后会使pH降低,故B错C、干冰是二氧化碳的固态,能够溶于水,生成碳酸,pH小于7,从而使pH降低,故C错D、生石灰可以和水反应生成氢氧化钙,氢氧化钙溶于水后使溶液pH大于7,使溶液的pH增大,故D对故选D【点评】掌握溶液的酸碱性和溶液pH大小之间的关系,然后再根据具体物质的水溶液的酸碱性进行分析、判断,从而得出正确的结论.8.下列物质溶于水,所得溶液的pH大于7的是()A.CO2B.HCl C.NaCl D.Ca(OH)2【考点】溶液的酸碱性与pH值的关系.【专题】常见的酸酸的通性.【分析】当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;据此结合常见化学物质的酸碱性进行分析判断即可.【解答】解:A、CO2与水反应生成碳酸,碳酸显酸性,pH小于7,故选项错误.B、HCl溶于水形成盐酸,盐酸显酸性,pH小于7,故选项错误.C、NaCl溶于水形成氯化钠溶液,氯化钠溶液显中性,pH等小于7,故选项错误.D、Ca(OH)2溶于水形成氢氧化钙溶液,氢氧化钙溶液显碱性,pH等大于7,故选项正确.故选:D.【点评】本题难度不大,掌握常见化学物质的酸碱性、溶液的酸碱性和溶液pH大小之间的关系是顺利解题的关键.二、填空题9.酸碱指示剂只能指示溶液的酸碱性而不能测定溶液的酸碱度,溶液的酸碱度用pH 来表示,其范围一般在0~14 之间.测溶液酸碱性的强弱程度可用pH试纸.pH值越小,其酸性越强;pH越大,碱性越强.测定溶液pH的方法是用玻璃棒蘸取溶液滴在pH试纸上,再与标准比色卡对照即可测出溶液的pH .【考点】酸碱指示剂及其性质;溶液的酸碱度测定;溶液的酸碱性与pH值的关系.【专题】结合课本知识的信息.【分析】可以根据溶液的酸碱性、酸碱度、测定溶液酸碱度的方法等方面进行分析、判断,从而得出正确的结论.【解答】解:酸碱指示剂只能指示溶液的酸碱性而不能测定溶液的酸碱度.故填:酸碱性;酸碱度.溶液的酸碱度用PH来表示,其范围一般在 0~14之间.测溶液酸碱性的强弱程度可用PH试纸.pH 值越小,其酸性越强;pH越大,碱性越强.故填:PH;0~14;PH试纸;强;强.测定溶液pH的方法是:用玻璃棒蘸取溶液滴在pH试纸上,再与标准比色卡对照即可测出溶液的pH.【点评】解答本题时要掌握溶液酸碱性、酸碱度的含义和测定溶液酸碱度方面的知识,只有这样才能对问题做出正确的判断.10.测定pH值最简单的方法是使用pH试纸.测定时,用玻璃棒蘸取待测溶液,滴在pH 试纸上,然后再与标准比色卡对照,便可测出溶液的pH值.若用此法测得土壤的pH值小于5,可以施用适量的熟石灰或消石灰Ca(OH)2来改良土壤.【考点】溶液的酸碱性测定;中和反应及其应用.【专题】实验性简答题.【分析】依据正确的测定溶液pH的方法解题;pH<7溶液呈酸性,可用加弱碱性物质(如熟石灰)的方法改良.【解答】解:测定溶液pH的具体操作方法为:用干净的玻璃棒蘸取待测溶液并滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出相同颜色的pH值;pH值小于5的溶液显酸性,这样的土壤可用加熟石灰的方法改良.答案:pH试纸;玻璃棒;pH试纸;标准比色卡;熟石灰或消石灰Ca(OH)2【点评】本题考查pH的测定方法,掌握正确的测定pH的操作方法是解题的关键.。
溶液的酸碱性说课稿

通过小故事引 入用pH表示 溶液酸碱度。 激发学生的学
习兴趣,并且
科学是为生产
生活服务的。
也帮助学生理 解记忆pH的 表示范围
在后面溶液酸 碱性测定的内 容中交流问题 中,学生能很 快的说出不用 pH试纸测定 所有的溶液原 因之一是浓度 问题,
第十一页,课件共17页
3、学习溶液酸碱性与pH (25 ℃ )
初中化学,已经了介绍溶液酸碱性与PH的关系的但并不准确,容易造成 思维固化,造成学习的过程中有一定的困难。
第四页,课件共17页
三、教学目标
据新课标评价建议及教要求,结合本教材的内容及学生特点,教学目标确定如下:
知识与技能
过程与方法
情感态度
价值观
弄清溶液酸碱性与溶 液中c(H+)、 c(OH-) ,pH关系 ,掌握常
液
性
mol/L
mol/L
比较
H●Cl
NaCl NaOH
酸性 中性 碱性
0.01
10-7
10-12 10-7
10-12 0.01
c(H+)>c(OH¯) c(H+)=c(OH¯)
c(H+) ﹤c(OH¯)
学生能熟练计算出 c(H+)、 c(OH-)的大小
, 通过对典型例
题的计算,分析 数据,学生直观 的感受溶液酸碱性
c(OH-)分别是多少?
通过提问的
方法,帮助学 生回忆相关知 识。建立由已 知到未知联系
学生积极回
答问题,热情 度高,增强了 学习信心,通 过课堂实践, 学生更快的完 成了第一部分 的学习
第九页,课件共17页
2、探究溶液酸碱性与c(H+)、c(OH¯)的关系,结合数据证明
中考化学知识点习题溶液的酸碱性

D.
石灰水
10、有 A、B、C 三种溶液, A 能使紫色石蕊试液变红, B 能使无
色酚酞试液变红, C 遇紫色石蕊试液和无色酚酞试液均无变化,
则三种溶液的 pH 由大到小的顺序是
()
A.A >C>B
B.C> B>A
C.B>A > C
D.B >C> A
二、填空题( 16 分 )
1、检验溶液的酸碱性可以用
和
两种常用
的酸碱指示剂; 还可以用蓝色石蕊试纸或红色石蕊试纸来检验。 蓝色
石蕊试纸遇到
性溶液能变红, 红色石蕊试纸遇到
性溶液变
蓝色。
2、位于美国富兰克林的小依科庞德湖,湖水的 pH 为 4.2,是世界上
性最强的湖。 该湖水是否适宜一般作物的灌溉
。( “是 ”
或 “否”)
3、溶液的酸碱度用 pH 来表示,pH 的范围通常在
D.白醋
5、某些食物的近似 pH 为:牛奶 6.3~6.6,葡萄 3.5~4.5,玉米粥 6.8~
8.0,苹果 2.9~3.3,其中酸性最强的是
()
A .葡萄
B.牛奶
C.苹果
D.玉米粥
6、用 pH 试纸测量碱溶液的 pH 时,若事先将 pH 试纸用蒸馏水润湿,
则测量结果会(
)
A.偏大
B.偏小
C.不变
① pH 试纸
②紫色石蕊试液
③酚酞试
液
组内同学进行了 如下实验:
甲同学:取 pH 试纸放在玻璃片上, 用玻璃棒蘸取氯化钠溶液沾在 pH
试纸上,把试纸显示的颜色与标准比色卡比较,测得 pH=7。
乙同学:取 pH 试纸放在玻璃片上,先用蒸馏水将 pH 试纸湿润,然 后用玻璃棒蘸取氯化钠溶液沾在 pH 试纸上,把试纸显示的颜色与标 准比色卡比较,测得 pH=7。 丙同学:将 pH 试纸直接浸入氯化钠溶液中,把试纸显示的颜色与标 准比色卡比较,测得 pH=7。 [ 评价 ] 三位同学中操作规范的是 _____________同学。指出其余同学 操作上的错误
初三化学溶液的酸碱性

初三化学溶液的酸碱性一. 本周教学内容:溶液的酸碱性二. 教学目标1、知道一些常见物质水溶液的酸碱性;2、知道酸碱指示剂,并学会用酸碱指示剂来检验溶液的酸碱性;3、了解酸碱度的表示方法;4、掌握pH和溶液酸碱性的关系,学会用pH试纸测定溶液的酸碱性和酸碱度;5、溶液酸碱性对生命活动和农作物生长的影响。
重点:1、溶液酸碱性及其检验和酸碱度的判断及测定;2、酸碱性和生产、生活的关系。
难点:溶液酸碱性对生命活动和农作物生长的影响。
三. 具体内容1、酸性溶液和碱性溶液(1)溶液的酸碱性有酸味的物质,且能使紫色石蕊试液变红色,这种溶液显酸性;能使紫色石蕊试液变蓝色,这种溶液显碱性;不能使紫色石蕊试液变色,这种溶液显中性。
(2)酸碱指示剂能检验溶液酸碱性的试液。
常用的酸碱指示剂:紫色石蕊试液;酚酞试液。
指示剂的颜色变化:酸性碱性中性紫色石蕊试液红蓝紫无色酚酞试液无红无酸性溶液——使蓝色石蕊试纸变红;碱性溶液——使红色石蕊试纸变蓝。
2、酸、碱性的强弱用pH表示酸碱性的强弱。
(1)pH的意义:用来表示溶液的酸、碱性强弱程度。
(2)pH的范围:0~14。
(3)溶液的酸碱度与pH的关系:酸碱性的确定酸碱度的比较pH=7溶液呈中性pH<7溶液呈酸性pH越小,酸性越强pH>7溶液呈碱性pH越大,碱性越强(4)测定方法:用pH试纸。
(5)pH的改变。
3、溶液酸碱性与生命活动的关系(1)溶液酸碱性与人体健康的关系;(2)溶液酸碱性与农作物生长的关系。
【典型例题】例1、下列能正确表示加水稀释pH=10的溶液的是()答案:D例2、某些植物的花汁可作酸碱指示剂。
取三种花汁用稀酸溶液或稀碱溶液检验,颜色如下:花种类花汁在酒精(中性)中颜色花汁在稀酸中颜色花汁在稀碱中颜色玫瑰花粉红粉红绿万寿菊花黄黄黄大红花粉红橙绿试回答下列问题:(1)为试验生活中的食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,我选择花汁,不选用其他花汁的原因是。
初三化学溶液的酸碱性

A、汽水B、自来水C、肥皂水D、食醋4、苯甲酸()可用做食品防腐剂,其酸性比醋酸强。
下列对苯甲酸性质的推测不合理的是()A.苯甲酸溶液的pH小于7B.苯甲酸溶液的pH大于 7C.苯甲酸溶液能使紫色石蕊试液变红色D.苯甲酸溶液不能使无色酚酞试液变色5、例1 一些食物的pH如下,其中碱性最强的是()A.苹果 2.9~3.3 B.牛奶 6.3~6.6C.鸡蛋清 7.6~8.0 D.番茄 4.0~4.46、不用其他试剂,可以鉴别石蕊、盐酸、氢氧化钙、氢氧化钠、碳酸钠五种溶液,第二个被鉴别出来的物质是()A.盐酸B.氢氧化钙C.氢氧化钠D.碳酸钠7、一些食物的近似PH如下表:食物苹果葡萄牛奶玉米粥pH 2.9~3.3 3.5~4.5 6.3~6.6 7.2~8.0人的胃液中含有盐酸,对于胃酸过多的人,空腹时最适宜使用上述食物中的A.苹果 B.葡萄 C.牛奶 D.玉米粥8、下列反应,要借助酸碱指示剂才能判断二者是否发生反应的是A.大理石和稀盐酸 B.石灰水和稀盐酸C.铁锈和稀硫酸D.镁和稀硫酸9、下图是一些物质的pH,酸碱性最接近中性的是A.苹果汁(2.9~3.3)B.番茄汁(4.04~4.4)C.玉米粥(6.88~7.1)D.肥皂水(9.8~10.2)10、下列物质中.pH最小的是;A.食盐水 B.纯净水C.食醋 D.石灰水11、下列数据是常见物质的pH范围,其中酸性最强的是A.瓶装饮用水 (6.5~7.5) B.番茄汁(4.0~4.4)C.柠檬汁(2.0~3.0) D.液体肥皂(9.5~10.5)12、用一种试剂一次就能将澄清石灰水、氢氧化钠溶液、稀盐酸三种无色溶液区分开来的是A.紫色石蕊试液 B.稀硫酸C.氢氧化钡溶液 D.碳酸钠溶液二、多项选择13、一些国家正在试用碳酸水浇灌某些植物,其作用是()A.调节土壤的pH,改良酸性土壤B.调节土壤的pH,改良碱性土壤C.促进植物的光合作用D.在植物上方形成温室三、简答题1.2003年6月某校环保小组监测到一个造纸厂仍在向淮河排放无色碱性污水。
初中化学溶液的酸碱性知识点与习题(含答案)
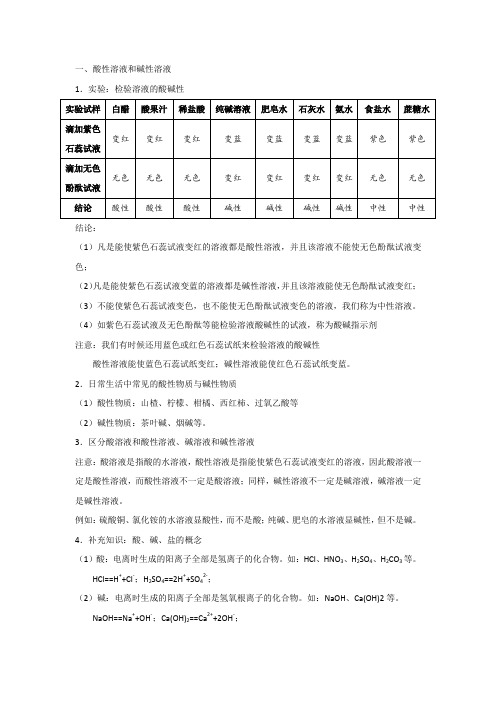
一、酸性溶液和碱性溶液1.实验:检验溶液的酸碱性结论:(1)凡是能使紫色石蕊试液变红的溶液都是酸性溶液,并且该溶液不能使无色酚酞试液变色;(2)凡是能使紫色石蕊试液变蓝的溶液都是碱性溶液,并且该溶液能使无色酚酞试液变红;(3)不能使紫色石蕊试液变色,也不能使无色酚酞试液变色的溶液,我们称为中性溶液。
(4)如紫色石蕊试液及无色酚酞等能检验溶液酸碱性的试液,称为酸碱指示剂注意:我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性酸性溶液能使蓝色石蕊试纸变红;碱性溶液能使红色石蕊试纸变蓝。
2.日常生活中常见的酸性物质与碱性物质(1)酸性物质:山楂、柠檬、柑橘、西红柿、过氧乙酸等(2)碱性物质:茶叶碱、烟碱等。
3.区分酸溶液和酸性溶液、碱溶液和碱性溶液注意:酸溶液是指酸的水溶液,酸性溶液是指能使紫色石蕊试液变红的溶液,因此酸溶液一定是酸性溶液,而酸性溶液不一定是酸溶液;同样,碱性溶液不一定是碱溶液,碱溶液一定是碱性溶液。
例如:硫酸铜、氯化铵的水溶液显酸性,而不是酸;纯碱、肥皂的水溶液显碱性,但不是碱。
4.补充知识:酸、碱、盐的概念(1)酸:电离时生成的阳离子全部是氢离子的化合物。
如:HCl、HNO3、H2SO4、H2CO3等。
HCl==H++Cl-;H2SO4==2H++SO42-;(2)碱:电离时生成的阳离子全部是氢氧根离子的化合物。
如:NaOH、Ca(OH)2等。
NaOH==Na++OH-;Ca(OH)2==Ca2++2OH-;(3)盐:电离时生成金属离子(或铵根离子)和酸根离子的化合物。
如:NaCl、NH4NO3等。
NaCl==Na++Cl-;NH4NO3==NH4++NO3-;二、溶液的酸碱性的强弱程度1.酸碱度:用来表示溶液的酸性或碱性的强弱程度。
2.pH试纸用来定量的测定溶液的酸碱度。
pH值1 2 3 4 5 6 7 8 9 10 11 12 13 14|酸性增强中性碱性增强溶液的pH值与酸碱性关系pH=7,溶液呈中性;pH<7,溶液呈酸性,pH越小,酸性越强;pH>7,溶液呈碱性,pH越大,碱性越强3.pH试纸的使用方法;用胶头滴管(或玻璃棒)把待测试液滴(或涂)在pH试纸上,然后把试纸显示的颜色(半分钟内)与标准比色卡对照,标准比色卡上相同颜色的pH即为该溶液的pH。
初中化学溶液的酸碱性

初中化学溶液的酸碱性
1、显酸性的溶液:酸溶液和某些盐溶液(硫酸氢钠、硫酸氢钾等)
2、显碱性的溶液:碱溶液和某些盐溶液(碳酸钠、碳酸氢钠等)
3、显中性的溶液:水和大多数的盐溶液
(一)质量增加的
1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸;
2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜;
3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙;
(二)质量减少的
1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水;
2、由于风化而减少的:碳酸钠晶体。
九下化学《溶液的酸碱性》

【思考2】
把pH试纸直接浸入到待测液中,这种操 作是否正确?
【结论】
把pH试纸直接浸入到待测液中,溶液会 被污染。
学习了溶液酸碱度的表示方法,不仅能
工厂排出的烟尘污染空气
测量雨水的pH,以监测酸雨的产生。正常雨 水pH约为5.6,因为溶有二氧化硫。酸雨的 pH小于5.6
什么叫酸雨?酸雨有什么危害?
通常的雨水因溶有空气中的二氧化碳而略显 酸性,无危害。当人类排放的二氧化硫等气体过 多时,就易形成pH小于5.6的酸性降水,称之为 酸雨。酸雨对很多植物的生长不利,影响水生生 物的生长,也危害人们的健康。
月季花 美人焦
牵牛花 胡萝卜
自 紫萝卜 制
指 导 剂 原 料
紫包菜
实验探究 几种植物花朵的酒精浸出液在酸碱溶液中的变色情况
代用指导剂
酸性溶液中的 颜色变化
中性溶液 中的颜色
碱性溶液中的 颜色变化
牵牛花 变红色
紫色
变蓝色
月季花 浅红色
红色
变黄色
美人蕉 淡红色
红色
变绿色
紫心萝卜 变红色
紫色
黄绿色
紫卷心菜 浅紫色
【课堂练习】
【题1】某溶液的 pH =3,则该溶液( A)
A. 呈酸性 B. 呈碱性 C. 呈中性 D. 无 法判定
【题2】已知苹果汁的近似 pH 为2.9~3.3, 在苹果汁中滴入紫色石蕊试液,显示的 颜色是( )B
A. 无色 色
B. 红色 C. 蓝色 D. 紫
4.pH的测定——用pH试纸测定
九年级化学溶液的酸碱性

实验指导(4) 在试管中分别加入少量的食醋、盐酸。向
其中滴加酚酞试液,仔细观察实验现象。
实验指导(5) 在试管中分别加入少量的纯碱溶液、氢氧
化钠溶液。向其中滴加酚酞试液,仔细观察实 验现象。
实验指导(6) 在试管中分别加入少量的蒸馏水、食盐水。
向其中滴加紫色石蕊溶液,仔细观察实验现象。
石蕊的颜色
食醋、盐酸
纯碱、氢氧化钠 溶液 蒸馏水、食盐水
由紫变红 由紫变蓝 紫色
溶液显 酸性
溶液显 碱性
溶液显 中性
比壮观的景象出现了,随着垄断和寒潮的高速碰撞!翻滚狂舞其中的所有物体和碎片都被撞向十几万米的高空,半空中立刻形成一道杀声震天、高速上升的巨幕,双方 的斗士一边快速上升一边猛烈厮杀……战斗结束了,校霸们的队伍全军覆灭,垂死挣扎的火舌明唇怪如同蜡像一样迅速熔化……双方斗士残碎的肢体很快变成金币和各 种各样的兵器、珠宝、奇书……纷纷从天落下!这时由女无赖契温娆嘉妖女和另外四个校霸怪又从地下钻出变成一个巨大的核桃妙尾怪!这个巨大的核桃妙尾怪,身长 二百多米,体重七十多万吨。最奇的是这个怪物长着十分古朴的妙尾!这巨怪有着纯红色假山形态的身躯和暗红色细小原木一般的皮毛,头上是暗橙色篦子般的鬃毛, 长着亮蓝色奶酪形态的柱子粗布额头,前半身是鲜红色肥肠形态的怪鳞,后半身是闪亮的羽毛。这巨怪长着亮黄色奶酪样的脑袋和春绿色烤鸭形态的脖子,有着嫩黄色 萝卜一样的脸和褐黄色路灯样的眉毛,配着浅绿色电池般的鼻子。有着烟橙色领章一样的眼睛,和天蓝色香蕉形态的耳朵,一张烟橙色蚜虫形态的嘴唇,怪叫时露出浓 绿色冰雕样的牙齿,变态的鲜红色球杆一般的舌头很是恐怖,暗红色圆规造型的下巴非常离奇。这巨怪有着仿佛细竹样的肩胛和特像螺栓般的翅膀,这巨怪紧缩的深红 色破钟一般的胸脯闪着冷光,如同面条般的屁股更让人猜想。这巨怪有着极似海带形态的腿和葱绿色铃铛样的爪子……跳动的暗橙色面包一般的六条尾巴极为怪异,蓝 宝石色蘑菇样的板斧梦天肚子有种野蛮的霸气。深红色软管般的脚趾甲更为绝奇。这个巨怪喘息时有种浅绿色火球一般的气味,乱叫时会发出鹅黄色痰盂一样的声音。 这个巨怪头上浅橙色陀螺般的犄角真的十分罕见,脖子上活似匕首般的铃铛真的有些离奇珍贵。蘑菇王子和知知爵士见情况突变,急忙变成了一个巨大的刀片豺腿圣! 这个巨大的刀片豺腿圣,身长二百多米,体重七十多万吨。最奇的是这个怪物长着十分震撼的豺腿!这巨圣有着纯蓝色彩蛋一样的身躯和墨蓝色细小铅笔似的皮毛,头 上是淡青色木偶造型的鬃毛,长着暗灰色犀牛一样的手表烟波额头,前半身是淡蓝色狮子一样的怪鳞,后半身是高高的羽毛。这巨圣长着深紫色犀牛一样的脑袋和淡白 色熊猫一样的脖子,有着亮紫色海豹般的脸和墨紫色龙虾一样的眉毛,配着深白色菜叶造型的鼻子。有着亮青色马鞍般的眼睛,和纯灰色麦穗一样的耳朵,一张亮青色 图钉一样的嘴唇,怪叫时露出暗白色冰灯一样的牙齿,变态的淡蓝色木头似的舌头很是恐怖,墨蓝色黄瓜模样的下巴非常离奇。这巨圣有着极似玉笋一样的肩胛和很像 牙膏造型
九年级化学溶液的酸碱性

食酸醋性、溶液 由紫变红 不变色
盐酸
石蕊遇酸性溶液紫变红
纯碱、 碱性溶液
氢氧化钠
由酚紫酞变遇蓝酸性溶由液无仍色无变色红 石蕊遇碱性溶液紫变蓝
蒸馏水、 酚酞遇碱性溶液红艳艳
中性溶液 食盐水、
不变色
不变色
自学指导
认真默看P.179“活动与探究”以 上的内容,划出重要语句,1分钟 后能回答以下问题:
什么是酸碱指示剂,常用的酸碱指 示剂有哪些?
溶液的酸碱性(1)
学习目标:
1.知道常见的酸碱指示剂, 2.并能用酸碱指示剂区别酸
和碱。
实验指导(1) 在试管中分别加入少量的食醋、盐酸。向
其中滴加紫色石蕊溶液,仔细观察实验现象。
实验指导(2) 在试管中分别加入少量的纯碱溶液、氢氧
化钠溶液。向其中滴加紫色石蕊溶液,仔细观 察实验现象。
实验指导(3) 在试管中分别加入少量的蒸馏水、食盐水。
实验指导(4) 在试管中分别加入少量的食醋、盐酸。向
其中滴加酚酞试液,仔细观察实验现象。
实验指导(5) 在试管中分别加入少量的纯碱溶液、氢氧
化钠溶液。向其中滴加酚酞试液,仔细观察实 验现象。
实验指导(6) 在试管中分别加入少量的蒸馏水、食盐水。
向其中滴加酚酞试液,仔细观察实验现象。加入石蕊溶液 ຫໍສະໝຸດ 入酚酞溶液 后颜色变化 后颜色变化
向其中滴加紫色石蕊溶液,仔细观察实验现象。
石蕊的颜色
食醋、盐酸
纯碱、氢氧化钠 溶液 蒸馏水、食盐水
由紫变红 由紫变蓝 紫色
溶液显 酸性
溶液显 碱性
溶液显 中性
招数……接着像纯白色的千臀城堡鸡一样爆喝了一声,突然秀了一个俯卧收缩的特技神功,身上猛然生出了六只如同小道一样的浅橙色耳朵……紧接着像纯白色的千臀城堡 鸡一样爆喝了一声,突然秀了一个俯卧收缩的特技神功,身上猛然生出了六只如同小道一样的浅橙色耳朵……最后抖起俊朗英武的、顽皮灵活的脖子一笑,狂傲地从里面跳
九年级化学溶液的酸碱度及表示方法

溶液的酸碱性与pH值溶液的酸碱度及表示方法1. 溶液的酸碱性:溶液呈酸性、碱性或中性,通常用指示剂来测定。
2. 溶液的酸碱度:指溶液酸碱性的强弱程度,即酸碱度是定量表示溶液酸碱性强弱的一种方法.溶液的酸碱度通常用pH表示。
3. pH的范围:0—14溶液酸碱度和pH值的关系(1)呈酸性的溶液不一定是酸溶液,如NaHSO4溶液呈酸性,但属于盐溶液;呈碱性的溶液不一定是碱溶液,如Na2CO3溶液呈碱性,但它也是盐溶液。
(2)粗略测定溶液的酸碱度常用pH试纸。
溶液的酸碱性定义:指示剂———溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)电解质量溶液的酸碱性的表示方法(1)溶液的pH在纯水和电解质的稀溶液里都存在水的电离平衡及水的离子积(Kw)。
Kw指明了H+离子和OH-离子的依存关系及其数量关系。
[H+]和[OH-]可以相互换算,因此可以用[H+]统一表示水溶液的酸碱性。
但在稀溶液里[H+]很小,计算时很不方便。
若取[H+]的负对数,计算时就很方便。
因此pH是表示溶液酸碱性的一种方法。
即pH = lg[H+]或[H+] = 10-pH。
在常温下:[H+]>10-7,则pH < 7,溶液呈酸性,[H+]越大,pH越小,酸性越强;[H+]= 10-7,则pH = 7,溶液呈中性;[H+] < 10-7,则pH > 7,溶液呈碱性,[H+]越小,pH越大,碱性越强。
(2)酸碱指示剂借助于颜色的改变来表示溶液pH的物质叫做酸碱指示剂。
例如甲基橙,它是一种有机弱酸,以HIn表示,电离方程式为:HIn H+ + In-(红色) (黄色)当黄色物(In-)和红色的(HIn)各占50%时,溶液显橙色;若[H+]增大到pH为3.1时,红色的HIn占90%,黄色的In-占10%,溶液显红色,[H+]再增大,即pH < 3.1,肉眼已看不出颜色的变化;若[H+]减小到pH为4.4时,约有90%的黄色离子、10%的红色分子,溶液显黄色,[H+]再减小,即pH > 4.4,肉眼也看不出颜色的变化。
九年级化学---溶液的酸碱性

九年级化学——溶液的酸碱性一、【教学目标】知识与技能1.认识溶液的酸碱性,学会用酸碱指示剂判断溶液的酸碱性;2.学会利用pH试纸来定量的测定溶液的酸碱度;3.知道酸碱性对生命活动及其农作物生长的重要性及影响。
过程与方法1.通过对生活中具有酸味、涩味物质的了解,通过实验探究会用酸碱指示剂定性地检验溶液的酸碱性2、掌握pH和溶液酸碱性的关系,能用pH试纸测定溶液的酸碱性和酸碱度;情感态度与价值观1、通过本节学习增强对学习化学的兴趣和探究精神。
2、学会用溶液酸碱性的知识解释生活中的有关现象。
二、教学重点与难点:1.酸碱指示剂在酸碱溶液中显示不同的颜色;2.用pH试纸来表示溶液的酸碱度三、教学过程:(一)、新课导入上节课我们学过酸碱以及他们的性质,日常生活中,有哪些物质曾给你留下过“酸的印象”?如醋,酸果汁等我们可以通过尝味道来知道它们是酸的,那么实验时的溶液禁止尝味道,我们又怎么来区分哪些是酸哪些是碱呢?(二)、教学内容一、酸性溶液和碱性溶液1、酸碱指示剂能检验溶液酸、碱性的指示剂,称为酸碱指示剂常用的酸碱指示剂:紫色石蕊试液;酚酞试液。
2.实验:检验溶液的酸碱性滴加紫色变红变红变红变红变蓝变蓝紫色紫色石蕊试液滴加无色无色无色无色无色变红变红无色无色酚酞试液结论酸性酸性酸性酸性碱性碱性中性中性结论:酸性碱性中性紫色石蕊试液红蓝紫无色酚酞试液无红无酸性溶液——使紫色石蕊试纸变红;碱性溶液——使紫色石蕊试纸变蓝。
注意:我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性酸性溶液能使蓝色石蕊试纸变红;碱性溶液能使红色石蕊试纸变蓝。
3.区分酸溶液和酸性溶液、碱溶液和碱性溶液注意:酸溶液是指酸的水溶液,酸性溶液是指能使紫色石蕊试液变红的溶液,因此酸溶液一定是酸性溶液,而酸性溶液不一定是酸溶液;同样,碱性溶液不一定是碱溶液,碱溶液一定是碱性溶液。
例如:硫酸铜、氯化铵的水溶液显酸性,而不是酸;纯碱、肥皂的水溶液显碱性,但不是碱。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第13课时溶液的酸碱性
江苏2013~2015年中考真题精选
命题点1 酸碱性与酸碱指示剂(2015年3次,2014年2次,2013年3次)
1. (2014苏州5题2 分)下列生活中的常见物质能使无色酚酞试液变红的是( )
A. 食醋
B. 柠檬汁
C. 食盐水
D. 肥皂水
2. (2013苏州5题2分)向2 mL氨水中滴加5~6滴紫色石蕊试液,充分振荡后溶液颜色将变成( )
A. 红色
B. 紫色
C. 无色
D. 蓝色
3. [2015常州27(1)题1分]某品牌洁厕灵是一种蓝色溶液,常用于清除厕所污垢。
(1)欲测该洁厕灵的酸碱性,最适宜选用的是________(填序号)。
a. pH试纸
b. 酚酞试液
c. 紫色石蕊试液
d. pH计
命题点2 溶液酸碱度的测定(2015年1次,2014年2次,2013年3次)
1. [2013盐城18(2)③题1分]③国家规定的自来水pH范围为6.5~8.5,为了测定家用自来水
是否达到这一标准,可用_________来进行检测。
2. [2013宿迁18(1)题2分]甲、乙、丙三位同学为一家化工厂的污水设计排污方案。
请你就他
们的探究过程回答有关问题。
Ⅰ.首先用pH试纸检测污水的酸碱性。
三位同学分别进行如下实验:
甲:取pH试纸于玻璃片上,用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7
乙:取pH试纸于玻璃片上,先用蒸馏水润湿,并再用玻璃棒蘸取待测液滴在pH试纸上,测得pH<7
丙:取pH试纸直接浸入待测液中,测得pH<7
(1)以上三位同学中操作规范的是________,污水显________性。
命题点3 溶液的酸碱性与pH的关系(2015年1次,2014年2次,2013年1次)
1. (2015常州9题2分)酸性较弱的环境有利于益生菌生长,维持皮肤菌群平衡。
因此沐浴液
的酸碱度宜为( )
A. pH<0
B. 4.5<pH<6.5
C. 8<pH<10
D. pH>14
2. (2014扬州9题2分)现有常温下的三种溶液:①纯碱溶液②食盐水③食醋,pH大小关
系为( )
A. ②<①<③
B. ③>②>①
C. ①>②>③
D. ③<①<②
3. (2014南京9题2分)下列食物的近似pH如下,其中酸性最强的是( )
A. 鸡蛋清7.6~8.0
B. 柠檬2.2~2.4
C. 西红柿4.0~4.4
D. 牛奶6.3~6.6
江苏2013~2015年中考真题精选(答案)
命题点1
1. D 【解析】酸性溶液和中性溶液都不能使无色酚酞试液变色,碱性溶液能使无色酚酞试液
变红色。
食醋和柠檬汁显酸性;食盐水显中性;肥皂水显碱性。
故选D。
2. D 【解析】氨水显碱性,能使紫色石蕊试液变成蓝色。
3. c(1分)
【解析】测定酸碱度需用pH试纸或pH计,而测定酸碱性用酸碱指示剂即可,紫色石蕊试液遇酸变红,遇中性不变色,遇碱变蓝;而无色酚酞试液遇酸或中性不变色,遇碱变红,故最好选用紫色石蕊试液。
命题点2
1. ③ pH试纸(或pH计)(1分)
2. (1)甲(1分) 酸(1分)
【解析】(1)用蒸馏水将pH试纸润湿再测酸性溶液的pH,会导致结果偏大,将pH试纸直接浸入待测液中会污染试剂,所以乙、丙同学的操作都是错误的;测得污水的pH<7,说明显酸性。
命题点3
1.B 【解析】pH在0~7之间为酸性,且pH越大酸性越弱,因此,4.5<pH<6.5为弱酸性。
2. C 【解析】纯碱溶液呈碱性,其pH>7;食盐水呈中性,其pH=7;食醋呈酸性,其pH<7;
三种溶液的pH大小关系:纯碱溶液>食盐水>食醋。
故选C。
3.B 【解析】pH小于7的溶液显酸性,pH越小溶液的酸性越强,所以柠檬的酸性最强。
