紫外–可见吸收光谱原理
2紫外吸收光谱分析
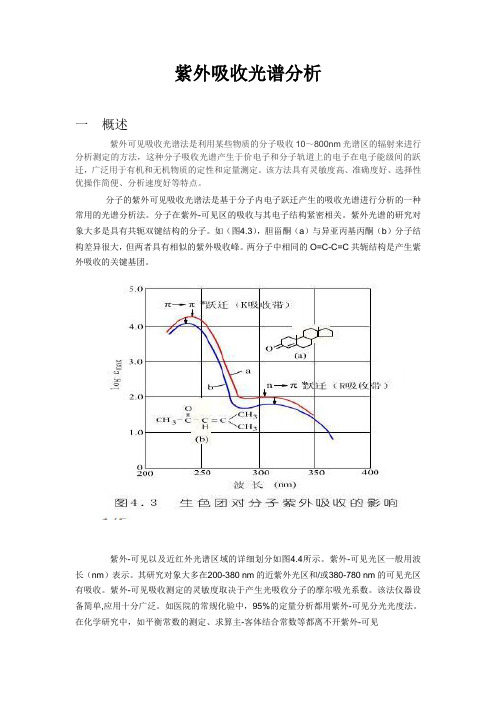
紫外吸收光谱分析一概述紫外可见吸收光谱法是利用某些物质的分子吸收10~800nm光谱区的辐射来进行分析测定的方法,这种分子吸收光谱产生于价电子和分子轨道上的电子在电子能级间的跃迁,广泛用于有机和无机物质的定性和定量测定。
该方法具有灵敏度高、准确度好、选择性优操作简便、分析速度好等特点。
分子的紫外可见吸收光谱法是基于分子内电子跃迁产生的吸收光谱进行分析的一种常用的光谱分析法。
分子在紫外-可见区的吸收与其电子结构紧密相关。
紫外光谱的研究对象大多是具有共轭双键结构的分子。
如(图4.3),胆甾酮(a)与异亚丙基丙酮(b)分子结构差异很大,但两者具有相似的紫外吸收峰。
两分子中相同的O=C-C=C共轭结构是产生紫外吸收的关键基团。
紫外-可见以及近红外光谱区域的详细划分如图4.4所示。
紫外-可见光区一般用波长(nm)表示。
其研究对象大多在200-380 nm的近紫外光区和/或380-780 nm的可见光区有吸收。
紫外-可见吸收测定的灵敏度取决于产生光吸收分子的摩尔吸光系数。
该法仪器设备简单,应用十分广泛。
如医院的常规化验中,95%的定量分析都用紫外-可见分光光度法。
在化学研究中,如平衡常数的测定、求算主-客体结合常数等都离不开紫外-可见二基本原理紫外可见吸收光谱的基本原理是利用在光的照射下待测样品内部的电子跃迁,电子跃迁类型有:(1)σ→σ* 跃迁指处于成键轨道上的σ电子吸收光子后被激发跃迁到σ*反键轨道(2)n→σ* 跃迁指分子中处于非键轨道上的n电子吸收能量后向σ*反键轨道的跃迁(3)π→π* 跃迁指不饱和键中的π电子吸收光波能量后跃迁到π*反键轨道。
(4)n→π* 跃迁指分子中处于非键轨道上的n电子吸收能量后向π*反键轨道的跃迁。
电子跃迁类型不同,实际跃迁需要的能量不同:σ→σ* ~150nmn→σ* ~200nmπ→π* ~200nmn→π* ~300nm吸收能量的次序为:σ→σ*>n→σ*≥π→π*>n→π*特殊的结构就会有特殊的电子跃迁,对应着不同的能量(波长),反反映在紫外可见吸收光谱图上就有一定位置一定强度的吸收峰,根据吸收峰的位置和强度就可以推知待测样品的结构信息三特点1、紫外可见吸收光谱所对应的电磁波长较短,能量大,它反映了分子中价电子能级跃迁情况。
紫外-可见吸收光谱的产生及基本原理

判别顺反异构体
H
H C C H
C C
H
顺式
反式 λmax=295nm εmax=27000
λmax=280nm εmax=13500
共平面产生最大共轭效应, εmax大
判别互变异构体
O CH3 C H O C C H OC2H5
H O O H O H O H
酮式:λmax=272nm,εmax=16
汞灯用于波长检定。
用积分球的检测器波长<2500nm。
单色器
将光源发射的复合光分解成单色光并可从中选出一任波 长单色光的光学系统。 ①入射狭缝:光源的光由此进入单色器; ②准光装置:透镜或返射镜使入射光成为平行光束; ③色散元件:将复合光分解成单色光;棱镜或光栅; ④聚焦装置:透镜或凹面反射镜,将分光后所得单色光聚焦 至出射狭缝; ⑤出射狭缝。
a
b c
比例常数,称为吸光系数
液层厚度,单位cm 浓度。当浓度 c 以 g· L-1 为单位,液层厚度 b 以 cm 为单位 时,吸光系数的单位为:L· g-1· cm-1
紫外分光光度法定性分析
比较吸收光谱曲线法:
可以将在相同条件下测得的未知物的吸收光谱与标准谱图 进行比较来作定性分析。如果吸收光谱的形状,包括吸收光谱 的λmax、λmin、吸收峰的数目、位置、拐点以及等完全一致,则 可以初步认为是同一化合物。
OH CH3 C H O C C OC2H5
O H
O
烯醇式:λmax=243nm,εmax=16000
纯度的控制和检验
a) 根据吸收光谱判断
含10-6M蒽的苯溶液
苯溶液
b) 根据lgε判断
4.10 例如:标准菲 lg 氯仿 max( 296 nm )
波谱分析第6章 紫外可见光谱(1)
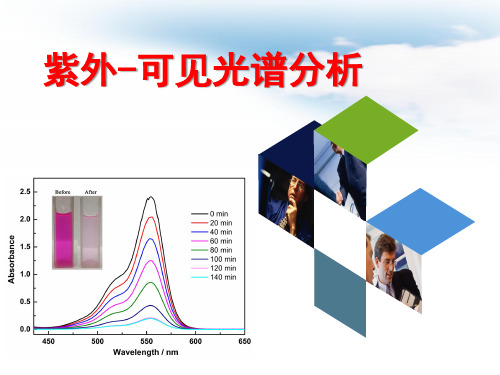
图 分子轨道的能级和电子跃迁类型
s*
*
E
n
s
跃迁能量大小:
σ→σ* > n →σ* > π→π* > n→π*
仅在远紫外区可能观察到它们的吸收峰。
杂原子非键轨道中的电子向σ*轨道的跃迁,一般在 200 nm左右。
电子由成键轨道向*轨道的跃迁。如具有一个孤 立键的乙烯,跃迁的吸收光谱约在165 nm。分子中 如有两个或多个键处于共轭的关系,则这种谱带将 随共轭体系的增大而向长波方向移动。
max
254nm
270nm
红移和蓝移 增色效应与减色效应
最大吸收波长(λmax);在峰旁边一个小 的曲折称为肩峰;在吸收曲线的波长最 短一端,吸收相当大但不成峰形的部分 称为末端吸收。整个吸收光谱的形状是
鉴定化合物的标志。
吸收带分类
根据电子和轨道的种类,可以把吸收谱带分为四 类: K 吸收带、R 吸收带、B 吸收带和 E 吸收带。
图 (a) Frank-Condon原理示意图
(b) 紫外光谱的精细结构
6.1.2 电子跃迁选择定则(Selection rule)
跃迁必须遵守选择定则
理论上,允许的跃迁,跃迁几率大,吸收强度高( max大);禁阻的跃迁,
跃迁几率小,吸收强度低或者观察不到。 实际上禁阻的跃迁也可以观察到,只是其强度要比允许跃迁要小得多。
紫外-可见光谱分析
6.1.1紫外-可见光谱的基本原理
紫外-可见吸收光谱(UV-VIS) 分子吸收10~800nm光谱区的电磁波而产生的吸收光谱。该数 量级能量的吸收,可导致分子的价电子由基态(S0)跃迁至高能 级的激发态(S1, S2, S3, …) 紫外-可见光区分为三个区域:
紫外吸收光谱(UV)
2.3 有机化合物基团分类
1)发色基团(200-400nm产生吸收的基团) n *, *
C
C, C
O ,
C
N,
O N O
*,n *
2)非发色基团(200-400nm不产生吸收的基团)
3)助色基团 本身为非发色基团,使发色基团吸收位置 移向 长波。 n *.助色能力 –F<CH3<-Cl<-Br<OH<OCH3<-NH2< -NHCH<-N(CH3)2<-NHC5H6<O-
⑴无环、非稠环二烯母体:
max= 基+nii
基-----是由非环或六环共轭二烯母体决定的基准值
max=217 nm
⑵异环(稠环)二烯母体:
max=214 nm
⑶同环(非稠环或稠环)二烯母体:
max=253 nm nii---是由双键上取代基种类和个数决定的校正项
190
210
230
250
270
290
310
330
350
370
¨¤ ² ³ nm
2)脂肪烃不饱和化合物
H
ⅰ单烯烃 C=C
H c c H
发色基团, 但
* 200nm.
max=162nm
助色基团取代
-OR 30(nm)
H
* (K带)发生红
-Cl 5(nm) CH3 5(nm)
移。
取代基 -SR -NR2 40(nm)
350
400
0.1 弱带
红位移——向长波长位移
兰位移——向短波长位移 浓色效应——摩尔吸光系数max增加 浅色效应——摩尔吸光系数max减少 强带——max≥ 104(多为允许跃迁)
紫外可见

波长在400~800 nm范围的 称为可见光谱
紫外-可见光谱法的特点
(1)灵敏度高, 常用于测定试样中1%-10-3 %的微量组分,甚至可测定低至 10-4 %-10-5 %的痕量组分。
(2)准确度较高, 相对误差为2%-10%。如采用精密分光光度计测量,相对
误差可减少至1%-2%。 (3)应用广泛, 几乎所有的无机离子和许多有机化合物都可直接或间接地用 此法测定。 (4)操作简便快速,仪器设备也不复杂
紫外-可见吸收光谱
Ultraviolet and visible spectrophotometry; UV-vis
目录
概述
基本原理 光谱图 紫外-可见吸收光谱常用概念 影响吸收的因素 介绍紫外可见光谱仪 紫外吸收光谱图的应用
1 概述
紫外-可见吸收光谱属于分子光谱。是通过分子中的价电子在分子轨道之
间的跃迁而产生的(包括振动和转动能级的跃迁)。利用物质的分子或离子 对紫外和可见光的吸收所产生的紫外-可见光谱及吸收程度可以对物质的组成、 含量和结构进行分析、测定、推断。
紫外光的波长范围是100~400 nm
可见光的波长范围是400~800 nm
远紫外区 这个区域的 吸收光谱 称真空紫外
近紫外区 一般的紫外光谱 是指这一区域的 吸收光谱
3.样品室
——又称吸收池——放置各种类型的比色皿和相应 的池架附件。吸收池主要有石英池和玻璃池两种。
在紫外区须采用石英池,可见区一般用玻璃池
4.检测器
——利用光电效应将透过吸收池的光信号变成可
测的电信号,常用的有光电池、光电管或光电倍增管 (CCD)。
5. 结果显示记录系统 ——检流计、数字显示、微机进行仪
d 轨道电子云分布及在
第三章 紫外-可见吸收光谱法

3-1 概述
3-1 概述
紫外光
波长为10-400nm的电磁辐射,分为远紫外光 的电磁辐射, 波长为 的电磁辐射 (10-200nm)和近紫外光(200-400nm)。 )和近紫外光( )。 远紫外光可被大气中的水气、 远紫外光可被大气中的水气、氮、氧和二氧化 碳所吸收,只能在真空中研究, 碳所吸收,只能在真空中研究,故又称真空紫 外光。我们讨论近紫外光谱。 外光。我们讨论近紫外光谱。
紫外-可见吸收光谱法 第三章 紫外 可见吸收光谱法
UltravioletUltraviolet-Visible Absorption Spectrometry UV-Vis UV-
章节内容
第一节 概述 紫外-可见吸收光谱 第二节 紫外 可见吸收光谱 第三节 紫外-可见分光光度计 紫外 可见分光光度计 紫外-可见吸收光谱法的应用 第四节 紫外 可见吸收光谱法的应用
(5)出射狭缝 紫外-可见分光光度计使用石英棱镜。 棱镜单色器的缺点在于色散率随波长变 化,得到的光谱呈非均匀排列,而且传递 光的效率较低。 光栅单色器在整个光学光谱区具有良好 的几乎相同的色散能力。因此现代紫外-可 见分光光度计 多采用光栅单色器。 (三)吸收池 (四)检测器 (五)信号显示器
二、分光光度计的构造类型
的配位体强度小于NH 如:H2O的配位体强度小于 3的, 的配位体强度小于 所以, ( 所以,Cu(H2O)6呈浅蓝色,吸收峰 ) 呈浅蓝色, 794nm;Cu(NH3)6深蓝色,吸收峰 深蓝色, ; ( 663nm。 。 一些常见配位体配位场强弱顺序: 一些常见配位体配位场强弱顺序: I-<Br-<Cl-<F-<OH-<C2O4-=H2O<SCN-< 吡啶=NH3<乙二胺 联吡啶 邻二氮菲 乙二胺<联吡啶 吡啶 乙二胺 联吡啶<邻二氮菲 <NO2-<CN-
紫外可见吸收光谱基本原理
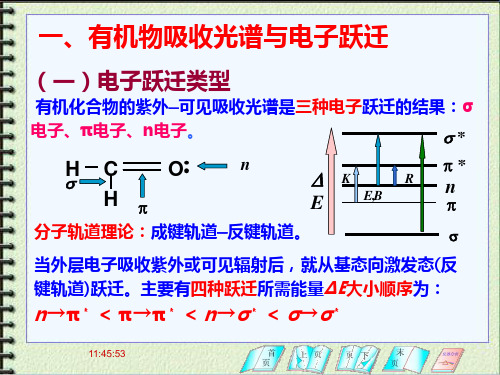
n→π* < π→π* < n→σ* < σ→σ*
11:51:47
2
σ→σ*跃迁
所需能量最大;σ电子只有吸收远紫外光的能量
才能发生跃迁;
饱和烷烃的分子吸收光谱出现在远紫外区; 吸收波长λ <200 nm; 例:甲烷的λ max为125nm , 乙烷λ max为135nm 。 只能被真空紫外分光光度计检测到; 作为溶剂使用;
max(甲醇) max(水) max(氯仿)
n → p*跃迁:蓝移; ;
max(正己烷)
p → p* n → p*
230 329
11:51:47
238 315
237 309
243 305
溶剂的影响
苯 酰 丙 酮 1 1:乙醚 2:水
2
250
300
极性溶剂使精细结构 消失;
11:51:47
11:51:47
11:51:47
精品课件!
11:51:47
精品课件!
11:51:47
(三) 金属离子影响下的配位体内π→π*跃迁 金属离子的微扰,将引起配位体吸收波长和 强度的变化。变化与成键性质有关,若共价 键和配位键结合,则变化非常明显。 茜素磺酸钠: 弱酸性介质:黄色(λ max=420nm) 弱碱性介质:紫红色(λ max=560nm )
一、有机物吸收光谱与电子跃迁
(一)电子跃迁类型
有机化合物的紫外—可见吸收光谱是三种电子跃迁的结果: σ电子、π电子、n电子。 s*
E p 分子轨道理论:成键轨道—反键轨道。
s
H
C H
OnKR Nhomakorabeap*
E,B
n
p
s
当外层电子吸收紫外或可见辐射后,就从基态向激发态(反 键轨道)跃迁。主要有四种跃迁所需能量ΔΕ大小顺序为:
紫外-可见吸收光谱法

助色团: (Auxochromous group) 有一些含有n电子的基团(如—OH、— OR、—NH2、—NHR、—X等),它们本身 没有生色功能(不能吸收λ>200nm的光) ,但当它们与生色团相连时,就会发生 —π*共轭作用,增强生色团的生色能 力(吸收波长向长波方向移动,且吸收强 度增加),这样的基团称为助色团。
(四) *跃迁
所需能量较小,吸收波长处于远紫外区 的近紫外端或近紫外区,最大吸收波长 λ在200nm左右,摩尔吸光系数εmax一般 在104L· -1· -1以上,属于强吸收。 mol cm 不饱和烃、共轭烯烃和芳香烃类均可发 生该类跃迁。
相关术语
生色团:(Chromogenesis group) 最有用的紫外—可见光谱是由π→π*和 n→π*跃迁产生的。这两种跃迁均要求有 机物分子中含有不饱和基团。这类含有π 键的不饱和基团称为生色团。简单的生 色团由双键或叁键体系组成,如乙烯基、 羰基、亚硝基、偶氮基—N=N—、乙炔 基、腈基等。
当入射光波长一定时,待测溶液的吸光度 A与其浓度和比例系数,与溶液性质、温度和入射波长有关。 当浓度以 g/L 表示时,称 k 为吸光系数,以 a 表示,即
A abc
当浓度以mol/L表示时,称 k 为摩尔吸光系数,以 表示, 即
A bc
比 a 更常用。 越大,表示方法的灵敏度越高。 与波长有关,因 此, 常以表示。
摩尔吸光系数ε 的讨论 • 吸收物质在一定波长和溶剂条件下的特征常数; • 不随浓度c和光程长度b的改变而改变。在温 度和波长等条件一定时,ε仅与吸收物质本身 的性质有关; 可作为定性鉴定的参数; 同一吸收物质在不同波长下的ε值是不同的。 在最大吸收波长λmax处的摩尔吸光系数,常以 εmax表示。εmax表明了该吸收物质最大限度的 吸光能力,也反映了光度法测定该物质可能达 到的最大灵敏度。
紫外-可见光吸收光谱

摩 尔 吸 收 系 A/bc(c, g/L) 数
A/bc(c, mol/L)
朗伯-比尔定律( Lambert-Beer 定律)
Ir I0 Ia
It
透光度 (transmittance) T=It/I0
吸光度 (absorbance) A= -lgT
Lambert – Beer 定律 1.光吸收定律的表达式及其含义 布格(Bouguer)和朗伯(Lambert)先后于1729年和1760年阐 明了光的吸收程度和吸收层厚度的关系: A∝ b 1852年比耳(Beer)又提出了光的吸收程度和吸收物浓度之 间也具有类似的关系: A∝ c 二者的结合称为朗伯-比耳定律,其数学表达式 为: A=- lgT = - lg( It / I0)= ε b c 式中:A:吸光度;T:透射率; b:液层厚度(光程长度),通常以cm为单位; c:溶液的摩尔浓度,单位mol· -1; L ε:摩尔吸光系数,单位L· -1· -1; mol cm
紫外-可见光谱 ΔE 电子 1 ~ 20ev
1 0
E1 υ υ υ
2
分 子 可 见 吸 收 光 谱
3 2 1 0 3 2 1 0 3 2 1 0
J J J
λ电子 1.25 ~ 0.06 μm
中红外光谱
1
ΔE振动 0.05 ~ 1ev λ振动 25 ~ 1.25 μm
0
E0 分子红外吸收光谱
当入射光波长一定时,待测溶液的吸光度A与其浓度和液层厚度成 正比,即
A kbc
k 为比例系数,与溶液性质、温度和入射波长有关。 当浓度以 g/L 表示时,称 k 为吸光系数,以 a 表示,即
A abc
当浓度以mol/L表示时,称 k 为摩尔吸光系数,以 表示,即
紫外-可见光谱

204nm
230~270nm
在230~270nm处有较弱 的一系列吸收带,称为精细 结构吸收带,亦称为B吸收 带。B吸收带的精细结构常 用来辨认芳香族化合物。
苯在乙醇中的紫外吸收光谱
22
苯环上有发色团且与苯环共轭时,E带与K带 合并,向长波方向移动,形成K—E合并带 例:
E1 E2 B
O
185 nm 204 nm 254 nm 245 278 319
18
例: 1-己烯 1.5-己二烯 1.3-己二烯 1.3.5-己三烯
λmax 177 178 217 258
104 2×104 2.1 × 104 4.3 × 104
• K 吸收带是共轭分子的特征吸收带,可用于判断 共轭结构——应用最多的吸收带
19
(3)B 吸收带和E吸收带 —苯环带 B吸收带:有苯环必有B带。230-270 nm 之间 有一系列吸收峰,中吸收,芳香族化合物的特征 吸收峰。 苯环上有取代基并与苯环共轭,精细结构消失
5.4 芳香族化合物 a. 苯及取代苯: 苯分子有三个共轭双键,因此有三个成键及三个反 键轨道, π→π* 跃迁较复杂,可以有不同的激发态。苯 有三个吸收带。
取代苯 • 烷基取代苯:影响小,由于超共轭效应,导致红移, 降低B- 带的精细结构; • 助色团取代苯:n 电子与苯环形成 p-π共轭,导致红移, 增强B-带的强度,降低B- 带的精细结构 连有推电子基团的红移强弱顺序为: CH3 < Cl < Br < OH < OCH3 < NH2 < O-
• 常用的是π→π*跃迁和n→π*,这两种跃迁都 需要分子中有不饱和基团提供π轨道。 • n→π*跃迁与π→π*跃迁的比较如下: π→π*
紫外-可见光谱分析

吸收曲线与最大吸收波长 max可用不同波长的单色
光照射,测吸光度得到——扫描
同一种物质对不同波长光的吸光度不同。吸光度最大
处称为吸收峰,所对应的波长称为最大吸收波长max
峰 肩
末端吸收 谷
吸收曲线可以提供 物质的结构信息,并 作为物质定性分析的 依据之一。 不同浓度的同一种物质,其吸收曲线形状相似λmax不变。而 对于不同物质,它们的吸收曲线形状和λmax则不同。
二、无机化合物的吸收光谱
无机化合物的UV-Vis光谱吸收光谱主要有: 电荷迁移跃迁及配位场跃迁
配位场跃迁( d一d、 f 一f 跃迁)
在配体存在下过渡金属元素5个能量相等的d 轨道和镧系、 锕系7个能量相等的的 f 轨道裂分,吸收辐射后,低能态的d 电子或f电子可以跃迁到高能态的d或f轨道上去。 绝大多数过渡金属离子都具有未充满的 d 轨道,按照晶体场 理论,当它们在溶液中与水或其它配体生成配合物时,受配 体配位场的影响,原来能量相同的 d轨道发生能级分裂,产 生 d-d 电子跃迁。 必须在配体的配位场作用下才可能产生, 所以称为配位场跃迁;
n<p
n
n
p
非极性溶剂中 极性溶剂中
n >p
n p
非极性溶剂中 极性溶剂中
溶剂的极性除了影响吸收峰的位置,还影响吸收光谱 的精细结构:
N HC
N
CH 对称四嗪
N
极性溶剂使精细结构消失
蒸汽中
环己烷
水中
4. 体系pH的影响
pH影响吸光物质的存在形态,产生不同的吸收光谱. 如苯酚,在酸性或中性水溶液中,有210.5nm及270nm 两个吸收带;而在碱性溶液中,则分别红移到235nm和
吸收波长为150~250nm,大部分在远紫外区
第五章 紫外-可见吸收光谱法
甲醇 n→σ*跃迁: λmax 183nm
π→π*跃迁:
所需能量较小,λ一般>200nm,εmax > 104。 不饱和基团(乙烯基、乙炔基) 不饱和烃、共轭烯烃和芳香烃类可发生此类跃迁。 乙烯 π→π*跃迁: λmax 165nm
丁二烯 π→π*跃迁: λmax 217nm
n→π*跃迁:
所需能量最小, λ >200nm, -C=N-
色——蓝色。
我们通常见到的有色物质,都是由于他们吸收了可见光的 部分光,呈现出吸收光颜色的互补色。
二、分子吸收光谱的产生
分子吸收光谱的形成是由于电子在能级之间的跃迁所引
起的。
分子内部具有电子能级、振动能级和转动能级。所以分
子的能量 E分子=E电+E振+E转 。
这些能量是量子化的,只有光辐射的能量恰好等于两能 级之间的能量差时,才能被吸收。
苯环本身分子振动、转动能级跃迁而产生的吸 收带,转动能级消失,谱带较宽。 • 芳香物的主要特征吸收带 • Λ= 230~270 nm, 具有精细结构 • ε~200
• 极性溶剂中,或苯环连有取代基
时,其精细结构消失
三、紫外-可见光谱中的常见吸收带
4、E带: (乙烯型ethylenic band) 由苯环环形封闭共轭体系的π→ π*跃迁产生 • 芳香族化合物的特征吸收带
三、紫外-可见光谱中的常见吸收带
2、K带:(共轭作用konjugation))) 由共轭双键的π→ π*跃迁产生 (—CH=CH—)n, —CH=C—CO— 特点:λmax>200nm,强ε>104 共轭体系增长, ε↑, λ↑(红移)
三、紫外-可见光谱中的常见吸收带
3、B带:(苯benzenoid)
有机波谱解析-第二章 紫外光谱

C
Hale Waihona Puke n<pOC
C
p*
n > p p*
n
n C
p* p
p*
n
p n 非极性
p
O 非极性
C C
p
极性
极性
n → p*跃迁:兰移; ; pp np
(4)尽量和文献中所用的溶剂一致。
(5)溶剂挥发性小、不易燃、无毒性、价格便宜。
5. 电子跃迁的类型
紫外吸收光谱是由价电子的能级跃迁而产生的,有机化 合物的紫外—可见吸收光谱是三种电子跃迁的结果:σ电子、 π电子、n电子。 s* n p* H C O
s
p E 分子轨道理论:成键轨道—反键轨道。
各种电子能级的能量及电子跃迁类型如右图
3. 紫 外 光 谱 图
横坐标:波长或频率 纵坐标:吸光度(A) 或 透过率(T)
紫外光谱(图)的特点: 吸收谱带少; 吸收谱带宽; 通常以谱带吸收最强的波长表示谱带位置,称 为最大吸收波长(λmax) ,是分子的特征常数, 与分子电子结构相关,可推测化合物中生色团类 型和共轭大小; 吸收强度以最大吸收波长处的摩尔吸光系数 (εmax)表示,也是分子特征常数和鉴定化合物 的重要依据。
H H c H
取代基 红移距离 -SR 45(nm)
c H
max=162nm 助色基团取代 p
-NR2 40(nm) -OR 30(nm)
p*(K带)发生红移。
-Cl 5(nm) CH3 5(nm)
(2)共轭烯烃中的
p → p*
紫外-可见吸收光谱法(UV-Vis)

max 一般 10
增大
A 1103 7 1 Cmin 1 10 mol L b 1104 1 1107 100 1108 g mL1 1000
3 ~104;灵敏
的 >104;个别的可达 105 106
若λ1= λ2
dA b dC
ε 1 = ε2= ε 在一定的浓度范围内 A= εbC
若λ1≠ λ2
2.303 f1 f 2b 2 ( λ1 λ 2 ) 210 ( λ1 λ 2 )bc d2A 0 λ 1bc λ 2bc 2 2 dC ( f110 f 210 )
1) 液气固介质均适用 2)入射光是单色光,平行光 3)稀溶液
朗伯-比尔定律
A = Kbc
(二)朗伯-比尔定律推导
Ix dIx S I0 db b It
-dIx ∝ Ix adn dn = csdb
-dIx∝ IxaCsdb -dIx/Ix=k Cdb
b dI x I0 I x k 0 cdb It
0
0
C
A = 0.434
(四)吸光系数
1. a ( L · g –1 · cm-1) 2.ε ( L · mol–1 · cm-1)
max
A KCb
A aCb A Cb
C: g / L C: mol/ L
吸光物质结构的特征参数;
吸光物质定量分析的灵敏度参数
3. 检出限与摩尔吸光系数 若可测量的吸光度为0.001
It ln kcb I0 It kcb lg Kcb I 0 2.303
A lg T Kbc
吸光度 与透射率
第十八章 紫外-可见光谱与荧光光谱

发射
1.2 基本原理(紫外-可见光谱)
H为普朗克常数,6.分子吸收光谱的形成
100-800 nm
1~20 eV
远紫外光区: 100-200 nm 近紫外光区: 200-400 nm 可见光区: 400-780 nm
用紫外—可见光照射分子时,会发生电 子能级的跃迁,对应产生的光谱,称为 紫外—可见吸收光谱 (又称电子光谱)
√
√
× ×
n—σ*
π—π* :波长 200
n - π* :能隙窄,近紫
外光区及可见光区吸收 检测对象:具有不饱和结 构的化合物 饱和烃作溶剂用!
1.4 无机化合物的电子跃迁类型
(1)电荷转移跃迁 (某些有机分子也存在这种跃迁)
D—A
h
D+—A- (激发态)
D
D:Donor A: Acceptor
端引入某取代基(如甲基、乙基等)或溶剂 效应)
同时,吸收强度发生改变:
末端吸收:在仪器极限处测出的吸收
增色效应:吸光强度增大 减色效应:吸光强度减小
肩峰:吸收曲线在下降或上升处有停顿, 或吸收稍微增加或降低的峰,是由于主 峰内隐藏有其它峰
溶剂效应
极性溶剂中:
非极性溶剂
ΔE1 ΔE2
极性溶剂
第十八章
紫外-可见光谱与荧光光谱
§1
§2
紫外-可见吸收光谱
荧光光谱
§1
1.1 光谱概述
反射
紫外-可见吸收光谱
入射光
吸收光谱: 红外光谱、紫 外光谱、原子吸收光谱、核 磁共振等 散射光谱:拉曼光谱
散射
吸收
物质
透射
发射光谱:原子发射光谱、 原子荧光光谱、 X 射线荧光 光谱法、分子荧光光谱法等
紫外吸收

σ*
反键轨道
π*
En
↑↓
π
↑↓
σ
↑↓
非键轨道 成键轨道
2
安徽师范大学
化学与材料科学学院
杨高升
常见有机化合物的紫外光谱吸收带主要有以下几种类型: 1. 远紫外(真空紫外)吸收带 最大吸收波长 < 200 nm,处于真空紫外区。主
2. 溶液酸度的影响 溶液酸度的变化可以改变某些有机化合物的存在形式,并导
致谱带发生位移。最典型的就是酚和芳香胺类化合物。例如
苯酚:
E2带 λmax (ε)
OH
211 nm (6200)
B 带 λmax (ε) 270 nm (1450)
−H+
苯胺:
O-
236 nm (9400)
287 nm (2600)
要是 σ→σ*跃迁引起的,是烷烃的吸收带。 2. 尾端(末端)吸收带 最大吸收波长虽在真空紫外区,但靠近 200 nm,吸收
带的尾部进入近紫外区。主要由 n→σ*跃迁引起,是含杂原子的饱和化合物的 吸收带。如饱和卤代烃、醇、胺等。 3. R 带 最大吸收波长 > 270 nm 的弱吸收带,摩尔吸光系数 ε 很小,一般 < 100。 由 n→π*跃迁引起,是含杂原子的不饱和化合物的吸收带。如醛、酮、硝基及 亚硝基化合物等。 4. K 带 最大吸收波长 > 200 nm 的强吸收带,摩尔吸光系数 ε 很大,一般 > 10000。由共轭体系的 π→π*跃迁引起,是共轭不饱和化合物的吸收带。如共 轭烯烃、共轭的不饱和羰基化合物等。 5. B 带 最大吸收波长 > 200 nm、强度中等且常伴有精细结构的宽吸收带,摩 尔吸光系数 ε 较小,一般 250 ~ 3000 之间。由芳环和芳香杂环化合物 π→π*跃 迁引起的,是芳环和芳香杂环化合物的特征吸收带。如苯的 B 带在 230 ~ 270 nm,为含有多重峰或精细结构的宽吸收带。 6. E带 也是芳香结构的特征吸收带。都是芳香体系中π→π*跃迁引起的。特点 是摩尔吸光系数ε很大,一般 > 10000。E带可分为E1带和E2带。如苯的E带就 有两个:184 nm(E1带,烯带,简单看作是乙烯的π→π*跃迁引起的)、204 nm
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫外–可见吸收光谱原理
紫外-可见吸收光谱是一种常用的光谱分析技术,用于分析物
质的化学结构和浓度。
它基于物质对紫外-可见光的吸收特性。
紫外-可见光谱是通过将被测物质溶解在适当的溶剂中,然后
用一束紫外-可见光照射样品,并测量样品对光的吸收来进行的。
紫外-可见吸收光谱的原理基于被测物质分子电子的激发和跃迁。
当物质处于基态时,其分子处于低能级的电子轨道上。
当紫外-可见光照射被测物质时,光子的能量能够被物质中的电
子吸收,使其跃迁到高能级的轨道上。
这种电子跃迁导致了紫外-可见光谱的吸收峰。
每种物质都有其特定的吸收特性,这是由其分子结构和化学键决定的。
不同的分子或化学键对不同波长的光具有不同的吸收能力。
通过测量光通过样品后的强度变化,可以得到吸收光谱。
紫外-可见吸收光谱通常以波长(nm)为单位进行测量。
在可
见光范围内,波长较长的光产生红色的吸收峰,而波长较短的光产生紫色的吸收峰。
在紫外光范围内,波长较长的光产生较低能级的吸收峰,而波长较短的光产生较高能级的吸收峰。
通过分析样品吸收光谱的形状和位置,可以确定样品中的物质种类和浓度。
此外,紫外-可见吸收光谱还可以用于分析反应
动力学、鉴定物质和定量测量等应用。
