化学
化学名称及符号

水银汞H g白金铂 Pt硫磺硫S金刚石、石墨、木炭碳C白磷、红磷、黄磷磷 P盐酸、盐镪水氢氯酸HCl硝镪水硝酸 HNO3硫镪水硫酸 H2SO4王水浓硝酸、浓盐酸(1:3)HNO3,HCl双氧水过氧化氢 H2O2铅丹、红丹、红铅四氧化三铅 Pb3O4砒霜、信石、白砒、砷华三氧化二砷 As2O3升汞、高汞氯化汞 Hg Cl2朱砂、辰砂、丹砂、银朱硫化汞HgS烧碱、火碱、苛性钠氢氧化钠N aOH苛性钾氢氧化钾 KO H消石灰、熟石灰氢氧化钙Ca(OH)2碱石灰、钠碱石灰氢氧化钠、氧化钙混合 Na OH,Ca O 碳铵碳酸氢铵NH4HC O3盐脑、电气药粉氯化铵NH4Cl硫铵硫酸铵 (N H4)2S O4碳酸气、干冰二氧化碳CO2笑气氧化二氮 N2O硅石、石英、水晶、玛瑙砂子二氧化硅 SiO2矾土、刚玉氧化铝 Al2O3生石灰、煅烧石灰氧化钙CaO锌白、锌氧粉氧化锌ZnO苫土、烧苫土氧化镁MgO苏打、纯碱碳酸铵N a2SO4小苏打、重碱碳酸氢钠 Na HCO3大苏打、海波硫代硫酸钠 Na2S2O3.5H2O褐铁矿2Fe2O3.3H2O芒硝、皮硝、马牙硝结晶硫酸钠 Na2SO4.10H2O泻盐、苦盐硫酸镁 MgSO4.7H2O口碱结晶碳酸钠 NaCO3.10H2O明矾硫酸铝钾 KAl(SO4)2.12H2O皓矾硫酸锌Z nSO4.7H2O胆矾硫酸铜 CuS O4.5H2O红矾重铬酸钾 K2Cr2O7无水芒硝、元明粉硫酸钠 Na2SO4水玻璃、泡花碱硅酸钠 NaSi O3硫化碱、臭碱硫化钠N a2S钾碱、草碱、草木灰碳酸钾 K2CO3硝石、火硝、土硝硝酸钾 KNO3灰锰氧、PP粉高锰酸钾KMnO4冰晶石氟铝酸钠Na3Al F6大理石、方解石、石灰石白垩碳酸钙 CaC O3萤石、氟石氟化钙 Ca F2钙硝石、挪威硝石硝酸钙 Ca(N O3)2电石碳化钙 CaC2铜绿、孔雀石碱式碳酸铜CU2(O H)2CO3重晶石、钡白硫酸钡 Ba SO4钠硝石、智利硝石硝酸钠 NaN O3生石膏、石膏硫酸钙C aSO4.2H2O熟石膏、烧石膏硫酸钙 2Ca SO4.H2O普钙、过磷酸钙磷酸二氢钙、硫酸钙 Ca(H2PO4)2,CaS O4 重钙磷酸二氢钙 Ca(H2PO4)2漂白粉次氯酸钙 Ca(ClO)2氯仿、绿仿三氯甲烷 CHC l3木精甲醇C H3OH甘油丙三醇 C2H5(OH)3石炭酸苯酚C6H5OH蚁酸甲酸 HCO OH草酸乙二酸HOOC-COOH福尔马林甲醛溶液(30%~40%) H CHO尿素碳酰胺 CO(N H2)安息香酸苯甲酸 C6H5COO H赤铜矿氧化亚铜 Cu2O软锰矿二氧化锰MnO2菱铁矿碳酸亚铁F eCO3辉铜矿硫化亚铜C u2S愚人金硫化亚铁 Fe S2铁丹、铁红、赭石、赤铁矿三氧化二铁 Fe2O3磁铁矿、铁黑四氧化三铁 Fe3O4绿矾七水合硫酸亚铁 Fe SO4.7H2O保险粉连二亚硫酸钠Na2S2O4醋酸乙酸C H3COO H常见物质颜色汇总1.红色 Fe(SCN)]2+ (血红色); Cu2O(砖红色); Fe2O3(红棕色); 红磷(红棕色); 液溴(深红棕色); F e(OH)3 (红褐色); I2的CC l4溶液(紫红色); Mn O4-(紫红色);Cu(紫红色); 在空气中久置的苯酚(粉红色).2.橙色: 溴水; K2Cr2O7溶液.3.黄色: Ag I(黄色); Ag Br(浅黄色); K2CrO4(黄色); Na2O2(淡黄色); S(黄色); F eS2(黄色); 久置浓HN O3(溶有NO2);工业浓盐酸(含F e3+); Fe3+水溶液(黄色);久置的K I溶液(被氧化成I2)4.绿色:Cu2(O H)2CO3; F e2+的水溶液; F eSO4.7H2O; Cl2(黄绿色); F2(淡黄绿色); C r2O35.蓝色: Cu(OH)2; Cu SO4.5H2O;Cu2+的水溶液; I2与淀粉的混合物.6.紫色:KMnO4(紫黑色); I2(紫黑色); 石蕊(pH=8--10); Fe3+与苯酚的混合物.7.黑色: F eO, Fe3O4, Fe S, C uS, Cu2S, Ag2S, P bS, CuO, MnO2, C粉.8.白色:Fe(OH)2, AgOH,无水C uSO4, Na2O, Na2CO3, NaHCO3, A gCl, BaSO4, Ca CO3, CaSO3 ,Mg(OH)2, Al(OH)3, 三溴苯酚, M gO, MgCO3, 绝大部分金属等.说明:①元素基本上按周期表的族序数排列;②物质基本上按单质、氢化物、氧化物及其水化物、盐、有机物的顺序排列;③许多物质晶状为无色,粉末状为白色,晶型不同可能有不同颜色;④硫化物和过渡元素化合物颜色较丰富。
化学常识100条

化学常识100条1.化学变化的特征是有新物质生成。
2.物理变化只是物质的状态、形状等发生改变,没有新物质生成。
3.分子是保持物质化学性质的最小粒子。
4.原子是化学变化中的最小粒子。
5.元素是具有相同核电荷数(即质子数)的一类原子的总称。
6.地壳中含量最多的元素是氧,其次是硅、铝、铁。
7.地壳中含量最多的金属元素是铝。
8.人体中含量最多的元素是氧。
9.人体中含量最多的金属元素是钙。
10.组成物质的基本成分是元素。
11.物质由分子、原子、离子等微观粒子构成。
12.分子由原子构成。
13.水由水分子构成。
14.铁由铁原子构成。
15.氯化钠由钠离子和氯离子构成。
16.分子在不断地运动。
17.分子间有间隔。
18.温度升高,分子运动速率加快。
19.压强增大,分子间间隔变小。
20.混合物由两种或两种以上物质组成。
21.纯净物由一种物质组成。
22.单质是由同种元素组成的纯净物。
23.化合物是由不同种元素组成的纯净物。
24.氧化物是由两种元素组成,其中一种是氧元素的化合物。
25.化学式表示物质的组成。
26.相对原子质量是以一种碳原子质量的1/12 为标准,其他原子的质量与它相比较所得到的比。
27.相对分子质量是化学式中各原子的相对原子质量的总和。
28.在化合物中,各元素正负化合价的代数和为零。
29.元素的化学性质主要由原子的最外层电子数决定。
30.金属元素的原子最外层电子数一般少于4 个。
31.非金属元素的原子最外层电子数一般多于4 个。
32.稀有气体元素的原子最外层电子数一般为8 个(氦为2 个)。
33.原子的核外电子是分层排布的。
34.原子结构示意图可以表示原子的核电荷数、电子层数以及各层上的电子数。
35.燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
36.燃烧需要同时满足三个条件:可燃物、与氧气接触、温度达到着火点。
37.灭火的原理是破坏燃烧的条件,即清除可燃物、隔绝氧气、降低温度至着火点以下。
38.缓慢氧化是进行得很缓慢,甚至不容易被察觉的氧化反应。
化学课件ppt

熟悉实验室常见的仪器设备,如烧杯、试管、滴 定管、容量瓶等。
分析化学实验技术
化学分析方法
掌握酸碱滴定法、络合滴定法、沉淀滴定法等常见的化学分析方 法。
仪器分析技术
了解色谱法、光谱法、质谱法等仪器分析技术的应用范围和原理 。
分析数据处理
掌握实验数据的处理方法,如误差分析、数据统计和结果分析等 。
反应速率方程
反应速率方程是表示反应速率与反应物浓度的关系,可以用来描述 化学反应进行的快慢和规律。
反应速率常数
反应速率常数是反应速率方程中的常数,表示反应进行的快慢程度 ,与反应的温度有关。
化学反应热力学
反应热
反应热是指在一定条件下,化学反应在单位质量下所释放 出来的热量,通常用焓变(ΔH)来表示。
能量守恒定律
能量守恒定律是指在一个封闭的 系统中,能量既不会凭空产生也 不会凭空消失,它只会从一种形
式转化为另一种形式。
化学基本计算
01
02
03
物质的量
物质的量是衡量物质数量 的单位,通常用摩尔表示 。
摩尔质量
摩尔质量是指单位物质的 量的物质所具有的质量。
阿伏伽德罗常数
阿伏伽德罗常数是指1摩 尔物质所含有的微粒数目 ,通常用NA表示。
化学课件
目录
CONTENTS
• 化学基础知识 • 化学物质与能量变化
• 化学反应与环境 • 化学实验与技术 • 化学应用与案例
• 复习与巩固
01 化学基础知识
CHAPTER
化学基本概念
物质的变化
物质的变化包括物理变化和化学 变化,其中化学变化是指物质在
化学反应中发生的质的变化。
化学反应
化学反应是指两种或两种以上的物 质相互作用,产生新的物质的过程 。
化学ppt课件

化学反应与能量转化
化学反应
化学反应是指分子破裂成原子,原子重新排列组合生成新物质的过程。
能量转化
化学反应中常常伴随着能量的转化,如放热或吸热等。
化学方程式及其计算
化学方程式
化学方程式是用化学符号和式子表示化学反应的式子。
化学方程式的计算
根据化学方程式,可以计算出反应物和生成物的质量比,也 可以计算出反应物和生成物的物质的量之比。
金属与非金属
金属
如铁(Fe)、铜(Cu)、铝(Al)、锌(Zn)等,具有良好的导电性和延 展性。
非金属
如碳(C)、硅(Si)、硫(S)、磷(P)等,一般不具有金属特性。
酸碱盐
• 酸:如盐酸# 人体所需的营养素
03
化学实验
实验室安全与操作规范
实验室安全意识
进入实验室前需要了解实验室的安全规定,遵循正确的操作规程,避免发生意外 事故。
2023
化学ppt课件
目录
• 化学基础知识 • 化学物质 • 化学实验 • 化学与生活 • 化学前沿 • 复习与考试指导
01
化学基础知识
化学的定义与性质
化学是一门研究物质变化的自然科学
化学是研究物质的组成、结构、性质和变化规律的自然科学。
化学性质
化学性质指的是物质在发生化学变化时所表现出来的性质。
3
研究特点
操纵单个原子和分计和制备具有特定化学结构 和功能的新分子和材料。
涉及领域
材料科学、生物学、医学、能 源、环境科学等。
研究热点
高效合成方法、不对称合成、 组合化学等。
06
复习与考试指导
学习方法与策略
制定学习计划
01
根据教学内容和自身情况,制定详细的学习计划,合理安排时
化学基础知识大全

化学基础知识大全化学基础知识大全一、基本概念1、物质得变化及性质ﻫ(1)物理变化:没有新物质生成得变化。
ﻫ①宏观上没有新物质生成,微观上没有新分子生成。
②常指物质状态得变化、形状得改变、位置得移动等。
ﻫ例如:水得三态变化、汽油挥发、干冰得升华、木材做成桌椅、玻璃碎了等等。
ﻫ (2)化学变化:有新物质生成得变化,也叫化学反应。
①宏观上有新物质生成,微观上有新分子生成。
②化学变化常常伴随一些反应现象,例如:发光、发热、产生气体、改变颜色、生成沉淀等.有时可通过反应现象来判断就是否发生了化学变化或者产物就是什么物质。
ﻫ(3)物理性质:物质不需要发生化学变化就能表现出来得性质.①物理性质也并不就是只有物质发生物理变化时才表现出来得性质;例如:木材具有密度得性质,并不要求其改变形状时才表现出来。
ﻫ②由感官感知得物理性质主要有:颜色、状态、气味等。
ﻫ③需要借助仪器测定得物理性质有:熔点、沸点、密度、硬度、溶解性、导电性等。
ﻫ(4)化学性质:物质只有在化学变化中才能表现出来得性质。
ﻫ例如:物质得金属性、非金属性、氧化性、还原性、酸碱性、热稳定性等。
ﻫ2、物质得组成原子团:在许多化学反应里,作为一个整体参加反应,好像一个原子一样得原子集团。
ﻫ离子:带电荷得原子或原子团。
元素:具有相同核电荷数(即质子数)得一类原子得总称.3、物质得分类ﻫ(1)混合物与纯净物混合物:组成中有两种或多种物质.常见得混合物有:空气、海水、自来水、土壤、煤、石油、天然气、爆鸣气及各种溶液。
ﻫ纯净物:组成中只有一种物质。
①宏观上瞧有一种成分,微观上瞧只有一种分子;②纯净物具有固定得组成与特有得化学性质,能用化学式表示;ﻫ③纯净物可以就是一种元素组成得(单质),也可以就是多种元素组成得(化合物)。
(2)单质与化合物单质:只由一种元素组成得纯净物。
可分为金属单质、非金属单质及稀有气体。
化合物:由两种或两种以上得元素组成得纯净物。
(3)氧化物、酸、碱与盐氧化物:由两种元素组成得,其中有一种元素为氧元素得化合物。
化学名词解释

百度文库-让每个人平等地提升自我化学名词解释1、元素一一具有相同核电荷数的同一类原子的总称。
2、单质一一由同一种元素组成的物质。
3、化合物一一由两种或两种以上元素的原子组成的物质。
4、纯净物一一凡含有一种单质或一种化合物的物质。
5、混合物一一由几种不同的单质或化合物混杂在一起形成的物质。
6、化学变化一一物质在发生变化时有新物质生成的变化叫做化学变化,也叫做化学反应。
7、酸一一能在水中电离释放出阳离子且全部是氢离子的化合物。
8、碱一一能在水中电离释放出阴离子且全部是氢阳根离子的化合物。
9、盐一一金属离子与酸根离子组成的化合物。
10、摩尔浓度一一1升溶液中含有溶质的摩尔数。
11、电解质一一化学上把溶于水后或在熔融状态下能导电的物质叫电解质。
12、误差一一测量值和真实值之间的差异叫误差。
13、硬度一一指水中某些易于形成沉淀的金属离子,通常指钙镁离子含量14、酸度一一水中含有能接受氢阳根离子的物质的量的总和。
15、碱度一一表示水中氢阳根、碳酸根、重碳酸根及其他一些弱酸盐类的总和。
16、指示剂一一滴定分析中,通过改变颜色指示化学计量点的试剂。
17、滴定终点一一在滴定分析中,指示剂变色点称为滴定终点。
18、标准溶液一一在分析中,已知准确浓度的溶液。
19、掩蔽剂一一一种能与干扰离子起作用而不影响试验结果的试剂。
20、生水——未经任何处理的天然水(江、河、湖、地下水等)。
21、碱性水一一其特征是碱度大于硬度的水。
22、锅炉补给水一一生水经各种方法净化处理后,用来补充热力发电厂汽水损失的水。
23、给水一一送进锅炉的水。
24、炉水一一在锅炉本体的蒸发系统中流动的水。
25、凝结水一一在汽轮机中作功后的蒸汽冷凝成的水。
26、冷却水一一用作冷却介质的水。
27、疏水一一指各种蒸汽管道和用汽设备中的蒸汽凝结水。
28、PH——氢离子浓度的负对数。
29、Pna——钠离子浓度的负对数。
30、树脂的工作交换容量一一树脂在实际条件下对离子的交换吸附能力。
高中化学ppt课件

03
化学实验基础
实验安全和操作规范
实验安全
确保实验环境安全,遵守实验安 全规定,避免发生意外事故。
操作规范
遵循正确的操作步骤和规范,确 保实验结果的准确性和可靠性。
实验器材和试剂
实验器材
了解和掌握实验所需的器材,如烧杯、试管、滴定管等,并 正确使用。
试剂
熟悉实验所需的试剂,了解其性质和使用方法,注意试剂的 储存和使用期限。
02
化学基础知识
原子结构和元素周期表
总结词
理解元素周期表的规律和元素性质的关系
总结词
掌握原子结构的基本理论
详细描述
元素周期表是化学学科中重要的工具,通过学习元素周期 表的排列规律,可以理解元素性质的变化趋势,如金属性 、非金属性、电负性等。
详细描述
原子结构包括原子核和核外电子,通过学习原子的电子排 布规律,可以理解元素的化学性质和反应机制。
实验设计和数据处理
实验设计
根据实验目的和要求,设计合理的实验方案,确保实验结果的准确性和可靠性 。
数据处理
掌握实验数据的记录、整理和分析方法,正确处理实验数据,得出科学结论。
04
化学在生活中的应用
生活中的化学物质
总结词
了解生活中的化学物质
详细描述
生活中常见的化学物质包括水、食盐、糖、醋酸、酒等,它们在我们的饮食、清 洁和日常用品中都有广泛应用。
05
化学前沿和展望
现代化学的发展趋势
绿色化学
随着环保意识的增强,绿色化学 成为未来化学发展的主要趋势, 旨在减少或消除化学品对人类健
康和环境的负面影响。
计算化学
利用计算机模拟和理论计算方法研 究化学反应过程和分子性质,为新 材料的发现和优化提供有力支持。
化学符号

1氢H(qīng)2氦He(hài)3锂Li(lǐ)4铍Be(pí)5硼B(péng)6碳C(tàn)7氮N(dàn)8氧O(yǎng)9氟F(fú)10氖Ne(nǎi)11钠Na(nà)12镁Mg(měi) 13铝Al(lǚ)14硅Si(guī)15磷P(lín)16硫S(liú)17氯Cl(lǜ)18氩Ar(yà)19钾K(jiǎ)20钙Cs(gài) 21钪Sc(kàng) 22钛Ti(tài)23钒V(fán)24铬Cr(gè)25锰M n(měng) 26铁FE(tiě)27钴Co(gǔ)28镍Ni(niè)29铜Cu(tóng) 30锌ZN(xīn) 31镓Ga(jiā)32锗Ge(zhě) 33砷As(shēn) 34硒Se(xī)35溴Br(xiù)36氪Kr(kè)37铷Rb(rú)38锶Sr(sī)39钇Y(yǐ)40锆Zr(gào) 41铌Nb(ní)42钼MO(mù) 43锝Tc(dé)44钌Ru(liǎo)45铑Rh(lǎo) 46钯Pd(bǎ) 47银Ag(yín) 48镉Cd(gé) 49铟In(yīn)50锡Sn(xī)51锑Sb(tī)52碲Te(dì)53碘I(diǎn)54氙Xe(xiān) 55铯Cs(sè) 56钡Bs(bèi)镧系57镧La(lán) 58铈Ca(shì) 59镨Pr(pǔ)60钕Nd(nǚ)61钷Pm(pǒ) 62钐Sm(shān) 63铕Eu(yǒu) 64钆Gd(gá) 65铽Tb(tè)66镝Dy(dī)67钬Ho(huǒ) 68铒Er(ěr)69铥Tm(diū) 70镱Yb(yì)71镥Lu(lǔ)72铪Hf(hā)73钽Ta(tǎn) 74钨W(wū)75铼Re(lái) 76锇Os(é)77铱Ir(yī)78铂Pt(bó)79金Au(jīn) 80汞Hg(gǒng) 81铊Tl(tā)82铅Pb(qiān) 83铋Bi(bì)84钋Po(pō)85砹At(ài)86氡Rn(dōng)87钫Fr(fāng)88镭Ra(léi)锕系89锕Ac(ā)90钍Th(tǔ)91镤Pa(pú)92铀U(yóu)93镎Np(ná)94钚Pu(bù)95镅Am(méi)96锔Cm(jú)97锫Bk(péi)98锎Cf(kāi)99锿Es(āi)100镄Fm(fèi)101钔Md(mén)102锘No(nuò)103铹Lr(láo)104钅卢Rf(lú)105钅杜Db(dù)106钅喜Sg(xǐ)107钅波Bh(bō)108钅黑Hs(hēi)109钅麦Mt(mài)110钅达Ds(dá)111钅仑Rg(lún)112Uub Cn113Uut114Uuq115Uup116Uuh117Uus118UuoH He Li Be B (氢氦锂铍硼) C N O F Ne (碳氮氧氟氖) Na Mg Al Si P (钠镁铝硅磷) S Cl Ar K Ca (硫氯氩钾钙)侵害从前,有一个富裕人家,用鲤鱼皮捧碳,煮熟鸡蛋供养着有福气的奶妈,这家有个很美丽的女儿,叫桂林,不过她有两颗绿色的大门牙(哇,太恐怖了吧),后来只能嫁给了一个叫康太的反革命。
初三化学常见化学式

初三化学常见化学式一、单质1. 金属单质- 铁:Fe- 铜:Cu- 铝:Al- 镁:Mg- 锌:Zn- 银:Ag- 金:Au(初中阶段了解)- 汞(水银):Hg2. 非金属单质- 氢气:H₂- 氧气:O₂- 氮气:N₂- 氯气:Cl₂- 碳(石墨、金刚石):C- 硫:S- 磷(白磷、红磷):P二、氧化物1. 金属氧化物- 氧化镁:MgO- 氧化铝:Al₂O₃- 氧化铁(三氧化二铁):Fe₂O₃(铁锈的主要成分) - 四氧化三铁:Fe₃O₄(磁铁矿的主要成分)- 氧化铜:CuO- 氧化钙(生石灰):CaO2. 非金属氧化物- 二氧化碳:CO₂- 一氧化碳:CO- 水:H₂O- 过氧化氢(双氧水):H₂O₂- 二氧化硫:SO₂- 三氧化硫:SO₃三、酸1. 盐酸:HCl(氯化氢气体的水溶液)2. 硫酸:H₂SO₄3. 硝酸:HNO₃四、碱1. 氢氧化钠:NaOH(俗称烧碱、火碱、苛性钠)2. 氢氧化钙:Ca(OH)₂(俗称熟石灰、消石灰,其水溶液叫石灰水)3. 氢氧化钾:KOH4. 氨水:NH₃·H₂O五、盐1. 氯化钠:NaCl(食盐的主要成分)2. 碳酸钠:Na₂CO₃(俗称纯碱、苏打)3. 碳酸氢钠:NaHCO₃(俗称小苏打)4. 碳酸钙:CaCO₃(大理石、石灰石的主要成分)5. 硫酸铜:CuSO₄- 硫酸铜晶体(五水硫酸铜):CuSO₄·5H₂O(俗称胆矾、蓝矾)6. 氯化银:AgCl(不溶于水和稀硝酸的白色沉淀)7. 硫酸钡:BaSO₄(不溶于水和稀硝酸的白色沉淀)8. 硝酸钾:KNO₃(复合肥料)。
化学基础知识

16gmol1
第1章 化学基础知识
§1.1 气体 (Gas)
二、实际气体的状态方程
1.实际气体 ( True Gas )
对于沸点很低的气体,如H2 、N2、O2 等,在压力不太高或温度不太低时,大致 都能很好遵守理想气体状态方程式。
对于大分子质量的气体,如Cl2,或在 很高压力、很低温度下,理想气体状态方 程式的应用会出现偏差。
3 .0L 0
第1章 化学基础知识
§1.1 气体 ( L o m 4l 1 k o K P 1 l 2 a9 3.00L
8
289kPa
p 总 82 .2 68 k 9 3 Pk 7 aP 2a kPa
反应时
O22H2
2H2O
第1章 化学基础知识
§1.1 气体 (Gas)
例:在 25℃下将0.100mol O2和0.350mol H2装入 3.00 L容器中,通电后氧气和氢气反 应生成水,剩下过量的氢气,求反应前后气体
的总压和各组分的分压。
解:反应前
pO2nOV2RT 0 .1m 00 8 o .3lk 1P 4 L K a 1m 1 o2lK 98 82.6kPa
§1.2 液体和溶液
x剂 x质
则: x剂x质x剂
x质
x质 x剂
x质
x质 x剂 x质
2.2.2 饱和蒸汽压
第1章 化学基础知识
§1.2 液体和溶液
1. 纯溶剂的饱和蒸汽压
在一定温度下,溶剂: 当V(蒸发)=V(凝聚),达动态平衡。
此时饱和蒸汽所产生的压强,为饱和蒸
汽压。表示为p*。
p*为液体性质,与温度有关。 同一液 体在不同温度有不同的饱和蒸汽压值。
溶液渗透压示意图
常见化学式大全
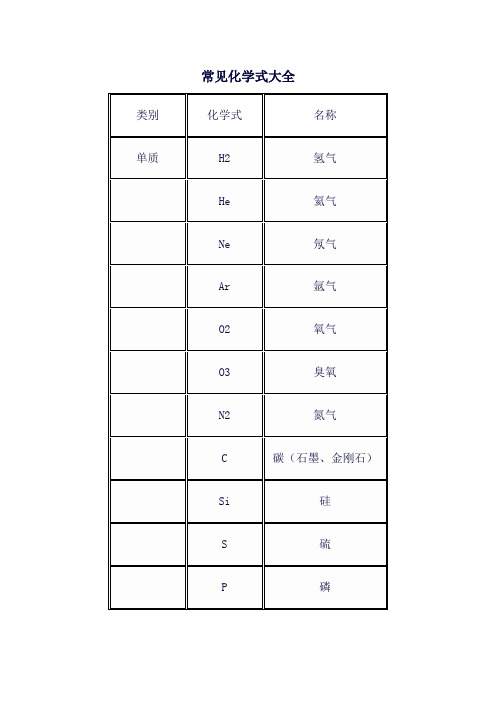
类别
化学式
名称
单质
H2
氢气
He
氦气
Ne
氖气
Ar
氩气
O2
氧气
O3
臭氧
N2
氮气
C
碳(石墨、金刚石)
Si
硅
S
硫
P
磷
Cl2
氯气
K
钾
Ca
钙
Na
钠
Mg
镁
Al
铝
Zn
锌
Fe
铁
Cu
铜
Hg
汞
Ag
银
氧化物
H2O
水
H2O2
过氧化氢
CO
一氧化碳
CO2
二氧化碳
SO3
三氧化硫
NO2
二氧化氮
SO2
二氧化硫
P2O5
五氧化二磷
氢氧化钙
Mg(OH)2
氢氧化镁
Al(OH)3
氢氧化铝
Zn(OH)2
氢氧化锌
Fe(OH)3
氢氧化铁
Fe(OH)2
氢氧化亚铁
Cu(OH)2
氢氧化铜
Ba(OH)2
氢氧化钡
NH3·H2O
氨水
NaCl
氯化钠
CuCl2
氯化铜
AlCl3
氯化铝
KCl
氯化钾
FeCl2
氯化亚铁
FeCl3
氯化铁
AgCl
氯化银
CaCl2
氯化钙
CaO
氧化钙
FeO
氧化亚铁
Fe2O3
氧化铁
Fe3O4
四氧化三铁
MgO
氧化镁
ZnO
什么是化学

什么是化学?
化学是一门自然科学,研究物质的组成、性质、结构、变化以及与能量的关系。
它是研究物质世界的基本科学之一,也是其他自然科学领域的重要基础。
化学的研究对象是物质,而物质是构成宇宙的基本要素,包括固体、液体、气体以及更微小的粒子如分子和原子。
化学家通过实验和理论研究,探索和解释物质的各种性质和变化规律。
化学的核心概念包括:
1. 原子结构:物质由原子构成,原子由质子、中子和电子组成。
原子的不同组合形成不同的元素。
2. 化学键和分子:原子通过化学键结合形成分子。
分子是具有独立存在和特定性质的微观粒子。
3. 反应和变化:化学反应是物质之间发生的变化过程,涉及化学键的断裂和形成。
化学反应可以导致物质的转化和性质的改变。
4. 物质的性质:化学研究物质的各种性质,包括物理性质(如颜色、密度、熔点、沸点等)和化学性质(如反应性、稳定性等)。
5. 反应速率和平衡:化学反应的速率和平衡状态是化学动力学和化学平衡的重要概念。
化学在日常生活中无处不在,它解释了我们周围发生的化学反应和变化。
化学的应用广泛,涵盖了许多领域,如药物研发、材料科学、环境保护、食品科学、能源和燃料等。
通过学习化学,人们可以深入了解物质的本质和性质,理解自然界和人类活动中的化学过程,探索新的物质和化学反应,为解决现实世界的问题提供科学依据和解决方案。
化学简介

能
源 国防
化
学 资源利用
材料 环境保护
医药卫生
9
化学寄语
化学并不坏
学科没有对错, 化学在不同的人 只有怎样应用 中发挥不同的 作用
不要恨化学
10
11
化学简介
化学简介
化学是一门研究物质的组成、结构和性 质及其变化规律的学科。 化学是一门以实验为基础的科学。
化学是一门中心学科,它与社会发展的各
个方面都有联系。
2
化学分类
无机化学
基础学科
有机化学
物理化学
分析化学
3
学科简介 无机 化学 有机 化学
无机化学—— 研究无机物质的组成、结构、 性质和变化规律的学科。
物理 化学 分析 化学
学科简介 无机 化学 有机 Section 化学 header
物理 化学 分析 化学
有机化学—— 研究有机化合物的组成、 结构、性质、合成以及有关理论 的科学。
学科分类 无机 化学 有机 化学 物理 Section 化学 header
分析 化学
物理化学—— 研究化学现象与物理现象之 间的相互关系,从中找出化学变化 普遍规律的科学。
学科简介 无机 化学 有机 化学
物理 化学 Section 分析 化学 header Section header
分析化学—— 研究物质化学组成与化学 结构的分析方法及其有关理论 的学科。
化学与社会
炼钢 转炉
化学 能源
石油 化工
化学 发电
8
化学是一门社会需要的中心科学农业衣 食建材
住 冶金
汽车
关于化学的知识

关于化学的知识化学是一门研究物质组成、性质、结构、变化以及它们之间相互作用的科学。
它是自然科学中的一支重要学科,也是应用科学中的关键领域之一。
下面将从化学的基本概念、分支学科以及应用领域等方面来介绍化学的知识。
一、化学的基本概念1. 原子:化学研究的基本粒子,由原子核和电子构成。
不同的元素由不同类型的原子组成。
2. 元素:由同种类型的原子组成的物质。
目前已知的元素有118种,常见的有氧、氢、碳、氮等。
3. 化合物:由两种或更多种元素组成的物质。
例如,水是由氢和氧两种元素组成的化合物。
4. 反应:化学变化的过程,包括物质的组成和性质的改变。
反应可以分为物理变化和化学变化两种类型。
5. 酸碱中和:酸和碱反应形成盐和水的过程,是化学反应中常见的一种类型。
6. 氧化还原反应:指物质失去或获得电子的过程。
氧化剂是指接受电子的物质,而还原剂是指提供电子的物质。
二、化学的分支学科1. 有机化学:研究有机物(含碳的化合物)的结构、性质和反应。
有机化学在药物合成、聚合物制备等方面具有重要应用。
2. 无机化学:研究无机物(不含碳的化合物)的结构、性质和反应。
无机化学在催化剂、材料科学等领域有广泛应用。
3. 物理化学:研究物质的物理性质和化学性质之间的关系,涉及热力学、动力学等方面的研究。
4. 分析化学:研究物质组成和性质的分析方法和技术,包括定性分析和定量分析等。
5. 生物化学:研究生物体内化学反应和物质代谢的过程,是生物学和化学的交叉学科。
三、化学的应用领域1. 医药领域:化学在药物合成和药物分析方面有重要应用,为疾病的治疗和预防提供了基础。
2. 材料科学:化学在材料合成和表征方面发挥着关键作用,例如新材料的开发和纳米材料的制备等。
3. 能源领域:化学在能源转化和储存方面有重要应用,例如太阳能电池和燃料电池等。
4. 环境保护:化学在污染物的检测和处理方面发挥着重要作用,为环境保护提供技术支持。
5. 食品科学:化学在食品加工和食品安全领域有广泛应用,例如食品添加剂的研发和食品中有害物质的检测等。
化学专业主要课程

化学专业主要课程
化学专业学习的课程主要有:无机化学、分析化学、有机化学、物理化学、高分子化学与物理、无机化学及实验、分析化学及实验、有机化学及实验、物理化学及实验、结构化学、仪器分析。
化学是一门普通高等学校本科专业,属化学类专业,基本修业年限为四年,授予理学学位。
化学专业学生在系统、扎实地掌握化学基础知识、基本理论和基本技能的基础上,还应掌握化学研究的基本方法和手段,具有较强的创新意识和实践能力,深入了解化学的学科前沿和发展趋势,了解生命、材料、能源、环境等相关学科的基础知识,能够在化学及相关领域从事科研、技术、教育等工作。
化学大学知识点总结

化学大学知识点总结一、化学的起源和发展1.1 化学的起源化学是一门研究物质的组成、性质、变化和应用的科学。
它的起源可以追溯到古代的炼金术。
古希腊人提出了许多有关物质构成的理论,如“四大素”说。
在中世纪欧洲,炼金术家尝试将非金属物质转化为黄金,推动了实验化学的发展。
18世纪以后,化学逐渐发展成为一门独立的科学领域。
1.2 化学的发展随着科学实验方法的逐渐成熟,化学逐渐从哲学和实验室中学科发展为一门自然科学。
18世纪的拉瓦锡、黑尔赫、拉瓦锡、博斯托和盖亚-路易斯,他们发现了一系列物质的元素,并整理出了化学元素周期表。
20世纪,量子力学的发展使得化学有了更加深入的解释。
现代化学研究涉及分子与原子领域,并与生物学、医学、材料科学和环境科学等学科紧密联系。
二、化学的基本概念2.1 物质物质是组成一切事物的基本单位,是占据空间并具有质量的实体。
根据组织结构和性质,物质可以分为元素和化合物。
元素是由同一种原子组成的物质,化合物则是由两种或两种以上不同化学元素组成的物质。
2.2 分子分子是由两个或两个以上原子通过共价键联结在一起形成的电中性的粒子。
分子的大小可以)描述单位,如常摄氏度/秒:安培秒: g.Term-12如果是简单分子,则可以表示为M(对于分子而言,M是一个很小的数字,通常在10-5至10-9之间表示为kg/ mol。
2.3 原子结构原子是构成一切物质的最小的单位。
原子的核心由质子和中子构成,质子和电子的数量决定了元素的性质。
现代化学通过量子力学理论对原子的结构和性质有了更深刻的认识。
2.4 元素周期表元素周期表是化学元素按照其原子序数增加顺序排列成的表。
元素周期表的主体是长周期表(俄歇夫表),按原子序数排列元素,同时显示化学元素的周期性。
这表明,元素周期表中的元素以相似的方式进行周期变化。
元素周期表有不同的布局形式,包括1S,内接双语,内接双关语和长周期表。
2.5 化学键化学键是物质中形成化合物的一种方式。
化学背诵知识点(超全)

第一章走进化学世界课题1物质的变化和性质一、物质的变化1、概念:物理变化——没有生成其它物质的变化。
例:石蜡熔化、水结成冰、汽油挥发化学变化——有其它物质生成的变化例:煤燃烧、铁生锈、食物腐败、呼吸2、判断变化依据:是否有其它(新)物质生成。
有则是化学变化,无则是物理变化3、相互关系:常常伴随发生,有化学变化则一定有物理变化,有物理变化则不一定有化学变化。
4、化学变化伴随现象:放热、吸热、发光、变色、放出气体和生成沉淀。
二、物质的性质物理性质:物质不需要化学变化就表现出的性质。
包括:颜色、状态、气味、熔点、沸点、密度、硬度、溶解性、挥发性、延展性、导电性、吸水性、吸附性等。
化学性质:物质在化学变化中表现出的性质。
可燃性、氧化性、还原性、活泼性、稳定性、腐蚀性、毒性等。
它们的区别是:物理性质不需要发生化学变化就能表现出来,而物质的化学性质则要在化学变化中才能表现出来。
三、物理变化、化学变化、物理性质、化学性质之间的区别与联系。
联系:在变化语句中加“能”或“可以”或“易”“会”“难于”等词语,变成了相应的性质。
物理变化化学变化概念没有生成其他物质的变化生成其他物质的变化伴随现象物质的形状、状态等发生变化常伴随有放热、发光、变色,放出气体、生成沉淀等本质区别变化时是否有其他物质生成实例石蜡熔化、水结成冰、汽油挥发煤燃烧、铁生锈、食物腐败、呼吸相互关系物质在发生化学变化的过程中一定伴随物理变化,如石蜡燃烧时会发生石蜡熔化的现象(物理变化)。
在发生物理变化时不一定伴随化学变化。
物理性质化学性质概念物质不需要发生化学变化就能表现出来的性质物质在化学变化中表现出来的性质实质物质的微粒组成结构不变所呈现出的性质。
物质的微粒组成结构改变时所呈现出的性质。
实例颜色、状态、气味、熔点、沸点、硬度、密度、溶解性、挥发性、吸附性、导电性、导热性、延展性等可燃性、氧化性、稳定性、助燃性、还原性等确定由感官直接感知或由仪器测定通过化学变化方可知区别是否需要通过化学反应表现出来课题2化学是一门实验为基础的科学一、化学研究的对象是物质,以实验为基础。
化学表(完整)
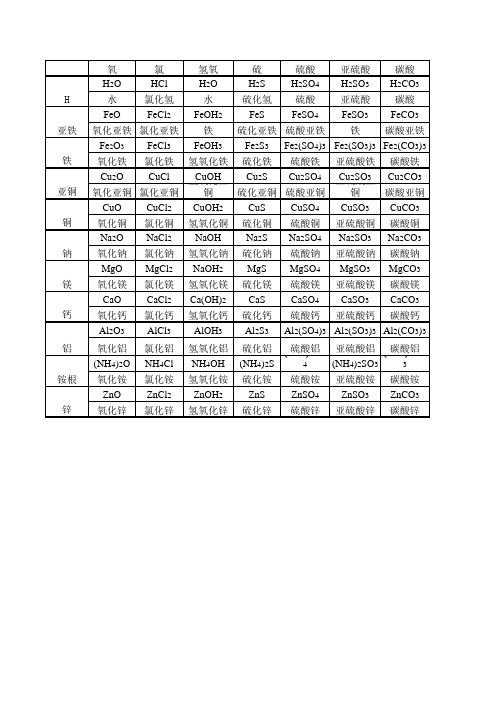
3
Fe(NO3)2
氯酸铁 磷酸铁 高锰酸铁 锰酸铁 硝酸铁
CuClO3 Cu3PO4 高Cu锰M酸nO亚4
氯酸亚铜 磷酸亚铜 Cu(M铜nO4)
Cu(ClO3)2 Cu3(PO4)2
2
氯酸铜 磷酸铜 高锰酸铜
Cu2MnO4 锰酸亚铜 CuMnO4 锰酸铜
CuNO3 硝酸亚铜 Cu(NO3)2 硝酸铜
H 亚铁 铁 亚铜 铜 钠 镁 钙 铝 铵根 锌
氧
氯
氢氧
硫
硫酸 亚硫酸 碳酸
H2O
HCl
H2O
H2S
H2SO4 H2SO3 H2CO3
水
氯化氢
水
硫化氢 硫酸 亚硫酸 碳酸
FeO
FeCl2 氢F氧eO化H2亚 FeS
FeSO4 亚F硫eS酸O3亚 FeCO3
氧化亚铁 氯化亚铁 铁 硫化亚铁 硫酸亚铁 铁 碳酸亚铁
Fe2O3 氧化铁
FeCl3 FeOH3 Fe2S3 Fe2(SO4)3 Fe2(SO3)3 Fe2(CO3)3 氯化铁 氢氧化铁 硫化铁 硫酸铁 亚硫酸铁 碳酸铁
Cu2O
CuCl 氢C氧uO化H亚 Cu2S Cu2SO4 亚C硫u2S酸O亚3 Cu2CO3
氧化亚铜 氯化亚铜 铜 硫化亚铜 硫酸亚铜 铜 碳酸亚铜
MgSO4 MgSO3 MgCO3 硫酸镁 亚硫酸镁 碳酸镁
CaO 氧化钙
CaCl2 Ca(OH)2 CaS 氯化钙 氢氧化钙 硫化钙
CaSO4 CaSO3 CaCO3 硫酸钙 亚硫酸钙 碳酸钙
Al2O3 AlCl3 AlOH3 Al2S3 Al2(SO4)3 Al2(SO3)3 Al2(CO3)3
氯酸
磷酸 高锰酸
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学★重在:各种反应各种会基本概念和基本理论、无机化学、有机化学这三大重点版块。
紧扣课本复习的同时,要注意概念的理解记忆,不要机械式地死记硬背,尽量把晦涩的概念转化为自己易懂的语言。
这个阶段的练习很重要,但切记不要题海战术。
练习之后对于错题要及时总结。
提炼这门课程的基本理论和重要结论,以及考试知识点,特别是新增考点和新修考点;对跨章节甚至跨学科的相关知识点进行初步综合。
同时进行专题训练,并对专题知识进行归纳总结(化学是可以把所有东西联系起来的,注重联系。
),对真题进行总结。
☞优化技巧:无机化学主要记忆各反应、反应中所产生的特殊气体、颜色沉淀等物理现象(解题突破口)。
有机部分,注重官能团的特征,能够参与反应的类型,反应特征,注意碳链结构的组合方式。
(解题突破口)推断题:找突破口多观察思考反应方程式,对重点反应类型、反应方程式要一提便知,并回顾和做题。
凡是顺路不通走逆路,二者皆阻从中间。
无机颜色、沉淀、气体,有机特殊反应、特殊官能团。
(有机题给的条件都用得到,甚至就是解题突破)一、俗名无机:纯碱、苏打、天然碱、口碱:Na2CO3小苏打:NaHCO3大苏打:Na2S2O3石膏(生石膏):CaSO4.2H2O 熟石膏:2CaSO4·.H2O 莹石:CaF2重晶石:BaSO4(无毒)石灰石、大理石:CaCO3生石灰:CaO 熟石灰、消石灰:Ca(OH)2烧碱、火碱、苛性钠:NaOH 绿矾:FaSO4·7H2O 干冰:CO2 明矾:KAl (SO4)2·12H2O 漂白粉:Ca (ClO)2和CaCl2 胆矾、蓝矾:CuSO4·5H2O 双氧水:H2O2皓矾:ZnSO4·7H2O 硅石、石英:SiO2刚玉:Al2O3 水玻璃、泡花碱、矿物胶:Na2SiO3铁红、铁矿:Fe2O3磁铁矿:Fe3O4黄铁矿、硫铁矿:FeS2铜绿、孔雀石:Cu2 (OH)2CO3菱铁矿:FeCO3赤铜矿:Cu2O 波尔多液:Ca (OH)2和CuSO4玻璃的主要成分:Na2SiO3、CaSiO3、SiO2过磷酸钙(主要成分):Ca (H2PO4)2和CaSO4重过磷酸钙(主要成分):Ca (H2PO4)2天然气、沼气、坑气(主要成分):CH4、水煤气:CO和H2光化学烟雾:NO2在光照下产生的一种有毒气体王水:浓HNO3与浓HCl(按体积比1:3混合而成)。
铝热剂:Al + Fe2O3或其它氧化物尿素:CO(NH2) 2有机:氯仿:CHCl3电石:CaC2电石气:C2H2 (乙炔) TNT:三硝基甲苯酒精、乙醇:C2H5OH 氟氯烃:是良好的制冷剂,有毒,但破坏O3层。
醋酸:冰醋酸、食醋CH3COOH 裂解气成分(石油裂化):烯烃、烷烃、炔烃、H2S、CO2、CO等。
甘油、丙三醇:C3H8O3焦炉气成分(煤干馏):H2、CH4、乙烯、CO等。
石炭酸:苯酚C6H6O 蚁醛:甲醛HCHO 福尔马林:35%—40%的甲醛水溶液蚁酸:甲酸HCOOH 葡萄糖:C6H12O6果糖:C6H12O6蔗糖:C12H22O11麦芽糖:C12H22O11淀粉:(C6H10O5)n 硬脂酸:C17H35COOH 油酸:C17H33COOH 软脂酸:C15H31COOH 安息香酸:苯甲酸水杨酸:邻羟基苯甲酸草酸:乙二酸HOOC—COOH 使蓝墨水褪色,强酸性,受热分解成CO2和水,使KMnO4酸性溶液褪色二、颜色铁:铁粉是黑色的;一整块的固体铁是银白色的。
Fe 2+——浅绿色 Fe 3O 4——黑色晶体 Fe(OH)2——白色沉淀 Fe 3+——黄色 Fe (OH)3——红褐色沉淀 Fe (SCN)3——血红色溶液FeO ——黑色的粉末 Fe (NH 4)2(SO 4)2——淡蓝绿色 Fe 2O 3——红棕色粉末 FeS ——黑色固体铜:单质是紫红色 Cu 2+——蓝色 CuO ——黑色 Cu 2O ——红色 CuSO 4(无水)—白色 CuSO 4·5H 2O ——蓝色 Cu 2 (OH)2CO 3 —绿色 Cu(OH)2——蓝色[Cu(NH 3)4]SO 4——深蓝色溶液BaSO 4 、BaCO 3 、Ag 2CO 3 、CaCO 3 、AgCl 、 Mg (OH)2 、三溴苯酚均是白色沉淀 Al(OH)3 白色絮状沉淀 H 4SiO 4(原硅酸)白色胶状沉淀Cl 2、氯水——黄绿色 F 2——淡黄绿色气体 Br 2——深红棕色液体 I 2——紫黑色固体 HF 、HCl 、HBr 、HI 均为无色气体,在空气中均形成白雾(酸液易挥发)CCl 4——无色的液体,密度大于水,与水不互溶 KMnO 4--——紫色 MnO 4-——紫色 Na 2O 2—淡黄色固体 Ag 3PO 4—黄色沉淀 S —黄色固体 AgBr —浅黄色沉淀AgI —黄色沉淀 O 3—淡蓝色气体 SO 2—无色,有剌激性气味、有毒的气体 SO 3—无色固体(沸点44.8 0C ) 品红溶液——红色 氢氟酸:HF ——腐蚀玻璃N 2O 4、NO ——无色气体 NO 2——红棕色气体 NH 3——无色、有剌激性气味气三、现象1、铝片与盐酸反应是放热的,Ba(OH)2与NH 4Cl 反应是吸热的;2、Na 与H 2O (放有酚酞)反应,熔化、浮于水面、转动、有气体放出;(熔、浮、游、嘶、红)3、焰色反应:Na 黄色、K 紫色(透过蓝色的钴玻璃)、Cu 绿色、Ca 砖红、Na +(黄色)、K +(紫色)。
4、Cu 丝在Cl 2中燃烧产生棕色的烟;5、H 2在Cl 2中燃烧是苍白色的火焰;6、Na 在Cl 2中燃烧产生大量的白烟;7、P 在Cl 2中燃烧产生大量的白色烟雾;8、SO 2通入品红溶液先褪色,加热后恢复原色;9、NH 3与HCl 相遇产生大量的白烟; 10、铝箔在氧气中激烈燃烧产生刺眼的白光;11、镁条在空气中燃烧产生刺眼白光,在CO 2中燃烧生成白色粉末(MgO ),产生黑烟;12、铁丝在Cl 2中燃烧,产生棕色的烟; 13、HF 腐蚀玻璃:4HF + SiO 2 = SiF 4 + 2H 2O14、Fe(OH)2在空气中被氧化:由白色变为灰绿最后变为红褐色;15、在常温下:Fe 、Al 在浓H 2SO 4和浓HNO 3中钝化;16、向盛有苯酚溶液的试管中滴入FeCl 3溶液,溶液呈紫色;苯酚遇空气呈粉红色。
17、蛋白质遇浓HNO 3变黄,被灼烧时有烧焦羽毛气味;18、在空气中燃烧:S ——微弱的淡蓝色火焰 H 2——淡蓝色火焰 H 2S ——淡蓝色火焰 CO ——蓝色火焰 CH 4——明亮并呈蓝色的火焰 S 在O 2中燃烧——明亮的蓝紫色火焰。
19.特征反应现象:(白色迅速变为灰绿色,慢慢变为红褐色])([])([32OH Fe OH Fe 红褐色白色沉淀空气−−→− 20.浅黄色固体:S 或Na 2O 2或AgBr21.使品红溶液褪色的气体:SO 2(加热后又恢复红色)、Cl 2(加热后不恢复红色)22.有色溶液:Fe 2+(浅绿色)、Fe 3+(黄色)、Cu 2+(蓝色)、MnO 4-(紫色)有色固体:红色(Cu 、Cu 2O 、Fe 2O 3)、红褐色[Fe(OH)3] 黑色(CuO 、FeO 、FeS 、CuS 、Ag 2S 、PbS ) 蓝色[Cu(OH)2] 黄色(AgI 、Ag 3PO 4) 白色{Fe(0H)2、CaCO 3、BaSO 4、AgCl 、BaSO 3}有色气体:Cl 2(黄绿色)、NO 2(红棕色)四、常用规律1、溶解性规律——见溶解性表;23、在惰性电极上,各种离子的放电顺序:阴极(夺电子的能力):Au3+ >Ag+>Hg2+ >Cu2+ >Pb2+ >Fa2+ >Zn2+ >H+ >Al3+>Mg2+ >Na+ >Ca2+ >K+阳极(失电子的能力):S2- >I- >Br–>Cl- >OH- >含氧酸根注意:若用金属作阳极,电解时阳极本身发生氧化还原反应(Pt、Au除外)4、双水解离子方程式的书写:(1)左边写出水解的离子,右边写出水解产物;(2)配平:在左边先配平电荷,再在右边配平其它原子;(3)H、O不平则在那边加水。
例:当Na2CO3与AlCl3溶液混和时: 3 CO32- + 2Al3+ + 3H2O = 2Al(OH)3↓+ 3CO2↑5、写电解总反应方程式的方法:(1)分析:反应物、生成物是什么;(2)配平。
例:电解KCl溶液:2KCl + 2H2O == H2↑+ Cl2↑+ 2KOH 配平:2KCl + 2H2O == H2↑+ Cl2↑+ 2KOH6、将一个化学反应方程式分写成二个电极反应的方法:(1)按电子得失写出二个半反应式;(2)再考虑反应时的环境(酸性或碱性);(3)使二边的原子数、电荷数相等。
例:蓄电池内的反应为:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O 试写出作为原电池(放电)时的电极反应。
写出二个半反应:Pb –2e- →PbSO4 PbO2 +2e- →PbSO4分析:在酸性环境中,补满其它原子:应为:负极:Pb + SO42- -2e- = PbSO4正极:PbO2 + 4H+ + SO42- +2e- = PbSO4 + 2H2O注意:当是充电时则是电解,电极反应则为以上电极反应的倒转:为:阴极:PbSO4 +2e- = Pb + SO42-阳极:PbSO4 + 2H2O -2e- = PbO2 + 4H+ + SO42-7、在解计算题中常用到的恒等:原子恒等、离子恒等、电子恒等、电荷恒等、电量恒等,用到的方法有:质量守恒、差量法、归一法、极限法、关系法、十字交法和估算法。
(非氧化还原反应:原子守恒、电荷平衡、物料平衡用得多,氧化还原反应:电子守恒用得多)8、电子层结构相同的离子,核电荷数越多,离子半径越小;9、晶体的熔点:原子晶体>离子晶体>分子晶体中学学到的原子晶体有:Si、SiC 、SiO2=和金刚石。
原子晶体的熔点的比较是以原子半径为依据的:金刚石> SiC > Si (因为原子半径:Si> C> O).10、分子晶体的熔、沸点:组成和结构相似的物质,分子量越大熔、沸点越高。
11、胶体的带电:一般说来,金属氢氧化物、金属氧化物的胶体粒子带正电,非金属氧化物、金属硫化物的胶体粒子带负电。
12、氧化性:MnO4- >Cl2 >Br2 >Fe3+ >I2 >S=4(+4价的S) 例:I2 +SO2 + H2O = H2SO4 + 2HI13、含有Fe3+的溶液一般呈酸性。
